一种多功能锰基纳米粒及其制备方法和医药用途
文献发布时间:2023-06-19 18:37:28
技术领域
本发明属于纳米材料技术和生物医药领域,具体是涉及一种多功能锰基纳米粒及其制备方法和医药用途。
背景技术
肿瘤微环境具有低pH(6.5-7.0)、高过氧化氢(H
化学动力学疗法(Chemodynamic therapy,CDT)是一类利用芬顿反应或类芬顿反应,通过将内源性H
MnO
Mn
虽然二氧化锰纳米材料展现出优异的CDT效果,但要实现其在制备肿瘤药物中的应用,仍面临诸多挑战,如水分散性差且不具有肿瘤靶向性等特点,难以实现药物的靶向转运及高效低毒的联合治疗。
青蒿素及其衍生物是一类含有过氧桥的倍半萜内酯类化合物,由于其在治疗疟疾方面的出色作用而广为人知。近年来,青蒿素及其衍生物已被研究证明具有抗癌效果,且具有较好的安全性,其中双氢青蒿素(Dihydroartemisinin,DHA)的抗癌活性是最好的。在DHA的抗癌机制中,最为广泛接受的是金属离子或过渡金属离子介导的过氧化物键断裂,形成碳自由基,促使细胞凋亡。但是DHA的水溶性差,体内半衰期短,难以在肿瘤部位集聚。
二甲双胍(Metformin,Met)是治疗II型糖尿病的一线用药,近年来流行病学和临床研究表明,二甲双胍在肿瘤预防、治疗和预后上展现出巨大的潜力,而且研究发现二甲双胍不仅能单独抑制肿瘤生长,还能显著提升肿瘤放疗、化疗和生物治疗等疗效。但是二甲双胍是水溶性小分子药物,难以通过常规纳米载体负载实现靶向递药。聚二甲双胍(PolyMet,PM)是以天然高分子聚合物壳聚糖(Chitosan,CH)为基础,在分子结构上接枝了大量的双胍基,从而沿袭了二甲双胍的抗肿瘤活性。同时,PM具有水溶性好、稳定性强等特点,能有效地修饰纳米载体,增强纳米载体在水中的稳定性。
透明质酸(Hyaluromic Acid,HA)分子是人体内必不可少的一种多聚糖,具有较好的生物相容性。
发明内容
发明目的:本发明的目的在于提供一种多功能锰基纳米粒,既可有效解决二氧化锰水分散性差/双氢青蒿素水溶性差、药物靶向性弱等问题,还能实现化疗和化学动力学疗法联合,发挥增强的化学动力学疗法抗肿瘤作用。
技术方案:本发明所述的多功能锰基纳米粒,包括二氧化锰、双氢青蒿素、聚二甲双胍和透明质酸,所述二氧化锰负载双氢青蒿素成为锰基纳米内核,所述聚二甲双胍包裹在锰基纳米内核表面形成锰基纳米复合物,透明质酸结合到锰基纳米复合物表面。
所述二氧化锰具有蜂窝孔状结构。
所述聚二甲双胍是由含伯氨基或仲氨基的盐酸化高分子与二氰二胺单体通过加成反应制得,所述含伯氨基或仲氨基的盐酸化高分子为壳聚糖、线性聚乙烯亚胺、聚赖氨酸、聚乙烯胺及聚烯丙胺中的一种。
所述的多功能锰基纳米粒的制备方法,其特征在于,包括以下步骤:
(1)二氰二胺通过化学反应接枝到含伯氨基或仲氨基的盐酸化高分子上得到聚二甲双胍;
(2)利用软膜板法以高锰酸钾和油酸制备蜂窝状二氧化锰;取所得的蜂窝状二氧化锰置于载体分散介质中分散,冻干,得到蜂窝状二氧化锰纳米颗粒;
(3)将蜂窝状二氧化锰纳米颗粒负载双氢青蒿素得到锰基纳米内核,聚二甲双胍包裹在锰基纳米内核表面,形成锰基纳米复合物,透明质酸进一步结合到载药锰基纳米复合物外层。
所述的多功能锰基纳米粒的制备方法,步骤(2)中所述载体分散介质为丙酮、二甲基亚砜、水、乙醇、甲醇或者N,N-二甲基甲酰胺中的一种或几种。
所述的多功能锰基纳米粒的制备方法,步骤(3)中通过物理吸附法将双氢青蒿素负载到二氧化锰的蜂窝孔状结构中。
所述的多功能锰基纳米粒的制备方法,步骤(3)中聚二甲双胍通过静电吸附作用包裹于锰基纳米内核表面。
所述的多功能锰基纳米粒的制备方法,步骤(3)中所述透明质酸结合到锰基纳米复合物表面的方法包括静电吸附与化学键连接。
所述的多功能锰基纳米粒在制备抗肿瘤药物中的用途。
所述的多功能锰基纳米粒在制备治疗乳腺癌药物中的用途。
多功能锰基纳米粒,二氰二胺通过化学反应接枝到含伯氨基的壳聚糖上得到聚二甲双胍PM,采用高锰酸钾还原制备蜂窝状的二氧化锰,蜂窝状二氧化锰通过物理吸附双氢青蒿素得到锰基纳米内核,PM包裹在锰基纳米内核表面,形成具有良好水分散性的锰基纳米复合物,透明质酸通过静电吸附或化学键连接进一步结合到载药锰基纳米复合物外层,构建了一种CD44受体靶向-PM稳定的多功能锰基纳米粒。
本发明中多功能锰基纳米粒的制备方法,包括以下步骤:
(1)PM的制备:
取含伯氨基或仲氨基的高分子粉末加入到盐酸溶液中,搅拌成糊状,并过夜进行盐酸化,得到盐酸化高分子溶液,冻干即得盐酸化高分子固体。取前述盐酸化高分子固体和二氰二胺溶解于盐酸溶液中,对反应体系进行加热,反应结束后,冷却至室温,抽滤后透析,收集透析液冻干,即得PM固体。
所述步骤(1)中,含伯氨基或仲氨基的高分子为壳聚糖、线性聚乙烯亚胺、聚赖氨酸、聚乙烯胺及聚烯丙胺中的一种;高分子粉末溶解于75-150mL 0.5-1.5%(m/m)盐酸中;盐酸化高分子固体溶解于15-50mL0.5-1.5%(m/m)盐酸中;盐酸化高分子固体与二氰二胺的质量比为1:2~1:20。
优选的,含伯氨基的高分子为壳聚糖;高分子粉末溶解于100mL 1%(m/m)盐酸中;盐酸化高分子固体溶解于20mL 0.75%(m/m)盐酸中;盐酸化高分子固体与二氰二胺的质量比为1:15。
(2)蜂窝状二氧化锰纳米颗粒的制备:
将高锰酸钾加入到超纯水中,常温下搅拌混匀,搅拌条件下将油酸缓慢加入到高锰酸钾溶液中,室温反应结束后,原溶液由紫红色变成深棕色浑浊液状态。通过离心收集产物,并用乙醇和超纯水分别洗涤几次,最后烘干,即得蜂窝状二氧化锰固体。取前述蜂窝状二氧化锰置于适量载体分散介质中,探头超声分散,将该水分散液冻干,得到蜂窝状二氧化锰纳米颗粒(M)。
所述步骤(2)中,高锰酸钾水溶液和油酸的体积比为150:4~600:4;高锰酸钾与油酸的物质的量比为1:7~1:1;高锰酸钾与油酸的反应时间为12h~36h;载体分散介质为丙酮、二甲基亚砜、水、乙醇、甲醇、N,N-二甲基甲酰胺中的一种或几种溶剂;M的超声处理时间为5~30min。
优选的,高锰酸钾水溶液和油酸的体积比为500:4;高锰酸钾与油酸的物质的量比为1:2;高锰酸钾与油酸的反应时间为24h;所述载体分散介质为水;M的超声处理时间为10min。
(3)锰基纳米内核的制备:
将一定量的DHA溶解于有机溶剂中,然后取步骤(2)所制备蜂窝状二氧化锰纳米颗粒加入到DHA溶剂中,探头超声分散,随后放置于真空干燥器中,缓慢蒸发有机溶剂,直到有机溶剂几乎蒸发完全;并用乙醇洗涤几次后冻干,得到锰基纳米内核(MD)。
所述步骤(3)中,有机溶剂为丙酮、二甲基亚砜、乙醇、甲醇、N,N-二甲基甲酰胺中的一种或几种溶剂;二氧化锰与DHA的超声混合处理时间为5~60min;二氧化锰与DHA的质量比为2:1~1:5;
优选的,所述有机溶剂为丙酮;二氧化锰与DHA的质量比为1:1;二氧化锰与DHA的超声混合处理时间为30min;
(4)PM修饰的锰基纳米复合物的制备:
取适量PM溶于纯水中,搅拌均匀,然后加入到步骤(3)所制备的锰基纳米内核水分散液中,避光搅拌。多余的PM通过离心的方法去除,得到PM修饰的载药锰基纳米复合物(MDP)。
所述步骤(4)中,PM与二氧化锰的质量比为1:1~1:8;PM水溶液的浓度为0.5mg/mL~4mg/mL;避光搅拌反应时间为0.5h~5h。
优选的,所述PM与二氧化锰的质量比为1:4;PM水溶液的浓度为2mg/mL;避光搅拌反应时间3h。
(5)透明质酸修饰的多功能锰基纳米粒的制备:
取适量透明质酸溶于纯水中,搅拌均匀后,在磁力搅拌条件下加入到步骤(4)制备的锰基纳米复合物中,避光条件下搅拌。反应结束后离心处理,以除去游离的HA,得到多功能锰基纳米粒(MDPH)。
所述步骤(5)中,透明质酸分子量在10-200KDa之间;透明质酸与PM的质量比为1:1-20:1;HA水溶液的浓度为1mg/mL~5mg/mL;避光搅拌反应时间为0.5h~12h;透明质酸与PM的结合的方法包括但不限于静电吸附与化学键连接。
优选的,所述透明质酸分子量为35KDa;透明质酸与PM的质量比为1:1.5;HA水溶液的浓度为4mg/mL;避光搅拌反应时间为6h;透明质酸与PM的结合的方法为静电吸附。
有益效果:本发明与现有技术相比,具有如下优点:(1)本发明制备的MDPH尺寸较小,分布均匀,具有良好的稳定性和生物安全性。(2)在本发明中,所述二氧化锰具有类芬顿活性,可直接分解肿瘤组织部位积累的大量过氧化氢产生·OH,从而通过CDT杀伤肿瘤。肿瘤部位的酸性和高过氧化氢微环境使得锰基纳米内核崩溃,并伴随着DHA和PM的释放,用于肿瘤化疗;而锰基纳米内核降解所得Mn
附图说明
图1为多功能锰基纳米粒的表征,其中,(a)蜂窝状二氧化锰纳米颗粒的透射电子显微镜(TEM)形貌图;(b)多功能锰基纳米粒的透射电子显微镜(TEM)形貌图;(c)多功能锰基纳米粒在过氧化氢条件下随时间的紫外-可见光吸收波长分析图;(d)PM水溶液的紫外-可见光吸收波长分析图;
图2:多功能锰基纳米粒的体外药效学评价,其中,(a)肿瘤细胞对纳米粒的摄取;(b)采用流式细胞术考察纳米粒的ROS产生能力;(c)不同浓度MDPH处理乳腺癌细胞4T1的细胞存活柱状图;(d)游离药物和制剂组对4T1细胞的24h的IC50;
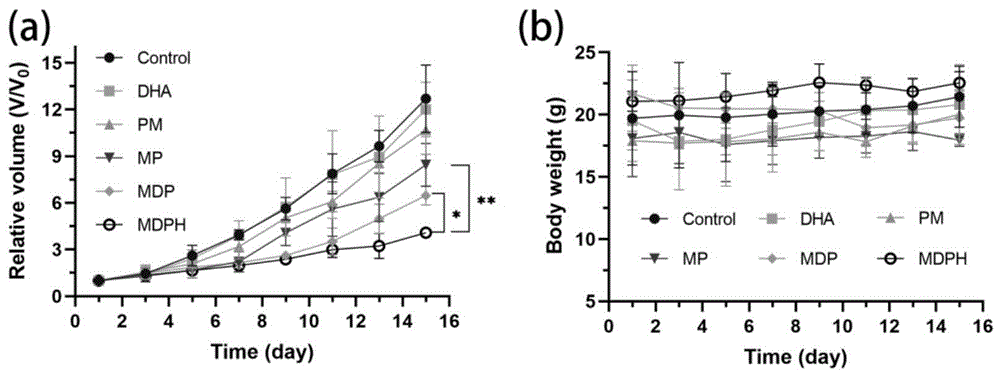
图3:多功能锰基纳米粒的体内药效学评价,其中,(a)不同实验组小鼠肿瘤体积随时间变化的曲线图;(b)不同实验组小鼠体重变化曲线图。
具体实施方式
本发明使用Zeta电势及动态光散射分析(DLS)、紫外光谱(UV-Vis)、透射电子显微镜(TEM)等手段进行表征;然后利用MTT法评价纳米粒的细胞毒性,利用流式细胞术检测细胞对纳米粒的摄取情况,利用倒置荧光显微镜检测细胞ROS的产生能力;最后建立小鼠原位乳腺癌模型进行抗肿瘤实验。具体测试结果如下:
实施例1.多功能锰基纳米粒的制备
(1)PM的制备:
取壳聚糖加入到1%浓度的盐酸溶液中,搅拌成糊状,并过夜进行盐酸化,得到盐酸化壳聚糖溶液,冻干即得盐酸化壳聚糖固体。取前述盐酸化壳聚糖固体和二氰二胺溶解于0.75%盐酸中,于100℃条件下反应5h,冷却至室温,抽滤后透析,收集透析液冻干,即得PM固体。
(2)蜂窝状二氧化锰纳米颗粒的制备:
取0.1g的高锰酸钾于100mL的烧杯中,然后加入50mL超纯水。常温下将上述溶液在磁力搅拌器上搅拌30min。待高锰酸钾完全分散在超纯水中后,取0.4mL油酸缓慢加入到高锰酸钾溶液中,室温继续反应24h。反应结束后,原溶液由紫红色变成深棕色浑浊液状态。通过离心收集产物,并用乙醇和超纯水分别洗涤几次,最后烘干,即得蜂窝状二氧化锰固体。取前述蜂窝状二氧化锰置于适量载体分散介质中,探头超声分散,将该水分散液冻干,得到蜂窝状二氧化锰纳米颗粒(M)。
(3)锰基纳米内核的制备:
取5mgDHA溶解于5mL丙酮中,然后将蜂窝状二氧化锰纳米颗粒加入DHA的丙酮溶液中,探头超声分散30min,随后放置于真空干燥器中,缓慢蒸发有机溶剂,直到有机溶剂几乎蒸发完全;并用乙醇洗涤几次后冻干,得到锰基纳米内核(MD)。
(4)PM修饰的锰基纳米复合物的制备:
按照PM与二氧化锰的质量比为1:4,取一定量的PM溶于纯水中,搅拌均匀,然后加入到步骤(3)制备的锰基纳米粒内核水分散液中,避光搅拌3h。多余的PM通过离心的方法去除,得到PM修饰的载药锰基纳米复合物(MDP)。
(5)HA修饰的多功能锰基纳米粒的制备:
按照HA与PM的质量比为1.5:1,取一定量HA溶于纯水中,搅拌均匀后,在磁力搅拌的作用下加入到步骤(4)制备的锰基纳米复合物水分散液中,避光条件下搅拌6h,由于阳离子氨基和阴离子羧基的强烈的静电相互作用,将HA吸附在MDP表面。反应结束后离心处理,以除去游离的HA,得到多功能靶向锰基纳米粒(MDPH)。
实施例2.多功能锰基纳米粒基本性质的测定
(1)TEM测试:
取100μL重悬后的二氧化锰纳米颗粒M和多功能锰基纳米粒MDPH,加超纯水稀释后,滴一滴于铜网上,晾干后用透射电子显微镜观察纳米粒形貌。图1(a)的TEM图表征显示,本发明方法制备出的锰纳米颗粒呈蜂窝状,颗粒分散均匀,尺寸均一、粒径约为107.97nm。图1(b)的TEM图表征显示,本发明方法制备出的多功能锰基纳米粒的粒径约为171.06nm,其形态呈蜂窝状,说明二氧化锰经过载药和外层高分子的修饰后,所得纳米粒的粒径较原始锰基纳米内核有所增大,但是纳米粒制备过程中的载药和外层修饰不会影响到锰基纳米内核的蜂窝形状。
(2)H
配置2mL、10μg/mL的MDPH溶液并加入一定量的H
(3)PM的UV-Vis测试:
本发明通过UV-Vis测试对制备出的PM进行表征,如图1(d)所示,二甲双胍在233nm处出现明显的紫外吸收,以壳聚糖为基础制备的PM,由于具有与二甲双胍同样的紫外吸收官能团双胍基,导致PM在233nm处也出现同样的强紫外吸收,说明壳聚糖与二氰二胺通过加成反应后,在壳聚糖上成功接枝双胍基,证明PM的成功合成。
(4)Zeta电势及水动力学直径测试:
取所制备的各纳米粒,用超纯水稀释至50μg/mL后,用于测量其表面电势和水动力学直径。如表1所示,DLS粒度仪测得合成的锰纳米颗粒平均Zeta电位为-19.6mV;当M负载疏水性的化疗药物DHA后,电势基本无变化,表明疏水性DHA负载进入锰纳米颗粒后,对锰纳米颗粒的电位基本无影响;MDP的平均Zeta电位为23.6mV,电势由负到正的变化证明了PM成功地包裹在锰基纳米粒内核外;当HA负载到PM稳定的多功能锰基纳米粒上后,平均Zeta电位转变为负值,证明HA成功地包裹到纳米颗粒上。
表1.
实施例3.多功能锰基纳米粒的细胞摄取情况考察:
为了考察细胞对多功能纳米粒的摄取情况,选用疏水性荧光染料香豆素6(Coumarin6)作为荧光探针,将实施例1步骤(3)中的DHA替换为香豆素6制备出对应的荧光标记的纳米粒,由实施例1步骤(4)制备出MCP;由实施例1步骤(5)制备出MCPH。细胞摄取部分的操作如下:将贴壁生长的4T1细胞去除培养基,用胰酶消化之后用含血清的1640培养基将其稀释。随后将4T1细胞以2×10
实施例4.细胞毒性试验:
采用MTT法,选择对数生长期的4T1鼠乳腺癌细胞,调整细胞数为8000/孔接种于96孔培养板,培养至细胞汇合度达80%。弃去培养基,将梯度浓度的游离药物DHA和PM以及MDPH纳米粒分别加入各孔中,设置5个复孔,每孔100μL,经过24h孵育后,每孔加入10μL MTT(5mg/mL)和90μL无血清的1640培养基4h后弃去上清液,随后弃去上清液,加入150μLDMSO溶解,低速振摇10min后用酶标仪在490nm下测定吸光度,测定纳米粒对4T1细胞的毒性。图2(c)实验结果所示,随着浓度的增加,MDPH的存活率下降,表明具有浓度依赖性的细胞毒性,即呈浓度-效应关系。毒性结果(图2(d))显示游离药物DHA对4T1细胞的毒性较弱,而游离药物PM具有较强的细胞毒性,游离MnO
实施例5.多功能锰基纳米粒对4T1细胞中ROS水平的影响
将处于对数生长期的4T1细胞以2×10
实施例6.多功能锰基纳米粒体内抗肿瘤研究
原位乳腺癌小鼠模型的建立:取对数生长期的4T1细胞并重悬于无血清培养基中,细胞悬液浓度调整为1x10
结果表明多功能锰基纳米粒可以安全有效的作为药物递送平台,结合肿瘤微环境特性,达到化疗协同化学动力学疗法、抑制肿瘤细胞的增殖的效果。
