一种不依赖小麦受体基因型的花粉纳米磁珠遗传转化方法
文献发布时间:2024-04-18 19:58:26
技术领域
本发明涉及农业生物技术领域,具体涉及一种不依赖小麦受体基因型的花粉纳米磁珠遗传转化方法。
背景技术
目前,基于最新的小麦基因组数据挖掘、克隆到的关键功能基因偏少,育种家可用的基因及其标记十分有限,当前可用的标记多局限于品质性状和抗病性等,需要不断加强小麦重要性状功能基因克隆、优异等位变异发掘和功能标记开发,使小麦全基因组选择和分子标记辅助育种技术与常规育种技术有机结合,加快小麦遗传改良,缩短育种年限,提高育种效率。小麦高效DNA导入技术是现代分子育种的重要手段,现有的DNA导入技术如基因枪法、农杆菌法、PEG介导等均过度依赖高效的小麦组培体系,而小麦组培培养严重受限于基因型,而且周期长,成本高,主栽品种的组培效率低的问题,难以满足小麦现代分子育种的需求。
小麦细胞壁限制了外源DNA进入细胞的能力。传统的基因枪轰击法通常涉及加大轰击压强,以增加质粒DNA通过细胞壁进入细胞内的效率。
不管是基因枪轰击,还是农杆菌侵染转化成功导入外源DNA后,需要确保细胞能够再生成植株,小麦愈伤组织的细胞再生的能力和效率受到基因型影响很大,导致目前小麦基因遗传转化的受体材料非常受限。
在导入质粒DNA时,常采用含有抗生素抗性基因的载体,然后通过培养选择对抗生素敏感的细胞。然而,在小麦中,抗生素抗性基因的有效选择可能存在一些挑战。传统的基因枪或农杆菌法转化获得的再生植株需要在培养基上进行抗生素筛选。
因此,急需建立一种高效小麦基因转化体系,突破我国小麦主栽品种功能基因转化的基因型受限的瓶颈问题,为小麦功能基因组分子育种提供强有力技术方法支撑。
发明内容
本发明的目的是提供一种不依赖小麦受体基因型的花粉纳米磁珠遗传转化方法。
根据本发明的不依赖小麦受体基因型的花粉纳米磁珠遗传转化方法,包括以下步骤:
提取及纯化目的质粒DNA,得到目的质粒DNA溶液;
将磁性纳米颗粒与所述目的质粒DNA溶液混合,并在10℃下结合10~20min得到磁性纳米颗粒与目的质粒DNA的复合物(MNP-DNA),磁性纳米颗粒其巨大的比表面积使其能够装载大容量的基因,且其体积微小而具有较强的穿透性,在花粉内高效地运输,并保持核酸分子较高的生物功能活性、最终实现高转染效率;
收集小麦花粉并过筛,所述小麦花粉直径为50-100μm;
配制小麦花粉培养液,以小麦花粉培养液重悬所述磁性纳米颗粒与目的质粒DNA的复合物,获得磁性纳米颗粒与目的质粒DNA的复合物的悬浮液,并将其加入到过筛小麦花粉中,搅拌,置于磁板上10℃静置转染15~20min;
转染结束后,吸去小麦花粉上层的悬浮液,并吸干水分;
撒小麦淀粉,将转染后的花粉和小麦淀粉混匀并分散,得花粉-小麦淀粉混合物,小麦淀粉可快速吸干转染小麦花粉表面的的水分,缩短花粉干燥时间,保持花粉活力;
将获得的花粉-小麦淀粉混合物过100目筛并收集;
利用毛笔对小麦雌蕊柱头进行授粉。
根据本申请的不依赖小麦受体基因型的花粉纳米磁珠遗传转化方法,其中,所述小麦花粉培养液的配方为:蔗糖150g/L、H
根据本申请的不依赖小麦受体基因型的花粉纳米磁珠遗传转化方法,其中,所述磁性纳米颗粒为聚乙烯亚胺修饰的磁性纳米颗粒,其内核为Fe
根据本申请的不依赖小麦受体基因型的花粉纳米磁珠遗传转化方法,其中,用碱裂解法提取及纯化质粒DNA,并用灭菌双蒸水稀释至1μg/μL;
根据本申请的不依赖小麦受体基因型的花粉纳米磁珠遗传转化方法,其中,所述磁性纳米颗粒与所述质粒DNA按质量比1:3混合,并在10℃下结合30min得到磁性纳米颗粒与DNA的复合物MNP-DNA。
根据本申请的不依赖小麦受体基因型的花粉纳米磁珠遗传转化方法,其中,收集小麦花粉并过100目筛除去花药,将过筛小麦花粉转移至培养皿中。
根据本申请的不依赖小麦受体基因型的花粉纳米磁珠遗传转化方法,其中,将小麦花粉过100目筛除去花药。
根据本申请的不依赖小麦受体基因型的花粉纳米磁珠遗传转化方法,其中,转染结束后,吸去小麦花粉上层的悬浮液,将转染后的花粉转移至100目尼龙布上铺匀,并用滤纸吸干水分,所述100目尼龙布孔径为25μm,可截留小麦花粉,而过滤液体,从而最大限度的保留转染的小麦花粉。
本发明的有益效果:
1.根据本发明的不依赖小麦受体基因型的花粉纳米磁珠遗传转化方法采用带正电荷的磁性纳米颗粒作为载体与带负电荷的DNA结合,在磁场作用下,结合了DNA的磁性纳米颗粒通过花粉孔将DNA转运至小麦花粉中,并通过授粉和结实的自然生殖过程,实现外源目的基因的导入及在花粉中的瞬时表达。
2.本发明的方法规避、克服了细胞壁的阻碍问题,通过纳米磁珠质粒复合物在磁场的牵引下进入花粉孔,从而实现外源DNA导入小麦花粉的过程;不涉及小麦愈伤组织再生问题,不受小麦基因型限制;不涉及再生植株抗性筛选问题。
3.本发明采用不依赖于基因型的纳米磁珠介导法,可实现目的基因在所有小麦中的高效导入和瞬时及稳定表达,突破了当前基于组织培养的主流小麦基因导入方法受限于极少数受体材料、导入效率低等瓶颈问题。该方法充分利用小麦开花结实的自然生殖过程,对受体材料和环境条件影响小,节省人力物力,成本低廉。其次,该转染方法操作快捷,从收集小麦花粉到完成转染并授粉的整个过程可在1-2h完成,极大限度的保持了小麦花粉的活力,有利于提高转化结实率,获得大量可供筛选的转化后代。再次,该方法简便高效,仅需提供既定磁场即可完成转化,无需昂贵的仪器设备,可在田间和基地实现大规模小麦转化,开展小麦功能基因组研究工作。
附图说明
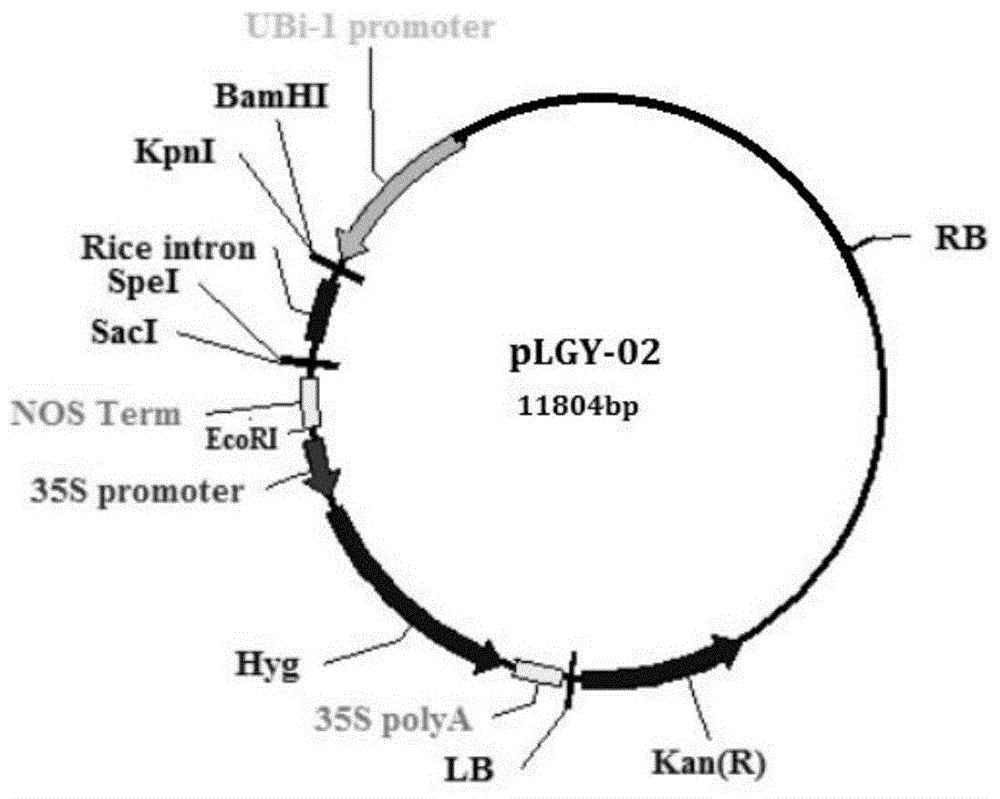
图1为载体pLGY-02结构示意图;
图2为小麦花粉纳米磁珠转染过程流程图;
图3显示ERFP基因在小麦花粉中激光共聚焦荧光检测,MNP+ERFP:磁转染ERFP基因的小麦花粉;MNP:仅加磁珠处理的小麦花粉;CK:未转染的小麦花粉;Merge:红色荧光和明场叠加;RFP:红色荧光;Bright:明场;
图4显示ERFP基因在T
图5为不同温度处理条件下ERFP基因在小麦花粉中红色荧光检测。
具体实施方式
以下实施例中,所用小麦材料为主栽品种:郑麦1860、郑麦7698、济麦22、济麦60、济麦70。
所用载体为含有红色荧光蛋白的表达载体pLGY-02,图谱如图1所示,该载体包括CaMV 35S启动子(p35S)和红色荧光蛋白基因ERFP(Enhance green fluorescentprotein),可用于荧光观察。
实施例1不依赖于小麦基因型的DNA导入
采用聚乙烯亚胺(polyethyleneimine,PEI)修饰的带正电荷的Fe
具体的花粉转染过程如图2所示。
1)用碱裂解法提取并纯化质粒DNA(pLGY-02),并用灭菌双蒸水稀释至1μg/μL;
2)将磁性纳米颗粒和质粒DNA按质量比1:3混匀,10℃结合30分钟,形成MNP-DNA复合物;
3)上午10点左右收集新鲜的小麦花粉,过100目筛子筛除花药,称取过筛花粉约5g,转移至直径9cm的塑料培养皿中;
4)用20mL小麦花粉培养液(含蔗糖150g/L、H
5)转染结束后,小心吸去花粉上层的悬浮液,将转染后的花粉转移至100目尼龙布上铺匀,并用滤纸吸干水分;
6)将尼龙布展开,均匀撒上约0.2g小麦淀粉,用干净刷子将黏在尼龙布上的花粉和小麦淀粉混匀,并分散成细小的颗粒;
7)将转染花粉与小麦淀粉混合后过100目筛,并转入纸袋中;
8)对小麦自交系雌蕊(提前去雄)25-30穗进行授粉,授粉14天后可见灌浆籽粒。
实施例2荧光跟踪导入过程(以济麦22为例)
ERFP基因在小麦花粉中的表达。蘸取适量转染后的花粉,接种于小麦花粉液体培养基上,10℃黑暗条件下培养20小时。用毛笔蘸取适量培养后的小麦花粉,在培养液轻柔分散开,并在激光共聚焦显微镜下用488nm激发光观察红色荧光。荧光观察结果所示。图3中,A.纳米磁珠转染ERFP基因的小麦花粉明场结果;B.纳米磁珠转染ERFP基因的小麦花粉暗场结果;C.纳米磁珠转染ERFP基因的小麦单个花粉放大的明场结果;D.纳米磁珠转染ERFP基因的小麦单个花粉放大的暗场结果;E.纳米磁珠未转染RFP的小麦花粉明场结果;F.纳米磁珠未转染RFP的小麦花粉暗场结果;RFP:红色荧光蛋白。如图3所示,转染了ERFP基因的花粉中可见红色荧光,而未转染的花粉中无红色荧光,证明通过纳米磁珠转染可将ERFP基因导入小麦花粉中并实现表达。
实施例3转染ERFP济麦22T
在三叶期,取转染ERFP的济麦22T
表1 UBI启动子引物信息
实施例4 ERFP基因在不同自交系中转化率分析
进一步分析纳米磁珠转化法在5种不同小麦品种转化效率。将CaMV 35S启动子驱动的ERFP基因转染郑麦1860、郑麦7698、济麦22、济麦60、济麦70花粉,收获种子并发芽。在三叶期,取T
表2不同受体品种转化率统计
实施例5小麦花粉孔开孔的温度对质粒DNA进入花粉的效率的影响
如图5所示,通过6℃、8℃、10℃、12℃、14℃、16℃温度梯度设置,激光共聚焦红色荧光分析发现10℃红色荧光蛋白信号最强,说明含有红色荧光蛋白的质粒DNA进入花粉孔的比例高,从而实现质粒DNA进入花粉的转化过程。
上述的实施例仅是本发明的部分体现,并不能涵盖本发明的全部,在上述实施例以及附图的基础上,本领域技术人员在不付出创造性劳动的前提下可获得更多的实施方式,因此这些不付出创造性劳动的前提下获得的实施方式均应包含在本发明的保护范围内。
- 一种不依赖于基因型的植物基因编辑方法
- 一种阪崎肠杆菌噬菌体偶联的纳米磁珠及其制备方法和应用
- 一种不依赖基因型的除虫菊遗传转化方法
- 一种以大豆子叶节为受体不依赖组织培养的大豆遗传转化新方法
