一种新型冠状病毒T细胞的抗原表位肽及其应用
文献发布时间:2023-06-19 11:13:06
技术领域
本发明涉及生物技术领域,具体地,涉及一种新型冠状病毒T细胞抗原表位肽及其应用。
背景技术
新型冠状病毒是2019年底发生的新型传染性肺炎的病原体,目前对病毒的来源尚不清楚,基因测序显示和蝙蝠SARS样冠状病毒、严重急性呼吸综合征冠状病毒(SARS-CoV),中东呼吸综合征冠状病毒(MERS-CoV)高度同源。目前尚没有特效药物报道。人体免疫系统对新型冠状病毒的免疫应答机制,包括抗原识别、免疫清除机制、免疫记忆保护机制等均不清楚。
根据对新型冠状病毒同源性较高的SARS等冠状病毒的研究显示,T细胞免疫应答在病毒感染后机体抗病毒防御以及机体免疫病理损伤过程中发挥了重要的作用,尤其是CD8
疫苗的作用原理是利用抗原表位活化机体的初始淋巴细胞,经过活化、增殖、分化后清除抗原物质。活化的淋巴细胞转变成记忆性淋巴细胞,在下一次同样的抗原物质侵入机体时,快速发挥免疫应答作用,清除抗原。目前的疫苗以诱发机体体液免疫应答,产生抗体为主。新冠病毒疫苗也以诱导抗体等体液免疫应答为主。目前尚没有针对T细胞的细胞免疫疫苗的研究报道。
CD8
发明内容
本发明的目的是为了克服现有技术的上述不足,提供一种新型冠状病毒T细胞的抗原表位肽及其应用,本发明的抗原表位肽可以和HLA-A2重链和HLA-A2轻链β2m蛋白组装成pMHC复合物,或直接负荷到抗原递呈细胞,从而活化T细胞,可用于新冠病毒疫苗研发、制备和药物研发、临床治疗。
本发明的第一个目的是提供一种新型冠状病毒T细胞的抗原表位肽。
本发明的第二个目的是提供一个种新型冠状病毒T细胞的抗原表位肽组合。
本发明的第三个目的是提供所述抗原表位肽和/或所述抗原表位肽组合在在制备抗原递呈细胞中的应用。
本发明的第四个目的是提供一种的pMHC复合物。
本发明的第五个目的是一种所述的pMHC复合物的制备方法。
本发明的第六个目的是一种抗原肽-抗原递呈细胞复合物。
本发明的第七个目的是一种用于活化T细胞的抗原肽-抗原递呈细胞复合物的制备方法。
本发明的第八个目的是所述的抗原表位肽、所述的抗原表位肽组合、所述的pMHC复合物、所述的抗原肽-抗原递呈细胞复合物中的一种或几种制备新型冠状病毒疫苗和/或药物中的应用。
本发明的第九个目的是所述的抗原表位肽、所述的抗原表位肽组合、所述的pMHC复合物、所述的抗原肽-抗原递呈细胞复合物中的一种或几种制备新型冠状病毒检测试剂中的应用。
为了实现上述目的,本发明是通过以下方案予以实现的:
T2A2细胞是一种通过重组基因工程技术表达人MHC-I类分子HLA-A2的抗原递呈细胞系。只有有效的抗原表位才能被其递呈,从而在其细胞表面形成稳定的pMHC复合物,因此可以作为刺激T细胞的人工抗原递呈细胞。
T细胞抗原表位单独无法工作,必须以pMHC复合物或抗原肽-抗原递呈细胞复合物的方式进行T细胞活化。本发明利用基因工程重组的HLA-A2重链和轻链蛋白,和鉴定出的新型冠状病毒T细胞表位进行联合复性,制备了pMHC复合物,直接将鉴定出的新型冠状病毒T细胞抗原表位负荷在抗原递呈细胞表面,制备了抗原肽-抗原递呈细胞复合物 (T2A2细胞),发现其可以有效活化健康人外周血中T细胞。活化的T细胞可以有效杀伤携带新冠病毒抗原的靶细胞。证明新发现的新型冠状病毒T细胞抗原表位具有完全的生物学活性,可以作为疫苗和免疫治疗的应用。
因此本发明要求保护一种新型冠状病毒T细胞的抗原表位肽,其氨基酸序列如SEQID NO:1~13任一所示。
SEQ ID NO:1:FVFLVLLPLV;
SEQ ID NO:2:FTISVTTEI;
SEQ ID NO:3:VVFLHVTYV;
SEQ ID NO:4:YIWLGFIAGL;
SEQ ID NO:5:VTWFHAIHV;
SEQ ID NO:6:FLHVTYVPA;
SEQ ID NO:7:SVLLFLAFV;
SEQ ID NO:8:FLLVTLAIL;
SEQ ID NO:9:FLFLTWICLL;
SEQ ID NO:10:LIFLWLLWPV;
SEQ ID NO:11:TLACFVLAAV;
SEQ ID NO:12:FVLAAVYRI;
SEQ ID NO:13:GLMWLSYFI。
本发明还要求保护一种新型冠状病毒T细胞的抗原表位肽组合,含有氨基酸序列如 SEQ ID NO:1~13所示的抗原表位肽中的任意几条。
所述抗原表位肽和/或所述抗原表位肽组合在在制备抗原递呈细胞中的应用,也属于本发明的保护范围。
本发明还要求保护一种的pMHC复合物,含有所述的抗原表位肽或含有所述的抗原表位肽组合。
一种pMHC复合物的制备方法,将HLA-A2重链、HLA-A2轻链β2m和所述的抗原表位肽或所述的抗原表位肽组合混合复性,纯化。
优选地,HLA-A2重链、HLA-A2轻链β2m和所述的抗原表位肽或所述的抗原表位肽组合的摩尔为1:2:10。
本发明还要求保护一种抗原肽-抗原递呈细胞复合物,表面有所述的抗原表位肽或所述的抗原表位肽组合的抗原递呈细胞。
优选地,所述抗原递呈细胞为T2A2细胞。
更优选地,T2A2细胞是过表达HLA-A2的T2细胞。
一种用于活化T细胞的抗原肽-抗原递呈细胞复合物的制备方法,将含有所述新型冠状病毒T细胞抗原表位肽与抗原递呈细胞混合孵育,之后用于T细胞活化。
优选地,所述抗原递呈细胞为T2A2细胞。
一种融合蛋白,含有所述的抗原表位肽组合。
所述的抗原表位肽、所述的抗原表位肽组合、所述的pMHC复合物、和/或所述的抗原肽-抗原递呈细胞复合物中的一种或几种制备新型冠状病毒疫苗和/或药物中的应用。
以及,所述的抗原表位肽、所述的抗原表位肽组合、所述的pMHC复合物、和/或所述的抗原肽-抗原递呈细胞复合物中的一种或几种制备新型冠状病毒检测试剂中的应用。
与现有技术相比,本发明具有以下有益效果:
本发明发现了13种新型冠状病毒T细胞抗原表位肽,并利用其制备得到了pMHC复合物单聚体,进一步制备得到pMHC复合物多聚体,其可以用于新型冠状病毒感染康复者外周血内抗原特异性T细胞的检测,并用于体外的T细胞活化实验,这些新型冠状病毒 T细胞抗原表位肽可以应用到新型冠状病毒相关的免疫检测中,值得深入研究和大力推广。
抗原表位肽和HLA-A2重链和HLA-A2轻链β2m蛋白组装成pMHC复合物,或直接负荷到抗原递呈细胞,从而活化T细胞,可用于新冠病毒疫苗研发、制备和药物研发、临床治疗,可应用于:
1)新冠疫苗的研发和制备。只有在感染后,机体产生免疫应答之后才会生成抗原特异性T细胞。故该T细胞的检测代表曾经感染过新冠病毒。
2)检测是否具有抵抗新冠病毒感染的细胞免疫功能。同上,待检者体内检测到新冠病毒抗原特异性T细胞,代表机体已经产生了T细胞免疫功能,根据其比例,可以评价机体对新型冠状病毒感染的T细胞免疫功能强弱。
3)监测病情。可用于对密切接触者、医学观察者、疑似和确诊患者的病情变化监测。
4)预后判断。如果机体不能产生T细胞免疫应答,或抗原特异性T细胞比例持续减少,则预示预后不佳。
附图说明
图1为验证丝裂霉素干预T2A2细胞是否影响与抗原肽的结合效果和其是否抑制T2A2细胞增殖;A:是验证丝裂霉素干预T2A2细胞是否影响与抗原肽的结合效果。设置 6组,分别T2A2空白组,T2A2(MC 10μg/mL,2h),T2A2(MC 20μg/mL,20min), T2A2(10μM阳性对照肽(甲型流感M1多肽,GILGFVFTL)),T2A2(MC 10μg/mL,2 h+10μM阳性对照肽),T2A2(MC 20μg/mL,20min+10μM阳性对照肽);B:结果汇总显示丝裂霉素干预的T2A2细胞后不影响与抗原肽结合。C:丝裂霉素抑制T2A2细胞增殖。流式仪检测第0天和第7天T2A2标记有CFSE的情况;D:结果汇总显示丝裂霉素(20μg/mL,20min)可抑制T2A2细胞增殖。
图2为新型冠状病毒T细胞共39种抗原表位的T2A2鉴定,阴性对照肽 (GLQRLGYVL,来源于寨卡病毒基因编码),阳性对照肽(甲型流感M1多肽, GILGFVFTL);A:15种新冠病毒抗原多肽的T2A2鉴定实验;B:15种新冠病毒抗原多肽的T2A2鉴定实验;C:9种新冠病毒抗原多肽的T2A2鉴定实验;A1、B1和C1:三次实验重复的小结。
图3为39种抗原肽形成pMHC复合物的检测及应用;A:ELISA法筛选39种新型冠状病毒T细胞抗原表位,用紫外敏感肽/MHC复合物和上述的39种肽进行肽交换分析,利用人HLA-A2酶联免疫分析,用酶标仪在450nm波长下测定吸光度(OD值)。空白对照::磷酸缓冲盐溶液(PBS);阳性对照肽(甲型流感M1多肽,GILGFVFTL);紫外线对照:紫外线照射的紫外线敏感肽;B:pMHC复合物组装后的DEAE cellulose离子交换柱纯化;C:pMHC复合物组装后的分子筛(GE Superdex75pg)纯化;D:流式细胞术检测HLA-A2
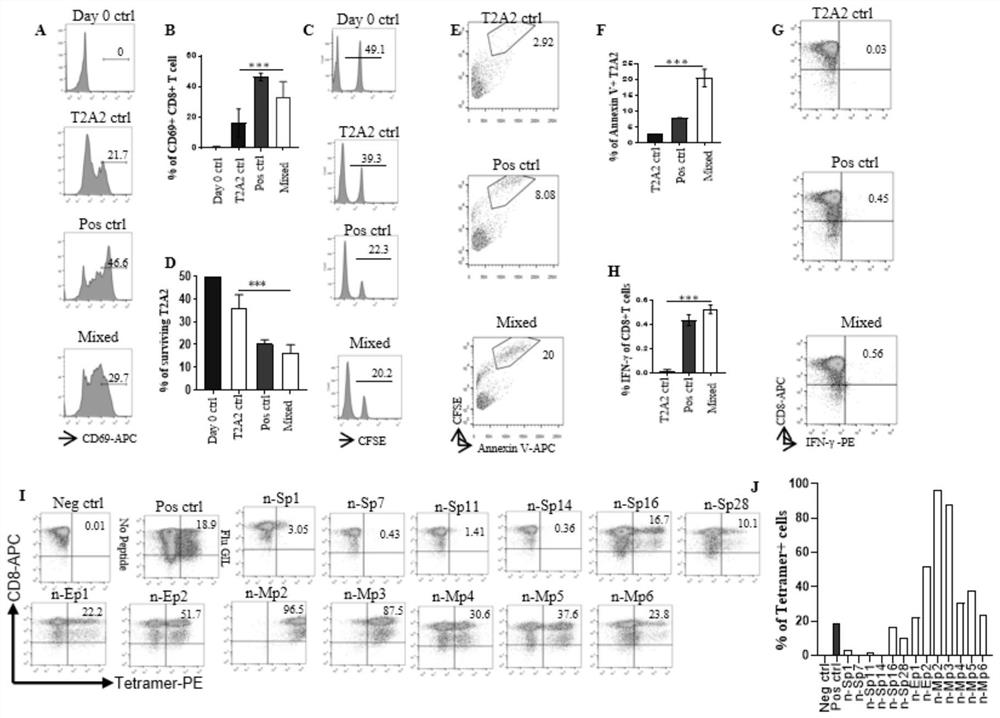
图4评价39种抗原肽对CD8+T细胞的活化和细胞毒性作用;A:T细胞活化标记物CD69的表达水平,上述39种抗原肽混合物诱导T细胞CD69表达,Blank(单纯的T2A2), T2A2-ctrl(T2A2不含肽与CD8+T细胞共培养),Pos-ctrl(甲型流感M1肽GILGFVFTL) 为阳性对照;B:结果汇总显示该抗原肽混合物可刺激T细胞活化;C:39种抗原肽诱导特异性CD8+T细胞介导的细胞的杀伤作用,CFSE标记的T2A2细胞为存活靶细胞;Day 0-ctrl:刺激前染色;T2A2-ctrl(T2A2不含肽与CD8+T细胞共培养);Pos-ctrl(甲型流感M1肽GILGFVFTL)为阳性对照;D:结果汇总显示上述抗原肽可杀伤靶细胞(T2A2 细胞);E:39种特异性CD8+T细胞介导的靶细胞的凋亡,T2A2-ctrl(T2A2不含肽与 CD8+T细胞共培养),Pos-ctrl(甲型流感M1肽GILGFVFTL)为阳性对照,流式细胞仪检测标记有CFSE和凋亡标记物Annexin V-APC的T2A2细胞的凋亡比例;F:结果汇总显示上述抗原肽可诱导靶细胞(T2A2细胞)凋亡;G:39种特异性特异性CD8+T细胞IFN- γ
具体实施方式
下面结合说明书附图及具体实施例对本发明作出进一步地详细阐述,所述实施例只用于解释本发明,并非用于限定本发明的范围。下述实施例中所使用的试验方法如无特殊说明,均为常规方法;所使用的材料、试剂等,如无特殊说明,为可从商业途径得到的试剂和材料。
实施例1新冠病毒HLA-A2限制性抗原表位的预测
一、实验方法
利用MHC-I结合工具(http://tools.iedb.org/mhci),对SARS-CoV-2武汉株(NC_045512.2)、 SARS-CoV-GD01株(AY278489.2)、MERS-CoV株(KF600612.1)和人冠状病毒OC43株(KF530099.1)的spike(S)、membrane(M)和nucleocapsid(N)蛋白序列进行T 细胞表位预测。所采用的预测方法为IEDB推荐的2.22(NetMHCpan-EL),MHC等位基因选择为HLA-A*02:01和HLA-A*02:06(中国人群中最常见的I类HLA基因型)。从 GISAID数据库中提取每个表位的变异序列(GISAID.org网站)以便进一步分析。
二、实验结果
筛选大量出高效特异的T细胞抗原表位候选物。其信息如表1所示。
表1新型冠状病毒T细胞抗原表位肽:
实施例2丝裂霉素干预T2A2细胞是否影响与抗原肽的结合
一、实验方法
取对数生长状态T2A2细胞(174x CEM.T2(
二、实验结果
丝裂霉素干预T2A2后,不影响与抗原肽的结合(图1A和图1B)。图1A显示T2A2 分别用10μg/mL处理2小时(组2)、20μg/mL处理20分钟后(组3)、以及T2A2加上阳性抗原表位肽同时分别用10μg/mL处理2小时(组5)、20μg/mL处理20分钟后(组 6),和药物未处理组(组1和组4)比较,抗原肽的结合不受影响(组4、5和6比较无区别)。图1B是图1A的统计图示。
实施例3丝裂霉素抑制T2A2细胞增殖
一、实验方法
取对数生长状态T2A2细胞,种植到96孔板,每孔10
二、实验结果
丝裂霉素MC干预T2A2后,可抑制该细胞增殖(图1C和图D)。图1C显示CFSE 标记成功(中间组第0天荧光峰值右移)。第7天后CFSE依旧显示单峰,代表T2A2细胞没有增殖,可以作为人工抗原递呈细胞而不会在混合培养中干扰T细胞生长。图1D是图1C的统计图示。
实施例4新冠病毒HLA-A2限制性抗原表位肽的鉴定
一、实验方法
人工合成实施例3预测得到的39种多肽,配置成浓度为10μM。取对数生长状态T2A2细胞,种植到96孔板,每孔10
二、实验结果
结果如图2A、图2B和图2C所示,结果显示39种抗原多肽均可以被抗原递呈细胞有效递呈。
实施例5 39种抗原多肽形成pMHC复合物的检测
一、实验方法
ELISA法检测实施例3预测得到的39种新型冠状病毒T细胞抗原表位,用紫外敏感肽(KILGFVFJV)/MHC复合物和上述的实施例3预测得到的39种肽进行肽交换分析,然后用纯化的人HLA-A2捕获抗体包被微孔板,制成固相抗体,往包被的微孔中依次加入上述与紫外敏感肽交换的39种肽,再与HRP标记的检测抗体结合,形成抗体-抗原-酶标抗体复合物,经过彻底洗涤后加底物TMB显色。TMB在HRP酶的催化下转化成蓝色,并在酸的作用下转化成最终的黄色。颜色的深浅和样品中的pMHC呈正相关,用酶标仪在450nm波长下测定吸光度(OD值)。
二、实验结果
结果如图3A所示,结果显示39种抗原多肽均可以形成pMHC复合物。
实施例6抗原表位肽的pMHC复合物单体的制备
一、实验方法
将HLA-A2重链、HLA-A2轻链β2m和实施例3中的每个抗原表位多肽分别按照 1:2:10的摩尔比逐步滴加至复性溶液(5M尿素,0.4M精氨酸,100mM Tris,3.7mM 胱胺,6.3mM半胱胺,2mM EDTA)中进行复性,得到抗原表位肽的pMHC复合物单体。pMHC复合物单体经过DEAE离子交换柱进一步纯化,以0.5M NaCl洗脱,并根据 OD280nm紫外吸收峰收集蛋白。随后经DEAE离子交换柱纯化后的蛋白根据分子量大小,通过Superdex 75pg分子筛纯化,以PBS洗脱,并根据OD280nm紫外吸收峰收集不同分子量蛋白。
二、实验结果
经过纯化后,得到抗原表位肽的pMHC复合物单体(图3B,C)。
实施例7抗原表位在新型冠状病毒感染康复者体内的应用
一、实验方法
由于表达的HLA-A2带有生物素结合位点,通过生物素和亲和素系统,将荧光标记的亲和素(PE-streptavidin)、生物素和pMHC复合物单体按照1:4:4的摩尔比例混合4℃避光孵育16~18小时,制备荧光标记的新冠病毒T细胞抗原表位tetramer(即tetramer-PE)。通过Superdex 75pg分子筛纯化,以PBS洗脱,并根据OD280nm紫外吸收峰收集不同分子量蛋白。
分离新型冠状病毒感染康复者复检时外周静脉血中的PBMC,并鉴定其HLA亚型,HLA-A2阳性PBMC样品进一步用制备得到的tetramer-PE和CD8-APC抗体进行染色,然后进行流式上机检测。
二、实验结果
结果显示,上述的实施例3得到的39种抗原表位肽tetramer可以识别新型冠状病毒感染康复者体内产生的抗原特异性CD8
实施例8新冠病毒HLA-A2限制性抗原表位肽活化T细胞
一、实验方法
T2细胞通过表达HLA-A2分子(T2A2)来活化T细胞。分离健康志愿者的外周静脉血中的单个核淋巴细胞(PBMC),并进一步分离CD8
二、实验结果
上述39种中共有13种不同抗原表位肽(n-Sp1、n-Sp7、n-Sp11、n-Sp14、n-Sp16、 n-Sp28、n-Ep1、n-Ep2、n-Mp2、n-Mp3、n-Mp4、n-Mp5、n-Mp6,氨基酸序列如SEQ ID NO:1~13所示)都能够活化T细胞表达CD69(图4A-B)。这13种抗原表位肽活化的 T细胞可以有效杀伤T2A2细胞,表现为存活T2A2比例下降(图4C-D)。同时残余的 T2A2细胞凋亡比例增加(图4E-F,CFSE和Annexin V双阳性)。T细胞的杀伤作用是通过分泌IFN-γ来实现(图4G-H)。最后,经过7天培养后,这13种抗原表位可以诱导出抗原特异性记忆T细胞(图4I-J)。综合所有数据,这13种抗原表位为有效抗原表位,可以被有效抗原递呈,活化T细胞,杀伤靶细胞,并诱导产生记忆T细胞。
最后所应当说明的是,以上实施例仅用以说明本发明的技术方案而非对本发明保护范围的限制,对于本领域的普通技术人员来说,在上述说明及思路的基础上还可以做出其它不同形式的变化或变动,这里无需也无法对所有的实施方式予以穷举。凡在本发明的精神和原则之内所作的任何修改、等同替换和改进等,均应包含在本发明权利要求的保护范围之内。
序列表
<110> 暨南大学
<120> 一种新型冠状病毒T细胞的抗原表位肽及其应用
<160> 13
<170> SIPOSequenceListing 1.0
<210> 1
<211> 10
<212> PRT
<213> 人工序列(Artificial Sequence)
<400> 1
Phe Val Phe Leu Val Leu Leu Pro Leu Val
1 5 10
<210> 2
<211> 9
<212> PRT
<213> 人工序列(Artificial Sequence)
<400> 2
Phe Thr Ile Ser Val Thr Thr Glu Ile
1 5
<210> 3
<211> 9
<212> PRT
<213> 人工序列(Artificial Sequence)
<400> 3
Val Val Phe Leu His Val Thr Tyr Val
1 5
<210> 4
<211> 10
<212> PRT
<213> 人工序列(Artificial Sequence)
<400> 4
Tyr Ile Trp Leu Gly Phe Ile Ala Gly Leu
1 5 10
<210> 5
<211> 9
<212> PRT
<213> 人工序列(Artificial Sequence)
<400> 5
Val Thr Trp Phe His Ala Ile His Val
1 5
<210> 6
<211> 9
<212> PRT
<213> 人工序列(Artificial Sequence)
<400> 6
Phe Leu His Val Thr Tyr Val Pro Ala
1 5
<210> 7
<211> 9
<212> PRT
<213> 人工序列(Artificial Sequence)
<400> 7
Ser Val Leu Leu Phe Leu Ala Phe Val
1 5
<210> 8
<211> 9
<212> PRT
<213> 人工序列(Artificial Sequence)
<400> 8
Phe Leu Leu Val Thr Leu Ala Ile Leu
1 5
<210> 9
<211> 10
<212> PRT
<213> 人工序列(Artificial Sequence)
<400> 9
Phe Leu Phe Leu Thr Trp Ile Cys Leu Leu
1 5 10
<210> 10
<211> 10
<212> PRT
<213> 人工序列(Artificial Sequence)
<400> 10
Leu Ile Phe Leu Trp Leu Leu Trp Pro Val
1 5 10
<210> 11
<211> 10
<212> PRT
<213> 人工序列(Artificial Sequence)
<400> 11
Thr Leu Ala Cys Phe Val Leu Ala Ala Val
1 5 10
<210> 12
<211> 9
<212> PRT
<213> 人工序列(Artificial Sequence)
<400> 12
Phe Val Leu Ala Ala Val Tyr Arg Ile
1 5
<210> 13
<211> 9
<212> PRT
<213> 人工序列(Artificial Sequence)
<400> 13
Gly Leu Met Trp Leu Ser Tyr Phe Ile
1 5
- 一种新型冠状病毒T细胞抗原表位肽、pMHC及其制备和应用
- 一种新型冠状病毒T细胞的抗原表位肽及其应用
