基于虚拟现实的药物设计云计算流程控制系统及其方法
文献发布时间:2023-06-19 09:30:39
技术领域
本发明属于基于人工智能的药物设计领域,尤其涉及基于虚拟现实技术的药物设计云计算流程控制方法。
背景技术
传统的计算机辅助药物设计方法,主要是基于结构的药物设计方法已经广泛的应用于新药研发领域。
这些传统的药物设计都是基于开源或者商业软件来完成,分为基于Linux平台或者基于Windows平台。
典型的药物设计方法或者软件有: Maestro软件, MOE软件,Amber 分子动力学软件,Autudock分子对接软件,Pymol显示软件,VMD显示软件等。
这些药物设计方法虽然广泛使用,但是有如下缺陷:
1.流程整合有限:开源软件一般都能够独立完成特定的计算任务,但是如果需要整合这些开源软件来完成更为复杂的功能,需要自行编写脚本整合多个软件,而且不同的软件有不同的输入输出格式等,整合会存在一定的难度。商业软件功能上更加完善,而且有相对完善的流程,但是软件费用一般也较为昂贵。因为是商业软件,如果想进行二次开发,也存在一定的接入难度。
2.不能跨平台调度:当前几乎所有的软件,如果需要使用云计算平台,都需要先手动登录、编写任务脚本,再提交到各自的平台上计算。
3.可视化主要是基于显示器的2D或者伪3D显示,对一些复杂的三维结构,如小分子和靶点的复合物,存在一定的展示难度。
发明内容
为了解决以上技术问题,本发明提供一种基于虚拟现实技术的药物设计云计算流程控制方法。
为实现上述目的,本发明所采用以下方案:
本发明主要是基于人工智能和虚拟现实技术的药物设计云计算流程控制系统,该系统包括药物设计模块组、交互和调度模块和虚拟现实药物设计模块;
所述的药物设计模块组包括验证模块、数据库模块、过滤模块、预处理模块、方法模块、分析模块;所述的药物设计模块组包括典型的药物设计方法和软件,具体包括 Maestro软件, MOE软件,Amber 分子动力学软件,Autudock分子对接软件,Pymol显示软件,VMD显示软件,以模块的形式展现,用户可以根据项目需求自由选择和组合相应的模块来进行计算;
所述的方法模块包括分子对接模块(Molecular docking),分子动力学模块(Molecular Dynamics),结合自由能计算模块(MMGBSA/MMPBSA),自由能微扰模块(FEP),药效团模块(Pharmacophore),人工智能分子生成模块,ADMET预测模块。
所述的交互和调度模块包括Jupyter单元和Majorana任务调度平台;
所述的Jupyter单元是与用户进行交互的界面,用户可以项目的需求通过Jupyter单元发出调用各种模块的指令完成进行相应的药物设计操作;也可以通过调用虚拟现实药物设计模块,使整个药物设计操作以虚拟现实的可视化操作方式完成,并展示操作的结果;
所述的Majorana任务调度平台是一个内部开发的调度系统,其功能是通过接收Jupyter单元发出的用户指令在药物设计模块组中调取相应的任务模块来计算,将计算任务提交到指定的云计算平台,并查看计算任务状态;所述的查看计算任务状态主要包括任务是否提交成功,任务占用CPU,GPU数,任务的状态(启动,执行,完成等),任务日志,输出文件等。
所述的云计算平台包括亚马逊云,腾讯云,阿里云,Majorana任务调度平台内置了对接各个云计算平台的任务执行脚本和任务监控脚本,用户可以根据计算的需求轻松实现跨平台云计算需求;
所述的虚拟现实药物设计模块包括虚拟现实硬件设备:显示器、虚拟现实眼镜,虚拟现实姿势识别器和电脑鼠标,通过操作虚拟现实硬件设备可以使药物设计云计算流程控制方法通过虚拟现实的可视化操作方式操作完成,并可以等计算完成后及时显示结果。
所述的虚拟现实药物设计模块中所述的可视化操作可以以2D或者3D的方式进行操作;
所述的虚拟现实药物设计模块中所述的显示结果可以以2D或者3D的方式进行展示;
所述的虚拟现实药物设计模块可以根据用户的需求自主选择是否采用虚拟现实的方式来操作;
基于虚拟现实技术的药物设计云计算流程控制方法,包括以下过程:
(a)小规模的验证
小规模的验证首先调用验证模块,包括预处理,数据库,方法和分析四个子模块,可以根据项目的实际需求选择所需要的子模块,通过选用合适的子模块进行分析,验证,得到相应的参数,并记录下来。
所述的小规模的验证是一个简单版本的流程,主要目的是小规模的验证计算方法在相应研究体系中的表现,验证完成后的参数会应用到正式的筛选流程当中;具体验证的子模块主要根据项目的实际需求来确定。
(b)数据读入
调用数据库模块读取原始的数据和结构,主要是从数据库中将靶点和小分子化合物的结构信息读入到工作流程中;
(c)过滤筛选
调用过滤模块对小分子数据库进行初步的过滤筛选,主要内容是通过成药性五规则过滤掉一些成药性不佳的分子;
(d)预处理
调用预处理模块处理数据库模块读取的靶点和小分子数据,进行正式计算前的预处理工作。一般预处理主要分为靶点的预处理和小分子的预处理。靶点的预处理主要包括:晶体结构中靶点缺失残基的修补,加氢,加电荷,氨基酸的质子化等,并保存成标准的PDB格式;
所述小分子的预处理方法为:数据库过滤后的每个小分子都要进行预处理,主要包括平面二维结构转三维结构,最低能量构象搜索,PKa计算,加氢,加电荷等,并保存成标准的格式,如SDF格式。
(e)计算分析
调用方法模块,根据实际的计算需求,调用相应的模块进行计算分析,方法模块中包括分子对接模块(Molecular docking),分子动力学模块(Molecular Dynamics),结合自由能计算模块(MMGBSA/MMPBSA),自由能微扰模块(FEP),药效团模块(Pharmacophore),人工智能分子生成模块,ADMET预测模块等主要计算分析模块;
(f)云计算
调用Majorana任务调度平台,根据方法模块的计算需求,提交计算任务到指定云平台(亚马逊云,腾讯云,阿里云等)并查看计算任务状态。Majorana是内部开发的一个调度系统,主要包括任务是否提交成功,任务占用CPU,GPU数,任务的状态(启动,执行,完成等),任务日志,输出文件。
(g)结果展示
调用分析模块分析展示结果,任务数据会自动写入到数据库模块中。展示结果主要根据方法模块中调用了哪些方法有关,主要内容包括对结合模式,分子动力学轨迹,化合物结构,化合物性质等,利用图表,动画展示这些化合物结构的稳定性,小分子靶点之间的关键相互作用,能量值等。此处以分子对接和自由能计算为例。分子对接完成后,系统可以展示软件计算得到的结合模式,标记关键的小分子和靶点之间的相互作用,如氢键,疏水相互作用,极性相互作用等,并可以输出成PNG格式图片,GIF动画等标准格式方便日后回看及展示。自由能计算可以展示如计算得到的自由能值,误差,动力学轨迹稳定性等,亦可以输出成PNG格式图片,GIF动画等方便日后回看及展示。
(h)循环执行
步骤(b)-(g)会循环执行,是否终止取决于预设的指标,比如预测得到100个活性较好的化合物,预测得到能量值在某个范围区间的分子等,满足标准可以停止次轮计算等。
基于虚拟现实技术的药物设计云计算流程控制方法的完整过程包括以上步骤(a)-(h),用户也可以根据项目的需求自由的组合步骤(a)-(h)。
本发明带来了如下有益效果:
a)实现了高通量、高并行的基于虚拟现实技术的药物设计云计算任务的跨平台调度。
b)无缝衔接了新药筛选流程的分子处理,评估,和分析等功能。
c)将所有分子对接及虚拟筛选任务的创建、提交和管理,结果分析和绘图等步骤集成到Jupyter中,实现了分子对接云计算流程的可视化操作。
d)引入了虚拟显示技术,可以更加真实的进行基于结构的理性药物设计。。
附图说明
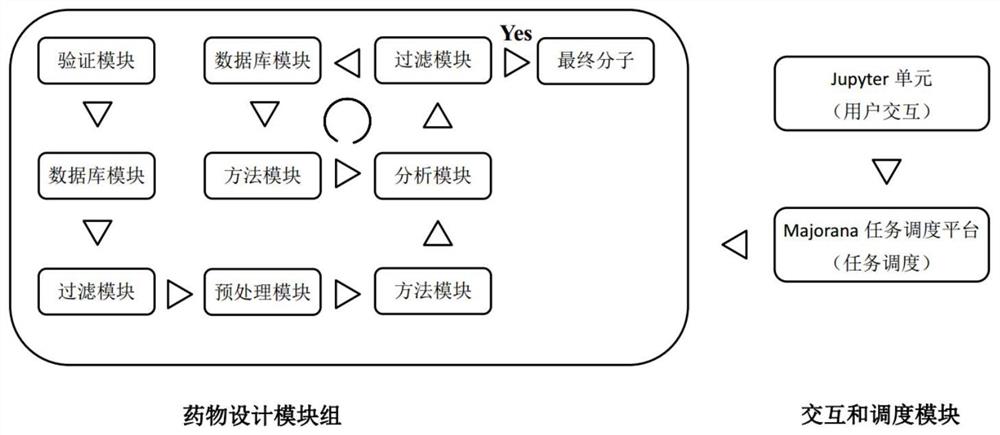
图1是基于虚拟现实技术的药物设计云计算流程控制方法的流程示意图。
图2是基于虚拟现实技术的药物设计云计算流程控制方法的验证模块具体内容。
图3是基于虚拟现实技术的药物设计云计算流程控制方法的方法模块具体内容。
图4 是实施例1生物实验测试-计算预测活性相关性图。
图5 是实施例2中,传统流程与Majorana任务调度系统的CPU运行时间的对比。
图6 是实施例3中药物设计方法结果展示图。
图7 是实施例4中分子描述结果展示图。
图8 是实施例4中结合模式结果展示图。
具体实施方式
下面结合附图,对本发明的较优的实施例作进一步的详细说明:
实施例1
如图1-3所示,基于人工智能和虚拟现实技术的药物设计云计算流程控制系统,该系统包括药物设计模块组、交互和调度模块和虚拟现实药物设计模块;
所述的药物设计模块组包括验证模块、数据库模块、过滤模块、预处理模块、方法模块、分析模块;所述的药物设计模块组包括典型的药物设计方法和软件,具体包括 Maestro软件, MOE软件,Amber 分子动力学软件,Autudock分子对接软件,Pymol显示软件,VMD显示软件,以模块的形式展现,用户可以根据项目需求自由选择和组合相应的模块来进行计算;
所述的方法模块包括分子对接模块(Molecular docking),分子动力学模块(Molecular Dynamics),结合自由能计算模块(MMGBSA/MMPBSA),自由能微扰模块(FEP),药效团模块(Pharmacophore),人工智能分子生成模块,ADMET预测模块。
所述的交互和调度模块包括Jupyter单元和Majorana任务调度平台;
所述的Jupyter单元是与用户进行交互的界面,用户可以项目的需求通过Jupyter单元发出调用各种模块的指令完成进行相应的药物设计操作;也可以通过调用虚拟现实药物设计模块,使整个药物设计操作以虚拟现实的可视化操作方式完成,并展示操作的结果;
所述的Majorana任务调度平台是一个内部开发的调度系统,其功能是通过接收Jupyter单元发出的用户指令在药物设计模块组中调取相应的任务模块来计算,将计算任务提交到指定的云计算平台,并查看计算任务状态;所述的查看计算任务状态主要包括任务是否提交成功,任务占用CPU,GPU数,任务的状态(启动,执行,完成等),任务日志,输出文件等。
所述的云计算平台包括亚马逊云,腾讯云,阿里云,Majorana任务调度平台内置了对接各个云计算平台的任务执行脚本和任务监控脚本,用户可以根据计算的需求轻松实现跨平台云计算需求;
本发明与已有技术不同在于:所述的虚拟现实药物设计模块包括虚拟现实硬件设备:显示器、虚拟现实眼镜,虚拟现实姿势识别器和电脑鼠标,通过操作虚拟现实硬件设备可以使药物设计云计算流程控制方法通过虚拟现实的可视化操作方式操作完成,并可以等计算完成后及时显示结果。这可以比传统的药物设计软件给用户带来更好的视觉效果,以及理解其中的分子机制,对用户的专业背景知识要求更少。
实施例2
针对一个靶点进行苗头化合物的筛选
首先进行小规模的验证,从数据库模块调用数据库中的小分子,数量在1千万左右,然后调用预处理模块对这些分子进行预处理,考虑到项目的目标是筛选苗头化合物,所以选择调用方法模块对分子对接方法进行了方法验证,找到了合适的筛选参数。
然后调用数据库模块读取原始的数据和结构,接着利用小规模的验证得到的参数,调用Majorana任务调度平台提交筛选任务,并实时跟踪计算结果。计算完成后,调用分析模块分析计算结果。根据计算结果,推荐筛选出的苗头化合物给生物测试团队,完成了计算任务。图4表示用本实施例的计算模块预测的小分子活性,推荐给生物测试团队后,与实验活性的相关性图。从图4中可以看出,计算预测活性和实验活性具有高度的相关性,表明了本实施例计算方法的可靠性。
本方法和其他传统方法对比,首先是流程化以及模块化的操作,方便了筛选工作的进行,提升了效率。 同时因为Majorana任务调度系统的使用,使得计算的跟踪,分析都更加方便,进一步提升了效率。图5表示,使用传统药物设计流程和Majorana任务调度系统的CPU运行时间对比,可以看出使用Majorana任务调度系统仅占传统流程运行时间的40%,表示流程化以及模块化的操作能显著提升工作效率。
实施例3
针对一个靶点开发一款新药的先导化合物
通过实施例1中筛选出了一些实验性质不错的候选苗头化合物,准备再次利用基于虚拟现实技术的药物设计云计算流程控制方法来优化此批苗头化合物,并最终得到先导化合物。
首先将设计的分子和靶点结构导入系统,调用虚拟现实药物设计模块,根据结合模式开展基于虚拟现实的药物设计。直接根据虚拟现实展示的结合模式来分析靶点和苗头化合物之间关键的结合模式,根据实际的计算需求调用相应的方法模块,接着调用Majorana任务调度平台,根据方法模块的计算需求,提交计算任务到云平台,并利用计算平台在后台进行云计算评估,并及时反馈给团队成员。团队成员根据计算评估反馈,并在虚拟现实技术的帮助下,再次观看结合模式,并重新设计分子,然后再次提交后台计算评估。经过多轮迭代,找到合理的候选先导化合物。过程中所有的数据,调度,都会记录到数据库,便于日后回溯复盘。
如图6所示,表示本实施例的药物设计流程的可视化。通过这个过程,可以观察到分子的片段切断与生长过程,以及不同骨架之间的跃迁路径。从这个可视化过程,可以了解到目标分子的逐步优化过程。本方法和其他传统方法对比,首先是流程化以及模块化的操作,方便了先导化合物优化工作的进行,提升了效率。 本案例中还使用了虚拟现实的药物设计模块,方便了对结果的分析和解读;同时因为Majorana任务调度系统的使用,使得计算的跟踪,分析都更加方便,进一步提升了效率。
实施例4
针对一个靶点开发一款新药并对外展示研发成果
从实施例1和实施例2的操作中得到了一些实验性质不错的候选先导化合物。利用基于虚拟现实技术的药物设计云计算流程控制方法,调用分析展示这批计算结果,展示出先导化合物包括结合模式,相互作用,能量值,稳定性,主成分分析在内的相关结果等。
如图7和图8所示,图7表示本实施例的计算方法对分子结构的描述,主要是通过分子指纹和键值对的方式,可以快速获得对大量分子的结构特征,并以数字化方式表示和存储。图8表示分子与蛋白的结合模式,从图中可以看出,不仅表示出了蛋白-配体间的基本相互作用,还进一步对相互作用类型做了聚类,得到一个类药效团的分析,可以获得更多关于蛋白-配体结合相互作用和驱动力的洞见。本方法和其他传统方法对比,首先是流程化以及模块化的操作,方便了结果的展示。
以上内容是结合具体的优选实施方式对本发明所作的进一步详细说明,不能认定本发明的具体实施只局限于这些说明。对于本发明所属技术领域的普通技术人员来说,在不脱离本发明构思的前提下,还可以做出若干简单推演或替换,都应当视为属于本发明的保护范围。
