抗革兰氏阴性菌化合物
文献发布时间:2023-06-19 11:35:49
技术领域
本发明涉及抗革兰氏阴性菌化合物。
背景技术
细菌所产生的具有抗菌作用的肽、蛋白质作为细菌素被熟知。细菌素为天然来源物质,因此,认为与由合成物质构成的抗菌剂相比,对人体的影响低,作为乳酸菌的乳酸乳球菌(Lactococcus lactis)所产生的作为细菌素的乳链菌肽(Nisin)在世界许多国家被批准作为防腐剂添加到食品中(例如,参照专利文献1、2)。
细菌素已知对产生菌的类似菌具有抗菌作用。因此,通常认为来自革兰氏阳性菌的细菌素对作为革兰氏阳性菌的产生菌的类似菌具有抗菌作用,而对革兰氏阴性菌不具有抗菌作用。
上述的乳链菌肽也是对革兰氏阳性菌具有抗菌作用,但对革兰氏阴性菌不具有抗菌作用。因此,乳链菌肽对例如鱼贝类所致的食物中毒的病原菌即肠炎弧菌没有抗菌作用。关于乳链菌肽以外的细菌素,例如,枯草菌素(Subtilin)和安琪阿宁(Entianin)也是对革兰氏阳性菌具有抗菌作用,但对革兰氏阴性菌不具有抗菌作用。认为这是因为革兰氏阴性菌的外膜形成了对来自革兰氏阳性菌的细菌素的屏障(例如,参照非专利文献1~3)。
另外,认为来自革兰氏阳性菌的细菌素对真菌也不具有抗菌作用。
现有技术文献
专利文献
专利文献1:日本专利第4111489号公报
专利文献2:日本专利第5738561号公报
非专利文献
非专利文献1:J.Barbosa,et al.,“Class I and Class II LanthipeptidesProduced by Bacillus spp.”,J.Nat.Prod.2015,78,2850?2866
非专利文献2:C.V.Prudencio,et al.,“Strategies for the use ofbacteriocins in Gram-negative bacteria:relevance in food microbiology”,J FoodSci Technol(September 2015),52(9):5408-5417
非专利文献3:善藤威史等,“乳酸菌细菌素的探索和应用”、Japanese Journal ofLactic Acid Bacteria,Vol.25,No.1,2014,Japan Society for Lactic Acid Bacteria
发明内容
如上所述,以往的细菌素由于仅对产生菌的类似菌具有抗菌作用,因此,抗菌谱窄。本发明是鉴于这样的情况而作出的,其目的在于提供抗菌谱广的抗菌化合物。
本发明的一个方面的抗革兰氏阴性菌化合物具有下述化学式1所示的氨基酸序列。
另外,本发明的一个方面的抗革兰氏阴性菌药物包含具有上述化学式1所示的氨基酸序列的抗革兰氏阴性菌化合物。
另外,本发明的一个方面的饮料或食物包含具有上述化学式1所示的氨基酸序列的抗革兰氏阴性菌化合物。
另外,本发明的一个方面的枯草杆菌(Bacillus subtilis)是能够产生具有上述化学式1所示的氨基酸序列的化合物的枯草杆菌。
另外,本发明的一个方面的抗革兰氏阴性菌药物包含能够产生具有上述化学式1所示的氨基酸序列的化合物的枯草杆菌。
另外,本发明的一个方面的饮料或食物包含能够产生具有上述化学式1所示的氨基酸序列的化合物的枯草杆菌。
另外,本发明的一个方面的枯草杆菌为枯草杆菌MT2株(保藏号:NITE BP-02767)。
另外,本发明的一个方面的抗革兰氏阴性菌药物包含枯草杆菌MT2株(保藏号:NITE BP-02767)。
另外,本发明的一个方面的饮料或食物包含枯草杆菌MT2株(保藏号:NITE BP-02767)。
另外,本发明的一个方面的抗革兰氏阴性菌化合物的制造方法包括:培养枯草杆菌,以及采集枯草杆菌所产生的具有上述化学式1所示的氨基酸序列的化合物。
另外,本发明的一个方面的抗革兰氏阴性菌化合物的制造方法包括:培养枯草杆菌MT2株(保藏号:NITE BP-02767),以及采集枯草杆菌MT2株(保藏号:NITE BP-02767)所产生的具有上述化学式1所示的氨基酸序列的化合物。
另外,本发明的一个方面的应用是具有上述化学式1所示的氨基酸序列的抗革兰氏阴性菌化合物在抗革兰氏阴性菌药物的制造中的应用。
另外,本发明的一个方面的应用是能够产生具有上述化学式1所示的氨基酸序列的化合物的枯草杆菌在抗革兰氏阴性菌药物的制造中的应用。
另外,本发明的一个方面的应用是枯草杆菌MT2株(保藏号:NITE BP-02767)在抗革兰氏阴性菌药物的制造中的应用。
另外,本发明的一个方面的肠炎的治疗方法包括对患者给予具有上述化学式1所示的氨基酸序列的抗革兰氏阴性菌化合物。
另外,本发明的一个方面的肠炎的治疗方法包括对患者给予能够产生具有上述化学式1所示的氨基酸序列的化合物的枯草杆菌。
另外,本发明的一个方面的肠炎的治疗方法包括对患者给予枯草杆菌MT2株(保藏号:NITE BP-02767)。
根据本发明,能够提供抗菌谱广的抗菌化合物。
附图说明
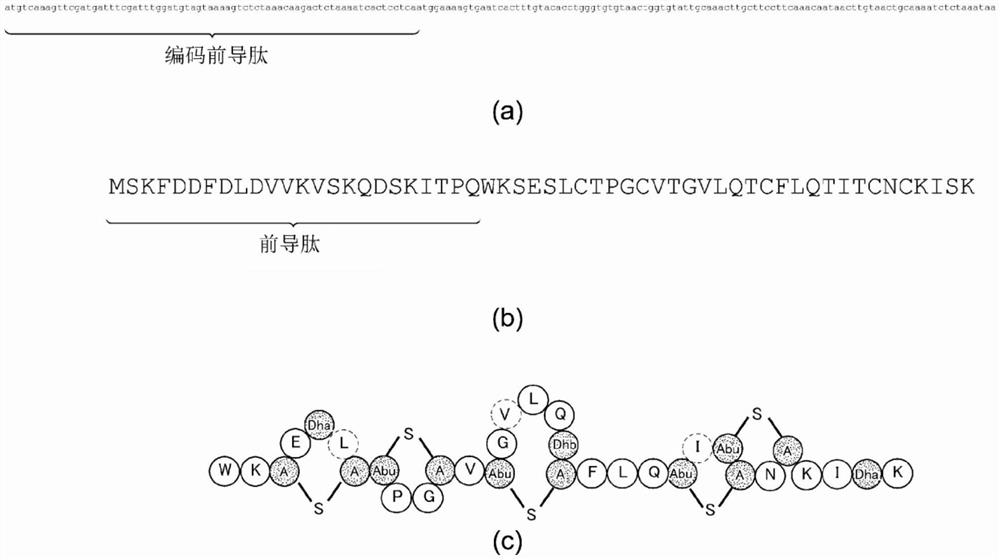
图1的(a)表示细菌素的生产基因,图1的(b)表示细菌素的前肽,图1的(c)表示细菌素(活性肽)。
图2是表示基于ANI法的枯草杆菌MT2株的全基因组序列与枯草芽胞杆菌枯草亚种(Bacillus subtilis subsp.subtilis)168的全基因组序列的同源解析的结果的图表。
图3是表示基于ANI法的枯草杆菌MT2株的全基因组序列与枯草芽胞杆菌枯草亚种6051-HGW的全基因组序列的同源解析的结果的图表。
图4是表示基于ANI法的枯草杆菌MT2株的全基因组序列与枯草芽胞杆菌斯氏亚种(Bacillus subtilis subsp.spizizenii)W23的全基因组序列的同源解析的结果的图表。
图5是表示基于ANI法的枯草杆菌MT2株的全基因组序列与特基拉芽孢杆菌(Bacillus tequilensis)FJAT-14262a的全基因组序列的同源解析的结果的图表。
图6是表示细菌素的质谱分析结果的图表。
图7是表示细菌素的抗菌活性的图表。
图8是表示细菌素的抗菌活性的图表。
具体实施方式
以下,对本发明的实施方式详细地进行说明。应予说明,以下所示的实施方式例示了将本发明的技术思想具体化的装置和方法,本发明的技术思想并不是将构成部件的组合等限定为下述内容。本发明的技术思想可以在请求保护的范围中加以各种变更。
本实施方式的抗革兰氏阴性菌化合物具有下述化学式2所示的氨基酸序列。下述化学式2所示的氨基酸序列为C
作为本实施方式的抗革兰氏阴性菌化合物显示抗菌作用的革兰氏阴性菌的例子,可举出弧菌属细菌。作为弧菌属细菌的例子,可举出肠炎弧菌、霍乱弧菌、非O1霍乱弧菌、拟态弧菌(Vibrio mimicus)、河弧菌(Vibrio fluvialis)、创伤弧菌(Vibrio vulnificus)、溶藻弧菌(Vibrio alginolyticus)、副溶血弧菌(Vibrio parahaemolyticus)、和弗氏弧菌(Vibrio furnissii)。
作为本实施方式的抗革兰氏阴性菌化合物显示抗菌作用的真菌的例子,可举出毛癣菌属菌。作为毛癣菌属菌的例子,可举出白癣菌(红色毛癣菌)(Trichophyton rubrum)、须毛癣菌、趾间毛癣菌(Trichophyton mentagrophytes)、毛癣菌(Trichophyton spp.)和疣状毛癣菌(Trichophyton verrucosum)。
作为本实施方式的抗革兰氏阴性菌化合物显示抗菌作用的革兰氏阳性菌的例子,可举出芽胞杆菌属菌。作为芽胞杆菌属菌的例子,可举出枯草杆菌(Bacillus subtilis)、蜡样芽孢杆菌(Bacillus cereus)、炭疽杆菌(Bacillus anthracis)和嗜热脂肪芽孢杆菌(Bacillus stearothermophilus)。枯草杆菌在酱油、味噌的制造过程中是有害的。
本实施方式的抗革兰氏阴性菌化合物是由例如枯草杆菌产生的。本实施方式的抗革兰氏阴性菌化合物来自作为革兰氏阳性菌的枯草杆菌,但对革兰氏阴性菌和真菌具有与对革兰氏阳性菌的抗菌作用同等的抗菌作用。因此,本实施方式的抗革兰氏阴性菌化合物可以不与辅助对革兰氏阴性菌的抗菌作用的处置并用。
作为辅助对革兰氏阴性菌的抗菌作用的处置,可举出食品防腐剂等防腐剂的添加。作为防腐剂,可举出螯合剂、表面活性剂、酸和盐。作为螯合剂的例子,可举出乙二胺四乙酸(EDTA)。作为表面活性剂的例子,可举出吐温80。作为酸和盐的例子,可举出乳酸、柠檬酸、焦磷酸、葡糖酸、乙酸、次氮基三乙酸、次氯酸、山梨酸、苯甲酸和多聚磷酸(polyphosphoric acid)以及它们的盐、磷酸三钠(tri-sodium phosphate)。
认为防腐剂使革兰氏阴性菌的外膜不稳定。以往,为了用来自革兰氏阳性菌的细菌素对革兰氏阴性菌进行杀菌,认为需要与这样的防腐剂并用。与此相对,本实施方式的抗革兰氏阴性菌化合物即使不与防腐剂并用,也能够显示对革兰氏阴性菌有效的抗菌作用。
另外,作为辅助对革兰氏阴性菌的抗菌作用的处置,可举出植物精油(plantessential oil)的添加。作为植物精油的例子,可举出牛至精油和百里香精油。认为植物精油中所含的百里酚、香芹酚使革兰氏阴性菌的外膜不稳定。但是,本实施方式的抗革兰氏阴性菌化合物即使不与植物精油并用,也能够显示对革兰氏阴性菌有效的抗菌作用。
另外,作为辅助对革兰氏阴性菌的抗菌作用的处置,可举出高压处理。高压处理是指例如施加30MPa以上的压力的处理。认为高压处理使革兰氏阴性菌的外膜不稳定。但是,本实施方式的抗革兰氏阴性菌化合物即使不与高压处理并用,也能够实现对革兰氏阴性菌的有效的抗菌作用。
另外,作为辅助对革兰氏阴性菌的抗菌作用的处置,可举出高温和低温处理。认为高温和低温处理使革兰氏阴性菌的外膜不稳定。另外,作为辅助对革兰氏阴性菌的抗菌作用的处置,可举出脉冲电场处理。脉冲电场处理由于提高革兰氏阴性菌的温度,因此,认为有与高温处理同样的效果。但是,本实施方式的抗革兰氏阴性菌化合物即使不与高温处理、低温处理、或脉冲电场处理并用,也能够实现对与革兰氏阴性菌的有效的抗菌作用。
能够产生本实施方式的抗革兰氏阴性菌化合物的枯草杆菌具有例如图1(a)和序列号1所示的细菌素的生产基因。序列号1中,1位~72位编码前导肽。将除编码该前导肽的部分以外的基因序列示于序列号2。能够产生本实施方式的抗革兰氏阴性菌化合物的枯草杆菌可以具有序列号2所示的基因序列。
图1(a)和序列号1所示的生产基因被转录、翻译,产生图1(b)和序列号3所示的细菌素的前肽。序列号3中,1位~24位为前导肽。将除该前导肽以外的氨基酸序列示于序列号4。
图1(b)和序列号3所示的细菌素的前肽在翻译后被修饰,将前导肽切断,从而产生具有图1(c)和上述化学式2所示的序列的活性肽。
序列号4所示的前肽的3位的丝氨酸在活性肽中被置换为丙氨酸。序列号4所示的前肽的5位的丝氨酸在活性肽中被置换为脱氢丙氨酸。序列号4所示的前肽的7位的半胱氨酸在活性肽中被置换为丙氨酸。序列号4所示的前肽的8位的苏氨酸在活性肽中被置换为氨基丁酸。
序列号4所示的前肽的11位的半胱氨酸在活性肽中被置换为丙氨酸。序列号4所示的前肽的13位的苏氨酸在活性肽中被置换为氨基丁酸。序列号4所示的前肽的18位的苏氨酸在活性肽中被置换为脱氢酪氨酸。序列号4所示的前肽的19位的半胱氨酸在活性肽中被置换为丙氨酸。
序列号4所示的前肽的23位的苏氨酸在活性肽中被置换为氨基丁酸。序列号4所示的前肽的25位的苏氨酸在活性肽中被置换为氨基丁酸。序列号4所示的前肽的26位的半胱氨酸在活性肽中被置换为丙氨酸。序列号4所示的前肽的28位的半胱氨酸在活性肽中被置换为丙氨酸。序列号4所示的前肽的31位的丝氨酸在活性肽中被置换为脱氢丙氨酸。
活性肽中,对应于序列号4所示的前肽的3位的丝氨酸的丙氨酸与对应于序列号4所示的7位的半胱氨酸的丙氨酸介由硫醚键形成羊毛硫氨酸。
活性肽中,对应于序列号4所示的前肽的8位的苏氨酸的氨基丁酸与对应于序列号4所示的11位的半胱氨酸的丙氨酸介由硫醚键形成3-甲基羊毛硫氨酸。
活性肽中,对应于序列号4所示的前肽的13位的苏氨酸的氨基丁酸与对应于序列号4所示的19位的半胱氨酸的丙氨酸介由硫醚形成3-甲基羊毛硫氨酸。
活性肽中,对应于序列号4所示的前肽的23位的苏氨酸的氨基丁酸与对应于序列号4所示的26位的半胱氨酸的丙氨酸介由硫醚键形成3-甲基羊毛硫氨酸。
活性肽中,对应于序列号4所示的前肽的25位的苏氨酸的氨基丁酸与对应于序列号4所示的28位的半胱氨酸的丙氨酸介由硫醚键形成3-甲基羊毛硫氨酸。
作为能够产生本实施方式的抗革兰氏阴性菌化合物的枯草杆菌之一的枯草杆菌MT2株在国家高级工业科学技术学院国际专利生物保藏中心(日本,邮政编号292-0818,千叶县木更津市上总镰足2-5-8 122号室)进行了国际保藏,保藏号为NITE BP-02767。枯草杆菌MT2株在2018年8月22日(国内保藏日)在国家高级工业科学技术学院国际专利生物保藏中心(日本)进行了国内保藏,并在2018年10月4日对国家高级工业科学技术学院国际专利生物保藏中心(日本)进行了基于布达佩斯条约的向国际保藏的移交请求。
本实施方式的抗革兰氏阴性菌化合物可以含有在医药品中。含有本实施方式的抗革兰氏阴性菌化合物的医药品可作为革兰氏阴性菌、革兰氏阳性菌和真菌的消毒剂使用。另外,含有本实施方式的抗革兰氏阴性菌化合物的医药品可作为肺炎、食物中毒和肠炎的治疗药使用。进而,含有本实施方式的抗革兰氏阴性菌化合物的医药品可作为白癣、念珠菌病、隐球菌病和曲霉病等真菌病的治疗药使用。
医药品包含有效量的本实施方式的抗革兰氏阴性菌化合物。有效量是指发挥抗菌作用所需的量,可根据对象菌、症状、患者的年龄、患者的体重和患者的性别等而适当决定。
含有本实施方式的抗革兰氏阴性菌化合物的医药品例如可以为片剂、胶囊、液体、乳膏、软膏、硬膏、凝胶、蜡和喷雾。另外,含有本实施方式的抗革兰氏阴性菌化合物的医药品例如以消毒剂、内服药、涂布治疗药等皮肤外用药和滴眼剂的形式提供。含有本实施方式的抗革兰氏阴性菌化合物的医药品例如可应用于肠等内脏、包括手指和脚趾的人体的皮肤、毛发、口腔和眼球等。另外,含有本实施方式的抗革兰氏阴性菌化合物的消毒剂例如也可应用于食品、炊具、医院等建筑物的墙壁、地板以及桌子等家具。
含有本实施方式的抗革兰氏阴性菌化合物的医药品可以根据目的适当地含有液体油脂、固体油脂、蜡、烃、高级脂肪酸、高级醇、酯、有机硅、保湿剂、水溶性高分子、增稠剂、被膜剂、金属离子螯合剂、低级醇、多元醇、糖类、氨基酸类、有机胺类、pH调节剂、皮肤营养剂、维生素类、香料、粉体、色材和水等医药品的配合成分。
本实施方式的抗革兰氏阴性菌化合物也可以含有在饮料或食物中。另外,本实施方式的抗革兰氏阴性菌化合物也可以含有在牙膏和口腔清洁剂等中。
能够产生本实施方式的抗革兰氏阴性菌化合物的枯草杆菌可以含有在医药品、饮料或食品中。例如,医药品、饮料或食品中所含有的枯草杆菌产生抗革兰氏阴性菌化合物,对革兰氏阴性菌、真菌和革兰氏阳性菌发挥抗菌作用。含有能够产生本实施方式的抗革兰氏阴性菌化合物的枯草杆菌的医药品的对象疾病、形状和用法等与含有本实施方式的抗革兰氏阴性菌化合物的医药品同样。
枯草杆菌MT2株(保藏号:NITE BP-02767)可以含有在医药品、饮料或食品中。含有枯草杆菌MT2株(保藏号:NITE BP-02767)的医药品的对象疾病、形状和用法等与含有本实施方式的抗革兰氏阴性菌化合物的医药品同样。
本实施方式的抗革兰氏阴性菌化合物例如可以通过将枯草杆菌在培养基中培养并采集枯草杆菌在培养基中产生的具有上述化学式2所示的氨基酸序列的肽而制造。从培养基采集肽并精制的方法没有特别限定。本实施方式的抗革兰氏阴性菌化合物也可以化学合成。
如上所述,本发明的各实施方式的抗革兰氏阴性菌化合物等具有由上述的任一个或多个的组合构成的以下的例子的构成和作用效果。
本实施方式的抗革兰氏阴性菌化合物为具有上述化学式2所示的氨基酸序列的抗革兰氏阴性菌化合物。本实施方式的抗革兰氏阴性菌化合物对革兰氏阴性菌、革兰氏阳性菌和真菌具有抗菌作用。
本实施方式的抗革兰氏阴性菌化合物可以由枯草杆菌(Bacillus subtilis)产生。另外,本实施方式的抗革兰氏阴性菌化合物可以由枯草杆菌MT2株(保藏号:NITE BP-02767)产生。本实施方式的抗革兰氏阴性菌化合物尽管来自作为革兰氏阳性菌的枯草杆菌,但对革兰氏阴性菌具有抗菌作用。
本实施方式的抗革兰氏阴性菌化合物显示抗菌作用的革兰氏阴性菌可以为弧菌属细菌。弧菌属细菌可以为肠炎弧菌。
本实施方式的抗革兰氏阴性菌化合物显示抗菌作用的革兰氏阴性菌显示抗菌作用的真菌可以为毛癣菌属菌。毛癣菌属菌可以为白癣菌和须毛癣菌或趾间毛癣菌。
本实施方式的抗革兰氏阴性菌化合物可以不与辅助对革兰氏阴性菌的抗菌作用的处置并用。辅助对革兰氏阴性菌的抗菌作用的处置可以为防腐剂的添加。防腐剂可以为螯合剂。本实施方式的抗革兰氏阴性菌化合物即使不与辅助对革兰氏阴性菌的抗菌作用的处置并用,也具有与对革兰氏阳性菌的抗菌作用同等的对革兰氏阴性菌的抗菌作用。
本实施方式的抗革兰氏阴性菌药物可以包含上述的抗革兰氏阴性菌化合物。本实施方式的饮料或食物可以包含上述的抗革兰氏阴性菌化合物。
本实施方式的枯草杆菌(Bacillus subtilis)可以是能够产生具有上述化学式2所示的氨基酸序列的化合物的枯草杆菌。
本实施方式的抗革兰氏阴性菌药物可以包含能够产生具有上述化学式2所示的氨基酸序列的化合物的枯草杆菌。本实施方式的饮料或食物可以包含能够产生具有上述化学式2所示的氨基酸序列的化合物的枯草杆菌。
本实施方式的枯草杆菌可以为枯草杆菌MT2株(保藏号:NITE BP-02767)。
本实施方式的抗革兰氏阴性菌药物可以包含上述的枯草杆菌MT2株(保藏号:NITEBP-02767)。本实施方式的饮料或食物可以包含上述的枯草杆菌MT2株(保藏号:NITE BP-02767)。
本实施方式的抗革兰氏阴性菌化合物的制造方法可以包括:培养枯草杆菌(Bacillus subtilis),以及采集枯草杆菌所产生的具有上述化学式2所示的氨基酸序列的化合物。
本实施方式的抗革兰氏阴性菌化合物的制造方法可以包括:培养枯草杆菌MT2株(保藏号:NITE BP-02767),以及采集枯草杆菌MT2株(保藏号:NITE BP-02767)所产生的具有上述化学式2所示的氨基酸序列的化合物。
本实施方式可以为上述的抗革兰氏阴性菌细菌素在抗革兰氏阴性菌药物的制造中的应用。
本实施方式可以为能够产生具有上述化学式2所示的氨基酸序列的化合物的枯草杆菌在抗革兰氏阴性菌药物的制造中的应用。
本实施方式可以为枯草杆菌MT2株(保藏号:NITE BP-02767)在抗革兰氏阴性菌药物的制造中的应用。
本实施方式的肠炎的治疗方法可以包括对患者给予上述的抗革兰氏阴性菌化合物。本实施方式的肠炎的治疗方法可以包括对患者给予能够产生具有上述化学式2所示的氨基酸序列的化合物的枯草杆菌。本实施方式的肠炎的治疗方法可以包括对患者给予枯草杆菌MT2株(保藏号:NITE BP-02767)。肠炎可以为食物中毒。
应予说明,以上说明的各实施方式是为了容易理解本发明而不是对本发明进行限定性解释。本发明可以在不脱离其主旨的情况下进行变更/改进,并且本发明中也包括其等同物。即,本领域技术人员对各实施方式加以适当设计变更而得的实施方式只要具备本发明的特征,则也包含在本发明的范围中。例如,各实施方式所具备的各要素、材料、条件和形状等并并不限定于所例示的内容,可以适当地变更。另外,各实施方式是例示,当然可以进行不同的实施方式中示出的构成的部分置换或组合,它们只要包含本发明的特征,则也包含在本发明的范围中。
实施例
以下,对本发明的实施例进行说明。但是,本发明当然并不限定于以下的实施例。
(实施例1:魁蒿发酵液的制备)
魁蒿叶中,一般认为一天中,在日出时间前后1小时、合计2小时的期间,乳酸菌的数量最大。另外,一般认为这些时间段以外,乳酸菌减少,光合细菌增加。因此,在这2小时的期间,从魁蒿叶的前端采集约20cm的部分。将采集的6.3kg的魁蒿叶立即放入其中铺有乙烯袋的第1腌渍桶中,在魁蒿叶上撒上3.2kg的糖蜜和0.6kg的粗盐后,将乙烯袋的口封闭并密封。在乙烯袋的上面载置重石,腌制魁蒿叶。
在几天后腌汁上升到魁蒿叶的上面,取下重石。接着,在第2腌渍桶中加入冲洗用的不含氯的10L的水,在水中放入魁蒿叶的腌渍物和10kg的腌汁。进一步准备第3腌渍桶,在第3腌渍桶的开口上载置金属网过滤器。从第2腌渍桶中一边用手搓洗一边一点点地取出魁蒿叶,在第3腌渍桶的开口上的金属网过滤器上用手掌轻轻地按压魁蒿叶,压榨出腌汁。
将魁蒿叶完全压榨后,将第2腌渍物汁中残留的腌汁通过金属网过滤器进行过滤。接着,在第3腌渍桶中的腌汁中溶解糖蜜(波照间黑糖)使最终浓度为10重量%,并且溶解粗盐使最终浓度为3重量%。然后,使第3腌渍桶的周围温度约为30℃,从而开始发酵。最初确认到大的气泡的发泡,逐渐变为细小的气泡的发泡,最终发泡结束。约1周后,发泡结束时的pH为3.8左右。将此时的腌汁作为魁蒿发酵液。
(实施例2:枯草杆菌的制备)
向乳酸菌MRS培养基(:蛋白胨1%、牛肉提取物1%、酵母抽提物0.5%、葡萄糖2%、吐温80 0.1%、柠檬酸铵0.5%、硫酸镁0.01%、硫酸锰0.005%、磷酸二钾0.2%,Difco公司制)滴加魁蒿发酵液,将魁蒿发酵液中所含的细菌在培养基中进行培养,根据需要进行几次传代培养。然后,将所培养的细菌涂抹在乳酸菌MRS琼脂培养基(向上述的MRS培养基添加3%琼脂而得的培养基)上进行培养,从生成的菌落采集细菌。
接着,以对孢子性乳酸菌即凝结芽孢杆菌(Bacillus coagulans)的抗菌活性作为指标,通过Spot on lawn检验法从所采集的细菌中选择具有抗菌性物质生产能力的菌株作为枯草杆菌MT2株。调查所选择的枯草杆菌MT2株的菌学性质,结果通过16S核糖体DNA(rDNA)的碱基序列的同源性的解析而鉴定为枯草杆菌(Bacillus subtilis)。
通过ANI(Average Nucleotide Identity,平均核苷酸一致性)法计算枯草杆菌MT2株的全基因组序列与一种已有的枯草杆菌株即枯草芽胞杆菌枯草亚种168的全基因组序列的同源值的平均值,结果如图2所示为98.5%,1.5%不同。
通过ANI法计算枯草杆菌MT2株的全基因组序列与一种已有的枯草杆菌株即枯草芽胞杆菌枯草亚种6051-HGW的全基因组序列的同源值的平均值,结果如图3所示为98.49%,1.51%不同。
通过ANI法计算枯草杆菌MT2株的全基因组序列与一种已有的枯草杆菌株即枯草芽胞杆菌斯氏亚种W23的全基因组序列的同源值的平均值,结果如图4所示为92.03%,7.97%不同。
通过ANI法计算枯草杆菌MT2株的全基因组序列与一种已有的枯草杆菌株即特基拉芽孢杆菌FJAT-14262a的全基因组序列的同源值的平均值,结果如图5所示为98.49%,1.51%不同。
根据以上所示的与已有的枯草杆菌株的比较,认为枯草杆菌MT2株是枯草杆菌的新株。枯草杆菌MT2株在国家高级工业科学技术学院国际专利生物保藏中心(独立行政法人制品评价技术基础机构)(日本)进行国际保藏,保藏号为NITE BP-02767。枯草杆菌MT2株具有序列号1、2所示的基因序列。
(实施例3:细菌素的制备)
将枯草杆菌MT2株在乳酸菌MRS培养基中在35℃以上且37℃以下进行3天需氧振荡培养。然后,将包含菌体的培养基以10000rpm在25℃下离心分离20分钟。进一步将离心分离后的培养基通过网眼0.45μm的灭菌过滤器进行过滤而除去菌体,得到培养上清液。
使用反相硅胶柱(Sep-Pac C18,Millipore公司制)将培养上清液中所含的细菌素浓缩。进一步通过使用Sephasil Peptide C185μST(Pharmacia公司制)的反向柱色谱对活性细菌素馏分进行分级。
使用基质辅助激光解吸电离飞行时间质谱仪(MALDI-TOFMS ultrafleX III,Bruker公司制)进行所分级的活性细菌素的质谱分析,结果如图6所示,精密分子量约为3346。应予说明,靶板使用MTP384 ground steel(Bruker daltonics)。另外,作为基质,在进行了各种研究的基础上使用α-氰基-4-羟基肉桂酸(HCCA)。对所分级的活性细菌素的氨基酸序列进行解析,结果具有上述化学式2所示的氨基酸序列。
(实施例4:细菌素的抗菌活性)
准备作为革兰氏阳性菌的枯草杆菌(Bacillus subtilis,NBRC 3134)、作为革兰氏阴性菌的肠炎弧菌(Vibrio parahaemolyticus,12711T)。在包含实施例3中制备的活性细菌素的pH为7.8的10mL的液体中接种以10
进而,准备作为真菌的白癣菌(Trichophyton mentagrophytes,NBRC 6124)。在包含实施例3中制备的活性细菌素的pH为7.8的10mL的液体中接种以10
序列表
<110> 株式会社村田制作所
<120> 抗革兰氏阴性菌化合物
<130> M18-01812
<160> 4
<170> PatentIn version 3.5
<210> 1
<211> 171
<212> DNA
<213> 枯草杆菌
<400> 1
atgtcaaagt tcgatgattt cgatttggat gtagtaaaag tctctaaaca agactctaaa 60
atcactcctc aatggaaaag tgaatcactt tgtacacctg ggtgtgtaac tggtgtattg 120
caaacttgct tccttcaaac aataacttgt aactgcaaaa tctctaaata a 171
<210> 2
<211> 99
<212> DNA
<213> 枯草杆菌
<400> 2
tggaaaagtg aatcactttg tacacctggg tgtgtaactg gtgtattgca aacttgcttc 60
cttcaaacaa taacttgtaa ctgcaaaatc tctaaataa 99
<210> 3
<211> 56
<212> PRT
<213> 枯草杆菌
<400> 3
Met Ser Lys Phe Asp Asp Phe Asp Leu Asp Val Val Lys Val Ser Lys
1 5 10 15
Gln Asp Ser Lys Ile Thr Pro Gln Trp Lys Ser Glu Ser Leu Cys Thr
20 25 30
Pro Gly Cys Val Thr Gly Val Leu Gln Thr Cys Phe Leu Gln Thr Ile
35 40 45
Thr Cys Asn Cys Lys Ile Ser Lys
50 55
<210> 4
<211> 32
<212> PRT
<213> 枯草杆菌
<400> 4
Trp Lys Ser Glu Ser Leu Cys Thr Pro Gly Cys Val Thr Gly Val Leu
1 5 10 15
Gln Thr Cys Phe Leu Gln Thr Ile Thr Cys Asn Cys Lys Ile Ser Lys
20 25 30
- 抗革兰氏阴性菌化合物
- 新型锌离子螯合剂及其制备和在抗革兰氏阴性菌感染中的应用
