泊洛沙姆在提高逆转录酶效率或提高逆转录酶抑制剂耐受性中的应用及添加剂混合物
文献发布时间:2023-06-19 12:11:54
技术领域
本发明专利涉及泊洛沙姆在提高逆转录酶效率或提高逆转录酶抑制剂耐受性中的应用,以及用于逆转录过程中的添加剂混合物,属于生物技术领域。
背景技术
RNA检测技术是医学领域做病原检测和标志物筛查的重要手段。逆转录酶介导的RNA互补cDNA合成是RNA检测技术的第一步。但是目前的逆转录酶及体系的逆转录效率较低,且对逆转录体系中的抑制剂如甲醛和异硫氰酸胍等极其敏感。这严重地影响了RNA检测技术的灵敏性和准确性,阻碍了RNA检测技术的发展。病理学来源RNA如提取自福尔马林固定石蜡包埋处理的样本(Formalin-Fixed and Parrffin-Embedded,FFPE)、咽拭子样本和血液样本等在提取过程中容易出现RNA含量低和抑制剂如异硫氰酸胍和甲醛等残留严重等问题,给RNA检测技术带来了很大的挑战。
从2019年底至今,新型肺炎COVID-19在全世界范围爆发和蔓延,给人类的生活带来极大的干扰。COVID-19是由新型冠状病毒2019-nCoV引起的,2019-nCoV是一类RNA病毒,其增殖过程是由RNA依赖性RNA聚合酶(RNA dependent RNA polymerase,RDRP)介导的,因此没有DNA产物。RNA检测技术由于操作简单、耗时短、灵敏度高和通量大,成为COVID-19诊断的主要方式。但是,新冠来源RNA样本一般来源于鼻咽拭子、肛拭子或肺泡提取液,在提取过程中极容易出现RNA提取量低和抑制剂残留严重等问题。因此,开发一款提高逆转录效率和抑制剂耐受性的酶或试剂,用以提高病理学样本中RNA检测的准确性和灵敏度,是迫切需要的。
发明内容
本发明提供了泊洛沙姆在提高逆转录酶效率或提高逆转录酶抑制剂耐受性中的应用。
优选的,所述泊洛沙姆为泊洛沙姆101、108、124、181、184、188、237、338或407。
优选的,所述抑制剂为甲醛、乙醇、盐酸胍、异硫氰酸胍、肝素、鞣酸、甲酰胺或苯酚。
本发明还提供了一种用于逆转录过程中的添加剂混合物,包括泊洛沙姆和谷氨酸钾。
优选的,所述添加剂混合物中泊洛沙姆的浓度为0-30%wt且不为零,谷氨酸钾浓度为0-1M且不为零,溶剂为水。
优选的,还包括聚乙烯醇磺酸(PVSA)。
优选的,所述PVSA的浓度为0-0.1%wt之间且不为零。
优选的,还包括L-组氨酸盐酸盐。
优选的,所述L-组氨酸盐酸盐的浓度范围在0-200mM之间且不为零。
优选的,还包括甜菜碱。
优选的,所述甜菜碱的浓度范围在0-1M之间且不为零。
优选的,还包括四乙基氯化铵。
优选的,所述四乙基氯化铵的浓度范围在0-10mM之间且不为零。
优选的,还包括硫酸铵。
优选的,所述硫酸铵的浓度范围在0-1M之间且不为零。
优选的,还包括Triton X-100。
优选的,所述Triton X-100的含量范围在0-5%wt之间且不为零。
本发明还提供了四乙基氯化铵、甜菜碱、L-组氨酸盐酸盐、谷氨酸钾、硫酸铵、Triton X-100或PVSA在提高逆转录酶效率或提高逆转录酶抑制剂耐受性中的应用。
本发明发现泊洛沙姆可以显著提高逆转录酶效率或提高逆转录酶抑制剂耐受性,以泊洛沙姆为核心成分,提供了一种提高逆转录酶效率和抑制剂耐受性的添加剂组合,这种添加剂混合物不仅能够提高正常高纯度RNA样本的逆转录产物(约8倍),对复杂来源RNA样本如FFPE RNA或含甲醛、乙醇、盐酸胍、异硫氰酸胍、肝素、鞣酸、甲酰胺和苯酚等逆转录抑制剂的RNA具有更强的耐受和更高的cDNA产量。这种逆转录酶添加物组合可以在RT-qPCR检测或RNA NGS建库上显著提高复杂来源病理学样本检测的灵敏度和准确性,非常适用于疾病快速诊断领域。
附图说明
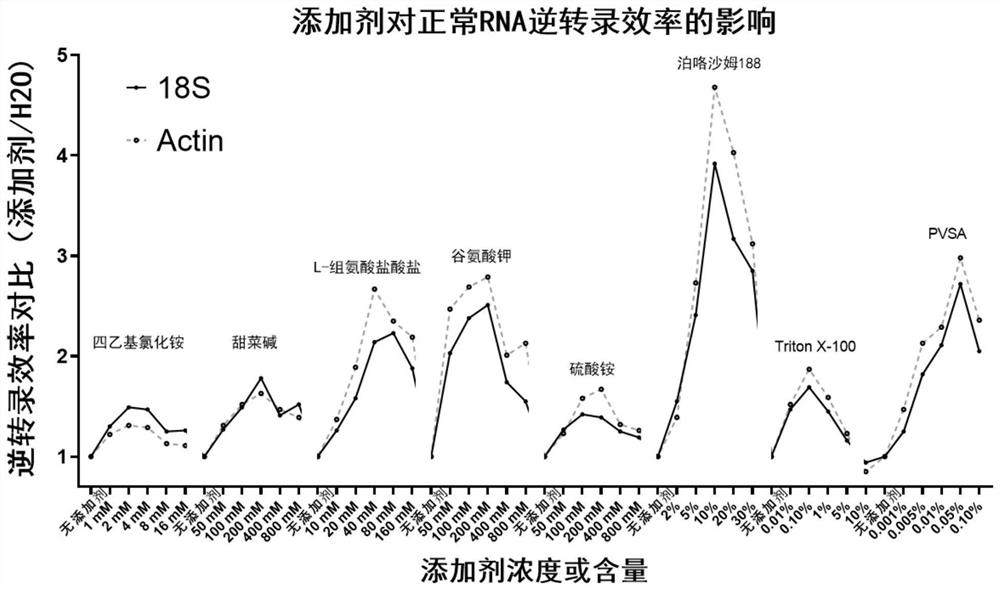
图1为不同添加剂对正常RNA逆转录的影响。
图2-4为不同添加剂对不同质量的FFPE RNA逆转录的影响。
图5为不同添加剂组合条件对逆转录效率的影响。
图6为添加剂对模板中甲醛的忍耐程度。
图7为添加剂对模板中乙醇的忍耐程度。
图8为添加剂对模板中盐酸胍的忍耐程度。
图9为添加剂对模板中异硫氰酸胍的忍耐程度。
图10为添加剂对模板中肝素的忍耐程度。
图11为添加剂对模板中鞣酸的忍耐程度。
图12为添加剂对模板中甲酰胺的忍耐程度。
图13为添加剂对模板中苯酚的忍耐程度。
图14为不同非离子型表面活性剂对模板中逆转录抑制剂的忍耐程度。
图15为不同泊咯沙姆组合物对模板中逆转录抑制剂的忍耐程度。
图16为添加剂对逆转录酶特异性的影响。
图17为添加剂对不同逆转录酶活性的影响。
图18-22为添加剂在RNA NGS建库过程中对不同质量RNA建库效果的影响。
具体实施方式
通过以下详细说明结合附图可以进一步理解本发明的特点和优点。所提供的实施例仅是对本发明方法的说明,而不以任何方式限制本发明揭示的其余内容。本实施例所使用的引物序列如表1,N为随机碱基,即A、T、C、G中任意一种碱基,V为A、C、G中任意一种碱基,OligodT23VN和Random Hexamers为用于逆转录的通用引物。
实施例1对正常细胞来源的RNA样本进行测试。
实施例中采用的Total RNA系按常规方法从培养的Human 293FT cell(GM-070006H,购自吉满生物科技(上海)有限公司)细胞提取,以下同。具体实施方式如下:
表2
混匀后瞬离。85℃ 5min,立即置于冰上5min。
表3
混匀后瞬离。25℃ 10min,42℃ 30min,85℃ 5min,4℃ hold;
稀释1000倍后,用Hieff
从定量结果可以看出(图1),不同添加剂在合适的范围内对逆转录效率都有一定的促进作用。其中四乙基氯化铵的最适浓度范围在1-4mM之间,甜菜碱的最适浓度范围在100-200mM之间,L-组氨酸盐酸盐的最适浓度范围在20-80mM之间,谷氨酸钾的最适浓度范围在50-200mM之间,硫酸铵的最适浓度范围在50-200mM之间,泊咯沙姆188的最适含量范围在5-20%之间,Triton X-100的最适含量范围在0.01-0.1%之间,PVSA的最适含量范围在0.005-0.05%之间。而且,泊咯沙姆188对逆转录效率的促进效果最好。
实施例2对不同质量程度的FFPE RNAA样本进行测试。
实施例中采用的FFPE RNA来自于石蜡包埋的组织,以下同。具体实施方式如下:
表4
混匀后瞬离。85℃ 5min,立即置于冰上5min。
表5
混匀后瞬离。25℃ 10min,42℃ 30min,85℃ 5min,4℃ hold;
稀释200倍后对18S rRNA和Actin RNA进行定量,定量引物见表1。定量结果见图2-图4。
从定量结果可以看出(图2-图4),不同添加剂在合适的范围内对FFPE RNA的逆转录效率效率具有显著的促进作用,尤其是对低质量的FFPE样本(DV200比较小)。泊咯沙姆188对RNA的逆转录促进效果最明显,对于低质量的FFPE RNA,体系中1%终浓度的poloxamer能够将逆转录效率提高20倍。
实施例3不同添加剂组合对逆转录效率的促进作用。
根据实施例1和例2的结果,我们设计了8款10×添加剂组合。
条件1:10%泊咯沙姆188;
条件2:10%泊咯沙姆188,100mM谷氨酸钾;
条件3:10%泊咯沙姆188,100mM谷氨酸钾,0.01%PVSA;
条件4:10%泊咯沙姆188,100mM谷氨酸钾,0.01%PVSA,40mM L-组氨酸盐酸盐;
条件5:10%泊咯沙姆188,100mM谷氨酸钾,0.01%PVSA,40mM L-组氨酸盐酸盐;
条件6:10%泊咯沙姆188,100mM谷氨酸钾,0.01%PVSA,40mM L-组氨酸盐酸盐,200mM甜菜碱;
条件7:10%泊咯沙姆188,100mM谷氨酸钾,0.01%PVSA,40mM L-组氨酸盐酸盐,200mM甜菜碱,2mM四乙基氯化铵;
条件8:10%泊咯沙姆188,100mM谷氨酸钾,0.01%PVSA,40mM L-组氨酸盐酸盐,200mM甜菜碱,2mM四乙基氯化铵,100mM硫酸铵;
条件8:10%泊咯沙姆188,100mM谷氨酸钾,0.01%PVSA,40mM L-组氨酸盐酸盐,200mM甜菜碱,2mM四乙基氯化铵,100mM硫酸铵,0.01%Triton X-100。
采用的实施例1和实施例2中FFPE RNA来自于石蜡包埋的组织,以下同。具体实施方式如下:
表6
混匀后瞬离。85℃ 5min,立即置于冰上5min。
表7
混匀后瞬离。25℃ 10min,42℃ 30min,85℃ 5min,4℃ hold;
稀释100倍后对18S rRNA和Actin RNA进行定量,定量引物见表1。定量结果见图5。
根据图5结果可以看出,加入添加剂后不管是正常RNA还是FFPE RNA,逆转录效率都得到有效的提升,且添加剂对FFPE RNA逆转录效率的提升更加明显。添加剂组合条件8的性能更加优越,是逆转录效率促进程度最高的组合条件。后面的实施案例都在这个条件下进行测试。实施例4-11验证了RNA提取过程中存在的一些污染物和抑制剂对逆转录酶效率的影响以及条件8中添加剂组合对逆转录酶抑制剂耐受性的作用。
实施例4添加剂组合对模板中甲醛的忍耐程度。
实施例中采用的含不同甲醛浓度的正常RNA样本,以下同。具体实施方式如下:
表8
混匀后瞬离。85℃ 5min,立即置于冰上5min。
表9
混匀后瞬离。25℃ 10min,42℃ 30min,85℃ 5min,4℃ hold;
稀释200倍后对18S rRNA和Actin RNA进行定量,定量引物见表1。定量结果见图6。
从定量结果可以看出(图6),添加剂的加入能够显著促进逆转录效率以及对模板中甲醛的耐受程度。
实施例5添加剂组合对模板中乙醇的忍耐程度。
实施例中采用的含不同乙醇浓度的正常RNA样本,以下同。具体实施方式如下:
表10
混匀后瞬离。85℃ 5min,立即置于冰上5min。
表11
混匀后瞬离。25℃ 10min,42℃ 30min,85℃ 5min,4℃ hold;
稀释200倍后对18S rRNA和Actin RNA进行定量,定量引物见表1。定量结果见图7。
从定量结果可以看出(图7),添加剂的加入能够显著促进逆转录效率以及对模板中乙醇的耐受程度。
实施例6添加剂组合对模板中盐酸胍的忍耐程度。
实施例中采用的含不同盐酸胍浓度的正常RNA样本,以下同。具体实施方式如下:
表12
混匀后瞬离。85℃ 5min,立即置于冰上5min。
表13
混匀后瞬离。25℃ 10min,42℃ 30min,85℃ 5min,4℃ hold;
稀释200倍后对18S rRNA和Actin RNA进行定量,定量引物见表1。定量结果见图8。
从定量结果可以看出(图8),添加剂的加入能够显著促进逆转录效率以及对模板中盐酸胍的耐受程度。
实施例7添加剂组合对模板中异硫氰酸胍的忍耐程度。
实施例中采用的含不同异硫氰酸胍浓度的正常RNA样本,以下同。具体实施方式如下:
表14
混匀后瞬离。85℃ 5min,立即置于冰上5min。
表15
混匀后瞬离。25℃ 10min,42℃ 30min,85℃ 5min,4℃ hold;
稀释200倍后对18S rRNA和Actin RNA进行定量,定量引物见表1。定量结果见图9。
从定量结果可以看出(图9),添加剂的加入能够显著促进逆转录效率以及对模板中异硫氰酸胍的耐受程度。
实施例8添加剂组合对模板中肝素的忍耐程度。
实施例中采用的含不同肝素浓度的正常RNA样本,以下同。具体实施方式如下:
表16
混匀后瞬离。85℃ 5min,立即置于冰上5min。
表17
混匀后瞬离。25℃ 10min,42℃ 30min,85℃ 5min,4℃ hold;
稀释200倍后对18S rRNA和Actin RNA进行定量,定量引物见表1。定量结果见图10。
从定量结果可以看出(图10),添加剂的加入能够显著促进逆转录效率以及对模板中肝素的耐受程度。
实施例9添加剂组合对模板中鞣酸的忍耐程度。
实施例中采用的含不同鞣酸浓度的正常RNA样本,以下同。具体实施方式如下:
表18
混匀后瞬离。85℃ 5min,立即置于冰上5min。
表19
混匀后瞬离。25℃ 10min,42℃ 30min,85℃ 5min,4℃ hold;
稀释200倍后对18S rRNA和Actin RNA进行定量,定量引物见表1。定量结果见图11。
从定量结果可以看出(图11),添加剂的加入能够显著促进逆转录效率以及对模板中鞣酸的耐受程度。
实施例10添加剂组合对模板中甲酰胺的忍耐程度。
实施例中采用的含不同甲酰胺浓度的正常RNA样本,以下同。具体实施方式如下:
表20
混匀后瞬离。85℃ 5min,立即置于冰上5min。
表21
混匀后瞬离。25℃ 10min,42℃ 30min,85℃ 5min,4℃ hold;
稀释200倍后对18S rRNA和Actin RNA进行定量,定量引物见表1。定量结果见图12。
从定量结果可以看出(图12),添加剂的加入能够显著促进逆转录效率以及对模板中甲酰胺的耐受程度。
实施例11添加剂组合对模板中苯酚的忍耐程度。
实施例中采用的含不同苯酚浓度的正常RNA样本,以下同。具体实施方式如下:
表22
混匀后瞬离。85℃ 5min,立即置于冰上5min。
表23
混匀后瞬离。25℃ 10min,42℃ 30min,85℃ 5min,4℃ hold;
稀释200倍后对18S rRNA和Actin RNA进行定量,定量引物见表1。定量结果见图13。
从定量结果可以看出(图13),添加剂的加入能够显著促进逆转录效率以及对模板中苯酚的耐受程度。
实施例12其他非离子型表面活性剂对模板中逆转录抑制剂的忍耐程度。
在之前的实施例中,我们验证了非离子型表面活性剂泊咯沙姆188在逆转录过程中能够有效提高逆转录酶对模板中抑制剂的忍耐程度。在本实施例中,我们验证了其他的非离子型表面活性剂对逆转录抑制剂的忍耐程度,如泊咯沙姆101、泊咯沙姆108、泊咯沙姆124、泊咯沙姆181、泊咯沙姆184、泊咯沙姆237、泊咯沙姆338、泊咯沙姆407、Triton X-100、Triton X-114、Tween 20、Tween 80、NP-40、IGEPAL CA630。具体实施方式如下:
根据实施例4-11的结果设计20×逆转录抑制剂混合物:1%甲醛,1%乙醇,200mM盐酸胍,200mM异硫氰酸胍,0.01U/ul肝素,0.05ug/ul鞣酸,1%甲酰胺,0.5%苯酚。
表24
混匀后瞬离。85℃ 5min,立即置于冰上5min。
表25
混匀后瞬离。25℃ 10min,42℃ 30min,85℃ 5min,4℃ hold;
稀释200倍后对18S rRNA和Actin RNA进行定量,定量引物见表1。定量结果见图14。
由图14可以看出,泊咯沙姆能够有效提高逆转录酶效率及对模板中抑制剂的耐受性,尤其是泊咯沙姆181、184、188、237、338和407效果更好。其他非离子型表面活性剂中,Triton X-114、Triton X-100、Tween-20有较明显的提高逆转录酶效率及对模板中抑制剂的耐受性的效果,Tween-80、NP40、CA630基本没有观察到效果。
实施例13泊咯沙姆组合物对模板中逆转录抑制剂的忍耐程度。
在本实施例中,我们验证了泊咯沙姆与实施例3中的条件8组合对模板中逆转录酶抑制剂的忍耐程度。
组合1:10%泊咯沙姆181,100mM谷氨酸钾,0.01%PVSA,40mM L-组氨酸盐酸盐,200mM甜菜碱,2mM四乙基氯化铵,100mM硫酸铵,0.01%Triton X-114。
组合2:10%泊咯沙姆184,100mM谷氨酸钾,0.01%PVSA,40mM L-组氨酸盐酸盐,200mM甜菜碱,2mM四乙基氯化铵,100mM硫酸铵,0.01%Triton X-114。
组合3:10%泊咯沙姆188,100mM谷氨酸钾,0.01%PVSA,40mM L-组氨酸盐酸盐,200mM甜菜碱,2mM四乙基氯化铵,100mM硫酸铵,0.01%Triton X-114。
组合4:10%泊咯沙姆237,100mM谷氨酸钾,0.01%PVSA,40mM L-组氨酸盐酸盐,200mM甜菜碱,2mM四乙基氯化铵,100mM硫酸铵,0.01%Triton X-114。
组合5:10%泊咯沙姆338,100mM谷氨酸钾,0.01%PVSA,40mM L-组氨酸盐酸盐,200mM甜菜碱,2mM四乙基氯化铵,100mM硫酸铵,0.01%Triton X-114。
组合6:10%泊咯沙姆338,100mM谷氨酸钾,0.01%PVSA,40mM L-组氨酸盐酸盐,200mM甜菜碱,2mM四乙基氯化铵,100mM硫酸铵,0.01%Triton X-114。
按照实施例3反应体系进行逆转录效率的测试,结果见图15。
结果如图15所示,不同泊咯沙姆组合物能够有效提高逆转录酶的逆转录效率,并显著提高逆转录酶对模板中抑制剂的耐受性。
实施例14添加剂组合对逆转录酶特异性的影响
我们利用oligodT23VN的引物对含有polyA尾巴的mRNA(如Gapdh和Actin mRNA)进行了特异性的逆转录,使用表1中Gapdh和Actin的qPCR引物(特异性靶标)和5.8S、18S、28SrRNA(不带polyA尾巴,为非特异性靶标)的qPCR引物验证添加剂对逆转录酶特异性影响。
具体实施方式如下:
表26
混匀后瞬离。85℃ 5min,立即置于冰上5min。
表27
混匀后瞬离。25℃ 10min,42℃ 30min,85℃ 5min,4℃ hold;
稀释200倍后对18S rRNA和Actin RNA进行定量,定量引物见表1。定量结果见图16。
从定量结果可以看出(图16),使用OligodT23VN引物特异性逆转录polyA RNA(包含Gapdh和Actin mRNA),而不逆转录核糖体RNA(包含5.8S、18S和28S rRNA)。通过定量PCR发现加入添加剂会显著提高特异性polyA RNA的逆转录,而不影响非特异性的核糖体RNA。这表明我们发明的添加剂可以在不提高逆转录酶非特异性的情况下显著提高逆转录酶的活性。
实施例15添加剂组合对不同逆转录酶效率的影响。
具体实施方式如下:
表28
混匀后瞬离。85℃ 5min,立即置于冰上5min。
表29
混匀后瞬离。25℃ 10min,42℃ 30min,85℃ 5min,4℃ hold;
稀释200倍后对18S rRNA和Actin RNA进行定量,定量引物见表1。定量结果见图17。
从定量结果可以看出(图17),添加剂的加入能够显著促进各类逆转录酶的活性。
实施例16添加剂组合对RNA NGS建库的影响。
本实施例使用翊圣生物的Hieff
取1μg RNA,先按照Hieff
取6μL RNA加入2.5μL DEPC水,加入8.5μL的2×Frag/Prime buffer,混匀后按照12252的说明书进行RNA片段化,作为不加添加剂组。
另取6μL RNA加入6μL的2×Frag/Prime buffer,混匀后按照12252的说明书进行RNA片段化,再加入2.5μL的2×Frag/Prime buffer和入2.5μL的10×添加剂组合,作为加入添加剂组。
分别在两组中加入8μL Strand Specificity Reagent和2μL StrandSpecificity Reagent。按照12252的说明书进行后续的RNA建库。
Qubit和Qsep-100用于文库质量检测,结果见图18-22。
如图18,我们发明的添加剂能够有效促进RNA NGS建库过程中文库的产量,尤其是低质量的FFPE样本。图19-图22显示了加入添加剂对文库的峰型无太大影响,说明添加剂不会影响到建库过程中片段大小的偏好性。
综上,我们发明了一种用于逆转录过程中提高逆转录酶活性和抑制剂耐受性的组合添加剂。这种添加剂混合物不仅能够提高正常高纯度RNA样本的逆转录产物(约8倍),对复杂来源RNA样本如FFPE RNA或含甲醛、乙醇、盐酸胍、异硫氰酸胍、肝素、鞣酸、甲酰胺和苯酚等逆转录抑制剂的RNA具有更强的耐受和更高的cDNA产量。这种逆转录酶添加物组合可以在RT-qPCR检测或RNA NGS建库上显著提高复杂来源病理学样本检测的灵敏度和准确性,非常适用于疾病快速诊断领域。
- 泊洛沙姆在提高逆转录酶效率或提高逆转录酶抑制剂耐受性中的应用及添加剂混合物
- 提高表面活性剂效率、抑制层状中间相、稳定单相区温度的方法以及借助添加剂和表面活性剂-油混合物降低含硅油的微乳状液中界面张力的方法
