代谢改善剂
文献发布时间:2023-06-19 09:29:07
技术领域
本发明涉及具有改善胰岛素抵抗性、改善垂体和肾上腺功能、以及减少内脏脂肪蓄积等作用的代谢改善剂。
背景技术
近年来,由饮食的西化导致的肥胖和内脏脂肪的增加、以及被认为是伴随其产生的生活方式病(高血压、高血脂、糖尿病、高尿酸血症等)或是由这些积累导致的代谢综合症的增加,已经成为了社会性的问题,在医疗方面上的财政负担正在急剧增加。
虽然人们由饮食导致的肥胖的原因主要在于脂肪和蛋白质的过量摄入,但可以认为它们导致内脏脂肪蓄积的机制是彼此不相同的,可以想象,在实际的肥胖病状中,这两者是复杂地交织在一起的。
例如,在因脂肪的过量摄入而导致内脏脂肪蓄积的情况下,由于不认为是体液酸化(酸中毒、酸性尿)、且体重增加与脂肪重量增加是同时进行的,因此可以认为是经历了一个被动的过程,即,因脂肪的过量摄入而没有去向的脂肪蓄积在内脏中。
另一方面,因蛋白质的过量摄入而导致的内脏脂肪蓄积具有如下特征:其因动物性蛋白质的过量摄入而引起,动物性蛋白质的过量摄入是蔬菜摄入不足和动物性蛋白质的摄入量增加的结果,可以认为是体液酸化(酸中毒、酸性尿),与此同时,脂肪重量在体重增加前就会增加。由于此时糖皮质激素会增加,因此可以认为是经历了一个主动的过程,即,开启了为了生存而想要储存脂肪的生物体机制。
一直以来对于由高脂饮食导致的肥胖和代谢综合症恶化的机理,已经使用大量的模型进行了研究。然而,还没有提出能够重现由高蛋白饮食导致的内脏脂肪蓄积的食饵性模型,关于因蛋白质摄入过量引起的内脏脂肪蓄积的研究尚未取得进展。已知作为动物性蛋白质的酪蛋白为高负荷的食饵性模型(Ann.Nutr.Metab.,50,p.299,2006),提出了酪蛋白量与钾量不同的4种饵食(13LK:13%酪蛋白+低(0.3%)K;13HK:13%酪蛋白+高(2%)K;26LK:26%酪蛋白+低(0.3%)K;以及26HK:26%酪蛋白+高(2%)K)。不过,此模型是为了酸中毒的研究而被提出的,并没有被用在解析导致内脏脂肪蓄积的机制、或是评价抑制内脏脂肪蓄积的机制和医药品上。
现有技术文献
非专利文献
非专利文献1:Ann.Nutr.Metab.,50,p.299,2006
发明内容
发明要解决的问题
本发明要解决的课题是提供一种代谢改善剂,其具有改善胰岛素抵抗性、改善垂体和肾上腺功能、减少内脏脂肪蓄积(例如抑制肠系膜脂肪组织的重量增加、抑制肠系膜脂肪细胞的增大)、抑制体液(例如血液、尿液)酸化、降低血糖值、降低血液中的中性脂肪(例如甘油三酯)的量、降低血液中的尿酸值、使下丘脑-垂体-肾上腺皮质系统(HPA轴)的亢进正常化等作用,更具体而言,本发明要解决的课题是提供一种医药品及食品,其对以肉食为主的蛋白质摄入过多而引起的代谢异常具有改善作用。
此外,本发明要解决的其他课题是提供一种实验模型动物,其能够用于解析蛋白质过量摄入导致的内脏脂肪增加和代谢综合症恶化的机制等,能够重现高蛋白负荷导致的内脏脂肪蓄积。
为了解决上述课题,本发明人等发现:作为重现酸中毒病状的模型而提出的高蛋白饮食的食饵性模型即酪蛋白高负荷大鼠模型(Ann.Nutr.Metab.,50,p.299,2006)所使用的饵食中,摄食组合了13%酪蛋白和低钾(0.3%)的饵食(13LK)的大鼠能够被用作可重现由蔬菜不足和以肉食为主的动物性蛋白质过量摄入而引起的内脏脂肪蓄积的食饵性模型大鼠。该模型大鼠通过一周的摄食,其肠系膜脂肪细胞与普通饵食(以植物性的大豆蛋白为主的饵食)相比明显增大。
进而,本发明人等使用上述模型大鼠,为提供具有改善胰岛素抵抗性、改善垂体和肾上腺功能以及减少内脏脂肪组织等作用的代谢改善剂而进行深入研究,结果发现,碱化剂、优选为柠檬酸盐具有改善胰岛素抵抗性、改善垂体和肾上腺功能、减少内脏脂肪蓄积(例如抑制肠系膜脂肪组织的重量增加、抑制肠系膜脂肪细胞的增大)、抑制体液(例如血液、尿液)酸化、降低血糖值、降低血液中的尿酸值、降低血液中的中性脂肪(例如甘油三酯)的量以及使下丘脑-垂体-肾上腺皮质系统(HPA轴)的亢进正常化等改善代谢异常的作用,作为代谢改善剂是有用的,并且,发现上述代谢改善剂对以肉食为主的动物性蛋白质的过量摄入引起的代谢异常的改善、例如代谢综合症的改善特别有效,由此完成了本发明。
即,通过本发明,可以提供包含碱化剂(例如酸中毒改善剂、尿碱化剂)作为有效成分的代谢改善剂。
根据本发明的优选方案,可以提供:碱化剂为柠檬酸盐的上述代谢改善剂;包含柠檬酸盐作为有效成分的上述代谢改善剂;包含柠檬酸钠和柠檬酸钾的混合物作为有效成分的上述代谢改善剂;包含柠檬酸钠水合物和柠檬酸钾的混合物作为有效成分的上述代谢改善剂。
进而,根据本发明的优选方案,可以提供:代谢改善是改善胰岛素抵抗性的上述代谢改善剂;代谢改善是改善垂体功能(例如抑制血液中ACTH增加)的上述代谢改善剂;代谢改善是改善肾上腺功能(例如抑制血液中和/或尿液中糖皮质激素(例如皮质醇)增加)的上述代谢改善剂;代谢改善是使下丘脑-垂体-肾上腺皮质系统(HPA轴)的亢进正常化的上述代谢改善剂(例如抑制肾上腺皮质分泌糖皮质激素(例如皮质醇);相对于血液中糖皮质激素(例如皮质醇)的量与血液中ACTH的量之比(血液中糖皮质激素(例如皮质醇)的量/血液中ACTH的量),降低血液中糖皮质激素(例如皮质醇)的量;相对于血液中的糖皮质激素(例如皮质醇),增加血液中ACTH的量与血液中糖皮质激素(例如皮质醇)的量之比(血液中ACTH的量/血液中糖皮质激素(例如皮质醇)的量));代谢改善是减少内脏脂肪蓄积(例如抑制肠系膜脂肪组织的重量增加、抑制肠系膜脂肪细胞的增大)的上述代谢改善剂;代谢改善是抑制体液(例如血液、尿液)酸化的上述代谢改善剂;代谢改善是降低血糖值的上述代谢改善剂;代谢改善是降低血液中的中性脂肪(例如甘油三酯)的量的上述代谢改善剂;代谢改善是降低血液中的尿酸值的上述代谢改善剂;代谢改善是改善由蛋白质过量摄入引起的代谢异常的上述代谢改善剂;代谢改善是改善由蛋白质过量摄入引起的肥胖中的代谢异常的上述代谢改善剂;代谢改善是预防和/或改善代谢综合症的上述代谢改善剂;代谢改善是预防和/或改善代谢性酸中毒的上述代谢改善剂;为了通过改善由蛋白质过量摄入引起的肥胖中的代谢异常来预防和/或治疗肥胖而使用的上述代谢改善剂;作为医药品的上述代谢改善剂;作为食品的上述代谢改善剂。
从其它观点出发,根据本发明,可以提供:用于制造上述代谢改善剂的碱化剂、优选为柠檬酸盐的使用;一种在包括人类的哺乳动物中改善代谢的方法,包含将有效量的柠檬酸盐对包括人类的哺乳动物进行给药的工序。
进一步从其它观点出发,根据本发明,可以提供一种带有内脏脂肪蓄积的模型动物的制作方法,上述内脏脂肪蓄积由蔬菜摄入不足和动物性蛋白质的过量摄入所导致,在该方法中,使大鼠摄食组合了13%酪蛋白和0.3%钾的饵食。在本发明的优选方式中,动物为大鼠,摄食优选能够持续1至4周。
进而,根据本发明可以提供:使用上述模型动物、优选模型大鼠来筛选针对由蛋白质过量摄入引起的代谢异常的改善剂的方法;使用上述模型动物、优选模型大鼠来筛选对代谢综合症具有预防和/或治疗作用的医药品的方法;以及使用上述模型动物、优选模型大鼠来判定针对由蛋白质过量摄入引起的代谢异常的改善剂或对代谢综合症具有预防和/或治疗作用的医药品的有效性的方法。
本发明的代谢改善剂具有改善胰岛素抵抗性、改善垂体功能(例如抑制血液中ACTH的量增加、或降低血液中ACTH的量)、改善肾上腺功能(例如抑制血液中和/或尿液中糖皮质激素(例如皮质醇)的量增加、或降低血液中和/或尿液中糖皮质激素(例如皮质醇)的量)、使下丘脑-垂体-肾上腺皮质系统(HPA轴)的亢进正常化(例如,抑制肾上腺皮质分泌糖皮质激素(例如皮质醇);相对于血液中糖皮质激素(例如皮质醇)的量与血液中ACTH的量之比(血液中糖皮质激素(例如皮质醇)的量/血液中ACTH的量),降低血液中糖皮质激素(例如皮质醇)的量;相对于血液中的糖皮质激素(例如皮质醇)的量,增大血液中ACTH的量与血液中糖皮质激素(例如皮质醇)的量之比(血液中ACTH的量/血液中糖皮质激素(例如皮质醇)的量))、减少内脏脂肪蓄积(例如抑制肠系膜脂肪组织的重量增加、抑制肠系膜脂肪细胞的增大)、抑制体液(例如血液、尿液)酸化、降低血糖值或抑制血糖值增加、抑制血液中胰岛素的量增加或降低血液中胰岛素的量、抑制血液中的尿酸值增加或降低血液中的尿酸值、以及降低血液中的中性脂肪(例如甘油三酯)的量等改善代谢异常的作用,例如,其作为针对由蛋白质的过量摄入引起的代谢异常的代谢改善剂是有用的,对由蔬菜摄入不足和动物性蛋白质的过量摄入引起的代谢异常的改善和代谢综合症的预防和/或治疗特别有效。此外,本发明的代谢改善剂对蛋白质的过量摄入的改善、优选由蔬菜摄入不足和动物性蛋白质的过量摄入引起的代谢异常的改善,以及代谢综合症的预防和/或治疗是有用的。
此外,由本发明所提供的模型动物、优选模型大鼠为如下的模型动物:能够重现代谢异常的模型动物,例如,能够重现由内脏脂肪增加(例如肠系膜脂肪组织的重量增加、肠系膜脂肪组织的尺寸增加)导致的肥胖的模型动物,能够诱发胰岛素抵抗性的模型动物,能够诱发垂体功能异常(例如血液中ACTH的增加)的模型动物,能够诱发肾上腺功能异常(例如血液中和/或尿液中糖皮质激素(例如皮质醇)的增加)的模型动物,能够诱发下丘脑-垂体-肾上腺皮质系统(HPA轴)的亢进(例如,使肾上腺皮质对糖皮质激素(例如皮质醇)的分泌增加;相对于血液中ACTH的量与血液中糖皮质激素(例如皮质醇)的量之比(血液中ACTH的量/血液中糖皮质激素(例如皮质醇)的量),降低血液中糖皮质激素(例如皮质醇)的量;相对于血液中的糖皮质激素(例如皮质醇)的量,增大血液中糖皮质激素(例如皮质醇)的量与血液中ACTH的量之比(血液中糖皮质激素(例如皮质醇)的量/血液中ACTH的量))的模型动物,能够诱发体液(例如血液、尿液)酸化的模型动物,能够诱发血液中胰岛素的量增加的模型动物,能够诱发血液中瘦素的量增加的模型动物,能够诱发血液中的尿酸值增加的模型动物,和/或能够诱发血糖值异常的模型动物。
优选为如下模型动物:能够重现由蔬菜摄入不足和以肉食为主的动物性蛋白质摄入量增加引起的代谢异常状态的食饵性模型动物,能够重现伴随由蔬菜摄入不足和动物性蛋白质过量摄入引起的代谢异常的内脏脂肪增加(例如肠系膜脂肪组织的重量增加、肠系膜脂肪细胞增大)的模型动物,能够重现代谢综合症状态的模型动物,能够用于筛选对由蛋白质过量摄入引起的代谢异常、特别是对由蔬菜摄入不足和动物性蛋白质过量摄入引起的代谢异常具有改善作用的医药品的模型动物,能够用于确认上述医药品的有效性的模型动物,除此以外,还能够用于解析由动物性蛋白质过量摄入引起的内脏脂肪蓄积(例如肠系膜脂肪组织的重量增加、肠系膜脂肪细胞增大)的机制、解析代谢综合症的发病机制等的模型动物。
附图说明
图1为表示如下结果的图:使用人肾上腺皮质癌细胞株,并调节培养液pH使细胞周围的环境处于酸性侧,由此确认到糖皮质激素(皮质醇)的排出增加。平均值±标准差(n=9),
图2为表示使大鼠自由摄食组合了13%酪蛋白和0.3%钾的、模仿肉食且缺乏蔬菜的饵食(13LK)时,其体重变化和能量摄入变化的图。CRF-1(标准饲料组),平均值±标准差,*p<0.05,***p<0.001vs CRF-1(双因素重复方差分析,Bonferroni检验)
图3为表示使大鼠自由摄食组合了13%酪蛋白和0.3%钾的、模仿肉食蔬菜的饵食(13LK)时,其(a)体重、脂肪组织重量、脂肪细胞尺寸、(b)脂肪细胞基因表达、(c)尿液pH、(d)血液pH、(e)血液HCO
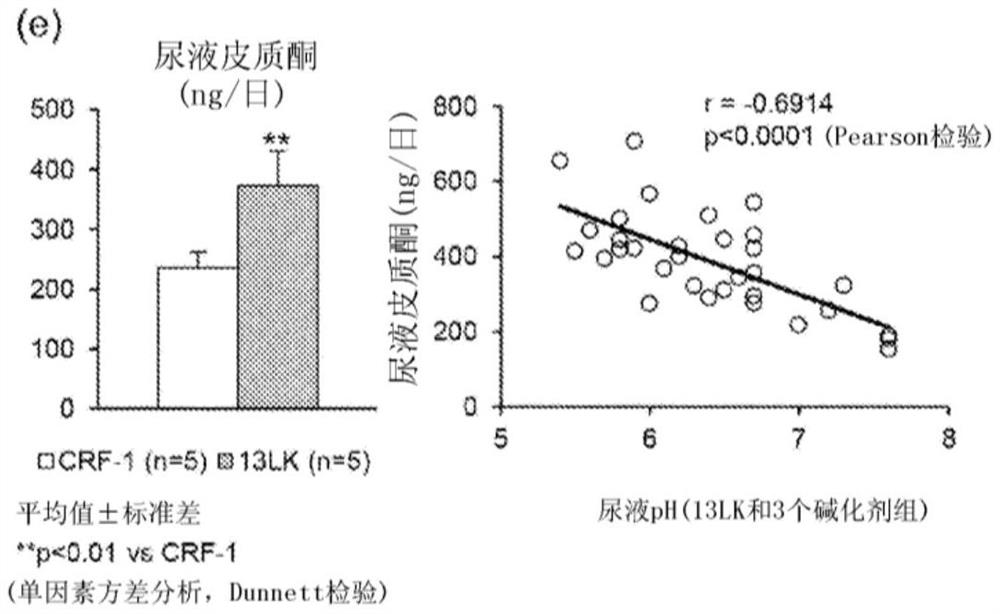
图4为表示使大鼠自由摄食组合了13%酪蛋白和0.3%钾的、模仿肉食且缺乏蔬菜的饵食(13LK)时,其(e)尿液中糖皮质激素(皮质酮)一日排泄量的变化以及与尿液中pH变化的相关关系的图。CRF-1(标准饲料组),平均值±标准差,
图5为使大鼠自由摄食组合了13%酪蛋白和0.3%钾的、模仿肉食且缺乏蔬菜的饵食(13LK)时,将其血液中糖皮质激素(皮质酮)和血液中ACTH的变化作为两个参数,考虑到它们一天中的变动而以Morning(非活动期)和Evening(活动期)来进行比较的图。CRF-1(标准饲料组),平均值±标准差,
图6为表示如下结果的图:使用本发明的模型大鼠(使用13LK作为饲料,经历一周的自由摄食),确认柠檬酸盐的作用。13LK(非给药组)、13LK+K/NaCit(柠檬酸盐给药组),平均值±标准差,
图7为表示如下结果的图:使用本发明的模型大鼠(使用13LK作为饲料,经历一周的自由摄食),确认柠檬酸盐的作用。13LK(非给药组)、13LK+K/Na Cit(柠檬酸盐给药组),平均值±标准差,
图8为将本发明的模型大鼠(使用13LK作为饲料,经历一周的自由摄食)、对本发明的模型大鼠进行柠檬酸盐给药的大鼠、以及以标准饲料作为饲料并经历一周的自由摄食的大鼠的血液中糖皮质激素(皮质酮:CORT)浓度与血液中ACTH浓度之比(CORT/ACTH和ACTH/CORT)以Morning(非活动期)和Evening(活动期)来进行比较的图。CRF-1(标准饲料组)、13LK(非给药组)、13LK+K/Na Cit(柠檬酸盐给药组),平均值±标准差,
图9为表示本发明的模型大鼠(使用13LK作为饲料,经历一周的自由摄食)、对本发明的模型大鼠进行柠檬酸盐给药的大鼠、以及以标准饲料作为饲料并经历一周的自由摄食的大鼠的血液中糖皮质激素(皮质酮:CORT)浓度与血液中ACTH浓度之比(CORT/ACTH和ACTH/CORT)跟皮质酮的相关关系的图。CRF-1(标准饲料组)、13LK(非给药组)、13LK+K/NaCit(柠檬酸盐给药组)
具体实施方式
本发明的代谢改善剂的特征在于包含碱化剂作为有效成分。作为碱化剂,能够使用例如柠檬酸盐、碳酸氢钠等,但不限定于这些。也可以使用2种以上碱化剂的混合物。作为柠檬酸的盐,能够使用例如柠檬酸钠(例如C
此外,对于作为本发明的医药品的有效成分的碱化剂来说,能够使用2种以上的柠檬酸盐的任意的混合物。例如,能够使用柠檬酸钠和柠檬酸钾的混合物。在该情况下,例如也可以将柠檬酸钠水合物与柠檬酸钾组合使用。作为包含这样的有效成分的医药品,能够将如下片剂用作本发明的代谢改善剂:在1片中含有柠檬酸钾231.5mg、柠檬酸钠水合物195.0mg。
在一个实施方式中,本发明提供的代谢改善剂除包含柠檬酸盐(例如柠檬酸钠和/或柠檬酸钾)外,还可以包含柠檬酸(例如柠檬酸酐)。
本发明的代谢改善剂具有改善胰岛素抵抗性、改善垂体功能、改善肾上腺功能、使下丘脑-垂体-肾上腺皮质系统(HPA轴)的亢进正常化、减少内脏脂肪蓄积、抑制体液(例如血液、尿液)酸化、降低血糖值、降低血液中的尿酸值、以及降低血液中的中性脂肪(例如甘油三酯)的量等改善代谢的作用。本发明的代谢改善剂的作用例如能够通过本说明书的实施例具体示出的方法来进行确认。更具体而言,能够使用可重现由蔬菜摄入量降低和以肉食为主的动物性蛋白质摄入量增加而引起的内脏脂肪增加的状态的本发明的模型动物、优选模型大鼠来确认改善胰岛素抵抗性、改善垂体功能、改善肾上腺功能、使下丘脑-垂体-肾上腺皮质系统(HPA轴)的亢进正常化、减少内脏脂肪蓄积、抑制体液(例如血液、尿液)酸化、降低血糖值、降低血液中的胰岛素的量、降低血液中的瘦素的量、降低血液中的尿酸值、以及降低血液中的中性脂肪(例如甘油三酯)的量等。
本发明的代谢改善剂例如能够用作应对由蛋白质的过量摄入引起的代谢异常的改善剂。优选对由蔬菜摄入不足和动物性蛋白质的过量摄入引起的代谢异常的改善、代谢综合症的预防和/或治疗有效。代谢综合症是除内脏脂肪蓄积外还呈现以下i)~iii)中2个症状的病状,i)血清脂质异常、ii)高血压、iii)高血糖。此外,本发明的代谢改善剂通过对由蛋白质的过量摄入引起的、优选是由蔬菜摄入不足和动物性蛋白质的过量摄入引起的代谢异常进行改善,从而能够用于预防和/或治疗由蛋白质的过量摄入引起的肥胖。
本发明的代谢改善剂的给药对象可以是患有代谢综合症的人、被认为内脏脂肪蓄积的人、内脏脂肪水平高的人或患有代谢性酸中毒的人。例如,本发明的代谢改善剂的给药对象可以是尿液酸化的人(例如尿液的pH为4.0以上且小于6.2的人)、尿酸值高的人(例如血液中尿酸值为6.0~7.0mg/dL的人、血液中尿酸值为7.0mg/dL以上的人)、血压高的人(例如收缩压为130~180mmHg或舒张压为85~109mmHg的人)、血糖值高的人(例如空腹时血糖值为100mg/dL~126mg/dL或126mg/dL以上的人)、或者血液中中性脂肪值高的人(例如血液中中性脂肪量为100mg/dL~149mg/dL或150mg/dL以上的人)。将本发明的代谢改善剂进行给药的结果是,本发明的代谢改善剂能够发挥改善胰岛素抵抗性或抑制胰岛素抵抗性恶化、改善垂体功能、改善肾上腺功能、使下丘脑-垂体-肾上腺皮质系统(HPA轴)的亢进正常化、减少内脏脂肪蓄积、抑制体液(例如血液、尿液)酸化、降低血糖值或抑制血糖值增加、降低血液中的尿酸值或抑制血液中的尿酸值增加、以及降低血液中的中性脂肪(例如甘油三酯)的量等改善代谢的作用。内脏脂肪水平可以由本领域的技术人员适当地进行判断,例如能够使用欧姆龙公司制的体脂计并按照该公司的判断标准进行判断。
本发明的医药品的给药方法没有特别限定,通常使用片剂、胶囊剂等固体制剂、或溶液剂、悬浮剂、糖浆剂等通过经口给药进行给药。根据需要,也能够制成静脉给药制剂等非经口给药制剂。片剂也可以含有除碱化剂之外的、药学上允许的添加剂(例如赋形剂、崩解剂、粘合剂、润滑剂),能够通过制药领域中公知的方法来制造。例如,片剂可以通过包含如下工序的方法制造:将碱化剂与赋形剂(例如乳糖、D-甘露醇、结晶纤维素、葡萄糖)、崩解剂(例如淀粉、羧甲基纤维素钙(CMC-Ca))、粘合剂(例如羟丙基纤维素(HPC)、明胶、聚乙烯吡咯烷酮(PVP))、润滑剂(例如硬脂酸镁、滑石)、和/或稳定剂(柠檬酸酐)等混合的工序;将混合物压片的工序。片剂可以是未包衣片,也可以是包衣片。
本发明的医药品的给药量也没有特别限定,已知蛋白质过量摄入会导致尿液发生酸化,给出了尿液的酸化存在成为显示由蛋白质过量摄入导致的代谢异常的指标的可能性,因此,通常优选选择对改善尿液酸化、优选使尿液碱化(例如在尿检中尿液pH在pH6.5以上的范围)所必须的给药量。例如,在使用柠檬酸盐作为尿碱化剂的情况下,作为柠檬酸钾·柠檬酸钠水合物配合剂,能够设为每日1~10g(例如1~6g)、优选每日3~6g左右的给药量,但并不限定于该给药量,能够根据要改善的代谢异常的种类、患者的体重、年龄等适当进行增减。
本发明的代谢改善剂的有效成分也可以用作食品。本发明提供的食品例如作为对由蛋白质的过量摄入引起的代谢异常具有改善作用的食品、或对由体液酸化引起的代谢异常具有改善作用的食品是有用的。
食品在不以治疗或预防疾病为目的的范围内,可以被人或其他哺乳动物(例如健康的人、健康的哺乳动物)所摄入。作为摄入本发明提供的食品的对象的例子,可举出:容易蔬菜摄入不足的健康人、容易摄入高蛋白饮食的健康人、蛋白质的摄入容易增多的健康人、容易蔬菜摄入不足且容易摄入高蛋白饮食的健康人、容易蔬菜摄入不足且蛋白质的摄入容易增多的健康人、蔬菜摄入不足的健康人、动物性蛋白质摄入过量的健康人、蔬菜摄入不足且动物性蛋白质摄入过量的健康人、内脏脂肪水平高的健康人、被认为是内脏脂肪蓄积的健康人、轻微肥胖的人(例如BMI为23~30的人或BMI为25~30的人)、内脏脂肪型肥胖的健康人、体液酸化的健康人(例如尿液酸化的健康人(例如尿液pH为4.5~6.0、5.0~6.0或5.5~6.0的健康人))、血压高的健康人(例如收缩压130mmHg~139mmHg或舒张压85mmHg~89mmHg的健康人)、血糖值高的健康人(例如空腹时血糖为正常高值(例如100mg/dL~110mg/dL)的健康人)、血液中中性脂肪值高的健康人(例如血液中中性脂肪的量为100mg/dL~149mg/dL的健康人)、以及尿酸值高的健康人(例如血液中尿酸值为6.0~7.0mg/dL的健康人)。作为摄入本发明提供的食品的对象的更进一步的例子,可举出具有选自以下i)~xi)的特性中至少1个的人(例如健康人):i)蛋白质(例如动物性蛋白质)摄入过量、ii)内脏脂肪水平高、iii)被认为是内脏脂肪蓄积、iv)轻微肥胖(例如BMI为23~30或BMI为25~30)、v)内脏脂肪型肥胖、vi)体液酸化(例如尿液pH为4.5~6.0、5.0~6.0或5.5~6.0)、vii)血压高(例如收缩压130mmHg~139mmHg或舒张压85mmHg~89mmHg)、viii)血糖值高(例如空腹时血糖为正常高值(例如100mg/dL~110mg/dL))、ix)血液中中性脂肪值高(例如血液中中性脂肪的量为100mg/dL~149mg/dL)、x)尿酸值高(例如血液中尿酸值为6.0~7.0mg/dL)、以及、xi)蔬菜摄入不足。应予说明,蛋白质摄入量的多寡例如可以参考日本人的饮食摄入标准(2015年版)(厚生劳动省)。
通过摄入本发明提供的食品,能够得到与本发明的代谢改善剂相同的效果。作为通过摄入本发明提供的食品而得到的效果的例子,可举出:改善胰岛素抵抗性或抑制胰岛素抵抗性恶化、改善垂体功能(例如抑制血液中ACTH的量增加、或降低血液中ACTH的量)、改善肾上腺功能(例如抑制血液中和/或尿液中糖皮质激素(例如皮质醇)的量增加、或降低血液中和/或尿液中糖皮质激素(例如皮质醇)的量)、使下丘脑-垂体-肾上腺皮质系统(HPA轴)的亢进正常化(例如,抑制肾上腺皮质分泌糖皮质激素(例如皮质醇);相对于血液中糖皮质激素(例如皮质醇)的量与血液中ACTH的量之比(血液中糖皮质激素(例如皮质醇)的量/血液中ACTH的量),降低血液中糖皮质激素(例如皮质醇)的量;相对于血液中的糖皮质激素(例如皮质醇)的量,增大血液中ACTH的量与血液中糖皮质激素(例如皮质醇)的量之比(血液中ACTH的量/血液中糖皮质激素(例如皮质醇)的量))、减少内脏脂肪蓄积(例如抑制肠系膜脂肪组织的重量增加、抑制肠系膜脂肪细胞的增大)、抑制体液(例如血液、尿液)酸化、降低血糖值或抑制血糖值增加、降低血液中的尿酸值或抑制血液中的尿酸值增加、降低血液中胰岛素的量或抑制血液中胰岛素的量增加、降低血液中瘦素的量或抑制血液中瘦素的量增加、降低血液中的中性脂肪(例如甘油三酯)的量、以及它们的组合。
作为食品的形式,只要是能够经口摄入的形式就没有特别限定,可以是补充剂,也可以是一般的食品形式。作为一般的食品的例子,可举出饮料(例如果汁等包含水果汁或蔬菜提取物的饮料、红茶饮料、运动饮料、加味水、减肥饮料)、麦芽糖、果冻、软糖和口香糖。对于本发明提供的食品而言,本领域技术人员能够根据食品的种类来适当地制造,例如,可以通过在食品材料中配合碱化剂来制造。对于食品所包含的碱化剂的含量而言,本领域技术人员也能够适当地设定,例如在使用柠檬酸钾和柠檬酸钠水合物的混合物的情况下,以柠檬酸钾和柠檬酸钠水合物的合计计算,食品中可以包含每1日摄入1~10g(例如1~6g)、优选为每1日摄入1~3g的柠檬酸钾和柠檬酸钠水合物。在本发明提供的食品为片剂的补充剂的情况下,例如可以按照上述医药品中片剂的制造方法进行制造,使每1片300mg~600mg的片剂中包含70~80重量%的碱化剂(例如柠檬酸钾和柠檬酸钠水合物)。在碱化剂为柠檬酸钾和/或柠檬酸钠水合物的情况下,本发明提供的食品还可以进一步包含柠檬酸(例如柠檬酸酐)。
作为本发明提供的实施方式的例子,可举出以下例子。
(1)包含碱化剂作为有效成分的代谢改善剂。
(2)根据(1)所述的代谢改善剂,其中,碱化剂为柠檬酸盐或碳酸氢钠。
(3)根据(1)所述的代谢改善剂,其中,碱化剂为柠檬酸盐或2种以上的柠檬酸盐的混合物。
(4)根据(1)至(3)中任一项所述的代谢改善剂,其代谢改善为改善由蛋白质过量摄入引起的代谢异常。
(5)根据(1)至(3)中任一项所述的代谢改善剂,其代谢改善为改善由蛋白质过量摄入引起的肥胖中的代谢异常。
(6)根据(1)至(3)中任一项所述的代谢改善剂,其代谢改善为改善代谢综合症中的代谢异常。
(7)根据(1)至(3)中任一项所述的代谢改善剂,其代谢改善为改善代谢性酸中毒中的代谢异常。
(8)根据(1)至(7)中任一项所述的代谢改善剂,其通过改善由蛋白质过量摄入引起的肥胖中的代谢异常,从而用于预防和/或治疗肥胖。
(9)根据(1)至(8)中任一项所述的代谢改善剂,其中,代谢改善剂为胰岛素抵抗性改善剂、体液酸化抑制剂、血糖降低剂、内脏脂肪蓄积减少剂、和/或血液中中性脂肪(例如甘油三酯)量降低剂。
(10)根据(1)至(9)中任一项所述的代谢改善剂,其中,代谢改善剂为血液中ACTH增加抑制剂、或者血液中和/或尿液中糖皮质激素增加抑制剂。
(11)根据(1)至(9)中任一项所述的代谢改善剂,其中,代谢改善剂为血液中ACTH降低剂、或者血液中和/或尿液中糖皮质激素降低剂。
(12)根据(1)至(11)中任一项所述的代谢改善剂,其中,代谢改善剂为下丘脑-垂体-肾上腺皮质系统(HPA轴)亢进正常化剂。
(13)根据(12)所述的代谢改善剂,其中,下丘脑-垂体-肾上腺皮质系统(HPA轴)亢进正常化为:抑制肾上腺皮质分泌糖皮质激素;相对于血液中的糖皮质激素的量,增大血液中ACTH的量与血液中糖皮质激素的量的比(血液中ACTH的量/血液中糖皮质激素的量);或者,相对于血液中糖皮质激素的量与血液中ACTH的量的比(血液中糖皮质激素的量/血液中ACTH的量),降低血液中糖皮质激素的量。
(14)根据(1)至(13)中任一项所述的代谢改善剂,其中,向哺乳动物(例如人)给药或使其摄入代谢改善剂的结果是,血液中的尿酸值降低和/或血液中的瘦素的量降低。
(15)根据(1)至(14)中任一项所述的代谢改善剂,其为食品。
(16)根据(1)至(15)中任一项所述的代谢改善剂,其中,该代谢改善剂是向内脏脂肪水平高的人给药、或被内脏脂肪水平高的人摄入。
(17)根据(1)至(16)中任一项所述的代谢改善剂,其中,该代谢改善剂是向具有下述i)~vi)特性的人给药、或被具有下述i)~vi)特性的人摄入:i)BMI为23以上且30以下、ii)血糖值高、iii)血压高、iv)血液中中性脂肪的量高、v)血液中尿酸值高、或者vi)i)~v)的组合。
(18)根据(1)至(17)中任一项所述的代谢改善剂,其中,该代谢改善剂是向体液酸化的人(例如由动物性蛋白质的过量摄入导致的体液(例如尿液)酸化的人)给药、或被体液酸化的人摄入。
(19)一种带有内脏脂肪蓄积的模型动物的制作方法,上述内脏脂肪蓄积由动物性蛋白质的过量摄入和蔬菜摄入不足所导致,在该方法中,使大鼠摄食组合了13%酪蛋白和0.3%钾的饵食。
(20)一种使用(19)所述的模型动物来筛选针对由蛋白质过量摄入引起的代谢异常的改善剂的方法。
(21)一种使用(19)所述的模型动物来判定针对由蛋白质过量摄入引起的代谢异常的改善剂的有效性的方法。
由本发明所提供的模型动物作为重现了伴随由蔬菜摄入不足和动物性蛋白质的过量摄入引起的代谢异常的内脏脂肪蓄积的模型动物,能够用于例如筛选对由蛋白质过量摄入引起的代谢异常、特别是由蔬菜摄入不足和动物性蛋白质的过量摄入引起的代谢异常具有改善作用的医药品,筛选对代谢综合症具有预防和/或治疗作用的医药品,确认上述医药品的有效性,但本发明的模型动物的用途不限定于上述特定的用途。作为本发明的模型动物,优选使用模型大鼠。在使用大鼠的情况下,能够通过自由摄食通常1~4周组合了13%酪蛋白和0.3%钾的饵食来制作本发明的模型大鼠,但摄食的方法和时间能够根据作为目标的内脏脂肪组织量、体液(例如血液、尿液)的酸度、血糖值和血液中的中性脂肪(例如甘油三酯)的量的程度等主要因素来适当变更。
作为现有的肥胖研究的模型动物的高脂饮食负荷模型动物、转基因模型动物到肥胖发病为止需要1至数月,与此相比,由本发明所提供的上述模型动物具有短时间内在内脏脂肪组织中产生变化这一特征。在本发明的模型动物中,在1周左右的摄食后,即使在体重上与对照组之间没有差异,在内脏脂肪组织上也可以观察到11βHSD-1mRNA的表达增加、内脏脂肪组织的重量增加和细胞尺寸的增大,进而在2周左右,可以认为是有明确的胰岛素抵抗性等代谢综合症的各种症状。虽然并不拘泥于任何特定的理论,但可以认为本发明的模型动物的病状发病机理是由生物体环境偏向酸性侧而引起的、肾上腺皮质对糖皮质激素的过量分泌,可以认为,在形成肥胖的初期阶段,肾上腺皮质对糖皮质激素的过量分泌触发了内脏脂肪的蓄积,导致肥胖发病。此外,可以理解为:通过用柠檬酸盐等碱化剂进行给药,本发明的模型动物中的代谢综合症的进行可以被抑制,这一点也支持上述肥胖发病机制。
实施例
以下,通过实施例对本发明进一步具体的说明,但是本发明的范围并不限定于下述的实施例。
例1
通过以下的方法,研究是否能够通过改良酪蛋白高负荷大鼠模型(Ann.Nutr.Metab.,50,p.299,2006)的饵食来制造肥胖模型,上述酪蛋白高负荷大鼠模型是能重现酸中毒病症的高蛋白饮食的食饵性模型。
在此之前,McCarty(McCarty MF.Acid-base balance may influence risk forinsulin resistance syndrome by modulating cortisol output.Med.Hypotheses 64:380-384,2005)已报道了酸中毒促进糖皮质激素的产生、库欣综合症被认为是内脏肥胖、以及向糖皮质激素活性物质的转化酶11β-HSD1与内脏脂肪蓄积有关,所以从上述这些内容出发,为了明确作用点,使用作为体外释放糖皮质激素(皮质醇)的靶细胞的人肾上腺皮质癌细胞株,并调节培养液pH使细胞周围的环境处于酸性侧,由此,确认到皮质激素的排出增加(图1)。
使大鼠(Wistar、雄性、n=9、年龄为5周、Charles River Laboratories Japan,Inc.)自由摄食组合了13%酪蛋白和0.3%钾的饵食(13LK),历时4周。作为对照组,使之同样地摄食以植物性蛋白质为主的标准饲料(CFR-1、Oriental Yeast Co.,ltd.制)。在1周后,未看到体重产生变化(图2),但可观察到1周后的尿液pH、血液pH、HCO
另外,也可以看到血液中皮质酮的增加,也可以观察到血液中ACTH的增加(活动期、图5)。与对照组相比,内脏脂肪(肠系膜脂肪)的重量增加,细胞尺寸也增大(图3的(a))。肠系膜脂肪中的11β-HSD1 mRNA表达也上升(图3的(b))。进而,血液中的瘦素为CRF-1组(n=10):0.38±0.19ng/mL、13LK组(n=10):2.13±0.31ng/mL,13LK组明显增加,还能够看到血液中胰岛素、血糖值和HOMA-R值也上升,可以认为是代谢综合症的症状(表1)。也可以发现血液中尿酸值的上升。
[表1]
平均值±标准差
糖皮质激素被称为生存激素,其与为了从冰河期(饥饿状态)中生存下来而获得的脂肪蓄积(=避免饥饿)相关,上述结果也与这一假设一致。如上所述,可以证明:用13LK作为饲料而制备的本发明的模型大鼠作为新的代谢综合症模型动物是有用的,特别是,作为由蔬菜不足和动物性蛋白质的过量摄入而产生的内脏脂肪蓄积的模型动物是有用的。此外,可以解析由生物体酸化和与之相伴的肾上腺皮质对糖皮质激素的过量分泌为起始而进展到内脏肥胖、代谢综合症的一系列的过程和病状机理。
例2
使用在例1中制备的本发明的模型大鼠(使用13LK作为饲料,经历一周的自由摄食),通过以下的方法确认柠檬酸盐的改善代谢的作用。制备包含柠檬酸盐的水溶液(在100mL中包含370mg的柠檬酸钾和312mg的柠檬酸钠水合物的水溶液),对上述模型大鼠进行一周的饮水给药(给药组:13LK+K/Na Cit),与非给药组(13LK)进行比较。一周内,未看到给药组与非给药组之间存在体重变化(图6(a))。
与例1同样地,确认各生物化学参数的变化,其结果是,在给药组中可以观察到尿液pH、血液pH上升,同时血液HCO
此外,在3组中比较皮质酮(CORT)分泌能力(CORT/ACTH比、分泌一定量的ACTH所必需的CORT的浓度)、ACTH分泌能力(ACTH/CORT比、即分泌一定量的CORT所必需的ACTH的浓度)(图8)。首先,对CORT/ACTH比而言,与早上(9:30-10:30)相比,在傍晚(16:30-17:30)显示出相当高的值,对于ACTH/CORT比而言,与早上相比,在傍晚显示出稳定的低值(图8)。在此,可以认为:如果柠檬酸盐给药组(13LK+K/Na Cit组)抑制垂体分泌ACTH,则为了分泌同等的ACTH量所需的CORT浓度就必须要增加,因此CORT/ACTH比会增加,另一方面,如果柠檬酸盐给药组(13LK+K/Na Cit组)抑制肾上腺皮质分泌CORT,则为了分泌同等的CORT量所需的ACTH浓度就必须要增加,因此ACTH/CORT比会增加。实际上,CORT/ACTH比无论是在早上还是傍晚,在3组间都没有差异,ACTH/CORT比虽然傍晚在3组间没有差异,但在早上,13LK+K/Na Cit组、CRF-1组与13LK组相比示出明显的高值(可看到示出高值的个体多)(图8)。由此,可以认为结果是:柠檬酸盐给药抑制垂体分泌ACTH的可能性较低,而是抑制肾上腺皮质分泌CORT。
实际上,当在3组间解析“实际的CORT分泌量与CORT分泌能力”、“实际的CORT分泌量与ACTH分泌能力”时,在图9的上段(A)中,直线的斜率不同,可以理解为“即使13LK组中CORT分泌能力低,实际的CORT分泌量也高,通过柠檬酸盐给药,使得CORT分泌降低,由此恢复到正常组的水平”。此外,在图9的下段(B)中,plot分布根据组的不同而不同,可以理解为“虽然在13LK组中不存在实际的CORT分泌量显示低值的个体,但通过柠檬酸盐给药,使得CORT分泌降低,从而出现了ACTH分泌能力上升的个体,由此恢复到正常组的水平”(图9)。可以理解为,通过柠檬酸盐给药,在13LK组中所看到的下丘脑-垂体-肾上腺皮质系统(HPA轴)的亢进已经正常化了。
[表2]
平均值±标准差#p<0.05vs 13LK(单因素方差分析,Dunnett检验)
例3
使用在例1中制备的本发明的模型大鼠(使用13LK作为饲料,经历一周的自由摄食),使用柠檬酸盐或碳酸氢钠作为碱化剂进行给药,确认尿液pH和尿液中的糖皮质激素(皮质酮)排泄量,结果示于表3。与对照组相比,在柠檬酸盐给药组和碳酸氢钠给药组中,尿液pH均上升,皮质酮排泄量均降低。
[表3]
- 肥胖抑制剂、抗痴呆症剂、除臭剂、抗老化剂、抗糖化剂、抗I型变态反应剂、抗高血压剂、风味改善剂、肌肉增强剂和骨代谢改善剂
- 糖代谢改善剂和糖代谢改善组合物
