含有卡巴拉汀的透皮治疗系统
文献发布时间:2023-06-19 10:18:07
技术领域
本发明涉及用于向体循环透皮施用卡巴拉汀的透皮治疗系统(TTS),以及所述透皮治疗系统的制造方法、治疗方法和用途。
背景技术
活性剂卡巴拉汀(也称为乙基甲基氨基甲酸(S)-3-[1-(二甲基氨基)乙基]苯酯,CAS号123441-03-2)是属于氨基甲酸苯酯家族的副交感神经剂或胆碱能剂。它具有以下化学式。
卡巴拉汀抑制丁酰胆碱酯酶和乙酰胆碱酯酶两者。通常,卡巴拉汀用于治疗阿尔茨海默病型轻度至中度痴呆症和帕金森氏病所致的痴呆症。
目前,卡巴拉汀可商购获得,例如以胶囊形式和透皮治疗系统形式。
可以名称
根据贴剂的尺寸,
与
因此,期望提供与
因此,本领域需要用于透皮施用卡巴拉汀的改进的透皮治疗系统。
发明内容
本发明的一个目的是提供用于透皮施用卡巴拉汀的TTS,其与当前可商购获得的卡巴拉汀TTS
本发明的另一个目的是提供用于透皮施用卡巴拉汀而不引起显著的皮肤刺激问题的TTS。
本发明的另一个目的是提供用于透皮施用卡巴拉汀的TTS,其适用于预防、治疗阿尔茨海默病、帕金森氏病相关的痴呆症和/或创伤性脑损伤症状或延缓阿尔茨海默病、帕金森氏病相关的痴呆症和/或创伤性脑损伤症状进展的方法,或适用于治疗由阿尔茨海默病或帕金森氏病引起的轻度至中度痴呆症的方法。
现已令人惊讶地发现,这些目的和其他目的中的至少一个是通过本发明实现的,根据一个方面,本发明涉及一种用于透皮施用卡巴拉汀的透皮治疗系统,所述系统包括含有卡巴拉汀的层结构,所述含有卡巴拉汀的层结构包括:
A)背衬层;
B)含有卡巴拉汀的层,其包含至少一种丙烯酸聚合物;和
C)皮肤接触层,其包含至少一种苯乙烯-异戊二烯-苯乙烯嵌段共聚物和至少一种增粘剂。
特别地,已经发现,由于TTS包括含有活性物的丙烯酸层以及附加皮肤接触层的事实,其中优选地至少一种苯乙烯-异戊二烯-苯乙烯嵌段共聚物和至少一种增粘剂以基于皮肤接触层的总重量的至少90重量%的总量、更优选以至少99重量%的总量存在于皮肤接触层中,使得渗透特性可与市售产品
本发明还涉及一种用于制造透皮治疗系统的方法,所述方法包括以下步骤:
1)通过组合至少以下组分来提供含有卡巴拉汀的涂覆组合物
i)卡巴拉汀;和
ii)至少一种丙烯酸聚合物;
2)将含有卡巴拉汀的涂覆组合物以提供所需面积重量的量涂覆于膜上,
3)干燥涂覆的含有卡巴拉汀的涂覆组合物以提供含有卡巴拉汀的层,
4)通过组合至少以下组分为附加皮肤接触层提供另外的涂覆组合物
a)至少一种苯乙烯-异戊二烯-苯乙烯嵌段共聚物;和
b)至少一种增粘剂;
5)根据步骤2和3涂覆并干燥另外的涂覆组合物,其中所述膜是离型衬垫,
6)将皮肤接触层的粘合剂侧层压到含有卡巴拉汀的层的粘合剂侧上,以提供具有所需释放面积的含有卡巴拉汀的层结构,
7)从含有卡巴拉汀的层结构中冲压出单独系统,
8)任选地将不含卡巴拉汀的自粘层结构粘附至单独系统,所述不含卡巴拉汀的自粘层结构还包括背衬层和不含卡巴拉汀的压敏粘合剂层,并且所述不含卡巴拉汀的自粘层结构比含有卡巴拉汀的自粘层结构的单独系统大。
定义
在本发明的含义内,术语“透皮治疗系统(TTS)”是指经由透皮递送将活性剂(例如卡巴拉汀)施用至体循环的系统,并且是指如下整个单独给药单元:在移除任选存在的离型衬垫后其施加至患者皮肤,并在含有活性剂的层结构中包含治疗有效量的活性剂,在所述含有活性剂的层结构之上任选地包括附加粘合剂覆层。含有活性剂的层结构可位于离型衬垫(可剥离保护层)上,因此所述TTS还可包括离型衬垫。在本发明的含义内,术语“TTS”特别指提供透皮递送的系统,而不包括例如经由离子电渗或微穿孔的活性物递送。透皮治疗系统也可称为透皮药物递送系统(TDDS)或透皮递送系统(TDS)。
在本发明的含义内,术语“含有卡巴拉汀的层结构”是指含有治疗有效量的卡巴拉汀的层结构,并且包括背衬层、含有卡巴拉汀的层和皮肤接触层。
在本发明的含义内,术语“治疗有效量”是指TTS中的活性剂的量,如果由TTS向患者施用,则所述量足以提供预防、治疗阿尔茨海默病、帕金森氏病相关的痴呆症和/或创伤性脑损伤症状或延缓阿尔茨海默病、帕金森氏病相关的痴呆症和/或创伤性脑损伤症状进展。TTS在系统中包含的活性物通常比实际上提供给皮肤和体循环的活性物更多。通常需要这种过量的活性剂以提供足够的驱动力,用于从TTS递送至体循环。
在本发明的含义内,术语“活性物”、“活性剂”等以及术语“卡巴拉汀”是指呈任意药学上可接受的化学及形态形式和物理状态的卡巴拉汀。这些形式包括但不限于:游离碱/游离酸形式的卡巴拉汀;质子化或部分质子化的卡巴拉汀;卡巴拉汀盐,共晶以及特别是通过添加无机或有机酸/碱形成的酸/碱加成盐,诸如盐酸卡巴拉汀或酒石酸卡巴拉汀;溶剂化物、水合物、包合物、络合物等;以及颗粒形式的卡巴拉汀(可以是微粉化的、结晶的和/或无定形的);以及前述形式的任意混合物。包含在介质诸如溶剂中的卡巴拉汀可以是溶解或分散的或者部分溶解和部分分散的。
当提到使用特定形式的卡巴拉汀制造TTS时,并不排除在最终的TTS中这种形式的卡巴拉汀与含有卡巴拉汀的层结构的其他成分之间的相互作用,例如盐形成或络合化。这表示,即使卡巴拉汀以游离碱/酸形式包含在内,但在最终的TTS中也可能以质子化或部分质子化/或去质子化或部分去质子化形式或者酸加成盐形式存在,或者,如果卡巴拉汀以盐形式包含在内,则部分卡巴拉汀可能在最终的TTS中以游离碱形式存在。除非另外指明,否则特别地层结构中的卡巴拉汀的量是指在制造TTS的过程中TTS中所包含的卡巴拉汀的量并基于游离碱形式的卡巴拉汀进行计算。例如,当制造过程中TTS中包含a)0.1mmol(等于25.03mg)卡巴拉汀碱或b)0.1mmol(等于40.04mg)酒石酸卡巴拉汀时,在本发明的含义内,层结构中卡巴拉汀的量在两种情况下均为0.1mmol或25.03mg。
在TTS的制造过程中,TTS中包含的卡巴拉汀起始原料可以呈颗粒形式。卡巴拉汀可以例如以颗粒和/或溶解的形式存在于含有卡巴拉汀的层结构中。
在本发明的含义内,术语“颗粒”是指包括单独颗粒的固体颗粒状材料,单独颗粒的尺度与材料相比可忽略不计。特别地,颗粒为固体,包括塑性/可变形固体,包括无定形和结晶材料。
在本发明的含义内,术语“分散”是指其中起始原料(例如卡巴拉汀)不完全溶解的步骤或步骤的组合。在本发明的意义上,分散包括根据起始原料的溶解度(例如卡巴拉汀在涂覆组合物中的溶解度)溶解一部分所述起始原料(例如卡巴拉汀颗粒)。
用于活性剂递送的TTS主要有两种类型,即基质型TTS和贮库型TTS。在基质型TTS中活性剂的释放主要由包括活性剂本身的基质控制。与之相对,贮库型TTS通常需要控速膜控制活性剂的释放。原则上基质型TTS也可含有控速膜。然而,基质型TTS的优势在于,相比于贮库型TTS,通常不需要定速膜,不会因膜破裂而发生剂量突释。概括地说,基质型透皮治疗系统(TTS)制造复杂性低且患者使用简便。
在本发明的含义内,“基质型TTS”是指其中活性物均匀地溶解和/或分散于聚合物载体即基质中的系统或结构,所述基质与活性剂和其余任选成分形成基质层。在这种系统中,基质层控制活性剂从TTS中的释放。优选地,基质层具有足够的自支撑内聚力,使得不需要其他层之间的密封。因此,在本发明的一个实施方案中,含有活性剂的层可以是含有活性剂的基质层,其中活性剂均匀地分布于聚合物基质中。在某些实施方案中,含有活性剂的基质层可包括两个含有活性剂的基质层,这两个含有活性剂的基质层可层压在一起。基质型TTS可以特别地是“粘合剂中的药物”类型的TTS的形式,是指其中活性物均匀地溶解和/或分散在压敏粘合剂基质中的系统。在这点上,含有活性剂的基质层也可称为含有活性剂的压敏粘合剂层或含有活性剂的压敏粘合剂基质层。根据本发明,包含溶解和/或分散于聚合物凝胶例如水凝胶中的活性剂的TTS根据本发明也被认为是基质型。
术语“贮库型TTS”是指具有含有活性剂的液体贮库的TTS。在这种系统中,活性剂的释放优选地由控速膜控制。特别地,贮库密封于背衬层与控速膜之间。因此,在一个实施方案中,含有活性剂的层可以是含有活性剂的贮库层,其优选地包括包含活性剂的液体贮库。此外,贮库型TTS通常还包括皮肤接触层,其中贮库层和皮肤接触层可由控速膜隔开。在贮库层中,活性剂优选地溶解于诸如乙醇或水等溶剂中或者溶解于硅油中。皮肤接触层通常具有粘合特性。
在本发明的含义内,贮库型TTS不应被理解为基质型的。然而,微贮库TTS(双相系统,其具有分散于聚合物外相中的含有活性物的内相的沉积物(例如球体、液滴))在本领域中被认为是基质型TTS与贮库型TTS的混合形式,就药物传输和药物递送概念而言,其不同于均匀单一相基质型TTS和贮库型TTS,但在本发明的含义内被认为是基质型的。可通过光学显微镜测量仪(例如通过包括相机例如Leica DSC320的Leica MZ16),以10与400倍之间的放大倍数(取决于所需的检测限)在不同位置拍摄微贮库的照片,来测定微贮库液滴的尺寸。通过使用成像分析软件,可测定微贮库的尺寸。
在本发明的含义内,术语“含有卡巴拉汀的层”是指含有活性剂卡巴拉汀并提供释放面积的层。所述术语涵盖含有卡巴拉汀的基质层和含有卡巴拉汀的贮库层。如果含有卡巴拉汀的层是含有卡巴拉汀的基质层,则所述层存在于基质型TTS中。存在附加皮肤接触层作为粘合剂层,并且可以提供粘合剂覆层。附加皮肤接触层通常制成不含活性剂。然而,由于浓度梯度,活性剂卡巴拉汀会随时间推移从基质层向附加皮肤接触层迁移,直至达到平衡。附加皮肤接触层可存在于含有卡巴拉汀的基质层上或通过膜(优选地是控速膜)与含有卡巴拉汀的基质层隔开。如果含有卡巴拉汀的层是含有卡巴拉汀的贮库层,则所述层存在于贮库型TTS中并且所述层包含处于液体贮库中的活性剂卡巴拉汀。另外,为了提供粘合特性,存在附加皮肤接触层。优选地,控速膜将贮库层与附加皮肤接触层隔开。附加皮肤接触层可制成不含活性剂或含有活性剂。如果附加皮肤接触层不包含活性剂,则活性剂会由于浓度梯度随时间推移从贮库层向皮肤接触层迁移,直至达到平衡。另外,可提供粘合剂覆层。
如本文所用,含有卡巴拉汀的层优选地是含有卡巴拉汀的基质层并且是指最终凝固层。优选地,在涂覆并干燥如本文所述的含有溶剂的涂覆组合物之后获得含有卡巴拉汀的基质层。或者,在熔融涂覆并冷却之后获得含有卡巴拉汀的基质层。还可通过层压两个或更多个具有相同组成的此类凝固层(例如干燥或冷却层)以提供所需的面积重量来制造含有卡巴拉汀的基质层。基质层可以是自粘的(以压敏粘合剂基质层的形式)。TTS包括附加皮肤接触层,用于提供足够的粘性。优选地,基质层是压敏粘合剂基质层。任选地,可存在粘合剂覆层。
在本发明的含义内,术语“压敏粘合剂”(也简称为“PSA”)是指具体通过指压粘附、具有永久粘结性、持粘力强且可从光滑表面移除而无残留的材料。压敏粘合剂层接触皮肤时“自粘”,即提供对皮肤的粘合性,使得通常无需在皮肤上进一步辅助固定。“自粘”层结构包括用于皮肤接触的压敏粘合剂层,其可被设置为压敏粘合剂基质层形式或附加层即压敏粘合剂皮肤接触层形式。仍可采用粘合剂覆层来增强粘合性。压敏粘合剂的压敏粘合特性取决于所使用的聚合物或聚合物组合物。
如本文所用,含有卡巴拉汀的基质层是如下的层:其含有溶解于或分散于至少一种丙烯酸聚合物中的活性剂卡巴拉汀,或者含有溶解于溶剂中以形成卡巴拉汀-溶剂混合物的活性剂卡巴拉汀,所述混合物以沉积物(特别是液滴)形式分散于至少一种聚合物中。优选地,所述至少一种丙烯酸聚合物是丙烯酸压敏粘合剂。在本发明的含义内,术语“压敏粘合剂层”是指由含有溶剂的粘合剂涂覆组合物涂覆于膜上并蒸发溶剂之后获得的压敏粘合剂层。
在本发明的含义内,术语“皮肤接触层”是指包括在含有卡巴拉汀的层结构中以在施用期间与患者皮肤直接接触的层。当TTS包括附加皮肤接触层时,含有卡巴拉汀的层结构的其他层不接触皮肤且无需具有自粘特性。如上所述,附着于含有卡巴拉汀的层的附加皮肤接触层会随时间推移吸收部分卡巴拉汀。可以使用附加皮肤接触层来增强粘附性。附加皮肤接触层和含有卡巴拉汀的层的尺寸通常是共延的且对应于释放面积。然而,附加皮肤接触层的面积也可大于含有卡巴拉汀的层的面积。在这种情况下,释放面积仍指含有卡巴拉汀的层的面积。
在本发明的含义内,术语“面积重量”是指指定层例如基质层的净重,单位为g/m
除非另外指明,否则“%”是指重量%。
在本发明的含义内,术语“聚合物”是指通过聚合一种或多种单体获得的由所谓重复单元组成的任意物质,并且包括由一种类型的单体组成的均聚物以及由两种或更多种类型的单体组成的共聚物。聚合物可具有任意构造,诸如直链聚合物、星形聚合物、梳形聚合物、刷形聚合物,在共聚物情况下可具有任意单体排列,例如交替共聚物、统计共聚物、嵌段共聚物或接枝聚合物。最小分子量根据聚合物类型而不同并且是本领域技术人员已知的。聚合物的分子量例如可高于2000道尔顿,优选地高于5000道尔顿,且更优选地高于10,000道尔顿。相应地,分子量低于2000道尔顿、优选地低于5000道尔顿或更优选地低于10,000道尔顿的化合物通常称为低聚物。
在本发明的含义内,术语“粘合剂覆层”是指自粘层结构,其不含活性剂且面积大于含有卡巴拉汀的结构,并且提供附加的粘附于皮肤的区域,但不提供活性剂卡巴拉汀的释放面积。粘合剂覆层因此增强了TTS的总体粘合特性。粘合剂覆层包括可提供闭塞或非闭塞特性的背衬层以及粘合剂层。优选地,粘合剂覆层的背衬层提供非闭塞特性。
在本发明的含义内,术语“背衬层”是指支撑含有卡巴拉汀的层或形成粘合剂覆层的背衬的层。在储存和施用期期间,TTS中的至少一个背衬层以及通常含有卡巴拉汀的层的背衬层对于层中包含的活性剂卡巴拉汀基本上不可渗透,并因此根据法规要求避免了活性物损失或交叉污染。优选地,背衬层也是闭塞的,意味着对于水和水蒸气基本上不可渗透。适合用于背衬层的材料包括聚对苯二甲酸乙二酯(PET)、聚乙烯(PE)、乙烯乙酸乙烯酯-共聚物(EVA)、聚氨酯及其混合物。因此,合适的背衬层是例如PET层压体、EVA-PET层压体和PE-PET层压体。合适的还有织造或非织造背衬材料。
根据本发明的TTS可由如在体外释放测试中测量的某些参数来表征。
在本发明的含义内,“体外释放速率”是使用Ph Eur/USP的旋转圆筒设备,在32℃下使用600ml脱气的0.9%氯化钠溶液并以50rpm旋转来测定的。在0.5、2、4、7和24小时,取出4ml样品,并使用经过验证的HPLC方法和UV光度检测器进行分析。
根据本发明的TTS还可由如在体外皮肤渗透测试中测量的某些参数来表征。
通常,体外渗透测试是在Franz扩散池中进行的,使用EVA膜(例如9%乙酸乙烯酯)和pH 5.5或7.4的磷酸盐缓冲液作为受体介质(32℃,含0.1%的叠氮化盐水)。
此外,体外渗透测试可以在Franz扩散池中进行,使用人或动物的皮肤,并且优选使用具有800μm的厚度和完整表皮的皮刀裂厚人类皮肤,并使用pH 5.5或7.4的磷酸盐缓冲液作为受体介质(32℃,含0.1%的叠氮化盐水),添加或不添加最多40体积%的有机溶剂,例如乙醇、乙腈、异丙醇、二丙二醇、PEG 400,使得受体介质可以例如含有60体积%pH 5.5的磷酸盐缓冲液、30体积%二丙二醇和10体积%乙腈。
如未另外指明,则体外渗透测试使用EVA膜(9%乙酸乙烯酯,50μm)和pH 5.5磷酸盐缓冲液作为受体介质(32℃,含0.1%叠氮化盐水)进行。使用经过验证的HPLC方法(色谱柱:不锈钢色谱柱,150mmx 3.9mm I.D.,填充有C18相(例如Novapak C18,4μm粒径,Waters)或等效色谱柱,色谱柱温度:20-25℃;流动相:乙腈/水20:80(v/v)+0.35mL TEA/100mL,pH3.5;必要时用磷酸(85%)调节pH;流速:1.0ml/分钟;压力:约100bar;进样量:20μL;检测:UV,210nm,停止时间:6分钟)定期测定渗透进受体介质的活性剂的量。取样品体积时将受体介质完全或部分替换为新鲜介质,并且所测量的活性剂的渗透量与最后两次取样点之间的渗透量有关,而非与至此为止的总渗透量有关。
因此,在本发明的含义内,参数“渗透量”的单位为μg/cm
渗透量还可以“累积渗透量”给定,所述累积渗透量对应于某一时间点渗透的活性剂的累积量。例如,在如上所述的体外渗透测试(其中在例如0小时、2小时、4小时、8小时、12小时和24小时时测量渗透到受体介质中的活性剂的量)中,12小时时活性剂的“累积渗透量”对应于从0小时至2小时、从2小时至4小时、从4小时至8小时以及从8小时至12小时的渗透量的总和。
在本发明的含义内,对于某段经过时间某一取样间隔内的参数“皮肤渗透速率”的单位为μg/cm
“累积皮肤渗透速率”可由对应的累积渗透量通过所述累积渗透量除以经过时间计算得到。例如,在如上所述的体外渗透测试(其中在例如0小时、2小时、4小时、8小时、12小时和24小时时测量渗透到受体介质中的活性剂的量)中,12小时时的“累积皮肤渗透速率”由12小时的累积渗透量(参见上文)除以12小时计算得到。
在本发明的含义内,上述参数“渗透量”和“皮肤渗透速率”(以及“累积渗透量”和“累积皮肤渗透速率”)是指由至少3次体外渗透测试实验计算得到的平均值。如未另外指明,则这些平均值的标准偏差(SD)是指校正样品标准偏差,施用以下公式计算:
其中n为样品尺寸,{x
根据本发明的TTS也可由如在体内临床研究中测量的某些参数来表征。
在本发明的含义内,参数“平均释放速率”是指在施用期间(例如,1至7天)活性剂通过人体皮肤释放到体循环中的平均释放速率,以μg/小时或mg/天为单位,并基于临床研究中在所述施用期间获得的AUC。
在本发明的含义内,术语“延长的时间段”是指至少约24小时、或至少约48小时、或至少约84小时、或至少约168小时、或至少约1天、或至少大约3.5天、或至少约7天的一段时间,或者是指约24小时至约168小时或1天至7天、或约24小时至约84小时或1天至3.5天的一段时间。
对于连续药物治疗,优选将药物施用频率保持足够高,以便维持治疗有效的血浆浓度。换句话说,两次剂型施用之间的间隔,也称为给药间隔,需要相应地进行调整。在本发明的含义内,术语“给药间隔”是指两次连续的TTS施用之间的时间段,即TTS被施加至患者皮肤的两个连续的时间点之间的间隔。一旦施加,TTS通常在整个给药间隔内保持在患者皮肤上,并且仅在给药间隔结束时移除,此时将新的TTS施加至皮肤。例如,如果给药间隔是24小时或1天,则将TTS施加至患者皮肤并保持在其上24小时或1天。24小时或1天后,将TTS从皮肤上移除,然后施加新的TTS。因此,24小时或1天的给药间隔允许全天候治疗的每日TTS更换模式。
在本发明的含义内,术语“室温”是指进行实验的实验室室内未经调节的温度,通常在15℃至35℃范围内,优选地在18℃至25℃范围内。
在本发明的含义内,术语“患者”是指已表现出表明需要治疗的特定一种或多种症状的临床表现的受试者、接受病状的预防性治疗的受试者、或经诊断患有待治疗的病状的受试者。
在本发明的含义内,术语“涂覆组合物”是指溶剂中包含所有基质层组分的组合物,所述涂覆组合物可涂覆于背衬层或离型衬垫上,以在干燥后形成基质层。
在本发明的含义内,术语“压敏粘合剂组合物”是指至少与溶剂(例如正庚烷或乙酸乙酯)混合的压敏粘合剂。
在本发明的含义内,术语“溶解”是指获得溶液的过程,所述溶液是澄清的且不包含任何肉眼可见的颗粒。
在本发明的含义内,术语“溶剂”是指任意液体物质,优选地是挥发性有机液体,诸如甲醇、乙醇、异丙醇、丙酮、乙酸乙酯、二氯甲烷、己烷、正庚烷、甲苯及其混合物。
附图说明
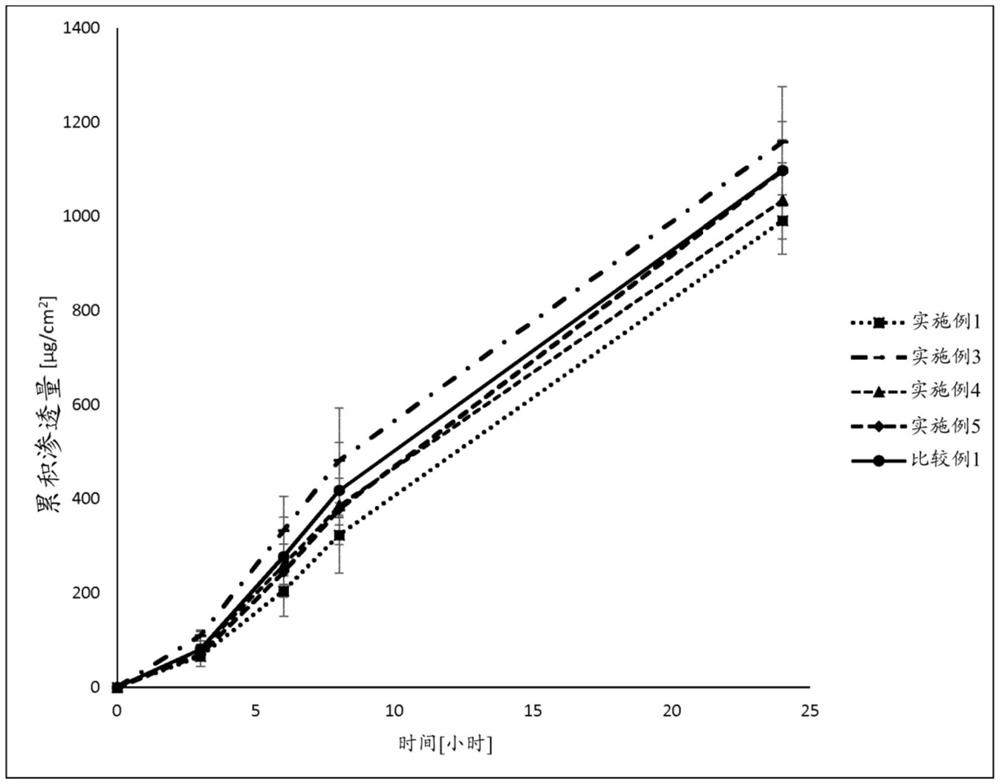
图1描绘了比较例1以及实施例1和3至5在生产后(“初始”)24小时内的累积卡巴拉汀的体外渗透。
图2描绘了比较例1和实施例2至5在生产后(“初始”)的粘合力。
图3描绘了比较例1和实施例1至5在生产后(“初始”)的剥离力。
图4描绘了比较例1和实施例1至5在生产后(“初始”)24小时内的卡巴拉汀的体外释放速率。
具体实施方式
TTS结构
本发明涉及一种用于透皮施用卡巴拉汀的透皮治疗系统,所述系统包括含有卡巴拉汀的层结构,所述含有卡巴拉汀的层结构包括:
A)背衬层;
B)含有卡巴拉汀的层,其包含至少一种丙烯酸聚合物;和
C)皮肤接触层,其包含至少一种苯乙烯-异戊二烯-苯乙烯嵌段共聚物和至少一种增粘剂。
根据本发明的TTS可以是基质型TTS或贮库型TTS,并且优选地是基质型TTS。
在根据本发明的基质型TTS中,卡巴拉汀均匀地溶解和/或分散于聚合物载体即基质中,所述基质与卡巴拉汀和其余任选成分形成基质层。因此,在本发明的一个实施方案中,含有卡巴拉汀的层可以是含有卡巴拉汀的基质层,其中卡巴拉汀均匀地分布于聚合物基质中。如果通过将两个基本相同组成的含有卡巴拉汀的基质层层压在一起来制备含有卡巴拉汀的基质层,则将所得双层视为一个含有卡巴拉汀的基质层。
在根据本发明的贮库型TTS中,含有卡巴拉汀的层是含有卡巴拉汀的贮库层,其优选地包括包含卡巴拉汀的液体贮库。贮库型TTS通常还包括皮肤接触层,其中贮库层和皮肤接触层优选地由控速膜隔开。优选地,皮肤接触层被制造成不含卡巴拉汀。
优选地,含有卡巴拉汀的层结构为含有卡巴拉汀的自粘层结构。优选的是,含有卡巴拉汀的层,优选为含有卡巴拉汀的基质层,是自粘的。因此,在一个优选的实施方式中,含有卡巴拉汀的层结构为含有卡巴拉汀的自粘层结构。可替代地或另外地,优选的是,含有卡巴拉汀的层直接附着于背衬层,使得在背衬层与含有卡巴拉汀的层之间没有另外的层。因此,获得了低复杂度的层结构,这在例如制造成本方面是有利的。
特别地,优选的是,含有卡巴拉汀的层结构包括不超过三个层。皮肤接触层在施用过程中在含有卡巴拉汀的自粘层结构与患者的皮肤之间提供足够的粘合性。
应当理解,根据本发明的TTS含有治疗有效量的卡巴拉汀。因此,在本发明的一个优选的实施方案中,含有卡巴拉汀的层结构含有治疗有效量的卡巴拉汀。含有卡巴拉汀的层结构中的卡巴拉汀优选以游离碱形式存在。下文进一步提供了关于根据本发明的TTS中的卡巴拉汀的优选的实施方案。
根据本发明优选的是,TTS的释放面积相当小。根据本发明的一个具体实施方案,释放面积在1至30cm
在本发明的一个优选的实施方案中,背衬层基本上是卡巴拉汀不可渗透的。此外,优选的是,背衬层是闭塞的。
根据本发明的某些实施方案,TTS还可包括粘合剂覆层。特别地,粘合剂覆层的面积大于含有卡巴拉汀的结构并附着于其上,用于增强透皮治疗系统的总体粘合特性。所述粘合剂覆层包括背衬层和粘合剂层。粘合剂覆层提供了附着在皮肤上的附加区域,但没有增加卡巴拉汀的释放面积。粘合剂覆层包含选自由以下组成的组的自粘聚合物或自粘聚合物混合物:有机硅丙烯酸杂化聚合物、丙烯酸聚合物、聚硅氧烷、聚异丁烯、苯乙烯-异戊二烯-苯乙烯共聚物及其混合物,所述自粘聚合物或自粘聚合物混合物可与含有卡巴拉汀的层结构中所含的任意聚合物或聚合物混合物相同或不同。
根据本发明的含有卡巴拉汀的层结构,诸如含有卡巴拉汀的自粘层结构,通常位于可剥离保护层(离型衬垫)上,在施加至患者皮肤表面之前即刻从所述可剥离保护层上取下。因此,TTS还可包括离型衬垫。以此方式得到保护的TTS通常储存在泡罩包装或接缝密封袋中。包装可为儿童安全和/或成人友好型。
含有卡巴拉汀的层
如以上更为详细地概述,根据本发明的TTS包括含有卡巴拉汀的层结构,所述含有卡巴拉汀的层结构包括含有卡巴拉汀的层。优选地,含有卡巴拉汀的层结构是含有卡巴拉汀的自粘层结构。因此,还优选的是,含有卡巴拉汀的层是自粘的含有卡巴拉汀的层,更优选地是自粘的含有卡巴拉汀的基质层。在一个优选的实施方案中,含有卡巴拉汀的层包含治疗有效量的卡巴拉汀。
在本发明的一个实施方案中,含有卡巴拉汀的层是含有卡巴拉汀的基质层。在另一个实施方案中,含有卡巴拉汀的层是含有卡巴拉汀的贮库层。优选的是,含有卡巴拉汀的层是含有卡巴拉汀的基质层。
含有卡巴拉汀的层包含:
1.卡巴拉汀,优选为游离碱形式;和
2.至少一种丙烯酸聚合物。
在一个优选的实施方案中,含有卡巴拉汀的层是含有卡巴拉汀的基质层,其包含
1.卡巴拉汀,优选为游离碱形式;和
2.至少一种丙烯酸聚合物。
在一个优选的实施方案中,本发明涉及一种含有卡巴拉汀的层结构,其中所述至少一种丙烯酸聚合物是丙烯酸压敏粘合剂。
在本发明的一个实施方案中,含有卡巴拉汀的层可以通过将卡巴拉汀(优选为游离碱形式)溶解、分散或部分溶解和部分分散而获得。结果,根据本发明的TTS的含有卡巴拉汀的层通常包含游离碱形式的卡巴拉汀。另外,在本发明的某些实施方案中,卡巴拉汀可以部分地以质子化形式存在。然而,优选的是,在含有卡巴拉汀的层中至少50mol%、优选至少75mol%的卡巴拉汀以游离碱形式存在。在一个特别优选的实施方案中,在含有卡巴拉汀的层中至少90mol%、优选至少95mol%、更优选至少99mol%的卡巴拉汀以游离碱形式存在。
在本发明的一个实施方案中,在含有卡巴拉汀的层结构中所含的卡巴拉汀的量在0.5至5mg/cm
在本发明的一个实施方案中,含有卡巴拉汀的层包含基于含有卡巴拉汀的层的总重量的20至40重量%、优选25至35重量%的量、最优选30重量%的量的卡巴拉汀。
在一个实施方案中,含有卡巴拉汀的基质层组合物可包含第二聚合物,或者可包含两种或更多种其他聚合物。
应当理解,根据本发明的TTS除了至少一种丙烯酸聚合物之外还可以包含一种或多种聚合物。示例性地,可以使用基于聚硅氧烷、丙烯酸酯、聚异丁烯或苯乙烯-异戊二烯-苯乙烯嵌段共聚物的聚合物。在本发明的一个实施方案中,另外的聚合物为基于聚硅氧烷、丙烯酸酯或聚异丁烯的压敏粘合剂。还可添加另外的聚合物,以增强内聚力和/或粘合性。在又一优选的实施方案中,本发明涉及一种透皮治疗系统,其中所述含有卡巴拉汀的层不包含渗透促进剂或增溶剂。
在本发明的某些实施方案中,丙烯酸聚合物以基于含有卡巴拉汀的层的总重量的5至40重量%、优选8至35重量%的量包含在含有卡巴拉汀的层中。
在本发明的一个优选实施方案中,含有卡巴拉汀的层中的丙烯酸聚合物不包含OH-基团作为官能团。取而代之的是,优选在含有卡巴拉汀的层中的丙烯酸聚合物是COOH-官能化的丙烯酸聚合物,优选可由一种或多种选自丙烯酸、丙烯酸2-乙基己酯、甲基丙烯酸缩水甘油酯和丙烯酸甲酯的单体获得的COOH-官能化的丙烯酸聚合物。特别优选地,含有卡巴拉汀的层中的丙烯酸聚合物是基于丙烯酸酯的压敏粘合剂Duro-Tak
在本发明的一个实施方案中,含有卡巴拉汀的层的面积重量在40至250g/m
皮肤接触层
如以上更为详细地概述,根据本发明的TTS的含有剂的层结构包括背衬层、含有卡巴拉汀的层和皮肤接触层。皮肤接触层优选与含有卡巴拉汀的层接触。
皮肤接触层包含至少一种苯乙烯-异戊二烯-苯乙烯嵌段共聚物。特别地,至少一种苯乙烯-异戊二烯-苯乙烯嵌段共聚物是基于苯乙烯-异戊二烯-苯乙烯嵌段共聚物的压敏粘合剂。下文进一步提供关于根据本发明的聚合物的更多细节。
在某些优选的实施方案中,至少一种苯乙烯-异戊二烯-苯乙烯嵌段共聚物以基于皮肤接触层的总重量的约20重量%至约90重量%、优选约30重量%至约80重量%、或约40重量%至约60重量%的量包含在皮肤接触层中。
皮肤接触层包含至少一种增粘剂。在一个优选的实施方案中,至少一种增粘剂是脂环族饱和烃树脂、或氢化松香甘油酯、或石蜡液体、或其混合物。下文进一步提供关于根据本发明的增粘剂的更多细节。
在某些优选的实施方案中,至少一种增粘剂以约20%至约80%、优选约35%至约65%的量包含在皮肤接触层中。
在一个优选的实施方案中,至少一种苯乙烯-异戊二烯-苯乙烯嵌段共聚物和至少一种增粘剂以基于皮肤接触层的总重量的约60∶40(w/w)至约40∶60(w/w)的比率、优选约50∶50(w/w)的比率包含在皮肤接触层中。
在一个优选的实施方案中,至少一种苯乙烯-异戊二烯-苯乙烯嵌段共聚物和至少一种增粘剂以约60∶40(w/w)至约40∶60(w/w)的比率包含在皮肤接触层中。
在另一个优选的实施方案中,至少一种苯乙烯-异戊二烯-苯乙烯嵌段共聚物和至少一种增粘剂以基于皮肤接触层的总重量的至少90重量%的总量、优选至少99重量%的总量存在于皮肤接触层中。优选地,皮肤接触层不包含丙烯酸聚合物。
皮肤接触层可包含活性剂。在一个优选实施方案中,皮肤接触层不含活性剂,也就是说在不添加活性剂的情况下制备而成。
皮肤接触层的面积重量可为5至120g/m
卡巴拉汀
根据本发明的TTS包括含有卡巴拉汀的层结构,所含有卡巴拉汀的层结构包括A)背衬层;B)含有卡巴拉汀的层,其包含至少一种丙烯酸聚合物;和C)皮肤接触层,其包含至少一种苯乙烯-异戊二烯-苯乙烯嵌段共聚物和至少一种增粘剂。
在本发明的一个实施方案中,在含有卡巴拉汀的层结构中所含的卡巴拉汀的量在0.5至5mg/cm
在本发明的一个实施方案中,含有卡巴拉汀的层结构优选地含有治疗有效量的卡巴拉汀。更优选地,在含有卡巴拉汀的层结构的含有卡巴拉汀的层中存在治疗有效量的卡巴拉汀。优选地,含有卡巴拉汀的层结构中的卡巴拉汀以游离碱形式存在。
在本发明的一个实施方案中,TTS中卡巴拉汀的总量的至少50mol%、优选至少75mol%以游离碱形式存在。在一个特别优选的实施方案中,TTS中卡巴拉汀的总量的至少90mol%、优选至少95mol%、更优选至少99mol%以游离碱形式存在。因此,优选的是,在含有卡巴拉汀的层中至少50mol%、优选至少75mol%的卡巴拉汀以游离碱形式存在。在一个特别优选的实施方案中,在含有卡巴拉汀的层中至少90mol%、优选至少95mol%、更优选至少99mol%的卡巴拉汀以游离碱形式存在。在某些实施方案中,含有卡巴拉汀的层不含卡巴拉汀盐。
在某些实施方案中,在含有卡巴拉汀的层中卡巴拉汀的量在基于含有卡巴拉汀的层的总重量的20至40重量%、优选25至35重量%的范围内,最优选地,在含有卡巴拉汀的层中卡巴拉汀以基于含有卡巴拉汀的层的总重量的30重量%的量存在。
在某些实施方案中,在含有卡巴拉汀的层中所含的卡巴拉汀的量在1至72mg、优选2至36mg的范围内,取决于贴剂尺寸。在尺寸为例如5cm
在本发明的一个实施方案中,含有卡巴拉汀的层可通过将游离碱形式的卡巴拉汀溶解或分散而获得。如果含有卡巴拉汀的层是含有卡巴拉汀的基质层,则所述层优选地可通过将游离碱形式的卡巴拉汀溶解或分散于聚合物载体中而获得,所述聚合物载体特别优选地包含至少一种丙烯酸聚合物。
在一个实施方案中,含有卡巴拉汀的层包含卡巴拉汀的药学上可接受的盐,诸如盐酸卡巴拉汀或酒石酸卡巴拉汀。然而,优选的是根据本发明,含有卡巴拉汀的层中的卡巴拉汀以游离碱形式存在。
在某些实施方案中,如根据Hyoscine Monography中的Ph.Eur.2.2.20测定通过定量滴定所确定的,卡巴拉汀的纯度为至少95%,优选为至少98%,并且更优选为至少99%。
丙烯酸聚合物
根据本发明,TTS在含有卡巴拉汀的层中包含至少一种丙烯酸聚合物。
在某些实施方案中,丙烯酸聚合物是丙烯酸压敏粘合剂。
丙烯酸压敏粘合剂通常在如正庚烷和乙酸乙酯的溶剂中供应和使用。压敏粘合剂的固体含量通常在20%与80%之间。
丙烯酸压敏粘合剂也可称为丙烯酸酯类压敏粘合剂或基于丙烯酸酯的压敏粘合剂。基于丙烯酸酯的压敏粘合剂的固体含量可优选地在20%与60%之间。此类基于丙烯酸酯的压敏粘合剂可包括或可不包括诸羟基、羧基、中和的羧基及其混合物的官能团。因此,术语“官能团”特别是指羟基和羧基以及去质子化的羧基。
相应的商业产品可以商品名Duro
可购得如下指定的基于丙烯酸酯的压敏粘合剂:
-Duro-Tak
-Duro-Tak
-Duro-Tak
-Duro-Tak
-Duro-Tak
在本发明的一个优选实施方案中,含有卡巴拉汀的层中的丙烯酸聚合物是基于丙烯酸酯的压敏粘合剂Duro-Tak
还可添加另外的聚合物,以增强内聚力和/或粘合性。
苯乙烯-异戊二烯-苯乙烯嵌段共聚物
根据本发明,TTS在皮肤接触层中包含至少一种苯乙烯-异戊二烯-苯乙烯嵌段共聚物。特别地,至少一种苯乙烯-异戊二烯-苯乙烯嵌段共聚物是基于苯乙烯-异戊二烯-苯乙烯嵌段共聚物的压敏粘合剂。
根据本发明的合适的苯乙烯-异戊二烯-苯乙烯共聚物是可例如以商标名JSR-SIS商购获得的。
在本发明的某些实施方案中,至少一种苯乙烯-异戊二烯-苯乙烯嵌段共聚物包含比率为约10∶90(w/w)至约30∶70(w/w)、优选比率为约15∶85(w/w)或约22∶78(w/w)的苯乙烯嵌段和异戊二烯嵌段。
在本发明的某些实施方案中,至少一种苯乙烯-异戊二烯-苯乙烯嵌段共聚物可通过使聚苯乙烯、聚异戊二烯和聚苯乙烯的三个嵌段聚合而获得,并且其平均分子量为约100,000至200,000。
具体的基于苯乙烯-异戊二烯-苯乙烯嵌段共聚物的压敏粘合剂可以商品名JSR-SIS5229和JSR-SIS5002获得。
还可添加另外的聚合物,以增强内聚力和/或粘合性。
增粘剂
根据本发明,TTS在皮肤接触层中包含至少一种增粘剂。在本发明的某些实施方案中,至少一种增粘剂是脂环族饱和烃树脂、氢化松香甘油酯、石蜡液体或其混合物。例如,至少一种增粘剂可以是包含脂环族饱和烃树脂和石蜡液体的混合物,或者是包含氢化松香甘油酯和石蜡液体的混合物。
脂环族饱和烃树脂在日本药典的专题中有详细描述。在本发明的某些实施方案中,脂环族饱和烃树脂可通过不饱和烃的聚合而获得,所述不饱和烃可通过在高温下分解石油石脑油而制备获得。
具体的脂环族饱和烃树脂可以商品名Arkon P-100从Arakawa Europe获得,并且其化学结构如下所述。
氢化松香甘油酯在日本药典的专题中有详细描述。在本发明的某些实施方案中,氢化松香甘油酯是可通过将松香氢化,然后用甘油酯化而获得的固体树脂。
具体的氢化松香甘油酯可以商品名Pinecrystal KE-100从Arakawa Europe获得,并且其化学结构如下所述。
石蜡液体是如欧洲药典(Ph.Eur.)中所定义的液体饱和烃的精制混合物。
根据本发明的某些实施方案,至少一种增粘剂以约20%至约80%、优选约35%至约65%的量包含在皮肤接触层中。
其他添加剂
根据本发明的TTS,并且特别是含有卡巴拉汀的层还可包含至少一种添加剂或赋形剂。所述添加剂或赋形剂优选地选自由以下组成的组:结晶抑制剂、增溶剂、填充剂、护肤物质、pH调节剂、防腐剂、增粘剂、软化剂、稳定剂和渗透促进剂,特别是选自结晶抑制剂、护肤物质、增粘剂、软化剂、稳定剂和渗透促进剂。更优选地,所述添加剂选自由以下组成的组:结晶抑制剂、增溶剂、填充剂、护肤物质、pH调节剂、防腐剂、增粘剂、软化剂、稳定剂和渗透促进剂,特别是选自结晶抑制剂、护肤物质、增粘剂、软化剂和稳定剂。此类添加剂可以基于含有卡巴拉汀的层的总重量的0.001至15重量%,例如1至10重量%或0.01至5重量%的量存在于含有卡巴拉汀的层中。
在某些优选的实施方案中,含有卡巴拉汀的层不包含其他添加剂,特别是含有卡巴拉汀的层不包含渗透促进剂或增溶剂。
应当注意的是,在药物制剂中,制剂组分是根据它们的理化和生理特性并且根据它们的功能来分类的。特别地,这意味着不排除属于一种类别的物质或化合物属于制剂组分的另一种类别。例如,某种聚合物可以是结晶抑制剂,也可以是增粘剂。一些物质可以是例如典型的软化剂,但同时充当渗透促进剂。技术人员能够基于其常识来确定某种物质或化合物属于制剂组分的哪种类别。在下文中,提供了关于赋形剂和添加剂的细节,然而,这些细节不应理解为排他性的。在本说明书中未明确列出的其他物质也可以根据本发明使用,并且对于制剂组分的一种类别明确列出的物质和/或化合物不排除在本发明的意义上用作另一种制剂组分。
在一个实施方案中,含有卡巴拉汀的层还包含结晶抑制剂。在一些实施方案中,结晶抑制剂可以基于含有卡巴拉汀的层的总重量的0.5至10重量%的量存在。结晶抑制剂的合适实例包括聚乙烯吡咯烷酮、乙酸乙烯酯/乙烯吡咯烷酮共聚物和纤维素衍生物。结晶抑制剂优选为聚乙烯吡咯烷酮,更优选为可溶性聚乙烯吡咯烷酮。结晶抑制剂可增加活性剂的溶解度或抑制活性剂的结晶。
在一个实施方案中,含有卡巴拉汀的层还包含稳定剂,其中所述稳定剂优选地选自生育酚及其酯衍生物和抗坏血酸及其酯衍生物。在一些实施方案中,稳定剂可以基于含有卡巴拉汀的层的总重量的0.001至2.0重量%、优选0.01至1.0重量%的量存在。在一些实施方案中,优选的稳定剂包括偏亚硫酸氢钠、脂肪酸的抗坏血酸酯诸如棕榈酸抗坏血酸酯、抗坏血酸、丁基化羟基甲苯、生育酚、乙酸生育酚酯和亚油酸生育酚酯。优选的稳定剂包括脂肪酸的抗坏血酸酯、抗坏血酸、生育酚、乙酸生育酚乙酸酯和亚油酸生育酚酯。特别优选的是生育酚。还特别优选的是生育酚和棕榈酸抗坏血酸酯的组合。
在一个实施方案中,含有卡巴拉汀的层还包含软化剂/增塑剂。示例性软化剂/增塑剂包括具有6至20个碳原子的直链或支链的饱和或不饱和的醇,甘油三酸酯和聚乙二醇。
在一个实施方案中,含有卡巴拉汀的层还包含增溶剂。增溶剂优选提高卡巴拉汀在含有卡巴拉汀的层中的溶解度。优选的增溶剂包括例如中链和/或长链脂肪酸的甘油酯、聚甘油酯、丙二醇酯和聚氧乙烯酯,诸如单亚油酸甘油酯,中链甘油酯和中链甘油三酸酯,通过蓖麻油与环氧乙烷反应制成的非离子型增溶剂,以及其还可含有脂肪酸或脂肪醇的任意混合物;纤维素和甲基纤维素及其衍生物,诸如羟丙基纤维素和乙酸羟丙甲纤维素琥珀酸酯;各种环糊精及其衍生物;非离子型三嵌段共聚物,其具有中心聚氧丙烯的疏水链,侧接两个聚氧乙烯的亲水链,称为泊洛沙姆;维生素E的水溶性衍生物;药物分级或团聚球形异麦芽酮糖醇;基于聚乙二醇、聚乙酸乙烯酯和聚乙烯己内酰胺的接枝共聚物,也缩写为PVAc-PVCap-PEG,并称为
然而,下文提到的渗透促进剂也可以充当增溶剂。
在一个实施方案中,含有卡巴拉汀的层还包含pH调节剂。合适的pH调节剂包括弱酸和碱,包括胺衍生物、无机碱衍生物和具有碱性或酸性官能团的聚合物。
在一个实施方案中,含有卡巴拉汀的层还包含防腐剂。合适的防腐剂包括对羟基苯甲酸酯、甲醛释放剂、异噻唑啉酮、苯氧乙醇和有机酸诸如苯甲酸、山梨酸、乙酰丙酸和茴香酸。
在一个实施方案中,含有卡巴拉汀的层还包含护肤物质。此类物质可用于避免或减少皮肤刺激,如通过皮肤反应评分所检测到的。合适的护肤物质包括固醇化合物,诸如胆固醇、右泛醇、α-甜没药醇和抗组胺药。护肤物质优选地以基于含有卡巴拉汀的层的总重量的1至10重量%的量使用。
在本发明的含义内,术语“可溶性聚乙烯吡咯烷酮”是指超过10%至少可溶于乙醇,优选地也可溶于水、二甘醇、甲醇、正丙醇、2-丙醇、正丁醇、氯仿、二氯甲烷、2-吡咯烷酮、聚乙二醇400、1,2丙二醇、1,4丁二醇、甘油、三乙醇胺、丙酸和乙酸的聚乙烯吡咯烷酮,也称为聚维酮。可商购获得的聚乙烯吡咯烷酮的实例包括由BASF供应的
在本发明的含义内,术语“K值”是指根据欧洲药典(Ph.Eur.)和美国药典(USP)中的“聚维酮”专题由聚乙烯吡咯烷酮在水中的相对粘度计算得到的值。
可以将诸如硅胶、二氧化钛和氧化锌的填充剂与聚合物结合使用,以便以所需的方式影响某些物理参数,诸如内聚力和粘结强度。
在一个实施方案中,含有卡巴拉汀的层还包含渗透促进剂。渗透促进剂是在增加活性剂渗透性的意义上影响角质层屏障特性的物质。渗透促进剂的一些实例是多元醇,诸如二丙二醇、丙二醇和聚乙二醇;油,诸如橄榄油、角鲨烯和羊毛脂;脂肪醚,诸如鲸蜡基醚和油基醚;脂肪酸酯,诸如肉豆蔻酸异丙酯;尿素和尿素衍生物,诸如尿囊素;极性溶剂,诸如二甲基癸基氧化磷、甲基鲸蜡基亚砜、二甲基月桂胺(dimethylaurylamine)、十二烷基吡咯烷酮、异山梨醇、二甲基丙酮、二甲基亚砜、癸基甲基亚砜和二甲基甲酰胺;水杨酸;氨基酸;烟酸苄酯;以及较高分子量的脂族表面活性剂,诸如月桂基硫酸盐。其他剂包括油酸和亚油酸、抗坏血酸、泛醇、丁基化羟基甲苯、生育酚、乙酸生育酚酯、亚油酸生育酚酯、油酸丙酯和棕榈酸异丙酯。
如果含有卡巴拉汀的层还包含渗透促进剂,则所述渗透促进剂优选地选自二甘醇单乙醚(transcutol)、己二酸二异丙酯、肉豆蔻酸异丙酯、棕榈酸异丙酯、乳酸月桂酯和二甲基丙烯脲。
已经发现,即使不存在渗透促进剂,TTS也能提供足够的活性剂的渗透性。因此,在本发明的某些实施方案中,含有卡巴拉汀的层不包含渗透促进剂或增溶剂。
释放特征
根据本发明的TTS被设计用于向体循环透皮施用卡巴拉汀持续预定的延长时间段,优选24小时。
在一个实施方案中,根据本发明的TTS通过透皮递送在约24小时的施用中提供150至3500μg/cm
在一个实施方案中,根据本发明的TTS在向患者皮肤施用TTS约24小时期间以大约恒定的速率透皮递送2至20mg的卡巴拉汀。
在一个实施方案中,如在使用EVA膜的Franz扩散池中所测量的,根据本发明的透皮治疗系统在24小时的时间段内提供约300μg/cm
在一个实施方案中,如在使用EVA膜(9%乙酸乙烯酯Cotran 9702 von 3M)的Franz扩散池中所测量的,根据本发明的透皮治疗系统提供如下的卡巴拉汀渗透量:
前3小时为0μg/cm
从第3小时至第8小时为80μg/cm
从第8小时至第24小时为210μg/cm
治疗方法/医疗用途
根据本发明的一个具体方面,根据本发明的TTS用于治疗人类患者的方法,优选用于预防、治疗阿尔茨海默病、帕金森氏病相关的痴呆症和/或创伤性脑损伤症状或延缓阿尔茨海默病、帕金森氏病相关的痴呆症和/或创伤性脑损伤症状进展的方法。根据本发明的另一个具体方面,TTS用于治疗人类患者的方法,优选用于治疗由阿尔茨海默病或帕金森氏病引起的轻度至中度痴呆症的方法。
在一个实施方案中,根据本发明的TTS用于治疗人类患者的方法,优选用于治疗人类患者的方法,优选用于预防、治疗阿尔茨海默病、帕金森氏病相关的痴呆症和/或创伤性脑损伤症状或延缓阿尔茨海默病、帕金森氏病相关的痴呆症和/或创伤性脑损伤症状进展的方法,或用于治疗人类患者的方法,优选用于治疗由阿尔茨海默病或帕金森氏病引起的轻度至中度痴呆症的方法,其中将所述透皮治疗系统以至少24小时、优选约24小时的给药间隔施加至患者皮肤。
在一个实施方案中,根据本发明的TTS用于治疗人类患者的方法,优选用于治疗人类患者的方法,优选用于预防、治疗阿尔茨海默病、帕金森氏病相关的痴呆症和/或创伤性脑损伤症状或延缓阿尔茨海默病、帕金森氏病相关的痴呆症和/或创伤性脑损伤症状进展的方法,或用于治疗人类患者的方法,优选用于治疗由阿尔茨海默病或帕金森氏病引起的轻度至中度痴呆症的方法,其中将所述透皮治疗系统以至少72小时、优选约84小时的给药间隔施加至患者皮肤。
在某些实施方案中,本发明涉及通过向患者皮肤施加如本发明所定义的透皮治疗系统来治疗人类患者的方法,特别是预防、治疗阿尔茨海默病、帕金森氏病相关的痴呆症和/或创伤性脑损伤症状或延缓阿尔茨海默病、帕金森氏病相关的痴呆症和/或创伤性脑损伤症状进展。在另外的某些实施方案中,本发明涉及通过向患者皮肤施加如本发明所定义的透皮治疗系统来治疗人类患者的方法,特别是治疗由阿尔茨海默病和帕金森氏病引起的轻度至中度痴呆症。
在一个实施方案中,本发明涉及一种治疗人类患者的方法,特别是预防、治疗阿尔茨海默病、帕金森氏病相关的痴呆症和/或创伤性脑损伤症状或延缓阿尔茨海默病、帕金森氏病相关的痴呆症和/或创伤性脑损伤症状进展,或者涉及一种治疗人类患者的方法,特别是治疗由阿尔茨海默病和帕金森氏病引起的轻度至中度痴呆症,其中将所述透皮治疗系统以至少24小时、优选约24小时的给药间隔施加至患者皮肤。
在一个实施方案中,本发明涉及一种治疗人类患者的方法,特别是预防、治疗阿尔茨海默病、帕金森氏病相关的痴呆症和/或创伤性脑损伤症状或延缓阿尔茨海默病、帕金森氏病相关的痴呆症和/或创伤性脑损伤症状进展,或者涉及一种治疗人类患者的方法,特别是治疗由阿尔茨海默病和帕金森氏病引起的轻度至中度痴呆症,其中将所述透皮治疗系统以至少72小时、优选约84小时的给药间隔施加至患者皮肤。
结合以上用途和治疗方法,根据本发明的TTS优选地以限定的给药间隔施加至受试者的至少一个身体表面,其选自上外臂(upper outer art)、上胸部、上背部或胸部侧面。
根据本发明的TTS的优选施加时间为至少24小时,优选约24小时(1天)或约84小时(3.5天),特别优选约24小时。在此时间之后,可以去除TTS,并可以另选地施加新的TTS,以便进行全天候治疗。
制造方法
本发明还涉及一种用于透皮治疗系统的含有卡巴拉汀的层(优选为含有卡巴拉汀的基质层)的制造方法。
根据本发明,所述制造根据本发明的透皮治疗系统的方法包括以下步骤:
1)通过组合至少以下组分来提供含有卡巴拉汀的涂覆组合物
i)卡巴拉汀;和
ii)至少一种丙烯酸聚合物;
2)将含有卡巴拉汀的涂覆组合物以提供所需面积重量的量涂覆于膜上,
3)干燥涂覆的含有卡巴拉汀的涂覆组合物以提供含有卡巴拉汀的层,
4)通过组合至少以下组分为附加皮肤接触层提供另外的涂覆组合物
a)至少一种苯乙烯-异戊二烯-苯乙烯嵌段共聚物;和
b)至少一种增粘剂;
5)根据步骤2和3涂覆并干燥另外的涂覆组合物,其中所述膜是离型衬垫,
6)将皮肤接触层的粘合剂侧层压到含有卡巴拉汀的层的粘合剂侧上,以提供具有所需释放面积的含有卡巴拉汀的层结构,
7)从含有卡巴拉汀的层结构中冲压出单独系统,
8)任选地将不含卡巴拉汀的自粘层结构粘附至单独系统,所述不含卡巴拉汀的自粘层结构还包括背衬层和不含卡巴拉汀的压敏粘合剂层,并且所述不含卡巴拉汀的自粘层结构比含有卡巴拉汀的自粘层结构的单独系统大。
在上述制造方法的步骤1)中,优选地将卡巴拉汀分散以获得均匀的涂覆组合物。
在本发明的某些实施方案中,丙烯酸聚合物以溶液形式提供,其中溶剂为乙酸乙酯或正庚烷。优选地,使用乙酸乙酯。优选地,丙烯酸聚合物的固体含量为20至70重量%。
在上述制造方法的步骤3)中,干燥优选地在20℃至90℃、更优选40℃至70℃的温度下进行。
在本发明的某些实施方案中,步骤2)中的膜是离型衬垫,在步骤3)之后将含有卡巴拉汀的层层压到背衬层,并且在步骤6)之前去除步骤2)的离型衬垫。
实施例
现参考所附实施例对本发明进行更全面的说明。然而,应当理解,以下说明仅为说明性的,而不应以任何方式视为对本发明的限制。实施例中提供的关于组合物中成分的量或面积重量的数值可能会由于制造可变性而略有变化。
比较例1
比较例1(Comp.1)等同于可商购获得的含有卡巴拉汀的TTS产品
分别根据实施例6和7,测定可商购获得的
结果在表6至7.18和图1至4中示出。
实施例1
涂覆组合物
实施例1的含有卡巴拉汀的涂覆组合物的配方总结在表1.1中。%值是指重量%的量。
表1.1
涂覆组合物的制备
在烧杯中装入丙烯酸压敏粘合剂Durotak 387-2353。在搅拌下加入卡巴拉汀碱。将混合物以约800rpm搅拌直至获得均匀的混合物(至少20分钟)。
涂覆组合物的涂覆
在含有卡巴拉汀的混合物制成不到24小时内,使用erichson涂覆器,使用移交刀实验室涂覆设备,将所得的含有卡巴拉汀的涂覆组合物涂覆于可粘箔(Scotchpak 9755AB1F)上。通过第一步在约室温(23±2℃)下干燥约10分钟,随后第二步在约60℃下干燥约20分钟,将溶剂除去。
选择涂层厚度,使得除去溶剂产生约60.0g/m
皮肤接触层
实施例1的皮肤接触层的配方总结在表1.2中。%值是指重量%的量。
表1.2
皮肤接触层的制备
在烧杯中装入苯乙烯异戊二烯嵌段共聚物和脂环族饱和烃树脂。将混合物以约800rpm搅拌直至获得均匀的混合物(至少20分钟)。
在混合物制成不到24小时内,使用erichson涂覆器,使用移交刀实验室涂覆设备,将所得组合物涂覆于可粘箔(Scotchpak 9755 AB1F)上。通过第一步在约室温(23±2℃)下干燥约10分钟,随后第二步在约60℃下干燥约20分钟,将溶剂除去。
选择涂层厚度,使得除去溶剂产生约30.0g/m
TTS的制备
然后从含有卡巴拉汀的自粘层结构中冲压出单独系统(TTS),并密封到主要包装材料的袋中。
实施例2
含有卡巴拉汀的层
实施例2的含有卡巴拉汀的层的配方对应于表1.1中总结的实施例1的含有卡巴拉汀的层。
皮肤接触层
实施例2的皮肤接触层的配方总结在表2中。%值是指重量%的量。
表2
皮肤接触层的制备
在烧杯中装入苯乙烯异戊二烯嵌段共聚物、脂环族饱和烃树脂和石蜡液体。将混合物以约800rpm搅拌直至获得均匀的混合物(至少20分钟)。
在混合物制成不到24小时内,使用erichson涂覆器,使用移交刀实验室涂覆设备,将所得组合物涂覆于可粘箔(Scotchpak 9755 AB1F)上。通过第一步在约室温(23±2℃)下干燥约10分钟,随后第二步在约60℃下干燥约20分钟,将溶剂除去。
选择涂层厚度,使得除去溶液产生约30.0g/m
TTS的制备
然后从含有卡巴拉汀的自粘层结构中冲压出单独系统(TTS),并密封到主要包装材料的袋中。
实施例3
含有卡巴拉汀的层
实施例3的含有卡巴拉汀的层的配方对应于表1.1中总结的实施例1的含有卡巴拉汀的层。
皮肤接触层
实施例3的皮肤接触层的配方总结在表3中。%值是指重量%的量。
表3
皮肤接触层的制备
在烧杯中装入苯乙烯异戊二烯嵌段共聚物、氢化松香甘油酯和α-生育酚。将混合物以约800rpm搅拌直至获得均匀的混合物(至少20分钟)。
在混合物制成不到24小时内,使用erichson涂覆器,使用移交刀实验室涂覆设备,将所得组合物涂覆于可粘箔(Scotchpak 9755 AB1F)上。通过第一步在约室温(23±2℃)下干燥约10分钟,随后第二步在约60℃下干燥约20分钟,将溶剂除去。
选择涂层厚度,使得除去溶液产生约30.0g/m
TTS的制备
然后从含有卡巴拉汀的自粘层结构中冲压出单独系统(TTS),并密封到主要包装材料的袋中。
实施例4
含有卡巴拉汀的层
实施例4的含有卡巴拉汀的层的配方对应于表1.1中总结的实施例1的含有卡巴拉汀的层。
皮肤接触层
实施例4的皮肤接触层的配方总结在表4中。%值是指重量%的量。
表4
皮肤接触层的制备
在烧杯中装入苯乙烯异戊二烯嵌段共聚物、脂环族饱和烃树脂、氢化松香甘油酯和α-生育酚。将混合物以约800rpm搅拌直至获得均匀的混合物(至少20分钟)。
在混合物制成不到24小时内,使用erichson涂覆器,使用移交刀实验室涂覆设备,将所得组合物涂覆于可粘箔(Scotchpak 9755 AB1F)上。通过第一步在约室温(23±2℃)下干燥约10分钟,随后第二步在约60℃下干燥约20分钟,将溶剂除去。
选择涂层厚度,使得除去溶液产生约30.0g/m
TTS的制备
然后从含有卡巴拉汀的自粘层结构中冲压出单独系统(TTS),并密封到主要包装材料的袋中。
实施例5
含有卡巴拉汀的层
实施例5的含有卡巴拉汀的层的配方对应于表1.1中总结的实施例1的含有卡巴拉汀的层。
皮肤接触层
实施例5的皮肤接触层的配方总结在表5中。%值是指重量%的量。
表5
皮肤接触层的制备
在烧杯中装入苯乙烯异戊二烯嵌段共聚物、氢化松香甘油酯、石蜡液体和α-生育酚。将混合物以约800rpm搅拌直至获得均匀的混合物(至少20分钟)。
在混合物制成不到24小时内,使用erichson涂覆器,使用移交刀实验室涂覆设备,将所得组合物涂覆于可粘箔(Scotchpak 9755 AB1F)上。通过第一步在约室温(23±2℃)下干燥约10分钟,随后第二步在约60℃下干燥约20分钟,将溶剂除去。
选择涂层厚度,使得除去溶液产生约30.0g/m
TTS的制备
然后从含有卡巴拉汀的自粘层结构中冲压出单独系统(TTS),并密封到主要包装材料的袋中。
实施例6
渗透量的测量
根据比较例1以及实施例1和3至5制备的TTS的渗透量是通过根据关于透皮贴剂质量的EMA指南(2014年10月23日采用)的实验使用10.0ml Franz扩散池确定的,其中使用厚度为50μm的EVA膜(9%乙酸乙烯酯;Scotchpak Cotran 9702,来自3M)。从TTS中冲压出释放面积为1.156cm
结果在表6和图1中示出。
表6
实施例7
稳定性
关于不同参数,即粘合力、剥离力、卡巴拉汀含量和体外释放,确定根据对比率1和实施例1至5制备的TTS的稳定性。
在制备TTS(初始)后进行相应的测量。
随后,将TTS储存在不同的储存条件下,并且在3个月和12个月后重复相应的测量。
储存条件为25℃和60%相对湿度(25℃/60%RH),或30℃和75%相对湿度(30℃/75%RH),或40℃和75%相对湿度(40℃/75%RH)。
在3个月(25℃/60%RH和40℃/75%RH)之后和12个月(25℃/60%RH,30℃/75%RH和40℃/75%RH)之后重复测量。对于实施例1和3,在12个月后不进行测量。
实施例7A
粘合力和剥离力的测量
测定根据比较例1和实施例1至5制备的TTS的粘合力和剥离力。
使用拉伸强度测试机对TTS进行粘合力测试。在测试前将样品在受控条件下于大约室温(23±2℃)和大约50%rh(相对湿度)下平衡24小时。将可粘箔的前几毫米拉下,并向敞开的粘合剂侧施加粘接带。然后,完全除去可粘箔,并将TTS以其粘合剂表面沿纵向方向放置在清洁的测试板(铝或不锈钢)的中心上。将测试板固定至拉伸强度机的下部夹具。将机器调整为零,将粘接带夹入机器的上部夹具中。拉力角设置为90°。在测量三个样品的粘合力之后,计算粘合力的平均值。测量值基于单位“N/TTS”[N/TTS]。
使用拉伸强度测试机对TTS进行剥离力测试。在测试前将样品在受控条件下于大约室温(23±2℃)和大约50%rh(相对湿度)下平衡24小时。此外,将样品切成具有25mm固定宽度和合适长度的片。将可粘箔的前几毫米拉下,并向敞开的粘合剂侧施加粘接带。然后,完全除去可粘箔,并将样品以其粘合剂表面沿纵向方向放置在清洁的测试板(铝或不锈钢)的中心上。将测试板固定至拉伸强度机的下部夹具。将机器调整为零,将粘接带夹入机器的上部夹具中。拉力角设置为90°,并且剥离速度为150mm/分钟。在测量三个样品的剥离力之后,计算剥离力的平均值。测量值基于单位“cN/TTS”[cN/TTS]。
如上所述,将TTS储存在不同的储存条件下,并在3个月和12个月后重复测量。
结果在表7.1至7.6中示出。比较例1和实施例1至5的生产后的初始粘合力和初始剥离力分别在图2和3中示出。
表7.1
表7.2
表7.3
表7.4
表7.5
表7.6
实施例7B
卡巴拉汀含量的测量
根据比较例1和实施例1至5制备的TTS的卡巴拉汀含量是通过使用经验证的HPLC方法确定的(色谱柱:150mm x 4.6mm内径不锈钢柱,5μm粒径,C8相,例如YMC碱性色谱柱(Fa.YMC);柱温:30℃;流动相:乙腈/0.1M KH
结果在表7.7至7.12中示出。
表7.7
表7.8
表7.9
表7.10
表7.11
表7.12
实施例7C
卡巴拉汀的体外释放速率的测量
根据比较例1和实施例1至5制备的TTS中的卡巴拉汀的体外释放速率通过使用PhEur/USP的旋转圆筒装置的实验来测定。使用双面胶带将TTS的背面固定到圆筒元件。在去除离型衬垫后,使圆筒下降到溶出介质(500ml,脱气,0.9%氯化钠溶液,32℃下)中,并以50rpm旋转。在0.5、2、4、7和24小时,取出4ml样品,并使用经验证的HPLC方法进行分析(色谱柱:不锈钢色谱柱,150mm x3.9mm I.D.,填充有C18相(例如Novapak C18,4μm粒径,Waters)或等效色谱柱,色谱柱温度:20-25℃;流动相∶乙腈/水20∶80(v/v)+0.35mL TEA/100mL,pH3.5;必要时用磷酸(85%)调节pH;流速:1.0ml/分钟;压力:约100bar;进样量:20μL;检测:UV,210nm,停止时间:6分钟)。
结果在表7.13至7.18中示出。比较例1和实施例1至5在24小时内的初始(生产后)卡巴拉汀的体外释放速率在图4中示出。
表7.13
表7.14
表7.15
表7.16
表7.17
表7.18
本发明特别涉及以下其他项目:
1.一种用于透皮施用卡巴拉汀的透皮治疗系统,所述系统包括含有卡巴拉汀的层结构,所述含有卡巴拉汀的层结构包括:
A)背衬层;
B)含有卡巴拉汀的层,其包含至少一种丙烯酸聚合物;和
C)皮肤接触层,其包含至少一种苯乙烯-异戊二烯-苯乙烯嵌段共聚物和至少一种增粘剂。
2.根据项目1所述的透皮治疗系统,
其中所述含有卡巴拉汀的层是含有卡巴拉汀的基质层,其包含:
i)卡巴拉汀;和
ii)丙烯酸聚合物。
3.根据项目1或2所述的透皮治疗系统,
其中所述含有卡巴拉汀的层结构含有治疗有效量的卡巴拉汀。
4.根据项目1至3中任一项所述的透皮治疗系统,
其中所述含有卡巴拉汀的层结构中的所述卡巴拉汀以游离碱形式存在。
5.根据项目1至4中任一项所述的透皮治疗系统,
其中在所述含有卡巴拉汀的层结构中所含的卡巴拉汀的量在0.5至5mg/cm
6.根据项目1至5中任一项所述的透皮治疗系统,
其中所述含有卡巴拉汀的层包含基于所述含有卡巴拉汀的层的总重量的20至40重量%、优选25至35重量%的量、最优选30重量%的量的卡巴拉汀。
7.根据项目1至6中任一项所述的透皮治疗系统,
其中所述丙烯酸聚合物是丙烯酸压敏粘合剂。
8.根据项目1至7中任一项所述的透皮治疗系统,
其中所述丙烯酸聚合物的量在基于所述含有卡巴拉汀的层的总重量的5至40重量%、优选8至35重量%的范围内。
9.根据项目1至8中任一项所述的透皮治疗系统,
其中所述丙烯酸聚合物可从选自以下的一种或多种单体获得:丙烯酸、丙烯酸丁酯、丙烯酸2-乙基己酯、甲基丙烯酸缩水甘油酯、丙烯酸2-羟基乙酯、丙烯酸甲酯、甲基丙烯酸甲酯、叔辛基丙烯酰胺和乙酸乙烯酯,优选地从选自以下的一种或多种单体获得:丙烯酸乙基己酯、甲基丙烯酸缩水甘油酯、丙烯酸2-羟基乙酯和乙酸乙烯酯。
10.根据项目1至9中任一项所述的透皮治疗系统,其中所述丙烯酸聚合物是COOH-官能化的丙烯酸聚合物,优选可由一种或多种选自丙烯酸、丙烯酸2-乙基己酯、甲基丙烯酸缩水甘油酯和丙烯酸甲酯的单体获得的COOH-官能化的丙烯酸聚合物,其以乙酸乙酯和己烷的溶液形式提供。
11.根据项目1至10中任一项所述的透皮治疗系统,
其中所述含有卡巴拉汀的层不包含渗透促进剂或增溶剂。
12.根据项目1至11中任一项所述的透皮治疗系统,
其中所述至少一种苯乙烯-异戊二烯-苯乙烯嵌段共聚物包含比率为10∶90(%)至30∶70(%)、优选比率为15∶85(%)或22∶78(%)的苯乙烯嵌段和异戊二烯嵌段。
13.根据项目1至12中任一项所述的透皮治疗系统,
其中所述至少一种苯乙烯-异戊二烯-苯乙烯嵌段共聚物可通过使聚苯乙烯、聚异戊二烯和聚苯乙烯的三个嵌段聚合而获得。
14.根据项目1至13中任一项所述的透皮治疗系统,
其中所述至少一种增粘剂是脂环族饱和烃树脂、或氢化松香甘油酯、或石蜡液体、或其混合物。
15.根据项目1至14中任一项所述的透皮治疗系统,
其中所述至少一种增粘剂是包含脂环族饱和烃树脂和石蜡液体的混合物。
16.根据项目1至15中任一项所述的透皮治疗系统,
其中所述至少一种增粘剂是包含氢化松香甘油酯和石蜡液体的混合物。
17.根据项目14或15所述的透皮治疗系统,
其中所述脂环族饱和烃树脂可通过不饱和烃的聚合而获得,所述不饱和烃可通过在高温下分解石油石脑油而制备获得。
18.根据项目14或16所述的透皮治疗系统,
其中所述氢化松香甘油酯是可通过将松香氢化,然后用甘油酯化而获得的固体树脂。
19.根据项目1至18中任一项所述的透皮治疗系统,
其中在所述皮肤接触层中所含的增粘剂的量在20至80%、优选35至65%的范围内。
20.根据项目1至19中任一项所述的透皮治疗系统,
其中所述一种或多种苯乙烯-异戊二烯-苯乙烯嵌段共聚物的量与所述一种或多种增粘剂的量的比率基于所述皮肤接触层的总重量在60∶40(w/w)至40∶60(w/w)之间,优选地其中所述一种或多种苯乙烯-异戊二烯-苯乙烯嵌段共聚物的量与所述一种或多种增粘剂的量的比率基于所述皮肤接触层的总重量为50∶50(w/w)。
21.根据项目1至20中任一项所述的透皮治疗系统,其中所述至少一种苯乙烯-异戊二烯-苯乙烯嵌段共聚物和所述至少一种增粘剂以基于所述皮肤接触层的总重量的至少90重量%的总量、优选至少99重量%的总量存在于所述皮肤接触层中。
22.根据项目1至21中任一项所述的透皮治疗系统,
其中所述皮肤接触层的面积重量在5至60g/m
23.根据项目1至22中任一项所述的透皮治疗系统,
其中所述含有卡巴拉汀的层的面积重量在40至250g/m
24.根据项目1至23中任一项所述的透皮治疗系统,
其中释放面积在1至30cm
25.根据项目1至24中任一项所述的透皮治疗系统,
其中所述透皮治疗系统通过透皮递送在约24小时的施用中提供150至3500μg/cm
26.根据项目1至25中任一项所述的透皮治疗系统,
如在使用EVA膜的Franz扩散池中所测量的,所述透皮治疗系统在约24小时的时间段内提供约300至1200μg/cm
27.根据项目1至26中任一项所述的透皮治疗系统,其用于治疗人类患者的方法,优选用于预防、治疗阿尔茨海默病、帕金森氏病相关的痴呆症和/或创伤性脑损伤症状或延缓阿尔茨海默病、帕金森氏病相关的痴呆症和/或创伤性脑损伤症状进展的方法。
28.根据项目1至27中任一项所述的透皮治疗系统,其用于治疗人类患者的方法,优选用于治疗由阿尔茨海默病或帕金森氏病引起的轻度至中度痴呆症的方法。
29.根据项目27或28所使用的透皮治疗系统,其中所述透皮治疗系统以至少24小时、优选约24小时的给药间隔施加至所述患者皮肤。
30.一种通过向患者皮肤施加如项目1至27中任一项所定义的透皮治疗系统来治疗所述人类患者的方法,特别是预防、治疗阿尔茨海默病、帕金森氏病相关的痴呆症和/或创伤性脑损伤症状或延缓阿尔茨海默病、帕金森氏病相关的痴呆症和/或创伤性脑损伤症状进展。
31.一种通过向患者皮肤施加如项目1至28中任一项所定义的透皮治疗系统来治疗所述人类患者的方法,特别是治疗由阿尔茨海默病和帕金森氏病引起的轻度至中度痴呆症。
32.根据项目30或31所述的治疗人类患者的方法,其中所述透皮治疗系统以至少24小时、优选约24小时的给药间隔施加至所述患者皮肤。
33.一种用于制造根据项目1至29中任一项所述的透皮治疗系统的方法,所述方法包括以下步骤:
1)通过组合至少以下组分来提供含有卡巴拉汀的涂覆组合物
i)卡巴拉汀;和
ii)至少一种丙烯酸聚合物;
2)将所述含有卡巴拉汀的涂覆组合物以提供所需面积重量的量涂覆于膜上,
3)干燥所述涂覆的含有卡巴拉汀的涂覆组合物以提供所述含有卡巴拉汀的层,
4)通过组合至少以下组分为附加皮肤接触层提供另外的涂覆组合物
a)至少一种苯乙烯-异戊二烯-苯乙烯嵌段共聚物;和
b)至少一种增粘剂;
5)根据步骤2和3涂覆并干燥所述另外的涂覆组合物,其中所述膜是离型衬垫,
6)将所述皮肤接触层的粘合剂侧层压到所述含有卡巴拉汀的层的粘合剂侧上,以提供具有所需释放面积的含有卡巴拉汀的层结构,
7)从所述含有卡巴拉汀的层结构中冲压出单独系统,
8)任选地将不含卡巴拉汀的自粘层结构粘附至所述单独系统,所述不含卡巴拉汀的自粘层结构还包括背衬层和不含卡巴拉汀的压敏粘合剂层,并且所述不含卡巴拉汀的自粘层结构比所述含有卡巴拉汀的自粘层结构的单独系统大。
34.根据项目33所述的制造方法,
其中步骤2)中的所述膜是离型衬垫,
其中在步骤3)之后将所述含有卡巴拉汀的层层压到背衬层,并且
其中在步骤6)之前去除步骤2)的所述离型衬垫。
35.根据项目33或34所述的含有卡巴拉汀的层的制造方法,其中所述丙烯酸聚合物以溶液形式提供,其中所述溶剂为乙酸乙酯或正庚烷。
36.一种通过根据项目33至35中任一项所述方法可获得的透皮治疗系统。
- 含有卡巴拉汀的透皮治疗系统
- 含有甾类激素和含有丙二醇单辛酸酯的透皮治疗系统
