一种γ-咔啉衍生物的合成方法
文献发布时间:2023-06-19 11:30:53
技术领域
本发明实施例涉及有机合成技术领域,尤其涉及一种γ-咔啉衍生物的合成方法。
背景技术
咔啉衍生物是一类重要的天然含氮生物碱,其分子结构是由吲哚并吡啶的三环结构组成,具有较大的平面芳香体系。具有抗菌、抗病毒、抗肿瘤以及抑制中枢神经系统等重要的生物活性和药理活性。据分子内吡啶氮原子位置的不同,分为α-咔啉,β-咔啉,γ-咔啉和δ-咔啉。其中,由于β-咔啉在自然界中存在最为广泛,它们能抑制拓扑异构酶、细胞周期蛋白依赖性激酶和DNA的合成。并能嵌入DNA中,所有这些作用使它们具有很强的抗肿瘤活性。然而,相对于被广泛研究的β-咔啉而言,γ-咔啉的相关研究较少。近些年,作为β-咔啉的生物电子等排体,γ-咔啉衍生物也越来越多地受到研究工作者的关注,对其进行了一系列的研究与结构优化。研究发现,γ-咔啉类衍生物不像β-咔啉类衍生物那样具有强烈的抗肿瘤活性。它们的生物学活性表现为5-HT受体的抑制作用。
目前,γ-咔啉衍生物的合成方法主要有:(1)利用含有特殊官能团(如胺基)的γ-咔啉作为原料进行衍生化和结构修饰。(2)利用吲哚亚胺或者吲哚肟醚与烯烃或者炔烃,通过金属催化的环化反应制备。(3)利用N-苯基吡啶胺作为原料,通过金属催化的分子内环化反应制备。(4)通过官能化的吲哚-3-甲醛与醛和乙酸铵的三组分串联反应制备。但是,现有方法存在一些不足:(1)原料来源不广泛,需要利用吲哚经过多步反应制备。(2)合成步骤繁琐且条件较为苛刻。(3)反应效率较低,且区域选择性不好,不具备放大反应前景。(4)γ-咔啉的氮原子上具有取代基团,不利于氮原子的后期结构修饰。
因此,利用简单易得的原料,发展一种“从头构建”、普遍适用且具有一定放大应用前景的合成方法,以高效地制备各种取代的-咔啉衍生物,这对于满足大量药物分子活性筛选的需求,以及快速开发γ-咔啉的候选药物具有重要意义。
发明内容
本发明实施例的目的是提供一种γ-咔啉衍生物的合成方法,该方法“从头构建”,利用简单易得的吲哚作为起始原料,原料来源广泛;合成步骤较简单;反应效率高;γ-咔啉的氮原子上没有取代基团,有利于氮原子的后期结构修饰。
本发明实施例的目的在于提供一种γ-咔啉衍生物的合成方法,所述方法包括:
将化合物I与R
将所述化合物II脱去嘧啶基团,获得化合物III;
将所述化合物III进行甲酰化反应,获得化合物IV;
将所述化合物IV进行串联的亚胺化和环化反应,获得化合物V所示的γ-咔啉衍生物;
其中,反应式如下所示:
取代基R
取代基R
进一步地,所述化合物I为将吲哚与2-氯嘧啶进行N取代反应获得。
进一步地,所述C-H烯基化反应中,加入催化剂和有机溶剂,所述催化剂包括AgOAc和[RhCp*Cl
进一步地,所述催化剂、所述化合物I和所述烯基硼酸酯的摩尔量比为:AgOAc:[RhCp*Cl
进一步地,所述C-H烯基化反应的温度为25~100℃,所述C-H烯基化反应的时间为4~30h。
进一步地,所述将所述化合物II脱去嘧啶基团,获得化合物III,包括:
将所述化合物II与乙醇钠或甲醇钠进行反应脱去嘧啶基团,获得化合物III。
进一步地,所述化合物II与所述乙醇钠的摩尔比为1:(3~5);所述化合物II与所述甲醇钠的摩尔比为1:(3~5)。
进一步地,所述甲酰化反应中加入POCl
进一步地,所述串联的亚胺化和环化反应中加入盐酸羟胺、乙酸钠和1,4-二氧六环,所述化合物IV、盐酸羟胺和乙酸钠的摩尔比为化合物IV:盐酸羟胺:乙酸钠=1:(1~4):(1~4)。
本发明实施例中的一个或多个技术方案,至少具有如下技术效果或优点:
本发明实施例提供的一种γ-咔啉衍生物的合成方法,所述方法包括:将化合物I与R
附图说明
为了更清楚地说明本发明实施例中的技术方案,下面将对实施例描述中所需要使用的附图作一简单地介绍,显而易见地,下面描述中的附图是本发明实施例的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图得到其它的附图。
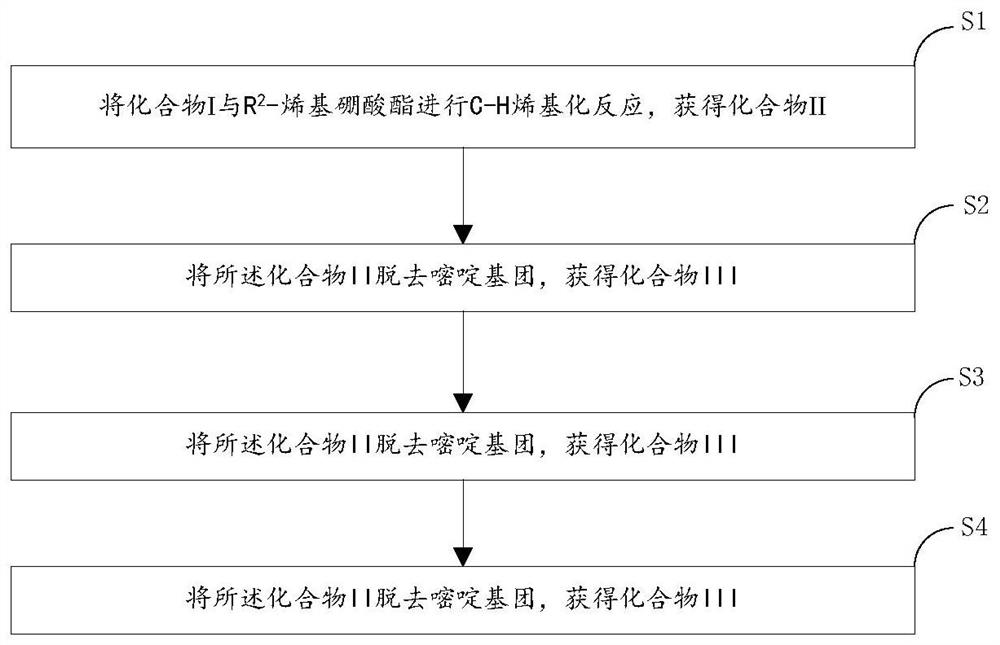
图1是本发明实施例提供的一种γ-咔啉衍生物的合成方法的流程图;
图2是本发明实施例1制备得到末端1,2-双取代吲哚乙烯衍生物的H NMR谱图;
图3是本发明实施例1制备得到末端1,2-双取代吲哚乙烯衍生物的C NMR谱图谱图;
图4为本发明实施例1制备得到末端1,2-双取代吲哚乙烯衍生物的高分辨质谱图;
图5是本发明实施例6制备得到末端1,2-双取代吲哚乙烯衍生物的H NMR谱图;
图6是本发明实施例6制备得到末端1,2-双取代吲哚乙烯衍生物的C NMR谱图谱图;
图7为本发明实施例6制备得到末端1,2-双取代吲哚乙烯衍生物的高分辨质谱图。
具体实施方式
下文将结合具体实施方式和实施例,具体阐述本发明实施例,本发明实施例的优点和各种效果将由此更加清楚地呈现。本领域技术人员应理解,这些具体实施方式和实施例是用于说明本发明实施例,而非限制本发明实施例。
在整个说明书中,除非另有特别说明,本文使用的术语应理解为如本领域中通常所使用的含义。因此,除非另有定义,本文使用的所有技术和科学术语具有与本发明实施例所属领域技术人员的一般理解相同的含义。若存在矛盾,本说明书优先。
除非另有特别说明,本发明实施例中用到的各种原材料、试剂、仪器和设备等,均可通过市场购买得到或者可通过现有方法制备得到。
本发明实施例提供的技术方案为解决上述技术问题,总体思路如下:
根据本发明实施例一种典型的实施方式,提供一种γ-咔啉衍生物的合成方法,如图1所示,所述方法包括:
S1、将所述化合物I与R
该实施方式中,化合物I可购买获得,也可将吲哚与2-氯嘧啶进行N取代反应获得;所述N取代反应中加入有机溶剂DMF和催化剂NaH,反应温度为0~130℃。所述吲哚和所述2-氯嘧啶的摩尔量比为(1~1.2):(1~1.2)。该比值过高或过低不利于反应完全;
所述R
步骤S1中,加入催化剂和有机溶剂,所述催化剂包括AgOAc和[RhCp*Cl
所述催化剂、所述化合物I和所述烯基硼酸酯的摩尔量比为:AgOAc:[RhCp*Cl
所述C-H烯基化反应的温度为20~100℃,所述C-H烯基化反应的时间为4~30h。所述反应温度过低或过高均不利于反应的进行或者反应完全。
S2、将所述化合物II脱去嘧啶基团,获得化合物III;
步骤S2中,将所述化合物II与乙醇钠或甲醇钠进行反应脱去嘧啶基团,获得化合物III。
所述化合物II与所述乙醇钠的摩尔比为1:(3~5);所述化合物II与所述甲醇钠的摩尔比为1:(3~5)。该比值过高或过低不利于反应完全;
S3、将所述化合物III进行甲酰化反应,获得化合物IV;
步骤S3中,所述甲酰化反应中加入催化剂POCl
具体地,加入DMF,冰浴冷却下向其中逐滴加入POCl3。搅拌10-30min后,向反应瓶中加入化合物III,然后升至室温,继续搅拌0.2-1h后,加入冰水,随后再加入1mol/L的NaOH溶液,进行后处理提纯:
所述化合物III、POCl
DMF的体积和化合物III的摩尔数的比值为(3~5):(0.5~2);该比值过高或过低不利于甲酰化反应完全;
S4、将所述化合物IV进行串联的亚胺化和环化反应,获得化合物V所示的γ-咔啉衍生物;
步骤S4中,加入盐酸羟胺、乙酸钠和1,4-二氧六环,所述化合物IV、盐酸羟胺和乙酸钠的摩尔比为化合物IV:盐酸羟胺:乙酸钠=1:(1~4):(1~4)。该比值过高或过低不利于反应完全;
其中,反应式具体如下所示:
取代基R
取代基R
本申请人发现利用简单易得的吲哚作为起始原料先后通过N取代反应、C-H烯基化反应、基团脱除反应、甲酰化反应、串联的亚胺化和环化反应成功获得化合物V所示的γ-咔啉衍生物;该方法“从头构建”,利用简单易得的吲哚作为起始原料,原料来源广泛,具有普遍适用且有一定放大应用前景的特点,对于快速地发现γ-咔啉医药农药候选分子,缩短研究周期具有一定的意义;合成步骤较简单;反应效率高;γ-咔啉的氮原子上没有取代基团,有利于氮原子的后期结构修饰。
下面将结合实施例及实验数据对本申请的一种γ-咔啉衍生物的合成方法进行详细说明。
实施例1
1、合成化合物(1-1)
在25mL反应瓶中加入吲哚(5mmol)、DMF(10mL)以及NaH(5mmol)。反应混合物在0℃下搅拌10分钟,再加入2-氯嘧啶(6mmol),然后升到室温至130℃反应,TLC检测至反应完全。进行后处理提纯:加入水(20mL)淬灭,用EA(20mL×3)萃取,合并有机相,用饱和NaCl(20mL×2)洗涤。分液后用无水硫酸镁干燥,减压除去有机溶剂,用硅胶柱层析分离纯化[V(石油醚):V(乙酸乙酯)=15:1],即得到纯净的产物,白色固体,产率:85%。
化合物(1-1)经检测:
2、合成化合物(1-2)
在15mL schlenk管中,加入化合物(1-1)(1mmol),苯乙烯基硼酸频哪醇酯(2mmol),AgOAc(2mmol),[RhCp*Cl
化合物(1-2)经检测:
HRMS m/z:calcd for C
3、合成化合物(1-3)
在25mL的反应瓶中,加入化合物(1-2)(1mmol)、乙醇钠(4mmol)以及DMSO(10mL)。反应混合物置于100℃下反应,TLC检测至反应完全。进行后处理提纯:反应混合物用水(20mL)淬灭,用EA(20mL×2)萃取,合并有机相,用饱和NaCl(20mL×1)洗涤。分液后用无水硫酸镁干燥,减压除去有机溶剂,用硅胶柱层析分离纯化[V(石油醚):V(乙酸乙酯)=15:1],即得到纯净的产物,白色固体,产率:64%。
化合物(1-3)经检测:
4、合成化合物(1-4)
在50mL反应瓶中加入DMF(4mL),冰浴冷却下向其中逐滴加入POCl
化合物(1-4)经检测:
HRMS m/z:calcd for C
5、合成化合物(1-5)
在25mL反应瓶中加入化合物(1-4)(1mmol)、盐酸羟胺(2mmol)、乙酸钠(2mmol)以及1,4-二氧六环(10mL),反应混合物回流反应,TLC检测至反应完全。进行后处理提纯:加入水(20mL)淬灭,用EA(20mL×3)萃取,合并有机相,用饱和NaCl(20mL×2)洗涤。分液后用无水硫酸镁干燥,减压除去有机溶剂,用硅胶柱层析分离纯化[V(石油醚):V(乙酸乙酯)=20:1],即得到纯净的产物,白色固体,产率:99%。
化合物(1-5)经检测:
HRMS m/z:calcd for C
实施例2
1、合成化合物(2-1)
在25mL反应瓶中加入4-苄基吲哚(5mmol)、DMF(10mL)以及NaH(5mmol)。反应混合物在0℃下搅拌10分钟,再加入2-氯嘧啶(6mmol),然后升到室温至130℃反应,TLC检测至反应完全。进行后处理提纯:加入水(20mL)淬灭,用EA(20mL×3)萃取,合并有机相,用饱和NaCl(20mL×2)洗涤。分液后用无水硫酸镁干燥,减压除去有机溶剂,用硅胶柱层析分离纯化[V(石油醚):V(乙酸乙酯)=15:1],即得到纯净的产物,白色固体,产率:80%。
2、合成化合物(2-2)
在15mL schlenk管中,加入化合物(2-1)(1mmol),苯乙烯基硼酸频哪醇(2mmol),AgOAc(2mmol),[RhCp*Cl
3、合成化合物(2-3)
在25mL的反应瓶中,加入化合物(2-2)(1mmol)、乙醇钠(4mmol)以及DMSO(10mL)。反应混合物置于100℃下反应,TLC检测至反应完全。进行后处理提纯:反应混合物用水(20mL)淬灭,用EA(20mL×2)萃取,合并有机相,用饱和NaCl(20mL×1)洗涤。分液后用无水硫酸镁干燥,减压除去有机溶剂,用硅胶柱层析分离纯化[V(石油醚):V(乙酸乙酯)=15:1],即得到纯净的产物,白色固体,产率:70%。
4、合成化合物(2-4)
在50mL反应瓶中加入DMF(4mL),冰浴冷却下向其中逐滴加入POCl
5、合成化合物(2-5)
在25mL反应瓶中加入化合物(2-4)(1mmol)、盐酸羟胺(2mmol)、乙酸钠(2mmol)以及1,4-二氧六环(10mL),反应混合物回流反应,TLC检测至反应完全。进行后处理提纯:加入水(20mL)淬灭,用EA(20mL×3)萃取,合并有机相,用饱和NaCl(20mL×2)洗涤。分液后用无水硫酸镁干燥,减压除去有机溶剂,用硅胶柱层析分离纯化[V(石油醚):V(乙酸乙酯)=20:1],即得到纯净的产物,白色固体,产率:96%。
实施例3
1、合成化合物(3-1)
在25mL反应瓶中加入5-甲基吲哚(5mmol)、DMF(10mL)以及NaH(5mmol)。反应混合物在0℃下搅拌10分钟,再加入2-氯嘧啶(6mmol),然后升到室温至130℃反应,TLC检测至反应完全。进行后处理提纯:加入水(20mL)淬灭,用EA(20mL×3)萃取,合并有机相,用饱和NaCl(20mL×2)洗涤。分液后用无水硫酸镁干燥,减压除去有机溶剂,用硅胶柱层析分离纯化[V(石油醚):V(乙酸乙酯)=15:1],即得到纯净的产物,白色固体,产率:84%。
2、合成化合物(3-2)
在15mL schlenk管中,加入化合物(3-1)(1mmol),苯乙烯基硼酸频哪醇(2mmol),AgOAc(2mmol),[RhCp*Cl
3、合成化合物(3-3)
在25mL的反应瓶中,加入化合物(3-2)(1mmol)、乙醇钠(4mmol)以及DMSO(10mL)。反应混合物置于100℃下反应,TLC检测至反应完全。进行后处理提纯:反应混合物用水(20mL)淬灭,用EA(20mL×2)萃取,合并有机相,用饱和NaCl(20mL×1)洗涤。分液后用无水硫酸镁干燥,减压除去有机溶剂,用硅胶柱层析分离纯化[V(石油醚):V(乙酸乙酯)=15:1],即得到纯净的产物,白色固体,产率:67%。
4、合成化合物(3-4)
在50mL反应瓶中加入DMF(4mL),冰浴冷却下向其中逐滴加入POCl
5、合成化合物(3-5)
在25mL反应瓶中加入化合物(3-4)(1mmol)、盐酸羟胺(2mmol)、乙酸钠(2mmol)以及1,4-二氧六环(10mL),反应混合物回流反应,TLC检测至反应完全。进行后处理提纯:加入水(20mL)淬灭,用EA(20mL×3)萃取,合并有机相,用饱和NaCl(20mL×2)洗涤。分液后用无水硫酸镁干燥,减压除去有机溶剂,用硅胶柱层析分离纯化[V(石油醚):V(乙酸乙酯)=20:1],即得到纯净的产物,白色固体,产率:98%。
实施例4
1、合成化合物(4-1)
在25mL反应瓶中加入6-溴吲哚(5mmol)、DMF(10mL)以及NaH(5mmol)。反应混合物在0℃下搅拌10分钟,再加入2-氯嘧啶(6mmol),然后升到室温至130℃反应,TLC检测至反应完全。进行后处理提纯:加入水(20mL)淬灭,用EA(20mL×3)萃取,合并有机相,用饱和NaCl(20mL×2)洗涤。分液后用无水硫酸镁干燥,减压除去有机溶剂,用硅胶柱层析分离纯化[V(石油醚):V(乙酸乙酯)=15:1],即得到纯净的产物,白色固体,产率:78%。
2、合成化合物(4-2)
在15mL schlenk管中,加入化合物(4-1)(1mmol),苯乙烯基硼酸频哪醇(2mmol),AgOAc(2mmol),[RhCp*Cl
3、合成化合物(4-3)
在25mL的反应瓶中,加入化合物(4-2)(1mmol)、乙醇钠(4mmol)以及DMSO(10mL)。反应混合物置于100℃下反应,TLC检测至反应完全。进行后处理提纯:反应混合物用水(20mL)淬灭,用EA(20mL×2)萃取,合并有机相,用饱和NaCl(20mL×1)洗涤。分液后用无水硫酸镁干燥,减压除去有机溶剂,用硅胶柱层析分离纯化[V(石油醚):V(乙酸乙酯)=15:1],即得到纯净的产物,白色固体,产率:60%。
4、合成化合物(4-4)
在50mL反应瓶中加入DMF(4mL),冰浴冷却下向其中逐滴加入POCl
5、合成化合物(4-5)
在25mL反应瓶中加入化合物(4-4)(1mmol)、盐酸羟胺(2mmol)、乙酸钠(2mmol)以及1,4-二氧六环(10mL),反应混合物回流反应,TLC检测至反应完全。进行后处理提纯:加入水(20mL)淬灭,用EA(20mL×3)萃取,合并有机相,用饱和NaCl(20mL×2)洗涤。分液后用无水硫酸镁干燥,减压除去有机溶剂,用硅胶柱层析分离纯化[V(石油醚):V(乙酸乙酯)=20:1],即得到纯净的产物,白色固体,产率:90%。
实施例5
1、合成化合物(5-2)
在15mL schlenk管中,加入化合物(1-1)(1mmol),4-甲基苯乙稀基硼酸频哪醇酯(2mmol),AgOAc(2mmol),[RhCp*Cl
2、合成化合物(5-3)
在25mL的反应瓶中,加入化合物(5-2)(1mmol)、乙醇钠(4mmol)以及DMSO(10mL)。反应混合物置于100℃下反应,TLC检测至反应完全。进行后处理提纯:反应混合物用水(20mL)淬灭,用EA(20mL×2)萃取,合并有机相,用饱和NaCl(20mL×1)洗涤。分液后用无水硫酸镁干燥,减压除去有机溶剂,用硅胶柱层析分离纯化[V(石油醚):V(乙酸乙酯)=15:1],即得到纯净的产物,白色固体,产率:80%。
3、合成化合物(5-4)
在50mL反应瓶中加入DMF(4mL),冰浴冷却下向其中逐滴加入POCl
4、合成化合物(5-5)
在25mL反应瓶中加入化合物(5-4)(1mmol)、盐酸羟胺(2mmol)、乙酸钠(2mmol)以及1,4-二氧六环(10mL),反应混合物回流反应,TLC检测至反应完全。进行后处理提纯:加入水(20mL)淬灭,用EA(20mL×3)萃取,合并有机相,用饱和NaCl(20mL×2)洗涤。分液后用无水硫酸镁干燥,减压除去有机溶剂,用硅胶柱层析分离纯化[V(石油醚):V(乙酸乙酯)=20:1],即得到纯净的产物,白色固体,产率:99%。
实施例6
1、合成化合物(6-2)
在15mL schlenk管中,加入化合物(1-1)(1mmol),4-苯基丁稀基硼酸频哪醇酯(2mmol),AgOAc(2mmol),[RhCp*Cl
2、合成化合物(6-3)
在25mL的反应瓶中,加入化合物(6-2)(1mmol)、乙醇钠(4mmol)以及DMSO(10mL)。反应混合物置于100℃下反应,TLC检测至反应完全。进行后处理提纯:反应混合物用水(20mL)淬灭,用EA(20mL×2)萃取,合并有机相,用饱和NaCl(20mL×1)洗涤。分液后用无水硫酸镁干燥,减压除去有机溶剂,用硅胶柱层析分离纯化[V(石油醚):V(乙酸乙酯)=15:1],即得到纯净的产物,白色固体,产率:71%。
3、合成化合物(5-4)
在50mL反应瓶中加入DMF(4mL),冰浴冷却下向其中逐滴加入POCl
4、合成化合物(5-5)
在25mL反应瓶中加入化合物(6-4)(1mmol)、盐酸羟胺(2mmol)、乙酸钠(2mmol)以及1,4-二氧六环(10mL),反应混合物回流反应,TLC检测至反应完全。进行后处理提纯:加入水(20mL)淬灭,用EA(20mL×3)萃取,合并有机相,用饱和NaCl(20mL×2)洗涤。分液后用无水硫酸镁干燥,减压除去有机溶剂,用硅胶柱层析分离纯化[V(石油醚):V(乙酸乙酯)=20:1],即得到纯净的产物,白色固体,产率:92%。
最后,还需要说明的是,术语“包括”、“包含”或者其任何其他变体意在涵盖非排他性的包含,从而使得包括一系列要素的过程、方法、物品或者设备不仅包括那些要素,而且还包括没有明确列出的其他要素,或者是还包括为这种过程、方法、物品或者设备所固有的要素。
尽管已描述了本发明实施例的优选实施例,但本领域内的技术人员一旦得知了基本创造性概念,则可对这些实施例作出另外的变更和修改。所以,所附权利要求意欲解释为包括优选实施例以及落入本发明实施例范围的所有变更和修改。
显然,本领域的技术人员可以对本发明实施例进行各种改动和变型而不脱离本发明实施例的精神和范围。这样,倘若本发明实施例的这些修改和变型属于本发明实施例权利要求及其等同技术的范围之内,则本发明实施例也意图包含这些改动和变型在内。
- 一种60富勒烯二氢咔啉类衍生物的合成方法
- 一种60富勒烯二氢咔啉类衍生物的合成方法
