基于掺杂碳量子点/PVA复合膜及其制备方法与检测四环素的应用
文献发布时间:2023-06-19 11:40:48
技术领域
本发明属于传感器合成技术和光化学分析领域,本发明涉及基于掺杂碳量子点/PVA复合膜及其制备方法与检测四环素的应用。
背景技术
公开该背景技术部分的信息仅仅旨在增加对本发明的总体背景的理解,而不必然被视为承认或以任何形式暗示该信息构成已经成为本领域一般技术人员所公知的现有技术。
四环素类(TCs)是一组来源于链霉菌属的抗生素。具有广谱活性。兽药中最常用的四环素类抗生素是四环素、土霉素、金霉素和多西环素。TC是一种广谱抗微生物药物,由于它的许多副作用,过度使用TC引起了世人的关注。食物中TC的长期积累可能会增加某些严重的风险,如微生物菌株的耐药性、过敏或毒性反应、骨骼生长抑制。因此,需要开发一种简单有效的方法来检测食品中的TC。四环素(TC)是一种多用途的广谱抗生素,对革兰氏阳性和革兰氏阴性菌具有较高的活性。由于其低成本和高抗菌活性,用于治疗人类或动物的细菌感染,也用于农业部门的饲料添加剂促进动物的生长和体重。由于TC的巨大毒性和副作用,过度使用TC引起了全世界的广泛关注。过量的残留或持续的长期摄入小剂量的TC会导致过敏反应、牙齿变色、骨骼发育不良、微泡性脂肪肝、胃肠紊乱和肝毒性的不良影响,并促进杆菌对抗生素的抗药性。根据欧盟(EU)法规,牛奶中兽用四环素的最大残留限量(MRL)为100μg/kg。因此,需要一种快速、灵敏和选择性的检测方法来检测食品中的TC残留。
据发明人研究了解,目前检测TC的分析方法,包括色谱法、电泳法、电化学法、分光光度法、酶联免疫吸附测定法等。但这些方法总有耗时、仪器昂贵、操作繁琐等缺点。相比之下,光学方法由于其优异的灵敏度和选择性、易于操作和快速响应而更优越。基于碳量子点的荧光传感方法被广泛应用于四环素的检测,例如,氮、硫掺杂碳点,氮掺杂碳点,氮化碳量子点等。然而,发明人发现,目前采用荧光方法检测四环素的分析都是在水介质中进行的,水介质不是传感器,碳量子点需要配置成水溶液,碳量子点配置溶液的器具携带不方便,同时若直接将碳量子点制备成水溶液,则会由于碳量子点的聚集产生荧光猝灭,导致检测灵敏度降低。
发明内容
为了解决现有技术的不足,本发明的目的是提供基于掺杂碳量子点/PVA复合膜及其制备方法与检测四环素的应用,本发明制备的复合膜作为荧光传感器能够对TC进行检测,携带方便,对TC的检测具有更高的灵敏度和更好的选择性,同时可以对TC进行实时监测。
为了实现上述目的,本发明的技术方案为:
第一方面,一种掺杂碳量子点,由3-氨基苯硼酸和柠檬酸作为前驱体合成获得。
本发明采用3-氨基苯硼酸和柠檬酸作为前驱体合成获得碳量子点(CDs),该碳量子点具有强荧光发射且能与四环素特异性结合使其荧光猝灭。
第二方面,一种基于掺杂碳量子点/PVA复合膜,包括碳量子点和聚乙烯水凝胶膜,聚乙烯水凝胶膜负载碳量子点,所述碳量子点由3-氨基苯硼酸和柠檬酸作为前驱体合成获得。
聚乙烯醇(PVA)由于其良好的机械和热性能以及优异的阻隔性能而被选为支撑载体。将CDs固定在PVA载体中可以稳定CDs的荧光,从而抑制CDs随时间的聚集而产生的荧光猝灭。
第三方面,一种基于掺杂碳量子点/PVA复合膜的制备方法,采用水热法将3-氨基苯基硼酸与柠檬酸制成碳量子点,将聚乙烯醇加入至碳量子点的水溶液中,加入交联剂进行交联,再将交联后物料去除水制成膜材料,即得基于掺杂碳量子点/PVA复合膜。
本发明采用聚乙烯醇作为支撑载体,不仅由于其具有良好的机械和热性能以及优异的阻隔性能,而且在制备过程中由于其具有凝胶性质,能够更好地将CDs固定在PVA中,从而能够更好的稳定CDs的荧光。
第四方面,一种上述基于掺杂碳量子点/PVA复合膜在检测四环素中的应用。
第五方面,一种检测四环素的荧光传感器,包括上述基于掺杂碳量子点/PVA复合膜。
第六方面,一种检测四环素的方法,将上述基于掺杂碳量子点/PVA复合膜或检测四环素的荧光传感器放入至含有四环素的待测溶液中浸泡,观察浸泡后的基于掺杂碳量子点/PVA复合膜或检测四环素的荧光传感器的颜色变化。
本发明的有益效果为:
1、本发明采用3-氨基苯硼酸和柠檬酸作为前驱体合成的碳量子点对四环素的选择性好,抗干扰性强。
2、本发明利用聚乙烯醇的凝胶性质,结合采用3-氨基苯硼酸和柠檬酸作为前驱体合成的碳量子点成功地制备了检测四环素的便携式以及视觉模式下的传感器。
3、本发明荧光传感器制备方法简单,操作方便,能够方便携带和视觉可视化,该荧光传感器在检测四环素方面具有很大的潜在应用价值及巨大的市场效益。
附图说明
构成本发明的一部分的说明书附图用来提供对本发明的进一步理解,本发明的示意性实施例及其说明用于解释本发明,并不构成对本发明的不当限定。
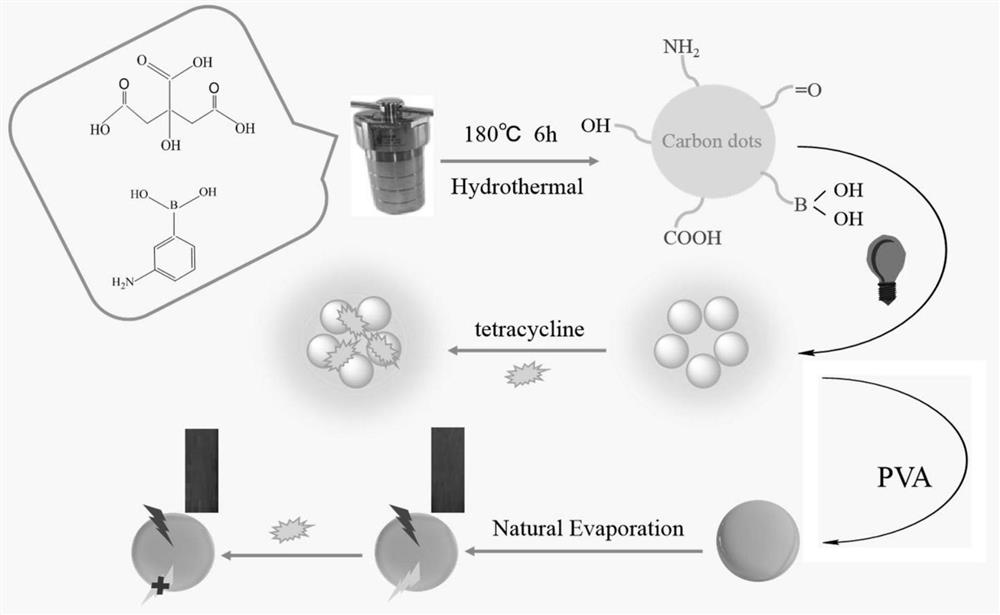
图1为本发明实施例合成四环素传感器的原理图;
图2为本发明实施例1制备的CDs的工作曲线示意图,A为荧光强度曲线,B为标准曲线,C为日光及紫外灯下不同浓度四环素的CDs照片;
图3为本发明对比例1和对比例2中不同种类的缓冲液对CDs和CDs-TC的荧光信号示意图;
图4为本发明对比例3和对比例4中不同pH值对CDs和CDs-TC的荧光信号示意图;
图5为本发明对比例5中NaCl浓度对CDs的荧光信号示意图;
图6为本发明对比例6中不同反应温度的荧光信号示意图;
图7为本发明对比例7中不同的反应时间的荧光信号示意图;
图8为本发明对比例8中前驱体摩尔质量比对合成CDs影响的荧光信号示意图;
图9为本发明实施例2的四环素传感器的选择性荧光信号示意图,A不同化学物质,B为不同抗生素;
图10为视觉模式下四环素传感器示意图,A为CDs-PVA膜的照片,B为具有不同CDs体积(从左至右,1000、800、400、100μL/mL)的CDs-PVA膜的照片,C为具有不同TC浓度(从左至右,0,0.01,0.05、0.1、0.5、1.0、2.0和5.0mg/mL)的CDs-PVA膜的照片,D为以不同浓度的四环素加标牛奶样品(从左至右,空白,只有牛奶样品,四环素加标0.01、0.1、1.0mg/mL)CDs-PVA膜的照片。
具体实施方式
应该指出,以下详细说明都是示例性的,旨在对本发明提供进一步的说明。除非另有指明,本文使用的所有技术和科学术语具有与本发明所属技术领域的普通技术人员通常理解的相同含义。
需要注意的是,这里所使用的术语仅是为了描述具体实施方式,而非意图限制根据本发明的示例性实施方式。如在这里所使用的,除非上下文另外明确指出,否则单数形式也意图包括复数形式,此外,还应当理解的是,当在本说明书中使用术语“包含”和/或“包括”时,其指明存在特征、步骤、操作、器件、组件和/或它们的组合。
为了开发一种便携式、高灵敏、快速检测TC的传感器,本发明提出了基于掺杂碳量子点/PVA复合膜及其制备方法与检测四环素的应用。
本发明的一种典型实施方式,提供了一种掺杂碳量子点,由3-氨基苯硼酸和柠檬酸作为前驱体合成获得。
通过实验表明,该碳量子点能够发射强荧光,而且四环素能够与该碳量子点特异性结构并使该碳量子点的荧光猝灭。
在一些实施例中,3-氨基苯基硼酸与柠檬酸进行水热反应获得掺杂碳量子点。本发明所述的水热反应或水热法是指,在密闭体系下,以水作为溶剂进行高温高压的反应或方法。
在一种或多种实施例中,水热反应的温度为160~200℃。当温度为176~184℃时,荧光强度更好。
在一种或多种实施例中,水热反应的时间为4~8h。当时间为5.6~6.4h时,荧光强度更好。
在一种或多种实施例中,3-氨基苯基硼酸与柠檬酸的质量比为1:0.2~5。当3-氨基苯基硼酸与柠檬酸的质量比1:0.9~1.1时,荧光强度更好。
本发明的另一种实施方式,提供了一种基于掺杂碳量子点/PVA复合膜,包括碳量子点和聚乙烯水凝胶膜,聚乙烯水凝胶膜负载碳量子点,所述碳量子点由3-氨基苯硼酸和柠檬酸作为前驱体合成获得。
本发明将CDs固定在PVA载体中可以稳定CDs的荧光,从而抑制CDs随时间的聚集而产生的荧光猝灭。
在一些实施例中,碳量子点与聚乙烯醇水凝胶膜的质量比为0.1~1:100~170。
本发明的第三种实施方式,提供了一种基于掺杂碳量子点/PVA复合膜的制备方法,采用水热法将3-氨基苯基硼酸与柠檬酸制成碳量子点,将聚乙烯醇加入至碳量子点的水溶液中,加入交联剂进行交联,再将交联后物料去除水制成膜材料,即得基于掺杂碳量子点/PVA复合膜。
本发明采用聚乙烯醇作为支撑载体,不仅由于其具有良好的机械和热性能以及优异的阻隔性能,而且在制备过程中由于其具有凝胶性质,能够更好地将CDs固定在PVA中,从而能够更好的稳定CDs的荧光。
在一些实施例中,聚乙烯醇加入至碳量子点的水溶液后,混合溶液中聚乙烯醇的浓度为90~110mg/mL。
在一些实施例中,加入交联剂后,混合溶液中交联剂的浓度为60~70mg/mL。
在一些实施例中,所述交联剂为尿素。
在一些实施例中,交联后将混合溶液至于模具中自然晾干获得基于掺杂碳量子点/PVA复合膜。
本发明的第四种实施方式,提供了一种上述基于掺杂碳量子点/PVA复合膜在检测四环素中的应用。
具体的,所述应用可以为在检测牛奶等食品中的四环素的应用,还可以在食品安全和/或环境分析四环素的实时监测中的应用。
本发明的第五种实施方式,提供了一种检测四环素的荧光传感器,包括上述基于掺杂碳量子点/PVA复合膜。
本发明的第六种实施方式,提供了一种检测四环素的方法,将上述基于掺杂碳量子点/PVA复合膜或检测四环素的荧光传感器放入至含有四环素的待测溶液中浸泡,观察浸泡后的基于掺杂碳量子点/PVA复合膜或检测四环素的荧光传感器的颜色变化。
在一些实施例中,待测溶液中的pH为3~10。当待测溶液中的pH为6.6~6.7时,检测效果更好。
为了使得本领域技术人员能够更加清楚地了解本发明的技术方案,以下将结合具体的实施例与对比例详细说明本发明的技术方案。
实施例1
四环素传感器的合成方法
简而言之,将4.8mg 3-氨基苯基硼酸和4.8mg柠檬酸溶解在5mL去离子水中,超声处理2分钟后将混合物转移至25mL聚四氟乙烯高压反应釜中,在真空干燥箱中180℃加热6h。冷却至室温后,将获得的溶液在离心机中离心纯化5分钟以除去反应残余物和凝聚粒子获得上清液。最后,将获得的浅黄色透明溶液保存在4℃下以备后用,采用滴涂法制备CDs/PVA复合膜。将PVA加入到CDs溶液中(CDs溶液的浓度为1.0mg/mL,加入PVA后,溶液中PVA的浓度为100mg/mL),然后将PVA加热至完全溶解后,向溶液中添加作为交联剂的尿素(65mg/mL)。加入交联剂后用玻璃棒搅拌10s,然后冷却。冷却后,将混合物滴在聚四氟乙烯模具中,在室温下自然晾晒蒸发水分形成CDs/PVA复合膜。
在最佳合成和传感条件下研究了TC检测的灵敏度。从图2中可以看出,CDs的荧光强度随着不同浓度的TC(0、1.8、2.5、3.6、5、10、20、40、60、80、100、120、150、200、250、300和350μM)有规律地降低。图2清楚地说明,随着TC浓度的增加,CDs的荧光逐渐被TC猝灭。相应的荧光强度变化(F
对比例1-对比例2为不同种类的缓冲液对CDs和CDs-TC荧光强度的影响,得到的荧光信号示意图,如图3所示。
对比例1
取20μL制备好的CDs原溶液放入1.5mL离心管中,然后向离心管中加入980μL配制好的不同种类的缓冲溶液混合均匀,在CDs最佳激发波长下用比色皿测定其荧光信号,从而得到不同种类缓冲溶液对CDs荧光信号的影响。
对比例2
取250μL上述制备好的混合溶液放入离心管中,然后向离心管中加入5μL配好的12.5mM的四环素溶液,然后在混匀器上混匀5分钟,在CDs最佳激发波长下用比色皿测定荧光信号,从而得到不同种类缓冲溶液对CDs-TC荧光信号的影响。
总结:通过对比例1-2,根据CDs和CDs-TC的荧光信号值(如图3所示),可以发现去离子水中CDs的荧光强度高于各缓冲溶液(HEPES,PB,PBS,Tris-HCl,HAc-NaAc)中CDs的荧光强度。此外,CDs-TC的荧光强度在去离子水中最低。由实验数据说明且考虑到该提议的简单性和易控制性,在随后的实验中选择pH为6.64的去离子水作为最佳检测条件。
对比例3-对比例4为不同pH值的水溶液对CDs和CDs-TC荧光强度的影响,得到的荧光信号示意图,如图4所示
对比例3
取20μL制备好的CDs原溶液放入1.5mL离心管中,然后向离心管中加入980μL配制好的不同pH值的水溶液混合均匀,在CDs最佳激发波长下用比色皿测定其荧光信号,从而得到不同pH值的水溶液对CDs荧光信号的影响。
对比例4
取250μL上述制备好的混合溶液放入离心管中,然后向离心管中加入5μL配好的12.5mM的四环素溶液,然后在混匀器上混匀5分钟,在CDs最佳激发波长下用比色皿测定荧光信号,从而得到不同pH值的水溶液对CDs-TC荧光信号的影响。
总结:通过对比例3-4,根据在不同pH值的水溶液中的所测得的CDs和CDs-TC的荧光信号值(如图4所示),可以看出,在3.0到10.0的pH值范围内没有观察到明显的荧光变化。这表明在宽的pH范围介质下,CDs和CDs-TC的荧光信号都可以保持稳定,即pH对CDs和CDs-TC的荧光信号几乎没有影响。
对比例5为盐浓度对CDs影响的荧光信号示意图,如图5所示。
取20μL制备好的CDs原溶液放入1.5mL离心管中,然后向离心管中加入980μL配制好的不同浓度的NaCl溶液混合均匀,在CDs最佳激发波长下用比色皿测定其荧光信号,从而得到不同浓度的盐溶液对CDs荧光信号的影响。
总结:通过对比例5,根据在不同浓度的NaCl溶液中所测得的CDs的荧光信号值(如图5所示),可以看出,NaCl溶液中CDs的荧光强度没有明显变化。实验数据表明,CDs具有很强的耐盐性。
对比例为6反应温度对合成CDs影响的荧光信号示意图,如图6所示。
对比例6
将4.8mg 3-氨基苯基硼酸和4.8mg柠檬酸溶解在5mL去离子水中,超声处理2分钟后将混合物转移至25mL聚四氟乙烯高压反应釜中,在真空干燥箱中分别在160,170,180,190,200℃加热6h。冷却至室温后,将获得的溶液在离心机中离心纯化5分钟以除去反应残余物和凝聚粒子获得上清液,用比色皿在CDs最佳激发波长下测定其荧光信号。
总结:由对比例6,根据在不同反应温度下合成的CDs所测得的荧光信号值(如图6所示),由图可以看出合成CDs的最佳反应温度为180℃。
对比例7为反应时间对合成CDs影响的荧光信号示意图,如图7所示。
将4.8mg 3-氨基苯基硼酸和4.8mg柠檬酸溶解在5mL去离子水中,超声处理2分钟后将混合物转移至25mL聚四氟乙烯高压反应釜中,在真空干燥箱中在180℃分别加热4、5、6、7、8h。冷却至室温后,将获得的溶液在离心机中离心纯化5分钟以除去反应残余物和凝聚粒子获得上清液,用比色皿在CDs最佳激发波长下测定其荧光信号。
总结:由对比例7,根据在不同反应时间下合成的CDs所测得的荧光信号值(如图7所示),由图可以看出合成CDs的最佳反应时间为6h。
对比例8为前驱体质量比对合成CDs影响的荧光信号示意图,如图8所示。
将柠檬酸和3-氨基苯基硼酸分别以质量比5:1、5:3、1:1(4.8g:4.8g)、3:5、1:5溶解在5mL去离子水中,超声处理2分钟后将混合物转移至25mL聚四氟乙烯高压反应釜中,在真空干燥箱中在180℃分别加热6h。冷却至室温后,将获得的溶液在离心机中离心纯化5分钟以除去反应残余物和凝聚粒子获得上清液,用比色皿在CDs最佳激发波长下测定其荧光信号。
总结:由对比例8,根据前驱体摩尔质量比合成的CDs所测得的荧光信号值(如图8所示),由图可以看出合成CDs的最佳前驱体质量比为1:1。
实施例2
用实施例1制备的四环素传感器。将250μM的四环素(TC),浓度均为500μM的牛血清白蛋白(BSA)、抗坏血酸(AA)、葡萄糖(Glu)、谷胱甘肽(GSH)、半胱氨酸(Cys)、丝氨酸(Ser)、赖氨酸(Lys)、苏氨酸(Thr)、组氨酸(His)、天冬氨酸(Asp)、Mg
实施例3
传感器的视觉模式
将实施例1采用滴涂法制备CDs/PVA复合膜作为四环素的视觉传感器。首先测试了CDs/PVA复合膜的荧光强度均匀性(如图10所示),发现CDs/PVA复合膜各处荧光强度几乎一样。接着研究了膜上CDs的负载量(1000μL/mL、800μL/mL、400μL/mL、100μL/mL,其中,PVA直接溶在1mLCDs原液中即为1000μL/mL,800μL/mL、400μL/mL、100μL/mL是指1mL溶液中CDs原液分别为800μL、400μL、100μL)对膜的荧光强度的影响,发现CDs的负载量较高时,蓝色荧光会更亮。因此,选择1000μL/ml CDs与PVA混合。随后将CDs负载量较高的CDs/PVA复合膜在浓度为0,0.01,0.05,0.1,0.5,1.0,2.0,5.0mg/mL的四环素溶液中浸泡10s,然后将它们晾干在紫外灯下拍照片,发现随着TC浓度的增加紫外灯下照片荧光强度逐渐减弱(如图10所示)。可以推断出CDs-PVA复合膜可用于在视觉模式下检测TC。此外,使用CDs-PVA膜检测牛奶样品中的TC。空白和不含TC的牛奶样品的CDs-PVA膜的荧光几乎相同。当将CDs-PVA膜浸入加有TC的牛奶样品中时,随着TC浓度的增加,荧光变化变弱。因此,该方法对牛奶中TC的检测具有良好的准确性和精确性,且具有广阔的应用前景。更重要的是简单便携,可在视觉模式下进行。
以上所述仅为本发明的优选实施例而已,并不用于限制本发明,对于本领域的技术人员来说,本发明可以有各种更改和变化。凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
- 基于掺杂碳量子点/PVA复合膜及其制备方法与检测四环素的应用
- 基于铕掺杂碳量子点比率荧光探针的四环素检测方法
