用于可充电电池单元的SO2基电解质和包括该SO2基电解质的可充电电池单元
文献发布时间:2023-06-19 12:02:28
技术领域
本发明涉及一种用于充电电池的SO
背景技术
可充电电池单元在很多技术领域都是非常重要的。可充电电池单元在很多情况下用于这样的应用场合,在所述应用场合中,仅需要具有相对较小的电流强度的小型可充电电池,如例如在使用移动电话的时候。但除此以外,对于用于高能应用的较大的可充电电池也存在很大的需求,其中以电池单元的形式大量存储能量对于车辆的电驱动是特别重要的。
对于这种可充电电池单元的一个重要的要求是具有高能量密度。这意味着,这种可充电电池单元的单位重量和单位体积应包含尽可能多的电能。为此,已经证明锂作为活性金属是特别有利的。可充电电池单元的活性金属是指这样的金属,所述金属的离子在所述电池充电或放电在电解质内部朝负极或正极迁移并在那里参与电化学过程。这些电化学过程直接或间接地导致向外部的电路释放电子或从外部的电路吸收电子。含有锂作为活性金属的可充电电池单元也称为锂离子电池。这种锂离子电池的能量密度可以通过提高电极的比容量或通过提高电池电压来提高。
锂离子电池的正极和负极均被设计为插入电极。在本发明的范围内,术语“插入电极”是指具有晶体结构的电极,在锂离子电池运行时活性金属的离子可以储存在晶体结构中或者从晶体结构中移出。这意味着,电极过程不仅可以在电极的表面上进行,而且也可以在晶体结构的内部进行。锂离子电池的负极包括碳涂层,所述碳涂层应用于由铜制成的导电元件上。所述导电元件提供了碳涂层和外部电路之间所需的电子导电连接。正极含有钴酸锂(LiCoO
电解质是每种充电电池的重要功能元件。所述电解质包含溶剂或溶剂混合物以及至少一种导电盐。固态电解质或离子液体不包含例如溶剂,而是仅包含导电盐。所述电解质与电池的正极和负极接触。导电盐中的至少一种离子(阴离子或阳离子)能在电解质中充分移动,从而可以通过离子传导在电极之间可以进行可充电电池功能所需的电荷传输。电解质在可充电电池单元的某一较高电压下被氧化电化学分解。这个过程通常会导致电解质组分发生不可逆的破坏并且由此导致可充电电池单元失效。当低于一定的电池电压时,还原过程也可以使得电解质分解。为了避免这种过程,正极和负极的选择应使得电池电压低于或高于电解质的分解电压。因此,电解质决定电压窗口,在所述电压窗口中,可充电电池单元能够可逆地运行。
现有技术已知的锂离子电池包含电解质,所述电解质由有机溶剂或溶剂混合物,以及溶解在其中的导电盐组成。所述导电盐是一种锂盐,如例如六氟磷酸锂(LiPF
因此,有机锂离子电池在稳定性以及长期运行安全性上存在问题。安全性风险特别也是由于有机溶剂或溶剂混合物的可燃性造成的。当有机锂离子电池着火或者甚至爆炸时,则电解质中的有机溶剂形成可燃物。为了避免出现此类安全性风险,必须采取其他的措施。这些措施尤其是包括非常精确地调节有机锂离子电池的充电和放电过程,以及优化电池结构。此外,所述有机锂离子电池还包括这样的组件,所述组件在温度意外升高时熔化,并且此时熔融塑料充满有机锂离子电池。由此避免了进一步不可控的升温。但这些措施导致增加了有机锂离子电池制造中的生产成本,并且导致增加了体积和重量。此外,这些措施降低了有机锂离子电池的能量密度。
有机锂离子电池的另一个缺点在于,在存在剩余水量时可能产生的任何水解产物对可充电电池单元的电池组件具有非常强的侵蚀性。例如对于通常在有机电池中使用的导电盐LiPF
因此,由现有技术已知的继续改进提供了使用基于二氧化硫(SO
例如,EP 1 201 004 B1公开了一种组成为LiAlCl
EP 2534719 B1公开了一种主要以LiAlCl
SO
表1:不同的盐在SO
发明内容
为了进一步改善SO
-具有宽的电化学窗口,从而在正极上不会出现氧化性电解质分解;
-在负极上构成稳定的涂覆层,所述涂覆层容量应较低,并且在进一步的运行中器件不会在负极上出现另外的还原性电解质分解;
-宽的电化学窗口为可充电电池单元使用高压阴极来运行提供了可能性;
-对于导电盐具有良好的溶解性,因此是良好的离子导体和电子绝缘体,从而促进离子传输并且可以将自放电限制在最低;
-相对于可充电电池单元的其他部组件(例如隔板、电极材料和电池包装材料)也是惰性的;
-能够抵抗例如电、机械或热的各种类型的不当使用;以及
-对于可充电电池单元的电池组件中的残留水量具有更高的稳定性。
这种电解质尤其适用于同时具有非常好的电能及功率数据、高运行可靠性和使用寿命,特别是大量的可用充电及放电循环的可充电电池单元中,而此时电解质在可充电电池单元的运行过程中不会分解。
另一方面,本发明的目的在于提供一种可充电电池单元,所述可充电电池单元包括SO
-改善的电气性能数据,特别是高能量密度;
-改善的过度充电性能和深度放电性能;
-较少的自放电;
-提高的使用寿命,特别是高的可用的充电及放电循环数;
-较小的总重量;
-提高的运行安全性,即使车辆在较为恶劣的环境条件下;以及
-降低的生产成本。
所述目的通过一种具有权利要求1的特征的SO
根据本发明的用于可充电电池单元的SO
式(I)
式(I)中:M是选自由碱金属、碱土金属、元素周期表第12族的金属和铝组成的组的金属。x是1至3的整数。取代基R
根据本发明的SO
在本发明的理解中,术语“C
在本发明的理解中,术语“C
在本发明的理解中,术语“C
在本发明的理解中,术语“C
在本发明的理解中,术语“C
在本发明的理解中,术语“C
这种电解质与现有技术已知的电解质相比的优点是,其含有的第一导电盐具有较高的氧化稳定性,因此在较高的电池电压的情况下基本上不会发生分解。这种电解质优选至少达到4.0V的电位,更为优选地至少达到4.2V的电位,更为优选地至少达到4.4V的电位,更为优选地至少达到4.6V的电位,更为优选地至少达到4.8V的电位,更为优选地至少达到5.0V的电位都是氧化稳定的。由此,在将这种电解质应用在可充电电池单元中时,在充电电池的两个电极的工作电位之内几乎没有或者没有电解质分解。因此,与现有技术已知的电解质相比,这明显延长了电解质的使用寿命。此外,这种电解质还是耐低温的。与现有技术已知的SO
本发明的另一个方面提供一种可充电电池单元。这种可充电电池单元包含上述的根据本发明的电解质,或者含有下述的根据本发明的电解质的有利实施方式。此外,根据本发明的可充电电池单元包括活性金属、至少一个正极、至少一个负极和壳体。
在根据本发明的电解质的第一种有利的实施方式中,取代基R
-C
-C
-C
-C
-苯基;和
-C
在根据本发明的电解质的这种有利的实施方式的情况下,术语“C
在根据本发明的电解质的这种有利的实施方式的情况下,术语“C
在根据本发明的电解质的这种有利的实施方式的情况下,术语“C
在根据本发明的电解质的这种有利的实施方式的情况下,术语“C
在根据本发明的电解质的这种有利的实施方式的情况下,术语“C
为了提高第一导电盐在SO
可以使所述取代基R
在根据本发明的电解质的另一种有利的实施方式中,所述第一导电盐选自以下组,该组由以下所示组成:
为了将电解质的电导率和/或其他特性调节到期望值,在一种有利的实施方式中,所述电解质含有至少一种与根据式(I)的第一导电盐不同的第二导电盐。这意味着,除了第一导电盐,所述电解质还可以含有另一种或多种的第二导电盐,所述第二导电盐的化学组成以及化学结构与第一导电盐不同。
在根据本发明的电解质另一种有利的实施方式中,所述第二导电盐是碱金属化合物,特别是锂化合物。所述碱金属化合物或锂化合物选自由铝酸盐、卤化物、草酸盐、硼酸盐、磷酸盐、砷酸盐和没食子酸盐组成的组。所述第二导电盐优选为四卤化铝酸锂,特别是LiAlCl
此外,在一种有利的实施方式中,所述电解质包含至少一种添加剂。所述添加剂选自由碳酸亚乙烯酯及其衍生物(vinylene carbonate and its derivatives)、碳酸乙烯亚乙酯及其衍生物(vinylethylene carbonate and its derivatives)、碳酸甲基亚乙酯及其衍生物(methylethylene carbonate and its derivatives)、(双草酸)酸硼酸锂(lithium(bisoxalato)borate)、二氟(草酸)硼酸锂(lithium difluoro(oxalato)borate)、四氟(草酸)磷酸锂(lithium tetrafluoro(oxalato)phosphate)、草酸锂(lithium oxalate)、2-乙烯基吡啶(2-vinylpyridine)、4-乙烯基吡啶(4-vinylpyridine)、环状外亚甲基碳酸酯(cyclic exomethylene carbonates)、磺酸内酯(sultones)、环状和非环状磺酸酯(cyclic and acyclic sulfonates)、非环状亚硫酸酯(acyclic sulfites)、环状和非环状亚磺酸酯(cyclic and acyclic sulfinates)、无机酸的有机酯(organic esters of inorganic acids)、环状和非环状烷烃(acyclic andcyclic alkanes),其中所述环状和非环状烷烃在1bar下的沸点至少为36℃、芳族化合物(aromatic compounds)、卤代环状和非环状磺酰亚胺(halogenated cyclic and acyclicsulfonylimides)、卤代环状和非环状磷酸酯(halogenated cyclic and acyclicphosphate esters)、卤代环状和非环状膦(halogenated cyclic and acyclicphosphines)、卤代环状和非环状亚磷酸酯(halogenated cyclic and acyclicphosphites)、卤代环状和非环状磷腈(halogenated cyclic and acyclicphosphazenes)、卤代环状和非环状硅胺(halogenated cyclic and acyclicsilylamines)、卤代环状和非环状卤代酯(halogenated cyclic and acyclichalogenated esters),卤代环状和非环状酰胺(halogenated cyclic and acyclicamides)、卤代环状和非环状酸酐(halogenated cyclic and acyclic anhydrides)和卤代有机杂环(halogenated organic heterocycles)组成的组。
在另一种有利的实施方式中,相对于电解质组成的总重量所述电解质具有以下组成:
(i)5至99.4重量%的二氧化硫,
(ii)0.6至95重量%的第一导电盐,
(iii)0至25重量%的第二导电盐,以及
(iv)0至10重量%的添加剂。
如上所述,电解质不仅可以包括根据式(I)的第一导电盐和第二导电盐,还可以包含根据式(I)的多种第一导电盐和多种第二导电盐。在后面一种情况下,上述的百分比也包括多种第一导电盐和多种第二导电盐。以电解质总体积的为基准,第一导电盐的摩尔浓度在0.05mol/L至10mol/L的范围内,优选地在0.1mol/L至6mol/L的范围内,特别优选地在0.2mol/L至3.5mol/L的范围内。
根据本发明的可充电电池单元的另一种有利的实施方式中提供了,相对于每摩尔导电盐,所述电解质含有至少0.1mol的SO
SO
基于可充电电池单元中含有的电解质的总量,所述电解质可以含有至少5重量%的SO
在本发明的范围内,所述电解质优选仅具有很小百分比的或者甚至完全没有百分比的至少一种有机溶剂。优选电解质中的例如一种溶剂或多种溶剂的混合物的形式存在的有机溶剂的比例为电解质重量的最高50重量%。特别优选的是,电解质重量的最高40重量%、最高30重量%、最高20重量%、最高15重量%、最高10重量%、最高5重量%或最高1重量%的较小比例是优选的。更为优选的是,所述电解质不含有机溶剂。由于有机溶剂的比例较低或者甚至完全不存在,所述电解质几乎是不可燃的或者根本不可燃的。这提高了利用这种SO
活性金属
下面说明根据本发明的可充电电池单元在活性金属方面的有利的改进方案:
在所述可充电电池单元的第一种有利的改进中,所述活性金属是:
-碱金属,特别是锂或钠;
-碱土金属,特别是钙;
-元素周期表第12族的金属,特别是锌;或者
-铝。
负极
下面说明根据本发明的可充电电池单元在负极方面的有利的改进:
所述可充电电池单元的一种有利的改进提供了所述负极是插入电极。所述插入电极优选包含作为活性材料的插入材料,在所述插入材料中,活性金属的离子在给所述可充电电池单元充电时被存储在插入材料中,并且在所述可充电电池单元放电时可以从插入材料中移除。这意味着电极过程不仅可以在负极的表面上进行,而且也可以在负极的内部进行。例如,如果使用基于锂的导电盐,则在给可充电电池单元充电期间锂离子可以储存在材料中,并且在所述可充电电池单元放电期间从所述插入材料中移除。所述负极优选包括碳作为活性材料或嵌入材料,特别是同素异形体石墨形式的碳。但也在本发明范围内的是,所述碳以天然石墨(絮状或圆形)、合成石墨(中间相石墨)、石墨化的中间相碳微球(MCMB)、具有碳涂层的石墨或无定形碳的形式存在。
在根据本发明的可充电电池单元的另一种有利的改进方案中,所述负极包括不含碳的嵌锂阳极活性材料,例如是钛酸锂(例如Li
根据本发明的可充电电池单元的另一种有利的改进提供了,含有锂的负电极包括形成合金的阳极活性材料。这种材料例如是储锂的金属和金属合金(例如Si、Ge、Sn、SnCo
在根据本发明的可充电电池单元的另一个有利的改进中,所述负极包含转化阳极活性材料。所述转化阳极活性材料可以例如是过渡金属氧化物,例如为锰氧化物(MnO
在根据本发明的可充电电池单元的另一种有利的改进中,所述负极包括金属,特别是金属锂。
根据本发明的可充电电池单元的另一种有利的改进提供了,所述负极是多孔的,此时,孔隙率优选最高为50%、更优选最高为45%、更优选最高为40%、更优选最高为35%、更优选最高为30%、更优选最高为20%、更优选最高为10%。孔隙率表示空腔体积占负极总体积的比值,所述空腔体积由所谓的孔或空腔构成。这种孔隙率会导致负极的内表面扩大,此外,所述孔隙率降低了负极的密度并且由此还减小了其重量。负极的各个孔在运行中优选完全被电解质填充。
根据本发明的充电电池的另一种有利的改进提供了所述负极具有放电元件。这意味着,所述负极除了所述活性材料或插入材料还包括放电元件。所述放电元件用于实现负极的活性材料的必要的电子导电连接。为此,所述放电元件与参与负极的电极反应的活性材料接触。所述放电元件可以被构造成薄金属片或薄金属箔的平面形式。所述薄金属箔优选具有穿孔结构或网状结构。优选地将负极的活性材料涂覆到所述薄金属片或薄金属箔的表面上。这种平面放电元件的厚度在5μm至50μm的范围内。平面的放电元件的厚度优选在10μm至30μm的范围内。在使用所述平面的放电元件时,所述负极可以具有至少20μm、优选至少40μm,并且特别优选至少60μm的总厚度。最大厚度为200μm以下、优选为150μm以下并且特别优选为100μm以下。在使用平面的放电元件时,负极的面积比容量优选至少为0.5mAh/cm
此外,也存在这样的可能性,即,所述放电元件可以以多孔金属,特别是金属泡沫的形式构造成三维的。术语“三维多孔的金属结构”这里是指任意由金属组成的结构,所述结构不仅如薄金属片或金属箔在平面电极的长度和宽度上延伸,而且也在其厚度尺寸上延伸。三维多孔金属结构具有足够多的孔,使得可以将负极的活性材料引入所述金属结构的孔中。所引入或施加的活性金属的量是负极的负载量。当放电元件被三维构造成多孔金属结构的形式,特别是以金属泡沫的形式时,则负极优选具有至少0.2mm,优选至少0.3mm,更为优选至少0.4mm,更为优选至少0.5mm,并且特别优选至少0.6mm的厚度。在这种情况下,与在有机锂离子电池中使用的负极相比,电极的厚度明显更大。一种有利的实施方式提供了,在使用金属泡沫形式的三维的放电元件时,负极的面积比容量优选至少为2.5mAh/cm
在根据本发明的电池的另一种有利的改进中,所述负极具有至少一种粘结剂。粘结剂优选是氟化粘结剂,特别是聚偏氟乙烯和/或由四氟乙烯、六氟丙烯和偏氟乙烯组成的三元聚合物。但也可以是由聚合物组成的粘结剂,所述聚合物由共轭羧酸,或由共轭羧酸的碱金属(alkali)、碱土金属(alkaline earth)或铵盐,或者由它们的组合的单体结构单元构建而成。此外,所述粘结剂也可以由基于单体苯乙烯和丁二烯结构单元的聚合物组成。此外,所述粘结剂也可以是包含羧甲基纤维素类的粘结剂。以正极的总重量为基准,所述粘结剂在负极中的浓度优选地最高为20重量%,更优选地最高为15重量%,更优选地最高为10重量%,更优选地最高为7重量%,更优选地最高为5重量%,最优选地最高为2重量%。
正极
下面说明根据本发明的可充电电池单元在正极方面的有利的改进:
在根据本发明的电池的另一种有利的改进方案中,正极包含至少一种作为活性材料的插层化合物。在本发明的范围内术语“插层化合物”是指前述的插入材料的一个子类别。插层化合物用作主体基质,所述主体基质具有彼此连接的空位。在可充电电池单元的放电过程中,活性金属的离子能够扩散到这些空位中并且能够存储在这些空位中。在活性金属的离子的这种掺入的情况下,主体基质仅发生很小的结构变化或完全不发生结构变化。所述插层化合物优选具有Li
-M'是至少一种选自由以下元素:Ti、V、Cr、Mn、Fe、Co、Ni、Cu和Zn组成的组中的金属;
-M”是至少一种选自由元素周期表中的第2族、第3族、第4族、第5族、第6族、第7族、第8族、第9族、第10族、第11族、第12族、第13族、第14族、第15族和第16族的元素组成的组中的元素;
-x和y大于0,
-z大于或等于0,以及
-a大于0。
标记y和z分别表示以M'或M”所代表的金属和元素的总量。例如M'包括两种金属M'
式Li
根据本发明的充电电池的另一种有利的改进提供了,M'由金属镍和锰组成,而M”是钴。此时,这涉及式Li
在根据本发明的可充电电池单元中,高压电极可以至少以高达4.0V的高电位、更为优选至少以高达4.2V的高电位、更为优选至少以高达4.4V的高电位、更为优选至少以高达4.6V的高电位、更为优选至少以高达4.8V的高电位和特别优选至少以高达5.0V的高电位循环运行。
根据本发明的可充电电池单元的另一种有利的改进提供了,所述正极至少包含一种选自由金属氧化物、金属卤化物和金属磷酸盐组成的组中的金属化合物,所述金属化合物的金属优选是元素周期表中原子序数为22至28的过渡金属,特别是钴、镍、锰或铁。
根据本发明的可充电电池单元的另一种有利的改进中提供了,所述正极具有放电元件。这意味着,所述正极除了所述活性材料还包括放电元件。所述放电元件用于实现正极的活性材料所需的电子导电连接。为此,所述放电元件与参与正极的电极反应的活性材料接触。
所述放电元件可以平面式地构造成薄金属片或薄金属箔的形式。所述薄的金属箔优选具有穿孔的或网状的结构。正极的活性材料优选涂覆到所述薄金属片或薄金属箔的表面上。这种平面放电元件的厚度在5μm至50μm的范围内。平面放电元件的厚度优选在10μm至30μm的范围内。在使用所述平面放电元件时,所述正极的总厚度可以至少为20μm,优选至少为40μm并且特别优选至少为60μm。最大厚度最高为200μm,优选最高为150μm并且特别优选最高为100μm。在使用平面放电元件时,负极的面积比容量优选至少为0.5mAh/cm
此外,正极的放电元件也可能被设计为三维多孔金属结构的形式,特别是金属泡沫的形式。三维多孔金属结构孔隙丰富,因此可以将正极的活性材料掺入所述金属结构的孔中。所引入或施加的活性材料的量为正极的负载量。当放电元件被设计为三维多孔金属结构的形式,特别是以金属泡沫的形式时,则正极优选具有至少0.2mm、优选至少0.3mm、更为优选至少0.4mm、更为优选至少0.5mm并且特别优选至少0.6mm的厚度。另一种有利的实施方式设定,在使用金属泡沫形式,特别是金属泡沫形式的三维放电元件时,正极的面积比容量优选至少为2.5mAh/cm
在根据本发明的电池的另一种有利的改进中,所述正极含有至少一种粘结剂。这种粘结剂优选是氟化粘结剂,特别是聚偏二氟乙烯和/或由四氟乙烯、六氟丙烯和偏氟乙烯形成的三元聚合物。但也可以是由聚合物形成的粘结剂,所述聚合物由共轭羧酸的单体结构单元或由共轭羧酸的碱金属盐、碱土金属盐或铵盐,或由其组合构成。此外,所述粘结剂也可以由聚合物组成,所述聚合物基于单体苯乙烯结构单元和丁二烯结构单元。此外,所述粘结剂也可以是选自羧甲基纤维素类的粘结剂。以正极的总重量为基准,所述粘结剂优选以最高20重量%,更优选最高15重量%,更优选最高10重量%,更优选最高7重量%、更优选最高5重量%、更优选最高2重量%的浓度存在。
可充电电池单元的结构
下面说明根据本发明的可充电电池单元在其构造方面的有利的改进:
为了改进所述可充电电池单元的功能,根据本发明的可充电电池单元另一种有利的改进提供了,所述充电电池包括多个负极和多个正极,所述负极和正极交替堆叠地设置在壳体中。此时,所述正极和负极优选分别通过隔膜相互电隔离。
所述隔膜可以由无纺布、膜、编织材料、针织材料、有机材料、无机材料或这些材料的组合构成。有机隔膜可以由未取代的聚烯烃(例如聚丙烯或聚乙烯)、部分至完全被卤素取代的聚烯烃(例如部分至完全被氟取代,特别是PVDF、ETFE、PTFE)、聚酯、聚酰胺或聚砜组成。包含有机和无机材料组合的隔膜例如是玻璃纤维纺织材料,在所述玻璃纤维织物中,玻璃纤维具有适当的聚合物涂层。所述涂层优选含有含氟聚合物,如例如聚四氟乙烯(PTFE)、乙烯-四氟乙烯共聚物(ETFE)、全氟乙烯丙烯(FEP)、THV(四氟乙烯、六氟丙烯和偏二氟乙烯的三元共聚物)、全氟烷氧基聚合物(PFA)、氨基硅烷、聚丙烯或聚乙烯(PE)。所述隔膜也可以折叠地存在与充电电池的壳体中,例如以所谓的“Z形折叠”的形式。对于这种Z形折叠,条状的隔膜以z形的方式通过或者绕所述电极地折叠。此外,所述隔膜也可以构造成隔膜纸。
在本发明的范围内的是,所述隔膜可以构造成护套,其中每个正极或每个负极都由所述护套包裹。所述护套可以由无纺布、膜、编织材料、针织材料、有机材料、无机材料或这些材料的组合构成。
正极的护套实现了可充电电池单元中均匀的离子迁移和离子分布。离子分布越均匀,特别是在负极中,负极可能的负载的量活性材料就越高,因此可充电电池单元的可用容量可以更高。同时,避免了可能与负载不均匀以及由此产生的活性金属沉积相关的风险。当可充电电池单元的正极用护套包裹时,这些优点主要起作用。
优选地,电极的面积尺寸和包套可以相互匹配,使得电极的护套的外部尺寸和没有护套的电极的外部尺寸至少在一个维度上匹配。
护套的面积优选可以大于电极的面积。在这种情况下,护套延伸超过电极的边界。覆盖在所述电极两侧的两层护套因此可以通过边缘连接在正极的边缘相互连接。
在根据本发明的可充电电池单元的另一种有利的实施方式中,负极具有护套,而正极不具有护套。
下面参考附图、实施例和实验来更详细地说明和解释本发明的其他有利的特性。
附图说明
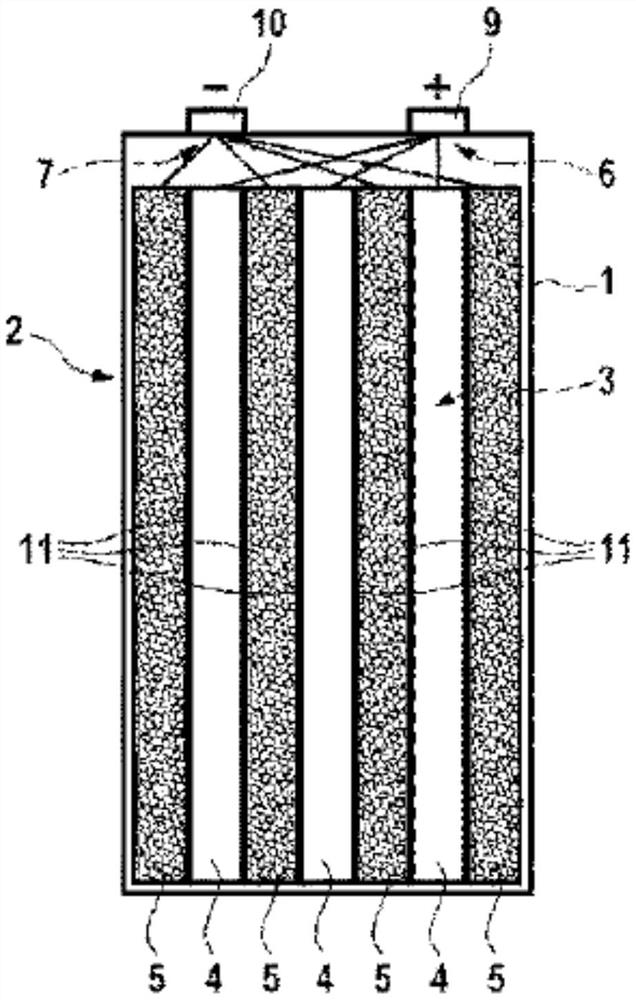
图1:示出了根据本发明的可充电电池单元的第一实施例的横截面图;
图2作为详细说明,示出图1的第一实施例的金属泡沫的三维多孔结构的电子显微图;
图3:示出了根据本发明的可充电电池单元的第二实施例用横截面图;
图4:示出了图3的第二实施例的细节;
图5:示出了根据本发明的可充电电池单元的第三实施例的分解图;
图6:示出了测试全电池的放电容量与循环次数的函数关系,所述测试全电池包括由化合物1和参比电解质组成的混合电解质,或由化合物3和参比电解质组成的混合电解质,或者包含所述对照电解质;
图7:伏特[V]为单位示出了充电电位和放电电位与测试全电池的电量百分比的函数关系,测试全电池填充有根据本发明的电解质的三个实施例1、2或3之一或者参比电解质;
图8:以伏特[V]为单位示出了测试全电池的电量百分比与电位的函数关系,测试全电池填充有根据本发明的第一实施例1的电解质;
图9:以伏特[V]为单位示出了充电/放电电流与测试全电池的累计电量的函数关系,测试全电池填充有根据本发明的第三实施例3的电解质;
图10:示出了参比全电池和测试全电池的放电容量的平均值与循环次数的函数关系,所述参比全电池填充有参比电解质,所述测试全电池填充有根据本发明的第一实施例1的电解质;
图11:示出了图10的两个全电池的内阻与循环次数的函数关系;
图12:示出了根据本发明的第一实施例1的电解质电导率[mS/cm]与浓度的函数关系;以及
图13:示出了当负极对锂充电时,参比全电池和两个测试全电池的电位[V]与电容的函数关系,所述容量与在负极表面形成涂层过程中负极的理论容量有关。
具体实施方式
图1示出根据本发明的可充电电池单元2的第一实施例的横横截面图。这个可充电电池单元2构造成棱柱形电池并且主要具有壳体1。所述壳体1包围电极阵列3,所述电极阵列包括三个正极4和四个负极5。正极4和负极5在所述电极阵列3中交替堆叠地设置。但壳体1还可以容纳更多正极4和/或负极5。通常优选的是,负极5的数量比正极4的数量多一个。这使得电解叠层的外端面由负极5的电极表面形成。电极4、5通过电极端子6、7与可充电电池单元2的相应的连接触点9、10连接。可充电电池单元2用SO
在本实施例中,电极4、5构造为扁平的,就是说构造成相对于表面积而言具有较小厚度的层。这些电极分别通过隔膜11相互分隔。可充电电池单元2的壳体1构造成基本上是长方体,其中,电极4、5和壳体1在横截面图中示出的壁垂直于图平面延伸,并且基本上直的和平坦的。但可充电电池单元2也可以构造成卷绕电池,其中电极由薄层构成,该薄层与隔离材料卷绕在一起。隔膜11一方面在空间上和电学上将正极4与负极5分开,并且另一方面特别是对活性材料的离子是可透过的。以这种方式形成了较大的电化学有效的表面,这种表面实现了相应地高的电流输出。
电极4、5还具有在图1中未示出的放电元件,所述放电元件用于实现相应电极的活性材料的电子导电连接。所述放电元件与参与相应电极4、5的电极反应的活性材料(在图1中未示出)相接触。所述放电元件构造成多孔金属泡沫的形式。金属泡沫在电极4、5的厚度尺寸上延伸。正极4和负极5的活性材料被引入金属泡沫的孔隙中,从而所述活性材料在这种金属结构的整个厚度上均匀地填充金属泡沫的孔。为了提高机械强度,所述正极4包含粘结剂。所述粘结剂是含氟聚合物。负极5包含作为活性材料的碳,碳以适于作为吸收锂离子的插入材料的形式存在。负极5的结构类似于正极4。
图2示出了图1的第一实施例的金属泡沫18的三维多孔结构的电子显微镜图像。根据所给出比例可以看出,孔P的平均直径大于100μm,这意味着是相对较大的。
图3示出了根据本发明的可充电电池单元3的第二实施例用横截面图。所述第二实施例与在图1中示出的第一实施例的区别在于,电极阵列3包括一个正极4和两个负极5。该正极4具有平面金属箔形式的放电元件34,在所述放电元件的两侧涂覆正极4的活性材料24。负极5还包括平面金属箔形式的放电元件35,在所述放电元件的两侧涂覆负极4的活性材料25。可选地,边缘电极,即封闭电极堆的电极的平面的放电元件可以仅在一侧涂覆活性材料。未涂覆的一侧朝向壳体的壁。
图4示出了平面的金属箔,所述金属箔分别用作图3的第二实施例中的正极4和负极5的放电元件34、35。所述金属箔具有厚度为20μm的穿孔的或网状的结构。
图5示出了根据本发明的可充电电池单元2的第三实施例的分解图。所述第三实施例与上述两个实施例的区别在于,正极4被护套13包围。其中,护套13的表面积大于正极4的表面积,其边界14在图2中用虚线示出。护套13在两侧覆盖正极4的涂层15、16上通过边缘连接结构17在正极4的圆周边缘相互连接。
用于下面描述的示例的对照电解质根据在专利文献EP 2 954 588B1中记载的方法来制备。首先在120℃下真空中将氯化锂(LiCl)干燥三天。在450℃下真空中将铝颗粒(Al)干燥两天。将LiCl、氯化铝(AlCl
为了进行下述实验,制备了根据本发明的电解质的三个实施方案1、2和3(下面称为电解质1、2和3)。为此,首先根据以下文献中描述的制备方法来制备了三种不同的根据式(I)的第一导电盐:
“I.Krossing,Chem.Eur.J.2001,7,490;
S.M.Ivanova et al.,Chem.Eur.J.2001,7,503;
Tsujioka et al.,J.Electrochem.Soc.,2004,151,A1418”
这三种不同的根据式(1)的第一导电盐在下文称为化合物1、2和3。这些化合物源自多氟烷氧基铝酸盐(Polyfluoroalkoxyaluminate)族,并且根据下面的反应式基于LiAlH
由此,形成了下面用总和或结构式示出的化合物1、2和3:
首先使化合物1、2和3重结晶以纯化。由此从第一导电盐中去除反应物LiAlH
此后,实现化合物1、2和3在SO
在低温下或在加压下按照下面列出的方法步骤1至4进行电极1、2和3的制造:
1)将相应的化合物1、2和3分别置于具有立管的压力活塞中,
2)抽出压力活塞,
3)使液态SO
4)重复步骤2+3,直至加入目标量的SO
除非在实验说明中另行说明,在电解质1、2和3中的化合物1、2和3各自的浓度为1mol/L(相对于1升电解质的摩尔浓度)。下述实验采用电解质1、2和3和参比电解质进行。
在下述试验中使用的全电池是具有两个负极和一个正极的可充电电池单元,所述负极和正极分别通过隔膜分开。正极具有作为活性材料的LiFePO
对于每个实验制造多个,即二至四个相同的全电池。实验所示的结果分别是由来自相同的全电池获得的测量值的平均值。
为了测试根据本发明的电解质对于全电池的循环性能的不利影响,首先制造混合电解质,所述混合电解质在参比电解质中含有少量的化合物1或化合物3。
为此,制备了由95重量%(wt%)的参比电解质和5wt%的化合物1或5wt%的化合物2组成的混合电解质。将这两种混合电解质与纯的参比电解质(100wt%)进行比较。为此,在根据实施例3的全电池中进行试验。为此,给全电池分别填充不同的电解质。以50mA的电流给所述全电池充电至3.6V的电位。保持3.6V的电位直至电流降低到40mA。以50mA的电流进行放电直到2.5V的电位。进行500次的充/放电循环。图6示出三个放电曲线,即放电容量与循环次数的函数关系。所有电解质表现出接近相同的放电容量变化过程。
由此可知,电解质1和3以及根据式(I)的第一导电盐对于循环性能没有产生任何严重的不利影响。
采用实施例1中制备的参比电解质和实施例2中制备的电解质1、2或3,在根据实施例3中制备的全电池中进行实验。参比电解质以及电解质1、2和3的导电盐的浓度分别为0.6mol/L的。用电解质填充四个全电池。以50mA的电流给这些全电池进行充电到3.6V的电位。保持3.6V的电位直到电流降低到40mA。以50mA的电流进行放电到2.5V的电位。图7在上部区域中示出了参照左侧y轴的示出刻度的充电曲线,在下部区域中示出了参照右侧y轴示出刻度的放电曲线。使用电解质1、2和3,全电池可以再次充电和放电。
为了验证电解质1、2和3的高压性能,在根据实施例3的全电池中进行实验。用在实施例2中提供的电解质填充所述全电池,以1升的电解质为基准,所述电解质含有作为第一导电盐的摩尔浓度为1mol/L的化合物1。
图8示出了上述全电池的电位(以[V]为单位)相对于电量百分比变化的曲线,该电量百分比是相对于全电池最大电量的百分比。用50mA的电流将所述全电池充电到5V的电位。保持这个电位直到充电电流降低到40mA。此后以50mA的电流进行放电到2.5V的放电电位。图6示出在本实验3中全电池的充/放电曲线。循环效率大于99.5%。这意味着,电解质的副反应或过充反应没有消耗掉容量。电解质1在这个电位范围内是稳定的。由此可以得出结论,含有第一导电盐的电解质能够用于出现高电池电压的高能电池,而第一导电盐不会在此过程中发生分解。
再次重复充/放电实验3,区别是,充电电位上限以0.2V的步长从3.6V增加到5.0V。就是说进行了8个循环。表2示出了在每种情况下分别达到的循环效率。
表2:与充电电位相关的循环效率
所达到的循环效率对于每个充电电位都相同,并且在高达5V的整个电位范围内电解质1都表现出稳定的特性。
在循环试验中将根据本发明的电解质3与参比电解质相比较。为此,使用三个如实施例3中所述的全电池。一个全电池填充参比电解质,给两个全电池填充电解质3。所述全电池的充电至3.6V的电位,并放电至2.5V。具有参比电解质的全电池以100mA的电流运行,适用较小的电导率的两个具有电解质3的全电池,分别以10mA或5mA充电或放电一次,并以5mA充电或放电一次。图9示出了所得到的充/放电曲线。所有的全电池都表现出稳定的充电和稳定的放电。在电流较小时,电解质3可达到的容量提高。
在本实验中,研究了作为在现有技术中使用的参比电解质的替代方案的根据本发明的电解质的用途。
本实验同样在实施例3中所述的全电池中进行。所述全电池用参比电解质(下面称为参比全电池)填充,或者用上述的根据本发明的电解质1(下面称为测试全电池)填充。因此参比全电池和测试全电池仅在所使用的电解质的类型方面有所不同。
从形成循环开始进行了多个循环试验。表3示出了在两种全电池在充电或放电中相应使用的充电或放电电流和最终充电或放电电压。此外,还给出了在最终充电电压为3.6V时充电电流(I
表3:循环实验数据
图10示出了作为循环次数的函数的这两种全电池的放电容量的平均值。具有长线条的虚线表示测试全电池的放电容量的平均值。为此使用了来自三次相同的测量得到的平均值。带有短线条的虚线表示参比全电池的放电容量。为此,使用了来自两次相同的测量得到的平均值。
放电容量的这些平均值分别用额定容量的百分比来表示。所述额定容量这样来获得:将正极的理论容量减去在第一次循环中在负极上形成覆盖层所消耗的容量。所述覆盖层在全电池首次充电时在负极上形成。覆盖层的形成会不可逆地消耗锂离子,从而相应的全电池可用于后续循环的循环容量较少。
两种全电池的放电容量的起始值约为额定容量的90%。两种全电池的放电容量随着循环次数增加而降低。到第500次循环时,参比全电池的容量下降了19%,剩余容量为71%。在第500次循环后,测试全电池的容量下降了22%,剩余容量为68%。从300次循环起,两条曲线的容量变化进程近似平行,并且表明有更为稳定的增长。两种全电池的特性是类似的,并且表明根据本发明的电解质可以用作参比电解质的替代方案。
实验6还示出了两种全电池的内阻随循环次数的变化过程,而图11示出了对于测试全电池以及测试全电池的结果。内阻是由于全电池的结构引起的全电池内部的损耗因子。在参比全电池的内阻略高于0.2Ohm。测试全电池开始时表现出约0.95Ohm的较高内阻,但从约第200次循环起所述内阻稳定地为0.8Ohm。
这些结果符合申请人的预期,因为在根据本发明使用的具有较大阴离子的电解质中锂离子传导性会变得略微困难。
为了确定电导率,制备具有不同化合物1的浓度的电解质1。对于化合物1的每个浓度,使用导电测量的方法确定电解质1的电导率。在控温后,将双电极传感器与溶液保持接触,并且在0至50mS/cm的测量范围内进行测量。表4示出不同的浓度、相应的SO
表4:电导率与电解质1中化合物1浓度的函数关系
图12示出了电解质1的电导率随化合物1的浓度的变化。可以看到,在化合物1的浓度为0.6mol/L时,电导率具有24.7mS/cm的最大值。与此相比,由现有技术已知的有机电解质,如例如LP30(1M LiPF6/EC-DMC(1:1重量))仅具有约10mS/cm的电导率。
在该实验中,研究了在第一次循环中用于在负极上形成覆盖层所消耗的容量。这个覆盖层在首次给全电池充电时在负极上形成。形成覆盖层不可逆地消耗锂离子,因此全电池可用于后续的循环的循环容量较少。
参比电解质、电解质1和电解质3均在该实验的全电池中进行检测。该结构对应于在示例3中所述的结构。在第一个实验中使用的参比电解质具有组成:LiAlCl
图13示出了当负极对锂充电时全电池的电位(以伏特为单位)与容量的函数关系,所述容量与负极的理论容量有关。这里,点状虚线示表示参比电解质的结果,而短划状虚线或实线表示根据本发明的电解质1和3的结果。所示出的三条曲线分别示出利用前面所述的全电池进行的多个实验的平均结果。首先用15mA的电流给全电池充电,直至达到125mAh的容量(Q
根据以下公式计算用于在负极上形成覆盖层的理论容量的百分比:
覆盖层的容量=(Q
Q
实验9:低温特性
为了确定与参比电解质相比,根据本发明的电解质的低温特性,将两个如实验1中所述的全电池一个用参比电解质填充,而另一个用电解质1填充。在20℃给两个全电池充电并再次放电。将所达到的放电容量作为100%。以10℃的温度步长降低全电池的温度并分别再次进行充/放电循环。得到的放电容量用20℃时的放电容量的百分比来表示。结果如表5所示。
表5:放电容量随温度的变化
具有电解质1的全电池表现出良好的低温特性。在-10℃时仍达到61%的容量,在-20℃时仍有31%。即使在-30℃仍能小部分放电。与此相反,具有参比电解质的全电池仅在-10℃还表现出放电能力。此时为21%的容量。
- 用于可充电电池单元的SO2基电解质和包括该SO2基电解质的可充电电池单元
- 用于非水电解质可充电电池的负极活性材料及其制备方法和包含该负极活性材料的非水电解质可充电电池
