一种增强宫颈癌放疗敏感性的靶向穿膜肽、修饰纳米颗粒复合物和制药应用
文献发布时间:2023-06-19 12:04:09
技术领域
本发明属于生物医药技术领域,涉及一种增强宫颈癌放疗敏感性的靶向穿膜肽、修饰纳米颗粒复合物和制药应用。
背景技术
宫颈癌是妇科常见的恶性肿瘤之一,死亡率仅次于乳腺癌,严重威胁着女性的健康。以手术联合放射治疗、化学治疗的综合治疗是目前宫颈癌治疗的主要手段,其疗效也得到国际上的一致认可。但在接受放射治疗的宫颈癌患者中,仍有约13%的患者出现了局部复发。这其中很大一部分原因是由于肿瘤发生了放疗耐受,并且由于放疗耐受的分子机制目前尚不明确,所以至今难以在患者放疗之前准确预测出放疗耐受的风险;另一方面,高剂量的放射治疗不仅会极大损伤盆腔区域的正常组织,还容易引起多种并发症;反之,若降低放射剂量则难以达到有效治疗目的,进而导致肿瘤复发。而放疗增敏是解决上述问题的重要策略之一。但是目前包括物理增敏(如加温、超短微波等)和化学增敏(如metronidazon化学增敏剂)等在内的增敏手段均因缺乏肿瘤靶向性而难以达到最佳疗效。因此,发展安全、高效的新型靶向基因治疗药物以增强放疗敏感性,降低放疗剂量,减少其副作用成为改善宫颈癌预后的重要治疗策略之一。
长链非编码RNA(lncRNA)是一类长度超过200个核苷酸的非编码RNA。近年来研究表明发现,lncRNA表达异常与包括宫颈癌在内的多种肿瘤的发生发展密切相关,它们通过改变肿瘤相关基因表达、影响细胞周期和干扰miRNA功能等途径,促进肿瘤细胞增殖、侵袭和转移,由此lncRNA正在成为肿瘤治疗的新靶点。生长阻滞特异性转录因子5(growtharrest specific 5,GAS5)是一种具有抑癌功能的lncRNA,在多种肿瘤细胞中表达下调。研究发现,在宫颈癌细胞中外源性高表达GAS5能抑制细胞增殖,诱导细胞凋亡,导致细胞周期阻滞,同时降低癌细胞侵袭迁移能力,增加细胞对抗癌药物顺铂的敏感性,并抑制移植瘤在动物体内生长。GAS5的抑癌功能与其诱捕miR-196a、miR-205和miR-21等密切相关。作为一种分子海绵,GAS5可通过miR-106b介导宫颈癌放疗增敏性。总之,GAS5是宫颈癌放疗增敏的新型治疗靶点。
细胞穿膜肽(cell-penetrating peptides,CPPs)作为一种新型的药物递送工具也备受关注。CPPs是一类不多于30个氨基酸残基组成的小分子多肽,具有跨膜转运能力,能够携带外源性大分子进入细胞,且在一定浓度范围内对宿主细胞无毒害作用。已有研究肿瘤靶向性精氨酸多肽作为药物递送载体,在肿瘤细胞中转运多肽片段或microRNA的效果。
目前已证实细胞穿膜肽R9作为一种新型靶向药物递送系统,可携带多肽片段靶向进入肿瘤细胞并发挥生物学作用。但是,R9复合体系存在稳定性较差的缺点,影响其发挥作用。阳离子聚合物-聚乙烯亚胺(PEI)是近年来研究最为广泛的非病毒纳米载体之一,可以通过压缩DNA与RNA形成非共价聚电解质复合物,复合物较小的纳米粒径和表面正电荷有利于复合物的细胞内吞。由于PEI具有转染效率较高,免疫应答低,生物兼容性好等特点,被认为是理想的药物递送载体。但影响PEI应用的主要瓶颈是其细胞毒性大、以及缺乏靶向性。
发明内容
为了克服上述现有技术的缺点,本发明的目的在于提供一种增强宫颈癌放疗敏感性的靶向穿膜肽、修饰纳米颗粒复合物和制药应用,该靶向穿膜肽能够可特异性、高效性进入宫颈癌中,通过调控PI3K/AKT途径及发挥microRNA“分子海绵”作用,从而提高放疗敏感性、降低放疗副作用。
为了达到上述目的,本发明采用以下技术方案予以实现:
本发明公开了一种增强宫颈癌放疗敏感性的靶向穿膜肽,该靶向穿膜肽为R9多肽,其氨基酸序列如SED.ID.NO.1所示。
本发明还公开了一种增强宫颈癌放疗敏感性的靶向穿膜肽纳米载药系统,该纳米载药系统是由上述的R9穿膜肽以双硫键SS偶联至聚乙烯亚胺PEI构成。
本发明还公开了一种增强宫颈癌放疗敏感性的靶向穿膜肽纳米颗粒复合物,该纳米颗粒复合物是由上述的纳米载药系统R9-SS-PEI携载lncRNA GAS5构建而成;其中:lncRNA GAS5为前列腺癌相关基因座lq25编码的lncRNA。
本发明还公开了上述的靶向穿膜肽纳米载药系统或上述的靶向穿膜肽纳米颗粒复合物在制备用于治疗宫颈癌的药物中的应用。
优选地,所述药物为具有宫颈癌的靶向性作用的药物。
优选地,所述的药物为增加宫颈癌放疗敏感性的药物。
优选地,所述的药物为正向调控PI3K/Akt通路、PTEN通路或miR-106表达水平的药物。
本发明公开了上述的靶向穿膜肽纳米载药系统或上述的靶向穿膜肽纳米颗粒复合物在制备宫颈癌放疗增敏剂中的应用。
与现有技术相比,本发明具有以下有益效果:
本发明以小分子二硫键(-SS-)修饰PEI,使得PEI的毒性得以大大降低;同时,也提高了PEI-核酸复合物的胶体稳定性,延长了其在体内的循环时间;同时利用肿瘤靶向多肽R9修饰PEI-核酸复合物,使得其解决了纳米颗粒在基因治疗研究中的靶向性问题。因此,REG有望被开发为增强宫颈癌放疗敏感性的有效手段。
附图说明
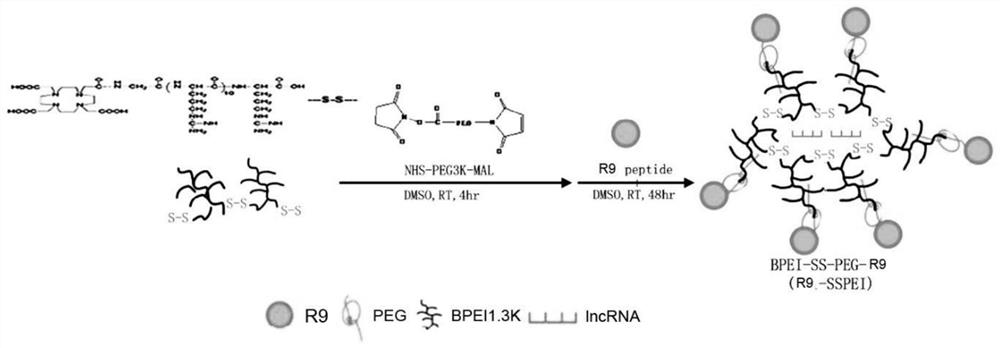
图1为本发明的R9-SSPEI-lncGAS纳米颗粒复合物的合成示意图;
图2为不同时间点R9-SSPEI-lncGAS纳米颗粒复合物转染Hela细胞后,细胞内lncGAS的表达情况;
图3为不同R9-SSPEI/lncGAS纳米颗粒复合物质量比作用下Hela,Siha的细胞毒性作用;
图4为化疗耐受宫颈癌细胞系Hela/R和Siha/R细胞系的建立结果图示;其中,A为Hela/R;B为Siha/R;
图5为R9-SSPEI/lncGAS在肿瘤细胞中的摄取图像;
图6为lncGAS在宫颈癌放疗耐受及放疗敏感细胞系中表达情况及对放疗敏感性的影响;其中,A为宫颈癌细胞系(Hela,Siha)及其放疗耐受细胞系(Hela-R,Siha-R)中LncGAS的表达差异B为放疗耐受细胞系Hela-R中过表达lncGAS后对细胞放疗生存率的影响;C为放疗耐受细胞系Siha-R中过表达lncGAS后对细胞放疗生存率的影响;
图7为小动物成像技术下R9在宫颈癌原位模型中各脏器摄取情况;
图8为R9-SSPEI/lncGAS纳米颗粒可抑制腹腔内肿瘤生长;其中,A为R9-SSPEI/lncGAS纳米颗粒相较于对照组肿瘤体积变化;B为R9-SSPEI/lncGAS纳米颗粒与对照组作用下肿瘤荧光变化。
具体实施方式
为了使本技术领域的人员更好地理解本发明方案,下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分的实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都应当属于本发明保护的范围。
需要说明的是,本发明的说明书和权利要求书及上述附图中的术语“第一”、“第二”等是用于区别类似的对象,而不必用于描述特定的顺序或先后次序。应该理解这样使用的数据在适当情况下可以互换,以便这里描述的本发明的实施例能够以除了在这里图示或描述的那些以外的顺序实施。此外,术语“包括”和“具有”以及他们的任何变形,意图在于覆盖不排他的包含,例如,包含了一系列步骤或单元的过程、方法、系统、产品或设备不必限于清楚地列出的那些步骤或单元,而是可包括没有清楚地列出的或对于这些过程、方法、产品或设备固有的其它步骤或单元。
下面结合附图对本发明做进一步详细描述:
本发明公开了一种增强宫颈癌放疗敏感性的靶向穿膜肽,所述的靶向多肽序列为:RRRRRRRRR。本发明还公开了一种用于宫颈癌放疗增敏的肿瘤靶向纳米颗粒,该纳米颗粒可特异性进入宫颈癌,并在体内外发挥抗肿瘤效果。在进一步的研究中发现可以该纳米颗粒在裸鼠体内可在宫颈癌原位模型及转移模型中均可特异性摄取并达到显著延长荷瘤鼠生存时间作用。而包括卵巢、心脏、肺、肝、肾脏等在内的脏器摄取率低,并未检测到细胞损伤作用。另外,荷瘤鼠在纳米颗粒给药组体内的PI3K/Akt通路蛋白显著下降,且存在miR-106“分子海绵”作用,这极有利于增强放疗敏感性。总之,该纳米颗粒是一种高效、特异、低毒性的放疗增敏剂。
实施例1 R9-SSPEI-lncGAS纳米颗粒复合物的合成
参见图1,具体合成过程如下:
将合成的lncGAS用甲醇(30ml)溶于烧瓶(100ml)中,样品用液氮净化、真空保存10-20min。用注射器加入计算量的硫化丙烯(多于BPEI1.2k 5摩尔)。该溶液在60℃下搅拌24h,反应混合物在减压下蒸发干燥,然后在甲醇中溶解,再在冰冷的二乙醚中沉淀两次。采用Ellman’s method测定产品硫醇组含量。BPEI-SH(0.5g)溶于无水二甲基亚砜(50ml)中,室温下搅拌48h,使硫醇基发生氧化交联。产物经D.I.水(mwco3500)的透析纯化,并进行了大量的冷冻干燥,其化学结构经质子核磁共振(NMR)证实。采用Ellman’s method测定了二硫化物的交联程度。将BPEI-SS(12当量)和MAL-PEG-NHS分别按1:5(v/v)的比例溶解于50ml无水甲醇和DMSO中,在室温中搅拌4h,然后加入R9多肽(1.2当量与MAL-PEG-NHS)。反应混合物在室温下再搅拌48小时,得到BPEI-SS-PEG-R9。
为了更准确地评价R9介导的肿瘤靶向性,以甲氧基聚乙二醇共轭BPEI-SS(BPEI-SS-MPEG)为对照。将MPEG5 k(1g,7mmol)、NPC(400mg,20mmol)和三乙胺(2.7ml,7mmol)溶于50ml二氯甲烷(MC)中,在冰浴中反应2h。反应混合物在室温搅拌16h后,在减压下蒸发干燥,溶解在MC中,然后在冷二乙醚中沉淀两次。以无水甲醇和二甲基亚砜为溶剂,以1:3(v/v)的比例溶解20ml的BPEI-SS(193mg,0.16mmol)和NPC活化的MPEG(40mg,6mmol),搅拌24h,对D.I.水(MWCO 10000)和冻干水进行大量纯化,质子核磁共振确证产物的化学结构。利用多肽合成器(APEX396,AAPP TEC,Louisville,KY,USA),按照标准的fluoren-9-ylmethoxycarbonyl(F-moc)化学方法,大量合成了相关联的R9多肽(RRRRRRRRR)。
实施例2 R9-SSPEI-lncGAS纳米颗粒复合物的稳定性检测
通过qRT-PCR实验测定纳米复合物的稳定性(图2)。50nM R9-SSPEI/lncGAS纳米颗粒复合物和50nM lncGAS(对照)分别和血清在37℃进行孵育,取不同时间点的样品进行qRT-PCR,观察lncGAS的稳定性。
实施例3 R9-SSPEI-lncGAS纳米颗粒复合物的细胞毒性检测
在宫颈癌细胞系Hela和Siha细胞中加入不同质量比的R9-SSPEI/lncGAS复合物(R9-SSPEI/lncGAS质量比为0.5、1、2、4、8、16)孵育48小时后进行MTT实验,检测细胞增殖情况,如图3所示。
实施例4细胞培养
宫颈癌细胞系Hela和Siha从ATCC细胞库购买。化疗耐受宫颈癌细胞系Hela/R和Siha/R细胞系的建立:首先对Hela和Siha细胞进行2Gy的放射辐照,大部分细胞发生凋亡,对少部分存活细胞传代培养3-5天,然后再次进行放射辐照,这一步骤进行循环重复,直到细胞接受放射辐照后有60%-90%的存活率,细胞被定义为放疗耐受宫颈癌细胞系,如图4所示。
实施例5 R9-SSPEI-lncGAS纳米颗粒复合物的细胞内摄取检测
使用CM-Dil染料标记宫颈癌细胞,将标记好的宫颈癌细胞以1×10
实施例6 R9-SSPEI-lncGAS纳米颗粒在细胞内的释放
考虑到lncGAS必须从R9-SSPEI载体中释放出来才能在细胞内发挥作用,所以下一步则需要检测R9-SSPEI-lncGAS载药系统是否能在宫颈癌细胞中释放出有功能的lncGAS。将FAM标记的lncGAS纳米颗粒转染肿瘤细胞后分别用qRT-PCR(引物序列见下表1)及流式细胞仪检测lncGAS在细胞内的释放,并进一步检测下游PI3K-AKT及miR-106表达情况判断lncGAS的生物学功能。
表1 qRT-PCR反应引物序列
实施例7宫颈癌细胞实验
在放疗敏感宫颈癌细胞系(Hela和Siha)和放疗耐受宫颈癌细胞系(Hela/R和Siha/R)中转染R9-SSPEI-lncGAS纳米颗粒,然后细胞经不同剂量γ射线辐照后进行各项细胞学检测:MTT实验检测细胞增殖能力;Annexin V/PI双染结合流式细胞术检测细胞凋亡;流式细胞术检测细胞周期;免疫荧光染色检测γ-H2AX foci确认细胞内DNA损伤修复;WB实验检测增殖marker(PCNA或Ki67)、凋亡marker(cleaved caspase 3、Bcl2、Bax)、Caveolin-1的蛋白表达水平。
结果参见图6所示,其中,A为宫颈癌细胞系(Hela,Siha)及其放疗耐受细胞系(Hela-R,Siha-R)中LncGAS的表达差异B为放疗耐受细胞系Hela-R中过表达lncGAS后对细胞放疗生存率的影响;C为放疗耐受细胞系Siha-R中过表达lncGAS后对细胞放疗生存率的影响;从图中可以看出,相较于宫颈癌放疗敏感细胞株(Hela、Siha),放疗耐受细胞株(Hela-R,Siha-R)表达显著降低。而在Hela-R、Siha-R细胞中过表达MLLT4-AS1后放疗敏感性均显著增强。
实施例8动物实验
为了研究R9-SSPEI-lncGAS纳米颗粒复合物在体内的摄取情况,将用FAM标记的LncGAS和SSPEI与R9-SSPEI两种载体进行偶联,形成两种聚合物,然后将两种聚合物通过静脉注射方式打入荷瘤鼠体内(另有一组注射生理盐水作为对照),经过四个小时后,处死动物并取肿瘤组织以及主要代谢器官(肝、脾、肾、心脏、脑、肺、卵巢),通过荧光成像系统观察两种纳米颗粒复合物在器官中的分布情况;摄取实验完成后将各组的肿瘤组织以及主要代谢器官组织进行匀浆后检测体内lncRNA的释放,同时留取部分肿瘤组织以及主要代谢器官组织以TUNEL法、免疫组化方法检测各组的内细胞凋亡情况。
结果如图7所示,不同载体携带生物素标记的lncGAS鼠尾动脉注射宫颈癌原位模型小鼠,4h后处死小鼠并立即取出重要脏器。小动物成像系统结果显示相较于对照组,R9-SSPEI/lncGAS可在肿瘤组织中特异性摄取。
进一步为了R9-SSPEI-lncGAS纳米颗粒复合物对体内肿瘤放疗敏感性的调节作用,首先利用放疗敏感和放疗耐受宫颈癌细胞系(2×10
结果如图8所示,R9-SSPEI/lncGAS纳米颗粒可抑制腹腔内肿瘤生长,且lncGAS在R11-SSPEI-miR-145纳米颗粒处理组中高表达。实验结果以均数±标准差(mean±SD)表示,用SPSS 19.0软件进行统计学分析,多组间均数比较采用单因素方差分析和t检验,双侧P<0.05为显著性检验标准。
综合本发明的以上结果表明,R9-SSPEI-lncGAS为宫颈癌治疗提供了一种新型高效的多肽靶向纳米药物递送系统,对宫颈癌放疗耐受和肿瘤复发的治疗策略具有重要意义。本发明公开的用于增强肿瘤放疗敏感性的靶向药物,该药物可特异性、高效性进入宫颈癌中,通过调控PI3K/AKT途径及发挥microRNA“分子海绵”作用,从而提高放疗敏感性、降低放疗副作用。阳离子聚合物-聚乙烯亚胺(PEI)是近年来研究最为广泛的非病毒纳米载体之一,可以通过压缩DNA与RNA形成非共价聚电解质复合物,复合物较小的纳米粒径和表面正电荷有利于复合物的细胞内吞。由于PEI具有转染效率较高,免疫应答低,生物兼容性好等特点,被认为是理想的药物递送载体。但影响PEI应用的主要瓶颈是其细胞毒性大、以及缺乏靶向性。为了解决此困难,本发明对PEI进行了修饰和改性的工作:以小分子二硫键(-SS-)修饰PEI,使得PEI的毒性得以大大降低;同时,也提高了PEI-核酸复合物的胶体稳定性,延长了其在体内的循环时间;同时利用肿瘤靶向多肽R9修饰PEI-核酸复合物,使得其解决了纳米颗粒在基因治疗研究中的靶向性问题。因此,REG有望被开发为增强宫颈癌放疗敏感性的有效手段。
以上内容仅为说明本发明的技术思想,不能以此限定本发明的保护范围,凡是按照本发明提出的技术思想,在技术方案基础上所做的任何改动,均落入本发明权利要求书的保护范围之内。
- 一种增强宫颈癌放疗敏感性的靶向穿膜肽、修饰纳米颗粒复合物和制药应用
- 一种双受体识别的串联型穿膜肽修饰的肿瘤靶向纳米递药系统
