UPLC-LTQ-Orbitrap-MS法检测芍药花中化学成分的方法
文献发布时间:2023-06-19 18:27:32
技术领域
本发明涉及检测技术领域,具体涉及一种UPLC-LTQ-Orbitrap-MS法检测芍药花中化学成分的方法。
背景技术
芍药是芍药科芍药属植物,主要以根部入药。芍药分为白芍和赤芍,白芍为栽培品,以炮制后干燥入药,具有补血养阴的功效;赤芍为野生品,以原药生用,具有凉血逐瘀的功效。芍药花不仅具有很好的观赏价值,芍药花制成花茶也具有养血柔肝,散郁祛瘀,清心润肺、护肤养颜等功效。
为了加速中药现代化的发展,有必要对中药化学成分进行研究。近年来,对于芍药化学成分的研究主要是基于芍药根部为基础的研究,而对芍药花中化学成分的研究相对较少。目前,有研究表明芍药花中的化学成分包括没食子酸、没食子酸甲酯、没食子酸乙酯、1,2,3,6-没食子酸酰-β-D-葡萄糖、1,2,3,4,6-没食子酸酰-β-D-葡萄糖、异槲皮素-3-O-β-D(6″-没食子酸酰)葡萄糖、山柰酚-3-O够-D-(6"-没食子酸酰)葡萄糖、1-O-没食子酰基-β-D-葡萄糖、山柰酚-3,7-O-β-D-二葡萄糖苷、芍药苷、芍药内酯苷等多种单萜类和多酚类物质,具有抗氧化及抗炎等药理作用。然而,目前对于芍药花提取方面的主要集中在黄酮类物质的提取,对于芍药花其它物质的的分离鉴定仍是一片空白。因此,明确芍药花提取物中的其它物质对于芍药花的应用具有重要意义。
中药成分复杂多样,将中药的特色与现代化技术相结合,快速、有效的研究中药中的成分,去阐明中药的药效物质基础及其作用机制十分有意义。与传统LC-MS相比,UPLC-LTQ-Orbitrap-MS高分辨质谱采用全扫描直接进样分析结合母离子列表筛选后二次进样的方法,并具有低分辨和高分辨平行检测功能。在正负离子模式下,根据准分子离子峰,碎片离子和二级质谱可筛选目标成分以及快速分析化合物的结构,通过Xcalibur软件得到的特征碎片与实际测定碎片质量的偏差均小于5ppm(δ≤6×10-6)。该方法是进行常规化合物鉴定和复杂成分分析的有效手段,能够在保证预测化合物分子式的准确性的同时更全面的鉴定芍药花中的化学成分,具有更高质量精度和更全面鉴定的特点。但是,采用UPLC-LTQ-Orbitrap-MS法检测芍药花中化学成分的方法尚未见报道。
我们在利用UPLC-LTQ-Orbitrap-MS法检测芍药花中化学成分的过程中发现,对芍药花提取物进行色谱条件分离时,多种色谱峰在10-15min处色谱峰叠加严重,且在20min以后存在严重的杂峰干扰。另外,在分析某些化合物时仍然存在碎片信息有限的问题,由此导致缺乏其它可以辅助定性的碎片信息。因此,有必要开发一种利用UPLC-LTQ-Orbitrap-MS技术结合母离子列表的方法快速筛选芍药花中的化学成分的方法,为芍药花化学成分的提取分离及其药效物质基础提供研究基础。
发明内容
为解决上述问题,本发明的目的在于提供一种利用UPLC-LTQ-Orbitrap-MS技术结合母离子列表的方法快速检测芍药花中化学成分的方法。
为实现上述目的,本发明的技术方案如下。
一种UPLC-LTQ-Orbitrap-MS法检测芍药花中化学成分的方法,包括以下步骤:
(1)样品预处理
将新鲜采摘的芍药花进行干燥、粉碎,然后加入提取溶剂,在85~95℃下回流提取,提取完成后,过滤,得到待测样品;
(2)采用UPLC-LTQ-Orbitrap-MS法分离所述待测样品,并对分离出的化学成分进行质谱检测,得到芍药花中各化学成分物质峰,然后对芍药花中各化学成分的物质峰进行定性分析;
步骤(2)中,分离所述待测样品的色谱条件如下:
色谱柱为shim-pack C18,250mm×4.6mm,5μm;
洗脱系统流动相A为体积比0.075%甲酸-水溶液;流动相B为乙腈;
梯度洗脱程序如下:
0~5min,流动相A与流动相B的体积比为95~86:5~14;
5~6.5min,流动相A与流动相B的体积比为86~85:14~15;
6.5~15min,流动相A与流动相B的体积比为78~69:22~31;
15~18min,流动相A与流动相B的体积比为69~5:31~95;
18~20min,流动相A与流动相B的体积比为5:95;
20~22min,流动相A与流动相B的体积比为5~95:95~5;
22~26min,流动相A与流动相B的体积比为95:5。
进一步,步骤(2)中,洗脱的流速为0.8mL/min;进样体积为5μL;柱温为30℃。
进一步,步骤(1)中,所述提取溶剂为水、甲醇水溶液或乙醇水溶液。
更进一步,所述提取液溶剂为体积比50%乙醇水溶液。
进一步,步骤(1)中,所述芍药花与所述提取溶剂的用量比为1g:20~30mL。
进一步,步骤(1)中,回流提取的时间为3~5h,冷却后用提取溶剂补足减失的重量。干燥的方法为冷冻干燥,当然也可以采用其他干燥方式。
进一步,步骤(2)中,分离出的化学成分为酪氨酸、对香豆酸、儿茶素、奎宁酸、莽草酸、没食子苷、3-没食子酰奎宁酸、没食子酰蔗糖、没食子酸、没食子酸甲酯、氧化芍药苷、槲皮素-3,7-二-O-葡萄糖苷、山奈酚-3,7-O-二葡萄糖、芍药内酯苷、芍药苷元酮、芍药苷、阿魏醛、牡丹皮苷E、异鼠李素-3,7-二-O-葡萄糖苷、谷氨酸、5-葡萄糖苷-7-葡萄糖醛酸苷、山奈酚-3-O-葡萄糖苷-7-O-鼠李糖苷、没食子酰芍药苷、1,2,3,4,6-O-五没食子酰葡萄糖、山奈酚-3-O-β-D-葡萄糖苷、苯甲酰芍药苷、柠檬酸、山奈酚、对羟基苯甲酸异丙酯、α-亚麻酸、芍药苷元B、没食子酸乙酯、菊苣酸、1,6-二-O-没食子酰基葡萄糖、5-羟甲基糠醛、苯甲酸。
进一步,步骤(2)中质谱检测条件如下:
离子源为HESI离子源,正负离子模式检测;离子源温度350℃,电离源电压4kV,毛细管电压35V,管透镜电压110V;
鞘气和辅助气均为高纯氮气,鞘气流速为45Arb;辅助气流流速为215Arb;
激活能量单位:0.25q;激活时间:30ms;归一化碰撞能量:35%;
傅里叶高分辨扫描范围:100~1200m/z。
一级扫描分辨率为70000。
质谱检测的数据扫描模式包括傅里叶变换高分辨全扫方式数据依赖性ddMS
本发明的有益效果:
1、本发明提供了基于UPLC-LTQ-Orbitrap-MS法检测芍药花中化学成分的方法,通过50%乙醇进行热回流提取,能够有效提取芍药花中的各化学成分,且对各成分的含量提取效果最好。本发明针对芍药花中各化学成分采用shim-pack C18色谱柱,以0.075%甲酸水溶液(A)-乙腈(B)为流动相进行二元梯度洗脱,使芍药花中各化学成分的峰形效果较好,且相邻峰之间的分离度好,大于1.5,能够达到完全分离。在正、负离子模式下采集数据,离子扫描范围为100~1000m/z。采用Waters UNIFI数据处理软件对采集的准分子离子峰信息进行检测并定性分析,通过结合质谱数据和文献数据进行鉴定,共鉴定出了芍药花中36个化合物,包括氨基酸类2个、有机酸类8个、黄酮类7个、鞣质类8个、萜类6个、糖苷类3个、酯类1个、醛类1个;其中奎宁酸、阿魏醛、菊苣酸、5-羟甲基糠醛首次在该种属中发现,对香豆酸、苯甲酸首次在芍药花中发现。进一步明确了芍药花中的化学成分的类型。本发明的方法为芍药花中化学成分的定性分析及其质量控制提供了一种高效、快速的分析方法,对今后进一步阐明芍药花药效物质基础以及进一步的资源开发利用提供数据支持。
2、本发明的方法利用UPLC-LTQ-Orbitrap-MS技术结合母离子列表的方法能够解决色谱峰叠加严重以及杂峰干扰的问题,并快速筛选芍药花中的化学成分,为芍药花化学成分的提取分离及其药效物质基础提供实验依据。
附图说明
图1是不同乙醇含量作为提取溶剂提取出的待测样品的色谱图以及混合标准品溶液的色谱图。
图2是以0.075%甲酸/水(A)-乙腈(B)作为流动相对待测样品进行检测的色谱图。
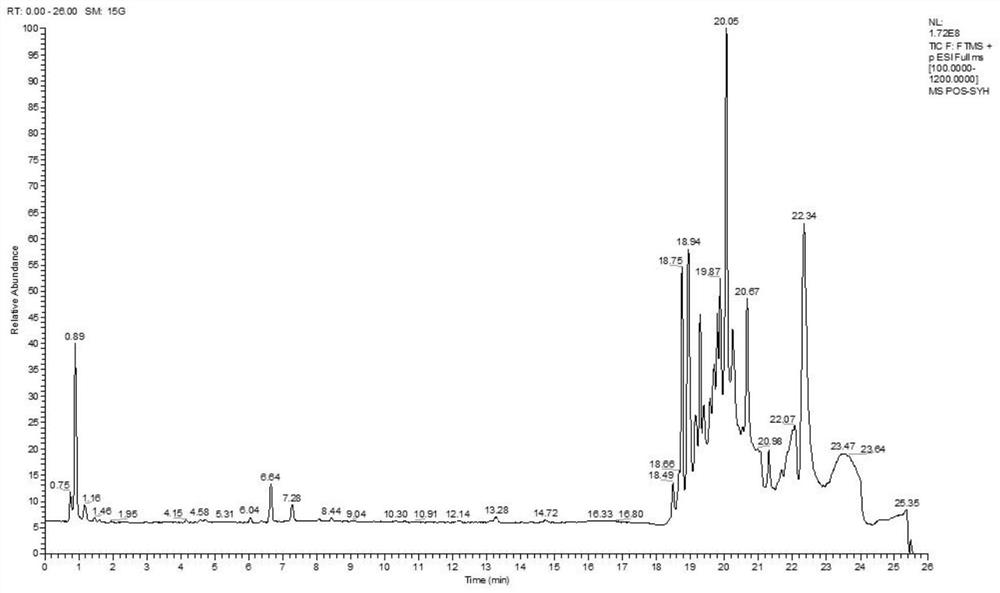
图3是采用“色谱条件-1”分离芍药花提取物的总离子流图TIC。
图4是采用“色谱条件-2”分离芍药花提取物的总离子流图TIC。
图5是采用“色谱条件-3”分离芍药花提取物的总离子流图TIC。
图6是芍药花中分离出的各化学成分的结构式。
图7是待测样品的正离子模式总离子流图(TIC)。
图8是待测样品的负离子模式总离子流图(TIC)。
图9是化合物33的一(C)级质谱图。
图10是化合物33的二(D)级质谱图。
图11是化合物35的一(C)级质谱图。
图12是化合物35的二(D)级质谱图。
图13是化合物33的总离子流图。
图14是化合物35的总离子流图。
具体实施方式
为了使本发明的目的、技术方案及优的更加清楚明白,以下结合附图及实施例,对本发明进行进一步详细说明。应当理解,此处所描述的具体实施例仅仅用以解释本发明,并不用于限定本发明。
基于本发明中的实施例,本领域普通技术人员在没有作出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
1、实验材料和仪器
1.1、实验材料
表1实验试剂
1.2、实验主要仪器
表2主要仪器
2、实验方法
2.1、色谱条件
采用shim-pack C18色谱柱(250mm×4.6mm,5μm),以0.075%甲酸/水(A)-乙腈(B)为流动相,设置柱温30℃,调整总流速为0.8mL/min;进样体积为5μL;梯度洗脱程序见表3。
表3梯度洗脱程序
2.2、质谱条件
HESI离子源,正、负离子模式,离子源温度350℃,电离源电压4KV,毛细管电压:35V,管透镜电压:110V;鞘气和辅助气均为高纯氮气(纯度>99.99%),鞘气流速:45arb,辅助气流流速:215arb;激活能量单位:0.25q;激活时间:30ms;归一化碰撞能量:35%;傅里叶高分辨扫描范围m/z:100~1200;一级扫描分辨率:70000;数据采用傅里叶变换高分辨全扫方式(TF,Full scan,Resolution 30000)数据依赖性(data-dependent acquisistion)ddMS
2.3、待测样品制备
将提前干燥处理过的芍药花干花苞粉碎,然后取处理好的芍药花粉末5g,放置于圆底烧瓶中,加入提取溶剂,混合均匀后,在100~110℃下回流提取3h,自然冷却后,称重,用提取溶剂补足减失的重量,摇匀。取提取液用滤纸滤过,再用0.45μm微孔滤膜对滤液进行过滤,即得待测样品。
提取溶剂选用50%乙醇。
2.4、混合标准品溶液的配置
1)没食子酸储备液:精密称取没食子酸标准品13.4mg溶于10mL甲醇,混合均匀得到1.34mg/mL的没食子酸储备液;
2)氧化芍药苷储备液:精密称取14.8mg氧化芍药苷溶于10mL甲醇中,混合均匀得到1.48mg/mL的氧化芍药苷储备液;
3)芍药内酯苷储备液:精密称取芍药内酯苷35.5mg于试管中,加入10mL甲醇,混合均匀得到3.55mg/mL的芍药内酯苷储备液;
4)芍药苷储备液:精密称取芍药苷18.4mg于试管中,加入10mL甲醇,混合均匀得到1.84mg/mL的芍药苷储备液;
5)1,2,3,4,6-五没食子酸酰葡萄糖储备液:精密称取1,2,3,4,6-五没食子酸酰葡萄糖35.5mg,溶于10mL甲醇中,混合均匀得到3.35mg/mL的1,2,3,4,6-五没食子酰葡萄糖储备液;
6)芦丁储备液:精密称取41.4mg芦丁,于10mL容量瓶中以甲醇定容,混合均匀得到4.14mg/mL的芦丁储备液。
7)苯甲酰芍药苷储备液:精密称取苯甲酰芍药苷16.1mg,于10mL容量瓶中,以甲醇为溶剂定容至刻度,混合均匀得到浓度为1.61mg/mL的苯甲酰芍药苷储备液。
8)山奈酚储备液:精密称取19.0mg,于10mL容量瓶中以甲醇定容,混合均匀得到1.90mg/mL的山奈酚储备液。
9)混合标准品溶液:准确量取上述8种标准品储备液各0.2mL至2mL道夫管中,混匀,得到浓度分别为食子酸167.5μg/mL、氧化芍药苷185μg/mL、芍药内酯苷443μg/mL、芍药苷230μg/mL、芦丁517μg/mL、1,2,3,4,6-五没食子酸酰葡萄糖443μg/mL、苯甲酰芍药苷201μg/mL、山奈酚237.5μg/mL的混合标准品溶液。
2.5、提取溶剂的选择
2.5.1、色谱条件
采用shim-pack C18色谱柱,以乙腈(A)-0.5%醋酸水(B)为流动相,设置柱温30℃,调整总流速为0.8mL/min;检测波长230nm;梯度洗脱程序见表1。
表1 HPLC梯度洗脱时间程序
2.5.2、提取溶剂的筛选
采用2.5.1的色谱条件进行提取溶剂的筛选试验;分别采用无水乙醇、90%乙醇、70%乙醇、50%乙醇、30%乙醇和超纯水作为提取溶剂用以提取芍药花中各化学成分,并以2.4的混合标准品溶液作为对照进行HPLC分析。通过对HPLC所得结果利用中药材指纹图谱对比软件进行比对,比较各提取溶剂提取出的芍药花中各化学成分在色谱图上的峰形效果,结果如图1所示。
图1是以不同浓度的乙醇溶液为提取溶剂提取芍药花中各化学成分的色谱图以及混合标准品溶液的色谱图。其中,没食子酸的出峰时间为7.3min;氧化芍药苷的出峰时间为18min,因230nm不是氧化芍药苷的最大吸收波长,因此图中显示不明显。由图1结果表明,以50%乙醇作为提取溶剂,对各化学成分的含量提取效果最好。
2.6、流动相的选择
以2.3的方法提取芍药花得到待测样品,检测待测样品中各成分时,采用2.5.1的条件进行流动相的筛选,筛选过程中其他条件不变,仅对流动相进行筛选;比较各流动相的分离效果。
通过对流动相进行筛选试验,分别采用0.5%醋酸溶液(A)-乙腈(B)、0.5%醋酸溶液(A)-甲醇(B)、0.075%甲酸/水(A)-乙腈(B)作为流动相进行比较研究。
图2是以0.075%甲酸/水(A)-乙腈(B)作为流动相对待测样品进行检测的色谱图。结果表明采用0.075%甲酸/水(A)-乙腈(B)作为流动相时,混合标准品溶液和待测样品的峰形较好,且相邻峰之间的分离度好,能够达到完全分离。
2.7、色谱条件优化
以2.3的方法提取芍药花得到待测样品,检测待测样品中各成分时,采用2.1的条件进行流动相的筛选,筛选过程中其他条件不变,仅对色谱条件进行筛选;比较各流动相的分离效果。
色谱条件-1:0-5min 95-86%A;5-6.5min 86-85%A;6.5-15min 78-69%A;15-18min 69-5%A;18-20min 5%A;20-22min 5-95%A;22-26min 95%A;
色谱条件-2:0-10min 96-86%A;10-20min 86-84%A;20-30min 84-75%A;30-35min 75-40%A;35-36min 40-96%A;36-40min 96%A;
色谱条件-3:0-13min 99-65%A;13-15min 65-50%A;15-17min 50%A;17-18min50-25%A;18-21min 25%A;21-22min 25-0%A;22-26min 0%A;26-27min 0-99%A;27-30min 99%A。
采用上述三种色谱条件对2.3的待测样品进行色谱分离,结果见图3-5。
图3是采用“色谱条件-1”分离芍药花提取物的总离子流图TIC。
图4是采用“色谱条件-2”分离芍药花提取物的总离子流图TIC。
图5是采用“色谱条件-3”分离芍药花提取物的总离子流图TIC。
将2.3的待测样品通过“色谱条件-2”分离,发现10-15min处色谱峰叠加严重;将10-15min处有机相比例梯度斜率变小,有改善,但4-8min色谱峰稀少,且20分钟后杂峰过多。将色谱梯度优化为“色谱条件-1”后,色谱峰分布均匀,响应稳定。因此最终确定以色谱条件-1为最佳的分离方法。
3、结果
3.1、质谱成分的分析与鉴别
超高效液相色谱及质谱条件下,分别测定正负离子模式下的总离子流图(TIC),见图7-8,并通过母离子列表法再次进样。
首先,与对照品图谱中各已知成分的保留时间、精确相对分子质量及[M-H]
其次,无对照品的化合物,使用Xcalibur 4.2SP1软件(Thermo FisherScientific)对质谱数据进行分析,通过高分辨率质谱信息包括一二级质谱、碎片离子和准分子离子峰等信息推导其可能的分子式,质谱偏差范围δ≤5ppm。由化学专业数据库和相关文献检索结合正、负离子模式下全扫图谱中离子丰度≥2×10
结合化合物的质谱及裂解规律进行分析和鉴别,共推测、鉴定出36个化合物,见图6。36个化合物的准确分子量、二级质谱数据等数据见表4,其中,列举了化合物33和35的一(C)、二(D)级质谱裂解图见图9~12,化合物33和35的总离子流图见图13~14。
表4芍药花中化学成分的质谱鉴定结果
3.2、成分鉴定
化合物1根据质谱上的准分子离子峰m/z:182.0812[M+H]
化合物2根据质谱上的准分子离子峰m/z:163.0393[M-H]
化合物3根据质谱上的准分子离子峰m/z:289.0712[M-H]
化合物4根据质谱上的准分子离子峰m/z:191.0551[M-H]
化合物5根据质谱上的准分子离子峰m/z:173.0451[M-H]
化合物6根据质谱上的准分子离子峰m/z:331.0633[M-H]
化合物7根据质谱上的准分子离子峰m/z:343.0661[M-H]
化合物8根据质谱上的准分子离子峰m/z:493.1183[M-H]
化合物9根据质谱上的准分子离子峰m/z:169.0139[M+H]
化合物10根据质谱上的准分子离子峰m/z:183.0294[M+H]
化合物11的准分子离子峰m/z:495.1498[M-H]
化合物12根据质谱上的准分子离子峰m/z:625.1391[M-H]
化合物13根据质谱上的准分子离子峰m/z:609.1445[M-H]
化合物14根据质谱上的准分子离子峰m/z:481.169[M-H]
化合物15的准分子离子峰为m/z:319.1174[M+H]
化合物16根据质谱上的准分子离子峰m/z:479.1547[M-H]
化合物17根据质谱上的准分子离子峰m/z:179.0708[M+H]
化合物18根据质谱上的准分子离子峰m/z:525.1603[M-H]-,推断该化合物的分子式C
化合物19根据质谱上的准分子离子峰m/z:639.1552[M-H]
化合物20准分子离子峰m/z:146.0457[M-H]-,分子式为C
化合物21准分子离子峰m/z:669.1653[M-H]
化合物22根据质谱上的准分子离子峰m/z:609.1445[M-H]
化合物23的准分子离子峰为m/z:631.1663[M-H]
化合物24负离子模式下的准分子离子峰为m/z:939.1114[M-H]
化合物25据质谱上的准分子离子峰m/z:447.0908[M-H]-,根据元素组成结合数据库分析,推断该化合物的分子式为C
化合物26负离子模式下的准分子离子峰为m/z:583.1810[M-H]
化合物27根据质谱上的准分子离子峰m/z:191.0188[M-H]
化合物28根据质谱上的准分子离子峰m/z:285.0400[M-H]
化合物29准分子离子峰m/z:181.0859[M-H]
化合物30准分子离子峰m/z:279.2316[M-H]
化合物31的准分子离子峰m/z:197.0807[M+H]
化合物32根据质谱上的准分子离子峰由于化合物21准分子离子峰m/z:197.0452[M+H]
化合物33准分子离子峰m/z:473.0720[M-H]-,产生的主要碎片离子有m/z:61.99、m/z:93.00、m/z:276.99、m/z:364.98,根据元素组成结合数据库分析推断该化合物的分子式为C
化合物34根据质谱上的准分子离子峰m/z:485.0921[M+H]
化合物35准分子离子峰m/z:125.0242[M-H]-,产生的主要离子碎片有m/z:67.03、m/z:98.02、m/z:125.04。根据元素组成结合数据库分析,推断该化合物的分子式为C
化合物36根据质谱上的准分子离子峰m/z:121.0288[M-H]
4、讨论
线性离子阱串联静电场轨道阱傅里叶变换高分辨质谱仪(LTQ-Orbitrap-MS),其中线性离子阱(LTQ)可以实现多级质谱功能,而静电场轨道阱(Orbitrap)可提供高分辨的质谱信息。UPLC-LTQOrbitrap-MS系统将超高效液相色谱与线性离子阱高分辨质谱技术相结合,既实现了超高效液相技术对于复杂样品快速分离的优势,又能够获得母离子、子离子及多级碎片离子的高分辨质谱信息,对于中药复杂体系中化学成分的鉴定与分析具有一定优势,多用于中药成分的快速鉴定。对于中药复杂体系中化学成分的鉴定与分析具有一定优势,多用于中药成分的快速鉴定。本发明利用UPLC-LTQ-Orbitrap-MS技术结合母离子列表的方法对芍药花的化学成分进行分析。
芍药花中的主要成分为鞣质类和糖苷类化合物,鞣质类(Tannins)又称单宁。是一类结构复杂的酚类化合物,在植物中广泛分布,具有收敛、止血、抗菌作用。其质谱裂解规律主要是18Da(H
本发明实施例的试验方法采用UPLC-LTQ Orbitrap MS技术得到芍药花中各化学成分,初步推断出芍药花中的36种化学成分,包括氨基酸类2个、有机酸类8个、黄酮类7个、鞣质类8个、萜类6个、糖苷类3个、酯类1个、醛类1个;其中,奎宁酸、儿茶素、L-亮氨酸、L-酪氨酸、对香豆酸、莽草酸、6-羟基山奈酚-3,6-二葡萄糖苷、异鼠李素-3,7-二-O-葡萄糖苷、芍药苷元、6-姜辣素、姜黄素、芍药苷元B、氧化芍药苷、阿魏醛、谷氨酸、对羟基苯甲酸异丙酯、柠檬酸、对羟基苯甲酸异丁酯、苯甲酸、菊苣酸、α-亚麻酸、芹菜素二葡萄糖苷、5-羟甲基糠醛、4-甲氧基苯乙酸、苯甲酰芍药苷、没食子酰芍药苷均首次在芍药花中被分离并检测出来。该方法为芍药花中化学成分的定性分析及其质量控制提供了一种高效、快速的分析方法,对今后进一步阐明芍药花药效物质基础以及进一步的资源开发利用提供数据支持。
以上仅为本发明的较佳实施例而已,并不用以限制本发明,凡在本发明的精神和原则之内所作的任何修改、等同替换和改进等,均应包含在本发明的保护范围之内。
- 一种芍药甘草汤中化学成分的测定方法及指纹图谱的建立方法
- 芍药甘草汤中17种化学成分的含量测定方法
