基于异构化驱动的不可逆开环聚合制备含硫聚合物的方法
文献发布时间:2023-06-19 19:28:50
技术领域
本发明涉及一种含硫聚合物及基于异构化驱动的不可逆开环聚合制备含硫聚合物方法。
背景技术
非张力五元环单体是一类非常有潜力的可再生单体,普遍存在于自然界的天然品中,亦可由淀粉、木质纤维素、或二氧化碳为原料大规模生产。然而,非张力五元环单体在室温条件下的开环聚合(ROP)通常是热力学禁止的,在文献和教科书中通常把这类化合物称为是“不可以聚合”的单体,这是因为它们非张力的五元环不能提供足够的环张力来驱动开环聚合(ROP),同时,由于开环聚合是一个典型的聚合/解聚的热力学平衡,热力学稳定性的五元环内酯在聚合过程易发生解聚反应。2016年,洪缪和Chen开创性的发展了非张力五元环内酯开环聚合的新策略(Nat.Chem.2016,8,42-49),即通过控制反应温度低于聚合上限温度和析出聚合物来破坏聚合-解聚平衡,但是极低的聚合反应温度严重阻碍了工业生产的适用性。
已公开的一种阴离子催化剂催化的聚合反应中,五元环硫羰代内酯单体被碱性的阴离子催化剂拔氢后,可亲核进攻单体γ位亚甲基(次甲基)发生异构化开环聚合,也可亲核进攻另一单体分子的硫羰基后失去一分子硫化氢发生酯缩合反应,生成二聚产物而非聚合物(如下所示),如何限制后一种酯缩合反应是聚合能否高效进行的关键。
迄今为止,仍缺乏一种可在温和条件下高效进行非张力五元环单体聚合,制备性能各异的可持续性聚硫酯材料的普适性方法。
发明内容
本发明所要解决的技术问题在于克服现有的非张力五元环单体在温和条件下难开环聚合的缺陷,而提供了一种不可逆开环聚合的新方法。本发明的制备方法为工业化生产环境友好的含硫高分子材料提供了便利。合成得到的含硫高分子具有分子量高、物理性能大范围可调、优异的降解性等优点,可用作塑料、橡胶、弹性体、纤维等制品。
本发明提供了一种含硫聚合物的制备方法,其包括以下步骤:有机溶剂中,在主催化剂存在下,将一种或一种以上的聚合单体进行聚合反应;
其中,所述的主催化剂为阴离子主催化剂或阳离子主催化剂;所述的阴离子主催化剂为膦腈碱、胍类有机碱、脒类有机碱、N-杂环卡宾类有机碱、N-杂环烯烃类有机碱、羧酸盐和硫代羧酸盐中的一种或多种;所述的阳离子主催化剂为两性离子对型催化剂、中性路易斯酸型催化剂和质子酸(酯)型催化剂中的一种或多种;
所述的聚合单体独立地为如式(I)所示的化合物:
其中,
R
或者,R
当所述的主催化剂为阴离子主催化剂时,则R
当所述的主催化剂为阴离子主催化剂时,且所述的聚合单体为一种时,则所述的聚合物单体不为
在一些实施方案中,R
在一些实施方案中,所述的如式(I)所示的化合物由以下任一结构所示:
/>
在一些实施方案中,
优选地,R
进一步优选地,R
(1)R
(2)R
(3)R
(4)R
(5)R
(6)R
(7)R
在一些实施方案中,
优选地,R
进一步优选地,R
在一些实施方案中,
优选地,R
进一步优选地,R
在一些实施方案中,
优选地,R
进一步优选地,R
在一些优选实施方案中,所述的如式(I)所示的化合物由以下任一结构所示:
在一些实施方案中,所述的聚合反应优选在保护气体氛围下进行,所述的保护气体可为本领域常规的保护气体,例如氮气和/或氩气。本发明中所述的保护气体即为本领域所述的惰性气体。
在一些实施方案中,所述的聚合单体与所述的有机溶剂的摩尔体积比可为本领域常规的摩尔体积比,优选0.2mol/L-10mol/L,更优选2.0mol/L-7.0mol/L,例如2.0mol/L或5.0mol/L。
在一些实施方案中,所述的有机溶剂可为本领域常规的有机溶剂。
优选地,所述的有机溶剂为直链烃类溶剂、卤代烃类溶剂、环状醚类溶剂、芳烃类溶剂、卤代芳烃类溶剂和酰胺类溶剂中的一种或多种,例如芳烃类溶剂和/或酰胺类溶剂,又例如甲苯和/或N,N-二甲基甲酰胺。所述的直链烃类溶剂优选正己烷、正庚烷和正戊烷中的一种或多种。所述的卤代烃类溶剂优选二氯甲烷、三氯甲烷、1,2-二氯乙烷和四氯乙烷中的一种或多种。所述的环状醚类溶剂优选四氢呋喃和/或二氧六环。所述的芳烃类溶剂优选甲苯、苯和二甲苯中的一种或多种,更优选甲苯。所述的卤代芳烃类溶剂优选邻二氯苯、邻二氟苯、邻二溴苯、氯苯、氟苯、溴苯和均三氯苯中的一种或多种,更优选邻二氯苯。所述的酰胺类溶剂优选N,N-二甲基甲酰胺。
在一些实施方案中,所述的聚合单体与所述的主催化剂的摩尔比可为本领域常规的摩尔比,优选20:1-1600:1,更优选100:1-1600:1,进一步优选400:1-1600:1,例如400:1、1200:1或1600:1。
在一些实施方案中,所述的阴离子主催化剂中,所述的膦腈碱可为本领域常规的膦腈碱。优选地,所述的膦腈碱由以下结构所示:
其中,R和R’独立地为C
更优选地,所述的膦腈碱为1-叔丁基-4,4,4-三(二甲氨基)-2,2-二[三(二甲氨基)-正膦亚基氨基]-2λ
更优选地,所述的膦腈碱还可为叔丁基亚氨基-三(二甲氨基)正膦(
在一些实施方案中,所述的阴离子主催化剂中,所述的胍类有机碱可为本领域常规的胍类有机碱。优选地,所述的胍类有机碱为1,5,7-三叠氮双环(4.4.0)癸-5-烯(TBD)和/或7-甲基-1,5,7-三氮杂二环[4.4.0]癸-5-烯(MTBD),其结构如下所示:
在一些实施方案中,所述的阴离子主催化剂中,所述的脒类有机碱可为本领域常规的脒类有机碱。优选地,所述的脒类有机碱为1,8-二氮杂二环[5.4.0]十一碳-7-烯(DBU),其结构如下所示:
在一些实施方案中,所述的阴离子主催化剂中,所述的N-杂环卡宾类有机碱可为本领域常规的N-杂环卡宾类有机碱。优选地,所述的N-杂环卡宾类有机碱由以下结构所示:
其中,R
更优选地,所述的N-杂环卡宾类有机碱为1,3-二叔丁基咪唑-2-亚基(I
在一些实施方案中,所述的阴离子主催化剂中,所述的N-杂环烯烃类有机碱可为本领域常规的N-杂环烯烃类有机碱。优选地,所述的N-杂环烯烃类有机碱由以下结构所示:
其中,R
更优选地,所述的N-杂环烯烃类有机碱为1,3,4-三甲基-2-(异亚丙烯基)-咪唑(NHO),其结构如下所示:
在一些实施方案中,所述的阴离子主催化剂中,所述的羧酸盐可为金属羧酸盐或有机羧酸盐。
优选地,所述的金属羧酸盐和有机羧酸盐中的阴离子独立地由以下结构所示:
其中,R
更优选地,所述的金属羧酸盐和有机羧酸盐中的阴离子独立地为乙酸阴离子。
优选地,所述的金属羧酸盐中的阳离子为碱金属(例如锂、钠、钾、铷或铯,又例如钾)阳离子。
优选地,所述的有机羧酸盐中的阳离子为季铵阳离子、咪唑鎓阳离子、膦腈鎓阳离子、双(三苯基膦)铵阳离子或脒鎓阳离子。
更优选地,所述的有机羧酸盐中的阳离子由以下任一结构所示:
其中,R
在一些实施方案中,所述的阴离子主催化剂中,所述的硫代羧酸盐可为金属硫代羧酸盐。
优选地,所述的硫代羧酸盐中的阴离子由以下结构所示:
其中,R
优选地,所述的硫代羧酸盐中的阳离子为碱金属(例如锂、钠、钾、铷或铯,又例如钾)阳离子。
更优选地,所述的硫代羧酸盐为硫代乙酸钾。
在一些优选实施方案中,所述的阴离子主催化剂可为膦腈碱和/或硫代羧酸盐,例如1-叔丁基-4,4,4-三(二甲氨基)-2,2-二[三(二甲氨基)-正膦亚基氨基]-2λ
在一些实施方案中,所述的阳离子主催化剂中,所述的两性离子对型催化剂可为本领域常规的两性离子对型催化剂。
优选地,所述的两性离子对型催化剂由以下结构所示:
[R]
(VIII)
其中,所述的[R]
更优选地,所述的碳正离子由以下结构所示:
/>
其中,R
更优选地,所述的硅正离子由以下结构所示:
其中,R
更优选地,所述的硅正离子还可由以下结构所示:
其中,R
更优选地,所述的氧鎓离子和所述的硫鎓离子分别由以下结构所示:
其中,R
更优选地,所述的氯鎓离子和所述的溴鎓离子分别由以下结构所示:
其中,R
更优选地,所述的碘鎓离子由以下结构所示:
/>
其中,R
更优选地,所述的卓鎓离子由以下结构所示:
更优选地,所述的硼酸阴离子和所述的铝酸阴离子由以下结构所示:
其中,X
更优选地,所述的磷酸阴离子由以下任一结构所示:
更优选地,所述的磺酸阴离子和所述的磺酰亚胺阴离子分别由以下结构所示:
其中,X
更优选地,所述的锑酸阴离子和所述的砷酸阴离子分别由以下结构所示:
其中,X
进一步优选地,所述的[R]
进一步优选地,所述的[R]
进一步优选地,所述的[R]
进一步优选地,所述的[R]
在一些实施方案中,所述的阳离子主催化剂中,所述的中性路易斯酸型催化剂可为本领域常规的中性路易斯酸型催化剂。
优选地,所述的中性路易斯酸型催化剂为硼络合物或铝络合物。
更优选地,所述的硼络合物为三烷基硼或三芳基硼。
更优选地,所述的铝络合物为三烷基铝、三芳基铝、烷基双酚铝、烷基二氯化铝或双烷基氯化铝。
进一步优选地,所述的三烷基硼和所述的三烷基铝分别由以下结构所示:
其中,R
进一步优选地,所述的三芳基硼和所述的三芳基铝分别由以下结构所示:
其中,R
进一步优选地,所述的烷基双酚铝由以下结构所示:
其中,R
进一步优选地,所述的烷基二氯化铝和所述的双烷基氯化铝分别由以下结构所示:
其中,R
进一步优选地,所述的中性路易斯酸型催化剂为硼络合物(例如三芳基硼,又例如B(C
更进一步优选地,所述的中性路易斯酸型催化剂为三芳基硼类化合物,较佳地为氟代的三芳基硼类化合物;例如B(C
进一步优选地,所述的中性路易斯酸型催化剂为铝络合物(例如三芳基铝,又例如Al(C
更进一步优选地,所述的中性路易斯酸型催化剂为三芳基铝类化合物,较佳地为氟代的三芳基铝类化合物;例如Al(C
在一些实施方案中,所述的阳离子主催化剂中,所述的质子酸(酯)型催化剂可为本领域常规的质子酸(酯)型催化剂。
优选地,所述的质子酸(酯)型催化剂为磺酸、磺酸酯、磺酰亚胺、N-取代磺酰亚胺、氧鎓类质子酸、硫鎓类质子酸。
优选地,所述的质子酸(酯)型催化剂为双膦酰亚胺酯类。
优选地,所述的质子酸(酯)型催化剂为磺酸、磺酸酯、磺酰亚胺、N-取代磺酰亚胺、氧鎓类质子酸或硫鎓类质子酸。
进一步优选地,所述的磺酸、磺酸酯、磺酰亚胺和N-取代磺酰亚胺分别由以下结构所示:
其中,X
更进一步优选地,所述的氧鎓类质子酸和硫鎓类质子酸分别由以下结构所示:
其中,R
更进一步优选地,所述的双膦酰亚胺酯类由以下结构所示:
其中,R
更进一步优选地,所述的质子酸(酯)型催化剂为双膦酰亚胺酯类,例如IDPi-CF
更进一步优选地,所述的质子酸(酯)型催化剂为氧鎓类质子酸,例如[H(Et
在一些优选实施方案中,所述的阳离子主催化剂为[Ph
在一些优选实施方案中,所述的阳离子主催化剂为[Ph
在一些实施方案中,所述的聚合反应还可在助催化剂的存在下进行,所述的助催化剂为氢键供体、氢键受体和路易斯酸中的一种或多种。
在一些优选实施方案中,所述的主催化剂与所述的助催化剂的摩尔比可为本领域常规的摩尔比,优选1:1-1:10,更优选1:1-1:5,例如1:1、1:2或1:3。
在一些优选实施方案中,所述的助催化剂中,所述的氢键供体可为本领域常规的氢键供体。
优选地,所述的氢键供体为醇、硫醇、羧酸、脲和硫脲中的一种或多种,例如醇、硫醇、和硫脲中的一种或多种,又例如二苯基甲醇、苯甲醇、1-辛硫醇、和N,N'-二异丙基硫脲中的一种或多种。所述的醇优选二苯甲醇和/或苯甲醇。所述的硫醇优选1-辛硫醇。所述的羧酸优选苯乙酸。所述的脲优选二乙基脲。所述的硫脲优选N,N'-二异丙基硫脲或1-[3,5-双(三氟甲基)苯基]-3-环己基硫脲。所述的硫脲更优选N,N'-二异丙基硫脲。
在一些优选实施方案中,所述的助催化剂中,所述的氢键受体可为本领域常规的氢键受体。
优选地,所述的氢键受体为冠醚、聚乙二醇二甲醚、环糊精、杯芳烃和氮杂环穴醚中的一种或多种,例如冠醚、聚乙二醇二甲醚中的一种或多种,又例如18冠6醚。所述的环糊精优选甲基β–环糊精。所述的杯芳烃优选O(1),O(2),O(3),O(4)-四甲基对叔丁基杯芳烃。所述的聚乙二醇二甲醚优选四乙二醇二甲醚。所述的氮杂环穴醚优选4,7,13,16,21-五氧杂-1,10-二氮杂二环[8.8.5]廿三烷。
在一些优选实施方案中,所述的助催化剂中,所述的路易斯酸可为本领域常规的路易斯酸。
优选地,所述的路易斯酸为碱金属化合物、碱土金属化合物、锌化合物、硼化合物、铝化合物和稀土化合物中的一种或多种,例如锌化合物,又例如二(五氟苯基)锌。所述的碱金属化合物优选氯化锂。所述的碱土金属化合物优选氯化镁。所述的锌化合物优选二乙基锌和/或二(五氟苯基)锌。所述的硼化合物优选三(五氟苯基)硼。所述的铝化合物优选三(五氟苯基)铝。所述的稀土化合物优选三[双(三甲基硅)氨基]镧。
在一些实施方案中,所述的聚合反应还可在引发剂的存在下进行,所述的引发剂为羧酸和/或硫代羧酸。
在一些优选实施方案中,所述的主催化剂与所述的引发剂的摩尔比可为本领域常规的摩尔比,优选1:1-1:10,更优选1:1-1:5,例如1:1、1:2或1:3。
在一些优选实施方案中,所述的引发剂中,所述的羧酸为乙酸、苯甲酸或苯丙酸。
在一些优选实施方案中,所述的引发剂中,所述的硫代羧酸为硫代乙酸或硫代苯甲酸。
在一些实施方案中,所述的聚合反应的聚合温度可为本领域常规的聚合温度,优选0-120摄氏度,更优选40-80摄氏度。
在一些实施方案中,所述的聚合反应的进程可通过本领域常规的手段进行监测(例如可通过
在一些优选实施方案中,所述的制备方法包括以下步骤:有机溶剂中,在主催化剂的存在下,将所述的聚合单体进行聚合反应,即可;所述的聚合单体与所述的主催化剂的摩尔比为100:1-1600:1。
在一些优选实施方案中,所述的制备方法包括以下步骤:有机溶剂中,在主催化剂和助催化剂的存在下,将所述的聚合单体进行聚合反应,即可;所述的聚合单体与所述的主催化剂的摩尔比为100:1-1600:1,所述的主催化剂与所述的助催化剂的摩尔比为1:1-1:10。
在一些优选实施方案中,所述的制备方法包括以下步骤:有机溶剂中,在主催化剂和引发剂的存在下,将所述的聚合单体进行聚合反应,即可;所述的聚合单体与所述的主催化剂的摩尔比为100:1-1600:1,所述的主催化剂与所述的引发剂的摩尔比为1:1-1:10。
在一些优选实施方案中,所述的聚合反应包括以下步骤:有机溶剂中,在主催化剂、或者、主催化剂和助催化剂、或者、主催化剂和引发剂的存在下,将所述的聚合单体进行聚合反应,即可。
在一些优选实施方案中,所述的聚合反应包括以下步骤:将所述的聚合单体加入到反应容器中,再将反应容器连接到有惰性气体保护的真空线上,加入有机溶剂、主催化剂、或者、主催化剂和助催化剂、或者、主催化剂和引发剂,室温反应、或者、加热至聚合温度,待聚合反应结束,即可。
在一些优选实施方案中,所述的聚合反应包括以下步骤:在手套箱中将所述的聚合单体加到反应瓶中,移出手套箱,将反应瓶连接到有惰性气体保护的真空线上,并加热至相应的聚合温度,然后向溶液中加入主催化剂、或者、主催化剂和助催化剂的有机溶剂的溶液,待聚合反应结束,即可。
在一些实施方案中,所述聚合反应的原料为所述的聚合单体、所述的阳离子主催化剂及所述的溶剂。
在一些实施方案中,所述聚合反应的原料为所述的聚合单体、所述的阴离子主催化剂及所述的溶剂。
在一些实施方案中,所述聚合反应的原料为所述的聚合单体、所述的阴离子主催化剂、所述的溶剂及所述的助催化剂。
在一些实施方案中,所述聚合反应的原料为所述的聚合单体、所述的阴离子主催化剂、所述的溶剂及所述的引发剂。
在一些实施方案中,所述聚合反应的原料为所述的聚合单体、所述的阴离子主催化剂、所述的溶剂、所述的引发剂及所述的助催化剂。
在一些优选实施方案中,所述的聚合反应结束后,还可进一步包括后处理,所述的后处理可包括以下步骤:将反应液与水溶液、烯丙基氯溶液和苯甲酸溶液中的一种或多种混合,再与乙醇混合,离心或过滤,干燥即可。所述的水溶液优选水的四氢呋喃溶液,其中水的四氢呋喃溶液体积比优选1/20或1/30;所述的烯丙基氯溶液优选烯丙基氯的甲苯溶液,所述的烯丙基氯的甲苯溶液体积比优选1/2;所述的苯甲酸优选苯甲酸的氯仿溶液,所述的苯甲酸的氯仿溶液质量体积比优选10mg/mL。水的四氢呋喃溶液、烯丙基氯的甲苯溶液和苯甲酸氯仿溶液的加入是为了终止聚合链的增长。与乙醇混合是使聚合物沉降,析出固定。所述的过滤或离心之后优选包括洗涤步骤,所述的洗涤的溶剂优选乙醇。所述的洗涤的次数优选2-5次(例如3次)。所述的干燥优选真空干燥。所述的干燥的温度优选25-60摄氏度。所述的干燥的时间优选20-100小时,例如24小时。
在一些优选实施方案中,所述的聚合单体为
在一些优选实施方案中,所述的聚合单体为
在一些优选实施方案中,所述的聚合单体为
在一些优选实施方案中,所述的聚合单体为
在一些优选实施方案中,所述的聚合单体为
在一些优选实施方案中,所述的聚合单体为
在一些优选实施方案中,所述的聚合单体为
在一些优选实施方案中,所述的聚合单体为
在一些优选实施方案中,所述的聚合单体为
在一些优选实施方案中,所述的聚合单体为
在一些优选实施方案中,所述的聚合单体为
在一些优选实施方案中,所述的聚合单体为
在一些优选实施方案中,所述的聚合单体为
在一些优选实施方案中,所述的聚合单体为
在一些优选实施方案中,所述的聚合单体为
在一些优选实施方案中,所述的聚合单体为
在一些优选实施方案中,所述的聚合单体为
在一些优选实施方案中,所述的聚合单体为
在一些优选实施方案中,所述的聚合单体为
在一些优选实施方案中,所述的聚合单体为
在一些优选实施方案中,所述的聚合单体为
在一些优选实施方案中,所述的聚合单体为
在一些优选实施方案中,所述的聚合单体为
在一些优选实施方案中,所述的聚合单体为
在一些优选实施方案中,所述的聚合单体为
在一些优选实施方案中,所述的聚合单体为
在一些优选实施方案中,所述的聚合单体为
在一些优选实施方案中,所述的聚合单体为
在一些优选实施方案中,所述的聚合单体为
在一些优选实施方案中,所述的聚合单体为
在一些优选实施方案中,所述的聚合单体为
在一些优选实施方案中,所述的聚合单体为
在一些优选实施方案中,所述的聚合单体为
在一些优选实施方案中,所述的聚合单体为
在一些优选实施方案中,所述的聚合单体为
在一些优选实施方案中,所述的聚合单体为
在一些优选实施方案中,所述的聚合单体为
在一些优选实施方案中,所述的聚合单体为
在一些优选实施方案中,所述的聚合单体为
在一些优选实施方案中,所述的聚合单体为
在一些优选实施方案中,所述的聚合单体为
在一些优选实施方案中,所述的聚合单体为
在一些优选实施方案中,所述的聚合单体为
在一些优选实施方案中,所述的聚合单体为
在一些优选实施方案中,所述的聚合单体为
在一些优选实施方案中,所述的聚合单体为
在一些优选实施方案中,所述的聚合单体为
本发明还提供了一种含硫聚合物,其按照本文所述的含硫聚合物的制备方法制备获得。
本发明还提供了一种含硫聚合物,所述含硫聚合物的主链由以下结构单元中一个或多个组成,
其中,所述的含硫聚合物的聚合度大于等于50,各基团的定义如本发明任一方案所述。
所述的含硫聚合物的结构中,每一个“()”内的结构表示一个结构单元,每个结构单元是相互独立的。
在一些实施方案中,所述的含硫聚合物的聚合度为50-4900,优选190-2450,进一步优选840-1600。
在一些实施方案中,所述的含硫聚合物的数均分子量大于等于3kg/mol,优选为大于等于5kg/mol,更优选10-500kg/mol,进一步优选20-250kg/mol,更进一步优选80-250kg/mol。
在一些实施方案中,所述的含硫聚合物的分子量分布为1.0-3.0,优选1.0-1.5。
在一些实施方案中,所述的含硫聚合物为均聚物或多元共聚物。
优选地,所述多元共聚物为无规共聚物或嵌段共聚物。
优选地,所述的多元共聚物为三元共聚物,各结构单元的摩尔百分比为5-90%。
在一些实施方案中,所述的含硫聚合物的玻璃化转变温度T
在一些实施方案中,所述的含硫聚合物的断裂拉伸率为638%-1451.30%。
在一些实施方案中,所述的含硫聚合物的屈服应力为9.05MPa。
在一些实施方案中,所述的含硫聚合物的断裂应力为16.62-24.27MPa。
在一些实施方案中,所述的含硫聚合物的弹性回复率为72.3%。
本发明中,如无特殊说明,“℃”指摄氏度;“h”指小时;“min”指分钟。
硼酸阴离子:根据含硼化合物的命名规则,“含硼阴离子都用硼酸根来表明”(《无机化学命名规则》,1982版,2194页),文中的硼酸阴离子指(五氟苯基)硼酸阴离子[B(C
在不违背本领域常识的基础上,上述各优选条件,可任意组合,即得本发明各较佳实例。
本发明所用试剂和原料均市售可得。
本发明的积极进步效果在于:
本发明的制备方法以异构化为热力学驱动力,而非传统的环张力,不受聚合上限温度的限制,可在25~120℃的温度下促使一系列非张力五元环单体(包括五元环硫羰代内酯和五元环硫羰代碳酸酯)在室温至高温下进行不可逆开环聚合。由于在开环过程中伴随着协同的异构化反应,生成的含硫聚合物不会解聚成初始单体,从而促使聚合反应正向进行直至初始单体消耗完,表现为不可逆的开环聚合,实现高效定量的单体转化。本发明可抑制回咬副反应的发生,成功地将回咬副产物的含量控制在低于1%,含硫聚合物的产率最高可达99%。
本发明制备的聚硫酯的数均分子量为3.2kg/mol~431.1kg/mol,分子量分布指数为1.01~2.05。数均分子量随着单体与催化剂的比例增长而呈线性增长,具有良好的分子量控制性本发明提供的聚硫酯其玻璃化转变温度T
本发明制得的含硫均聚物及共聚物,为工业化生产环境友好的含硫高分子材料提供了便利。合成得到的含硫高分子具有分子量高、物理性能大范围可调、优异的降解性等优点,可用作塑料、橡胶、弹性体、纤维等制品。
附图说明
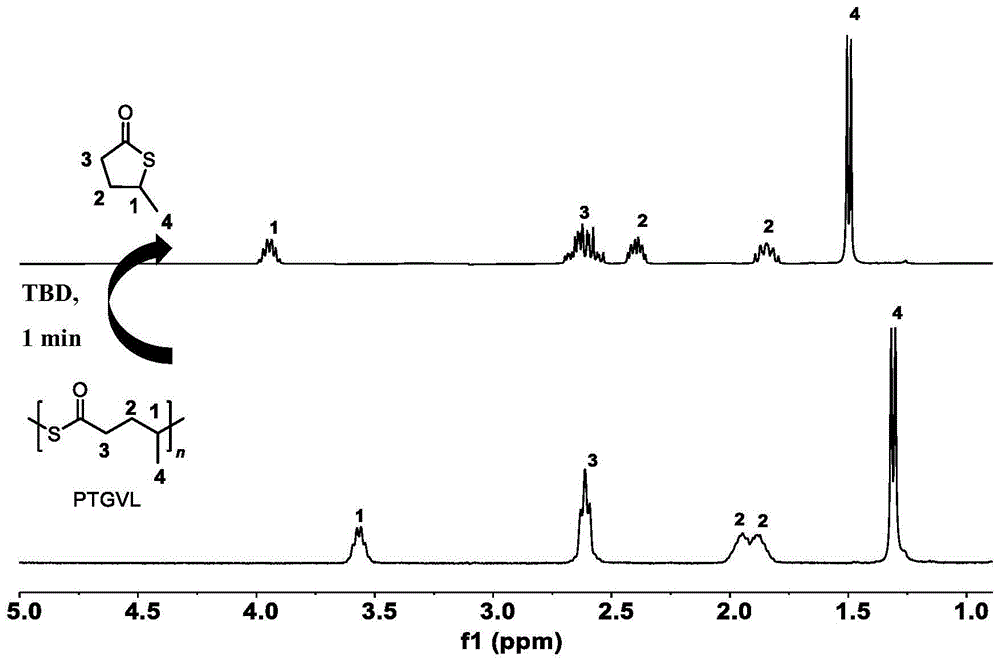
图1为实施例2得到的聚(γ-硫代戊内酯)的
图2为实施例2得到的聚(γ-硫代戊内酯)的
图3为实施例3得到的聚(γ-硫代已内酯)的
图4为实施例3得到的聚(γ-硫代己内酯)的
图5为实施例4得到的聚(γ-硫代庚内酯)的
图6为实施例4得到的聚(γ-硫代庚内酯)的
图7为实施例5得到的聚(γ-硫代辛内酯)的
图8为实施例5得到的聚(γ-硫代辛内酯)的
图9为实施例6得到的聚(γ-硫代壬内酯)的
图10为实施例6得到的聚(γ-硫代壬内酯)的
图11为实施例7得到的聚(γ-硫代癸内酯)的
图12为实施例7得到的聚(γ-硫代癸内酯)的
图13为实施例8得到的聚(γ-硫代十一内酯)的
图14为实施例8得到的聚(γ-硫代十一内酯)的
图15为实施例9得到的聚(γ-硫代十二内酯)的
图16为实施例9得到的聚(γ-硫代十二内酯)的
图17为实施例10得到的聚(γ-甲基-γ-硫代癸内酯)的
图18为实施例10得到的聚(γ-甲基-γ-硫代癸内酯)的
图19为实施例11得到的聚(β-甲基-γ-硫代辛内酯)的
图20为实施例11得到的聚(β-甲基-γ-硫代辛内酯)的
图21为实施例12得到的聚(α-甲基γ-硫代丁内酯)的
图22为实施例12得到的聚(α-甲基γ-硫代丁内酯)的
图23为实施例13得到的聚(β-甲基γ-硫代丁内酯)的
图24为实施例13得到的聚(β-甲基γ-硫代丁内酯)的
图25为实施例14得到的无规共聚物的
图26为实施例15得到的聚(顺式六氢异苯并噻吩-1-酮)的
图27为实施例15得到的聚(顺式六氢异苯并噻吩-1-酮)的
图28为实施例21得到的嵌段共聚物的
图29为实施例22得到的聚(单硫代碳酸丙烯酯)的
图30为实施例22得到的聚(单硫代碳酸丙烯酯)的
图31为聚(γ-硫代戊内酯)的M
图32为实施例2得到的聚(γ-硫代戊内酯)的TGA曲线。
图33为实施例3-10得到的聚(γ-硫代己内酯)(缩写:PTGCL)、聚(γ-硫代庚内酯)(缩写:PTGHL)、聚(γ-硫代辛内酯)(缩写:PTGOL)、聚(γ-硫代壬内酯)(缩写:PTGNL)、聚(γ-硫代癸内酯)(缩写:PTGDL)、聚(γ-硫代十一内酯)(缩写:PTGUDL)、聚(γ-硫代十二内酯)(缩写:PTGDDL)和聚(γ-甲基-γ-硫代癸内酯)(缩写:PTGMDL)的DSC曲线。
图34为实施例2得到的聚(γ-硫代戊内酯)(缩写:PTGVL)的DSC曲线、实施例12-13得到的聚(α-甲基-γ-硫代丁内酯)(缩写:PαMeTBL)和聚(β-甲基-γ-硫代丁内酯)(缩写:PβMeTBL)的DSC曲线、实施例11得到的聚(β-甲基-γ-硫代辛内酯)(缩写:PTWL)和实施例15得到的聚(顺式六氢异苯并呋喃-1-酮)(缩写:P3,4-S6TBL)的DSC曲线。
图35为实施例2得到的聚(γ-硫代丁戊酯)在1,5,7-三叠氮双环(4.4.0)癸-5-烯催化下的降解图。
图36为实施例1得到的γ-硫羰代戊内酯的
图37为实施例36得到的聚-(S)-4-甲基-1,3-二氧戊环-2-硫酮的
图38为实施例36得到的聚-(S)-4-甲基-1,3-二氧戊环-2-硫酮的
图39为实施例38得到的聚-(rac)-4-氯甲基-1,3-二氧戊环-2-硫酮的
图40为实施例39得到的聚-(R)-4-氯甲基-1,3-二氧戊环-2-硫酮的
图41为实施例41得到的聚4-苯基-1,3-二氧戊环-2-硫酮的
图42为实施例41得到的聚4-苯基-1,3-二氧戊环-2-硫酮的
图43为实施例35得到的聚-1,3-二氧戊环-2-硫酮(缩写:PEMTC)、实施例36得到的聚-(S)-4-甲基-1,3-二氧戊环-2-硫酮(缩写:S-PPMTC)、实施例37得到的聚-(R)-4-甲基-1,3-二氧戊环-2-硫酮(缩写:R-PPMTC)、实施例38得到的聚-4-氯甲基-1,3-二氧戊环-2-硫酮(缩写:PCMMTC)和实施例41得到的聚4-苯基-1,3-二氧戊环-2-硫酮(缩写:PBMTC)的DSC曲线叠加图。
图44为实施例39得到的聚-(R)-4-氯甲基-1,3-二氧戊环-2-硫酮(缩写:R-PCMMTC)的DSC曲线图。
图45为实施例40得到的聚-(S)-4-氯甲基-1,3-二氧戊环-2-硫酮(缩写:S-PCMMTC)的DSC曲线图。
图46为实施例14得到的三元共聚物的力学拉伸测试图。
图47为实施例14得到的三元共聚物的循环拉伸测试图。
图48为实施例44得到的聚-(S)-(γ-硫代戊内酯)(缩写:S-PTNGVL)的DSC曲线图。
图49为实施例44得到的聚-(S)-(γ-硫代戊内酯)(缩写:S-PTNGVL)的力学拉伸测试图。
具体实施方式
下面通过实施例的方式进一步说明本发明,但并不因此将本发明限制在所述的实施例范围之中。下列实施例中未注明具体条件的实验方法,按照常规方法和条件,或按照商品说明书选择。
实施例1
本发明所述聚合单体为自制产品,其初始原料为商品化的五元环内酯和环碳酸酯,经一步反应制备而成,制备方法没有特殊的限制,优选按照以下科技论文所述的方法进行制备:Matsumoto Y,Nakatake D,Yazaki R,Ohshima T.Chemistry–A EuropeanJournal,2018,24(23):6062-6066。所有化合物的合成步骤均类似,现以γ-硫羰代戊内酯的合成为例说明:
在1L的茄形瓶中加入121.3g(0.3mol)的劳森试剂,加入500mL的无水甲苯搅拌,形成黄色悬浊液,然后向其中加入50.1g的γ-戊内酯(0.5mol),回流搅拌5h。反应完成后,待反应温度降至常温后,加入200mL饱和碳酸钾溶液搅拌30min,分液,水相用无水甲苯萃取三次后,合并有机相。用无水硫酸钠干燥、过滤旋干后,用石油醚/乙醚梯度洗脱(40:1~5:1)柱层析收集第二组分。随后将单体加入氢化钙干燥3天后,100mTorr、60℃减压蒸馏后置于手套箱中保存待用。
本发明得到的γ-硫羰代戊内酯单体为淡黄色的液体,得到的γ-硫羰代戊内酯单体的质量为48.3g,计算得到收率为83.2%。
本发明将合成得到的γ-硫羰代戊内酯单体进行核磁共振(NMR)表征,
实施例2
在氩气气氛的手套箱中,在室温下向干燥的5mL玻璃瓶中,将0.005mmol的[Ph
本发明采用示差扫描热量法(DSC)检测聚(γ-硫代戊内酯)的熔融温度和玻璃化转变温度,结果表明,本实施例制备的聚(γ-硫代戊内酯)其玻璃化转变温度为-15.4℃。
本发明采用凝胶渗透色谱法(GPC)检测聚(γ-硫代戊内酯)的分子量和分子量分布,以四氢呋喃作为洗脱剂,流速为1.0mL/min,以聚甲基丙烯酸甲酯为标准品做标准曲线,结果表明,本实施例制备的聚(γ-硫代戊内酯)其数均分子量为27.5kg/mol,分子量分布为1.16。
实施例3
在氩气气氛的手套箱中,在室温下在干燥的5mL玻璃瓶中,将0.005mmol的[Ph
保持反应温度在室温,搅拌反应2.5h后,取少量样品溶于氘代氯仿,通过
本发明采用示差扫描热量法(DSC)检测聚(γ-硫代己内酯)的熔融温度和玻璃化转变温度,结果表明,本实施例制备的聚(γ-硫代己内酯)其玻璃化转变温度为-20.8℃。
本发明采用凝胶渗透色谱法(GPC)检测聚(γ-硫代己内酯)的分子量和分子量分布,以四氢呋喃作为洗脱剂,流速为1.0mL/min,以聚甲基丙烯酸甲酯为标准品做标准曲线,结果表明,本实施例制备的聚(γ-硫代己内酯)其数均分子量为33.6kg/mol,分子量分布为1.33。
实施例4
在氩气气氛的手套箱中,室温下在干燥的玻璃瓶中,将0.005mmol的[Ph
保持反应温度在室温,搅拌反应2.5h时后,取少量样品溶于氘代氯仿,通过
本发明采用示差扫描热量法(DSC)检测聚(γ-硫代庚内酯)的熔融温度和玻璃化转变温度,结果表明,本实施例制备的聚(γ-硫代庚内酯)其玻璃化转变温度为-21.5℃。
本发明采用凝胶渗透色谱法(GPC)检测聚(γ-硫代庚内酯)的分子量和分子量分布,以四氢呋喃作为洗脱剂,流速为1.0mL/min,以聚甲基丙烯酸甲酯为标准品做标准曲线,结果表明,本实施例制备的聚(γ-硫代庚内酯)其数均分子量为38.1kg/mol,分子量分布为1.36。
实施例5
在氩气气氛的手套箱中,室温下在干燥的玻璃瓶中,将0.005mmol的[Ph
保持反应温度在室温,搅拌反应2.5h,取少量样品溶于氘代氯仿,通过
本发明采用示差扫描热量法(DSC)检测聚(γ-硫代辛内酯)的熔融温度和玻璃化转变温度,结果表明,本实施例制备的聚(γ-硫代辛内酯)其玻璃化转变温度为-32.3℃。
本发明采用凝胶渗透色谱法(GPC)检测聚(γ-硫代辛内酯)的分子量和分子量分布,以四氢呋喃作为洗脱剂,流速为1.0mL/min,以聚甲基丙烯酸甲酯为标准品做标准曲线,结果表明,本实施例制备的聚(γ-硫代辛内酯)其数均分子量为34.5kg/mol,分子量分布为1.33。
实施例6
在氩气气氛的手套箱中,室温下在干燥的5mL玻璃瓶中,将0.005mmol的[Ph
保持反应温度在室温,搅拌反应2.5h后,取少量样品溶于氘代氯仿,通过
本发明采用示差扫描热量法(DSC)检测聚(γ-硫代壬内酯)的熔融温度和玻璃化转变温度,结果表明,本实施例制备的聚(γ-硫代壬内酯)其玻璃化转变温度为-38.8℃。
本发明采用凝胶渗透色谱法(GPC)检测聚(γ-硫代壬内酯)的分子量和分子量分布,以四氢呋喃作为洗脱剂,流速为1.0mL/min,以聚甲基丙烯酸甲酯为标准品做标准曲线,结果表明,本实施例制备的聚(γ-硫代壬内酯)其数均分子量为46.4kg/mol,分子量分布为1.26。
实施例7
在氩气气氛的手套箱中,在干燥的5mL玻璃瓶中,将0.005mmol的[Ph
保持反应温度在室温,搅拌反应2.5h后,取少量样品溶于氘代氯仿,通过
本发明采用示差扫描热量法(DSC)检测聚(γ-硫代癸内酯)的熔融温度和玻璃化转变温度,结果表明,本实施例制备的聚(γ-硫代癸内酯)其玻璃化转变温度为-44.8℃。
本发明采用凝胶渗透色谱法(GPC)检测聚(γ-硫代癸内酯)的分子量和分子量分布,以四氢呋喃作为洗脱剂,流速为1.0mL/min,以聚甲基丙烯酸甲酯为标准品做标准曲线,结果表明,本实施例制备的聚(γ-硫代癸内酯)其数均分子量为43.3kg/mol,分子量分布为1.31。
实施例8
在氩气气氛的手套箱中,在干燥的5mL玻璃瓶中,将0.005mmol的[Ph
保持反应温度在室温,搅拌反应2.5h,取少量样品溶于氘代氯仿,通过
本发明采用示差扫描热量法(DSC)检测聚(γ-硫代十一内酯)的熔融温度和玻璃化转变温度,结果表明,本实施例制备的聚(γ-硫代十一内酯)其玻璃化转变温度为-50.0℃。
本发明采用凝胶渗透色谱法(GPC)检测聚(γ-硫代十一内酯)的分子量和分子量分布,以四氢呋喃作为洗脱剂,流速为1.0mL/min,以聚甲基丙烯酸甲酯为标准品做标准曲线,结果表明,本实施例制备的聚(γ-硫代十一内酯)其数均分子量为37.1kg/mol,分子量分布为1.37。
实施例9
在氩气气氛的手套箱中,在干燥的5mL玻璃瓶中,将0.005mmol的[Ph
保持反应温度在室温,搅拌反应2.5h,取少量样品溶于氘代氯仿,通过
/>
本发明采用示差扫描热量法(DSC)检测聚(γ-硫代十二内酯)的熔融温度和玻璃化转变温度,结果表明,本实施例制备的聚(γ-硫代十二内酯)其玻璃化转变温度为-56.7℃。
本发明采用凝胶渗透色谱法(GPC)检测聚(γ-硫代十二内酯)的分子量和分子量分布,以四氢呋喃作为洗脱剂,流速为1.0mL/min,以聚甲基丙烯酸甲酯为标准品做标准曲线,结果表明,本实施例制备的聚(γ-硫代十二内酯)其数均分子量为56.2kg/mol,分子量分布为1.58。
实施例10
在氩气气氛的手套箱中,在干燥的5mL玻璃瓶中,将0.005mmol的[Ph
保持反应温度在室温,搅拌反应48h后,取少量样品溶于氘代氯仿,通过
本发明采用示差扫描热量法(DSC)检测聚(γ-甲基-γ-硫代癸内酯)的熔融温度和玻璃化转变温度,结果表明,本实施例制备的聚(γ-甲基-γ-硫代癸内酯)其玻璃化转变温度为-34.8℃。
本发明采用凝胶渗透色谱法(GPC)检测聚(γ-甲基-γ-硫代癸内酯)的分子量和分子量分布,以四氢呋喃作为洗脱剂,流速为1.0mL/min,以聚甲基丙烯酸甲酯为标准品做标准曲线,结果表明,本实施例制备的聚(γ-甲基-γ-硫代癸内酯)其数均分子量为12.8kg/mol,分子量分布为1.42。
实施例11
在氩气气氛的手套箱中,在干燥的5mL玻璃瓶中,将0.005mmol的[Ph
保持反应温度在室温,搅拌反应5h后,取少量样品溶于氘代氯仿,通过
本发明采用示差扫描热量法(DSC)检测聚(β-甲基-γ-硫代辛内酯)的熔融温度和玻璃化转变温度,结果表明,本实施例制备的聚(β-甲基-γ-硫代辛内酯)其玻璃化转变温度为3.4℃。
本发明采用凝胶渗透色谱法(GPC)检测聚(β-甲基-γ-硫代辛内酯)的分子量和分子量分布,以四氢呋喃作为洗脱剂,流速为1.0mL/min,以聚甲基丙烯酸甲酯为标准品做标准曲线,结果表明,本实施例制备的聚(β-甲基-γ-硫代辛内酯)其数均分子量为38.6kg/mol,分子量分布为1.29。
实施例12
在氩气气氛的手套箱中,在干燥的Schlenk瓶中加入0.02mmol的硫代乙酸钾和0.2mL N,N-二甲基甲酰胺,然后加入2mmol(232mg,0.2mL)的α-甲基-γ-硫羰代丁内酯单体,单体的初始浓度为5mol/L,催化剂硫代乙酸钾的浓度为50mmol/L,单体与硫代乙酸钾的摩尔比例为100:1。
移出手套箱并将Schlenk瓶连接到有氩气保护的真空线上,在80℃下搅拌反应2h。聚合反应完成后,加入0.15mL含有0.05mL烯丙基氯的甲苯溶液终止反应,取少量溶液进行
本发明采用示差扫描热量法(DSC)检测聚(α-甲基-γ-硫代丁内酯)的熔融温度和玻璃化转变温度,结果表明,本实施例制备的聚(α-甲基-γ-硫代丁内酯)其玻璃化转变温度为-30.2℃。
本发明采用凝胶渗透色谱法(GPC)检测聚(α-甲基-γ-硫代丁内酯)的分子量和分子量分布,以四氢呋喃作为洗脱剂,流速为1.0mL/min,以聚甲基丙烯酸甲酯为标准品做标准曲线,结果表明,本实施例制备的聚(α-甲基-γ-硫代丁内酯)其数均分子量为8.6kg/mol,分子量分布为1.03。
实施例13
在氩气气氛手套箱中,在干燥的Schlenk瓶中加入0.928g(8mmol,0.8mL)β-甲基-γ-硫羰代丁内酯单体,移出手套箱并将Schlenk瓶连接到有氩气保护的真空线上,在80℃下搅拌10分钟后,分别用0.8mL的甲苯溶解0.005mmol的
本发明对得到的反应液核磁共振氢谱检测,结果显示单体的转化率为99.8%,β-甲基-γ-硫代丁内酯副产物:聚(β-甲基-γ-硫代丁内酯)的比例为3:97。
本发明采用示差扫描热量法(DSC)检测聚(β-甲基-γ-硫代丁内酯)的熔融温度和玻璃化转变温度,结果表明,本实施例制备的聚(β-甲基-γ-硫代丁内酯)其玻璃化转变温度为-30.4℃。
本发明采用凝胶渗透色谱法(GPC)检测聚(β-甲基-γ-硫代丁内酯)的分子量和分子量分布,结果表明,本实施例制备的聚(β-甲基-γ-硫代丁内酯)其数均分子量为251.0kg/mol,分子量分布为1.56。
实施例14
在氩气气氛手套箱中,在干燥的Schlenk瓶中加入0.327g(3.2mmol,280μL)γ-硫羰代丁内酯和0.022g(0.17mmol,20μL)β-乙烯基-γ-硫羰代丁内酯单体,移出手套箱并将Schlenk瓶连接到有氩气保护的真空线上,在80℃下搅拌10分钟后,用0.4mL的甲苯溶解0.01mmol的
本发明对得到的反应液核磁共振氢谱检测,结果显示单体的转化率为99.9%,生成产物中回咬副产物:共聚物的比例为5:95。
本发明采用示差扫描热量法(DSC)检测共聚物的熔融温度和玻璃化转变温度,结果表明,本实施例制备的三元共聚物其玻璃化转变温度为-47.89℃,熔融温度为59.51℃。
本发明采用凝胶渗透色谱法(GPC)检测三元共聚物的分子量和分子量分布,结果表明,本实施例制备的三元共聚物其数均分子量为65.0kg/mol,分子量分布为1.73。
本发明对制得的三元无规共聚物进行力学性能的测试:力学拉伸测试实验表明三元无规共聚物的断裂伸长率为1451.30%,断裂应力为16.62MPa;另外循环拉伸测试实验表明该三元无规共聚物的弹性回复率为72.3%。
实施例15
在氩气气氛的手套箱中,在干燥的Schlenk瓶中0.1mL的甲苯、0.01mL的均三甲苯和1mmol(156mg,0.14mL)的顺式六氢异苯并呋喃-1-硫酮单体,取0.01mL的溶液进行
移出手套箱并将Schlenk瓶连接到有氩气保护的真空线上,在80℃下搅拌反应4h。聚合反应完成后,加入0.15mL含有0.05mL烯丙基氯的甲苯溶液终止反应,取少量溶液进行
本发明采用示差扫描热量法(DSC)检测聚(顺式六氢异苯并噻吩-1-酮)的熔融温度和玻璃化转变,结果表明,本实施例制备的聚(顺式六氢异苯并噻吩-1-酮)其玻璃化转变温度为65.1℃。
本发明使用热重力分析仪(TGA)测定本实施制得的聚(顺式六氢异苯并噻吩-1-酮)的热稳定性,得到的聚合物初始分解温度(T
本发明采用凝胶渗透色谱法(GPC)检测聚(顺式六氢异苯并噻吩-1-酮)的分子量和分子量分布,以四氢呋喃作为洗脱剂,流速为1.0mL/min,以聚甲基丙烯酸甲酯为标准品做标准曲线,结果表明,本实施例制备的聚(顺式六氢异苯并噻吩-1-酮)其数均分子量为22.6kg/mol,分子量分布为1.23。
实施例16
在氩气气氛的手套箱中,在干燥的Schlenk瓶中加入0.02mmol的硫代乙酸钾、0.02mmol的18冠6醚和0.2mL甲苯,然后加入2mmol(232mg,0.2mL)的α-甲基-γ-硫羰代丁内酯单体,单体的初始浓度为5mol/L,催化剂硫代乙酸钾的浓度为50mmol/L,单体与硫代乙酸钾和18冠6醚的摩尔比例为100:1:1。
移出手套箱并将Schlenk瓶连接到有氩气保护的真空线上,在80℃下搅拌反应5h。聚合反应完成后,加入0.15mL含有0.05mL烯丙基氯的甲苯溶液终止反应,取少量溶液进行
本发明采用示差扫描热量法(DSC)检测聚(α-甲基-γ-硫代丁内酯)的熔融温度和玻璃化转变,结果表明,本实施例制备的聚(α-甲基-γ-硫代丁内酯)其玻璃化转变温度为-30.2℃。
本发明采用凝胶渗透色谱法(GPC)检测聚(α-甲基-γ-硫代丁内酯)的分子量和分子量分布,以四氢呋喃作为洗脱剂,流速为1.0mL/min,以聚甲基丙烯酸甲酯为标准品做标准曲线,结果表明,本实施例制备的聚(α-甲基-γ-硫代丁内酯)其数均分子量为11.4kg/mol,分子量分布为1.02。
实施例17
在氩气气氛的手套箱中,在干燥的Schlenk瓶中加入0.01mol的苯甲酸、0.01mmol的
移出手套箱并将Schlenk瓶连接到有氩气保护的真空线上,在80℃下搅拌反应1h。聚合反应完成后,加入0.15mL含有0.05mL烯丙基氯的甲苯溶液终止反应,取少量溶液进行
本发明采用示差扫描热量法(DSC)检测聚(α-甲基-γ-硫代丁内酯)的熔融温度和玻璃化转变,结果表明,本实施例制备的聚(α-甲基-γ-硫代丁内酯)其玻璃化转变温度为-30.2℃。
本发明采用凝胶渗透色谱法(GPC)检测聚(α-甲基-γ-硫代丁内酯)的分子量和分子量分布,以四氢呋喃作为洗脱剂,流速为1.0mL/min,以聚甲基丙烯酸甲酯为标准品做标准曲线,结果表明,本实施例制备的聚(α-甲基-γ-硫代丁内酯)其数均分子量为20.0kg/mol,分子量分布为1.05。
实施例18
在氩气气氛的手套箱中,在室温下在干燥的5mL玻璃瓶中,将0.005mmol的[Ph
保持反应温度在室温,搅拌反应18h后,取少量样品溶于氘代氯仿,通过
本发明采用示差扫描热量法(DSC)检测聚(γ-硫代戊内酯)的熔融温度和玻璃化转变,结果表明,本实施例制备的聚(γ-硫代戊内酯)其玻璃化转变温度为-9.8℃。
本发明采用凝胶渗透色谱法(GPC)检测聚(γ-硫代戊内酯)的分子量和分子量分布,以四氢呋喃作为洗脱剂,流速为1.0mL/min,以聚甲基丙烯酸甲酯为标准品做标准曲线,结果表明,本实施例制备的聚(γ-硫代戊内酯)其数均分子量为133.2kg/mol,分子量分布为1.76。
实施例19
在氩气气氛的手套箱中,在干燥的玻璃瓶中加入0.01mmol的[H(Et
保持反应温度在室温,在聚合过程中取少量样品溶于氘代氯仿进行
本发明采用凝胶渗透色谱法(GPC)检测聚(γ-硫代戊内酯)的分子量和分子量分布,以四氢呋喃作为洗脱剂,流速为1.0mL/min,以聚甲基丙烯酸甲酯为标准品做标准曲线,结果表明,本实施例制备的聚(γ-硫代戊内酯)其数均分子量为32.9kg/mol,分子量分布为1.46。
实施例20
在氩气气氛的手套箱中,在干燥的Schlenk瓶中加入0.01mmol的B(C
移出手套箱并将Schlenk瓶连接到有氩气保护的真空线上,在80℃下搅拌反应1.5h。聚合反应完成后,然后加入2mL水/四氢呋喃混合液(体积比1:30)淬灭反应。取少量样品溶于氘代氯仿进行
本发明采用凝胶渗透色谱法(GPC)检测聚(γ-硫代戊内酯)的分子量和分子量分布,以四氢呋喃作为洗脱剂,流速为1.0mL/min,以聚甲基丙烯酸甲酯为标准品做标准曲线,结果表明,本实施例制备的聚(γ-硫代戊内酯)其数均分子量为74.0kg/mol,分子量分布为1.65。
实施例21
在氩气气氛手套箱中,在干燥的Schlenk瓶中加入0.232g(2.0mmol,200μL)α-甲基-γ-硫羰代丁内酯和0.40mL溶有2.3mg(0.02mmol)硫代乙酸钾的N,N-二甲基甲酰胺溶液。移出手套箱并将Schlenk瓶连接到有氩气保护的真空线上,在80℃下搅拌反应2.5小时至α-甲基-γ-硫羰代丁内酯反应完。随后用注射器加入0.204g(2.0mmol,175μL)的γ-硫羰代丁内酯单体,继续反应1小时。单体α-甲基-γ-硫羰代丁内酯的初始浓度为3.3mol/L,γ-硫羰代丁内酯的初始浓度为2.6mol/L。催化剂硫代乙酸钾的浓度为66.7mmol/L,α-甲基γ-硫羰代丁内酯与γ-硫羰代丁内酯和硫代乙酸钾摩尔比例为100:100:1。
聚合反应完成后,加入0.15mL含有0.05mL烯丙基氯的甲苯溶液终止反应,取少量溶液进行
本发明采用示差扫描热量法(DSC)检测共聚物的熔融温度和玻璃化转变温度,结果表明,本实施例制备的三元共聚物其玻璃化转变温度为-32.90℃,熔融温度为92.74℃。
本发明采用凝胶渗透色谱法(GPC)检测三元共聚物的分子量和分子量分布,结果表明,本实施例制备的三元共聚物其数均分子量为32.2kg/mol,分子量分布为1.09。
实施例22
在氩气气氛手套箱中,在干燥的Schlenk瓶中加入0.236g(2.0mmol,200μL)硫羰代碳酸丙烯酯和0.20mL溶有2.3mg(0.02mmol)硫代乙酸钾的N,N-二甲基甲酰胺溶液。移出手套箱并将Schlenk瓶连接到有氩气保护的真空线上,催化剂硫代乙酸钾的浓度为50mmol/L,单体硫羰代碳酸丙烯酯的初始浓度为5mol/L,硫羰代碳酸丙烯酯和硫代乙酸钾摩尔比例为100:1。
聚合反应完成后,加入0.15mL含有0.05mL烯丙基氯的甲苯溶液终止反应,取少量溶液进行
本发明采用凝胶渗透色谱法(GPC)检测聚单硫代碳酸丙烯酯的分子量和分子量分布,结果表明,本实施例制备的聚单硫代碳酸丙烯酯其数均分子量为9.2kg/mol,分子量分布为1.53。
实施例23
在氩气气氛的手套箱中,在干燥的5mL玻璃瓶中,将0.005mmol的[Ph
保持反应温度在室温,搅拌反应1.0h后,取少量样品溶于氘代氯仿,通过
本发明采用凝胶渗透色谱法(GPC)检测聚单硫代碳酸丙烯酯的分子量和分子量分布,以四氢呋喃作为洗脱剂,流速为1.0mL/min,以聚甲基丙烯酸甲酯为标准品做标准曲线,结果表明,本实施例制备的聚单硫代碳酸丙烯酯其数均分子量为10.2kg/mol,分子量分布为1.65。
实施例24
在氩气气氛手套箱中,在干燥的Schlenk瓶中加入4mmol(464.5mg,0.43mL)的α-甲基γ-硫羰代丁内酯单体,移出手套箱并将Schlenk瓶连接到有氩气保护的真空线上,在80℃下搅拌10分钟。用0.43mL的甲苯溶解0.01mmol的TBD以及0.01mmol的PhCOOH,并将该溶液加入到上述的Schlenk瓶中,单体的初始浓度为5mol/L,催化剂TBD及引发剂PhCOOH的浓度为12.5mmol/L,单体与TBD/PHCOOH的摩尔比例为400:1:1。
保持反应温度在80℃,聚合反应17h后,加入质量浓度为10mg/mL苯甲酸的氯仿溶液溶解产物,取少量溶液进行
本发明采用凝胶渗透色谱法(GPC)检测聚(α-甲基-γ-硫代丁内酯)的分子量和分子量分布,以四氢呋喃作为洗脱剂,流速为1.0mL/min,以聚甲基丙烯酸甲酯为标准品做标准曲线,结果表明,本实施例制备的聚(α-甲基-γ-硫代丁内酯)其数均分子量为22.6kg/mol,分子量分布为1.20。
实施例25
在氩气气氛手套箱中,在干燥的Schlenk瓶中加入2mmol(232.5mg,0.22mL)的α-甲基γ-硫羰代丁内酯单体,移出手套箱并将Schlenk瓶连接到有氩气保护的真空线上,在80℃下搅拌10分钟。用0.22mL的甲苯溶解0.02mmol的DBU以及0.02mmol的PhCOSH,并将该溶液加入到上述的Schlenk瓶中,单体的初始浓度为5mol/L,催化剂DBU及引发剂PhCOSH的浓度为50mmol/L,单体与DBU/PHCOSH的摩尔比例为100:1:1。
保持反应温度在80℃,聚合反应5h后,加入质量浓度为10mg/mL苯甲酸的氯仿溶液溶解产物,取少量溶液进行
本发明采用凝胶渗透色谱法(GPC)检测聚(α-甲基-γ-硫代丁内酯)的分子量和分子量分布,以四氢呋喃作为洗脱剂,流速为1.0mL/min,以聚甲基丙烯酸甲酯为标准品做标准曲线,结果表明,本实施例制备的聚(α-甲基-γ-硫代丁内酯)其数均分子量为9.9kg/mol,分子量分布为1.02。
实施例26
在氩气气氛手套箱中,在干燥的Schlenk瓶中加入2mmol(232.5mg,0.22mL)的α-甲基γ-硫羰代丁内酯单体,移出手套箱并将Schlenk瓶连接到有氩气保护的真空线上,在80℃下搅拌10分钟。用0.22mL的甲苯溶解0.01mmol的I
保持反应温度在80℃,聚合反应1h后,加入质量浓度为10mg/mL苯甲酸的氯仿溶液溶解产物,取少量溶液进行
本发明采用凝胶渗透色谱法(GPC)检测聚(α-甲基-γ-硫代丁内酯)的分子量和分子量分布,以四氢呋喃作为洗脱剂,流速为1.0mL/min,以聚甲基丙烯酸甲酯为标准品做标准曲线,结果表明,本实施例制备的聚(α-甲基-γ-硫代丁内酯)其数均分子量为9.39kg/mol,分子量分布为1.01。
实施例27
在氩气气氛手套箱中,在干燥的Schlenk瓶中加入4mmol(464.5mg,0.43mL)的α-甲基γ-硫羰代丁内酯单体,移出手套箱并将Schlenk瓶连接到有氩气保护的真空线上,在80℃下搅拌10分钟。用0.43mL的甲苯溶解0.01mmol的NHO N-杂环烯烃催化剂,并将该溶液加入到上述的Schlenk瓶中,单体的初始浓度为5mol/L,催化剂NHO的浓度为12.5mmol/L,单体与NHO的摩尔比例为400:1。
保持反应温度在80℃,聚合反应2h后,加入质量浓度为10mg/mL苯甲酸的氯仿溶液溶解产物,取少量溶液进行
本发明采用凝胶渗透色谱法(GPC)检测聚(α-甲基-γ-硫代丁内酯)的分子量和分子量分布,以四氢呋喃作为洗脱剂,流速为1.0mL/min,以聚甲基丙烯酸甲酯为标准品做标准曲线,结果表明,本实施例制备的聚(α-甲基-γ-硫代丁内酯)其数均分子量为43.6kg/mol,分子量分布为1.08。
实施例28
在氩气气氛手套箱中,在干燥的Schlenk瓶中加入4mmol(464.5mg,0.43mL)的α-甲基γ-硫羰代丁内酯单体,移出手套箱并将Schlenk瓶连接到有氩气保护的真空线上,在80℃下搅拌10分钟。用0.43mL的甲苯溶解0.01mmol的
保持反应温度在80℃,聚合反应1h后,加入质量浓度为10mg/mL苯甲酸的氯仿溶液溶解产物,取少量溶液进行
本发明采用凝胶渗透色谱法(GPC)检测聚(α-甲基-γ-硫代丁内酯)的分子量和分子量分布,以四氢呋喃作为洗脱剂,流速为1.0mL/min,以聚甲基丙烯酸甲酯为标准品做标准曲线,结果表明,本实施例制备的聚(α-甲基-γ-硫代丁内酯)其数均分子量为20.0kg/mol,分子量分布为1.05。
实施例29
在氩气气氛的手套箱中,在室温下在干燥的5mL玻璃瓶中,将0.01mmol的[Et
保持反应温度在室温,搅拌反应1h后,取少量样品溶于氘代氯仿,通过
本发明采用凝胶渗透色谱法(GPC)检测聚(γ-硫代戊内酯)的分子量和分子量分布,以四氢呋喃作为洗脱剂,流速为1.0mL/min,以聚甲基丙烯酸甲酯为标准品做标准曲线,结果表明,本实施例制备的聚(γ-硫代戊内酯)其数均分子量为10.2kg/mol,分子量分布为1.47。
实施例30
在氩气气氛的手套箱中,在干燥的玻璃瓶中加入0.01mmol的Ph
保持反应温度在室温,在聚合过程中取少量样品溶于氘代氯仿进行
本发明采用凝胶渗透色谱法(GPC)检测聚(γ-硫代戊内酯)的分子量和分子量分布,以四氢呋喃作为洗脱剂,流速为1.0mL/min,以聚甲基丙烯酸甲酯为标准品做标准曲线,结果表明,本实施例制备的聚(γ-硫代戊内酯)其数均分子量为8.4kg/mol,分子量分布为1.35。
实施例31
在氩气气氛的手套箱中,在干燥的玻璃瓶中加入0.01mmol的Me
保持反应温度在室温,在聚合过程中取少量样品溶于氘代氯仿进行
本发明采用凝胶渗透色谱法(GPC)检测聚(γ-硫代戊内酯)的分子量和分子量分布,以四氢呋喃作为洗脱剂,流速为1.0mL/min,以聚甲基丙烯酸甲酯为标准品做标准曲线,结果表明,本实施例制备的聚(γ-硫代戊内酯)其数均分子量为6.8kg/mol,分子量分布为1.26。
实施例32
在氩气气氛的手套箱中,在干燥的玻璃瓶中加入0.01mmol的[Et
保持反应温度在室温,在聚合过程中取少量样品溶于氘代氯仿进行
本发明采用凝胶渗透色谱法(GPC)检测聚(γ-硫代戊内酯)的分子量和分子量分布,以四氢呋喃作为洗脱剂,流速为1.0mL/min,以聚甲基丙烯酸甲酯为标准品做标准曲线,结果表明,本实施例制备的聚(γ-硫代戊内酯)其数均分子量为20.5kg/mol,分子量分布为1.06。
实施例33
在氩气气氛的手套箱中,在干燥的玻璃瓶中加入0.01mmol的C
保持反应温度在室温,在聚合过程中取少量样品溶于氘代氯仿进行
本发明采用凝胶渗透色谱法(GPC)检测聚(γ-硫代戊内酯)的分子量和分子量分布,以四氢呋喃作为洗脱剂,流速为1.0mL/min,以聚甲基丙烯酸甲酯为标准品做标准曲线,结果表明,本实施例制备的聚(γ-硫代戊内酯)其数均分子量为32.3kg/mol,分子量分布为1.88。
实施例34
在氩气气氛的手套箱中,在干燥的玻璃瓶中加入0.01mmol的Al(C
保持反应温度在室温,在聚合过程中取少量样品溶于氘代氯仿进行
本发明采用凝胶渗透色谱法(GPC)检测聚(α-甲基-γ-硫代丁内酯)的分子量和分子量分布,以四氢呋喃作为洗脱剂,流速为1.0mL/min,以聚甲基丙烯酸甲酯为标准品做标准曲线,结果表明,本实施例制备的聚(α-甲基-γ-硫代丁内酯)其数均分子量为431.1kg/mol,分子量分布为1.80。
实施例35
在氩气气氛的手套箱中,在干燥的10mL史莱克瓶中称取0.01mmol的[Et
保持反应温度在0℃,搅拌反应10min后,取少量上层清液溶于氘代氯仿,通过
本发明采用示差扫描热量法(DSC)检测聚(1,3-二氧戊环-2-硫酮)的熔融温度和玻璃化转变温度,结果表明,本实施例制备的聚(1,3-二氧戊环-2-硫酮)其玻璃化转变温度为24.5℃。
实施例36
在氩气气氛的手套箱中,在干燥的10mL史莱克瓶中称取0.01mmol的[Et
保持反应温度在0℃,搅拌反应120min后,取少量样品溶于氘代氯仿,通过
将聚合物进行核磁共振(NMR)检测,
本发明采用示差扫描热量法(DSC)检测聚-(S)-4-甲基-1,3-二氧戊环-2-硫酮的熔融温度和玻璃化转变温度,结果表明,本实施例制备的聚(S)-4-甲基-1,3-二氧戊环-2-硫酮其玻璃化转变温度为17.2℃。
本发明采用凝胶渗透色谱法(GPC)检测聚-(S)-4-甲基-1,3-二氧戊环-2-硫酮的分子量和分子量分布,以四氢呋喃作为流动相,流速为1.0mL/min,以聚甲基丙烯酸甲酯为标准品做标准曲线,结果表明,本实施例制备的聚-(S)-4-甲基-1,3-二氧戊环-2-硫酮数均分子量为38.9kg/mol,分子量分布为1.26。
实施例37
在氩气气氛的手套箱中,在干燥的10mL史莱克瓶中称取0.01mmol的[Et
保持反应温度在0℃,搅拌反应50min后,取少量样品溶于氘代氯仿,通过
本发明采用凝胶渗透色谱法(GPC)检测聚-(R)-4-甲基-1,3-二氧戊环-2-硫酮的分子量和分子量分布,以四氢呋喃作为流动相,流速为1.0mL/min,以聚甲基丙烯酸甲酯为标准品做标准曲线,结果表明,本实施例制备的聚-(R)-4-甲基-1,3-二氧戊环-2-硫酮数均分子量为45.3kg/mol,分子量分布为1.04。
本发明采用示差扫描热量法(DSC)检测聚-(R)-4-甲基-1,3-二氧戊环-2-硫酮的熔融温度和玻璃化转变温度,结果表明,本实施例制备的聚-(R)-4-甲基-1,3-二氧戊环-2-硫酮其玻璃化转变温度为18.2℃
实施例38
在氩气气氛的手套箱中,在干燥的10mL史莱克瓶中称取0.01mmol的[Et
保持反应温度在0℃,搅拌反应10min后,取少量样品溶于氘代氯仿,通过
本发明采用示差扫描热量法(DSC)检测聚4-(氯甲基)-1,3-二氧戊环-2-硫酮的熔融温度和玻璃化转变温度,结果表明,本实施例制备的聚4-(氯甲基)-1,3-二氧戊环-2-硫酮其玻璃化转变温度为41.6℃。
本发明采用凝胶渗透色谱法(GPC)检测聚4-(氯甲基)-1,3-二氧戊环-2-硫酮的分子量和分子量分布,以四氢呋喃作为流动相,流速为1.0mL/min,以聚甲基丙烯酸甲酯为标准品做标准曲线,结果表明,本实施例制备的聚4-(氯甲基)-1,3-二氧戊环-2-硫酮数均分子量为25.8kg/mol,分子量分布为1.37。
实施例39
在氩气气氛的手套箱中,在干燥的10mL史莱克瓶中称取0.01mmol的[Et
保持反应温度在0℃,搅拌反应10min后,取少量上层清液溶于氘代氯仿,通过
本发明采用示差扫描热量法(DSC)检测聚-(R)-4-(氯甲基)-1,3-二氧戊环-2-硫酮的熔融温度和玻璃化转变温度,结果表明,本实施例制备的聚(R)-4-(氯甲基)-1,3-二氧戊环-2-硫酮其玻璃化转变温度为39.8℃,熔融温度为162.8℃。
本发明采用凝胶渗透色谱法(GPC)检测聚-(R)-4-(氯甲基)-1,3-二氧戊环-2-硫酮的分子量和分子量分布,以四氢呋喃作为流动相,流速为1.0mL/min,以聚甲基丙烯酸甲酯为标准品做标准曲线,结果表明,本实施例制备的聚-(R)-4-(氯甲基)-1,3-二氧戊环-2-硫酮数均分子量为24.5kg/mol,分子量分布为1.35。
实施例40
在氩气气氛的手套箱中,在干燥的10mL史莱克瓶中称取0.01mmol的[Et
保持反应温度在0℃,搅拌反应10min后,取少量上层清液溶于氘代氯仿,通过
本发明采用示差扫描热量法(DSC)检测聚-(S)-4-(氯甲基)-1,3-二氧戊环-2-硫酮的熔融温度和玻璃化转变温度,结果表明,本实施例制备的聚-(S)-4-(氯甲基)-1,3-二氧戊环-2-硫酮其玻璃化转变温度为39.0℃,熔融温度为163.0℃。
本发明采用凝胶渗透色谱法(GPC)检测聚-(S)-4-(氯甲基)-1,3-二氧戊环-2-硫酮的分子量和分子量分布,以四氢呋喃作为流动相,流速为1.0mL/min,以聚甲基丙烯酸甲酯为标准品做标准曲线,结果表明,本实施例制备的聚-(S)-4-(氯甲基)-1,3-二氧戊环-2-硫酮数均分子量为19.3kg/mol,分子量分布为1.43。
实施例41
在氩气气氛的手套箱中,在干燥的10mL史莱克瓶中称取0.01mmol的[Et
保持反应温度在0℃,搅拌反应10min后,取少量样品溶于氘代氯仿,通过
本发明采用示差扫描热量法(DSC)检测聚4-苯基-1,3-二氧戊环-2-硫酮的熔融温度和玻璃化转变温度,结果表明,本实施例制备的聚4-苯基-1,3-二氧戊环-2-硫酮其玻璃化转变温度为59.5℃。
本发明采用凝胶渗透色谱法(GPC)检测聚4-苯基-1,3-二氧戊环-2-硫酮的分子量和分子量分布,以四氢呋喃作为流动相,流速为1.0mL/min,以聚4-苯基-1,3-二氧戊环-2-硫酮为标准品做标准曲线,结果表明,本实施例制备的聚单硫代碳酸酯其数均分子量为19.7kg/mol,分子量分布为2.05。
实施例42
在氩气气氛的手套箱中,在干燥的5mL玻璃瓶中称取0.05mmol(7.6mg,0.0074mL)的DBU和0.05mmol(5.4mg,0.0052mL)的苯甲醇相混合,加入1.0mL甲苯至充分溶解。然后向5mL玻璃瓶中加入5mmol(590.7mg,0.47mL)的硫羰代碳酸酯单体(R)-4-甲基-1,3-二氧戊环-2-硫酮,在25℃下反应。单体的初始浓度为3.7mol/L,催化剂DBU的浓度为37mmol/L,单体与DBU的摩尔比例为100:1。
保持反应温度在25℃,搅拌反应60h后,取少量样品溶于氘代氯仿,通过
本发明采用凝胶渗透色谱法(GPC)检测聚单硫代碳酸酯的分子量和分子量分布,以四氢呋喃作为流动相,流速为1.0mL/min,以聚甲基丙烯酸甲酯为标准品做标准曲线,结果表明,本实施例制备的聚单硫代碳酸酯其数均分子量为4.9kg/mol,分子量分布为1.38。
实施例43
在氩气气氛的手套箱中,在干燥的5mL玻璃瓶中称取0.05mmol(7.6mg,0.0074mL)的DBU和0.05mmol(5.4mg,0.0052mL)的苯甲醇相混合,加入0.5mL甲苯至充分溶解。在另一个5mL玻璃瓶中称取0.05mmol(18.5mg)的1-[3,5-双(三氟甲基)苯基]-3-环己基硫脲和5mmol(590.7mg,0.47mL)的硫羰代碳酸酯单体(R)-4-甲基-1,3-二氧戊环-2-硫酮相混合,加入0.5mL甲苯至充分溶解。将两个玻璃瓶中溶液充分混合后在25℃下反应。单体的初始浓度为3.7mol/L,催化剂DBU的浓度为37mmol/L,单体与DBU的摩尔比例为100:1。
保持反应温度在25℃,搅拌反应120h后,取少量样品溶于氘代氯仿,通过
本发明采用凝胶渗透色谱法(GPC)检测聚单硫代碳酸酯的分子量和分子量分布,以四氢呋喃作为流动相,流速为1.0mL/min,以聚甲基丙烯酸甲酯为标准品做标准曲线,结果表明,本实施例制备的聚单硫代碳酸酯其数均分子量为3.2kg/mol,分子量分布为1.49。
实施例44
在氩气气氛的手套箱中,在室温下在干燥的20mL玻璃瓶中,将0.005mmol的[Et
保持反应温度在室温,搅拌反应18h后,取少量样品溶于氘代氯仿,通过
本发明采用示差扫描量热法(DSC)检测聚-(S)-(γ-硫代戊内酯)的熔融温度和玻璃化转变温度,结果表明,本实施例制备的聚-(S)-(γ-硫代戊内酯)其玻璃化转变温度约为–8.8℃,熔点约为82.3℃。
本发明采用热重力分析仪(TGA)测定检测聚-(S)-(γ-硫代戊内酯)的热稳定性,结果表明,本实施例制备的聚-(S)-(γ-硫代戊内酯)其初始分解温度(T
本发明采用凝胶渗透色谱法(GPC)检测聚-(S)-(γ-硫代戊内酯)的分子量和分子量分布,以四氢呋喃作为洗脱剂,流速为1.0mL/min,以聚甲基丙烯酸甲酯为标准品做标准曲线,结果表明,本实施例制备的聚-(S)-(γ-硫代戊内酯)其数均分子量为106.1kg/mol,分子量分布为1.40。
对本发明制得的聚-(S)-(γ-硫代戊内酯)进行力学拉伸测试,结果表明,本实施例制备的(S)-聚(γ-硫代戊内酯)其断裂伸长率为638%,屈服应力为9.05MPa,断裂应力为24.27MPa。
实施例45
在氩气气氛的手套箱中,在室温下在干燥的20mL玻璃瓶中,将0.005mmol的[Et
保持反应温度在室温,搅拌反应18h后,取少量样品溶于氘代氯仿,通过
本发明采用示差扫描量热法(DSC)检测聚-(R)-(γ-硫代戊内酯)的熔融温度和玻璃化转变温度,结果表明,本实施例制备的聚-(R)-(γ-硫代戊内酯)其玻璃化转变温度约为–8.9℃,熔点约为81.0℃。
本发明采用凝胶渗透色谱法(GPC)检测聚-(R)-(γ-硫代戊内酯)的分子量和分子量分布,以四氢呋喃作为洗脱剂,流速为1.0mL/min,以聚甲基丙烯酸甲酯为标准品做标准曲线,结果表明,本实施例制备的聚-(R)-(γ-硫代戊内酯)其数均分子量为101.2kg/mol,分子量分布为1.68。
对比例1
在氩气气氛的手套箱中,在干燥的Schlenk瓶中加入0.02mmol的硫代乙酸钾、0.02mmol的18冠6醚和0.2mL N,N-二甲基甲酰胺,然后加入2mmol(232mg,0.2mL)的γ-硫羰代戊内酯单体,单体的初始浓度为5mol/L,催化剂硫代乙酸钾的浓度为50mmol/L,单体与硫代乙酸钾和18冠6醚的摩尔比例为100:1:1。
移出手套箱并将Schlenk瓶连接到有氩气保护的真空线上,在80℃下搅拌反应48h后,加入0.15mL含有0.05mL烯丙基氯的甲苯溶液终止反应,取少量溶液进行
效果实施例1:性能参数测定:
1.1分子量控制性
本发明通过型号为Waters E2695的凝胶渗透色谱仪测定聚硫酯的数均分子量(M
在[Ph
1.2热学性能分析
本发明通过TA公司的TGA 550热重力分析仪进行热重分析(TGA),得到聚合物的热分解温度,热重分析测试在N
本发明通过TA公司型号为DSC 2000的示差扫描量热仪,对上述实施例制得的聚硫酯进行示差扫描热量法(DSC)分析,代表性曲线如图33和34所示。测试结果表明,本发明提供的聚硫酯的玻璃化转变温度T
其中,实施例3-10得到的聚(γ-硫代己内酯)(缩写:PTGCL)、聚(γ-硫代庚内酯)(缩写:PTGHL)、聚(γ-硫代辛内酯)(缩写:PTGOL)、聚(γ-硫代壬内酯)(缩写:PTGNL)、聚(γ-硫代癸内酯)(缩写:PTGDL)、聚(γ-硫代十一内酯)(缩写:PTGUDL)、聚(γ-硫代十二内酯)(缩写:PTGDDL)和聚(γ-甲基-γ-硫代癸内酯)(缩写:PTGMDL)的DSC曲线如图33所示。
实施例2得到的聚(γ-硫代戊内酯)(缩写:PTGVL)的DSC曲线、实施例12-13得到的聚(α-甲基-γ-硫代丁内酯)(缩写:PαMeTBL)和聚(β-甲基-γ-硫代丁内酯)(缩写:PβMeTBL)的DSC曲线、实施例11得到的聚(β-甲基-γ-硫代辛内酯)(缩写:PTWL)和实施例15得到的聚(顺式六氢异苯并呋喃-1-酮)(缩写:P3,4-S6TBL)的DSC曲线如图34所示。
实施例35得到的聚-1,3-二氧戊环-2-硫酮(缩写:PEMTC)、实施例36得到的聚-(S)-4-甲基-1,3-二氧戊环-2-硫酮(缩写:S-PPMTC)、实施例37得到的聚-(R)-4-甲基-1,3-二氧戊环-2-硫酮(缩写:R-PPMTC)、实施例38得到的聚-4-氯甲基-1,3-二氧戊环-2-硫酮(缩写:PCMMTC)和实施例41得到的聚4-苯基-1,3-二氧戊环-2-硫酮(缩写:PBMTC)的DSC曲线叠加图如图43所示。
实施例39得到的聚-(R)-4-氯甲基-1,3-二氧戊环-2-硫酮(缩写:R-PCMMTC)的DSC曲线图如图44所示。
实施例40得到的聚-(S)-4-氯甲基-1,3-二氧戊环-2-硫酮(缩写:S-PCMMTC)的DSC曲线图如图45所示。
实施例44得到的聚-(S)-聚(γ-硫代戊内酯)(缩写:S-PTGVL)的DSC曲线图如图48所示。
1.3力学性能测试
本发明对实施例所制得聚合物进行力学性能的测试,首先用四氟乙烯模板将聚合物通过热压制备成聚合物膜并裁成哑铃型拉伸样条,拉伸的有效尺寸是10×5×1mm
实施例44制得的聚-(S)-(γ-硫代戊内酯)力学拉伸测试结果如图49所示,力学拉伸测试(如图49所示)实验表明制备的(S)-聚(γ-硫代戊内酯)其断裂伸长率为638%,屈服应力为9.05MPa,断裂应力为24.27MPa。这表明本发明提供的聚(γ-硫代丁内酯)是一种强而韧的高分子材料,力学拉伸测试各项指标均优于低密度聚乙烯(断裂伸长率为430%,断裂应力为10.6MPa)和等规聚丙烯(断裂伸长率为420%,断裂应力为26.0MP),接近高密度聚丙烯的拉伸性能(断裂伸长率为420%,断裂应力为26.0MP)。在断裂伸长率方面,聚-(S)-(γ-硫代戊内酯)是商品化低密度聚乙烯和等规聚丙烯的1.5倍,说明其韧性要明显优于商品化低密度聚乙烯和等规聚丙烯。
对实施例14制得的三元无规共聚物进行力学性能的测试:力学拉伸测试(如图46所示)断裂伸长率为1451.30%,断裂应力为16.62MPa;另外循环拉伸测试(如图47所示)实验表明该三元无规共聚物的弹性回复率为72.3%,这表明本发明提供的三元无规共聚物是一种强而韧的弹性体高分子材料。力学拉伸测试各项指标均优于商业化的乙丙橡胶(断裂伸长率为275.0%,断裂应力为5.70Mpa,回复率为50-80%)。
1.4可降解性分析
本发明所述的聚硫酯和聚单硫代碳酸酯具有商品化聚烯烃无法比拟的可降解性。以聚(γ-硫代戊内酯)为例,在特定条件下可发生快速可控的降解:常温下,当加入1,5,7-三叠氮双环(4.4.0)癸-5-烯(TBD)为降解催化剂时,1min之内实施例4所得聚(γ-硫代戊内酯)即可快速定量的降解成γ-硫代戊内酯,如图35所示。具体的反应过程为:取232.4mg在干燥过的聚(γ-硫代戊内酯)溶解于2.5mL无水的二氯甲烷中,向得到的透明溶液中加入0.5mL TBD(0.02mol/L)的二氯甲烷溶液,搅拌反应1min即发现聚合物已完全降解成γ-硫代戊内酯。
通过对本发明所得聚合物进行以上性能分析,可见,本发明制得的含硫均聚物及共聚物,为工业化生产环境友好的含硫高分子材料提供了便利。合成得到的含硫高分子具有分子量高、良好的分子量控制性、物理性能大范围可调、优异的降解性等优点,可用作塑料、橡胶、弹性体、纤维等制品,具有广泛的应用。
- 基于氨基环氧基开环聚合的苯硼酸聚合物及其制备方法和应用
- 一种低温热可逆型热塑性聚氨酯聚合物的制备方法及聚合物
- 一种具有阻燃性能的线性热可逆聚氨酯聚合物的制备方法及聚合物
- 基于降冰片烯的开环聚合物,降冰片烯开环聚合物的加氢产物及它们的制备方法
- 基于降冰片烯的开环聚合物,降冰片烯开环聚合物的加氢产物及它们的制备方法
