用于治疗癌症的mRNA及在制备抗癌药中的应用
文献发布时间:2024-01-17 01:16:56
技术领域
本发明属于生物医药领域,特别是涉及用于治疗癌症的mRNA及在制备抗癌药中的应用。
背景技术
ecDNA最早是在1964年由Alix Bassel和Yasuo Hoota对高等生物的染色体进行研究的时候发现的。科学家们发现ecDNA大量存在于人类多种癌症类型中,而在正常组织中几乎观察不到ecDNA的存在。癌基因扩增是一种常见的癌症突变类型,可发生在染色体内的均质染色区或染色体外。近一半的癌症类型中存在染色体外DNA(ecDNA),与其他局部扩增相比,携带癌基因的ecDNA的扩增与癌症患者更差的预后密切相关。癌基因扩增是癌细胞生存的手段,由于ecDNA是维持癌基因表达所必需的,而ecDNA的消除影响了癌细胞的存活,因此一些癌细胞是嗜ecDNA的,这使得将ecDNA做为癌症的治疗靶点具有重要意义。减少肿瘤细胞中的ecDNA将对癌症治疗领域产生卓越贡献。
近十年来,mRNA药物受到越来越多的关注。mRNA药物的传递和转录机制使其能够克服传统药物的局限性,为治疗依赖于蛋白质表达的疾病提供了新的途径。经过数十年的研究与发展,mRNA药物已经具备了以下优势:1.安全性,mRNA不具有传染性,也不能整合进基因组,不存在感染或导致基因突变的潜在风险,且抗原性弱,不易发生过敏等不良反应,mRNA也能够被细胞降解,在体内半衰期可以通过使用各种修饰和递送方法来调节;2.高疗效,mRNA是最小的遗传载体,经过合适的修饰会使mRNA更稳定,能够高效翻译为蛋白;3.便于生产,mRNA主要由体外转录反应进行生产,成本低,产量高,具有大量生产的潜力;4.灵活性,与传统的药物不同,mRNA药物可以很容易地改变其序列以适应不同的治疗需求。mRNA药物需要通过载体输送到细胞内部,才能被转录和翻译。常见的载体分为病毒载体与非病毒载体。其中,病毒载体虽然递送效率高,但存在免疫原性和毒性等安全性问题,限制了其临床应用。非病毒载体主要包括基于脂质的递送系统、基于聚合物的纳米颗粒和无机纳米颗粒。其中,脂质纳米颗粒(LNP)是寡核苷酸药物和mRNA药物使用最广泛的非病毒递送系统之一,其优点包括易于生产,可生物降解,能够保护RNA分子免受RNase降解和肾脏清除,促进胞吞,抑制内体的降解。近年来,mRNA药物在治疗肿瘤方面取得了巨大的进展。相比传统的小分子化学药物,mRNA药物治疗肿瘤的优势在于靶点更加精准,具有更高的特异性和选择性,可塑性强,同时毒副作用低,不会对患者DNA造成永久性影响等。截至2023年3月,全球已有20余种mRNA抗肿瘤药物进入临床试验,几个mRNA药物已被证明能有效抑制肿瘤生长和扩散,同时对于转移性癌症也有一定的疗效。尽管目前尚未有用于肿瘤治疗的mRNA获批上市,但是已有不少药物进入II期临床,发展趋势非常迅速。未来,基于mRNA技术的肿瘤治疗将迎来全新的发展机遇,并将成为今后肿瘤治疗的一个重要方向。
发明内容
本发明的目的是克服现有技术的不足,提供用于治疗癌症的mRNA。
本发明的第二个目的是提供用于治疗癌症的mRNA在制备抗癌药中的应用。
本发明的第三个目的是提供包括上述用于治疗癌症的mRNA的药物复合物。
本发明的技术方案概述如下:
用于治疗癌症的mRNA,mRNA为DNase1L3 mRNA或GC-DNase mRNA,所述DNase1L3mRNA的碱基序列如SEQ ID NO.1所示;所述GC-DNase mRNA的碱基序列如SEQ ID NO.2所示。
所述癌症为肝癌、肺癌或乳腺癌。
用于治疗癌症的mRNA在制备抗癌药中的应用。
包括上述用于治疗癌症的mRNA的药物复合物,是将所述用于治疗癌症的mRNA与一种或多种脂质复合,制成脂质体、脂质纳米颗粒或脂质复合物。
本发明的优点:
本发明的两种用于治疗癌症的mRNA,首次以ecDNA作为癌症治疗的靶点,通过减少肿瘤中的ecDNA含量发挥抗肿瘤作用,在建立的癌症动物模型中,包括肝细胞癌,乳腺癌和肺癌,两种mRNA治疗均显著减小了肿瘤体积,减缓了肿瘤的生长,延长了小鼠的生存期。
附图说明
图1为肝癌模型小鼠肿瘤生长曲线;
图2为肺癌模型小鼠肿瘤生长曲线。
图3为乳腺癌模型小鼠肿瘤生长曲线。
图4为肝癌模型小鼠生存曲线。
图5为肺癌模型小鼠生存曲线。
图6为乳腺癌模型小鼠生存曲线。
图7为肝癌模型小鼠肿瘤组织免疫组织化学染色病理评分。
图8为肺癌模型小鼠肿瘤组织免疫组织化学染色病理评分。
图9为乳腺癌模型小鼠肿瘤组织免疫组织化学染色病理评分。
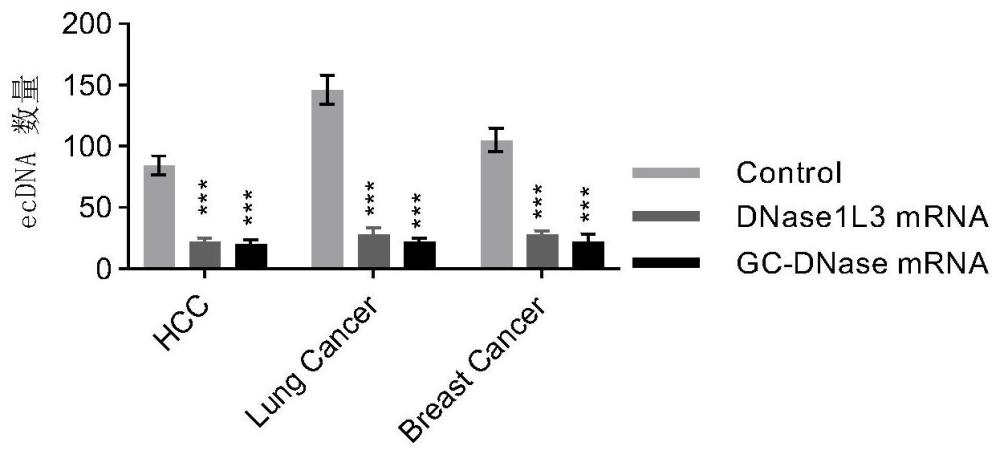
图10为实施例2,3,4的模型小鼠肿瘤组织ecDNA含量统计。
具体实施方式
下面通过具体实施例对本发明作进一步的说明。
实施例1
用于治疗癌症的mRNA,其mRNA为DNase1L3 mRNA或GC-DNase mRNA,所述DNase1L3mRNA的碱基序列如SEQ ID NO.1所示;所述GC-DNase mRNA的碱基序列如SEQ ID NO.2所示。
DNase1L3 mRNA或GC-DNase mRNA为人工合成。
mRNA由体外转录进行生产。首先分别合成DNase1L3 mRNA的DNA模板序列SEQ IDNO.3和GC-DNase mRNA的DNA模板序列SEQ ID NO.4,将DNA模板序列分别克隆至质粒载体pUC57-mini-Kana-BsmBI free-terminator-T7 deleted-100A-BspQI(市售)中,进行体外转录,纯化,分别获得DNase1L3 mRNA和GC-DNase mRNA。
实施例2
mRNA-LNP脂质纳米颗粒的制备(mRNA分别为DNase1L3 mRNA和GC-DNase mRNA)
将体外合成的mRNA进行LNP包裹,LNP包裹委托锘海生物科学仪器(上海)有限公司完成。公司采用FlowOrigin M1脂质纳米粒试剂盒,通过铭汰Microflow系列微流控纳米药物递送平台,进行mRNA的包裹,得到mRNA-LNP脂质纳米颗粒用于小鼠尾静脉注射给药。
实施例3
mRNA处理SCID小鼠中患者来源的肿瘤异种移植肝癌模型的治疗功效的评价(mRNA分别为DNase1L3 mRNA和GC-DNase mRNA)
取8个新鲜的手术肿瘤组织(F0),在8名患者手术后立即冻存,未经任何其他处理。根据《赫尔辛基宣言》,每个病人都签署了书面的知情同意书,并在南开大学伦理委员会批准后进行。将F0组织的碎片皮下分别植入8只4-6周龄SCID小鼠中,当肿瘤大小达到100-200mm
与对照组小鼠相比,两组mRNA(mRNA分别为DNase1L3 mRNA和GC-DNase mRNA)治疗组小鼠的肿瘤体积显著减小,肿瘤生长速度减慢,小鼠的生存期也明显延长。同时,组织病理学分析结果显示,肿瘤部位相应mRNA药物所编码的蛋白水平表达量升高,且与肿瘤恶性演进相关的蛋白标志物包括Vimentin,Twist1和Zeb1表达水平显著降低。此外,肿瘤组织部位的ecDNA含量在mRNA治疗组中显著降低。
实施例4
mRNA处理BALB/c-nude小鼠中肺癌模型的治疗功效的评价(mRNA分别为DNase1L3mRNA和GC-DNase mRNA)
肺癌细胞A549长至铺满培养皿底达到80%以上。观察到细胞活力旺盛,使用胰蛋白酶消化细胞,并用PBS清洗。通过细胞计数板进行计数,并用预冷PBS重悬细胞。选择6-8周龄的BALB/c-nude鼠,进行皮下注射1×10
与对照组小鼠相比,两组mRNA(mRNA分别为DNase1L3 mRNA和GC-DNase mRNA)治疗组小鼠的肿瘤体积显著减小,肿瘤生长速度减慢,小鼠的生存期也明显延长。同时,组织病理学分析结果显示,肿瘤部位相应mRNA药物所编码的蛋白水平表达量升高,且与肿瘤恶性演进相关的蛋白标志物包括Vimentin,Twist1和Zeb1表达水平显著降低。此外,肿瘤组织部位的ecDNA含量在mRNA治疗组中显著降低。
实施例5
mRNA处理BALB/c-nude小鼠中乳腺癌模型的治疗功效的评价(mRNA分别为DNase1L3 mRNA和GC-DNase mRNA)
将MDA-MB-231乳腺癌细胞(1×10
与对照组小鼠相比,两组mRNA(mRNA分别为DNase1L3 mRNA和GC-DNase mRNA)治疗组小鼠的肿瘤体积显著减小,肿瘤生长速度减慢,小鼠的生存期也明显延长。同时,组织病理学分析结果显示,肿瘤部位相应mRNA药物所编码的蛋白水平表达量升高,且与肿瘤恶性演进相关的蛋白标志物包括Vimentin,Twist1和Zeb1表达水平显著降低。此外,肿瘤组织部位的ecDNA含量在mRNA治疗组中显著降低。
实验证明,用本发明的mRNA按本领域常规技术手段制备的脂质体或脂质复合物也可以制备用于治疗癌症的mRNA的药物复合物。
- 一种三萜类化合物及其制备方法和在制备抗癌药物中的应用
- 葛根素衍生物在制备抗癌药物中的应用以及一种治疗癌症的药物
- 葛根素衍生物在制备抗癌药物中的应用以及一种治疗癌症的药物
