基于数字PCR检测鼻咽癌中EB病毒的引物探针组合
文献发布时间:2024-01-17 01:26:37
技术领域
本发明涉及医学检测技术领域,具体涉及一种用于检测EB病毒的引物组合及其试剂盒。
背景技术
鼻咽癌(Nasopharyngeal carcinoma,NPC)是来源于鼻咽粘膜上皮的恶性肿瘤,主要流行于中国南部、东南亚及非洲北部等地区。鼻咽癌发病分布具有独特的地域特点,其高发于我国南方地区,尤其是在两广的分布呈现典型的聚集的现象,具有代表性的有广东的中山地区和广西的苍梧县,发病率高达50/100000。鼻咽癌男性发病率约为女性的2-3倍,在中国南方男性中的发病率高达30.9/10万人。鼻咽癌的发生一般认为主要与遗传因素、环境因素和EB病毒(Epstein-Barr virus,EBV)感染等密切相关。现已证实EBV感染是鼻咽癌发生的重要原因之一。
EB病毒(Epstein-Barr virus,EBV)是Epstein和Barr在1964年首先从非洲儿童淋巴瘤(Burkitt淋巴瘤)的活检组织中发现的一种DNA病毒颗粒,属于γ病毒亚科,EBV基因组长约172Kb,编码约85个基因,EBV具有疱疹病毒潜伏感染的特点,在潜伏期和裂解期表达不同的病毒基因和蛋白。EBV潜伏期表达的基因主要包括6个核抗原(EBV nuclear antigens,EBNAs),即EBNA1、EBNA2、EBNA3A、EBNA3B、EBNA3C和BNA-LP,2个EBV编码小RNA(EBV-encodedsmall RNAs,EBERs),即EBER1和EBER2,3个潜伏膜蛋白(latent membrane proteins,LMPs),即LMP1、LMP2A和LMP2B,BamHI-A向右开放读码框的转录产物(BamHI-A rightwardtranscripts,BARTs)以及微小RNAs(micro RNAs,包括miR-BHRF1和miR-BART)。在裂解性感染时,大量的病毒结构基因和调节基因表达,包括即刻早期基因、早期基因和晚期基因。
EB病毒在世界范围内广泛存在,90%的成年人携带EBV。EBV感染多为无症状感染,但部分人群可发生良性或恶性疾病。EB病毒除了可引发鼻咽癌之外,还与多种肿瘤的发生有关,如Burkitt淋巴瘤、霍奇金淋巴瘤、NK/T细胞淋巴瘤、胃癌、移植后淋巴增生性疾病等,总的来说,EBV与1.5%的人类癌症有关。鼻咽癌是所有EBV相关肿瘤中与EBV关系最为密切的肿瘤,病毒学检测显示所有鼻咽癌细胞中均可检测到EBV DNA和EBV编码物质。
当前,鼻咽癌的诊断以鼻腔镜的检测为主,但由于操作烦琐、价格昂贵,不便于鼻咽癌检测的普及。以放射治疗为主的综合治疗是治疗鼻咽癌的主要方式,随着该疗法的广泛应用,鼻咽癌患者的5年生存率达80%以上,因此临床上鼻咽癌的早诊早治成为提高患者生存率、改善预后的关键突破口。
血浆EBV DNA检测是继EBV抗体检测之后最后关注的指标,已经获得了广泛的认可。在鼻咽癌治疗中检测血浆EB DNA的原理是由于鼻咽癌肿瘤细胞在凋亡的过程中会释放EB V DNA。这些由NPC释放的EBV DNA片段与病毒裂解阶段释放片段相比具有更短小的特点(少于181bp),这使得它们可以通过聚合酶链式反应(PCR)的方法进行分析和定量。
血浆中EBV DNA检测不但在鼻咽癌的诊断和筛查中表现出较高的应用价值,事实上,目前已经应用于鼻咽癌管理的整个流程,包括与TNM分期做为参考进行治疗方的制定,治疗过程的监测,治疗之后预测预后,治疗后是否辅助化疗方案的制定等。
实时荧光定量PCR方法是目前血浆EBV DNA检测应用最普遍的方法。常规临床应用中使用实时荧光定量PCR方法检测血浆EBV DNA会受到检测阈值的限制,导致即使同一样本在不同实验室中,检测的EBV DNA水平存在显著的实验室间差异。且对于低拷贝靶标的样本,荧光定量PCR检测方法的灵敏度和精确度不足,不利于进行鼻咽癌早期筛查以及治疗后的监测和预后。因此有必要研制出灵敏度更高、更精确的血浆EBV DNA定量监测试剂盒,以提高EBV DNA检测临床应用的可靠性。
数字PCR是近年来出现的较为先进的方法,液滴芯片式数字PCR平台采用绝对定量的方式,不依赖标准曲线和定量参考品,直接检测目标序列的拷贝数,它的原理是将一个标准PCR反应通过芯片分配到大量微小的油包水液滴当中,每个液滴种包含或不包含一个或多个拷贝的目标分子(DNA模板),实现“单分子模板PCR扩增,”在芯片中进行PCR扩增后,通过拍照对液滴方式来检测液滴的荧光强度,最后通过阳性液滴的比例计算出目标核酸分子的绝对拷贝数。因此,使用该方法进行EBV DNA检测和定量,有望提高检测的灵敏度和准确度。
目前临床上检测EBV-DNA主要是结合实时荧光定量PCR技术和TaqMan技术,根据EB病毒基因组保守区域设计特异引物及TaqMan探针,该探针能与引物扩增区域中间的一段DNA模板发生特异性结合,在PCR延伸过程中,Taq酶的外切酶活性将探针5′段荧光基团切下来,使之游离在体系中,脱离3′段淬灭基团的淬灭作用而发出荧光,可供相应荧光仪器检测,从而实现对EB病毒核酸的检测。在实时荧光定量PCR技术中,引物探针组合是决定检测灵敏度和特异性的关键因素。
目前国内外已有多款基于实时荧光定量PCR技术检测EB病毒的试剂盒,但是这些试剂盒检测灵敏度相对偏低,不利于临床应用中该病毒引发的疾病中的肿瘤早筛和预后治疗。因此提高EB病毒检测的灵敏度,在EB病毒感染疾病的诊断及临床应用中尤为重要。
发明内容
根据第一方面,在一实施例中,提供一种引物组合,所述引物组合用于检测EB病毒,所述引物组合用于检测第一目标序列、第二目标序列、第三目标序列中的至少一种,所述第一目标序列包含SEQ ID NO:1所示核苷酸序列所构成的组,所述第二目标序列包含SEQID NO:5所示核苷酸序列所构成的组,所述第三目标序列包含SEQ ID NO:9所示核苷酸序列所构成的组。
根据第二方面,在一实施例中,提供一种试剂盒,包括第一方面任意一项所述的引物组合。
根据第三方面,在一实施例中,提供第一目标序列、第二目标序列、第三目标序列中的至少一种在制备检测试剂中的用途;所述第一目标序列包含SEQ ID NO:1所示核苷酸序列所构成的组,所述第二目标序列包含SEQ ID NO:5所示核苷酸序列所构成的组,所述第三目标序列包含SEQ ID NO:9所示核苷酸序列所构成的组。
在一实施例中,本发明提供的引物可以明显提高临床检测EB病毒的灵敏度,特别是针对早期样本的检测具有较高准确性。
附图说明
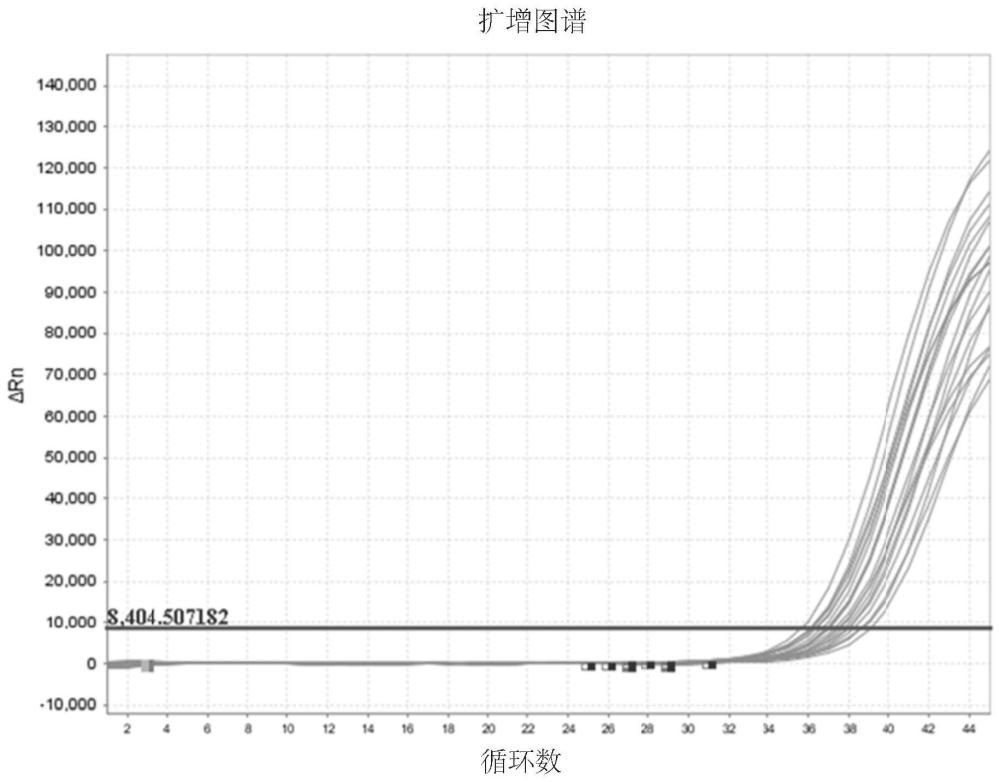
图1为qPCR平台最低检测下限LOD检测图;
图2为数字PCR平台低浓度样本(400copies/mL)测定图。
具体实施方式
下面通过具体实施方式结合附图对本发明作进一步详细说明。在以下的实施方式中,很多细节描述是为了使得本申请能被更好的理解。然而,本领域技术人员可以毫不费力的认识到,其中部分特征在不同情况下是可以省略的,或者可以由其他材料、方法所替代。在某些情况下,本申请相关的一些操作并没有在说明书中显示或者描述,这是为了避免本申请的核心部分被过多的描述所淹没,而对于本领域技术人员而言,详细描述这些相关操作并不是必要的,他们根据说明书中的描述以及本领域的一般技术知识即可完整了解相关操作。
另外,说明书中所描述的特点、操作或者特征可以以任意适当的方式结合形成各种实施方式。同时,方法描述中的各步骤或者动作也可以按照本领域技术人员所能显而易见的方式进行顺序调换或调整。因此,说明书和附图中的各种顺序只是为了清楚描述某一个实施例,并不意味着是必须的顺序,除非另有说明其中某个顺序是必须遵循的。
本文中为部件所编序号本身,例如“第一”、“第二”等,仅用于区分所描述的对象,不具有任何顺序或技术含义。
根据第一方面,在一实施例中,提供一种引物组合,所述引物组合用于检测EB病毒,所述引物组合用于检测第一目标序列、第二目标序列、第三目标序列中的至少一种,所述第一目标序列包含SEQ ID NO:1所示核苷酸序列所构成的组,所述第二目标序列包含SEQID NO:5所示核苷酸序列所构成的组,所述第三目标序列包含SEQ ID NO:9所示核苷酸序列所构成的组。
在一实施例中,所述引物组合用于检测第一目标序列。
在一实施例中,所述引物组合包含第一引物组合、第二引物组合、第三引物组合中的至少一种;
所述第一引物组合包含SEQ ID NO:2~3所示核苷酸序列所构成的组中的至少一种;
所述第二引物组合包含SEQ ID NO:6~7所示核苷酸序列所构成的组中的至少一种;
所述第三引物组合包含SEQ ID NO:10~11所示核苷酸序列所构成的组中的至少一种。
在一实施例中,所述第一引物组合用于检测第一目标基因。
在一实施例中,所述第二引物组合用于检测第二目标基因。
在一实施例中,所述第三引物组合用于检测第三目标基因。
在一实施例中,所述引物组合包含第一引物组合、第二引物组合、第三引物组合中的至少两种。
在一实施例中,所述引物组合包含第一引物组合、第二引物组合、第三引物组合中的全部。
在一实施例中,所述引物组合为第一引物组合。
在一实施例中,根据第一目标序列、第二目标序列、第三目标序列设计的引物、探针均在本发明的保护范围之内。
在一实施例中,本发明提供的引物组合所适用的方法包括但不限于qPCR、数字PCR。
在一实施例中,所述引物组合用于数字PCR检测。
在一实施例中,所述引物组合用于检测EB病毒。
在一实施例中,所述引物组合用于制备数字PCR检测试剂盒。
根据第二方面,在一实施例中,提供一种试剂盒,包括第一方面任意一项所述的引物组合。
在一实施例中,所述试剂盒还包含探针。
在一实施例中,所述探针包含SEQ ID NO:4、8、12所示核苷酸序列所构成的组中的至少一种。
在一实施例中,包含SEQ ID NO:4所示核苷酸序列所构成的组的探针用于靶向第一目标序列。
在一实施例中,包含SEQ ID NO:8所示核苷酸序列所构成的组的探针用于靶向第二目标序列。
在一实施例中,包含SEQ ID NO:12所示核苷酸序列所构成的组的探针用于靶向第三目标序列。
在一实施例中,任一所述探针的一端修饰有荧光基团,另一端修饰有淬灭基团。
在一实施例中,所述试剂盒还包含内参基因。
在一实施例中,所述试剂盒还包含用于检测内参基因的引物、探针。
在一实施例中,所述试剂盒为数字PCR检测试剂盒。
根据第三方面,在一实施例中,提供第一目标序列、第二目标序列、第三目标序列中的至少一种在制备检测试剂中的用途;所述第一目标序列包含SEQ ID NO:1所示核苷酸序列所构成的组,所述第二目标序列包含SEQ ID NO:5所示核苷酸序列所构成的组,所述第三目标序列包含SEQ ID NO:9所示核苷酸序列所构成的组。
在一实施例中,所述检测试剂用于检测EB病毒。
在一实施例中,所述检测试剂为数字PCR检测试剂。
在一实施例中,本发明公开了一种用于检测鼻咽癌中EB病毒的引物、探针和试剂盒。本发明设计了一组用于数字PCR平台中检测EB病毒的引物与探针组合,并进一步构建了检测试剂盒。该组引物、探针和试剂盒具有检测灵敏度高、特异性强、精确度高等特点,有利于提高鼻咽癌中EBV检测的准确性和特异性,适用于EB病毒精确定量,可广泛的应用于鼻咽癌临床诊断领域中,对于鼻咽癌的早期预防、诊断以及治疗后监测和预后都具有积极的指导意义和应用价值。本试剂盒同时检测人β-actin基因作为内参,可对采样、提取和PCR扩增等步骤进行质控,检测结果准确可靠。
在一实施例中,本发明提供一组检测EB病毒的引物和探针组合,该引物组在荧光定量PCR平台和数字PCR平台检测EB病毒灵敏度和特异性均较好,可适用于EB病毒核酸的精确定量。
在一实施例中,本发明公开了一组检测EB病毒的引物和探针组合。该组引物、探针在EB病毒检测中具有检测灵敏度高、特异性强、精确度高等特点,有利于提高EBV检测的准确性和特异性,适用于EB病毒精确定量。且该引物组可用同时适用于荧光定量PCR平台和数字PCR平台,在两个平台中性能验证均较好。
在一实施例中,本发明提供了检测靶标序列,以及针对这个靶标所设计的引物及探针引物。
在一实施例中,本发明的探针序列的荧光基团和淬灭基团可有多种选择。
在一实施例中,EBV探针序列中FAM荧光基团或BHQ1淬灭基团可有多种替代选择,比如FAM基团可替换为HEX、VIC、CY5、ROX和TAMRA等,淬灭基团可替换为BHQ2、TAMRA等等。
在一实施例中,引物探针浓度可有多种替代选择:
1)qPCR平台中引物探针使用浓度:引物使用浓度范围100nM-1000nM,优选为浓度200nM。探针使用浓度范围50nM-250nM,优选为100nM。
2)数字PCR平台EBV靶标检测引物探针使用浓度:引物使用浓度400nM,探针使用浓度200nM。β-actin检测引物探针使用浓度:引物使用浓度300nM,探针使用浓度150nM。
内参基因引物探针序列
本发明设计的内参基因引物探针,检测人β-actin基因作为内参,可对采样、提取和PCR扩增等步骤进行质控,确保检测过程的准确可靠。同时该内参基因不对目的基因造成竞争性抑制,不会影响目的基因检测的灵敏度和准确性。
在一实施例中,EBV预混液成分可以包括:
50mM Tris-HCl、10mM KCl、5mM(NH
在一实施例中,本发明提供的试剂盒整体检测流程,使用该流程的关键步骤如提取、纯化、扩增、检测所使用的先后顺序、浓度及反应时间可以有其他选择。
在一实施例中,本发明使用的引物可以明显提高临床检测的灵敏度。特别是针对早期样本的检测具有较高准确性。
实施例1
1.生物分子序列:
EBV检测目标序列的引物探针序列:
(1)EBV引物组1及检测目标序列:
目标序列1:TCGCCCAGTCCTACCAGAGGGGGCCAAGAACCCAGACGAGTCCGTAG AAGGGTCCTCGTCCAGCAAGAAGAGGAGGTGGTAAGCGGTTCACCTTCAG(SEQ ID NO:1)
上游引物EBV-F1:TCGCCCAGTCCTACCAGAG(SEQ ID NO:2)
下游引物EBV-R1:CTGAAGGTGAACCGCTTACC(SEQ ID NO:3)
探针序列EBV-P1:FAM-CCGTAGAAGGGTCCTCGTCCAGC-BHQ1(SEQ ID NO:4)
(2)EBV引物组2及检测目标序列:
目标序列2:GGATTAGGCTGCCTCAAGTTGCATCAGCCAGGGCTTCATGCCCTCCTC AGTTCCCTAGTCCCCGGGCTTCAGGCCCCCTCCGTCCCCGTCCTCCAGAGACCCGGGCT TCAGGCCCTGCCTCTCCTGTTACCCTTTTAGAACC(SEQ ID NO:5)
上游引物EBV-F2:GGATTAGGCTGCCTCAAGTT(SEQ ID NO:6)
下游引物EBV-F2:GGTTCTAAAAGGGTAACAGGAGA(SEQ ID NO:7)
探针序列EBV-P2:FAM-TCATGCCCTCCTCAGTTCCCTAGT-BHQ1(SEQ ID NO:8)
(3)EBV引物组3及检测目标序列:
目标序列3:TATCGGGCCAGAGGTAAGTGGACTTTAATTTTTTCTGCTAAGCCCAACA CTCCACCACACCCAGGCACACACTACACACACCCACCCGTCTCAGGGTCCCCTCGGAC AGCTCCTAAGAAGGCA(SEQ IDNO:9)
上游引物EBV-F3:TATCGGGCCAGAGGTAAGTG(SEQ ID NO:10)
下游引物EBV-R3:TGCCTTCTTAGGAGCTGTCC(SEQ ID NO:11)
探针序列EBV-P3:FAM-TTTCTGCTAAGCCCAACACTCCAC-BHQ1(SEQ ID NO:12)
EBV DNA检测靶标引物探针使用浓度:引物使用浓度400nM,探针使用浓度200nM。
(4)内参基因:β-actin的引物探针序列
上游引物ACTB-F:GTGGATCAGCAAGCAGGAGTAT(SEQ ID NO:13)
下游引物ACTB-R:CAAGAAAGGGTGTAACGCAACT(SEQ ID NO:14)
探针序列ACTB-P:HEX-ATCGTCCACCGCAAATGCTTCTAGG-BHQ1(SEQ ID NO:15)
β-actin检测引物探针使用浓度:引物使用浓度300nM,探针使用浓度150nM。
2.试剂盒组成
表1
3.样本要求及处理
(1)样本要求:血浆样本
(2)样本采集及处理:
1)用一次性无菌针头抽取受试者静脉血2~3mL于EDTA-抗凝管中,立即轻轻颠倒采血管5~10次,使抗凝剂与静脉血充分混匀。
2)将采血管中的全血样本放置在离心机中,在1900×g(3000rpm)的转速以及+4℃的温度条件下将血液样本离心10min。
3)小心将血浆上清吸取出来,不碰到白膜层。
4)将分离出来的血浆转移到一支新的离心管中。
5)将血浆样本在16000×g的转速以及+4℃的温度条件下离心10min。
6)小心将上清转移到一支新的离心管中,不碰到沉淀。
7)如果得到的血浆在当天内进行提取,则可以在进一步处理前保存在2-8℃的条件下。如果长期保存,则将血浆冻存在-80℃条件下,并在下次游离核酸提取实验前放置于室温孵化。
(3)样本提取
1)取1mL血浆加入到5mL离心管中;
2)加入50μL蛋白酶K和150μL裂解液,震荡混匀5秒;
3)60℃条件下温育20分钟;
4)加入1250μL绑定液和60μL磁珠分散液至样品中,室温震荡混匀6分钟,期间颠倒混匀数次,瞬时离心收集;
5)将离心管放置在磁力架上,静置约5分钟,待溶液澄清后,小心移除上清;
6)加入1000μL蛋白清洗液1,涡旋混匀15秒,瞬时离心收集;
7)将离心管放置在磁力架上,静置约5分钟,待溶液澄清后,小心移除上清;
8)加入1000μL漂洗液2,涡旋混匀15秒,瞬时离心收集;
9)将离心管放置在磁力架上,静置约5分钟,待溶液澄清后,小心移除上清;
10)重复第8-9步一次;
11)短暂离心,将离心管置于磁力架上,小心吸尽上清;
12)空气干燥5-10min至磁珠表面无反光;
13)加入100μL灭菌水进行洗脱,涡旋打散磁珠,静置3-5分钟,其间轻轻震荡1-2次加速DNA溶解;
14)将离心管置于磁力架上,静置3分钟。转移DNA溶液至新的1.5mL离心管中;
15)提取的核酸可直接用于检测,若样本提取后不立即检测,可存于-80℃备用,避免反复冻融。
4.PCR扩增
1)根据样本数量配制PCR扩增MIX。
表2
2)样本模板加样:取10μL阳性对照、阴性对照或样本提取的核酸加入到反应体系中,混匀,离心除气泡。
3)上机:将混匀好的反应试剂加入到芯片的样本孔,在油相孔中加入70μL液滴生成油,然后将芯片的样本孔和油相孔盖上密封垫,将芯片放入仪器相应位置,在软件界面输入相应信息进行液滴生成及扩增等程序
4)扩增程序
表3
5)结果分析:检测结束后,在软件分析界面进行数据分析,可以根据散点图和阳性对照结果,划定合适的阳性阈值线,得到各样本检测值。
5.最低检测下限测试
本实施例使用的标准品为广州邦德盛生物科技有限公司EB病毒脱氧核糖核酸(EBV DNA)液体标准物质GBW(E)090681,可以溯源到国际标准物质1st WHO InternationalStand ard for Epstein-Barr Virus(EBV)for Nucleic Acid AmplificationTechnlques,NIBSC code:09/260。该标准品浓度定值为5.4E+05IU/mL,换算为拷贝数浓度值为2.41E+06copies/mL。
最低检测下限测试
将标准品稀释至1000copies/mL、600copies/mL和400copies/mL进行测试,测试本实施例试剂盒的最低检测下限。此外使用同一组引物探针在QPCR平台进行最低检测下限测试,对比数字PCR平台和QPCR平台的测试结果。
1)数字PCR平台数据
表4
表5
表6
2)qPCR平台数据
表7
结论:本实施例试剂盒在数字PCR平台最低检测下限为600copies/mL,在该低浓度下检测CV值为46.46%,明显低于qPCR平台在600copies/mL条件下的CV值55.85%,因此本实施例试剂盒在低浓度下检测结果更加稳定,有利于低浓度临床样本的检测。
6.临床样本对比结果
采用本实施例的试剂盒基于数字PCR平台的EB病毒核酸检测试剂盒对96例诊断为鼻咽癌病人的血浆样本进行检测,其结果与医院qPCR检测结果进行对比,其中医院使用的是圣湘生物科技有限公司EB病毒核酸定量检测试剂盒(PCR-荧光探针法)。结果显示,本实施例试剂盒检测96例鼻咽癌病人样本,其中检出EBV DNA的患者95例,检测灵敏度为98.96%;医院采用和的qPCR法检测96例鼻咽癌病人样本,其中检出EBV DNA的患者84例,检测灵敏度为87.5%。(结果见下表)
表8
结论:综上所述,本实施例的基于数字PCR平台的EB病毒核酸检测试剂盒检测鼻咽癌患者血浆EBV DNA,检测灵敏度达到98.96%,而医院使用的某公司基于qPCR技术的EB病毒核酸检测试剂盒检测灵敏度为87.5%。本实施例的试剂盒具有灵敏度高,定量准确,快速简便的特点,有利于提高检测鼻咽癌患者中血浆EBV DNA的灵敏度和准确度,也可作为临床检测试剂盒。该检测方法可作为鼻咽癌的辅助诊断方法和临床治疗效果的监测手段,具有潜在的应用价值。
实施例2
1.生物分子序列:
(1)EBV检测目标序列:
TCGCCCAGTCCTACCAGAGGGGGCCAAGAACCCAGACGAGTCCGTAGAAGGGTCCTCGTCCAGCAAGAAGAGGAGGTGGTAAGCGGTTCACCTTCAG(SEQ ID NO:1)
(2)EBV检测目标序列的引物探针序列:
上游引物EBV-F:TCGCCCAGTCCTACCAGAG(SEQ ID NO:2)
下游引物EBV-R:CTGAAGGTGAACCGCTTACC(SEQ ID NO:3)
探针序列EBV-P:FAM-CCGTAGAAGGGTCCTCGTCCAGC-BHQ1(SEQ ID NO:4)
2.qPCR平台应用:
(1)qPCR平台中引物探针使用浓度:引物使用浓度200nM,探针使用浓度100nM。
(2)反应体系:
表9
(3)扩增程序:50℃2min;95℃5min;95℃15s,60℃30s,共45个循环。
(4)qPCR平台最低检测下限LOD检测
构建含有EBV扩增目的基因片段的重组质粒(上海生工生物),将质粒梯度稀释至600copies/mL、400copies/mL和200copies/mL进行最低检测下限测试,每个浓度测试20次,采用95%最低检出率为检测下限。
表10
图1为qPCR平台最低检测下限LOD检测图(400copies/mL)。
结论:最低检测下限为400copies/mL。
2.数字PCR平台应用
(1)数字PCR平台中引物探针使用浓度:引物使用浓度400nM,探针使用浓度200nM。
(2)反应体系:
表11
(3)扩增程序:95℃5min;95℃15s,60℃30s,共45个循环。
(4)结果分析:检测结束后,在软件分析界面进行数据分析,可以根据散点图和阳性对照结果,划定合适的阳性阈值线,得到各样本检测值。
(5)数字PCR平台低浓度样本测定
构建含有EBV扩增目的基因片段的重组质粒,稀释至400copies/mL进行测试。
表12
图2为数字PCR平台低浓度样本(400copies/mL)测定图。可见,本实施例提供的试剂盒可检测低浓度样本。
以上应用了具体个例对本发明进行阐述,只是用于帮助理解本发明,并不用以限制本发明。对于本发明所属技术领域的技术人员,依据本发明的思想,还可以做出若干简单推演、变形或替换。
- 拉沙病毒快速荧光PCR检测试剂盒及其引物探针组合
- 一种汉坦病毒极速荧光PCR检测试剂盒及其引物探针组合
- 一种基于BTNAA体系检测犬瘟热病毒的引物对、引物和探针组合物、试剂及试剂盒
- 一种基于BTNAA体系检测犬细小病毒的引物对、引物和探针组合物、试剂及试剂盒
- 用于检测鼻咽癌中EB病毒的引物、探针及试剂盒
- 一种基于数字PCR检测新型冠状病毒的引物探针组合及其应用
