一种用于牙槽骨修复的复合材料及其制备方法
文献发布时间:2024-01-17 01:27:33
技术领域
本发明涉及纳米生物医药技术领域,具体涉及一种用于牙槽骨修复的复合材料及其制备方法。
背景技术
牙拔除术后局部牙槽嵴会发生改建或吸收,导致缺损部位的骨量减少,影响义齿修复和种植牙的植入,严重时还会导致周围软组织的萎缩,影响生活质量。
目前,临床上针对该病症的主要治疗手段是引导骨再生(Guided BoneRegeneration,GBR)技术。它主要是将软组织屏障膜和骨填充材料搭配使用,利用屏障膜可形成的空间,让成骨细胞或血管内皮细胞长入,同时隔离上层覆盖的非成骨性软组织细胞的侵入。此类屏障膜主要为:可吸收的胶原膜,其最主要的缺点是力学性能差、降解速度快,不能维持稳定的成骨空间。利用骨填充材料的骨传导作用,为宿主的骨组织提供生物支架,从而促进骨组织的再生,该类材料多选自自体骨、异体骨和合成的陶瓷材料等,以颗粒和块状的形式提供。此类材料的缺点是塑形性差,易分散,导致医生操作不方便,且降解速率与新生骨成骨速率不匹配,导致异物反应时间长,给患者带来诸多不适。现有的骨填充材料存在以下缺陷:(1)现有骨填充材料不能提供独立的成骨空间,需搭配软组织屏障膜使用,手术成本高,操作繁琐;(2)现有骨填充材料所需软组织屏障膜,力学性能差、降解速度快,不能稳定维持成骨空间;(3)现有骨填充材料塑形性差、易分散,使用时操作不方便;(4)现有骨填充材料降解速率与新生骨成骨速率不匹配,导致异物反应时间长,引导骨组织再生能力差。
基于现有骨填充材料存在的不足,一种理想的牙槽骨修复材料应具备以下特点:①具有特定的组织屏障作用和一定的力学性能,可形成独立稳定的成骨空间,为牙槽骨修复提供良好的支架环境;②可随意塑形,不溢散,便于临床医生的操作;③降解速率和成骨速率相匹配,增强引导骨组织再生的能力,提高患者的体验感。
发明内容
本发明的目的在于:针对现有骨填充材料存在的缺陷而提供一种用于牙槽骨修复的复合材料及其制备方法,本发明用于牙槽骨修复的复合材料主要由具有软组织屏障作用的致密层和引导骨组织再生的疏松层构成,其满足了理想的牙槽骨修复材料所需的独立稳定的成骨空间、随意塑形,降解速度适宜等特点,解决了现有骨填充材料所面临的痛点。
本发明是通过如下技术方案实现的:
一种用于牙槽骨修复的复合材料,其特征在于,所述的复合材料由具有软组织屏障作用的致密层和具有引导骨组织再生作用的疏松层组成;其中:所述的致密层为纳米纤维堆叠而成的纤维膜,由聚酯类医用高分子材料经静电纺丝而成;所述的疏松层作为骨修复的支架材料,由复合型支架材料经静电纺丝加工而成;所述的复合型支架材料由纳米级无机填充材料和聚酯类医用高分子材料键合而成。
具体的,本发明复合材料中的无机纳米填充材料具有较高的比表面积,在生理环境下与组织界面接触并发生作用,形成化学键合,可为新生的骨组织提供生长所需的钙、磷等营养物质;而聚酯类医用高分子材料经静电纺丝、3D打印等技术加工后,可形成骨修复所需的屏障系统,并完美的实现其支架的功能,可为新生骨的生长提供良好的生理环境。所以本发明将纳米级无机填充材料和聚酯类医用高分子材料通过键合的方式,获得一种降解速率适宜的复合型支架材料。
在本发明提供的用于牙槽骨修复的复合材料中:所述的致密层为纳米纤维堆叠而成的纤维膜,其是由聚酯类医用高分子材料经静电纺丝加工而成,较目前常用的可降解生物膜,其具有较高的机械强度、可控的降解速率,可以为缺损的骨组织提供稳定的成骨空间,起到良好的屏蔽作用,防止软组织的入侵。
在本发明提供的用于牙槽骨修复的复合材料中:所述的疏松层作为骨修复的支架层,其是由复合型支架材料经特定的静电纺丝工艺加工而成;本发明所得的疏松层具有可随意塑形、不溢散以及降解速率可控等特点。
进一步的,一种用于牙槽骨修复的复合材料:所述的致密层的纤维直径为10-10000nm,所述致密层的厚度为0.1-0.5cm。
优选的,所述的致密层纤维的直径为50-5000nm;优选的,所述的致密层的厚度为0.25-0.5cm。
进一步的,一种用于牙槽骨修复的复合材料:所述的聚酯类医用高分子材料选自聚(L-丙交酯-co-D,L-丙交酯)、聚L-丙交酯、聚(L-丙交酯-co-乙交酯)、聚(L-丙交酯-co-ε-己内酯)及其改性物的一种;所述的纳米级无机填充材料选自氨基羟基磷灰石、掺硅盐碳酸钙、β-磷酸三钙、生物活性玻璃、双相磷酸钙陶瓷中的一种;所述聚酯类医用高分子材料的特性粘度为1.3-7.0dL/g。
一种用于牙槽骨修复的复合材料的制备方法,其特征在于,该方法包括如下步骤:
一、致密层的制备:
S1、将聚酯类医用高分子材料溶于第一溶剂中,然后再加入第二溶剂,搅拌均匀,形成纺丝液A;
S2、将所述纺丝液A进行静电纺丝,得到静电纺丝膜;具体的,该步骤S2中的静电纺丝工艺为:将纺丝液A装入注射器中,针头孔径为0.4mm、注射速度1.5-2.5ml/h、电压15-30kv、接收距离8-22cm,进行静电纺丝,得到静电纺丝膜;
S3、将所述静电纺丝膜烘干,然后堆叠,得到致密层;
二、疏松层的制备:
S1、将纳米级无机填充材料干燥,然后溶于有机溶剂中,并通入HX气体进行反应,得到卤代的纳米级无机填充材料;其中:X选自Cl、Br、I中的一种;
S2、将聚酯类医用高分子材料溶于所述有机溶剂中,得到溶解液;向卤代的纳米级无机填充材料中滴加所述溶解液,然后回流搅拌;回流搅拌后去除所述有机溶剂,将所得产物清洗,干燥,得到纳米级无机填充材料和聚酯类医用高分子材料的键合产物,为复合型支架材料;
S3、将所述复合型支架材料溶解,然后加入第三溶剂,并搅拌均匀,得到纺丝液B;
S4、将所述纺丝液B静电纺丝,纺丝后干燥,获得塑形性好的棉絮状疏松层;
三、复合材料的制备:
S1、将所述疏松层超声焊接于所述致密层上,制得用于牙槽骨修复的复合材料。
进一步的,一种用于牙槽骨修复的复合材料的制备方法:一、致密层的制备:S1、将聚酯类医用高分子材料溶于第一溶剂中,且聚酯类医用高分子材料的浓度为16-20wt%,然后再加入第二溶剂,搅拌均匀,形成纺丝液A;其中:所述的第一溶剂为三氯甲烷;所述的第二溶剂选自二甲基苯酰胺、六氟异丙醇、DMSO、三氟乙醇、四氢呋喃、DMF、甲苯中的一种;所述第一溶剂与所述第二溶剂的质量比为1:(1-2)。
进一步的,一种用于牙槽骨修复的复合材料的制备方法:二、疏松层的制备:步骤S1、将纳米级无机填充材料在40-60℃下真空干燥24-48小时,然后将其溶于有机溶剂中,在常温下缓慢通入HX气体反应1-3小时,得到卤代的纳米级无机填充材料;其中:所述的有机溶剂为三氯甲烷,所述纳米级无机填充材料与所述有机溶剂的质量比为1:(2-5)。具体的,该步骤中真空度在200bar以下。
进一步的,一种用于牙槽骨修复的复合材料的制备方法:二、疏松层的制备:步骤S2、将聚酯类医用高分子材料溶于三氯甲烷中,得到含10-20wt%聚酯类医用高分子材料的溶解液;然后向卤代的纳米级无机填充材料中滴加所述溶解液并回流搅拌8-12小时;反应后旋转蒸发去除三氯甲烷,将所得产物用纯化水冲洗2-3小时,在70-90℃下干燥2-4小时,得到纳米级无机填充材料和聚酯类医用高分子材料的键合产物;其中:卤代的纳米级无机填充材料与所述聚酯类医用高分子材料的摩尔比为1:(1-2)。
进一步的,一种用于牙槽骨修复的复合材料的制备方法:二、疏松层的制备:步骤S3、将所得键合产物溶于三氯甲烷中,且键合产物的浓度为18-26wt%,然后再加入第三溶剂,并搅拌均匀,得到纺丝液B;其中:所述的第三溶剂与所述三氯甲烷的质量比为1:(1-2),所述的第三溶剂选自二甲基苯酰胺、六氟异丙醇、DMSO、三氟乙醇、四氢呋喃、DMF、甲苯中的一种。
进一步的,一种用于牙槽骨修复的复合材料的制备方法:二、疏松层的制备:步骤S4、将所述纺丝液B采用喇叭口或离心纺方式进行静电纺丝,纺丝后在80-120℃下烘干2-4小时,获得塑形性好的棉絮状疏松层。
进一步的,一种用于牙槽骨修复的复合材料的制备方法:三、复合材料的制备:S1、将所述的致密层平铺于不锈钢界面上,使用超声波焊接机,压力为0.1-0.3Mpa,焊接时间0.1-0.3s/每点,将所述疏松层按0.1-0.3mm每点的距离焊接在所述致密层上,制得用于牙槽骨修复的复合材料。
本发明的有益效果:
(1)本发明提供了一种用于牙槽骨修复的复合材料,是由具有软组织屏障作用的致密层和引导骨组织再生的疏松层通过超声波焊接而成;本发明将引导骨再生(GBR)技术所需的软组织屏障膜和骨填充材料合二为一,解决了现有牙槽骨缺损修复材料需要软组织屏障膜搭配使用,不能提供独立成骨空间的问题。
(2)在本发明提供的用于牙槽骨修复的复合材料中,具有软组织屏障作用的致密层是由聚酯类医用高分子材料经静电纺丝所得,其降解性能可控,可提供稳定的成骨空间;具有引导骨组织再生作用的疏松层是由纳米级无机填充材料和聚酯类医用高分子键合后,再经静电纺丝技术所得,其具有可随意塑形、无骨粉溢散、结构稳定便于使用操作、同时降解性能适宜等优点,可为再生的骨组织提供良好的支架环境。
(3)本发明制备的用于牙槽骨修复的复合材料克服了现有骨填充材料必须搭配软组织屏障膜结合使用的弊端,成功实现了屏障与填充的双重作用,降低了手术成本。本发明制备的复合材料解决了现有牙槽骨缺损修复材料不能屏蔽软组织入侵,需要与软组织屏障膜搭配使用的技术壁垒。
(4)本发明提供的用于牙槽骨修复的复合材料的降解速率与新生骨的成骨速率相匹配,其解决了现有骨填充材料降解速率与新生骨成骨速率不匹配,导致异物反应时间长,引导骨组织再生能力差的问题,本发明的复合材料引导骨再生能力强,患者体验感好。
(5)本发明提供的用于牙槽骨修复的复合材料解决了现有骨填充材料塑形性差、易分散,医生操作使用不方便等缺陷;本发明的复合材料还解决了现有骨填充材料所搭配的软组织屏障膜力学性能差、降解速度快,不能提供稳定成骨空间的难题。
(6)本发明提供的用于牙槽骨修复的复合材料是由致密层与疏松层经超声焊接制得,其致密层具有较高的机械强度、可控的降解速率,可以为缺损的骨组织提供稳定的成骨空间,起到良好的屏蔽作用,防止软组织的入侵;疏松层具有可随意塑形(塑形性好)、不溢散、降解速率可控的特点;本发明基于传统的牙槽骨修复技术需要骨填充材料和软组织屏障膜搭配使用,其操作不方便,使用成本高,所以本发明的牙槽骨修复用复合支架材料由具有软组织屏障作用的致密层和引导骨组织再生的疏松层通过超声波焊接而成,完美的实现了屏蔽软组织和引导骨组织再生的双重作用。
(7)本发明制备的复合型支架材料是将纳米级无机填充材料与有机高分子(聚酯类医用高分子材料)材料通过亲核反应方式将两种材料键合在一起,能够避免纳米材料引起溶血、刺激等不良反应。
(8)本发明所述的用于牙槽骨修复的复合材料是由有机材料和无机材料键合后,经过静电纺丝、超声波焊接而成,其可塑性强、使用便捷、降解速率适宜,是一种良好的双层生物材料。
(9)现有的无机骨填充材料用于牙槽骨的修复一般为粒径0.5-1.0nm的颗粒,所以塑形性差、易分散,导致医生操作使用不方便,而本发明所提供的用于牙槽骨修的复合材料其上层为致密的膜层,可随意裁剪,下层为通过静电纺丝所得的疏松层,可根据缺损的部位随意塑形,所以本发明所提供的牙槽骨修复材料临床使用更便捷。
附图说明
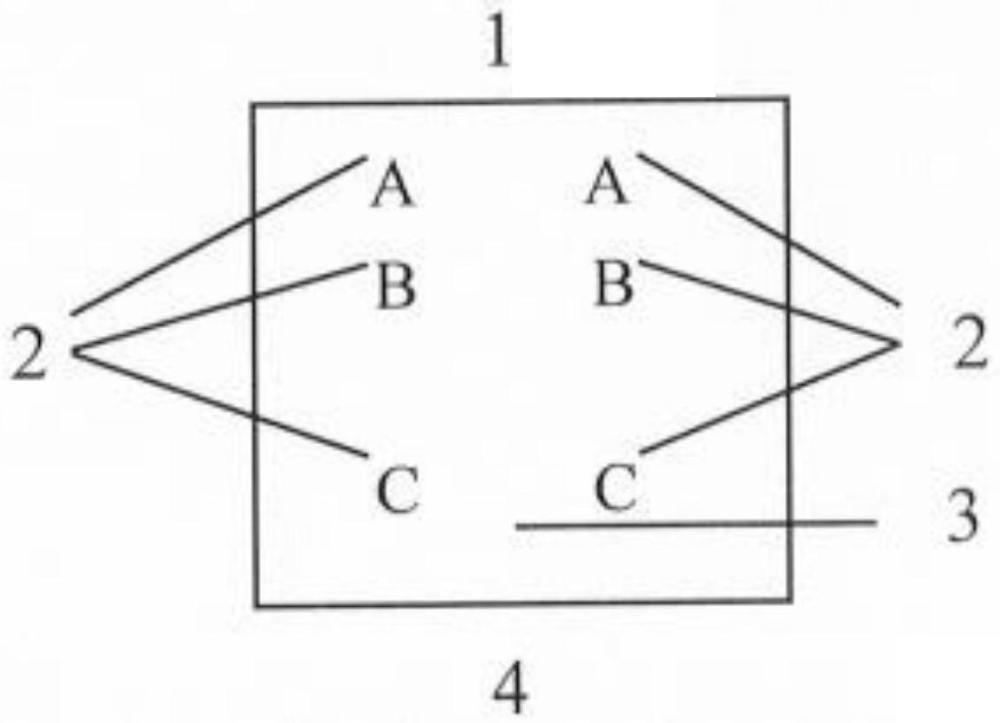
图1为注射诱导迟发型超敏反应的注射示意图。
具体实施方式
下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明的一部分实施例,而不是全部的实施例。以下对至少一个示例性实施例的描述实际上仅仅是说明性的,决不作为对本发明及其应用或使用的任何限制。基于本发明中的实施例,本领域普通技术人员在没有作出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
实施例1
一种用于牙槽骨修复的复合材料,其特征在于,所述的复合材料由具有软组织屏障作用的致密层和具有引导骨组织再生作用的疏松层经超声焊接而成;其中:所述的致密层为纳米纤维堆叠而成的纤维膜,由聚酯类医用高分子材料经静电纺丝而成;所述的疏松层作为骨修复的支架材料,由复合型支架材料经静电纺丝加工而成;所述的复合型支架材料由纳米级无机填充材料(氨基纳米级羟基磷灰石,粒径:100-300nm)和聚酯类医用高分子材料(聚L-丙交酯,特性粘度:1.5-2.0dL/g)键合而成。
上述实施例1所述的一种用于牙槽骨修复的复合材料的制备方法,包括如下具体步骤:
一、致密层的制备:
S1、将聚酯类医用高分子材料(聚L-丙交酯)溶于三氯甲烷中,且保证聚L-丙交酯的浓度为18wt%,然后再加入与三氯甲烷同种质量的六氟异丙醇,搅拌均匀,形成纺丝液A;
S2、将所得纺丝液A装入注射器中,针头孔径为0.4mm、注射速度1.5ml/h、电压18kv、接收距离15cm,进行静电纺丝,得到静电纺丝膜,为聚酯类医用高分子膜;该步骤中的静电纺丝技术采用的是针纺的方式,接收的界面为直径5-10cm平面接收;
S3、将所得静电纺丝膜在80℃下烘干4小时,然后将所得静电纺丝膜堆叠,得到致密层;
二、疏松层的制备:
S1、将纳米级无机填充材料(氨基纳米级羟基磷灰石)在50℃下真空干燥48小时(真空度在200bar以下),材料干燥后溶于三氯甲烷中(纳米级无机填充材料与三氯甲烷的质量比为1:3),然后在常温搅拌下缓慢通入HBr气体反应3小时,得到卤代的纳米级无机填充材料;
S2、将一定量的聚L-丙交酯溶于三氯甲烷中,得到含10wt%聚L-丙交酯的三氯甲烷溶液,称为溶解液;向上述所得卤代的纳米级无机填充材料中滴加所述溶解液(注意:氨基纳米级羟基磷灰石与聚L-丙交酯的摩尔比为1:1),然后回流搅拌12小时;回流搅拌后旋转蒸发去除三氯甲烷,然后将键合后所得产物用纯化水冲洗2小时,在80℃下烘干4小时,即得到纳米级无机填充材料和聚酯类医用高分子材料的键合产物,为复合型支架材料;
S3、将所得复合型支架材料溶解于三氯甲烷中并搅拌均匀,且复合型支架材料的浓度为20wt%,然后加入与三氯甲烷相同质量的六氟异丙醇,并搅拌均匀,得到纺丝液B;
S4、将所得纺丝液B静采用喇叭口方式进行电纺丝,纺丝后在90℃下烘干4小时,获得塑形性好的棉絮状疏松层;具体的,在该步骤中:静电纺丝作业喇叭口方式为:将静电纺丝液B放入2支20ml注射器中,并通过推进泵以1.4ml/h的流速喷向中间旋转肉头两侧12cm处,同时分别给与2个注射器针头各7KV的正负压,纺丝后在在80℃下烘干4小时,即得到可随意塑形的且呈棉絮状的疏松层;
三、复合材料的制备:
S1、将所得致密层平铺于不锈钢界面上,使用超声波焊接机,压力为0.2Mpa,焊接时间0.2s/每点,将所得疏松层按0.2mm每点的距离焊接在致密层上,制得用于牙槽骨修复的复合材料。
上述实施例1中所述的氨基纳米级羟基磷灰石的制备方法包括如下具体步骤:
(1)将硝酸钙溶于纯化水中(质量比为1:2),然后用氨水调节pH至10.5,用电炉加热至沸腾;
(2)加热沸腾后,在200rpm的搅拌条件下,缓慢滴加20%的磷酸氢氨溶液(其中:硝酸钙和磷酸氢氨溶液的质量比为1.5:1),滴加时间控制在15分钟,滴加完毕后继续反应5小时;
(3)反应完毕后,放置于800℃的马弗炉中煅烧6小时,即得氨基纳米级羟基磷灰石。
实施例2
一种用于牙槽骨修复的复合材料,其特征在于,所述的复合材料由具有软组织屏障作用的致密层和具有引导骨组织再生作用的疏松层经超声焊接而成;其中:所述的致密层为纳米纤维堆叠而成的纤维膜,由聚酯类医用高分子材料经静电纺丝而成;所述的疏松层作为骨修复的支架材料,由复合型支架材料经静电纺丝加工而成;所述的复合型支架材料由纳米级无机填充材料(氨基纳米级羟基磷灰石,粒径:100-300nm)和聚酯类医用高分子材料(聚(L-丙交酯-co-乙交酯)(85:15),特性粘度:2.5-3.5dL/g)键合而成。
上述实施例2所述的一种用于牙槽骨修复的复合材料的制备方法,包括如下具体步骤:
一、致密层的制备:
S1、将聚酯类医用高分子材料(聚(L-丙交酯-co-乙交酯))溶于三氯甲烷中,且保证聚(L-丙交酯-co-乙交酯)的浓度为16wt%,然后再加入与三氯甲烷同种质量的DMSO,搅拌均匀,形成纺丝液A;
S2、将所得纺丝液A装入注射器中,针头孔径为0.4mm、注射速度1.5ml/h、电压25kv、接收距离18cm,进行静电纺丝,得到静电纺丝膜,为聚酯类医用高分子膜;该步骤中的静电纺丝技术采用的是针纺的方式,接收的界面为直径10cm平面接收;
S3、将所得静电纺丝膜在105℃下烘干2小时,然后将所得静电纺丝膜堆叠,得到致密层;
二、疏松层的制备:
S1、将纳米级无机填充材料(氨基纳米级羟基磷灰石)在50℃下真空干燥48小时(真空度在200bar以下),材料干燥后溶于三氯甲烷中(纳米级无机填充材料与三氯甲烷的质量比为1:3),然后在常温搅拌下缓慢通入HBr气体反应3小时,得到卤代的纳米级无机填充材料;
S2、将一定量的聚(L-丙交酯-co-乙交酯)溶于三氯甲烷中,得到含15wt%聚(L-丙交酯-co-乙交酯)的三氯甲烷溶液,称为溶解液;向上述所得卤代的纳米级无机填充材料中滴加所述溶解液(注意:氨基纳米级羟基磷灰石与聚(L-丙交酯-co-乙交酯)的摩尔比为1:1),然后回流搅拌10小时;回流搅拌后旋转蒸发去除三氯甲烷,然后将键合后所得产物用纯化水冲洗2小时,在80℃下烘干4小时,即得到纳米级无机填充材料和聚酯类医用高分子材料的键合产物,为复合型支架材料;
S3、将所得复合型支架材料溶解于三氯甲烷中并搅拌均匀,且复合型支架材料的浓度为18wt%,然后加入与三氯甲烷相同质量的DMSO,并搅拌均匀,得到纺丝液B;
S4、将所得纺丝液B静采用离心纺方式进行电纺丝,纺丝后在120℃下烘干2小时,获得塑形性好的棉絮状疏松层;具体的,在该步骤中:静电纺丝作业离心纺方式为:将静电纺丝液B放入20ml注射器中,并通过推进泵以1.2ml/h的流速喷出,同时给与喷头8Kv的电压,在距离喷头3cm处设置可旋转的接收盘,接收盘直径10cm,接收盘转速为16rpm,纺丝后在120℃下烘干2小时,即得到可随意塑形的且呈棉絮状的疏松层;
三、复合材料的制备:
S1、将所得致密层平铺于不锈钢界面上,使用超声波焊接机,压力为0.2Mpa,焊接时间0.2s/每点,将所得疏松层按0.2mm每点的距离焊接在致密层上,制得用于牙槽骨修复的复合材料。
实施例3
一种用于牙槽骨修复的复合材料,其特征在于,所述的复合材料由具有软组织屏障作用的致密层和具有引导骨组织再生作用的疏松层经超声焊接而成;其中:所述的致密层为纳米纤维堆叠而成的纤维膜,由聚酯类医用高分子材料经静电纺丝而成;所述的疏松层作为骨修复的支架材料,由复合型支架材料经静电纺丝加工而成;所述的复合型支架材料由纳米级无机填充材料(掺硅盐碳酸钙,粒径:20-200μm)和聚酯类医用高分子材料(聚(L-丙交酯-co-ε-己内酯))(70:30),特性粘度:1.3-1.8dL/g)键合而成。
上述实施例3所述的一种用于牙槽骨修复的复合材料的制备方法,包括如下具体步骤:
一、致密层的制备:
S1、将聚酯类医用高分子材料(聚(L-丙交酯-co-ε-己内酯))溶于三氯甲烷中,且保证其浓度为20wt%,然后再加入与三氯甲烷同种质量的DMSO,搅拌均匀,形成纺丝液A;
S2、将所得纺丝液A装入注射器中,针头孔径为0.4mm、注射速度2.0ml/h、电压15kv、接收距离18cm,进行静电纺丝,得到静电纺丝膜,为聚酯类医用高分子膜;该步骤中的静电纺丝技术采用的是针纺的方式,接收的界面为直径8cm平面接收;
S3、将所得静电纺丝膜在105℃下烘干2小时,然后将所得静电纺丝膜堆叠,得到致密层;
二、疏松层的制备:
S1、将纳米级无机填充材料(掺硅盐碳酸钙)在60℃下真空干燥36小时(真空度在200bar以下),材料干燥后溶于三氯甲烷中(纳米级无机填充材料与三氯甲烷的质量比为1:3),然后在常温搅拌下缓慢通入HBr气体反应3小时,得到卤代的纳米级无机填充材料;
S2、将一定量的聚(L-丙交酯-co-ε-己内酯)溶于三氯甲烷中,得到含20wt%聚(L-丙交酯-co-ε-己内酯)的三氯甲烷溶液,称为溶解液;向上述所得卤代的纳米级无机填充材料中滴加所述溶解液(注意:掺硅盐碳酸钙与聚(L-丙交酯-co-ε-己内酯)的摩尔比为1:1),然后回流搅拌12小时;回流搅拌后旋转蒸发去除三氯甲烷,然后将键合后所得产物用纯化水冲洗2小时,在80℃下烘干4小时,即得到纳米级无机填充材料和聚酯类医用高分子材料的键合产物,为复合型支架材料;
S3、将所得复合型支架材料溶解于三氯甲烷中并搅拌均匀,且复合型支架材料的浓度为25wt%,然后加入与三氯甲烷相同质量的DMSO,并搅拌均匀,得到纺丝液B;
S4、将所得纺丝液B静采用离心纺方式进行电纺丝,纺丝后在120℃下烘干2小时,获得塑形性好的棉絮状疏松层;具体的,在该步骤中:静电纺丝作业离心纺方式为:将静电纺丝液B放入20ml注射器中,并通过推进泵以1.4ml/h的流速喷出,同时给与喷头8Kv的电压,在距离喷头5cm处设置可旋转的接收盘,接收盘直径10cm,接收盘转速为16rpm,纺丝后在105℃下烘干2小时,即得到可随意塑形的且呈棉絮状的疏松层;
三、复合材料的制备:
S1、将所得致密层平铺于不锈钢界面上,使用超声波焊接机,压力为0.2Mpa,焊接时间0.2s/每点,将所得疏松层按0.2mm每点的距离焊接在致密层上,制得用于牙槽骨修复的复合材料。
测试:
一、化学性能测试:
(1)溶剂残留测试:将上述实施例1-3所得用于牙槽骨修复的复合材料分别溶于二氯甲烷(样品浓度5%)中,使用气相色谱对残留溶剂进行检测,其测试结果参见下表1。
表1为上述实施例1-3所得复合材料的溶剂残留测试结果
由表1的测试结果可以看出,本发明制备的用于牙槽骨修复的复合材料中的溶剂残留量低,可以放心使用。
(2)水分含量测试:使用卡尔费休法对上述实施例1-3所制得的用于牙槽骨修复的复合材料进行水分检测,在环境湿度小于RH40%的条件下,连续测试三次,取平均值;为确保所制备产品的储存稳定性,产品的水分含量应不大于10%,具体的测试结果参见下表2。
表2为实施例1-3合材料所得复合材料的含水量测试结果
由表2的测试结果可以看出,本发明制得的用于牙槽骨修复的复合材料其含水量交底,能够满足长期稳定储存的要求。
二、物理性能测试:
(1)酸碱度测试:将实施例1-3所得产品按照0.1g/ml的比例加入浸提液(纯化水),在(37±1)℃的环境中下浸提72小时,取上清液得到供试液,按《中国药典》(2020版第四部)通则0631pH值测定法检测,结果在6-8之间符合标准;实施例1-3的测试结果参见下表3。
表3为本发明实施例1-3所得产品的酸碱度测试结果
由表3的测试结果可以看出,本发明制得的用于牙槽骨修复的复合材料的酸碱度符合要求。
(2)致密层抗拉强度测试:将实施例1-3制备的用于牙槽骨修复的复合材料中的致密层裁剪下来,并将其裁剪为1cm*2cm的膜片,然后使用万能试验机进行拉力测试,试验机速度设置10nm/min;启动机器,进行拉力测试,其测试结果参见下表4。
表4为实施例1-3所得复合材料中致密层的抗拉强度测试结果
本发明的致密层起到软组织屏障的作用,同时为新生组织提供独立的成骨空间。该类软组织屏障膜植入时需与自身组织缝合,并需维持植入后的一定形态,所以需要一定的抗拉强度。从表4的测试数据可以看出,本发明的致密层具有优于可吸收胶原膜力学性能。
(3)抗压强度测试:对上述实施例1-3制得的用于牙槽骨修复的复合材料进行抗压强度测试,其测试结果参见下表5。
表5为实施例1-3所制得的复合材料的抗压强度测试结果
本发明制备的用于牙槽骨修复的复合材料将有机高分子材料与羟基磷灰石进行键合的目的是改善其降解性以及塑形性的问题,这种方式可能存在力学性能下降的风险,但从上述表5的测试数据可以看出,本发明所制备的产品的抗压强度较羟基磷灰石材料无明显的下降。
三、生物学评价研究:
(1)细胞毒性:将实施例1-3所制得的复合材料依据0.1g/ml的浸提比例(浸提液为10%胎牛血清的MEM培养液),在37℃下浸提24小时,然后参考GB/T16886.5中的MTT法进行细胞毒试验,试验细胞相对活力值实施例1-3分别为87.9%、86.4%、88.2%,没有潜在的细胞毒性。
(2)迟发型超敏反应:将实施例1-3所制备的产品分别用0.9%氯化钠注射液和棉籽油制备成浸提液,将浸提液经皮内注射于10只白化豚鼠,然后进行封闭敷贴,用来诱导迟发型超敏反应。其中:注射方式如图1所示,图1中标记:1-头部,2-0.1ml皮内注射点,3-去毛的肩胛骨内侧部位,4-尾部。
结论:动物经激发后在24小时和48小时观察时间内,均为产生级别大于“0”的反应,说明了本发明制得的产品没有在白化豚鼠上引起迟发型超敏反应。
(3)体外降解性能研究:将实施例1-3所得材料用生理盐水浸湿后,将其疏松层压缩,放入装有模拟体液的锥形瓶中(浸提比例0.1g/ml),置于37℃条件下,在100rpm的恒温摇床中,每周观察材料变化(因纳米无机材料无法模拟体外降解性能,降解结束时间以医用高分子材料降解完成为终点),测试结果参见下表6。
表6为体外降解性能测试结果
与天然的无机材料相比,无机材料主要通过给新生骨提供无机的营养物质,被缓慢的吸收,其降解周期在2年以上;与现有的软组织屏障膜相比,现有的软组织屏障膜材料降解速率较快,不能维持长久的成骨空间,降解速率与成骨速率不匹配。由上述表6测试的数据可以看出,本发明制备的用于牙槽骨修复的复合材料的降解周期在14周到20周之间,而牙槽骨的修复周期通常在3个月左右,所以本发明制备提供了一种可以与新生骨成骨速率相匹配的新材料,更益于牙槽骨的生长。
上述为本发明的较佳实施例仅用于解释本发明,并不用于限定本发明。凡由本发明的技术方案所引伸出的显而易见的变化或变动仍处于本发明的保护范围之中。
- 一种用于制备育苗容器的水溶致孔性完全生物降解复合材料及制备方法和基于其的育苗容器
- 一种用于电气绝缘的自修复环氧树脂的制备及修复方法
- 一种刮痕自修复尼龙复合材料及其制备方法
- 一种牙齿修复用改性纳米羟基磷灰石复合材料的制备方法
- 一种用于牙槽骨缺损修复的组织工程化材料制备方法
- 一种用于牙槽骨缺损修复的医用镁合金屏障膜及其制备方法
