一种利用冲击波促进药物渗透的透皮给药微针贴片及其制备方法
文献发布时间:2024-04-18 19:58:21
技术领域
本发明属于医疗技术领域,具体涉及一种利用冲击波促进药物渗透的透皮给药微针贴片及其制备方法。
背景技术
通过微针系统进行透皮给药是近年发展起来的一种无痛、微创、不易感染且效果显著的新型药物注射技术,利用化学和物理手段,使药物以一定速率通过皮肤释放进如体内,进入体循环产生全身或局部治疗作用。其优点体现在:药物吸收不受消化道内pH、食物、转运时间等因素影响;避免肝脏首过效应;克服因吸收过快产生血药浓度过高而引起的不良反应;可持续控制给药速度,灵活给药等。
皮肤中表皮层的最外层角质层是目前透皮给药最大的障碍。角质层厚约20um,角质层细胞及填充在角质层细胞间的天然物质,包括脂质、游离氨基酸、吡咯烷酮羧酸和盐类等,结合在一起发挥天然屏障功能,阻止药物经皮肤进入体内。早期透皮给药主要使用贴剂,使亲脂性、低分子量的药物通过角质层进入局部,发挥作用。随着对皮肤结构的研究深入,开始使用物理及化学方法破坏角质层,从而解除了对药物本身的限制。作为第三代透皮给药技术,微针将药物装载在微米尺寸大小的针尖阵列上,施加到患者身上后缓慢释放出药物。相较于其他透皮手段,微针能直接将药物递送到皮肤真皮层,使药物快速进入局部区域,或进入皮肤真皮下毛细血管网从而进入全身血液循环。此外,微针对皮肤的损伤较小,其便捷性赋予了很好的患者依从性。目前,已有研究者把可溶性微针作为药物载体,用于治疗深部组织疾病,如骨质疏松。Akira Yamamoto等成功开发了可溶性微针阵列装载阿仑膦酸和甲状旁腺激素用于治疗骨质疏松模型动物,Hyungil Jung等则开发了装载了特立帕肽的可溶性微针。这些研究证实了微针用于深组织疾病治疗的可行性。
但由于药物从微针针尖释放是一个被动的、非靶向的过程,药物从针尖释放后仍不具有聚集性,无法明显增加局部药物浓度,因而需要增加药物渗透深度,促进药物在局部聚集。已有研究提出使用物理和化学方法促进药物在皮肤中的渗透深度,如利用多功能颗粒在皮肤中反应产生气体,从而推动纳米颗粒的运动。但是目前尚缺乏相关的途径及方案促进纳米颗粒及药物在深部疾病区域的渗透及释放,如骨组织的渗透尚无解决方案。
冲击波是一种特殊的波,相较于超声,冲击波的空化效应更显著,在穿透过程中几乎不产热,能量丢失小。冲击波正负压力差值较超声大,所产生的压力更大,渗透更远,可达骨组织。经冲击波刺激后,一些钙盐沉积矿化,矿化沉积增多,利于介导新生骨重建,从而完成骨组织的修复。同时,在冲击波的作用下,冲击波响应型的含药纳米颗粒会吸收冲击波的能量,从而促进其径向运动,并且随着冲击波次数的增加,药物颗粒随之会被破坏,从而释放出药物。
发明内容
本发明所要解决的技术问题就是提供一种利用冲击波促进药物渗透的透皮给药微针贴片及其制备方法,利用冲击波增加微针中纳米载体颗粒渗透进深部组织,并在局部组织周围进行释放。采用的技术方案为:
一种利用冲击波促进药物渗透的透皮给药微针贴片,所述微针贴片包括基底,基底的一面有数个微针,数个均匀排布的微针形成微针阵列,所述微针包括具有冲击波响应性的唑来膦酸纳米颗粒(ZOL-NPs)和可溶性微针基质;所述唑来膦酸纳米颗粒是以唑来膦酸(ZOL)为骨架,与钙离子结合后形成的;所述微针基质包括透明质酸(HA)。
优选的,所述微针为圆锥形,高900微米,底部直径为400微米。
一种利用冲击波促进药物渗透的透皮给药微针贴片的制备方法,包括以下步骤:
(1)制备ZOL-NPs,以PEG与Tween 80构成的胶束为模板,搅拌均匀,在表面缀合氯化钙后,加入ZOL溶液,继续搅拌,去除模板以后,即可得到ZOL-NPs;
(2)将分散好的ZOL-NPs悬液添加进聚二甲基硅氧烷(PDMS)微针阵列模具的凹槽中,放置于真空烘箱中抽真空,弃去凹槽中多余悬液,添加HA溶液以填满凹槽,干燥过夜,即可得到所述的微针贴片。
每个微针阵列可以由10*10个微针构成,每个微针阵列平均可装载纳米颗粒约为1.3mg。微针阵列也可以有12*12、16*16个微针等构成。
优选的,所述步骤(1)中,PEG要先溶解于一定体积的Tris-HCl中,再逐滴加入到Tween80中,边滴加边搅拌,直到充分搅拌。
作为进一步的优选,PEG的质量与Tris-HCl的体积比为1:15~20(g/ml),PEG与Tween80的质量比为1:10~20;
作为进一步的优选,PEG与Tween 80的质量比为3:40。
作为进一步的优选,充分搅拌均匀后,还需要在常温水浴条件下超声20~30min,一般在25℃。
优选的,超声完后,将CaCl
优选的,所述步骤(2)中,抽真空至-30mmHg,20~30min。
优选的,所述步骤(2)中,干燥温度为40~60℃。
一种利用冲击波促进药物渗透的透皮给药微针贴片在透皮给药输送至深组织的应用,尤其是渗透至骨组织。
与现有技术相比,本发明的有益之处在于:
本发明的一种利用冲击波促进药物渗透的透皮给药微针贴片,能够显著提高药物的透皮输送效率,在冲击波作用下,ZOL-NPs吸收冲击波的能量转化为动能,实现了ZOL-NPs向深组织的渗透,可以直达靶向部位,不受消化、吸收、转运时间等的影响;
本发明的一种利用冲击波促进药物渗透的透皮给药微针贴片,ZOL-NPs储藏量高,10*10的微针阵列最多可搭载13.0±0.3mg的ZOL-NPs颗粒,在冲击波作用下更容易破碎以释放出相关药物,如唑来膦酸,钙离子等,从而发挥相关作用,如抑制破骨细胞、促进成骨细胞、促进骨组织的修复等,透皮给药输送至深组织提供了一种新思路。
附图说明
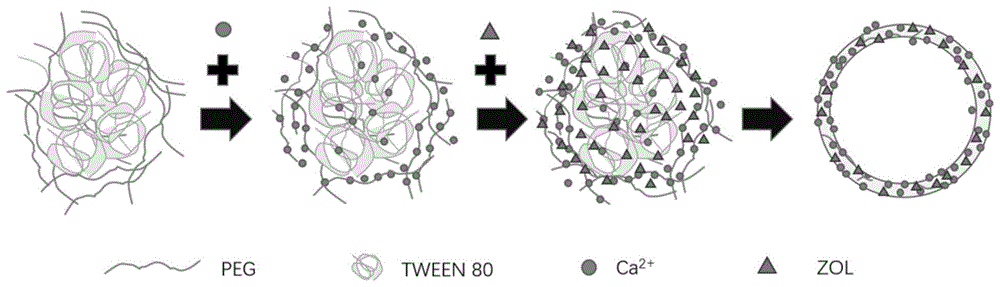
图1为本发明实施例1制备的ZOL-NPs颗粒的制备过程示意图。
图2为本发明实施例1制备的ZOL-NPs颗粒的SEM照片、水合粒径大小及红外图谱(从左到右)。
图3为搭载不同荧光素标记的纳米颗粒装载进微针后微针在荧光显微镜镜下的照片。
图4为骨髓巨噬细胞和骨髓间充干细胞与不同浓度纳米颗粒孵育后细胞活力结果。
图5为冰冻切片镜下观察到的微针刺入皮肤后所形成的孔洞
图6为不同治疗组治疗骨质疏松大鼠后骨指标改善情况。
图7为ESW+MN与静脉注射唑来膦酸两者治疗骨质疏松大鼠后骨指标改善情况。
具体实施方式
附图仅用于示例性说明;对于本领域的技术人员来说,附图中的某些公知结构及其说明可能省略,因此,不能理解为对本发明的限制。
下面结合附图对本发明的技术方案和效果做详细说明。
实施例1
一种利用冲击波促进药物渗透的透皮给药微针贴片的制备方法,包括以下步骤:
(1)如图1所示,制备ZOL-NPs,通过模板法制成,形成球型的纳米颗粒,并且成功携带唑来膦酸药物。
a.配制Tris-HCl溶液:称取0.6057g Tris-Base,溶解在10mL二次水中,用浓盐酸调节pH至8.0。
配制CaCl
b.称取0.15g PEG,溶解于3mL Tris-HCl中,逐滴加入到2g吐温80中,边加边搅拌,充分搅拌均匀后水浴25℃超声20min。
c.取3.5mL CaCl
d.收集反应体系,4℃下反复离心,离心力10000g,沉淀即为ZOL-NPs。
如图2所示,ZOL-NPs呈球型,电镜下大小为66.12±18.68nm,紫外吸收光谱及傅里叶转换红外光谱显示纳米颗粒表面具有ZOL特征峰,表示ZOL药物的成功缀合。
(2)微针的制备,微针基质材料是透明质酸,能成功刺入皮肤,释放出ZOL-NPs。
将分散好的ZOL-NPs悬液添加进PDMS微针阵列模具的凹槽中,放置于真空烘箱中抽真空至-30mmHg,30min,弃去凹槽中多余悬液,添加HA溶液以填满凹槽,40℃干燥过夜,即可得到所述的微针贴片。
所制备的微针贴片,微针针尖为圆锥形,高900微米,底部直径为400微米,每个阵列由10*10个微针构成。如图3所示为用钙黄绿素(calcein)和cy5荧光素标记的ZOL-NPs颗粒装载进微针后的荧光照片可溶性微针基质中装载了纳米颗粒药物,纳米颗粒药物分散于所述微针基质中,本实施例中微针阵列可装载纳米颗粒约为1.3mg。
实施例2
一种利用冲击波促进药物渗透的透皮给药微针贴片的制备方法,包括以下步骤:
(1)如图1所示,制备ZOL-NPs,通过模板法制成,形成球型的纳米颗粒,并且成功携带唑来膦酸药物。
a.称取0.2g PEG,溶解于3.5mL Tris-HCl中,逐滴加入到4g吐温80中,边加边搅拌,充分搅拌均匀后水浴30℃超声15min。
b.取5.0mL CaCl
c.收集反应体系,6℃下反复离心,离心力10000g,沉淀即为ZOL-NPs。
(2)微针的制备,微针基质材料是透明质酸,能成功刺入皮肤,释放出ZOL-NPs。
将分散好的ZOL-NPs悬液添加进PDMS微针阵列模具的凹槽中,放置于真空烘箱中抽真空至-30mmHg,30min,弃去凹槽中多余悬液,添加HA溶液以填满凹槽,50℃干燥过夜,即可得到所述的微针贴片。
所述制备的微针贴片,每个阵列由12*12个微针构成,所述微针阵列可装载纳米颗粒约为1.9mg。其他未述及的地方同实施例1。
实施例3
一种利用冲击波促进药物渗透的透皮给药微针贴片的制备方法,包括以下步骤:
(1)如图1所示,制备ZOL-NPs,通过模板法制成,形成球型的纳米颗粒,并且成功携带唑来膦酸药物。
a.称取0.2g PEG,溶解于3mL Tris-HCl中,逐滴加入到3g吐温80中,边加边搅拌,充分搅拌均匀后水浴25℃超声30min。
b.取4.0mL CaCl
c.收集反应体系,5℃下反复离心,离心力10000g,沉淀即为ZOL-NPs。
(2)微针的制备,微针基质材料是透明质酸,能成功刺入皮肤,释放出ZOL-NPs。
将分散好的ZOL-NPs悬液添加进PDMS微针阵列模具的凹槽中,放置于真空烘箱中抽真空至-30mmHg,30min,弃去凹槽中多余悬液,添加HA溶液以填满凹槽,60℃干燥过夜,即可得到所述的微针贴片。
所述制备的微针贴片,每个阵列由10*10个微针构成,所述微针阵列可装载纳米颗粒约为1.4mg。其他未述及的地方同实施例1。
对本发明实施例1制备的所述微针贴片进行测试。
测试例1,ZOL-NPs的细胞毒性:
将不同浓度的ZOL-NPs与骨髓巨噬细胞(BMM)和骨髓间充质细胞(BMSC)孵育后,利用CCK-8法检测细胞活力。用相同剂量的ZOL作为对比,同时使用空白对比。
以唑来膦酸浓度为基准,统一化颗粒浓度。配置100μM的ZOL-NPs悬液,分别滴加进骨髓巨噬细胞(BMM)和骨髓间充质细胞(BMSC)培养基中,使得ZOL-NPs浓度为0.5、1、2、5、10μM,孵育24h后,根据CCK-8试剂商品化产品说明书,用酶标仪检测细胞活力。
实验结果见图4。如图4所示,ZOL-NPs较ZOL,相同浓度下无明显细胞毒性差异。
测试例2,微针贴片渗透能力测试
将制备好的搭载ZOL-NPs的微针刺入猪皮30分钟后,移除表面微针贴片,固定、脱水猪皮,制备10um厚度切片,显微镜下观察刺入深度。
实验结果见图5所示,猪皮切片有明显针孔,可深达500um,由此判断微针可成功刺入皮肤。
测试例3,测试治疗大鼠的骨质疏松的效果
首先制备去势骨质疏松性大鼠模型:无菌条件下结扎两侧卵巢后饲养1个月。
剃去模型大鼠股骨周围毛发,将大鼠分组:OVX组(模型大鼠),SHAM组(正常健康鼠),微针贴片组(单次施加一个微针阵列),微针结合冲击波组(单次施加一个微针阵列后施加2bar冲击波2000次)。微针与冲击波均施加在大鼠左侧。
麻醉后,根据分组对大鼠进行处理,1个月后对各组的大鼠股骨进行CT扫描。
实验结果如图6所显示,相较于其他治疗组,微针结合冲击波组明显改善单侧股骨指标(左侧),表示微针结合冲击波组能显著地保护局部区域,实现骨质疏松骨折预防保护效果。
同时,新增唑来膦酸组(200ug/kg),以测试本发明的全身治疗效果,结果见图7。可发现大鼠右侧股骨骨指标同样得到改善,表示出递送系统对于非治疗侧的系统性治疗效果。
本发明中使用的英文缩写的含义:
HA-hyaluromic acid,透明质酸
ZOL-Zoledronic acid,唑来膦酸
ZOL-NPs-唑来膦酸纳米颗粒
CaP-磷酸钙
PEG-聚乙二醇;
Tris-HCl-三羟甲基氨基甲烷盐酸盐;
PDMS-聚二甲基硅氧烷;
Calcein-钙黄绿素。
图6、图7中各骨指标:
BV/TV--骨体积分数;Tb.Th--骨小梁厚度;Tb.Sp--骨小梁分离度;Tb.N--骨小梁数;BS/BV:骨表面积骨体积比值。
当然,上述说明并非是对本发明的限制,本发明也并不仅限于上述举例,本技术领域的技术人员在本发明的实质范围内所做出的变化、改型、添加或替换,也应属于本发明的保护范围。
- 一种治疗类风湿性关节炎的微针透皮给药贴片及其制备方法
- 一种载药微针、载药微针贴片、电调控药物释放微针系统及载药微针制备方法
- 一种治疗类风湿性关节炎的微针透皮给药贴片及其制备方法
