一种鉴别新冠肺炎的标志物及其应用
文献发布时间:2023-06-19 11:47:31
技术领域
本发明属于医药生物领域,涉及一种鉴别新冠肺炎的标志物及其应用,具体是通过检测IL-2水平来识别既往感染SARS-CoV-2。
背景技术
细胞因子是一种多肽类细胞调节物质的总称,包括白细胞介素、干扰素、生长因子、细胞刺激因子、肿瘤坏死因子等。细胞因子主要由外周的免疫细胞合成(如巨噬细胞、淋巴细胞、纤维母细胞)。IL-1β、IL-2、IL-4、IL-5、IL-6、IL-8、IL-10、IL-12p70、IL-17、INF-γ、TNF-α、IFN-α等因子为人体免疫中常见的细胞炎症因子,在人体免疫调节中发挥着重要作用。例如IL-1β、IL-6、TNF-α在骨性关节炎、冠状动脉粥样硬化综合症及脑梗死中发挥作用,IL-2、IL-4、IL-5、IL-6、IL-10、INF-γ等由辅助性T细胞Th1和Th2细胞分泌,参与调节Th1和Th2细胞功能的动态平衡,维持机体正常的细胞免疫和体液免疫功能,当机体受到异已抗原攻击导致机体免疫功能平衡发生变化时,Th1和Th2细胞中某一亚群功能升高,另一亚群功能降低,从而Th1和Th2分泌的各的细胞因子浓度也会产生相对应的变化。IL-17主要由参与固有免疫和某些炎症的发生,IL-17具有强大的招募中性粒细胞的独特之处及促进多种细胞因子释放的作用,参与了机体多种炎性疾病的发生。其具有强大的致炎性,是炎症反应的微调因子,它能促进机体局部产生趋化因子,如IL-8、单核细胞趋化蛋白(MCP-1)、生长调节因子-a,从而使得单核细胞和中性粒细胞的迅速增多,能够刺激产生IL-6和前列腺素-2,增强局部炎症。IL-8、IL-12p70、TNF-α等表达水平则在病毒行感染、尖锐湿疣患者血清中显著增高。
新冠肺炎全球蔓延,严重威胁人类健康,研发方便、快捷、有效的生物标志物来及时预测新冠患者至关重要。
发明内容
本发明的目的在于发现感染SARS-CoV-2的标志物,以用于识别既往感染SARS-CoV-2。本发明通过研究发现细胞因子IL-2可以作为否感染过SARS-CoV-2的指标。
本发明通过研究发现新冠康复患者的血液经过SARS-CoV-2抗原肽的刺激后,其IL-2水平相对于健康对照有明显升高,因此,IL-2检测指标适用于临床上快速检测,其可作为检测是否感染过SARS-CoV-2的新指标,能够用于鉴别无症状感染者,也有助于临床流行病学调查。
本发明提供下述技术方案:
用于检测IL-2表达水平的试剂具有制备检测是否感染过SARS-CoV-2的试剂盒的应用。
SARS-CoV-2抗原肽和用于检测IL-2表达水平的试剂具有制备预测是否感染过SARS-CoV-2的试剂盒的应用。
一种检测是否感染过SARS-CoV-2的试剂盒,包含用于检测IL-2表达水平的试剂;进一步地,还包含SARS-CoV-2抗原肽。
进一步地,所述的检测IL-2表达水平的试剂包括ELISA法、化学发光法等方法使用的试剂。
进一步地,所述的试剂盒的检测样本为取自待测主体的血液样本。
本发明具有如下优点和有益效果:本发明用IL-2的表达水平作为检测是否感染过SARS-CoV-2的指标,检测方法简单、检测速度快,灵敏度强(86.4%)和特异度高(96.7%)。
附图说明
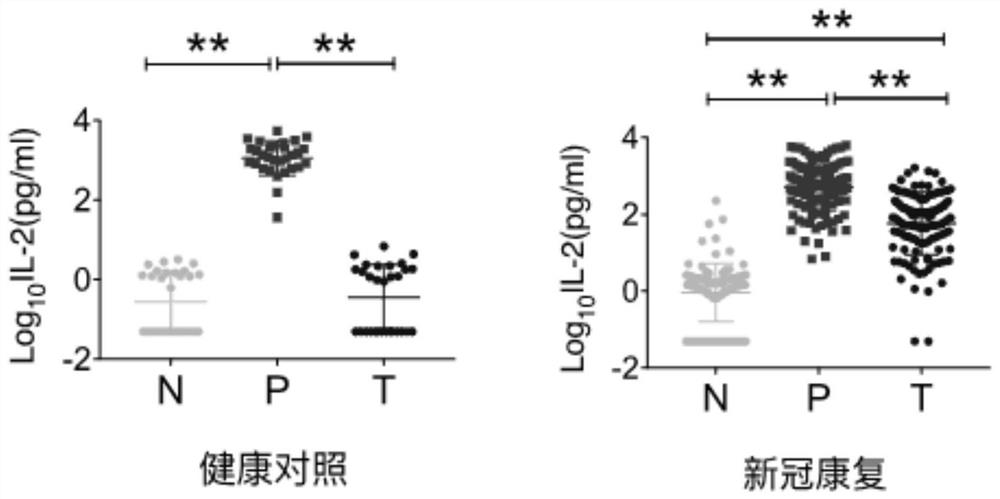
图1是新冠康复患者和健康对照经阴性对照培养液(N)、阳性对照培养液(P)、测试培养液(T)和SARS-CoV-2抗原肽刺激后IL-2的表达情况图。
图2是ROC曲线图。
具体实施方式
以下实施例用于进一步说明本发明,但不应理解为对本发明的限制,其他的任何未背离本发明的精神实质与原理下所作的改变、修饰、替代、组合、简化,均应为等效的置换方式,都包含在本发明的保护范围之内。
若未特别指明,实施例中所用的技术手段为本领域技术人员所熟知的常规手段。
实施例1
1.标本的收集
1.1标本来源
本研究对自124名在武汉大学中南医院住院、SARS-CoV-2感染后康复的COVID-19恢复期患者(男性62名,女性62名),中位年龄52岁(23-83岁),及另外招募的30名健康捐赠者的血液进行检测。这些样本检测在流式细胞仪(BD,美国,FACSCanto II)上完成。
1.2标本要求
1.2.1标本:全血
1.2.2采集:
全血:静脉血样本用EDTA抗凝管收集。
1.2.3保存和运输:待测样本需要抽血后4小时内按上述处理并检测,如无法在4小时内检测,需按上述处理完毕后4℃放置不超过24小时。超过24小时需将采集的全血在-20℃环境下保存不超过一年。样本保存不宜反复冻融(不超过三次)。2-8℃运输。
2.检验方法
2.1实验前准备
3孔细胞培养板;
阴性对照培养液(N):RPMI-1640培养基;
阳性对照培养液(P):含phytohemagglutinin(PHA,植物凝集素)1.6mg/mL;
测试培养液(T):含SARS-CoV-2抗原肽混合肽,SARS-CoV nucleoprotein(N)protein、0.015μg/mL,receptor-binding domain(RBD)of the Spike(S)protein、0.03μg/mL,S1(N-terminal ectodomain containing the RBD)、0.015μg/mL,and N-S1、0.03μg/mL。
十二项细胞因子检测试剂盒(流式荧光法)(购自江西赛基生物技术有限公司),该试剂盒主要组成成分为捕获微球混合液、定量标准品、荧光检测试剂、样品稀释液等,见下表1。
表1
该试剂盒中的捕获微球混合液中有12种荧光强度不同的捕获微球,捕获微球表面分别包被IL-1β、IL-2、IL-4、IL-5、IL-6、IL-8、IL-10、IL-12p70、IL-17、INF-y、TNF-α、IFN-α特异性抗体,捕获微球分别与待测样本中的IL-1β、IL-2、IL-4、IL-5、IL-6、IL-8、IL-10、IL-12p70、IL-17、INF-γ、TNF-α、IFN-α特异性结合后,再与PE标记的荧光检测试剂结合,捕获微球、待测样本、检测抗体形成双抗夹心复合物(捕获微球+待测样本+PE标记的待测抗体),通过分析双抗夹心复合物的荧光强度,得到待测样本的IL-1β、IL-2、IL-4、IL-5、IL-6、IL-8、IL-10、IL-12p70、IL-17、INF-γ、TNF-α、IFN-α的含量。
2.2细胞因子的体外释放
1)采集:全血采集量不低于4mL;
2)培养液分装:在生物安全柜内将阴性对照培养液(N)、阳性对照培养液(P)、测试培养液(T)按照培养板手柄方向自左向右依次加入至细胞培养板相应孔内,100μL/孔;
3)全血分装:八小时内在安全生物柜内分别将1mL混匀后全血分装到细胞培养板相应孔内,1mL/孔。
4)培养:盖紧培养板上盖,迅速放入37℃电热恒温培养箱培养16-24小时,培养过程中保持细胞培养板平放,不可颠倒。
5)收集:培养结束后,将细胞培养板放置于平整桌面上,静置1min小心开盖,从每个细胞培养板孔中吸取上清进行检测;注意:不可吸到细胞层,防止溶血。
2.3标准管制备
1)打开定量标准品(B),将标准品转移到离心管中,并标记该管为最高浓度;
2)2mL样品稀释液(D)重悬标准品,室温下放置15min;
3)用吸头轻轻混匀标准品,避免剧烈震荡;取9根实验上样管,分别标记为1:2、1:4、1:8、1:16、1:32、1:64、1:128、1:256、1:512,每管加入300μL样品稀释液(D);
4)从最高浓度标准品管吸取300μL液体到1:2管中,吹打混匀,从1:2管中吸取300μL液体到1:4中,吹打混匀,如此混匀,如此类推,直到1:512管;如下表2示:
表2
5)标准品管中加入25μL梯度稀释好的标准品;
2.4测试细胞因子表达:
1)样本管中每管加入25μL的待测样本,阴性对照管加入25μL生理盐水;
2)涡旋混匀捕获微球混合液(A),在每个实验管中加入25μL;
3)所有实验管加入25μL的荧光检测试剂(C);
4)实验管涡旋充分混匀后,室温下避光孵育2.5小时;
5)每管实验管中加入1mL PBS溶液,200g离心5min后,小心吸去上清;
6)每管加入100μL PBS溶液,静置等待检测。
7)荧光检测:将实验管按照标准品管、阴性对照管、样品管的顺序依次在校准好状态的流式细胞仪上进行荧光检测。要求每个实验管涡旋混匀3-5秒后立即检测。
3.结果分析
结果显示,新冠康复和健康对照分别都用阴性对照培养液(N)、阳性对照培养液(P)、测试培养液(T)刺激,经P(含phytohemagglutinin)刺激后两组的IL-2都升高,但经过T(含SARS-CoV-2抗原肽)刺激后,两组IL-2升高有明显差异,新冠康复患者IL-2水平明显升高(图1);使用SPSS软件,用健康对照的lg(T/N)及新冠康复的lg(T/N)做ROC曲线,曲线下面积(AUC)为0.935,灵敏度为86.4%,特异度为96.7%,cut-off值2.99(T/N>2.99)(图2、表3)。
表3
- 一种鉴别新冠肺炎的标志物及其应用
- 一种诊断标志物及其在区分新冠病毒感染和新冠病毒灭活疫苗接种中的应用
