一种治疗NPM1突变急性髓系白血病的药物组合物及其应用
文献发布时间:2023-06-19 11:49:09
技术领域
本发明属于肿瘤治疗技术领域,涉及一种治疗NPM1突变急性髓系白血病的药物组合物及其应用。
背景技术
急性髓细胞白血病或急性髓系白血病(acute myeloid leukemia,AML)是一种常见的侵袭性血液恶性肿瘤,以骨髓和外周血中髓系原始细胞异常克隆增生为主要特征,是成人尤其是老年人最常见的急性白血病类型。据美国国家癌症研究所(NCI)统计,近10年来,白血病发病率每年14.1/万人,死亡率每年6.3/万人,占新发肿瘤疾病的3.4%。AML的预后差,<65岁的患者中五年生存率为34.4%,>65岁的患者则仅为5%。
化疗是AML的主要治疗手段,指南提示AML(非APL)的标准诱导化疗方案是蒽环类药物联合标准剂量阿糖胞苷(Ara-C)(即3+7方案),在达到临床缓解和骨髓检查血液状态恢复后继以大剂量Ara-C为基础的巩固治疗。在使用标准化疗方案治疗后有50%-70%的病人可以得到缓解,但是有超过一半的年轻成年人和80%-90%的老年病人会复发。尽管白血病的发病机制尚不明确,但是比较公认的是AML起源于造血干细胞或具有自我更新潜能的干细胞样特性的祖细胞的致瘤转化,由于这种具有干细胞特性的白血病细胞能够耐受化疗,从而容易导致AML的高复发率,也导致AML总体生存率较差。虽然诱导化疗后造血干细胞移植(HSCT)有治愈AML的潜力,但是对于老年患者该治疗方式并不可行。寻找其他治愈方式是AML治疗的迫切需求。
免疫疗法旨在启动或重新启动个体对抗肿瘤的免疫力,此种方法有望治愈各种类型的肿瘤。目前存在多种免疫疗法,在这些肿瘤免疫疗法中,肿瘤疫苗可以诱导持久的免疫力,具有安全性和可靠性。肿瘤疫苗的作用机制为诱导肿瘤特异性T细胞的生成及扩增,同时重新激活已存在于机体自身的处于休眠或无反应状态的肿瘤特异性T细胞。尽管肿瘤疫苗具有用于肿瘤免疫治疗的巨大潜力,但某些患者的临床结果仍然欠佳,过去,这可能归因于肿瘤抗原的选择,因为传统的肿瘤疫苗主要针对肿瘤相关抗原,这种抗原除了存在于肿瘤细胞,也可存在于正常细胞。随着测序技术的发展,目前越来越多的肿瘤突变基因被发现,这有利于新抗原肿瘤疫苗的构建。
在AML中,核仁磷酸蛋白1(NPM1)突变(ΔNPM1或mutNPM1)为最常见的突变之一,其发生率达30%-35%。NPM1广泛表达于核仁,它可以在细胞核和细胞质之间穿梭,参与核糖体蛋白的组装和运输,调控中心体的复制以及调控肿瘤抑制因子ARF的表达,在维持细胞正常生物活动中起着重要作用。NPM1的突变会导致该蛋白从细胞核转移至细胞质,导致AML的发生。NPM1具有不同的突变类型,然而,尽管突变类型不同,但大部分的突变都在蛋白质C末端产生了相同的氨基酸序列,这种稳定氨基酸序列的产生意味着突变的NPM1可作为免疫治疗的良好靶点。
免疫治疗是目前治疗急性髓系白血病的新型治疗方法,其中,多肽疫苗可以调动机体的免疫系统,是一种安全有效的治疗方法,故针对ΔNPM1的肿瘤疫苗为治疗NPM1突变的AML的有效方法。然而,肿瘤微环境是一种复杂的环境,其中,肿瘤细胞抗原免疫逃逸是导致单用多肽疫苗治疗失败的重要原因。因此,通过与其他化合物的组合治疗改善肿瘤微环境以及增强肿瘤细胞免疫原性是保障肿瘤多肽疫苗治疗成功的重要因素之一。
发明内容
为了解决上述背景技术中所提出的问题,本发明的目的在于提供一种治疗NPM1突变的AML的药物组合物及其应用。
为了达到上述目的,本发明所采用的技术方案为:一方面,本发明提供了一种ΔNPM1表达促进剂在制备增强靶向ΔNPM1的肿瘤疫苗治疗NPM1突变急性髓系白血病疗效的药物中的应用。
另一方面,本发明提供了一种ΔNPM1表达促进剂在制备增强靶向ΔNPM1的肿瘤疫苗对NPM1突变急性髓系白血病细胞杀伤作用的药物中的应用。
另一方面,本发明提供了一种ΔNPM1表达促进剂与靶向ΔNPM1的肿瘤疫苗联用在制备治疗NPM1突变急性髓系白血病的药物中的应用。
再一方面,本发明提供了一种治疗NPM1突变急性髓系白血病的药物组合物,包括ΔNPM1表达促进剂和靶向ΔNPM1的肿瘤疫苗。
再一方面,本发明提供了一种试剂盒,包括上述所述的治疗NPM1突变急性髓系白血病的药物组合物。
进一步地,所述ΔNPM1表达促进剂包括地西他滨或其药学上可接受的盐或其水合物。
进一步地,所述靶向ΔNPM1的肿瘤疫苗为靶向ΔNPM1的CTL表位肽疫苗。
进一步地,所述靶向ΔNPM1的CTL表位肽疫苗包括氨基酸序列如CLAVEEVSL、AVEEVSLRK、CLAVEEVSLRK、VEEVSLRK、AVEEVSLR所示的多肽。
本发明的有益效果是:申请人在体外实验中发现,地西他滨可上调细胞膜上ΔNPM1的表达。本发明将地西他滨或其药学上可接受的盐或其水合物与靶向ΔNPM1的肿瘤疫苗联合运用,该联合用药物组合物成功地将化学疗法和肿瘤疫苗免疫疗法结合起来,具有较高的生物安全性,具有比单一化学疗法或单一肿瘤疫苗免疫疗法更强的抗肿瘤活性,为肿瘤的治疗提供了新的策略和思路;同时能够降低化疗药物的使用剂量,降低化疗药物产生的毒副作用,降低肿瘤患者的治疗成本;同时,化疗药物通过上调肿瘤细胞表面肿瘤抗原,从而诱导出更强的抗肿瘤特异性免疫反应,发挥持续的免疫疗法和化疗的协同效应。本发明地西他滨(De citabine)或其药学上可接受的盐或其水合物与靶向NPM1突变的肿瘤疫苗的组合用于罹患NPM1突变急性髓系白血病(AML)的患者具有很好的治疗效果。
附图说明
图1为OCI-AML3/HLA-A*1101细胞在不同浓度的地西他滨下增殖能力的结果图;
图2为地西他滨作用于OCI-AML3/HLA-A*1101细胞的凋亡流式结果图;
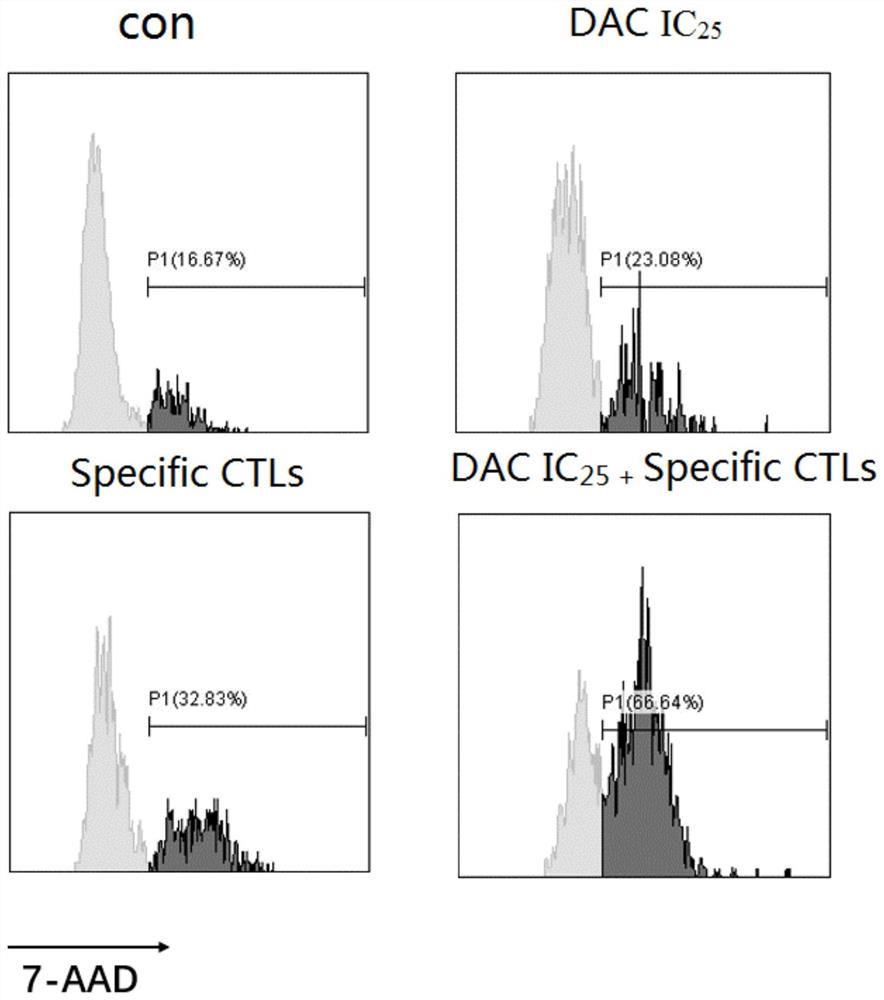
图3为地西他滨和特异性CTL协同杀伤OCI-AML3/HLA-A*1101的结果图。
具体实施方式
下面通过具体实施方式来进一步说明本发明的技术方案。本领域技术人员应该明了,所述实施例仅仅是帮助理解本发明,不应视为对本发明的具体限制。
说明书和权利要求书中所使用的缩写的含义列于下表中:
实施例1
本实施例所需的实验材料和试剂包括:
细胞系:OCI-AML3;
化学治疗药物:地西他滨(Decitabine,缩写DAC);
转染病毒:HLA-A*1101;
多肽:靶向ΔNPM1的可作用于HLA-A*1101的多肽,AVEEVSLRK。
1、构建HLA-A*1101阳性的OCI-AML3细胞
(1)收集状态良好的OCI-AML3细胞,用无血清RPMI-1640重悬细胞,以每孔2×10
(2)用病毒转染增强液Eni.S稀释病毒,按MOI=100加入病毒液,,37℃、5%CO
(3)感染72h后,在荧光显微镜下观察GFP的表达情况。
2、制备靶向ΔNPM1的可作用于HLA-A*1101的肿瘤治疗性疫苗:
(1)常规聚蔗糖-泛影分离人新鲜全血,获得外周血单个核细胞(PBMC),用含有10%胎牛血清的RPMI-1640完全培养基调整细胞浓度为3.0×10
(2)次日每孔分别加入多肽至终浓度为10μg/ml;
(3)每2~3天半量换液并补充IL-2至终浓度为50U/ml;
(4)每周用多肽对PBMC进行刺激,即每组分别加入多肽至终浓度为10μg/ml;
(5)第三轮刺激后收集细胞,得到效应细胞CTL。
3、检测地西他滨抑制HLA-A*1101阳性的OCI-AML3细胞增殖的能力:
(1)细胞处理:收集生长对数期的OCI-AML3/HLA-A*1101细胞,按1.0×10
(2)细胞处理72小时后,每孔加入10μl CCK-8;
(3)将96孔板置于细胞培养箱中孵育3h;
(4)取450nm波长,用酶标仪进行检测96孔板中每个孔的吸光度值(A);
(5)结果计算:细胞增殖率=1-(A处理组-A空白组)/(A非处理组-A空白组)×100%。
地西他滨抑制OCI-AML3/HLA-A*1101细胞增殖能力的结果图如图1所示,地西他滨对OCI-AML3/HLA-A*1101增殖的抑制作用随浓度的增高逐渐增高,在浓度为0.1μM时,抑制率达到25.04±2.36%,由此看出,地西他滨对OCI-AML3/HLA-A*1101的毒性作用是随浓度逐渐增加的,0.1μM可视为地西他滨作用与OCI-AML3/HLA-A*1101的IC
4、CTL表位肽诱导的特异性CTL对地西他滨预处理后OCI-AML3/HLA-A*1101特异性杀伤效应的检测:
(1)靶细胞制备:
①靶细胞:OCI-AML3/HLA-A*1101细胞
②用含10%胎牛血清的RPMI-1640完全培养基培养OCI-AML3/HLA-A*1101细胞,调整地西他滨浓度至地西他滨作用于OCI-AML3/HLA-A*1101细胞的IC
③预处理72小时后,收集OCI-AML3/HLA-A*1101细胞,PBS洗涤两次;
(2)效应细胞制备:将2中制备得到的效应细胞CTL,用含5%胎牛血清的RPMI-1640培养基调整至1×10
(3)杀伤效率检测:
①分组:OCI-AML3/HLA-A*1101细胞加PBS组,地西他滨预处理OCI-AML3/HLA-A*1101细胞组,OCI-AML3/HLA-A*1101细胞与特异性CTL共孵育组,经地西他滨预处理后OCI-AML3/HLA-A*1101细胞与特异性CTL共孵育组;
②经上述处理的OCI-AML3/HLA-A*1101细胞用细胞膜染料CFSE预染;
③按照分组将OCI-AML3/HLA-A*1101细胞按1×10
④按效靶比10:1加入特异性CTL,补充各孔含5%胎牛血清的RPMI-1640培养基至终体积为100μl;
⑤细胞铺板后,37℃,5%CO
⑥在50μl的1×Assays Buffer中加入5ul7-AAD染料,混匀;
⑦收集上述各分组细胞加入7-AAD染料中,混匀;室温、避光反应15min;
⑧加入450μl的1×Assays Buffer悬浮细胞并于1小时内用流式细胞仪进行检测。
检测结果如图3所示,将预处理后的OCI-AML3/HLA-A*1101细胞与特异性CTL共孵育12小时后,培养体系中7-AAD阳性比例上调,且上调幅度大于单独使用地西他滨及单独与特异性CTL共孵育的培养体系,表明地西他滨与特异性CTL可产生协同作用杀伤肿瘤细胞。
以上实验证明,上调NPM1突变AML细胞系(OCI-AML3细胞)膜上ΔNPM1的表达可增强靶向ΔNPM1的肿瘤疫苗的肿瘤杀伤作用;地西他滨和靶向ΔNPM1的肿瘤疫苗在肿瘤杀伤方面具有显著的协同作用,具体地,地西他滨和靶向ΔNPM1的肿瘤疫苗联合使用比单独使用地西他滨或单一肿瘤疫苗免疫疗法具有更强的抗肿瘤活性。
综上,地西他滨可通过上调肿瘤细胞表面肿瘤特异性抗原从而增强肿瘤疫苗的肿瘤杀伤作用,地西他滨与特异性CTL可产生协同作用杀伤肿瘤细胞。因此,本发明将地西他滨与肿瘤疫苗联合运用,在肿瘤特异性免疫治疗领域有着巨大的开发应用潜力。
以上所述仅为本发明的具体实施方式,不是全部的实施方式,本领域普通技术人员通过阅读本发明说明书而对本发明技术方案采取的任何等效的变换,均为本发明的权利要求所涵盖。
- 一种治疗NPM1突变急性髓系白血病的药物组合物及其应用
- 一种治疗急性髓系白血病的联合用药物组合物及其应用
