一种基于层析纯化的连续纯化装置和方法
文献发布时间:2023-06-19 19:00:17
技术领域
本发明涉及层析纯化领域,具体地涉及一种基于层析纯化的连续纯化装置和方法。
背景技术
层析技术亦称为色谱技术,是生物行业应用最广泛的分离纯化及检测鉴别技术,比较著名的应用有气相色谱、高效液相色谱等。在制药工业中常用的层析技术属于液相色谱技术,是工业化制药中主流的分离纯化工艺方法。
工业化层析技术以分子排阻层析技术为基础,在分子排阻层析的介质上耦联上不同属性的分子基团发展出各种吸附类层析,如(阴/阳)离子交换层析、疏水层析、亲和层析、反相层析等层析技术,而每一步纯化工艺基本采用一种层析技术下的一种层析介质。不同于普通分子排阻(普通分子排阻采用自制凝胶网状结构为阻碍介质,小分子运动快在前,大分子运动慢在后),工业化的分子排阻介质为多孔状微球,填充层析柱形成阻碍介质,小分子进入微球的孔中运动更慢,大分子不能进入微球孔中反而运动快,从而形成大分子在前而小分子在后的分离谱带。
层析技术的基本操作是以层析介质为固定相,以缓冲液及待纯化样品为流动相,依次通过固定相,样品流过固定相后不同性质的组分会分先后流出固定相,从而达到分离纯化的目的,一般把样品进入固定相的操作过程称为上样,纯化后收集流出的目标组分的过程称为下样或收样,上样后用缓冲液冲出未吸附组分的过程称为冲洗或流洗,冲洗后用缓冲液冲出吸附组分的过程称为洗脱,吸附类层析上样条件不吸附的流出组分称为流穿液;通过实时监测,流出的不同组分在监测图谱上显示为监测值先上升后下降的峰图,每1个监测峰代表1类不同的组分,因此常用峰来命名不同的组分,如流穿峰、洗脱峰、第1峰、第2峰等
发明内容
本发明的目的是提供一种基于层析纯化的连续纯化装置及方法,通过省略多步纯化中间的上样和收样环节,在管道中完成所有设计的纯化流程后再收样,将多步纯化生产工艺连续化实施,实现生产连续化及自动化;并通过连续化工艺设计实现混合层析、混合纯化一步法。
为实现上述目的,本发明采取以下技术方案:
一种基于层析纯化的连续纯化装置,其特征在于,包括:
多个纯化通路,即2个或以上纯化通路,每个纯化通路至少包括1套泵系统、1套柱位选择阀阀门系统以及1套监测系统,可以各自、同时并行进行样品纯化工艺操作;
通过阀门控制流动相的流路,选择性的串联多个纯化通路中的两个柱位选择阀上的层析柱,以完成纯化过程中纯化目标在两个层析柱中的转移;
其中,所述柱位选择阀是一种多选一的层析柱并联连接阀门;通过柱位阀切换不同的层析柱,以实现更少的纯化通路进行更多层析柱的连续纯化。
所述多个纯化通路的串联,可以是2个纯化通路的循环串联,也可以是更多个纯化通路的循环串联,通过循环使用纯化通路、减少纯化通路来节省设备资源,而增加纯化通路来节约工艺等待时间;
连接在柱位选择阀上的层析柱可以根据不同的工艺设计,填充不同的层析介质或非层析介质;
连接在柱位选择阀上的是还可以同样一端进液、一端出液的其他纯化载体;
每个纯化通路中还包括阀门来控制多纯化通路中层析柱的串联;
一种基于层析纯化的连续纯化方法,其特征在于,包括:
多个纯化通路同时并行进行多个纯化工艺流程各自的清洗、准备、洗脱、再生等正常操作流程;
选择性连接两个纯化通路中的两个层析柱,在串联状态下完成纯化目标从一个层析柱到另一个层析柱的转移;
使用其中一个纯化通路按正常纯化工艺流程进行第一步纯化工艺,到需要收集纯化目标时,将纯化目标通过管道及阀门控制传递到第二个纯化通路的层析柱中,同时开始第二步纯化的进样环节,在第二个纯化通路中完成第二步纯化;如此循环,直至完成所有支持的纯化工艺流程;
通过层析技术选择或工艺设计,纯化目标在连续纯化层析柱中转移的过程中保持了前面纯化的分离状态及稀释状态,以便于进一步纯化分离,且不会进一步稀释,从而达到多合一一步纯化的效果;反之也可将一步层析拆分为多步层析进行连续纯化或连续循环层析,达到层析介质分段寿命管理及无限柱高的目的;
通过选择不同的层析介质、非层析纯化介质或其他纯化载体,以及提供不同缓冲液环境达到混合层析或混合纯化的目的;
通过将设计好的多步纯化生产工艺进行连续化、系统化转换,并将工艺流程进行定时或参数化、条件化控制,达到自动化生产的目的;
本发明由于采取以上技术方案,其具有以下优点:
通过连续纯化装置设计、系统支持以及流程方法控制,可以减少纯化的损失,减少样品稀释,提高制品的产量;或者引入更多纯化步骤,提高制品的质量(纯度);连续化的工艺控制可以促进生产自动化;开创连续纯化的工艺设计方法,简化流程,实现混合层析、混合纯化,达到纯化技术多合一的效果,或者一步层析一拆多,实现层析介质分段寿命管理或连续循环的无限柱高的应用方向。
附图说明
通过阅读下文优选实施方式的详细描述,各种其他的优点和益处对于本领域普通技术人员将变得清楚明了。附图仅用于示出优选实施方式的目的,而并不认为是对本发明的限制。在整个附图中,用相同的附图标记表示相同的部件。在附图中:
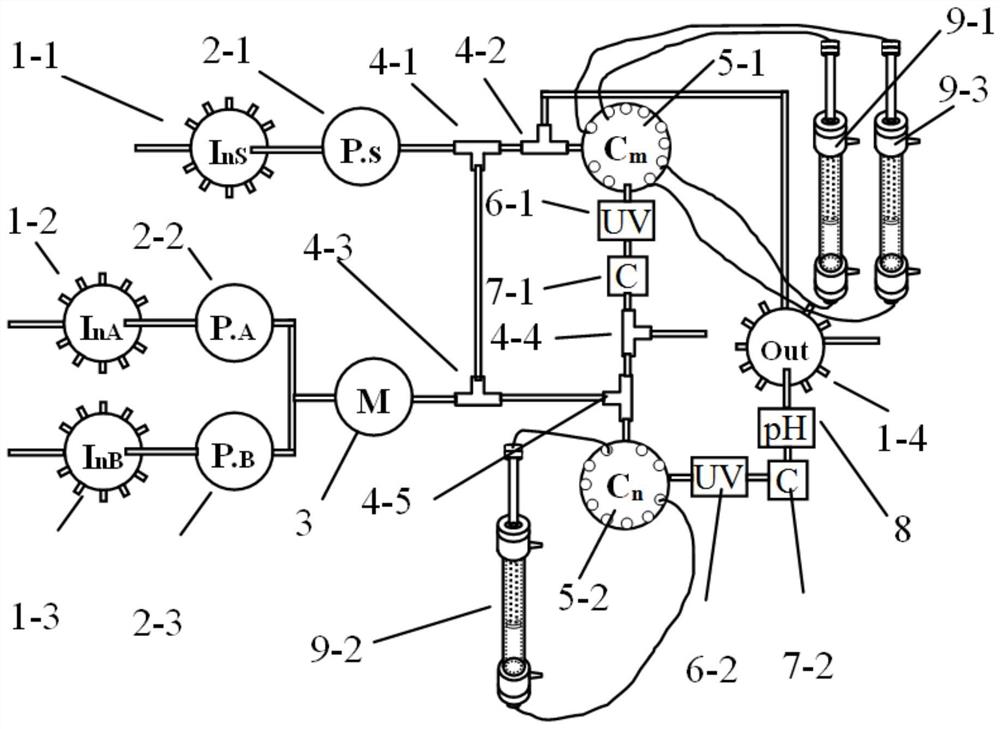
图1是连续纯化系统流路设计图。
附图中各标记表示如下:
1-1/1-2/1-3/1-4多通路选择阀
2-1/2-2/2-3/泵
3混和器
4-1/4-2/4-3/4-4/4-5三通阀
5-1/5-2柱位选择阀
6-1/6-2紫外监测仪
7-1/7-2电导率监测仪
8pH值监测仪
9-1/9-2/9-3层析柱
具体实施方式
下面将参照附图更详细地描述本发明的示例性实施方式。虽然附图中显示了本发明的示例性实施方式,然而应当理解,可以以各种形式实现本发明而不应被这里阐述的实施方式所限制。相反,提供这些实施方式是为了能够更透彻地理解本发明,并且能够将本发明的范围完整的传达给本领域的技术人员。
稀释层高理论
稀释层高理论基于以下现象:
层析柱串联延长等效于同长度层析柱在层析介质相同,在柱效合格、工作流速相同的前提下,4根直径16mm且柱介质高20cm的层析柱串联后,与1根16mm,柱介质高80cm的层析柱纯化效果基本一致的。
层析柱延长后纯化后样品稀释度变化不大在样品足够纯且不与层析介质吸附的前提下,10mL样品经过1根直径16mm且柱介质高80cm的层析柱以后,峰宽约15mL;经过2根同样的柱子后,峰宽约16mL。而如果分两次纯化上样,就是上样10mL收样16mL,2次上样16mL收样22mL,稀释度会增加。
为了解释上述现象,可以进行以下设定:
稀释过程通过峰宽来说明,计算过程使用10%峰高处峰宽,以提升结论的广泛性。在层析柱中,与溶液体积相关的峰宽,保留体积等按线性流速的算法,即溶液体积÷层析柱截面积换算成“线性高度”,以提升结论的广泛性,如线性层高、稀释层高、样品层高等。
上述现象反应了样品在层析柱中的稀释规律:
当上样量的线性高度达到一定值时(6~8cm),峰尖样品保持了上样前浓度,峰尖前后形成线性高度9~12cm的稀释层,收样层高约等于稀释层高;当上样量的线性高度超过“一定值”时,峰顶形成与上样前浓度差不多的平台峰,而平台峰的前后稀释层线性高度不变,即样品在层析柱中的稀释层高不变,收样层高约等于稀释层高加平台层高;当上样量的线性高度低于“一定值”时,所有样品均被稀释,峰尖低于上样前浓度,峰尖前后的稀释层相互交叉反复稀释,稀释层仍然约有9~12cm,即样品在层析柱中的稀释层高不变,收样层高约等于稀释层高,但相对于上样量,稀释比却大大增加。
根据以上规律,申请人发现在层析柱的柱效测定中,规定采用1%的上样量,远低于稀释层高(柱高一般不超过100cm),这就导致了柱直径越大则柱效检测结果越低的天然缺陷,只有柱高与柱直径等比放大才能弥补这一缺陷,但这是不太可能实现的;另外,根据柱效计算公式,柱效的影响因素为保留体积和半峰宽,保留体积约等于柱体积,且与层析介质有关,那么对于装填介质的柱效影响最大的是半峰宽,半峰宽则受上样量的线性高度影响,上样高度与稀释层高相差越大,计算的柱效越低,而不是因为层析柱装填的不好;因此反应层析柱装填好坏的最佳参数是稀释层高。
稀释层高理论:单一组分的生化分子在相同层析介质的层析柱中流动与前后流动相稀释形成稀释层的线性高度是相对固定的,稀释层高值越低层析柱装填效果越好,对于分子排阻分离越有利。
层析柱的稀释层高可以用15~30cm上样量上样测定,测量用试剂及测量流速参考柱效测量方法,计算方法为:
Hx = h1 - h0 公式1
其中:Hx–稀释层高;h1-10%峰高处线性峰宽;h0-上样量线性高度。
分子排阻色谱分离中,是样品层高在线性柱高的距离内与杂质分子因速度差而分离,自身长度与“跑道”的长度一样重要,这也是稀释层高或样品线性高度计算的意义所在。
在以上例子中,单个层析柱的收样的稀释层高与双柱收样的稀释层高几乎一致,约6cm;这就为多柱串联的可行性研究提供了更简洁的理论依据。
通过本理论,可以确定,在条件相同的前提下,样品在层析柱中的线性高度是不变的,在进入不同介质的层析柱后,如果进入Hx值更大的层析柱,样品的线性高度h1会增加,增加后的稀释层高不会超过层析柱的Hx;反之,样品的线性高度h1不会增加。同样,可以用h1与柱高的比值来确定样品的最佳分离柱高,再通过连续层析系统延长柱高,以获得最佳分离。一般串联的方法由于压力或流速的限制不可能无限延长柱高,而最佳分离柱高可能会达到数米甚至更高。
尽管我们可以通过上样体积和出样体积来计算差来计算理论的稀释层高,但是实际上样品中不同组分在层析柱中占据的柱体积与它的流速有关,比如外水体积中的组分流速较快,它所占据的柱高度是约是上样层高的3倍,而最小的盐类分子所占据的柱体积约等于上样体积加稀释体积,样品中纯化目标在层析柱中的实际层高是我们在连续层析纯化中选择层析柱高度可能需要考虑的问题。在连续层析纯化过程中,纯化目标在不吸附的情况下具有相对固定的稀释层高,制品在层析柱中的理论高度决定了分子排阻的分离效果与层析过程中的稀释效应,而制品在层析柱中的实际高度决定了分子排阻层析的上样量以及层析柱体积的准备量。
基于稀释层高相对稳定的现象,结合层析纯化操作的一般流程,本发明提出了一种将多种层析技术结合起来的连续纯化方法,在进行了多步层析纯化后,收样的浓度及稀释度能基本维持在与一步层析相同的水平;同时还设计了一套装置以实现更方便的连续层析实施与控制。
连续层析纯化装置
连续层析纯化装置由多个单独的纯化通路组成,附图1展示了一套由两个纯化通路组成的连续纯化系统流路图:
第一条纯化通路(流路1)由多通路选择阀1-1、泵2-1、三通阀4-1、三通阀4-2、柱位选择阀5-1、紫外监测仪6-1、电导监测仪7-1、三通阀4-4用管道连接而成;
第二条纯化通路(流路2)由多通路选择阀1-2、泵2-2、多通路选择阀1-3、泵2-3、混合器3、三通阀4-3、三通阀4-5、柱位选择阀5-2、紫外监测仪6-2、电导监测仪7-2、pH监测仪8、多通路选择阀1-4用管道连接而成;
其中柱位选择阀上可以连接多个层析柱,同一时间,只有一根层析柱连接在通路中,下一个时间也可以选择另一根层析柱连接在通路中;
概括来说,一条纯化通路由1套泵系统、1套柱位选择阀阀门系统及1套监测系统组成;泵系统可以是一个泵的单泵,也可以是双泵加混合器的配液泵系统;柱位选择阀阀门系统可以是一个柱位选择阀实现足够多层析柱的连接,也可以是多个柱位选择阀并联实现更多层析柱的连接;1套监测系统可以是一个或多个监测仪,按需配置。其他三通阀的存在是为了实现两个纯化通路中柱位选择阀的串联,而多通路选择阀1-1、1-2、1-3可以连接纯化所需的各种流动相,多通路选择阀1-4可以为不同的组分峰选择不同的出口。
通过阀门切换,可以把第二条纯化通路中的柱位选择阀(层析柱)串联在第一条纯化通路后面,以完成纯化目标的转移,连接顺序为:
流路3:多通路选择阀1-1、泵2-1、三通阀4-1、三通阀4-2、柱位选择阀5-1、紫外监测仪6-1、电导监测仪7-1、三通阀4-4、三通阀4-5、柱位选择阀5-2、紫外监测仪6-2、电导监测仪7-2、pH监测仪8、多通路选择阀1-4
通过阀站切换,也可以把第一条纯化通路中的柱位选择阀(层析柱)串联在第二条纯化通路后面,以完成纯化目标的转移,连接顺序为:
流路4:多通路选择阀1-2、泵2-2、多通路选择阀1-3、泵2-3、混合器3、三通阀4-3、三通阀4-5、柱位选择阀5-2、紫外监测仪6-2、电导监测仪7-2、pH监测仪8、多通路选择阀1-4、三通阀4-2、柱位选择阀5-1、紫外监测仪6-1、电导监测仪7-1、三通阀4-4。
这样就可以实现两个纯化通路的循环使用,由于柱位选择阀可以不同的层析柱,这样就可以在下一个循环时使用不同的层析柱,从而实现几乎无限层析柱的连续纯化;但是由于不同纯化工艺使用的流速不一样,柱体积不一样等因素,上一步工艺的收样时间与下一步工艺的上样时间可能不是完美切合的,这样就需要等待,或者在系统设计时加入更多的纯化通路来防止“堵车”。
连续层析纯化方法
连续纯化的基本方法是通过多个纯化通路同时并行进行多个纯化工艺流程各自的清洗、准备、洗脱、再生等正常操作流程;然后选择性连接两个纯化通路中的两个层析柱,在串联状态下完成纯化目标从一个层析柱到另一个层析柱的转移;
具体到纯化工艺操作是使用其中一个纯化通路按正常纯化工艺流程进行第一步纯化工艺,到需要收集纯化目标时,将纯化目标通过管道及阀门控制传递到第二个纯化通路的层析柱中,同时开始第二步纯化的进样环节,在第二个纯化通路中完成第二步纯化;如此循环,直至完成所有支持的纯化工艺流程;
通过层析技术选择或工艺设计,纯化目标在连续纯化层析柱中转移的过程中保持了前面纯化的分离状态及稀释状态,以便于进一步纯化分离,且不会进一步稀释,从而达到多合一一步纯化的效果;反之也可将一步层析拆分为多步层析进行连续纯化或连续循环层析,达到层析介质分段寿命管理及无限柱高的目的;
示例1吸附类层析及前后换液一步法
吸附类层析对缓冲液的要求较高,经典三步法(换液,层析,换液)本身步骤已经过多,常常需要考虑与其他纯化方法进行融合或替代,如浓缩洗滤换液,分子排阻层析纯化加换液,这就使得吸附类层析考虑问题会更复杂,三步法经过连续纯化后几乎可以当作一步纯化再看待。
工艺设定:假设某一吸附类层析工艺是在溶液1条件下上样,溶液2条件下洗脱杂质,溶液3条件下洗脱纯化目标,而溶液4是纯化目标的稳定保存条件;要实现这工艺条件一般思路为,首先要通过一个分子排阻层析将样品缓冲液更换为溶液1,然后进行吸附层析,最后通过分子排阻层析将洗脱的纯化目标缓冲液更换为溶液4。如附图1,设定层析柱9-1装填分子排阻介质,柱高约50cm;层析柱9-2装填某吸附类层析介质,柱高约5cm。则连续纯化的操作流程如下:
1、流路1层析柱9-1在线,依次进行层析柱9-1的清洗、溶液1冲洗至平衡、上样、溶液1流洗;同时流路2(层析柱9-2在线)进行层析柱9-2的清洗、溶液1冲洗平衡并暂停等待;
2、流路1紫外监测仪6-1监测到目标峰出现,立即切换流路3,让纯化目标流进层析柱9-2中,直至全部进入后切换回流路1;
3、流路1继续流洗杂质峰,并清洗再生,再用溶液4冲洗至平衡后暂停等待;流路2继续冲洗溶液1至流穿峰全部流出,再用溶液2洗脱至杂质峰全部流出,再用溶3洗脱,
4、紫外监测仪6-2监测到目标峰出现,立即切换流路4,让目标峰全部进入层析柱9-1中,然后切流路2;
5、流路1继续冲洗溶液4,收集目标峰,清洗再生,完成;流路2继续清洗再生,完成。
吸附复合分子排阻层析方法
在示例1中,假设吸附类层析在溶液1条件下的流穿峰即为纯化目标(不需要溶液2、溶液3洗脱),则纯化目标经过层析柱9-1、层析柱9-2流穿,再回到层析柱9-1,在流经层析柱9-2时有一些杂质被吸附了,纯化目标流动规律没有受到吸附影响,而吸附类层析介质具有分子排阻介质的基架,这样目标制动的流动轨迹就像一个三柱串联的分子排阻层析一样,却又能通过吸附去除部分杂质。这个方法比较适用于一些稳定差不能使用吸附类层析进行纯化的生物制品。
分子排阻无限柱高实现方法
分子排阻层析理论上柱高越高分离效果越好,但是柱高受层析介质耐压限制,一般不超过1米,多柱串联也会因累积压力而不得不降低流速,降低流速会严重影响工作效率。而连续纯化提供了短层析柱无限串联扩展柱高的可能,而且由于短柱可以以更高的液体流速分开进液,纯化效率会更高,填充介质的耐用性会更好,然后无限柱高可以用2-3根短层析柱循环使用来实现,不需要准备无数短层析柱,可以节省大量层析介质。
在示例1中,假设层析柱9-2中填充的是与层析柱9-1相同的分子排阻层析介质,则纯化目标在流经层析柱9-1、层析柱9-2,再回到层析柱9-1,这样纯化目标流经的层析柱高已可以达到150cm,如果需要,这个循环还可以继续下去,无限循环就可以做到无限柱高。
假定一个分子排阻层析工艺需要上样10升浓缩液,分两次纯化完,每次上样5升,按10%上样量计算,需要50升柱体积的层析介质,一般考虑选用一个能装50升介质的层析柱或2个各装25升介质的层析柱串联,还要在总柱高与纯化时长之间平衡,选择直径35cm柱高52cm的层析柱1个速度更快,纯化效果差;选择直径25cm柱高51cm的层析柱2个串联纯化效果更好,速度较慢。连续纯化设计则考虑样品是否能完整进入单根层析柱,这与目标峰位置及上样量有较大的关系,如果目标峰在第1峰最先流出,则前面的例子中可以选择直径25cm柱高34cm的层析柱2个进行连续纯化,节省略1/3的层析介质。
如果工艺要求的上样量减半(5%)则可以节省2/3的层析介质(传统需要100升层析介质进行纯化),如果工艺要求的上样量达到15%则不能节省介质,只有提速的效果,大于15%则需要使用更多的层析介质,拆分为连续纯化毫无意义
如果目标峰在最后出现,层析介质直接节省90%左右(上样10%),目标峰在中间位置则要根据实际情况计算,节省的介质应在33%-90%之间。
柱效的影响:柱效差,峰变宽,保留时间变短,需要更多的柱高更多的介质来完整保留样品;目标样品均一度的影响:目标样品不同程度聚集造成大小不一、相互分离,拉长了峰宽,需要更多的柱高,更多的介质来完整保留样品。总之需要根据实际的保留时间与峰宽来核算。
示例4分子排阻层析介质寿命管理方法
通常层析柱的寿命与样品杂质堵塞介质上端(层析柱进液端)有很大的关系,堵塞后压力增大,压力过高会使层析介质塌陷,通常用减流速来降压,减流速会影响工作效率,减到一定程度需要重新装填介质时就是层析柱寿命终止,层析介质多次装填后,柱效不合格或流速不合格则宣告层析介质寿命终止。连续纯化的条件下,传统一根层析柱的介质被分散到2-3根短层析柱中,往往样品进入的第1根层析柱会堵塞,而后面的层析柱不会,这样后面层析柱的使用寿命会无限延长,第1根层析由于更短支持更高的流速寿命会更长一些,短柱装填介质也更容易,介质寿命可能更短,但只影响第1根层析柱,第1根层析柱可以是传统柱高的1/3、1/5,或者更短,可以精准地抛弃堵塞的介质,或者装填更便宜的脱盐介质来拦截这些易堵的杂质。
通过选择不同的层析介质、非层析纯化介质或其他纯化载体,以及提供不同缓冲液环境达到混合层析或混合纯化的目的;示例1也属于混合层析,还可以把更多其他类型的层析技术添加到连续纯化的序列中来。
通过将设计好的多步纯化生产工艺进行连续化、系统化转换,并将工艺流程进行定时或参数化、条件化控制,达到自动化生产的目的。自动化的前提条件是排除人工参与的中间环节,连续纯化装置与方法正是去掉了多步纯化的中间环节;然后是设备的操作按扭转化为计算机指令,再对计算机指令进行流程编辑、条件化流程控制,最终完全摆脱人工的参与,实现自动化。
连续纯化对纯化方法设计的影响及优势:
提升回收率/生产自动化对于已确定的纯化工艺流程,在更换为连续纯化流程之后,可以消除上样和收样容器残留的损失;消除峰收集时对峰前后截取的损失;能避免反复稀释,提高收样的浓度;通过连续纯化系统设计,能实现纯化生产自动化,消除生产过程人的影响;
提高工作效率层析流程中,清洗、平衡、上样、洗脱过程可以交替进行,样品始终在层析柱中流转,不用等待层析柱清洗,不用等待上样,避免了类似的时间浪费;多步纯化的上样收样都需要人工干预,限制了自动化流程,连续纯化系统完善后,中间纯化不需要上样收样,完全可以像一次层析一样利用非工作时间自动化反复进行;
开创连续纯化的工艺设计方法,简化流程,实现混合层析、混合纯化,达到纯化技术多合一的效果,或者一步层析一拆多,实现层析介质分段寿命管理或连续循环的无限柱高的应用方向,突破纯化步骤的限制,提升药品生产质量,提高用药安全水平。
根据本申请的一个实施例,提供一种基于层析纯化的连续纯化装置,包括:
多个纯化通路,每个纯化通路包括泵、管道和层析柱,每个纯化通路能够单独地用于样品的纯化;和
柱位选择阀,柱位选择阀设置在多个纯化通路之间,用于能够选择地连通多个纯化通路中的至少两个,使得多个纯化通路中的至少两个层析柱并联或者串联。
层析柱中装填有分子排阻层析介质和/或阴离子交换层析介质。
多个纯化通路包括第一纯化通路、第二纯化通路和第三纯化通路;
第一纯化通路包括第一层析柱、第二纯化通路包括第二层析柱和第三纯化通路包括第三层析柱;
在第一层析柱和第三层析柱中装填有分子排阻层析介质,在第二层析柱中装填有阴离子交换层析介质;
在第一状态下,通过柱位选择阀选择地连通第一纯化通路和第三纯化通路,以使得第一层析柱与第三层析柱并联;
在第二状态下,通过柱位选择阀选择地连通第一纯化通路和第二纯化通路,以使得第一层析柱与第二层析柱串联在通路中。
第一层析柱的柱高小于或等于第二层析柱的柱高的三分之一到五分之一。
第一层析柱还装填脱盐介质。
还包括阀门,样品中的杂质通过阀门被选择性地抛弃。
泵用于泵送缓冲液,多个纯化通路中的缓冲液是相同或不同的溶液。
根据本申请的一个实施例,提供基于层析纯化的连续纯化装置进行连续纯化的方法,包括:
选择地连通多个纯化通路中的两个,使得多个纯化通路中的两个层析柱串联,以完成样品的转移;
选择地连通多个纯化通路中的两个,使得多个纯化通路中的两个层析柱并联,以分别完成样品的纯化。
通过流动相流路控制,将多个纯化通路中的一个纯化通路所收集的样品串联连接到多个纯化通路中的另一个纯化通路的进样阶段,如此循环,使得多个纯化通路串联连接以完成全部纯化,并且其中在多个纯化通路中的每一个纯化通路中的纯化相对独立,而且目标制品保持第1次纯化过程中的稀释状态和分离状态,以便于进一步分离纯化,并且不会进一步稀释。
流动相流路控制包括:
通过阀门切换将2个柱位选择阀的串联或逆向串联,通过2个上柱位选择阀切换不同的层析柱,以循环的方式让目标制品依次流经多个层析柱以实现连续纯化;同时,2个柱位选择阀解除串联状态,单独泵入流动相以完成纯化前的清洗准备及纯化后的清洗再生工作。
最后应说明的是:以上实施例仅用以说明本发明的技术方案,而非对其限制;尽管参照前述实施例对本发明进行了详细的说明,本领域的普通技术人员应当理解:其依然可以对前述各实施例所记载的技术方案进行修改,或者对其中部分技术特征进行等同替换;而这些修改或者替换,并不使相应技术方案的本质脱离本发明各实施例技术方案的精神和范围。
- 一种纤维素热解纯化挤出装置及基于该装置的纯化方法
- 蛋白A亲和层析法纯化抗体的方法以及抗体的纯化方法
- 一种脉冲激光重熔纯化金属铀表面的方法、其装置及其制备的纯化层
- 一种模拟移动床连续层析色谱系统及其应用以及纯化辅酶Q10的方法
- 一种模拟移动床连续层析色谱系统及其应用以及纯化辅酶Q10的方法
