一种通用型猪蓝耳病毒检测引物组合物、试剂盒及检测方法
文献发布时间:2023-06-19 19:30:30
技术领域
本发明属于病毒检测技术领域,具体涉及一种通用型猪蓝耳病毒检测引物、试剂盒及检测方法。
背景技术
猪蓝耳病俗称猪繁殖与呼吸综合征(Porcine reproductive andrespiratorysyndrome,PRRS),是猪的重要传染病,以妊娠母猪繁殖障碍和各年龄段猪呼吸道症状为主要特征。猪蓝耳病是由猪繁殖呼吸与综合征病毒引起的,该病严重影响其生殖功能,临床主要特征为流产、产死胎、木乃伊胎、弱胎、呼吸困难,在发病过程中会出现短暂性的两耳皮肤紫绀,故又称为蓝耳病。
目前对猪蓝耳病毒的检测所采用的方法主要还是传统常规的分离鉴定法、Elisa方法及普通PCR检测。传统常规的分离鉴定法,操作烦琐,耗时长,漏诊率高;ELISA方法相对简便,快速,但对于微量或杂质较多的样品,其特异性和灵敏度较低,可能造成漏诊或误诊。PCR作为一种新型的分子生物学技术,自诞生以来,由于它的特异性、敏感性高,能在短时间内得到大量的目的片段,使之成为当今发明研究的重要手段之一。
近些年,已有应用于检测高致病性猪蓝耳病毒的相关报道和专利。公开号为CN104711369A的专利“高致病性猪蓝耳病病毒的检测引物、探针及检测方法”采用了实时荧光定量PCR方法检测高致病性的猪蓝耳病病毒;公开号为CN110453015A的专利“猪蓝耳病病毒实时荧光定量PCR检测试剂盒及引物”提供了用于猪蓝耳病病毒检测的引物,能够同时有效检测经典猪蓝耳病病毒、高致病性猪蓝耳病病毒、新型变异高致病性猪蓝耳病病毒。
发明内容
本发明的目的在于提供一种通用型猪蓝耳病毒检测引物、试剂盒及检测方法,可以检测到1copies/uL的检出限,有较高的灵敏度,且检测的特异性高,稳定性好,适用于种猪场蓝耳病净化的检测监测工作。
本发明的技术方案如下:
本发明提供一种通用型猪蓝耳病毒检测引物,所述检测引物组合物如SEQID No:1和SEQ ID No:2所示。
本发明提供一种通用型猪蓝耳病毒检测探针,所述探针如SEQ ID NO.3所示。
进一步的,所述探针的核苷酸序列的5’端标记FAM荧光报告基团,3’端标记通用型BHQ1荧光淬灭基团。
本发明提供一种通用型猪蓝耳病毒检测试剂盒,包括PCR反应液,所述PCR反应液包括如SEQ ID No:1和SEQ ID No:2所示的引物组合物以及如SEQ IDNO.3所示的探针。
进一步的,所述上游引物和下游引物浓度为0.1-1μm,探针浓度为0.1-1μm。
进一步的,所述试剂盒还包括酶系、阳性对照和阴性对照;其中,阳性对照为猪蓝耳病毒质粒,阴性对照为超纯水。
本发明还一种通用型猪蓝耳病毒检测方法,采用如上所述的通用型猪蓝耳病毒检测试剂盒进行荧光定量qRT-PCR检测,其中,试剂盒包括如SEQ ID No:1和SEQ ID No:2所示的引物组合物和如SEQ ID NO.3所示的探针。
进一步的,所述通用型猪蓝耳病毒检测方法具体包括如下步骤:
S1、反应体系配制:取出PRRSV Mix、酶系、阳性对照和阴性对照,置于室温下完全融解,充分颠倒混匀后短暂离心,配制成PCR反应液;其中,PRRSV Mix包括上游引物、下游引物、荧光探针、buffer和过滤水;
S2、根据检测样品的数量向每个PCR反应管中加入PCR反应液,然后取阴性对照、待检样品RNA、阳性对照分别加入到不同的PCR反应管中,盖紧管盖,将PCR反应管瞬时离心;
S3、荧光PCR操作:将瞬时离心好的PCR管放入荧光PCR检测仪内,采用一步法使逆转录和扩增在同一管中进行反应,选择FAM荧光检测通道,收集FAM荧光信号;
S4、结果判定:通过荧光定量PCR仪自带软件读取相应的Ct值,报告基团FAM有扩增曲线出现的即是PCR反应液,若是无扩增曲线产生,则说明样品中不含PCR反应液,其中扩增曲线CT值小于35的判断为阳性,CT值大于35而小于40的判断为可疑,需重复实验,第二次CT值仍在这个范围的判断为阳性。
进一步的,所述步骤S1中按照PRRSV Mix和酶系以(14×n)μL+(1×n)μL=(15×n)μL的比例计算所需配制反应数,再充分混匀。
进一步的,所述步骤S3中荧光PCR操作的反应设置如下:第一阶段,50℃逆转录15min;第二阶段,95℃预变性2.5-3min;第三阶段,93-95℃变性10s,55-60℃延伸30s,共40-45个循环;荧光收集在第二阶段每次循环的55-60℃延伸时进行,选择FAM荧光检测通道,收集FAM荧光信号。
相较于现有技术,本发明的有益效果在于:
1、本发明提供的检测试剂盒及检测引物组合可以准确实现样本中猪蓝耳病毒的检测分析,其检出限为1copies/uL,与现有技术相比,灵敏度有显著的提高,且检测的特异性高,稳定性好,适用于种猪场蓝耳病净化的检测监测工作,显著提高养殖效益,解决在蓝耳病在非病毒血症期检出率低以及毒株多变、隐蔽的问题,具有广阔的应用前景。
2、采集猪蓝耳病毒的临床样品,临床样品包括猪血液、鼻咽拭子、扁桃体和肺组织。按照本发明的检测方法进行病毒检测,结果表明,所检测的临床样品均为猪蓝耳病毒阳性,符合率为100%。
附图说明
图1为本发明实施例4的标准质粒的标准曲线绘制步骤中得到的的扩增曲线图;
图2为本发明实施例4的标准质粒的标准曲线绘制步骤中得到的标准曲线图;
图3为本发明实施例4的特异性检测结果;
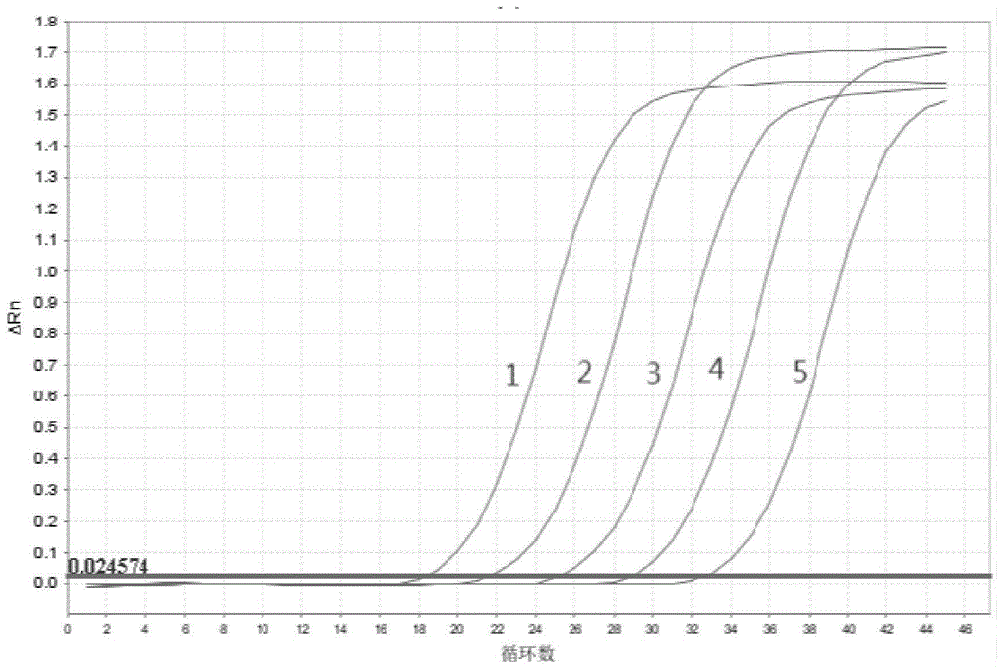
图4为本发明实施例4中的敏感性验证曲线;
图5本发明实施例4中临床样品检测试验的检测结果。
具体实施方式
为了使本发明要解决的技术问题、技术方案及有益效果更加清楚明白,以下结合实施例,对本发明做进一步的详细说明。应当理解,此处所描述的具体实施例仅仅用以解释本发明,并不用于限定本发明;
在本发明中所披露的范围的端点和任何值都不限于该精确的范围或值,这
些范围或值应当理解为包含接近这些范围或值的值;对于数值范围来说,各个范围的端点值之间、各个范围的端点值和单独的点值之间,以及单独的点值之间可以彼此组合而得到一个或多个新的数值范围,这些数值范围应被视为在本文中具体公开;
下述实施例中所用的材料、试剂等,如无特殊说明,均可从商业途径得到;
下述实施例中的实验方法,如无特殊说明,均为常规方法。
实施例1
根据猪蓝耳病毒(PRRSV)基因DNA Star软件序列比对结果,利用探针引物设计软件Primer Express5.0设计出一对检测引物组合物和一条探针,所述检测引物组合物如下所示:
上游引物PRRSV-F:TGTGCTTGYTAGGCCG,其为SEQ ID NO.1序列;
下游引物PRRSV-R:CGGACGACRAATGCGTG,其为SEQ ID NO.2序列;
所述荧光探针PRRSV-P:FAM-TCTGGCCCCTGCCCACCAC-BHQ1,其为SEQ ID NO.3序列,FAM为荧光报告基因,BHQ1为荧光淬灭基因。
实施例2
一种通用型猪蓝耳病毒检测试剂盒,用于猪血液、鼻咽拭子、扁桃体和肺组织等样品中猪蓝耳病毒(PRRSV)核酸的检测,包括PCR反应液,所述PCR反应液包括如SEQ ID No:1和SEQ ID No:2所示的上下游引物以及如SEQ ID NO.3所示的探针;
上游引物PRRSV-F:TGTGCTTGYTAGGCCG,其为SEQ ID NO.1序列;
下游引物PRRSV-R:CGGACGACRAATGCGTG,其为SEQ ID NO.2序列;
所述荧光探针PRRSV-P:FAM-TCTGGCCCCTGCCCACCAC-BHQ1;
其中,上下游引物、荧光探针、buffer和过滤水构成PRRSV Mix,所述上游引物和下游引物浓度为0.1-1μm,探针浓度为0.1-1μm;PRRSV Mix和酶系以(14×n)μL+(1×n)μL=(15×n)μL的比例计算所需配制反应数构成PCR反应液;所述试剂盒还包括阳性对照和阴性对照。
在本实施例中,检测试剂盒每管成分和含量如下所示:
实施例3
一种通用型猪蓝耳病毒检测方法,采用通用型猪蓝耳病毒检测试剂盒进行荧光定量qRT-PCR检测,具体包括如下步骤:
S1、反应体系配制:取出PRRSV Mix、酶系、阳性对照和阴性对照,置于室温下完全融解,充分颠倒混匀后短暂离心,配制成PCR反应液;按照PRRSV Mix和酶系以(14×n)μL+(1×n)μL=(15×n)μL的比例计算所需配制反应数,充分混匀,配制成PCR反应液;其中,PRRSVMix包括上游引物、下游引物、荧光探针、buffer和过滤水;
S2、根据检测样品的数量向每个PCR反应管中加入PCR反应液,然后取阴性对照、待检样品RNA、阳性对照分别加入到不同的PCR反应管中,盖紧管盖,将PCR反应管瞬时离心;
其中,当待检样品为猪血液、鼻咽拭子、扁桃体和肺组织等样品时,可直接采用全自动核酸提取试剂盒或RNA提取试剂盒提取RNA,提取好的样品在2~8℃条件下保存应不超过24h;在-20℃条件下保存应不超过半年,若长期保存,须放置-80℃冰箱;
S3、荧光PCR操作:将瞬时离心好的PCR管放入荧光PCR检测仪内,采用一步法使逆转录和扩增在同一管中进行反应,反应设置如下:第一阶段,50℃逆转录15min;第二阶段,95℃预变性2.5-3min;第三阶段,93-95℃变性10s,55-60℃延伸30s,共40-45个循环;荧光收集在第二阶段每次循环的55-60℃延伸时进行,选择FAM荧光检测通道,收集FAM荧光信号;
S4、结果判定:通过荧光定量PCR仪自带软件读取相应的Ct值,报告基团FAM有扩增曲线出现的即是PCR反应液,若是无扩增曲线产生,则说明样品中不含PCR反应液,其中扩增曲线CT值小于35的判断为阳性,CT值大于35而小于40的判断为可疑,需重复实验,第二次CT值仍在这个范围的判断为阳性。
实施例4性能测试
(1)荧光定量标准曲线的建立
测定纯化后RNA转录本的浓度,利用拷贝数计算公式:计算出其拷贝数,以10倍做梯度稀释,已知浓度的标准品质粒进行10倍浓度梯度稀释:10
(2)特异性验证实验
猪蓝耳病病毒阳性标准品、阴性样品作为对照,在同一份样本中加入含有临床症状与蓝耳病相似的经典猪瘟病毒、II-型猪圆环病毒和猪丹毒杆菌,均为阳性的猪源性样品,混匀器充分混匀后取200uL提取核酸,对其进行检测,结果如图3所示,结果显示只有猪蓝耳病病毒阳性标准品能扩增出靶序列的特征性曲线,其他均未扩增出靶序列曲线;说明本发明所建立的检测方法具有良好的特异性。
(3)敏感性验证实验
将标准品按照1.0×10
(4)临床样品验证实验
采集猪蓝耳病毒的临床样品,临床样品包括猪血液、鼻咽拭子、扁桃体和肺组织;提取RNA,按提供荧光定量的反应体系及程序进行荧光定量PCR;结果表明,所有的阳性都全部检出,未存在漏检的情况出现,所检测的临床样品均为猪蓝耳病毒阳性,符合率为100%。
提供上述实施例是为了更好地进一步理解本发明,并不局限于所述最佳实施方式,不对本发明的内容和保护范围构成限制,任何人在本发明的启示下或是将本发明与其他现有技术的特征进行组合而得出的任何与本发明相同或相近似的产品,均落在本发明的保护范围之内。
- 一种基于BTNAA体系检测犬瘟热病毒的引物对、引物和探针组合物、试剂及试剂盒
- 一种基于BTNAA体系检测犬细小病毒的引物对、引物和探针组合物、试剂及试剂盒
- 一种A型塞尼卡病毒检测引物、试剂盒、病毒检测方法和应用
- 用于检测猪圆环病毒3型的PCR引物对、试剂盒及检测方法
- 一种用于检测副猪嗜血杆菌的RPA引物、RPA探针、试剂盒及核酸检测方法
- 一种用于检测猪蓝耳病毒的探针引物组合物、试剂盒及其应用
- 一种用于猪蓝耳病毒核酸检测的引物组合、试剂盒及其应用
