使用深度学习的自动调节监测
文献发布时间:2024-04-18 19:58:21
本申请要求于2021年3月23日提交的名称为“使用深度学习的自动调节监测[AUTOREGULATION MONITORING USING DEEP LEARNING]”的美国专利申请号17/210,222的优先权,该美国专利申请的全部内容通过援引并入本文。
技术领域
本公开涉及监测患者的自动调节状态。
背景技术
临床医生可以监测患者的一个或多个生理参数,例如,以监测患者的自动调节状态。自动调节是一种反应机制,有机体借助该反应机制通过复杂的肌源性、神经源性和代谢机制在广泛的全身血压变化范围内调节血流。在自动调节期间,小动脉扩张或收缩以试图维持适当的血流。自动调节可以发生在各种器官和器官系统中,诸如大脑、肾脏、胃肠道等。在脑自动调节的示例中,当脑血压降低时,脑小动脉会扩张以试图维持血流。当脑压升高时,脑小动脉会收缩以减少可能导致大脑损伤的血流。
发明内容
本公开描述了使用机器学习确定患者的脑自动调节状态的示例装置、系统和技术。例如,一种系统可以被配置为接收指示患者在一定时间段内的血压的血压信号和指示所述患者在所述时间段内的区域脑氧饱和度的氧饱和度信号。所述系统可以将患者的血压和患者的区域脑氧饱和度以及与患者相关联的附加数据输入到脑自动调节模型中,以确定患者的脑自动调节模型。
脑自动调节模型可以包括神经网络算法,该神经网络算法已经经由使用来自患者群体的训练数据进行机器学习训练来训练。这种训练数据可以包括患者群体的血压数据和区域脑氧饱和度数据以及经标记的地面真值,以使神经网络算法能够学习患者的血压与区域脑氧饱和度之间的关系以及这种关系与脑自动调节状态之间的关联。
在一些示例中,用于训练神经算法的训练数据还可以包括从血压数据和区域脑氧饱和度数据得出的附加数据,诸如血压数据的梯度、区域脑氧饱和度数据的梯度以及指定血压数据与区域脑氧饱和度数据之间的相关性的脑血氧指数。进一步地,在一些示例中,训练数据还可以包括诸如用于指示患者是否正在接受心肺转流术手术的转流标志等附加数据。
与使用可能仅基于患者的血压数据的机械式算法相比,通过使用包括已经经由机器学习训练来训练的神经网络算法的脑自动调节模型来确定患者的脑自动调节状态,本公开的技术可以使脑自动调节监测装置能够更准确地确定患者的脑自动调节状态,并且减少假阳性和假阴性。因此,本公开中所公开的技术提供了技术优点。
在一个示例中,本公开描述了一种方法,所述方法包括:接收指示患者在一定时间段内的血压的血压信号和指示所述患者在所述时间段内的区域脑氧饱和度的氧饱和度信号;使用脑自动调节模型的神经网络算法,至少部分地基于所述患者在所述时间段内的血压和所述患者在所述时间段内的区域脑氧饱和度来确定所述患者的脑自动调节状态;以及向输出装置发送指示所述患者的脑自动调节状态的信号。
在另一示例中,本公开描述了一种系统,所述系统包括:血压感测装置;氧饱和度感测装置;以及处理电路系统,所述处理电路系统被配置为:从所述血压感测装置接收指示患者在一定时间段内的血压的血压信号,并且从所述氧饱和度感测装置接收指示所述患者在所述时间段内的区域脑氧饱和度的氧饱和度信号;使用脑自动调节模型的神经网络算法,至少部分地基于所述患者在所述时间段内的血压和所述患者在所述时间段内的区域脑氧饱和度来确定所述患者的脑自动调节状态;以及向输出装置发送指示患者的脑自动调节状态的信号。
在另一示例中,本公开描述了一种非暂态计算机可读可存储介质,所述介质包括指令,当所述指令当被处理电路系统执行时使所述处理电路系统:接收指示患者在一定时间段内的血压的血压信号和指示所述患者在所述时间段内的区域脑氧饱和度的氧饱和度信号;使用脑自动调节模型的神经网络算法,至少部分地基于所述患者在所述时间段内的血压和所述患者在所述时间段内的区域脑氧饱和度来确定所述患者的脑自动调节状态;以及向输出装置发送指示患者的脑自动调节状态的信号。
在另一示例中,本公开描述了一种设备,该设备包括:用于接收指示患者在一定时间段内的血压的血压信号和指示患者在所述时间段内的区域脑氧饱和度的氧饱和度信号的装置;用于使用脑自动调节模型的神经网络算法,至少部分地基于所述患者在所述时间段内的血压和所述患者在所述时间段内的区域脑氧饱和度来确定所述患者的脑自动调节状态的装置;以及用于向输出装置发送指示所述患者的脑自动调节状态的信号的装置。
在附图和下文的说明中阐述了一个或多个示例的细节。根据本说明书和附图以及权利要求书,其他特征、目的和优点将是清楚的。
附图说明
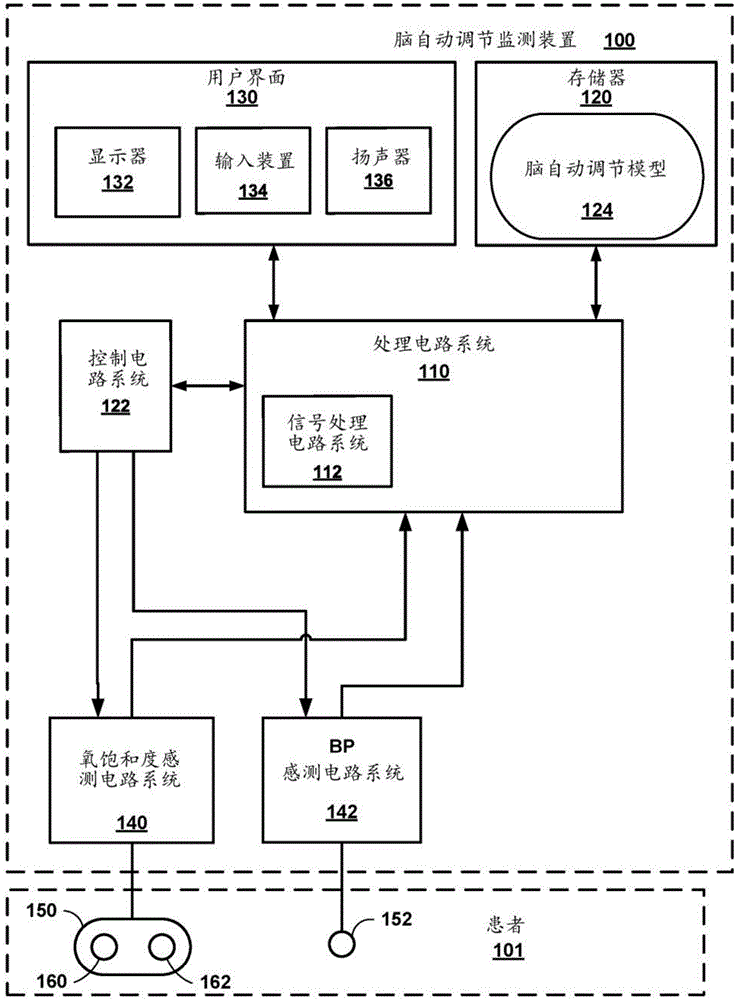
图1是展示了示例脑自动调节监测系统的概念框图。
图2展示了可以对图1所示的脑自动调节模型执行训练的示例训练系统的细节。
图3展示了图1和图2的示例脑自动调节模型的示例深度学习架构。
图4展示了图1和图2的示例脑自动调节模型的示例深度学习架构。
图5展示了使用图3和图4的深度学习架构进行脑自动调节状态分类的结果的示例图形。
图6展示了包括脑自动调节信息的示例用户界面。
图7是展示了用于监测患者的脑自动调节状态的示例方法的流程图。
图8是展示了用于监测患者的脑自动调节状态的示例方法的流程图。
具体实施方式
图1是展示了示例脑自动调节监测系统100的概念框图。如图1所示,脑自动调节监测系统100包括处理电路系统110、存储器120、控制电路系统122、用户界面130、感测电路系统140和142、以及感测装置150和152。在图1所示的示例中,用户界面130可以包括显示器132、输入装置134和/或扬声器136,该扬声器可以是被配置为生成和输出噪声的任何合适的音频装置并且可以包括任何合适的电路系统。在一些示例中,自动调节监测系统100可以被配置为确定和输出(例如,显示在显示器132上)患者101的自动调节状态,例如,在医疗手术期间或用于更长期的监测(诸如在重症监护室(ICU)中或用于胎儿监测)。临床医生可以经由用户界面130接收有关患者的脑自动调节状态信息的信息,并且基于脑自动调节状态信息调整对患者101的治疗或疗法。
当患者101表现出受损的自动调节状态时,患者101可能会经历不适当的血流,这可能是不希望的。如果血压梯度和氧饱和度梯度在一定时间段内呈现一致趋势(例如,朝同一方向变化),则患者101的自动调节系统可能是受损的。患者101的完好无损的自动调节状态发生在一定的血压范围内,该血压范围限定在自动调节下限(LLA)与自动调节上限(ULA)之间。例如,低于自动调节下限(LLA)时,流向相应器官的血流量的下降可能导致局部缺血并且对相应的器官产生不利影响。高于自动调节上限(ULA)时,流向相应器官的血流量的增加可能导致充血,这可能导致相应的器官肿胀或水肿。例如,在医疗手术期间,临床医生可以监测患者的自动调节状态,并且采取一个或多个措施使患者保持处于或使患者处于完好无损的自动调节状态,诸如通过升高或降低患者的血压。
本文所描述的处理电路系统110以及其他处理器、处理电路系统、控制器、控制电路系统等可以包括一个或多个处理器。处理电路系统110可以包括诸如一个或多个微处理器、数字信号处理器(DSP)、专用集成电路系统(ASIC)或现场可编程门阵列(FPGA)等集成电路系统、离散逻辑电路系统、模拟电路系统的任何组合。在一些示例中,处理电路系统110可以包括多个部件,诸如一个或多个微处理器、一个或多个DSP、一个或多个ASIC、或者一个或多个FPGA、以及其他离散或集成逻辑电路系统、和/或模拟电路系统的任何组合。
控制电路系统122可以操作性地耦合到处理电路系统110。控制电路系统122被配置为控制感测装置150和152的操作。在一些示例中,控制电路系统122可以被配置为提供定时控制信号,以协调感测装置150和152的操作。例如,感测电路系统140和142可以从控制电路系统122接收一个或多个定时控制信号,感测电路系统140和142可以使用这些定时控制信号来打开和关闭相应的感测装置150和152,诸如以使用感测装置150和152周期性地收集校准数据。在一些示例中,处理电路系统110可以使用定时控制信号来与感测电路系统140和142进行同步操作。例如,处理电路系统110可以基于定时控制信号使模数转换器和解复用器的操作与感测电路系统140和142同步。
存储器120可以被配置为存储例如患者101的监测生理参数值,诸如血压值、氧饱和度值、区域脑氧饱和度(rSO2)值、一个或多个脑自动调节状态值、一个或多个非脑自动调节状态值、生理参数、平均动脉压(MAP)值或其任何组合。存储器120还可以被配置为存储这些数据,诸如,包括经修改值和未修改值在内的自动调节状态值、阈值和速率、平滑函数、高斯滤波器、置信度量、预期自动调节函数、历史患者血压值数据和/或对自动调节极限的估计。阈值和速率、平滑函数、高斯滤波器、置信度量、预期自动调节函数和历史患者血压值数据可以在使用装置100的整个过程中和在多个患者之间保持不变,或者这些值可以随时间变化。
在一些示例中,存储器120可以存储程序指令,诸如神经网络算法。程序指令可以包括可由处理电路系统110执行的一个或多个程序模块。例如,存储器120可以存储脑自动调节模型124,该脑自动调节模型可以是经由机器学习来训练以确定患者101的脑自动调节状态的模型。当由处理电路系统110执行时,这些程序指令(诸如脑自动调节模型124的程序指令)可以使处理电路系统110提供本文中赋予它的功能。程序指令可以体现在软件、固件和/或RAMware中。存储器120可以包括易失性、非易失性、磁性、光学或电介质中的任何一种或多种,诸如随机存取存储器(RAM)、只读存储器(ROM)、非易失性RAM(NVRAM)、电可擦除可编程ROM(EEPROM)、闪存、或者任何其他数字介质。
用户界面130可以包括显示器132、输入装置134和扬声器136。在一些示例中,用户界面130可以包括更少或附加的部件。用户界面130被配置为向用户(例如,临床医生)呈现信息。例如,用户界面130和/或显示器132可以包括监视器、阴极射线管显示器、平板显示器(诸如液晶(LCD)显示器)、等离子显示器、发光二极管(LED)显示器、和/或任何其他合适的显示器。在一些示例中,用户界面130可以是带有内置显示器或独立显示器的以下各项的一部分:在临床或其他环境中使用的多参数监视器(MPM)或其他生理信号监视器、个人数字助理、移动电话、平板计算机、膝上型计算机、任何其他合适的计算装置或其任何组合。
在一些示例中,处理电路系统110可以被配置为通过用户界面130(诸如显示器132)向用户呈现图形用户界面。图形用户界面可以包括经由显示器132对患者的一个或多个生理参数值的指示,诸如血压值、氧饱和度值、关于自动调节状态的信息(例如,脑自动调节状态值和/或非脑自动调节状态值)、脉搏率信息、呼吸率信息、其他患者生理参数、或其组合。用户界面130还可以包括被配置为生成音频输出并向用户投射该音频输出的电路系统和其他部件,诸如扬声器136。
在一些示例中,处理电路系统110还可以从诸如用户等其他来源(未示出)接收输入信号。例如,处理电路系统110可以从输入装置134接收输入信号,该输入装置诸如键盘、鼠标、触摸屏、按钮、开关、麦克风、操纵杆、触摸板、或任何其他合适的输入装置或输入装置的组合。输入信号可以包含关于患者101的信息,诸如生理参数、提供给患者101的治疗等。处理电路系统110可以在其根据处理电路系统110执行的任何确定或操作中使用附加的输入信号。
在一些示例中,如果处理电路系统110确定患者101的脑自动调节状态为受损,则处理电路系统110可以呈现指示受损的通知。该通知可以包括指示患者101的脑自动调节状态的视觉、听觉、触觉或体觉通知(例如,警报信号)。在一些示例中,处理电路系统110和用户界面130可以是同一装置的一部分或被支撑在一个壳体(例如,计算机或监视器)内。在其他示例中,处理电路系统110和用户界面130可以是被配置为通过有线连接或无线连接(例如,通信接口)进行通信的单独装置。
氧饱和度感测电路系统140和血压感测电路系统(统称为感测电路系统140和142)可以被配置为接收由相应的感测装置150和152感测的生理信号并且将这些生理信号传送到处理电路系统110。感测装置150和152可以包括被配置为感测患者的生理参数的任何传感硬件,诸如但不限于一个或多个电极、光接收器、血压袖带等。所感测的生理信号可以包括指示患者101的生理参数(诸如但不限于血压、区域氧饱和度、血容量、心率和呼吸)的信号。例如,感测电路系统140和142可以包括但不限于:血压感测电路系统、氧饱和度感测电路系统、区域氧饱和度感测电路系统、区域脑氧饱和度感测电路系统、血容量感测电路系统、心率感测电路系统、温度感测电路系统、心电图(ECG)感测电路系统、脑电图(EEG)感测电路系统或其任何组合。
在一些示例中,感测电路系统140和142和/或处理电路系统110可以包括信号处理电路系统112,该信号处理电路系统被配置为对所感测的生理信号执行任何合适的模拟调节。例如,感测电路系统140和142可以将未改变的(例如,原始)信号传送到处理电路系统110。处理电路系统110(例如,信号处理电路系统112)可以被配置为通过例如滤波(例如,低通、高通、带通、陷波或任何其他合适的滤波)、放大、对接收到的信号执行运算(例如,取导数、求平均)、执行任何其他合适的信号调节(例如,将电流信号转换为电压信号)或其任何组合来将原始信号修改为可用信号。在一些示例中,经调节的模拟信号可以由信号处理电路系统112的模数转换器处理,以将经调节的模拟信号转换为数字信号。在一些示例中,信号处理电路系统112可以对信号的模拟或数字形式进行操作,以分离出信号的不同分量。在一些示例中,信号处理电路系统112可以对转换后的数字信号执行任何合适的数字调节,诸如低通、高通、带通、陷波、求平均或任何其他合适的滤波、放大、对信号执行运算、执行任何其他合适的数字调节或其任何组合。在一些示例中,信号处理电路系统112可以减少数字检测器信号中的样本数量。在一些示例中,信号处理电路系统112可以去除接收到的信号中的暗贡献或环境贡献。附加地或替代地,感测电路系统140和142可以包括信号处理电路系统112,以用于修改一个或多个原始信号并且将一个或多个经修改的信号传送到处理电路系统110。
在一些示例中,氧饱和度感测装置150是区域氧饱和度传感器,该区域氧饱和度传感器被配置为生成指示患者101的某一区域内的静脉、动脉和/或毛细血管系统内的血氧饱和度的氧饱和度信号。例如,氧饱和度感测装置150可以被配置为放置在患者101的皮肤上(诸如在患者101的额头上),以确定特定组织区域(例如,患者101的额叶皮层或另一脑位置)的区域氧饱和度。氧饱和度感测装置150可以包括发射器160和检测器162。发射器160可以包括至少两个发光二极管(LED),每个发光二极管被配置为发射不同波长的光,例如,红光或近红外光。如本文所使用的,术语“光”可以指由辐射源产生的能量,并且可以包括超声波、无线电、微波、毫米波、红外线、可见光、紫外线、伽马射线或X射线电磁辐射光谱中的一者或多者内的任何波长。在一些示例中,光驱动电路系统(例如,在感测装置150、感测电路系统140、控制电路系统122和/或处理电路系统110内)可以提供光驱动信号以驱动发射器160并且使发射器160发射光。在一些示例中,发射器160的LED发射约600纳米(nm)至约1000nm范围内的光。在特定的示例中,发射器160的一个LED被配置为发射约730nm的光,并且发射器160的另一个LED被配置为发射约810nm的光。在其他示例中可以使用其他波长的光。
检测器162可以包括与发射器160相对“靠近”(例如,在近侧)定位的第一检测元件和与发射器160相对“远离”(例如,在远侧)定位的第二检测元件。在一些示例中,第一检测元件和第二检测元件可以被选择为对光源160的所选择的目标能谱特别敏感。在“近”和“远”检测器162处都可以接收到多个波长的光强度。例如,如果使用两个波长,则可以在每个位置对比这两个波长,并且可以对比所得的信号,以得出与在“远”检测器处接收到的光透射通过患者的某一区域(例如,患者的颅骨)时所通过的另外的组织(除了“近”检测器接收到的光所通过的组织之外的组织,例如大脑组织)相关的氧饱和度值。
在操作中,光在穿过患者101的包括皮肤、骨骼、其他浅层组织(例如,非脑组织和浅层脑组织)和/或深层组织(例如,深层脑组织)在内的组织后可以进入检测器162。检测器162可以将接收到的光的强度转换为电信号。光强度可以与组织中的光吸收率和/或反射率直接相关。可以减去来自皮肤和头骨的表面数据,以生成目标组织随时间变化的氧饱和度信号。上述这种技术可以称为近红外光谱(NIRS),并且氧饱和度信号可以称为NIRS信号。
氧饱和度感测装置150可以将氧饱和度信号(例如,区域氧饱和度信号)提供给处理电路系统110或任何其他合适的处理装置,以使其能够评估患者101的自动调节状态。基于光信号确定氧饱和度的其他示例细节可以在于2018年1月9日发布的名称为“用于确定区域血氧饱和度的方法和系统[Methods and Systems for Determining Regional BloodOxygen Saturation]”的共同受让的美国专利号9,861,317中找到。
在操作中,血压感测装置152和氧饱和度感测装置150可以各自放置在患者101的身体的相同或不同部分。例如,血压感测装置152和氧饱和度感测装置150可以在物理上彼此分开,并且可以分开放置在患者101上。作为另一示例,血压感测装置152和氧饱和度感测装置150在某些情况下可以是同一传感器的一部分或由单个传感器壳体支撑。例如,血压感测装置152和氧饱和度感测装置150可以是集成血氧系统的一部分,该集成血氧系统被配置为无创地测量血压(例如,基于体积描记法(PPG)信号中的时间延迟)和区域氧饱和度。血压感测装置152或氧饱和度感测装置150中的一者或两者可以进一步被配置为测量其他参数,诸如血红蛋白、呼吸率、呼吸努力、心率、饱和模式检测、对刺激的反应(诸如脑电双频指数(BIS)或肌电图(EMG)对电刺激的反应)等。虽然图1中展示了示例脑自动调节监测系统100,但图1中展示的部件并不旨在限制。在其他示例中可以使用附加或替代的部件和/或实施方式。
血压感测装置152可以是被配置为生成指示患者101的采集部位处的血压的血压信号的任何传感器或装置。例如,血压感测装置152可以包括被配置为无创地监测血压的血压袖带、被配置为无创地生成PPG信号的传感器、或用于有创地监测患者101的动脉中的血压的动脉导管。在一些示例中,血压信号可以包括采集血压的波形的至少一部分。在一些示例中,采集部位可以包括患者101的股动脉、患者101的桡动脉、患者101的足背动脉、患者101的肱动脉或其组合中的至少一者。在一些示例中,血压感测装置152可以包括多个血压感测装置。例如,多个血压感测装置中的每个血压感测装置可以被配置为获得患者101的多个采集部位中的相应采集部位处的相应血压。多个采集部位可以包括患者101的相似或不同的动脉。
在一些示例中,血压感测装置152可以包括一个或多个脉搏血氧传感器。通过处理从单个脉搏血氧传感器获得的单个PPG信号内的两个或更多个特征点之间的时间延迟,可以得出采集血压。基于从单个脉搏血氧传感器获得的单个PPG信号的某些分量之间的时间延迟的比较来得出血压的其他示例细节在于2008年9月30日提交的名称为“用于无创血压监测的系统和方法[Systems and Methods for Non-Invasive Blood PressureMonitoring]”的共同受让的美国专利申请公开号2009/0326386中进行了描述。在其他情况下,患者101的血压可以经由放置在患者101身上多个位置处的多个脉搏血氧传感器来连续无创地监测。如于2003年7月29日发布的名称为“连续无创血压监测方法和设备[Continuous Non-invasive Blood Pressure Monitoring Method and Apparatus]”的共同受让的美国专利号6,599,251中所描述的,可以从多个脉搏血氧传感器获得多个PPG信号,并且可以将PPG信号相互比较以估计患者101的血压。
无论血压感测装置152的形式如何,其都可以被配置为生成指示患者101随时间变化的血压(例如,动脉血压)的血压信号。在血压感测装置152包括多个血压感测装置的示例中,血压信号可以包括多个血压信号,每个血压信号指示患者101的相应采集部位处的血压。血压感测装置152可以将血压信号提供给感测电路系统142、处理电路系统110、或任何其他合适的处理装置,以使其能够评估患者101的自动调节状态。
根据本公开的各个方面,处理电路系统110可以被配置为接收由感测电路系统142和感测装置152生成的指示患者101在一定时间段内的血压的血压信号,以及由感测电路系统140和感测装置150生成的指示患者101在该时间段内的区域氧饱和度的氧饱和度信号。处理电路系统110所处的时间段可以是先前的30秒、60秒、90秒、120秒或任何其他合适的时间段。
指示患者101在一定时间段内的血压的血压信号可以指示患者101的平均动脉压(MAP),即患者101在单个心动周期期间的平均(即均值)血压。因此,在一些示例中,血压信号可以指示患者101在该时间段期间的每个心动周期的MAP。
由氧饱和度信号指示的患者101的区域氧饱和度(rSO2)可以是患者101的大脑的区域氧饱和度。在一些示例中,氧饱和度感测装置150可以包括放置在患者101的不同部分上的多个传感器,诸如放置在患者101头部右侧或右侧附近的传感器,以及放置在患者101头部左侧或左侧附近的传感器。在该示例中,指示患者101的区域氧饱和度的氧饱和度信号可以包括(来自放置在患者101头部右侧的氧饱和度传感器的)指示患者101的第一区域脑氧饱和度的第一氧饱和度信号,以及(来自放置在患者101头部左侧的氧饱和度传感器的)指示患者101的第二区域脑氧饱和度的第二氧饱和度信号。
处理电路系统110可以被配置为至少部分地基于接收到的指示患者101在该时间段内的血压和/或患者101的区域氧饱和度的信号,确定与患者101在该时间段期间的血压和/或患者101在该时间段期间的区域氧饱和度相关联的生理数据。例如,处理电路系统110可以至少部分地基于在该时间段期间患者101的血压与患者101的区域氧饱和度之间的线性相关性来确定患者101在该时间段期间的脑血氧指数(COx)。例如,处理电路系统110可以根据血液中的脑氧饱和度(rSO
在一些示例中,处理电路系统110可以确定患者101在该时间段(也称为窗口)期间的MAP的梯度,该梯度可以是患者101的MAP在该时间段内的变化。处理电路系统110还可以确定患者101在该时间段期间的区域脑氧饱和度的梯度,该梯度可以是患者101在该时间段内的区域脑氧饱和度的变化。
处理电路系统110可以被配置为使用脑自动调节模型124,至少部分地基于患者101在该时间段期间的血压和患者101在该时间段期间的区域氧饱和度来确定患者101的脑自动调节状态。如在整个本公开中进一步详细描述的,脑自动调节模型124可以包括经由机器学习来训练以确定患者101的脑自动调节状态的神经网络算法。处理电路系统110可以执行脑自动调节模型124,并且可以使用患者101在该时间段期间的MAP和患者101在该时间段期间的区域氧饱和度作为脑自动调节模型124的输入,以从脑自动调节模型124生成指示患者101的脑自动调节状态的输出。
在一些示例中,处理电路系统110还可以将与患者101在该时间段期间的血压和/或患者101在该时间段期间的区域氧饱和度相关联的附加信息输入到脑自动调节模型124中,以基于该附加信息确定患者101的脑自动调节状态。例如,处理电路系统110可以输入以下各项中的一项或多项:患者101在该时间段期间的血压(例如,MAP)的梯度、患者101在该时间段期间的区域脑氧饱和度的梯度、患者101在该时间段期间的COx、或指示患者101在该时间段期间正在接受心肺转流术手术的转流标志。
在一些示例中,如果处理电路系统110接收到NIRS信号形式的氧饱和度信号,则处理电路系统110可以将指示患者101的区域脑氧饱和度的原始NIRS信号输入到脑自动调节模型124中。在一些示例中,如果处理电路系统110接收到包括(来自放置在患者101头部右侧的氧饱和度传感器的)指示患者101的第一区域脑氧饱和度的第一氧饱和度信号以及(来自放置在头部左侧的氧饱和度传感器的)指示患者101的第二区域脑氧饱和度的第二氧饱和度信号的氧饱和度信号,则处理电路系统110可以将第一区域脑氧饱和度信号和第二区域脑氧饱和度信号两者都输入到脑自动调节模型124中。例如,处理电路系统110可以将两个单独的值输入到脑自动调节模型124中,或者可以将这两个值的平均值输入到脑自动调节模型124中。在一些示例中,处理电路系统110还可以将患者101的血氧饱和度(SpO2)输入到脑自动调节模型124中。
在一些示例中,处理电路系统110还可以将关于患者101的附加信息输入到脑自动调节模型124中,并基于该附加信息确定患者101的脑自动调节状态。例如,这种附加信息可以包括与患者101在该时间段期间的血压相关联的形态特征和/或与患者101在该时间段期间的区域氧饱和度相关联的形态特征。附加信息还可以包括患者101在该时间段期间除MAP以外的血压,诸如患者101在该时间段期间的收缩压或舒张压。附加信息还可以包括关于患者101的患者人口统计数据,诸如患者的年龄、患者的年龄、关于患者101的饮食和生活方式的信息(例如,患者101是否是吸烟者)等。基于附加信息所指示的变量,患者的脑自动调节状态可能有所不同。
处理电路系统110可以被配置为执行脑自动调节模型124,以基于输入到脑自动调节模型124的信息来输出患者101的脑自动调节状态的指示。例如,脑自动调节模型124可以输出指示患者101的脑自动调节状态是否为以下状态之一的值:完好无损、受损或未知。完好无损的脑自动调节状态可以指示患者101的脑自动调节控制机制正常工作,而受损的脑自动调节状态可以指示患者101的脑自动调节控制机制不正常工作。完好无损的脑自动调节功能发生在限定在LLA与ULA之间的血压范围内。使用脑自动调节模型124确定脑自动调节状态可以使处理电路系统110能够例如在确定特定于患者101的LLA和ULA之前或在无需对其进行确定的情况下,就快速确定患者101的脑自动调节功能。
在一些示例中,脑自动调节模型124是经由机器学习来训练的神经网络算法,其用于将包括指示患者101的血压的血压信号和指示患者101的区域氧饱和度的氧饱和度信号在内的多个信号作为输入来确定患者101的脑自动调节状态。
神经网络算法或人工神经网络可以包括利用定义规则的节点的可训练或自适应算法。例如,多个节点中的相应节点可以利用诸如非线性函数或if-then规则等函数来基于输入生成输出。多个节点中的相应节点可以沿着一条边连接到多个节点中的一个或多个不同节点,使得该相应节点的输出包括不同节点的输入。这些函数可以包括:可以使用输入和期望输出的训练集来确定或调整的参数,诸如多个信号或值(诸如来自患者101或患者群体的血压信号或(多个)血压值和与血压信号同时被测量的患者101或患者群体的氧饱和度信号或(多个)氧饱和度值)之间的预定关联;以及诸如反向传播学习规则等学习规则。反向传播学习规则可以利用将期望的输出与由神经网络算法产生的输出进行比较的一个或多个误差测量,通过改变参数来训练神经网络算法以最小化一个或多个误差测量。
示例神经网络包括多个节点,这些节点中的至少一些具有节点参数。可以向神经网络算法的第一节点提供(输入)这样的输入:该输入至少包括由氧饱和度感测装置150或氧饱和度感测电路系统140生成并指示患者101在一定时间段内的区域脑氧饱和度的氧饱和度信号,以及由血压感测装置152或血压感测电路系统142生成并指示患者101在该时间段内的血压的血压信号。在一些示例中,输入可以包括多个输入,每个输入被输入到相应的节点。第一节点可以包括被配置为基于输入和一个或多个可调的节点参数来确定输出的函数。在一些示例中,神经网络可以包括传播函数,该传播函数被配置为基于前一个节点的输出和偏置值来确定后一个节点的输入。在一些示例中,可以将学习规则配置为修改一个或多个节点参数以产生有利输出。例如,有利输出可以受到一个或多个阈值的约束和/或用于最小化一个或多个误差测量。有利输出可以包括单个节点、一组节点或多个节点的输出。
神经网络算法可以迭代修改节点参数直到输出包括有利输出为止。通过这种方式,处理电路系统110可以被配置为迭代地评估神经网络算法的输出,并基于对神经网络算法的输出的评估迭代地修改至少一个节点参数,以基于经修改的神经网络算法确定患者(诸如患者101)的脑自动调节状态。
在一些示例中,使用脑自动调节模型124,处理电路系统110可以通过确定与患者101的脑自动调节状态为完好无损的置信度相关联的第一值和与患者101的脑自动调节状态为受损的置信度相关联的第二值来确定患者101的脑自动调节状态。因此,处理电路系统110可以执行脑自动调节模型124,以至少部分地基于与患者101的脑自动调节状态为完好无损的置信度相关联的第一值和与患者101的脑自动调节状态为受损的置信度相关联的第二值来确定患者101的脑自动调节状态。
例如,使用脑自动调节模型124,处理电路系统110可以为第一值和第二值中的每一个确定介于0与1之间的数值。如果脑自动调节模型124指示第一值大于第二值,则脑自动调节模型124可以输出指示患者101的脑自动调节状态为完好无损的值。相反地,如果脑自动调节模型124确定第二值大于第一值,则脑自动调节模型124可以输出指示患者101的脑自动调节状态为受损的值。例如,如果脑自动调节模型124确定与患者101的脑自动调节状态为完好无损的置信度相关联的值为0.8,并且与患者101的脑自动调节状态为受损的置信度相关联的值,则脑自动调节模型124可以输出指示患者101的脑自动调节状态为完好无损的值。
在一些示例中,如果脑自动调节模型124在将患者101的脑自动调节状态分类为完好无损或受损方面没有足够的置信度,则脑自动调节模型124可以输出指示患者101的脑自动调节状态为未知的值。在一些示例中,如果与患者101的脑自动调节状态为完好无损的置信度相关联的值和与患者101的脑自动调节状态为受损的置信度相关联的值之间的差值小于或等于阈值,则脑自动调节模型124可以输出指示患者101的脑自动调节状态为未知的值。例如,如果与患者101的脑自动调节状态为完好无损的置信度相关联的值为0.6,与患者101的脑自动调节状态为受损的置信度相关联的值为0.4,并且阈值为0.2,则脑自动调节模型124可以输出指示患者101的脑自动调节状态为未知的值。
在一些示例中,脑自动调节模型124可以对由脑自动调节模型124确定的值执行后处理,以确定患者101的脑自动调节状态。例如,脑自动调节模型124可以将与患者101的脑自动调节状态为完好无损的置信度相关联的值和先前确定的与在患者101的当前血压相同的血压下患者101的脑自动调节状态为完好无损的置信度相关联的值进行平均。类似地,脑自动调节模型124可以将与患者101的脑自动调节状态为受损的置信度相关联的值和先前确定的与在患者101的当前血压相同的血压下患者101的脑自动调节状态为受损的置信度相关联的值进行平均。也就是说,当脑自动调节模型124确定与患者101的脑自动调节状态为完好无损的置信度相关联的值和与患者101的脑自动调节状态为受损的置信度相关联的值时,这些值可能与确定这些值时患者101的血压相关联,并且处理电路系统110可以将患者101的血压与置信度值的关联存储在存储器120中。
在一些示例中,当脑自动调节模型124确定与患者101的脑自动调节状态为完好无损的置信度相关联的值以及与在患者101的给定血压下患者101的脑自动调节状态为受损的置信度相关联的值时,脑自动调节模型124可以查找存储在存储器120中的与相同血压相关联的置信度值。脑自动调节模型124可以将与患者101的脑自动调节状态为完好无损的置信度相关联的值和先前确定的与在患者101的当前血压相同的血压下患者101的脑自动调节状态为完好无损的置信度相关联的值进行平均,并且可以将与患者101的脑自动调节状态为受损的置信度相关联的值和先前确定的与在患者101的当前血压相同的血压下患者101的脑自动调节状态为受损的置信度相关联的值进行平均。
因此,脑自动调节模型124可以将与患者101的脑自动调节状态为完好无损的置信度相关联的平均值和与患者101的脑自动调节状态为受损的置信度相关联的平均值进行比较,以确定患者101的脑自动调节状态。如果脑自动调节模型124确定与患者101的脑自动调节状态为完好无损的置信度相关联的平均值大于或等于与患者101的脑自动调节状态为受损的置信度相关联的平均值,并且如果这两个值之间的差值大于阈值,则脑自动调节模型124可以确定患者101的脑自动调节状态为完好无损。如果脑自动调节模型124确定与患者101脑自动调节状态为受损的置信度相关联的平均值大于或等于与患者101的脑自动调节状态为完好无损的置信度相关联的平均值,并且如果这两个值之间的差值大于阈值,则脑自动调节模型124可以确定患者101的脑自动调节状态为受损。如果这两个平均值之间的差值小于或等于阈值,则脑自动调节模型124可以确定患者101的脑自动调节状态为未知。
一旦处理电路系统110已经确定了患者101的脑自动调节状态,处理电路系统110就可以生成指示患者101的脑自动调节状态的信息并将该信息输出到输出装置,例如用户界面130。处理电路系统110将该信息递送到用户界面130。在一些示例中,该信息可以使用户界面130(例如,显示器132、扬声器136和/或单独的(多个)显示器(未示出))能够呈现图形用户界面,该图形用户界面包括指示患者101的脑自动调节状态的信息(诸如脑自动调节状态值)和/或大脑的受损自动调节状态的指示。在一些示例中,自动调节状态的指示可以包括呈现给用户的文本、颜色和/或音频。处理电路系统110可以进一步被配置为在图形用户界面上呈现一个或多个脑自动调节状态值、一个或多个自动调节极限(例如,LLA和/或ULA)、(多个)血压、(多个)氧饱和度等的指示。除了图形用户界面之外或作为其替代方案,处理器电路系统110可以被配置为经由扬声器136生成和呈现指示所确定的患者101的脑自动调节状态的信息。例如,响应于检测到患者101受损的脑自动调节状态,处理电路系统110可以经由扬声器136生成声音警报。
在一些示例中,脑自动调节监测系统100(例如,处理电路系统110或用户界面130)可以包括通信接口以使脑自动调节监测系统100能够与外部装置交换信息。通信接口可以包括任何合适的硬件、软件或者两者,其可以允许脑自动调节监测系统100与电子电路系统、装置、网络、服务器或其他工作站、显示器或其任何组合进行通信。例如,处理电路系统110可以经由通信接口从外部装置接收血压值、氧饱和度值或预定数据(诸如预定的脑自动调节状态值、预定的非脑自动调节状态值、或预定的调整值)。
仅出于说明目的对脑自动调节监测系统100的部件进行说明和描述,这些部件被展示和描述为单独部件。在一些示例中,一些部件的功能可以组合在单个部件中。例如,处理电路系统110和控制电路系统122的功能可以组合在单个处理器系统中。另外,在一些示例中,本文展示和描述的脑自动调节监测系统100的一些部件的功能可以划分到多个部件。例如,控制电路系统122的一些或全部功能可以在处理电路系统110或感测电路系统140和142中执行。在其他示例中,一个或多个部件的功能可以以不同的顺序执行,或者可以不是必需的。
图2展示了可以对图1所示的脑自动调节模型124执行训练的示例训练系统200的细节。图2仅展示了训练系统200的一个特定示例,并且具有更多、更少或不同部件的许多其他示例装置也可以被配置为根据本公开的技术来执行操作。
虽然训练系统200的部件在图2的示例中显示为单个装置的一部分,但在一些示例中,这些部件可以位于不同装置内部和/或成为不同装置的一部分。例如,在一些示例中,训练系统200可以表示“云”计算系统。因此,在这些示例中,图2中所展示的模块可以跨越多个计算装置。在一些示例中,训练系统200可以表示组成“云”计算系统的服务器集群的多个服务器之一。在其他示例中,训练系统200可以是图1所示的脑自动调节装置100的示例。
如图2的示例所示,训练系统200包括一个或多个处理器202、一个或多个通信单元204以及一个或多个存储装置208。存储装置208进一步包括脑自动调节模型124、训练模块212和训练数据214。部件202、204和208中的每一个都可以互连(物理上、通信地和/或操作性地)以进行部件间的通信。在图2的示例中,部件202、204和208可以通过一个或多个通信信道206耦合。在一些示例中,通信信道206可以包括系统总线、网络连接、进程间通信数据结构、或任何其他用于传送数据的信道。脑自动调节模型124、训练模块212和训练数据214还可以相互传送信息以及与训练系统200中的其他部件传送信息。
在图2的示例中,一个或多个处理器202(各自包括处理电路系统)可以在训练系统200内实施功能和/或执行指令。例如,一个或多个处理器202可以接收并执行由存储装置208存储的指令,这些指令执行训练模块212的功能。在执行期间,由一个或多个处理器202执行的这些指令可以使训练系统200将信息存储在存储装置208内。一个或多个处理器202可以执行训练模块212的指令,以使用训练数据214来训练脑自动调节模型124。也就是说,训练模块212可以由一个或多个处理器202操作以执行本文描述的训练系统200的各种动作或功能。
在图2的示例中,一个或多个通信单元204可以操作用于经由一个或多个网络通过在该一个或多个网络上发送和/或接收网络信号的方式与外部装置(例如,图1的装置100)通信。例如,训练系统200可以使用通信单元204在诸如蜂窝无线电网络等无线电网络上发送和/或接收无线电信号。同样,通信单元204可以在诸如全球定位系统(GPS)网络等卫星网络上发送和/或接收卫星信号。通信单元204的示例包括网络接口卡(诸如以太网卡)、光收发器、射频收发器、或者可以发送和/或接收信息的任何其他类型的装置。通信单元204的其他示例可以包括近场通信(NFC)单元、
在图2的示例中,一个或多个存储装置208可以操作用于存储用于在训练系统200的操作期间进行处理的信息。在一些示例中,存储装置208可以表示临时存储器,这意味着存储装置208的主要目的不是长期存储。例如,训练系统200的存储装置208可以是易失性存储器,其被配置用于短期存储信息,并且因此在断电的情况下不会保留存储的内容。易失性存储器的示例包括随机存取存储器(RAM)、动态随机存取存储器(DRAM)、静态随机存取存储器(SRAM)以及本领域已知的其他形式的易失性存储器。
在一些示例中,存储装置208还表示一个或多个计算机可读存储介质。也就是说,存储装置208可以被配置为比临时存储器存储更大量的信息。例如,存储装置46可以包括通过电源通/断周期保留信息的非易失性存储器。非易失性存储器的示例包括磁性硬盘、光盘、软盘、闪存或各种形式的电可编程存储器(EPROM)或电可擦除可编程(EEPROM)存储器。在任何情况下,在图2的示例中,存储装置208可以存储与脑自动调节模型124、训练模块212和训练数据214相关联的程序指令和/或数据。
在图2的示例中,训练系统200可以执行训练模块212,以使用训练数据214来训练脑自动调节模型124,以便通过训练脑自动调节模型124将一个或多个特征与患者的脑自动调节状态相关联来更准确和/或更快地确定患者的脑自动调节状态。脑自动调节模型124可以包括诸如递归神经网络、卷积神经网络等深度学习架构,该深度学习架构包括多个层,以从脑自动调节模型124的输入逐步提取更高级别的特征。
在一些示例中,训练模块212训练脑自动调节模型124来使用患者的血压(诸如患者的MAP)和患者的区域脑氧饱和度作为输入,并基于患者的MAP和区域脑氧饱和度确定患者的脑自动调节状态(诸如,脑自动调节状态是完好无损、受损还是未知)。具体地,训练模块212训练脑自动调节模型124来使用诸如患者在一定时间段期间的MAP和区域脑氧饱和度等输入,基于该时间段期间的输入确定患者在紧接该时间段之后的脑自动调节状态。因此,如果时间段为30秒,则训练模块212可以训练脑自动调节模型124来基于诸如在30秒的时间段内患者的MAP和患者的区域脑氧饱和度等输入确定患者在紧接这30秒的时间段之后的脑自动调节状态。
例如,训练模块212可以通过提供诸如在数小时、数天等时间内的MAP和区域脑氧饱和度等数据来训练脑自动调节模型124,并且可以通过提供用于标记数据中的时间点以指示脑自动调节状态为完好无损或受损的真值标签来训练脑自动调节模型124。例如,如果训练模块212是训练脑自动调节模型124来基于30秒的时间段期间的输入确定患者在紧接该时间段之后的脑自动调节状态,则训练模块212可以标记30秒处的数据以指示与从时间0秒到30秒的数据(例如,MAP和区域脑氧饱和度)相关联的脑自动调节状态,标记31秒处的数据以指示与从时间1秒到31秒的数据相关联的脑自动调节状态,标记32秒处的数据以指示与从时间2秒到32秒的数据相关联的脑自动调节状态等。
在一些示例中,训练模块212可以通过从患者的MAP中减去MAP的均值并通过从患者的区域氧饱和度中减去平均区域脑氧饱和度来训练脑自动调节模型124。例如,对于0秒到30秒的时间段,训练模块212可以从自0秒到30秒的时间段期间的MAP中减去整个训练数据的MAP的均值,并且可以从自0秒到30秒的时间段期间的区域氧饱和度中减去整个训练数据的区域脑氧饱和度的均值,并且可以使用所得的值作为输入来训练脑自动调节模型124。
从患者的MAP中减去MAP的均值并通过从患者的区域氧饱和度中减去平均区域脑氧饱和度可以有助于防止脑自动调节模型124中的经训练神经网络基于MAP的绝对值过度拟合,诸如防止脑自动调节模型124被训练为学习到小于50的MAP通常是与受损的脑自动调节状态相关联。替代地,训练模块212可以训练脑自动调节模型124来基于该时间段期间MAP中的趋势与区域脑氧饱和度中的趋势之间的关系来确定患者的脑自动调节状态。
除了MAP和区域脑氧饱和度之外,训练模块212还训练脑自动调节模型124来使用每个时间段内的数据作为输入,该数据诸如但不限于以下一项或多项:在该时间段期间MAP的梯度(例如,作为时间序列)、在该时间段期间区域脑氧饱和度的梯度(例如,作为时间序列)、在该时间段期间的脑血氧指数、指示患者在该时间段期间是否正在接受可能影响血压值的医疗手术(例如,心肺转流术手术)的标志、指示在该时间段期间的区域脑氧饱和度的原始NIRS信号、来自放置在患者的头部左侧和右侧的氧饱和度传感器的氧饱和度信号(作为两个单独的信号或作为组合(例如,平均)信号)、与在该时间段期间的血压相关联的形态特征和/或与在该时间段期间的区域氧饱和度相关联的形态特征、在该时间段期间的血液动力学相关的信号(诸如,收缩压或舒张压)、与患者相关联的人口统计数据等。
在一些示例中,训练模块212训练脑自动调节模型124也使用患者的血氧饱和度(SpO2)作为输入。使用患者的血氧饱和度来训练自动调节模型124可以允许脑自动调节模型124应对由于与脑血流无关的血氧饱和度变化而引起的区域脑氧饱和度的变化。例如,训练模块212可以训练脑自动调节模型124来学习到由于与脑血流无关的血氧饱和度变化而导致的区域脑氧饱和度的变化不一定是患者的自动调节状态发生变化的迹象。
在一些示例中,用于训练脑自动调节模型124的训练数据214仅包括来自患者101的数据,而不包括来自其他受试者的数据。在其他示例中,训练数据214可以包括来自患者群体的数据,该患者群体可以包括也可以不包括患者101。在一些示例中,一旦训练模块212使用训练数据214训练了脑自动调节模型124,训练模块212就可以通过使用一组尚未遇到的测试数据来测试脑自动调节模型124,其方式为使用脑自动调节模型124来确定由该脑自动调节模型124基于测试数据对脑自动调节状态的分类与测试数据的预期脑自动调节状态的分类的匹配程度。通过这种方式,训练模块212可以评估并进一步改进脑自动调节模型124。
当训练模块212完成了对脑自动调节模型124的训练时,脑自动调节模型124可以被安装、上传或以其他方式转移到自动调节监测系统100。在一些示例中,训练模块212可以将脑自动调节模型124的副本上传或以其他方式转移到另一服务器或云,并且自动调节监测系统100可以经由诸如因特网、虚拟专用网络、局域网等网络脑自动调节模型124。
在一些示例中,训练模块212可以能够训练脑自动调节模型124来确定除大脑以外的器官的自动调节状态,诸如肾脏、胃肠道等的自动调节状态。特别地,除了区域脑氧饱和度数据之外,训练模块212还可以使用来自这些其他器官的附加信号作为训练数据214来训练脑自动调节模型124以确定除大脑以外的器官的自动调节状态。可以从中更直接地确定非脑器官的自动调节状态的生理参数可能相对难以测量。因此,基于脑自动调节状态值确定非脑器官的自动调节状态会是有用的,例如,如于2021年3月2日发布的发明人为Addison等人且名称为“非脑器官自动调节状态确定[NON-CEREBRAL ORGAN AUTOREGULATIONSTATUSDETERMINATION]”的美国专利号10,932,673中所描述的。该美国专利号10,932,673通过援引以其全文并入本文。
图3展示了图1和图2的示例脑自动调节模型124的示例深度学习架构300。虽然深度学习架构300在图3中被展示为用于训练长短期记忆(LSTM)模型的LSTM深度学习架构,但任何其他深度学习架构可以同样适合于训练脑自动调节模型124。
如图3所示,深度学习架构300可以包括序列输入层302、双向长短期记忆(BiLSTM)层304、丢弃层306、BiLSTM层308、丢弃层310、BiLSTM层312、全连接层314、softmax层316和分类层318。序列输入层302可以连接到BiLSTM层304。BiLSTM层304可以具有16个隐藏单元并且可以连接到丢弃层306。丢弃层306可以具有0.01的丢弃比,并且可以连接到BiLSTM层308。BiLSTM层308可以具有8个隐藏单元并且可以连接到丢弃层310。丢弃层310可以具有0.01的丢弃比并且可以连接到BiLSTM层312,BiLSTM层312可以具有4个隐藏单元并且可以连接到全连接层314。全连接层314可以连接到softmax层316。Softmax层316可以连接到分类层318。
序列输入层(诸如序列输入层302)将序列数据输入到神经网络。因此,序列输入层302接收用于训练深度学习架构300的特征,诸如一个或多个患者随时间变化的MAP和区域脑氧饱和度。
丢弃层(诸如丢弃层306和310)以给定的概率随机将输入元素设置为零。通过随机将输入元素设置为零,丢弃层可以使元素在训练阶段期间被忽略。在训练阶段期间选择性地忽略元素可以防止训练数据的过度拟合。
BiLSTM层(诸如BiLSTM层304、308和312)学习时间序列或序列数据的时间步长之间的双向长期依赖关系。这些依赖关系对于网络在每个时间步长从完整的时间序列中学习可能很有用。
全连接层(诸如全连接层314)将输入(例如,来自BiLSTM层312)乘以权重矩阵,然后加上偏置向量。softmax层(诸如softmax层316)将softmax函数应用于输入(例如,来自全连接层314)。softmax函数可以用作神经网络分类器(例如,脑自动调节模型124)的最后一个激活函数,以将全连接层314的输出归一化为预测输出类别的概率。
分类层(诸如分类层318)使用由softmax层316针对深度学习架构300的输入而输出的预测输出类别的概率将输入指派给两个或更多个互斥类别之一,并且可以将输入的输出类别输出到脑自动调节模型124,以作为训练具有深度学习架构300的脑自动调节模型124的结果。
图4展示了图1和图2的示例脑自动调节模型124的示例深度学习架构400。虽然深度学习架构400在图4中被展示为用于训练卷积神经网络(CNN)模型的CNN,但任何其他深度学习架构可以同样适合于训练脑自动调节模型124。
如图4所示,深度学习架构400的一部分包括卷积层404、最大池化层406、加法层408、批归一化层410、修正线性单元(ReLU)层412、丢弃层414、卷积层416、批归一化层418、ReLU层420、丢弃层422、卷积层424、最大池化层426和加法层428。图4中展示的深度学习架构400的部分可以只是CNN(即深度学习架构400)的隐藏层的一部分(即并非全部),并且深度学习架构可以包括图4中未示出的其他附加层。
二维卷积层(诸如卷积层404、416和424)将滑动卷积滤波器应用于该层的输入。该层通过沿输入以垂直和水平方式移动滤波器并计算权重和输入的点积、然后加上偏置项来对输入进行卷积。
最大池化层(诸如最大池化层406和426)通过将输入划分为矩形池化区域并计算每个区域的最大值来执行下采样。最大池化层跟随在卷积层之后以进行下采样,从而减少与跟随在最大池化层之后的层的连接数量,并减少在跟随在最大池化层之后的层中要学习的参数的数量。最大池化层还可以减少神经网络模型中的过度拟合。
加法层(诸如加法层408和428)逐个元素地将来自多个神经网络层的输入相加。在深度学习架构400的示例中,加法层408可以将来自卷积层404和最大池化层406的输入相加,并且加法层428可以将来自卷积层424和最大池化层426的输入相加。
批归一化层(诸如批量归一化层410和418)在小批量上对每个输入通道进行归一化。批归一化层可以加快CNN的训练并降低对网络初始化的敏感度。批归一化层可以用在卷积层与ReLU层之间,因此在深度学习架构400中,批归一化层410用在卷积层404与ReLU层412之间,并且批归一化层418用在卷积层416与ReLU层420之间。
ReLU层(诸如ReLU层412和420)对输入的每个元素执行阈值运算,其中,任何小于零的值都设置为零。ReLU层可以允许在大型复杂数据集上更快且更有效地训练深度学习架构400。
丢弃层(诸如丢弃层414和422)以给定的概率随机将输入元素设置为零。通过随机将输入元素设置为零,丢弃层可以使元素在训练阶段期间被忽略。在训练阶段期间选择性地忽略元素可以防止训练数据的过度拟合。
图5展示了使用图3和图4的深度学习架构进行脑自动调节状态分类的结果的示例图形。如图5所示,图形500A展示了使用图3的LSTM深度学习架构300进行脑自动调节状态分类的结果,并且图形500B展示了使用图4的CNN深度学习架构400进行脑自动调节状态分类的结果。
图形500A和图形500B中的每一个都展示了接受者工作特征(ROC)曲线,该曲线是展示二元分类器系统在其辨别阈值变化时的诊断能力的图形绘制。图形500A和图形500B各自的y轴是脑自动调节模型124对脑自动调节状态进行分类的真阳性率(TPR),并且图形500A和图形500B各自的y轴是脑自动调节模型124对脑自动调节状态进行分类的假阳性率(FPR)。
图形500A中的接受者工作特征(ROC)曲线502A展示了使用通过LSTM(诸如图3的LSTM深度学习架构300)训练的脑自动调节模型124针对测试集中的单个受试者(例如,患者101)的分类结果。ROC曲线下方的面积502A(也称为AUROC)可以等于分类器使随机选择的阳性实例排名高于随机选择的阴性实例的概率,其为0.93。使用LSTM训练的脑自动调节模型124的准确度可以为0.72,使用LSTM训练的脑自动调节模型124的灵敏度可以为0.95,并且使用LSTM训练的脑自动调节模型124的特异性可以为0.71。
图形500B中的接受者工作特征(ROC)曲线502B展示了使用通过CNN(诸如图4的CNN深度学习架构400)训练的脑自动调节模型124针对测试集中的单个受试者(例如,患者101)的分类结果。ROC曲线下方的面积502B(也称为AUROC)可以等于分类器使随机选择的阳性实例排名高于随机选择的阴性实例的概率,其为0.97。使用CNN训练的脑自动调节模型124的准确度可以为0.93,使用CNN训练的脑自动调节模型124的灵敏度可以为0.86,并且使用CNN训练的脑自动调节模型124的特异性可以为0.94。
图6展示了包括脑自动调节信息的示例用户界面。如图6所示,图形用户界面(GUI)600是脑自动调节监测系统100的处理电路系统110可以输出的界面的示例,该界面显示在显示器132上以提供患者101的脑自动调节状态。图形用户界面600包括患者101随时间变化的血压值602的图形。
GUI 600中的安全区604可以展示高于LLA的区,而GUI 600中的非安全区606可以展示低于LLA的区。通过展示患者101的血压值602是在安全区604还是非安全区606内,GUI600展示了患者101的血压值602与患者101的脑自动调节状态之间的关系。如GUI 600所展示的,血压值602处于安全区604,直到血压值602在时间t1处降至低于LLA到达非安全区606,然后直到血压值602在时间t2处恢复到高于LLA,并因此处于安全区604。
图7是展示了用于监测患者的脑自动调节状态的示例方法的流程图。尽管关于脑自动调节监测系统100的处理电路系统110(图1)对图7进行了描述,但在其他示例中,不同的处理电路系统可以单独或与处理电路系统110组合来执行图7的技术的任何部分。
如图7所示,该方法包括处理电路系统110收集关于患者101在一定时间段内的患者数据(702)。例如,可以收集30秒、60秒、90秒、120秒等时间内的患者数据。例如,如果时间段为30秒,则处理电路系统110可以收集从时间t秒开始到时间t+30秒为止的患者数据。
为了收集患者数据,处理电路系统110可以接收指示患者101的血压(诸如患者101的MAP)的血压信号,以及指示患者101的区域氧饱和度(诸如患者101的区域脑氧饱和度)的氧饱和度信号。例如,感测装置150和152可以生成血压信号和氧饱和度信号,这两种信号由处理电路系统110接收,如上所述。
在一些示例中,处理电路系统110对所收集的患者数据执行清洗(704)。例如,处理电路系统110可以移除无效值(诸如超出有效值范围的任何数据部分的值),对数据值执行平滑处理,对值执行插值等。
处理电路系统110将所收集的患者数据(例如,经清洗的患者数据)提供给脑自动调节模型124(706)。在一些示例中,为了将所收集的患者数据提供给脑自动调节模型124,处理电路系统110可以将患者101在该时间段内的血压(例如,MAP)和患者101在至少相同时间段内的区域脑氧饱和度作为输入提供给脑自动调节模型124。在一些示例中,如果由处理电路系统110接收的区域脑氧饱和度信号包括两个或更多个区域脑氧饱和度值,则处理电路系统110可以分别将该两个或更多个区域脑氧饱和度值中的每一个作为输入提供给脑自动调节模型124,或者可以将该两个或更多个区域脑氧饱和度值的平均值作为输入提供给脑自动调节模型124。
在一些示例中,处理电路系统110可以从患者101在该时间段内的血压和患者101在该时间段内的区域脑氧饱和度得出一个或多个值,并且可以将所得出的一个或多个值作为输入提供给脑自动调节模型124。例如,处理电路系统110可以确定患者101在该时间段内的MAP的梯度,并且可以确定患者101在该时间段内的区域脑氧饱和度的梯度,并且可以将所确定的梯度作为输入提供给脑自动调节模型124。
在一些示例中,处理电路系统110可以将与患者101相关联的附加数据作为输入提供给脑自动调节模型124。例如,处理电路系统110可以将以下各项作为输入提供给脑自动调节模型124:指示患者101在该时间段期间是否正在接受心肺转流术手术或其他医疗手术的转流标志;患者101在该时间段内的血压和/或区域脑氧饱和度的形态特征(例如,原始血压信号、原始PPG信号等,包括原始血压信号和原始PPG信号的峰值、位置、面积等);患者101在该时间段内的患者101收缩压和/或舒张压;患者101的人口统计数据,诸如身高、体重、年龄、性别、疾病状态和体重指数等。
处理电路系统110执行脑自动调节模型124,以基于输入的数据输出患者101的脑自动调节状态的指示(708)。也就是说,处理电路系统110可以使用脑自动调节模型124将患者101的脑自动调节状态分类为以下状态之一:完好无损、受损或未知。
在一些示例中,脑自动调节模型124可以基于输入的数据确定与患者101处于完好无损状态相关联的置信度值和与患者101处于受损状态相关联的置信度值,并且可以基于所确定的置信度值确定患者101的脑自动调节状态。例如,如果脑自动调节模型124确定与患者101处于完好无损状态相关联的置信度值高于与患者101处于受损状态相关联的置信度值,则处理电路系统110使用模型124确定患者101的脑自动调节状态为完好无损。相反地,如果脑自动调节模型124确定与患者101处于受损状态相关联的置信度值高于与患者101处于完好无损状态相关联的置信度值,则处理电路系统110使用模型124确定患者101的脑自动调节状态为受损。
在一些示例中,脑自动调节模型124确定置信度差值阈值。如果脑自动调节模型124确定与患者101处于受损状态相关联的置信度值和与患者101处于完好无损状态相关联的置信度值之间的差值小于或等于置信度差值阈值,则处理电路系统110可以使用脑自动调节模型124确定患者101的脑自动调节状态为未知。
在一些示例中,脑自动调节模型124可以将当前确定的与患者101处于受损状态相关联的置信度值和在与患者101的当前血压相同的血压下、先前的与患者101处于受损状态相关联的置信度值进行平均,以确定与患者101处于受损状态相关联的平均置信度值。类似地,脑自动调节模型124可以将当前确定的与患者101处于完好无损状态相关联的置信度值和在与患者101的当前血压相同的血压下、先前的与患者101处于完好无损状态相关联的置信度值进行平均,以确定与患者101处于完好无损状态相关联的平均置信度值。脑自动调节模型124可以诸如通过使用上述技术将与患者101处于完好无损状态相关联的平均置信度值和与患者101处于受损状态相关联的平均置信度值进行比较,以确定患者101的脑自动调节状态。
在一些示例中,脑自动调节模型124可以响应于确定与患者101处于完好无损状态和处于受损状态相关联的置信度值,将这些置信度值记录在存储器120中存储的置信度矩阵中。置信度矩阵中的值可以用于后验计算患者101的脑自动调节状态。
响应于确定患者101的脑自动调节状态,处理电路系统110还可以返回收集关于患者101在一定时间段内的患者数据(702)。在一些示例中,处理电路系统110可以等待时间过去一秒,然后再返回收集关于患者101在一定时间段内的患者数据。
该方法进一步包括,响应于确定患者101的脑自动调节状态,处理电路系统110输出患者101的脑自动调节状态的指示(诸如用于显示在显示器132上)(712)。例如,处理电路系统110可以输出图形用户界面(诸如图6的图形用户界面600),该图形用户界面可以提供当前确定的患者101的脑自动调节状态以及与患者101相关联的附加信息,诸如患者101的血压、患者101的区域脑氧饱和度等。
图8是展示了用于监测患者的脑自动调节状态的示例方法的流程图。尽管关于脑自动调节监测系统100的处理电路系统110(图1)对图8进行了描述,但在其他示例中,不同的处理电路系统可以单独或与处理电路系统110组合来执行图8的技术的任何部分。
如图8所示,脑自动调节监测系统100的处理电路系统110可以接收指示患者101在一定时间段内的血压的血压信号和指示患者101该时间段内的区域脑氧饱和度的氧饱和度信号(802)。处理电路系统110可以使用脑自动调节模型124的神经网络算法,至少部分地基于患者101在该时间段内的血压和患者101在该时间段内的区域脑氧饱和度来确定患者101的脑自动调节状态(804)。处理电路系统110可以向输出装置发送指示患者101的脑自动调节状态的信号(806)。
在一些示例中,使用脑自动调节模型124的神经网络算法来确定患者101的脑自动调节状态进一步至少部分地基于以下各项中的一项或多项:患者101在该时间段内的血压的梯度、患者101在该时间段内的区域脑氧饱和度的梯度、患者101在该时间段内的脑氧合指数。
在一些示例中,处理电路系统110进一步被配置为使用脑自动调节模型124的神经网络算法,至少部分地基于指示患者101在该时间段期间正在接受心肺转流术手术的转流标志来确定患者101的脑自动调节状态。
在一些示例中,神经网络算法是经由对训练数据214的机器学习来训练的,以将患者101的脑自动调节状态分类为以下状态之一:受损、完好无损或未知。
在一些示例中,训练数据214包括以下各项中的两项或更多项:一个或多个患者随时间变化的血压、一个或多个患者随时间变化的区域脑氧饱和度值、一个或多个患者在多个时间段中的每个时间段内的血压的梯度、一个或多个患者在多个时间段中的每个时间段内的区域脑氧饱和度的梯度、一个或多个患者在多个时间段中的每个时间段内的血压和区域脑氧饱和度的脑氧合指数(COx)、指示一个或多个患者在多个时间段中的每个时间段期间是否正在接受心肺转流术手术的一个或多个转流标志、以下各项中的一项或多项的形态特征:在多个时间段中的每个时间段期间的血压或区域脑氧饱和度、一个或多个患者随时间变化的收缩压、一个或多个患者随时间变化的舒张压、或与一个或多个患者相关联的人口统计数据。
在一些示例中,一个或多个患者随时间变化的血压包括,对于这些时间段中的每个时间段,在相应时间段期间的血压减去随时间变化的血压的均值,并且一个或多个患者随时间变化的区域脑氧饱和度包括,对于这些时间段中的每个时间段,在相应时间段期间的区域脑氧饱和度减去随时间变化的区域脑氧饱和度的均值。
在一些示例中,处理电路系统110可以进一步被配置为使用脑自动调节模型124的神经网络算法,至少通过以下操作确定患者101的脑自动调节状态:确定与患者101的脑自动调节状态为完好无损相关联的第一置信度分数,确定与患者101的脑自动调节状态为受损相关联的第二置信度分数,并至少部分地基于将第一置信度分数和第二置信度分数进行比较来将患者101的脑自动调节状态分类为以下状态之一:受损、完好无损或未知。
在一些示例中,为了对患者101的脑自动调节状态进行分类,处理电路系统101进一步被配置为确定第一置信度分数与第二置信度分数之间的差值是否在置信度阈值内,并且响应于确定第一置信度分数与第二置信度分数之间的差值小于或等于置信度阈值,将患者的脑自动调节状态分类为未知。
在一些示例中,处理电路系统101进一步被配置为:将与患者101的脑自动调节状态为完好无损相关联的平均第一置信度分数确定为与患者101的脑自动调节状态为完好无损相关联的、患者当前血压下的第一置信度分数和当前血压下的第一组先前确定的置信度分数的平均值;将与患者101的脑自动调节状态为受损相关联的平均第二置信度分数确定为与患者101的脑自动调节状态为受损相关联的、患者当前血压下的第二置信度分数和当前血压下的第二组先前确定的置信度分数的平均值,并通过将平均第一置信度分数和平均第二置信度分数进行比较来对患者101的脑自动调节状态进行分类,以将患者101的脑自动调节状态分类为以下状态之一:受损、完好无损或未知。
本公开中描述的技术将归属于装置100、处理电路系统110、控制电路系统122、感测电路系统140、142或各种组成部件的技术包括在内,并且可以至少部分地以硬件、软件、固件或其任何组合实施。例如,可以在一个或多个处理器中实施这些技术的不同方面,包括一个或多个微处理器、DSP、ASIC、FPGA或任何其他等效集成或离散逻辑电路以及这种部件的任何组合,在如临床医生或患者编程器等编程器、医疗装置或其他装置中将这些部件具体化。例如,处理电路系统、控制电路系统和感测电路系统以及本文中描述的其他处理器和控制器可以至少部分地实施为或包括一个或多个可执行应用程序、应用程序模块、库、类、方法、对象、例程、子例程、固件和/或嵌入式代码等。
在一个或多个示例中,可以以硬件、软件、固件或其任何组合实施在本公开中所描述的功能。如果是以软件实施,那么这些功能可以作为一个或多个指令或代码被存储在计算机可读介质上并且由基于硬件的处理单元执行。计算机可读介质可以是包括用指令编码的非暂态计算机可读存储介质的制品。被嵌入或被编码至包括被编码的非暂态计算机可读存储介质的制品中的指令诸如当被包括或被编码至非暂态计算机可读存储介质中的指令由一个或多个处理器来执行时可以使一个或多个可编程处理器或其他处理器来实施本文所描述的技术中的一种或多种技术。示例非暂态计算机可读存储介质可以包括RAM、ROM、可编程ROM(PROM)、可擦除可编程ROM(EPROM)、电可擦除可编程ROM(EEPROM)、闪存、硬盘、光盘ROM(CD-ROM)、软盘、磁带盒、磁性介质、光学介质、或任何其他计算机可读存储装置或有形计算机可读介质。
在一些示例中,计算机可读存储介质包括非暂态介质。术语“非暂态”可以指示该存储介质不是以载波或所传播的信号来实施的。在某些示例中,非暂态存储介质可以存储可随时间改变的数据(例如,在RAM或高速缓存中)。
本文描述的功能可以在专用的硬件和/或软件模块内提供。将不同的特征描绘成模块或单元旨在突显功能方面的不同,并非暗示此类模块或单元必须由不同的硬件或软件部件来实施。反之,与一个或多个模块或单元相关联的功能可以由不同硬件或软件部件来执行,或者集成在共同的或不同的硬件或软件部件内。此外,这些技术可以在一个或多个电路或逻辑元件中完全实施。
以下条款包括本文描述的示例主题。
条款1:一种方法,包括:由处理电路系统接收指示患者在一定时间段内的血压的血压信号和指示所述患者在所述时间段内的区域脑氧饱和度的氧饱和度信号;由所述处理电路系统使用脑自动调节模型的神经网络算法,至少部分地基于所述患者在所述时间段内的血压和所述患者在所述时间段内的区域脑氧饱和度来确定所述患者的脑自动调节状态;以及由所述处理电路系统向输出装置发送指示所述患者的脑自动调节状态的信号。
条款2:如条款1所述的方法,其中,使用所述脑自动调节模型的神经网络算法确定所述患者的脑自动调节状态进一步包括:由所述处理电路系统至少部分地基于以下各项中的一项或多项来确定所述脑自动调节状态:所述患者在所述时间段内的血压的梯度;所述患者在所述时间段内的区域脑氧饱和度的梯度;或所述患者在所述时间段内的脑氧合指数。
条款3:如条款1或2所述的方法,其中,使用所述脑自动调节模型的神经网络算法确定所述患者的脑自动调节状态进一步包括:由所述处理电路系统至少部分地基于指示所述患者在所述时间段期间正在接受心肺转流术手术的转流标志来确定所述脑自动调节状态。
条款4:如条款1至3中任一项所述的方法,其中,所述神经网络算法是经由对训练数据的机器学习来训练的,以将所述患者的脑自动调节状态分类为以下状态之一:受损、完好无损或未知。
条款5:如条款4所述的方法,其中,所述训练数据包括以下各项中的两项或更多项:一个或多个患者随时间变化的血压;所述一个或多个患者随时间变化的区域脑氧饱和度值;所述一个或多个患者在多个时间段中的每个时间段内的血压的梯度;所述一个或多个患者在所述多个时间段中的每个时间段内的区域脑氧饱和度值的梯度;基于所述一个或多个患者在所述多个时间段中的每个时间段内的血压和区域脑氧饱和度确定的脑氧合指数(COx);指示所述一个或多个患者在所述时间段中的每个时间段期间是否正在接受心肺转流术手术的一个或多个转流标志;在所述时间段中的每个时间段期间的血压或区域脑氧饱和度中的一项或多项的形态特征;所述一个或多个患者随时间变化的收缩压;所述一个或多个患者随时间变化的舒张压;或与所述一个或多个患者相关联的人口统计数据。
条款6:如条款5所述的方法,其中:所述一个或多个患者随时间变化的血压包括,对于所述时间段中的每个时间段,在相应时间段期间的血压减去随时间变化的所述血压的均值;以及所述一个或多个患者随时间变化的区域脑氧饱和度值包括,对于所述时间段中的每个时间段,在相应时间段期间的区域脑氧饱和度值减去随时间变化的区域脑氧饱和度值的均值。
条款7:如条款4至6中任一项所述的方法,其中,使用所述脑自动调节模型的神经网络算法确定所述患者的脑自动调节状态进一步包括:由所述处理电路系统确定与所述患者的脑自动调节状态为完好无损相关联的第一置信度分数;由所述处理电路系统确定与所述患者的脑自动调节状态为受损相关联的第二置信度分数;以及由所述处理电路系统至少部分基于将所述第一置信度分数和所述第二置信度分数进行比较来将所述患者的脑自动调节状态分类为以下状态之一:受损、完好无损或未知。
条款8:如条款7所述的方法,其中,对所述患者的脑自动调节状态进行分类进一步包括:由所述处理电路系统确定所述第一置信度分数与所述第二置信度分数之间的差值是否在置信度阈值内;以及响应于确定所述第一置信度分数与所述第二置信度分数之间的差值小于或等于置信度阈值,由所述处理电路系统将所述患者的脑自动调节状态分类为未知。
条款9:如条款7或8所述的方法,进一步包括:由所述处理电路系统将与所述患者的脑自动调节状态为完好无损相关联的平均第一置信度分数确定为与所述患者的脑自动调节状态为完好无损相关联的、所述患者当前血压下的第一置信度分数和所述当前血压下的第一组先前确定的置信度分数的平均值;将与所述患者的脑自动调节状态为受损相关联的平均第二置信度分数确定为与所述患者的脑自动调节状态为受损相关联的、所述患者当前血压下的第二置信度分数和所述当前血压下的第二组先前确定的置信度分数的平均值;并且其中,对所述患者的脑自动调节状态进行分类进一步包括:由所述处理电路系统将所述平均第一置信度分数和所述平均第二置信度分数进行比较,以将所述患者的脑自动调节状态分类为以下状态之一:受损、完好无损或未知。
条款10:一种系统,包括:血压感测装置;氧饱和度感测装置;以及处理电路系统,所述处理电路系统被配置为:从所述血压感测装置接收指示患者在一定时间段内的血压的血压信号,并且从所述氧饱和度感测装置接收指示所述患者在所述时间段内的区域脑氧饱和度的氧饱和度信号;使用脑自动调节模型的神经网络算法,至少部分地基于所述患者在所述时间段内的血压和所述患者在所述时间段内的区域脑氧饱和度来确定所述患者的脑自动调节状态;以及向输出装置发送指示患者的脑自动调节状态的信号。
条款11:如条款10所述的系统,其中,使用所述脑自动调节模型的神经网络算法来确定所述患者的脑自动调节状态进一步至少部分地基于以下各项中的一项或多项:所述患者在所述时间段内的血压的梯度;所述患者在所述时间段内的区域脑氧饱和度的梯度;或所述患者在所述时间段内的脑氧合指数。
条款12:如条款10或11所述的系统,其中,所述处理电路系统进一步被配置为使用所述脑自动调节模型的神经网络算法,至少部分地基于指示所述患者在所述时间段期间正在接受心肺转流术手术的转流标志来确定所述患者的脑自动调节状态。
条款13:如条款10至12中任一项所述的系统,其中,所述神经网络算法是经由对训练数据的机器学习来训练的,以将所述患者的脑自动调节状态分类为以下状态之一:受损、完好无损或未知。
条款14:如条款13所述的系统,其中,所述训练数据包括以下各项中的两项或更多项:一个或多个患者随时间变化的血压;所述一个或多个患者随时间变化的区域脑氧饱和度值;所述一个或多个患者在多个时间段中的每个时间段内的血压的梯度;所述一个或多个患者在所述多个时间段中的每个时间段内的区域脑氧饱和度的梯度;所述一个或多个患者在所述时间段中的每个时间段内的血压和区域脑氧饱和度的脑血氧指数(COx);指示所述一个或多个患者在所述时间段中的每个时间段期间是否正在接受心肺转流术手术的一个或多个转流标志;以下各项中的一项或多项的形态特征:在所述时间段中的每个时间段期间的所述血压或所述区域脑氧饱和度;所述一个或多个患者随时间变化的收缩压;所述一个或多个患者随时间变化的舒张压;或与所述一个或多个患者相关联的人口统计数据。
条款15:如条款14所述的系统,其中:所述一个或多个患者随时间变化的血压包括,对于所述时间段中的每个时间段,在相应时间段期间的血压减去随时间变化的所述血压的均值;并且所述一个或多个患者随时间变化的区域脑氧饱和度包括,对于所述时间段中的每个时间段,在相应时间段期间的区域脑氧饱和度减去随时间变化的所述区域脑氧饱和度的均值。
条款16:如条款13至15中任一项所述的系统,其中,所述处理电路系统被配置为使用所述脑自动调节模型的神经网络算法,至少通过以下操作确定所述患者的脑自动调节状态:确定与所述患者的脑自动调节状态为完好无损相关联的第一置信度分数;确定与所述患者的脑自动调节状态为受损相关联的第二置信度分数;以及至少部分地基于将所述第一置信度分数与所述第二置信度分数进行比较来将所述患者的脑自动调节状态分类为以下状态之一:受损、完好无损或未知。
条款17:如条款16所述的系统,其中,为了对所述患者的脑自动调节状态进行分类,所述处理电路系统进一步被配置为:确定所述第一置信度分数与所述第二置信度分数之间的差值是否在置信度阈值内;以及响应于确定所述第一置信度分数与所述第二置信度分数之间的差值小于或等于置信度阈值,将所述患者的脑自动调节状态分类为未知。
条款18:如条款16或17所述的系统,其中,所述处理电路系统进一步被配置为:将与所述患者的脑自动调节状态为完好无损相关联的平均第一置信度分数确定为与所述患者的脑自动调节状态为完好无损相关联的、所述患者当前血压下的第一置信度分数和所述当前血压下的第一组先前确定的置信度分数的平均值;将与所述患者的脑自动调节状态为受损相关联的平均第二置信度分数确定为与所述患者的脑自动调节状态为受损相关联的、所述患者当前血压下的第二置信度分数和所述当前血压下的第二组先前确定的置信度分数的平均值;以及通过将所述平均第一置信度分数与所述平均第二置信度分数进行比较来对所述患者的脑自动调节状态进行分类,以将所述患者的脑自动调节状态分类为以下状态之一:受损、完好无损或未知。
条款19:一种非暂态计算机可读可存储介质,包括:接收指示患者在一定时间段内的血压的血压信号和指示所述患者在所述时间段内的区域脑氧饱和度的氧饱和度信号;使用脑自动调节模型的神经网络算法,至少部分地基于所述患者在所述时间段内的血压和所述患者在所述时间段内的区域脑氧饱和度来确定所述患者的脑自动调节状态;以及向输出装置发送指示患者的脑自动调节状态的信号。
条款20:如条款19所述的非暂态计算机可读可存储介质,其中,使所述处理电路系统使用所述脑自动调节模型的神经网络算法确定所述患者的脑自动调节状态的所述指令进一步使所述处理电路系统:确定与所述患者的脑自动调节状态为完好无损相关联的第一置信度分数;确定与所述患者的脑自动调节状态为受损相关联的第二置信度分数;以及至少部分地基于将所述第一置信度分数与所述第二置信度分数进行比较来将所述患者的脑自动调节状态分类为以下状态之一:受损、完好无损或未知。
已描述了本公开的各个示例。设想了所描述的系统、操作或功能的任何组合。这些和其他示例落入以下权利要求的范围内。
权利要求书(按照条约第19条的修改)
1.一种系统,包括:
血压感测装置;
氧饱和度感测装置;以及
处理电路系统,所述处理电路系统被配置为:
从所述血压感测装置接收指示患者在一定时间段内的血压的血压信号,并且从所述氧饱和度感测装置接收指示所述患者在所述时间段内的区域脑氧饱和度的氧饱和度信号;
使用脑自动调节模型的神经网络算法,至少部分地基于所述患者在所述时间段内的血压和所述患者在所述时间段内的区域脑氧饱和度来确定所述患者的脑自动调节状态,其中,所述神经网络算法是经由对训练数据的机器学习来训练的,以将所述患者的脑自动调节状态分类为以下状态之一:受损、完好无损或未知;并且
向输出装置发送指示所述患者的脑自动调节状态的信号。
2.如权利要求1所述的系统,其中,使用所述脑自动调节模型的神经网络算法来确定所述患者的脑自动调节状态进一步至少部分地基于以下各项中的一项或多项:
所述患者在所述时间段内的血压的梯度;
所述患者在所述时间段内的区域脑氧饱和度的梯度;或者
所述患者在所述时间段内的脑氧合指数。
3.如权利要求1或2中任一项所述的系统,其中,所述处理电路系统进一步被配置为使用所述脑自动调节模型的神经网络算法,至少部分地基于指示所述患者在所述时间段期间正在接受心肺转流术手术的转流标志来确定所述患者的脑自动调节状态。
4.如权利要求1至3中任一项所述的系统,其中,所述训练数据包括以下各项中的两项或更多项:
一个或多个患者随时间变化的血压;
所述一个或多个患者随时间变化的区域脑氧饱和度值;
所述一个或多个患者在多个时间段中的每个时间段内的血压的梯度;
所述一个或多个患者在所述多个时间段中的每个时间段内的区域脑氧饱和度的梯度;
所述一个或多个患者在所述时间段中的每个时间段内的血压和区域脑氧饱和度的脑血氧指数(COx);
指示所述一个或多个患者在所述时间段中的每个时间段期间是否正在接受心肺转流术手术的一个或多个转流标志;
以下各项中的一项或多项的形态特征:在所述时间段中的每个时间段期间的所述血压或所述区域脑氧饱和度;
所述一个或多个患者随时间变化的收缩压;
所述一个或多个患者随时间变化的舒张压;或者
与所述一个或多个患者相关联的人口统计数据。
5.如权利要求4所述的系统,其中:
所述一个或多个患者随时间变化的血压包括,对于所述时间段中的每个时间段,在相应时间段期间的血压减去随时间变化的所述血压的均值;并且
所述一个或多个患者随时间变化的区域脑氧饱和度包括,对于所述时间段中的每个时间段,在相应时间段期间的区域脑氧饱和度减去随时间变化的所述区域脑氧饱和度的均值。
6.如权利要求1至5中任一项所述的系统,其中,所述处理电路系统被配置为使用所述脑自动调节模型的神经网络算法,至少通过以下操作确定所述患者的脑自动调节状态:
确定与所述患者的脑自动调节状态为完好无损相关联的第一置信度分数;
确定与所述患者的脑自动调节状态为受损相关联的第二置信度分数;以及
至少部分地基于将所述第一置信度分数与所述第二置信度分数进行比较来将所述患者的脑自动调节状态分类为以下状态之一:受损、完好无损或未知。
7.如权利要求6所述的系统,其中,为了对所述患者的脑自动调节状态进行分类,所述处理电路系统进一步被配置为:
确定所述第一置信度分数与所述第二置信度分数之间的差值是否在置信度阈值内;并且
响应于确定所述第一置信度分数与所述第二置信度分数之间的差值小于或等于置信度阈值,将所述患者的脑自动调节状态分类为未知。
8.如权利要求6或7中任一项所述的系统,其中,所述处理电路系统进一步被配置为:
将与所述患者的脑自动调节状态为完好无损相关联的平均第一置信度分数确定为与所述患者的脑自动调节状态为完好无损相关联的、所述患者当前血压下的第一置信度分数和所述当前血压下的第一组先前确定的置信度分数的平均值;
将与所述患者的脑自动调节状态为受损相关联的平均第二置信度分数确定为与所述患者的脑自动调节状态为受损相关联的、所述患者当前血压下的第二置信度分数和所述当前血压下的第二组先前确定的置信度分数的平均值;并且
通过将所述平均第一置信度分数与所述平均第二置信度分数进行比较来对所述患者的脑自动调节状态进行分类,以将所述患者的脑自动调节状态分类为以下状态之一:受损、完好无损或未知。
9.一种非暂态计算机可读可存储介质,所述介质包括指令,所述指令当被执行时使处理电路系统:
接收指示患者在一定时间段内的血压的血压信号和指示所述患者在所述时间段内的区域脑氧饱和度的氧饱和度信号;
使用脑自动调节模型的神经网络算法,至少部分地基于所述患者在所述时间段内的血压和所述患者在所述时间段内的区域脑氧饱和度来确定所述患者的脑自动调节状态,其中,所述神经网络算法是经由对训练数据的机器学习来训练的,以将所述患者的脑自动调节状态分类为以下状态之一:受损、完好无损或未知;以及
向输出装置发送指示所述患者的脑自动调节状态的信号。
- 一种钻孔煤岩电荷深度监测自动调节装置及使用方法
- 使用自动编码器减小心内心电图噪声及使用深度学习训练损失函数以细化心内和体表心电图
