通过单自由度腔室分割对心脏功能的超声诊断
文献发布时间:2024-04-18 19:58:21
本申请是2016年02月05日提交的申请号为201680014504.6、名称为“通过单自由度腔室分割对心脏功能的超声诊断”的发明专利申请的分案申请。
技术领域
本发明涉及医学诊断超声系统,并且具体涉及单自由度心脏腔室分割的使用。
背景技术
超声成像通常被用于通过测量诸如射血分数和心脏输出量来诊断心脏功能。这样的测量要求要在心脏腔室的二维和三维图像中勾画出在心脏的各种时相处在心脏腔室中的血液的体积。通常,已经由用户手动描记腔室的心内膜边界来生成诸如左心室的心脏腔室的体积的测量结果。由于不同的用户在确定在哪里定位所述描记的过程中所使用的标准的差异,这样的描记经受显著的变化性。已经开发了自动化的方法以尝试使这种边界描记自动化,诸如在美国专利6491636(Chenal等人)中所描述的自动化的描记技术。在该技术中,定位腔室的解剖学标志,包括二尖瓣平面角以及心脏腔室的顶端。多个标准、专家确认的心内膜形状中的一个然后被拟合到这些标志。自动绘制的边界然后能够通过橡皮条手动地调节,借此,用户移动所述边界上的控制点以在心内膜上调节其最终的位置。针对在收缩末期和舒张末期心脏阶段处拍摄的图像来完成该处理。两个边界能够被比较或相减以估计射血分数或心脏输出。例如,US2009/0136109公开了通过比较所识别的心内膜边界(其限定心肌的内表面)与所识别的心外膜边界(其限定心肌的外表面)来产生心肌厚度体积。US2009/0136109中的心肌厚度体积是中空的,其中,内部的中空空间是心脏腔室的体积。在EP 2434454 A2中描述了类似的方法,其中,基于所检测的左心室(LV)边界来计算LV的体积。EP 2434454 A2的系统使用各种机器学习,以用于定位和跟踪心脏壁。这些训练技术基于训练数据集,其使用针对机器学习所收集的已知案例的数据库。能够通过诸如自动辛普森算法(盘规则(rule of disks))的公认的方法来估计射血分数,以测量随着心脏的每次收缩射出的腔室体积的分数。
但是自动化的图像分析方法并不总是产生所有用户都接受的心脏腔室勾画。这种不成功大部分是由于所述自动方法不能持续对任意给定用户相信边界应当被放置的边界进行定位。这种不良性能主要是由于在不同用户之间关于指定真实边界在哪里的解剖学标志的变化性。
发明内容
本发明的目标是为用户提供一种简单的自动化工具,以用于勾画可接受心脏腔室边界的位置。另外的目标是,这样的勾画是标准化的,并且能够比较和产生在不同用户之中可接受的结果。这样的结果将一个临床医师的方法总结成单个值,其能够被具有相同工具的其他临床医师所理解并被传送到所述其他临床医师。
根据本发明的原理,描述了一种诊断超声系统和方法,其诊断心脏性能。采集心脏的腔室的图像,并且图像被分割以勾画心肌的内边界和外边界,或者替代地,勾画心肌的若干(3+)边界。优选地,这是利用自动化的图像分析处理器(诸如使用心脏模型数据的图像分析处理器)来完成的。提供了用户控制,其使得用户能够定义相对于一个、两者或若干分割边界的用户偏好的腔室边界位置。所述用户控制提供了单值、单自由度,用户可以对其进行改变以定位真实的腔室边界,诸如相对于分割的边界的距离的百分比。所述单值能够与相同工具的其他用户共享,使得其他用户能够利用其他图像获得与相同的结果,并且因此,实现了心脏腔室边界识别的标准化。
附图说明
在附图中:
图1以框图形式图示了根据本发明的原理构造的超声诊断成像系统。
图2是图示根据本发明的原理的图1的QLQB处理器的边界检测细节的框图。
图3a和3b图示了对于边界检测有用的左心室的标志。
图4a、4b和4c图示了被用于自动边界检测的专家导出的心内膜边界形状。
图5a和5b图示了左心室的图像中的心外膜和心内膜的勾画。
图6是根据本发明的操作可变形的心脏模型以找到心脏边界的流程图。
图7a和7b是舒张末期和收缩末期处的左心室的心脏图像,其中,已经描记了心内膜边界以及非致密心肌与致密心肌之间的界面。
图8a和8b图示了图7b的收缩末期超声图像,其中,用户定义的边界已经被定位在图7b中勾画的两个心脏边界之间的距离的0%和100%处。
图8c图示了心脏图像,其中,用户定义的边界被定位在从心内膜描记到致密的心肌界面的距离的40%处。
图8d图示了根据本发明的实施例的单自由度用户控制,其中,用户定义的边界被相对于心肌的若干边界进行定位。
图9图示了来自双平面图像的用户定义的心脏腔室,其是使用盘规则在体积上测量的。
图10图示了来自对体积测量的3D超声图像准备的用户定义的心脏腔室线框架模型。
具体实施方式
首先参考图1,以框图形式示出了根据本发明的原理构造的超声诊断成像系统10。超声探头12包括发射和接受超声脉冲的超声换能器的阵列14。所述阵列可以为用于二维成像的一维线性或弯曲阵列,或者可以为换能器元件的二维矩阵,用于在三个维度上电子地操控波束。阵列14中的超声换能器发射超声能量,并且接收响应于该发射而返回的回波。发射频率控制单元20通过被耦合到阵列14中的超声换能器的发射/接受(“T/R”)开关22以期望的频率或频率带来控制超声能量的发射。所述换能器阵列被激活以发射信号的时间可以被同步到内部系统时钟(未示出),或者可以被同步到诸如心脏周期的身体机能,针对所述心脏周期,由ECG设备26提供心脏周期波形。当心搏在其周期的期望相位时(如由ECG设备26提供的所述波形确定的),命令所述探头采集超声图像。这例如实现在舒张末期和收缩末期心脏阶段处的采集。由发射频率控制电路20所生成的超声能量的频率和带宽是由中央控制器28所生成的控制信号f
来自所发射的超声能量的回波由阵列14中的换能器来接收,所述换能器生成回波信号,当所述系统使用数字射束形成器时所述回波信号通过T/R开关22而被耦合并且通过模数(“A/D”)转换器30而被数字化。也可以使用模拟波束形成器。A/D转换器30以由中央控制器28所生成的信号f
来自阵列14中的个体换能器的回波信号样本被波束形成器32延迟和加和以形成相干回波信号。针对具有二维阵列的3D成像,优选地将波束形成器区分为被定位在探头中的微波束形成器与系统主机中的主波束形成之间,如在美国专利6013032(Savord)和美国专利6375617(Fraser)中所描述的。然后通过数字滤波器34对数字相干回波信号进行滤波。在所图示的超声系统中,单独地控制发射频率和接收器频率,使得波束形成器32自由地接收与所发射的带不同的频率带,例如谐波频带。数字滤波器34对所述信号进行带通滤波,并且也能够将所述频带移位到较低的或基带频率范围。例如,所述数字滤波器能够是在美国专利No.5833613中所公开的类型的滤波器。来自组织的经滤波的回波信号被从数字滤波器34耦合到B模式处理器36以用于常规B模式图像处理。
对比剂(例如微泡)的经滤波的回波信号被耦合到对比剂信号处理器38。对比剂常常被用于相对于在心脏腔室的血池中的对比剂更为清晰地勾画心内膜壁,或者被用于执行对心肌的微脉管系统的灌注研究,例如,如在美国专利6692438中所描述的。对比信号处理器38优选通过脉冲反转技术将从谐波对比剂返回的回波分离,其中,源自多个不同地调制的脉冲到图像位置的发射的回波被组合以消除基波信号分量并增强谐波信号分量。优选的脉冲反转技术在例如美国专利6186950中进行了描述。
来自数字滤波器34的滤波回波信号也被耦合到多普勒处理器40,用于常规的多普勒处理,以产生速度和功率多普勒信号。来自这些处理器的输出信号可以被显示为平面图像,并且也被耦合到3D图像处理器42,用于对三维图像的绘制,所述三维图像被存储在3D图像存储器44中。可以如在美国专利US 5720291,以及在美国专利US 5474073和US 5485842中描述的那样,执行三维绘制,在此通过引用并入其全部内容。
来自对比信号处理器38、B模式处理器和多普勒处理器的信号,以及来自3D图像存储器44的三维图像信号被耦合到影像回放
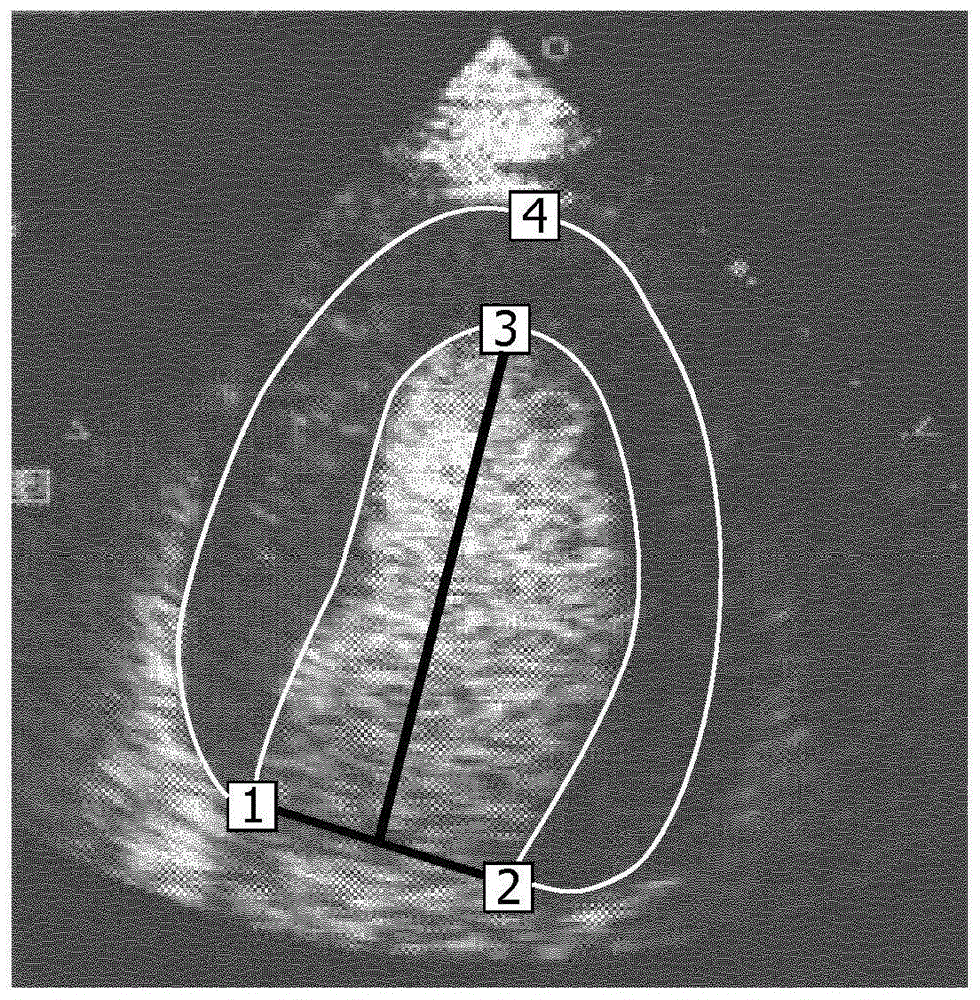
图2图示了QLAB处理器根据本发明的原理来勾画用户定义的心脏腔室边界的操作的进一步的细节。心脏超声图像是由心脏图像数据60的源来提供的,其可以是影像回放存储器48、3D图像存储器44、或者图1的图像处理器36、38或40之一。所述心脏图像被转发到自动边界检测(ABD)处理器62。ABD处理器可以是完全自动的或者半自动的(用户辅助的)图像处理器,其勾画心脏图像中的腔室的边界,下文中描述了其中的几个。在典型半自动ABD系统中,用户利用操纵图像上的光标的、通常被定位在超声系统控制面板上的鼠标或轨迹球的指向设备或者利用工作站键盘在所述心脏图像上指定第一标志。例如,在图3a的范例中,所指定的第一标志是在所图示的视图中的左心室(LV)底侧的内侧二尖瓣环(MMA)。当用户点击在图像中的MMA时,出现图形标记,诸如在图中由数字“1”指示的白色控制点。在该范例中,用户然后指定第二标志,外侧二尖瓣环(LMA),其是利用图3b中的数字“2”指示的第二白色控制点来标记的。由ABD处理器产生的线然后自动地连接两个控制点,其在左心室的该纵向视图的情况下指示二尖瓣平面。用户然后将指针移动到心内膜顶点,所述心内膜顶点是在左心室腔内的最上侧点。在用户将指针移动到所述图像中的该第三标志时,左心室心内膜腔的模板形状在用户操作的指针搜寻LV腔室的顶点时动态地跟随光标、扭曲和拉伸,如在图5a中所示。在图5a被示为白线的该模板由第一和第二控制点1和2来锚定并且通过第三控制点,当用户点击在顶点处的点时,所述第三控制点被定位在所述顶点处,来定位所述第三控制点3。在图4a、4b和4c中示出了典型的LV腔室边界模板。这些模板是根据在许多患者中的LV心内膜边界的许多专家描记来确定的。图4a的模板是典型的许多正常患者的拉长的模板。图4b的模板82在形状上是更为球形的,患有充血性心脏衰竭的许多患者的特性。模板84是又一第三种可能,较像泪滴形。由ABD处理器62选择最佳地匹配由用户识别的三个解剖学标志的模板,并且对其进行扭曲以适配三个用户定义的标志。当被定位和匹配到所述标志时,心内膜腔模板80、82或84提供了对LV的心内膜的近似描记,如在图5a中所示的。在图5a的范例中,二分左心室的黑线在指针接近并且指定顶点时跟随所述指针。该黑线被固定在指示二尖瓣平面的线的中心与左心室顶点之间,本质上指示在二尖瓣的中心与腔的顶点之间的中心线。
一旦ABD处理器62已经发现LV的心内膜线,其然后试图找到心外膜边界。在图5b中图示了这种情况,其中,用户已经移动了光标并且在图像中的暗心肌外部的顶点4上进行点击。图5的图像是对比增强的谐波图像,其中,LV的腔室已经被浸没以对比剂,但是对比剂尚未完全灌注心肌,这是为什么LV腔室相对于在该图像中的较暗的周边心肌显得非常明亮。当用户在心外膜顶点上进行点击时,如之前的情况,ABD处理器选择与图4的模板相似的外部或心外膜模板并且将其适配到心外膜,如在图5b中所图示。心脏图像现在具有通过由图形生成器66产生的描记在图像中勾画出的其心内膜边界(连接1、3和2标记的线)、血池心肌表面以及其心外膜边界(连接1、4和2标记的线)、心脏的最外部表面两者。
替代要求用户交互的半自动操作,ABD处理器可以如在前述美国专利6491636中所描述地完全自动地勾画LV的边界。如在本文中所解释的,图像处理器能够被配置为自动地找到二尖瓣角和顶点,然后将模板适配到自动定位的标志。然而,用于自动地勾画心肌边界的优选技术是利用心脏模型,如在图6中所图示。心脏模型是对典型心脏的组织结构的空间定义的数学描述,其能够被匹配到如在诊断图像中出现的心脏,从而定义被成像的心脏的具体解剖结构。图6的过程在90处以对心脏图像的采集开始。然后在92处通过利用广义霍夫变换处理图像数据而在心脏图像中定位心脏的位置。在该点处,心脏的姿态尚未被定义,因此,在94处,通过针对整个心脏模型使用单个相似性变换来校正对图像数据中的心脏的平移、旋转和缩放过程中的未对准。接下来,在96处,所述模型被变形,并且仿射变换被分配到心脏的具体区域。在98处,通过允许心脏模型相对于逐段仿射变换而变形来缓解关于变形的约束,并且形状约束的可变形模型被重定尺寸和变形,使得模型的每个部分匹配实际患者解剖结构,如在心脏循环的所捕获的阶段处的图像中所示。所述模型因此被准确地适配到心脏图像中所示的器官边界,从而定义包括心内膜线的边界、非致密的心肌与致密心肌之间的界面、以及心外膜边界。在这样的心脏模型的优选实施方案中,首先找到在非致密心肌与致密心肌之间的界面,因为这通常表现为在超声图像中的明亮区域与中等量度区域之间的明确定义的梯度。由于期望能够找到出现在超声图像中的更少明确定义的内皮线的可变位置,心内膜边界通常在心脏模型中是较不明确定义的。不像图5a和5b的对比增强的心脏图像,未增强的超声图像一般将在围绕心肌相对高强度回波组织与中等强度的心肌之间表现出相对尖锐的强度梯度,以及在心肌与低强度的腔室的血池之间表现出相对较少的梯度。这有利地准许当在不存在对比剂的情况下采集诊断图像时首先辨别外部心肌边界,然后辨别内部心内膜边界。当已经找到边界的坐标,它们被传送到图形生成器66,其生成将所述图像叠加在所计算的位置中的迹线。
图7示出了两幅超声图像,一幅超声图像具有勾勒的在舒张末期的心肌的两个边界(图7a),并且第二幅超声图像具有描记的在收缩末期的两个心肌边界(图7b)。在这些图像中,以黑色描记致密心肌边界,并且以白色描记心内膜边界。利用这样绘制的两个边界,用户利用在控制面板70上的用户控件来控制腔室边界勾画器64来指示在用户希望定位真实腔室边界的两条迹线之间的位置。在一种实施方案中,用户操作单变量控件,通过所述单变量控件,用户能够将真实的心内膜边界定位在偏移先前绘制的心内膜边界与非致密信息和致密信息之间的先前绘制的界面之间的距离的选定百分比的位置处。图8a图示了当单变量控件被设定为0%时图7b的收缩末图像,并且图8b图示了在用户控件被设定为100%的情况下的相同图像,在这种情况下,白线边界被定位在心肌的外部。还通过图1的系统中的图形生成器来产生对用户定义的边界的视觉描记,以用于叠加在超声图像上。用户设定的边界被定位在所测量的正交于心内膜迹线的所需要的位置处,并且被定位在两个边界之间的距离的所需要的百分比处。在这些范例中,出于易于图示的目的,未示出两条心肌边界迹线,其是一种可能的实施方案,但是如果需要的话,也可以示出自动绘制的迹线。
图8c图示了如下情况,其中,用户已经调节了用户定位的边界(被示为白线),使得其是从心内膜迹线朝向致密心肌截面的距离的40%。这是通过在其条102中向左或向右移动滑块100来完成的。在由用户操纵滑块时,用户控制的边界迹线100在心肌的两个边界之间前后移动。在图8c的范例中,滑块100被示为显示屏上的软键控件,其由鼠标或其他用户接口控件来操纵,但是滑动可以替代地是物理滑块、旋钮或开关、或常规超声系统控制面板上的轨迹球。所述用户控件也能够被实施为摇杆控制器、切换按钮、列表框或数值输入框。如果用户针对大多数情况具有优选的百分百,这能够被存储为默认值。在图8c的范例中,数值百分比被显示在屏幕上并且在滑块100移动时改变。在图8d中也示出了所识别的心肌边界的一部分的放大视图104。用户点击左侧的图像的心肌的点,并且心肌的该部分出现在放大视图104中,其中,在心肌边界106(外边界)与108(内边界)之间示出的用户操纵的边界110。在用户操纵滑块100时,边界110在系统绘制的两个边界106与108之间移动。
用户操纵的边界110也能够使用如在放大视图104’中所示的超过100%的范围来定位。用户定义的位置A(110’A)被定位为超出致密心肌边界106’并且以超过100%的范围来表达,而用户定义的位置C(110’C)被定位在心内膜迹线108’内并且以负百分比的范围中来表达。被定位在心内膜与致密心肌边界之间中的用户定义的位置B(110’B)能够以0%与100%之间的范围来表达。
替代地,为了用户方便,用户操纵(定义)的边界能够相对于如在图8d(右侧视图104’的较下方)中图示的三个轮廓而移动:致密心肌边界106’和心内膜边界108”,其分别对应于如与在前面的范例中相同的百分比100%和0%;并且额外的边界109’对应于200%的百分比值,其中,所述额外的边界109’被定位在心外膜边界处。在所图示的范例中,滑块100被调节为在与致密心肌边界106’与心外膜边界109’的用户定义的边界110’位置相对应的150%的值。所述第三边界的替代方案是接近如下事实:存在超出所述致密边界(106’)的另一边界,其是心外膜边界(在该范例中被表达为额外的边界),所述心外膜边界也可以通过超声图像中的可注意和可检测的梯度来表征,其可以被用于限制单自由度的滑块。该心外膜边界也能够通过边界图像处理器来识别。所述滑块是单自由度控件。用户通过设置由滑块控制的单个值来简单地设置全部围绕腔室的边界110的位置。所述值被传送到其他用户,所述其他用户能够通过使用单个数值的值来获得相同的结果。
图9和10图示了本发明的用户定义的心脏腔室能够如何被用于测量诸如心脏输出和射血分数的参数。在图9的透视视图中,在表示二尖瓣平面的基底220上示出了LV的同时采集的双平面的两个用户定义的边界210和212。在230处示出了两个边界的顶部标记。在该范例中,两个双平面图像边界的图像平面正交于彼此。在两个边界210和212内的体积被数学地分成与基平面220平行的间隔的平面222。这些平面如所示地在a,a处与边界210的左侧相交,并且c,c处与边界210的右侧相交。所述平面在b,b处与迹线212的近侧相交。
如在图9中所示,椭圆形被数学地适配到每个平面222的四个相交点a、b、c、d。尽管能够使用曲线或样条而非椭圆形,包括弧形和不规则形状,但是椭圆形提供如下优点:当利用椭圆形来实践时,辛普森方程已经在临床上得到验证。由平面222和椭圆形定义的盘的体积能够通过盘规则来计算以估计LV的体积。
图10示出了构建的三维心脏腔室图像的用户定义的边界的线框模型。所述线框的水平区段232、234、236是边界线,所述边界线在交点a、b、c和d处与垂直边界区段21、212相交。所述水平区段平行于二尖瓣平面基底220。在线框内的体积能够通过经修改的盘计算规则或其他体积估计技术来确定。当如在图9或10中所示的针对收缩末期阶段图像计算的体积被从针对舒张末期图像计算的体积减去并且由其相除时,结果是射血分数估计。
本领域技术人员将容易实现对以上内容的其他变型。替代百分比量化,用户定义的边界能够被定位在距手动或自动跟踪的边界的递增的距离处。能够以距离来校准所述滑块,使得用户定义的边界的位置是例如与参考边界的用户定义的若干毫米的偏移。除了使用两个跟踪的边界之外,能够参考单边界跟踪来定位用户定义的边界,或者能够处在距超过两个边界的内插偏移量处。也能够使用超过100%的范围来定位用户定义的边界;其能够被定位在心内膜迹线内或者能够被定位为超出心外膜或致密心肌边界。
- 通过单自由度腔室分割对心脏功能的超声诊断
- 使用具有用户控制的心脏模型腔室的心脏功能的超声诊断
