BeSO4染毒大鼠血清差异表达蛋白检测与分析方法
文献发布时间:2023-06-19 11:08:20
技术领域
本发明涉及铍暴露所致疾病实验研究领域,特别是一种BeSO
背景技术
铍(Beryllium,Be)是一种天然存在的元素,拥有许多优良性质,被广泛应用于核工业、武器系统、航天航空业、电子信息系统、生物医疗领域。在上述领域中,铍通常是以化合物而非单质的形式存在,暴露于铍化合物中可致急性铍病、铍致敏、慢性铍病、肺癌疾病。
通过检测不难发现,长期处于铍暴露环境(即暴露在含有铍化合物的环境)中的人员,血液和/或支气管肺泡中的T细胞、B细胞大量增殖并发生改变,同时血液中的蛋白质表达的稳态也遭到破坏。
血清是血液中的重要组成成分,血清中物质的改变能在很大程度上揭示血液的变化,甚至预示着疾病的产生。很多情况下疾病的产生可以通过血清中某些物质的变化来反应。
因此,研究血清中蛋白表达谱的变化有助于揭示BeSO
发明内容
本发明的目的是克服现有技术的不足,而提供一种一种BeSO
本发明的技术方案是:BeSO
S01、获取大鼠血清:
a、选10只健康的雄性大鼠,随机分为5只一组的对照组和5只一组的染毒组,分别正常喂水喂食饲养6周,染毒组在第2周滴注0.25ml的BeSO
b、染毒组和对照组共10只大鼠均用乙醚麻醉,再用腹主动脉采血法分别收集血液于10个真空采血管中;
c、将10个真空采血管静置30min,然后对10个真空采血管进行离心处理,使血清和血细胞分层,离心完成后,分别吸取10个真空采血管内的上层血清待用,共得到10份血清;
S02、样品制备:
a、每份血清取60ul,分别加入540ul结合缓冲液,得到10份600ul的稀释血清样本;
b、准备10个分离柱和10个收集管A,将10个分离柱除去上盖后分别放入10个收集管A内,通过分离柱的上端开口向分离柱内部加入0.85ml的结合缓冲液,以激活分离柱内部的吸附材料;
c、将600ul的稀释血清样本加入分离柱内,再向分离柱内加入600ul的结合缓冲液,使稀释血清样本中除了高丰度蛋白之外的蛋白全部被吸附在分离柱内部的吸附材料上,稀释血清样本中的高丰度蛋白从分离柱下端排出并进入收集管A内;
d、准备10个收集管B,使用清洗剂冲洗分离柱内部的吸附材料,将除了高丰度蛋白之外的蛋白冲刷下来,收集到收集管B中;
e、准备10个超滤管,分别测定10个收集管B中溶液的蛋白质浓度,根据每份溶液的蛋白质浓度,在10份溶液中分别取含有150ug蛋白质的溶液量,转移到各超滤管的内管中;
S03、蛋白还原处理:
a、在10个超滤管的内管中分别加入浓度为10mM的DTT溶液,将各超滤管中的溶液量补足至500ul,再对各超滤管进行离心处理,离心处理后,丢弃各超滤管外管中的滤出液;
b、重复b分步骤至少两次,使清洗剂被DTT充分置换掉;
c、将10个超滤管静置1h,使超滤管内管中的蛋白质与DTT充分发生还原反应;
S04、蛋白烷基化处理:
a、在10个超滤管的内管中分别加入浓度为20mM的IAA溶液,将各超滤管中的溶液量补足至500ul;再对各超滤管进行离心处理,离心处理后,丢弃超滤管外管中的滤出液;
b、重复a步骤至少两次,使DTT被IAA充分置换掉;
c、将10个超滤管静置于37℃的孵育箱中避光静置1h,使超滤管内管中的蛋白质与IAA充分发生烷基化反应;
S05、蛋白酶解:
a、在10个超滤管的内管中分别加入浓度为100mM的TEAB溶液,将各超滤管中的溶液量补足至500ul;再对各超滤管进行离心处理,离心处理后,丢弃超滤管外管中的滤出液;
b、重复a步骤至少两次,使IAA被TEAB充分置换掉;
c、准备10个收集管C,将10个超滤管内管中的溶液一一对应的转移至10个收集管C中,分别添加胰蛋白酶至各收集管C中,各收集管C均于37℃的温度下进行酶解反应14-16h;
S06、对蛋白进行TMT标记:
使用TMT标签对酶解后的10个收集管C中的样品进行标记,每管样品使用一个标签,各收集管C均置于37℃的孵育箱中进行标记反应1h,标记反应完成后,各收集管C中分别加入8ul的5%质量浓度的羟胺溶液,静置15min,以终止标记反应;
S07、对样品进行LC-MS/MS检测:
a、将染毒组的5管样品混合为一管,命名为A管,将对照组的5管样品混合为一管,命名为B管,再分别对A管和B管内的溶液进行浓缩干燥,然后在A管和B管内分别加入200ul的0.1%FA溶解干燥浓缩后的样品,之后对A管和B管内的溶液分别进行分组分,各获得45管分馏样品,将所有的分馏样品浓缩蒸干以待后续试验使用;
b、将染毒组的45管浓缩蒸干样品分别命名为C
c、将对照组的45管浓缩蒸干样品分别命名为D
d、将染毒组和对照组共30管溶液于质谱仪进行上机检测,针对检测数据使用UniProt人数据库进行搜索,获得包含蛋白种类、丰度信息和相对分子量的原始数据;
S08、GO和KEGG富集分析:
a、按照P value<0.05、|FC|>1.2的标准,通过Persue软件对原始数据进行筛选,找到差异表达蛋白;
b、基于R语言“clusterProfiler”及“org.Hs.eg.db”两个软件包对差异表达蛋白进行GO富集分析和KEGG富集分析,通过GO富集分析获取差异表达蛋白的生物学功能、分布位置和分子功能,通过KEGG富集分析获取差异表达蛋白参与BeSO
c、从KEGG富集分析得到的多种信号途径中,选出与BeSO
S09、PPI网络图分析:
a、将参与了信号途径的蛋白输入String在线数据库进行检索,将检索结果保存为TSV格式文件;
b、通过Cytoscape软件对TSV格式文件进行可视化分析,绘制出PPI网络图;
c、结合PPI网络图,从参与了信号途径的蛋白中筛选出关键蛋白,所述关键蛋白同时与至少2种蛋白具有相关性。
本发明进一步的技术方案是:S01步骤中,BeSO
本发明进一步的技术方案是:S01步骤中,大鼠的品种为SD大鼠。
本发明再进一步的技术方案是:S01步骤中,真空采血管静置于4℃的冰箱中。
本发明更进一步的技术方案是:S02步骤中,收集管A和收集管B的容量均为15ml;
本发明更进一步的技术方案是:S03步骤中,通过离心处理使小于3Kda的蛋白质进入超滤管外管中,大于3Kda的蛋白质被截留在超滤管内管中。
本发明更进一步的技术方案是:S03步骤中,超滤管静置于37℃的孵育箱中。
本发明更进一步的技术方案是:S05步骤中,每100ug的蛋白质需要添加的胰蛋白酶量为1mg。
本发明更进一步的技术方案是:S06步骤中,收集管C静置于37℃的孵育箱中。
本发明与现有技术相比具有如下优点:
1、利用TMT标记的定量蛋白质组学技术和生物信息学分析技术,一方面实现了快速且高通量的检测BeSO
2、TMT标记的定量蛋白质组学技术,具有灵敏度高、高通量、分离能力强、适应范围广的特点,可获得不同样品间相同肽段的定量信息,为进一步得到蛋白质的定量数据奠定了基础。
以下结合图和实施例对本发明作进一步描述。
附图说明
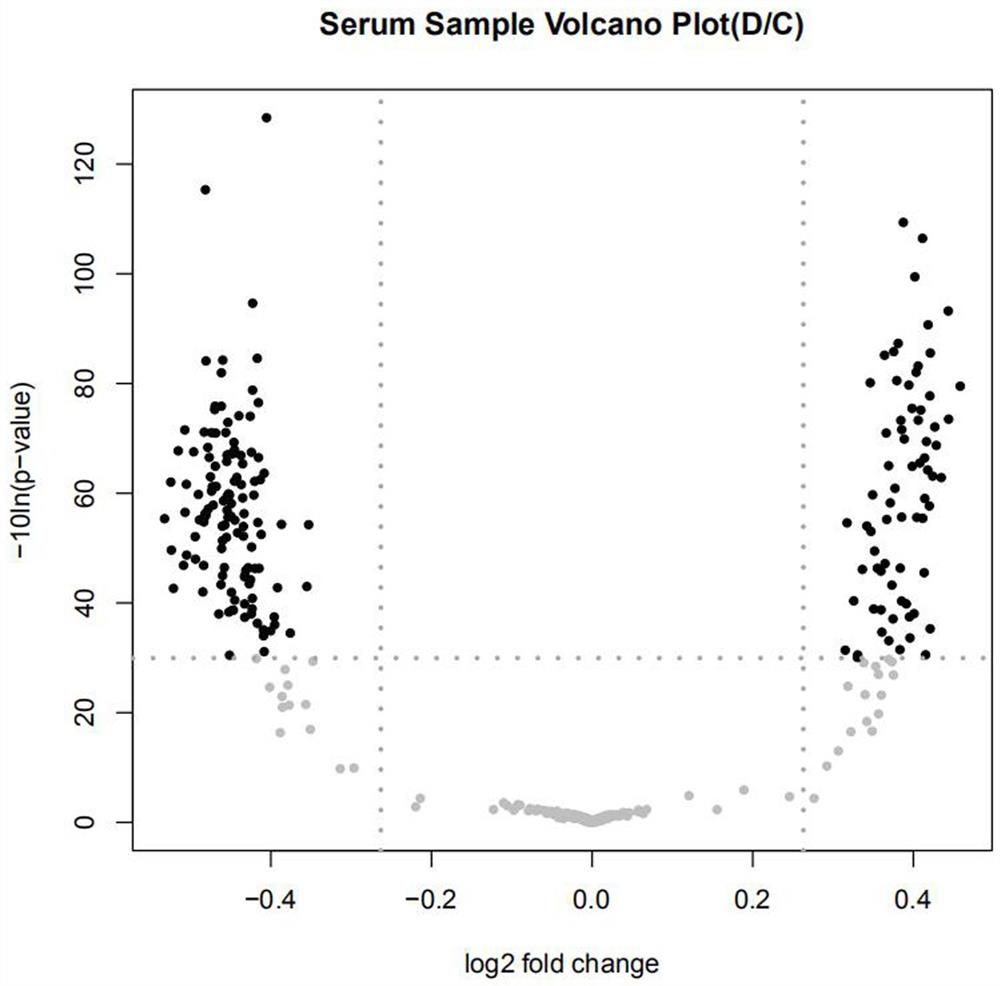
图1为S08步骤中的差异表达蛋白火山图;
图2为S08步骤中的差异表达蛋白聚类热图;
图3为S08步骤中的GO-Cellular Component分析图;
图4为S08步骤中的GO-Biological Process分析图;
图5为S08步骤中的GO-Molecular Function分析图;
图6为S08步骤中的KEGG富集分析图;
图7为S08步骤中的细胞色素P450对异生物代谢信号通路图;
图8为S09步骤中的PPI网络图。
具体实施方式
实施例1:
BeSO
S01、获取大鼠血清:
a、选10只健康的雄性大鼠,随机分为5只一组的对照组和5只一组的染毒组,分别正常喂水喂食饲养6周,染毒组在第2周滴注0.25ml的BeSO
b、染毒组和对照组共10只大鼠均用乙醚麻醉,再用腹主动脉采血法分别收集血液于10个真空采血管中;
c、将10个真空采血管静置30min,然后对10个真空采血管进行离心处理,使血清和血细胞分层,离心完成后,分别吸取10个真空采血管内的上层血清待用,共得到10份血清。
本步骤中,BeSO
本步骤中,大鼠的品种为SD大鼠。
本步骤中,真空采血管静置于4℃的冰箱中。
本步骤中,离心处理的温度为4℃,转速为3500rmp/min,时间为15min。
S02、样品制备:
a、每份血清取60ul,分别加入540ul结合缓冲液,得到10份600ul的稀释血清样本;
b、准备10个分离柱和10个收集管A,将10个分离柱除去上盖后分别放入10个收集管A内,通过分离柱的上端开口向分离柱内部加入0.85ml的结合缓冲液,以激活分离柱内部的吸附材料;
c、将600ul的稀释血清样本加入分离柱内,再向分离柱内加入600ul的结合缓冲液,使稀释血清样本中除了高丰度蛋白之外的蛋白全部被吸附在分离柱内部的吸附材料上,稀释血清样本中的高丰度蛋白从分离柱下端排出并进入收集管A内;
d、准备10个收集管B,使用清洗剂冲洗分离柱内部的吸附材料,将除了高丰度蛋白之外的蛋白冲刷下来,收集到收集管B中;
e、准备10个超滤管,分别测定10个收集管B中溶液的蛋白质浓度,根据每份溶液的蛋白质浓度,在10份溶液中分别取含有150ug蛋白质的溶液量,转移到各超滤管的内管中。
本步骤中,收集管A和收集管B的容量均为15ml。
本步骤中,定义高丰度蛋白为血清中的白蛋白、IgG、IgA、纤维蛋白原、转铁蛋白、触珠蛋白、抗胰蛋白酶,定义低丰度蛋白为血清中除去高丰度蛋白之外的其它蛋白。
S03、蛋白还原处理:
a、在10个超滤管的内管中分别加入浓度为10mM的DTT溶液,将各超滤管中的溶液量补足至500ul,再对各超滤管进行离心处理,离心处理后,丢弃各超滤管外管中的滤出液;
b、重复b分步骤至少两次,使清洗剂被DTT充分置换掉;
c、将10个超滤管静置1h,使超滤管内管中的蛋白质与DTT充分发生还原反应。
本步骤中,通过离心处理使小于3Kda的蛋白质进入超滤管外管中,大于3Kda的蛋白质被截留在超滤管内管中。
本步骤中,离心处理的温度为4℃,转速为14000rpm/min,时间为15min。
本步骤中,超滤管静置于37℃的孵育箱中。
S04、蛋白烷基化处理:
a、在10个超滤管的内管中分别加入浓度为20mM的IAA溶液,将各超滤管中的溶液量补足至500ul;再对各超滤管进行离心处理,离心处理后,丢弃超滤管外管中的滤出液;
b、重复a步骤至少两次,使DTT被IAA充分置换掉;
c、将10个超滤管静置于37℃的孵育箱中避光静置1h,使超滤管内管中的蛋白质与IAA充分发生烷基化反应。
本步骤中,离心处理的温度为4℃,转速为14000rpm/min,时间为15min。
S05、蛋白酶解:
a、在10个超滤管的内管中分别加入浓度为100mM的TEAB溶液,将各超滤管中的溶液量补足至500ul;再对各超滤管进行离心处理,离心处理后,丢弃超滤管外管中的滤出液;
b、重复a步骤至少两次,使IAA被TEAB充分置换掉;
c、准备10个收集管C,将10个超滤管内管中的溶液一一对应的转移至10个收集管C中,分别添加胰蛋白酶至各收集管C中,各收集管C均于37℃的温度下进行酶解反应14-16h。
本步骤中,每100ug的蛋白质需要添加的胰蛋白酶量为1mg。
本步骤中,离心处理的温度为4℃,转速为14000rmp/min,时间为15min。
S06、对蛋白进行TMT标记:
使用TMT标签(标签产品型号为Thermo Scientific™ TMT™ )对酶解后的10个收集管C中的样品进行标记,染毒组的5个收集管C使用一批标签,对照组的5个收集管使用另一批标签,各收集管C均置于37℃的孵育箱中进行标记反应1h,标记反应完成后,各收集管C中分别加入8ul的5%质量浓度的羟胺溶液,静置15min,以终止标记反应。
本步骤中,收集管C静置于37℃的孵育箱中。
S07、对样品进行LC-MS/MS检测:
a、将染毒组的5管样品混合为一管,命名为A管,将对照组的5管样品混合为一管,命名为B管,再分别对A管和B管内的溶液进行浓缩干燥,然后在A管和B管内分别加入200ul的0.1%FA溶解干燥浓缩后的样品,之后对A管和B管内的溶液分别进行分组分,各获得45管分馏样品,将所有的分馏样品浓缩蒸干以待后续试验使用;
b、将染毒组的45管浓缩蒸干样品分别命名为C
c、将对照组的45管浓缩蒸干样品分别命名为D
d、将染毒组和对照组共30管溶液于质谱仪进行上机检测,针对检测数据使用UniProt人数据库进行搜索,提取染毒组被染毒的蛋白质和对照组未被染毒的蛋白质的量化数据到excel表格中,该excel中的数据即为原始数据,原始数据中包含蛋白种类、丰度信息和相对分子量信息。
本步骤中,b、c分步骤不分先后次序。
S08、GO和KEGG富集分析:
a、按照P value<0.05、|FC|>1.2的标准,通过Persue软件对原始数据进行筛选,找到196种差异表达蛋白,其中,显著上调差异蛋白有71种,显著下调差异蛋白有125种;
b、基于R语言“clusterProfiler”及“org.Hs.eg.db”两个软件包对上述的196种差异表达蛋白进行GO富集分析和KEGG富集分析,通过GO富集分析获取差异表达蛋白的生物学功能、分布位置和分子功能,通过KEGG富集分析获取差异表达蛋白参与BeSO
c、从KEGG富集分析得到的多种信号途径中,选出与BeSO
本步骤中,参看图1-2,通过火山图(通过graphpad prism 7软件制作)和聚类热图(通过omicshare云平台制作)更加直观的展示了染毒组和对照组间的差异表达蛋白的分布状况。
本步骤中,参看图3-5,GO富集分析结果显示,差异表达蛋白参与了肌原纤维、肌膜炎、细胞皮层的细胞成分,差异表达蛋白参与了氧化还原辅酶代谢过程、DNA生物合成过程的调控、活性氧代谢过程的生物过程,差异表达蛋白涉及了氧化还原酶活性、乙酰辅酶A C-乙酰转移酶活性、谷胱甘肽结合的分子功能。
本步骤中,参加图6,KEGG富集分析结果显示,BeSO
本步骤中,参看图7,细胞色素P450对异生物代谢信号通路图显示,在5种参与了信号途径的蛋白中,这些蛋白基本参与了整个通路途径。
S09、PPI网络图分析:
a、将参与了信号途径的5种蛋白输入String在线数据库进行检索,将检索结果保存为TSV格式文件;
b、通过Cytoscape软件对TSV格式文件进行可视化分析,绘制出PPI网络图;
c、结合PPI网络图,从参与了“调控细胞色素P450对异生物的代谢”这一信号途径的蛋白中筛选出3种关键蛋白(ADH1、GSTA1、GSTP1),所述关键蛋白同时与至少2种蛋白具有相关性。
本步骤中,参看图8,在5种参与了“调控细胞色素P450对异生物的代谢”信号途径的蛋白中,有3种蛋白与至少两种蛋白具有关联性,分别为ADH1、GSTA1、GSTP1,故被确定为关键蛋白。
本发明提供的方法结合了蛋白质组学技术和生物信息学分析技术,BeSO
- BeSO4染毒大鼠血清差异表达蛋白检测与分析方法
- BeSO4染毒大鼠肺组织差异表达蛋白检测与分析方法
