新的化合物和包含其的有机发光器件
文献发布时间:2023-06-19 10:44:55
技术领域
本申请要求于2018年11月27日向韩国知识产权局提交的韩国专利申请第10-2018-0148563号和于2019年11月14日向韩国知识产权局提交的韩国专利申请第10-2019-0145978号的优先权或权益,其公开内容通过引用整体并入本文。
本公开内容涉及新的化合物和包含其的有机发光器件。
背景技术
通常,有机发光现象是指通过使用有机材料将电能转换为光能的现象。利用有机发光现象的有机发光器件具有诸如宽视角,优异的对比度,快速的响应时间,优异的亮度、驱动电压和响应速度的特性,并因此进行了许多研究。
有机发光器件通常具有包括阳极、阴极和介于阳极与阴极之间的有机材料层的结构。有机材料层通常具有包含不同材料的多层结构以增强有机发光器件的效率和稳定性,例如,有机材料层可以由空穴注入层、空穴传输层、发光层、电子传输层、电子注入层等形成。在有机发光器件的结构中,如果在两个电极之间施加电压,则空穴从阳极注入有机材料层,电子从阴极注入有机材料层,当注入的空穴和电子彼此相遇时,形成激子,并且当激子再落至基态时发光。
持续需要开发用于在如上所述的有机发光器件中使用的有机材料的新材料。
[现有技术文献]
[专利文献]
(专利文献1)韩国未审查专利公开第10-2000-0051826号
发明内容
技术问题
本公开内容的目的是提供新的有机发光材料和包含其的有机发光器件。
技术方案
本公开内容的一个方面提供了由以下化学式1表示的化合物:
[化学式1]
其中,在化学式1中,
X
Ar
其中,
R
各R
a为0至8的整数,
各R
n为0至8的整数。
本公开内容的另一个方面提供了有机发光器件,其包括:第一电极;设置成与第一电极相对的第二电极;以及设置在第一电极与第二电极之间的一个或更多个有机材料层,其中有机材料层的一个或更多个层包含由化学式1表示的化合物。
有益效果
上述由化学式1表示的化合物可以用作有机发光器件的有机材料层的材料,并且可以在有机发光器件中改善效率,实现低驱动电压和/或改善寿命特性。特别地,由化学式1表示的化合物可以用作空穴注入材料、空穴传输材料、空穴注入和传输材料、发光材料、电子传输材料、或电子注入材料。
附图说明
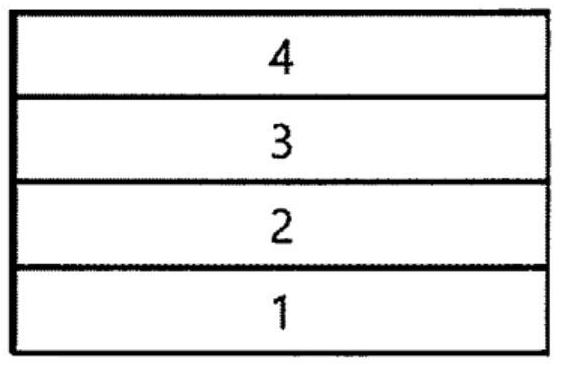
图1示出了包括基底1、阳极2、发光层3和阴极4的有机发光器件的实例。
图2示出了包括基底1、阳极2、空穴注入层5、空穴传输层6、发光层3、空穴阻挡层7、电子传输层8、电子注入层9和阴极4的有机发光器件的实例。
图3示出了包括基底1、阳极2、空穴注入层5、空穴传输层6、电子阻挡层10、发光层3、空穴阻挡层7、电子传输层8、电子注入层9和阴极4的有机发光器件的实例。
具体实施方式
在下文中,将更详细地描述本公开内容的实施方案以促进理解本发明。
本发明的一个实施方案提供了由化学式1表示的化合物。
如本文所用,符号
如本文所用,术语“经取代或未经取代的”意指未经取代或者经选自以下的一个或更多个取代基取代:氘;卤素基团;腈基;硝基;羟基;羰基;酯基;酰亚胺基;氨基;氧化膦基;烷氧基;芳氧基;烷基硫基;芳基硫基;烷基磺酰基;芳基磺酰基;甲硅烷基;硼基;烷基;环烷基;烯基;芳基;芳烷基;芳烯基;烷基芳基;烷基胺基;芳烷基胺基;杂芳基胺基;芳基胺基;芳基膦基;或包含N、O和S原子中的至少一者的杂环基,或者未经取代或者经以上例示的取代基中的两个或更多个取代基连接的取代基取代。例如,“两个或更多个取代基连接的取代基”可以为联苯基。即,联苯基也可以为芳基,并且还可以被解释为两个苯基连接的取代基。
在本说明书中,羰基的碳原子数没有特别限制,但优选为1至40。具体地,羰基可以为具有以下结构式的化合物,但不限于此。
在本说明书中,酯基可以具有其中酯基的氧可以被具有1至25个碳原子的直链、支链或环状烷基,或者具有6至25个碳原子的芳基取代的结构。具体地,酯基可以为具有以下结构式的化合物,但不限于此。
在本说明书中,酰亚胺基的碳原子数没有特别限制,但优选为1至25。具体地,酰亚胺基可以为具有以下结构式的化合物,但不限于此。
在本说明书中,甲硅烷基具体包括三甲基甲硅烷基、三乙基甲硅烷基、叔丁基二甲基甲硅烷基、乙烯基二甲基甲硅烷基、丙基二甲基甲硅烷基、三苯基甲硅烷基、二苯基甲硅烷基、苯基甲硅烷基等,但不限于此。
在本说明书中,硼基具体包括三甲基硼基、三乙基硼基、叔丁基二甲基硼基、三苯基硼基和苯基硼基,但不限于此。
在本说明书中,卤素基团的实例包括氟、氯、溴、或碘。
在本说明书中,烷基可以为直链或支链,并且其碳原子数没有特别限制,但优选为1至40。根据一个实施方案,烷基的碳原子数为1至20。根据另一个实施方案,烷基的碳原子数为1至10。根据另一个实施方案,烷基的碳原子数为1至6。烷基的具体实例包括甲基、乙基、丙基、正丙基、异丙基、丁基、正丁基、异丁基、叔丁基、仲丁基、1-甲基-丁基、1-乙基-丁基、戊基、正戊基、异戊基、新戊基、叔戊基、己基、正己基、1-甲基戊基、2-甲基戊基、4-甲基-2-戊基、3,3-二甲基丁基、2-乙基丁基、庚基、正庚基、1-甲基己基、环戊基甲基、环己基甲基、辛基、正辛基、叔辛基、1-甲基庚基、2-乙基己基、2-丙基戊基、正壬基、2,2-二甲基庚基、1-乙基-丙基、1,1-二甲基-丙基、异己基、2-甲基戊基、4-甲基己基、5-甲基己基等,但不限于此。
在本说明书中,烯基可以为直链或支链,并且其碳原子数没有特别限制,但优选为2至40。根据一个实施方案,烯基的碳原子数为2至20。根据另一个实施方案,烯基的碳原子数为2至10。根据又一个实施方案,烯基的碳原子数为2至6。其具体实例包括乙烯基、1-丙烯基、异丙烯基、1-丁烯基、2-丁烯基、3-丁烯基、1-戊烯基、2-戊烯基、3-戊烯基、3-甲基-1-丁烯基、1,3-丁二烯基、烯丙基、1-苯基乙烯基-1-基、2-苯基乙烯基-1-基、2,2-二苯基乙烯基-1-基、2-苯基-2-(萘基-1-基)乙烯基-1-基、2,2-双(二苯基-1-基)乙烯基-1-基、茋基、苯乙烯基等,但不限于此。
在本说明书中,环烷基没有特别限制,但其碳原子数优选为3至60。根据一个实施方案,环烷基的碳原子数为3至30。根据另一个实施方案,环烷基的碳原子数为3至20。根据又一个实施方案,环烷基的碳原子数为3至6。其具体实例包括环丙基、环丁基、环戊基、3-甲基环戊基、2,3-二甲基环戊基、环己基、3-甲基环己基、4-甲基环己基、2,3-二甲基环己基、3,4,5-三甲基环己基、4-叔丁基环己基、环庚基、环辛基等,但不限于此。
在本说明书中,芳基没有特别限制,但优选具有6至60个碳原子,并且可以为单环芳基或多环芳基。根据一个实施方案,芳基的碳原子数为6至30。根据一个实施方案,芳基的碳原子数为6至20。作为单环芳基,芳基可以为苯基、联苯基、三联苯基等,但不限于此。多环芳基的实例包括萘基、蒽基、菲基、芘基、苝基、
在本说明书中,芴基可以被取代,并且两个取代基可以彼此连接以形成螺环结构。在芴基被取代的情况下,可以形成
在本说明书中,杂环基为包含O、N、Si和S中的一者或更多者作为杂原子的杂环基,并且其碳原子数没有特别限制,但优选为2至60。杂环基的实例包括噻吩基、呋喃基、吡咯基、咪唑基、噻唑基、
在本说明书中,芳烷基、芳烯基、烷基芳基和芳基胺基中的芳基与芳基的前述实例相同。在本说明书中,芳烷基、烷基芳基和烷基胺基中的烷基与烷基的前述实例相同。在本说明书中,杂芳基胺中的杂芳基可以应用杂环基的前述描述。在本说明书中,芳烯基中的烯基与烯基的前述实例相同。在本说明书中,可以应用芳基的前述描述,不同之处在于亚芳基为二价基团。在本说明书中,可以应用杂环基的前述描述,不同之处在于亚杂芳基为二价基团。在本说明书中,可以应用芳基或环烷基的前述描述,不同之处在于烃环不是一价基团而是由两个取代基结合而形成。在本说明书中,可以应用杂环基的前述描述,不同之处在于杂环不是一价基团而是由两个取代基结合而形成。
优选地,X
优选地,X
优选地,Ar
其中,
R
各R
a为0至8的整数。
优选地,R
最优选地,Ar
优选地,R
更优选地,R
优选地,n可以为0或1。
由化学式1表示的化合物的代表性实例如下:
由化学式1表示的化合物可以例如根据如以下反应方案1所示的制备方法来制备,其他剩余的化合物可以以类似的方式来制备。
[反应方案1]
在反应方案1中,X
反应方案1中的第一个反应为Suzuki偶联反应,其优选在钯催化剂和碱的存在下进行,用于Suzuki偶联反应的反应性基团可以如本领域中已知的进行改变。反应方案1中的第二个反应为胺取代反应,其优选在钯催化剂和碱的存在下进行,用于胺取代反应的反应性基团可以如本领域中已知的进行改变。以上制备方法可以在下文描述的制备例中进一步体现。
本发明的另一个实施方案提供了包含上述由化学式1表示的化合物的有机发光器件。作为实例,提供了有机发光器件,其包括:第一电极;设置成与第一电极相对的第二电极;以及设置在第一电极与第二电极之间的一个或更多个有机材料层,其中有机材料层的一个或更多个层包含由化学式1表示的化合物。
本公开内容的有机发光器件的有机材料层可以具有单层结构,或者其可以具有其中堆叠有两个或更多个有机材料层的多层结构。例如,本公开内容的有机发光器件可以具有包括空穴注入层、空穴传输层、发光层、电子阻挡层、电子传输层、电子注入层等作为有机材料层的结构。然而,有机发光器件的结构不限于此,并且其可以包括更少数目的有机材料层。
此外,有机材料层可以包括发光层,其中发光层可以包含由化学式1表示的化合物。
此外,有机材料层可以包括空穴传输层、空穴注入层、或者用于同时进行空穴传输和空穴注入的层,其中空穴传输层、空穴注入层、或者用于同时进行空穴传输和空穴注入的层可以包含由化学式1表示的化合物。
此外,电子传输层、电子注入层、或者用于同时进行电子传输和电子注入的层可以包含由化学式1表示的化合物。
此外,有机材料层包括发光层和空穴传输层,其中发光层或空穴传输层可以包含由化学式1表示的化合物。
此外,根据本公开内容的有机发光器件可以为其中阳极、一个或更多个有机材料层、和阴极顺序地堆叠在基底上的正常型有机发光器件。此外,根据本公开内容的有机发光器件可以为其中阴极、一个或更多个有机材料层、和阳极顺序地堆叠在基底上的倒置型有机发光器件。例如,图1和图2示出了根据本公开内容的实施方案的有机发光器件的结构。
图1示出了包括基底1、阳极2、发光层3和阴极4的有机发光器件的实例。在这样的结构中,由化学式1表示的化合物可以包含在发光层中。
图2示出了包括基底1、阳极2、空穴注入层5、空穴传输层6、发光层3、空穴阻挡层7、电子传输层8、电子注入层9和阴极4的有机发光器件的实例。在这样的结构中,由化学式1表示的化合物可以包含在空穴注入层、空穴传输层、发光层、空穴阻挡层、电子传输层和电子注入层中的一个或更多个层中。
图3示出了包括基底1、阳极2、空穴注入层5、空穴传输层6、电子阻挡层10、发光层3、空穴阻挡层7、电子传输层8、电子注入层9和阴极4的有机发光器件的实例。在这样的结构中,由化学式1表示的化合物可以包含在空穴注入层、空穴传输层、电子阻挡层、发光层、空穴阻挡层、电子传输层和电子注入层中的一个或更多个层中。
根据本公开内容的有机发光器件可以通过本领域已知的材料和方法来制造,不同之处在于有机材料层的一个或更多个层包含由化学式1表示的化合物。此外,当有机发光器件包括复数个有机材料层时,有机材料层可以由相同材料或不同材料形成。
例如,根据本公开内容的有机发光器件可以通过在基底上顺序地堆叠第一电极、有机材料层和第二电极来制造。在这种情况下,有机发光器件可以通过以下来制造:使用PVD(物理气相沉积)法例如溅射法或电子束蒸镀法在基底上沉积金属、具有导电性的金属氧化物、或其合金以形成阳极,在阳极上形成包括空穴注入层、空穴传输层、发光层和电子传输层的有机材料层,然后在有机材料层上沉积可以用作阴极的材料。除了这样的方法之外,有机发光器件还可以通过在基底上顺序地沉积阴极材料、有机材料层和阳极材料来制造。
此外,在制造有机发光器件时,由化学式1表示的化合物可以通过溶液涂覆法以及真空沉积法形成为有机材料层。在本文中,溶液涂覆法意指旋涂、浸涂、刮涂、喷墨印刷、丝网印刷、喷洒法、辊涂等,但不限于此。
除了这样的方法之外,有机发光器件还可以通过在基底上顺序地沉积阴极材料、有机材料层和阳极材料来制造(国际公开WO2003/012890)。然而,制造方法不限于此。
作为实例,第一电极为阳极,第二电极为阴极,或者替代地,第一电极为阴极,第二电极为阳极。
作为阳极材料,通常优选使用具有大功函数的材料,使得空穴可以顺利地注入有机材料层。阳极材料的具体实例包括:金属,例如钒、铬、铜、锌和金,或其合金;金属氧化物,例如氧化锌、氧化铟、氧化铟锡(ITO)和氧化铟锌(IZO);金属和氧化物的组合,例如ZnO:Al或SnO
作为阴极材料,通常优选使用具有小功函数的材料,使得电子可以容易地注入有机材料层。阴极材料的具体实例包括:金属,例如镁、钙、钠、钾、钛、铟、钇、锂、钆、铝、银、锡和铅,或其合金;多层结构材料,例如LiF/Al或LiO
空穴注入层是用于注入来自电极的空穴的层,并且空穴注入材料优选为这样的化合物:其具有传输空穴的能力,因此具有阳极中的空穴注入效应和优异的对发光层或发光材料的空穴注入效应,防止发光层中产生的激子移动至电子注入层或电子注入材料,并且形成薄膜的能力优异。优选地,空穴注入材料的HOMO(最高占据分子轨道)在阳极材料的功函数与周围有机材料层的HOMO之间。空穴注入材料的具体实例包括金属卟啉、低聚噻吩、基于芳基胺的有机材料、基于六腈六氮杂苯并菲的有机材料、基于喹吖啶酮的有机材料、基于苝的有机材料、蒽醌、基于聚苯胺和基于聚噻吩的导电聚合物等,但不限于此。
空穴传输层是接收来自空穴注入层的空穴并将空穴传输至发光层的层,并且其适当地为可以接收来自阳极或空穴注入层的空穴并将空穴转移至发光层的具有大的空穴迁移率的材料。其具体实例包括基于芳基胺的有机材料、导电聚合物、同时存在共轭部分和非共轭部分的嵌段共聚物等,但不限于此。
电子阻挡层是设置在空穴传输层与发光层之间以防止阴极注入的电子转移至空穴传输层而没有在发光层中复合的层,其也可以被称为电子抑制层。电子阻挡层优选为具有比电子传输层小的电子亲和力的材料。
发光材料优选为这样的材料:其可以接收分别从空穴传输层和电子传输层传输的空穴和电子,并使空穴和电子结合以发出可见光区域内的光,并且对荧光或磷光具有良好的量子效率。发光材料的具体实例包括:8-羟基-喹啉铝配合物(Alq
发光层可以包含主体材料和掺杂剂材料。主体材料可以为稠合芳族环衍生物、含杂环的化合物等。稠合芳族环衍生物的具体实例包括蒽衍生物、芘衍生物、萘衍生物、并五苯衍生物、菲化合物、荧蒽化合物等。含杂环的化合物的实例包括咔唑衍生物、二苯并呋喃衍生物、梯子型呋喃化合物、嘧啶衍生物等,但不限于此。特别地,优选地,由化学式1表示的化合物可以作为主体包含在内。
包含由化学式1表示的化合物的有机材料层可以同时包含除了由化学式1表示的化合物之外的化合物。由化学式1表示的化合物与其他化合物的重量比可以为1:99至99:1,更优选为10:90至90:10。
掺杂剂材料的实例包括芳族胺衍生物、苯乙烯胺化合物、硼配合物、荧蒽化合物、金属配合物等。具体地,芳族胺衍生物为经取代或未经取代的具有芳基氨基的稠合芳族环衍生物,并且其实例包括具有芳基氨基的芘、蒽、
空穴阻挡层是设置在电子传输层与发光层之间以防止阳极注入的空穴转移至电子传输层而没有在发光层中复合的层,其也可以被称为空穴抑制层。空穴阻挡层优选为具有大的电离能的材料。
电子传输层是接收来自电子注入层的电子并将电子传输至发光层的层,并且电子传输材料适当地为这样的材料:其可以很好地接收来自阴极的电子并将电子转移至发光层,并且具有大的电子迁移率。电子传输材料的具体实例包括:8-羟基喹啉的Al配合物;包含Alq
电子注入层是注入来自电极的电子的层,并且优选为这样的化合物:其具有传输电子的能力,具有注入来自阴极的电子的效应以及将电子注入发光层或发光材料的优异效应,防止由发光层产生的激子移动至空穴注入层,并且形成薄膜的能力也优异。电子注入层的具体实例包括芴酮、蒽醌二甲烷、联苯醌、噻喃二氧化物、
金属配合物化合物的实例包括8-羟基喹啉锂、双(8-羟基喹啉)锌、双(8-羟基喹啉)铜、双(8-羟基喹啉)锰、三(8-羟基喹啉)铝、三(2-甲基-8-羟基喹啉)铝、三(8-羟基喹啉)镓、双(10-羟基苯并[h]喹啉)铍、双(10-羟基苯并[h]喹啉)锌、双(2-甲基-8-喹啉)氯镓、双(2-甲基-8-喹啉)(邻甲酚)镓、双(2-甲基-8-喹啉)(1-萘酚)铝、双(2-甲基-8-喹啉)(2-萘酚)镓等,但不限于此。
根据使用的材料,根据本公开内容的有机发光器件可以为前侧发射型、后侧发射型、或双侧发射型。
此外,除有机发光器件之外,由化学式1表示的化合物还可以包含在有机太阳能电池或有机晶体管中。
将通过以下实施例更详细地描述本公开内容的具体实施方案。然而,提供这些实施例仅用于举例说明目的,并且本公开内容的范围不限于此。
[制备例]
制备例1:化合物1的制备
1)化合物A1的制备
将2-氯-4-(菲-2-基)-6-苯基-1,3,5-三嗪(15.0g,41mmol)和(3-氯-4-氟苯基)硼酸(7.1g,41mmol)溶解在200mL四氢呋喃中。向其中添加2M碳酸钾溶液(80mL),然后添加四-(三苯基膦)钯(0.47g,0.4mmol),将混合物回流1.5小时。在反应完成之后,将反应混合物冷却至室温,分离并除去水层,用无水硫酸镁干燥,在减压下浓缩,将所得混合物从氯仿和乙醇中重结晶以得到化合物A1(14.0g,产率:74%)。
MS:[M+H]
2)化合物A2的制备
在氮气气氛下将化合物A1(14.0g,30mmol)、双(频哪醇)二硼(8.5g,33mmol)和乙酸钾(5.9g,61mmol)混合,将混合物添加到210ml二
MS:[M+H]
3)化合物A3的制备
在氮气气氛下在圆底烧瓶中将化合物A2(11.9g,22mmol)和2-氯-4,6-二苯基-1,3,5-三嗪(5.8g,22mmol)溶解在160ml四氢呋喃中,然后将碳酸钾(5.9g,43mmol)溶解在90mL水中并添加到其中,然后添加四-(三苯基膦)钯(0.25g,0.2mmol),然后加热并搅拌2小时。将反应温度降至室温,将反应期间产生的固体过滤,用水和四氢呋喃洗涤,然后干燥以得到化合物A3(12.3g,产率:87%)。
MS:[M+H]
4)化合物1的制备
将9H-咔唑(3.1g,18.7mmol)和叔丁醇钾(3.6g,37.4mmol)添加到120mL二甲基甲酰胺中并在搅拌下加热。当开始回流时,向其中添加化合物A3(12.3g,18.7mmol)并回流5小时。将反应温度降至室温,在水中经历反向沉淀并过滤。将滤出物溶解在氯仿中并用水洗涤。分离并除去水层,用无水硫酸镁干燥,然后在减压下浓缩,将所得混合物从四氢呋喃中重结晶以得到化合物1(9.6g,产率:64%)。
MS:[M+H]
制备例2:化合物2的制备
以与制备例1中相同的方式制备化合物2,不同之处在于使用2-氯-4-(9,9-二甲基-9H-芴-2-基)-6-苯基-1,3,5-三嗪代替2-氯-4-(菲-2-基)-6-苯基-1,3,5-三嗪。
MS:[M+H]
制备例3:化合物3的制备
以与制备例1中相同的方式制备化合物3,不同之处在于使用4-(4-氯-6-苯基-1,3,5-三嗪-2-基)-9-苯基-9H-咔唑代替2-氯-4-(菲-2-基)-6-苯基-1,3,5-三嗪。
MS[M+H]
制备例4:化合物4的制备
以与制备例1中相同的方式制备化合物4,不同之处在于使用2-氯-4-(二苯并呋喃-4-基)-6-苯基-1,3,5-三嗪代替2-氯-4-(菲-2-基)-6-苯基-1,3,5-三嗪并使用2-氯-4-苯基-6-(苯基-d
MS[M+H]
制备例5:化合物5的制备
以与制备例1中相同的方式制备化合物5,不同之处在于使用2-氯-4-(萘-2-基)-6-苯基-1,3,5-三嗪代替2-氯-4-(菲-2-基)-6-苯基-1,3,5-三嗪并使用2-([1,1'-联苯]-3-基)-4-氯-6-苯基-1,3,5-三嗪代替2-氯-4,6-二苯基-1,3,5-三嗪。
MS[M+H]
制备例6:化合物6的制备
以与制备例1中相同的方式制备化合物6,不同之处在于使用2-氯-4,6-双(苯基-d
MS[M+H]
制备例7:化合物7的制备
以与制备例1中相同的方式制备化合物7,不同之处在于使用2-氯-4,6-二苯基嘧啶代替2-氯-4-(菲-2-基)-6-苯基-1,3,5-三嗪并使用2-氯-4-(二苯并呋喃-4-基)-6-苯基-1,3,5-三嗪代替2-氯-4,6-二苯基-1,3,5-三嗪。
MS[M+H]
制备例8:化合物8的制备
1)化合物B1的制备
将2-氯-4,6-二苯基-1,3,5-三嗪(50.0g,19mmol)和(3-氯-4-氟苯基)硼酸(32.6g,19mmol)溶解在1000mL四氢呋喃中。向其中添加2M碳酸钾溶液(200mL),然后添加四-(三苯基膦)钯(2.2g,1.9mmol),将混合物回流2小时。在反应完成之后,将反应混合物冷却至室温,分离并除去水层,用无水硫酸镁干燥,然后在减压下浓缩,将所得混合物从氯仿和乙醇中重结晶以得到化合物B1(51.9g,产率:77%)。
MS:[M+H]
2)化合物B2的制备
在氮气气氛下将化合物B1(51.9g,143mmol)、双(频哪醇)二硼(40.1g,158mmol)和乙酸钾(28.1g,287mmol)混合,将混合物添加到950ml二
MS:[M+H]
3)化合物B3的制备
在氮气气氛下在圆底烧瓶中将化合物B2(10.0g,22.1mmol)和2-氯-4-苯基-6-(三亚苯-2-基)-1,3,5-三嗪(9.2g,22.1mmol)溶解在200mL四氢呋喃中,然后将碳酸钾(6.1g,44mmol)溶解在100mL水中并添加到其中,然后添加四(三苯基膦)钯(0.25g,0.2mmol),然后加热并搅拌2小时。将反应温度降至室温,将反应期间产生的固体过滤,用水和四氢呋喃洗涤,然后干燥以得到化合物B3(13.5g,产率:86%)。
MS:[M+H]
4)化合物8的制备
将9H-咔唑(3.2g,19.0mmol)和叔丁醇钾(3.7g,38.1mmol)添加到135mL二甲基甲酰胺中并在搅拌下加热。当开始回流时,向其中添加化合物B3(13.5g,19.0mmol)并回流6小时。将反应温度降至室温,在水中经历反向沉淀并过滤。将滤出物溶解在氯仿中并用水洗涤。分离并除去水层,用无水硫酸镁干燥,然后在减压下浓缩,将所得混合物从四氢呋喃中重结晶以得到化合物8(10.7g,产率:65%)。
MS:[M+H]
制备例9:化合物9的制备
以与制备例8中相同的方式制备化合物9,不同之处在于使用2-氯-4-(二苯并呋喃-3-基)-6-苯基-1,3,5-三嗪代替2-氯-4-苯基-6-(三亚苯-2-基)-1,3,5-三嗪。
MS[M+H]
制备例10:化合物10的制备
以与制备例8中相同的方式制备化合物10,不同之处在于使用2-(4-氯-6-苯基-1,3,5-三嗪-2-基)-9-苯基-9H-咔唑代替2-氯-4-苯基-6-(三亚苯-2-基)-1,3,5-三嗪。
MS[M+H]
制备例11:化合物11的制备
以与制备例8中相同的方式制备化合物11,不同之处在于使用9-(4-氯-6-苯基-1,3,5-三嗪-2-基)-9H-咔唑代替2-氯-4-苯基-6-(三亚苯-2-基)-1,3,5-三嗪。
MS[M+H]
[实施例]
实施例1
将其上涂覆有厚度为
在由此准备的ITO透明电极上,将以下化合物HI-A热真空沉积至
实施例2至11
以与实施例1中相同的方式制造实施例2至11的有机发光器件,不同之处在于使用下表1所示的化合物代替化合物1作为主体材料。
比较例1和2
以与实施例1中相同的方式制造比较例1和2的有机发光器件,不同之处在于使用下表1所示的化合物代替化合物1作为主体材料。在表1中,化合物C1和C2分别如下。
[实验例]
通过向实施例1至11和比较例1至2中制造的有机发光器件施加电流来测量电压、效率和寿命(T95),结果示于下表1中。此时,通过施加10mA/cm
[表1]
如上表1所示,确定与比较例的有机发光器件相比,在使用根据本公开内容的一个实施方案的化合物作为发光层的主体制造的有机发光器件的情况下,其在电压、效率和寿命方面表现出优异的性能。推测这是因为当芳基或杂芳基稠合的环取代基经含氮杂环例如三嗪取代时,对于电子和空穴传输是有利的,并且可以在分子结构方面改善分子的稳定性。此外,当将实施例1与比较例2比较时,确定根据咔唑与三嗪之间是否存在亚苯基连接基而出现电压和寿命的差异。
<附图标记说明>
1:基底 2:阳极
3:发光层 4:阴极
5:空穴注入层 6:空穴传输层
7:空穴阻挡层 8:电子传输层
9:电子注入层 10:电子阻挡层
- 新的有机电致发光器件用化合物及包含该化合物的有机电致发光器件
- 新有机电致发光化合物和包含该化合物的有机电致发光器件
