一种多功能中药有机酸接枝壳聚糖季铵盐广谱抗菌剂及其制备方法
文献发布时间:2023-06-19 12:13:22
技术领域
本发明属于抗菌材料制备技术领域,特别是涉及一种具备抗菌、抗炎和抗氧化等多种功能的中药有机酸接枝壳聚糖季铵盐广谱抗菌剂及其制备方法。
背景技术
自然界中存在着多种有害细菌等微生物,使得人类遭受传染、诱发疾病。随着社会生活水平与科技水平的不断提高,开发一种安全无毒、性能稳定、抗菌性能良好的广谱抗菌剂对人们来说至关重要,尤其是针对食品安全、医用材料领域。传统的抗菌剂主要包括抗生素与金属纳米粒子,这些抗菌剂抗菌性能良好,杀菌作用迅速,反应强烈,被广泛运用于各个抗菌领域。Ye(Ye S.Flexible Amoxicillin-Grafted Bacterial Cellulose Spongesfor Wound Dressing: In Vitro and in Vivo Evaluation.ACS Appl MaterInterfaces.2018,10:5862-5870.)通过在氧化后的细菌纤维素上接枝阿莫西林制备出抗菌敷料。Wei(WeiS.Synthesis and antimicrobial activity of copper nanoparticleloaded regenerated bacterial cellulose membranes.RCS advances.2016,6: 65879-65884.)通过在细菌纤维素上载入铜纳米粒子制备出抗菌材料。但是在应用过程中,这些抗菌剂也存在着一些缺点,例如抗生素容易产生生物抗性,金属纳米粒子常伴随着一定的生物毒性。另一方面,由于使用环境的复杂性,除了抗菌需求外,还需抗炎、抗氧化等性能。因此,开发出一种既有广谱抗菌性能且不易产生生物抗性,同时安全无毒,还具有抗炎、抗氧化等性能的抗菌剂变得尤为重要。
壳聚糖季铵盐(HACC),是通过将壳聚糖(CS)季铵化而得到的一种带有更多正电荷的水溶性多糖衍生物。HACC结构式中大分子主链与CS保持一致,仅通过季铵化引入了季铵盐基团,所以,CS所有的特性,HACC仍旧保留,如CS的成膜性、抗菌性、除湿保湿性、絮凝性、良好的医学特性等等;当然,HACC也保留了所引入的季铵盐的特性,即抗菌性、良好的水溶性、保湿性。
HACC的抗菌机理与壳聚糖相同。然而,在壳聚糖的基础上抗菌性有所增强,其主要原因是HACC所带正电比壳聚糖强,所以其对带有阴离子的细菌吸附力强,增加了细菌的死亡率。但是这也暴露了HACC一个最大的缺陷,即其抗菌机理与属性使得它抗菌的广谱性受到限制,仅针对带有阴离子的革兰氏阳性菌有抗菌作用,而对革兰氏阴性菌则不能表现出很好的抗菌作用,从而使得其抗菌的广谱性受到了极大的限制。由于HACC存在着大量活泼的氨基与羧基,有利于通过物理或者化学改性的方式对其进行修饰,如共混、交联等方法可对 HACC进行功能化。然而共混制备出来的复合物多伴随结构与性能稳定性差,经济成本较大等缺陷。利用交联等其他化学技术手段对HACC进行改性制备过程复杂,化学试剂残留较多,难以产生良好的经济效益。
发明内容
面对现有技术中存在的上述问题,本发明的目的在于提供一种多功能中药有机酸接枝 HACC广谱抗菌剂及其制备方法,制备得到的多功能中药有机酸接枝HACC广谱抗菌剂除了具备抗菌性能外,还包含抗炎、抗氧化中至少一种性能。
第一方面,本发明提供一种多功能中药有机酸接枝壳聚糖季铵盐广谱抗菌剂,包括壳聚糖季胺盐分子以及接枝在壳聚糖季胺盐分子上的中药有机酸,所述壳聚糖季胺盐分子为壳聚糖和季铵盐反应合成的壳聚糖衍生物,所述季铵盐为2,3-环氧丙基三甲基氯化铵、十二烷基二甲基苄基氯化铵、氯丙胺三甲基氯化铵、羟丙基三甲基氯化铵中的至少一种,所述中药有机酸为没食子酸、龙胆酸、丹参酚酸、原儿茶酸、水杨酸、咖啡酸中至少一种;其中按反应原料计,所述壳聚糖季胺盐分子与中药有机酸的质量比为1:(1~4)。
本发明中采用中药有机酸对HACC进行改性,保留了HACC对于革兰氏阳性菌和耐药菌的抗菌性,而且引入了带负电基团例如羧基和/或羟基的中药有机酸,增加了对革兰氏阴性菌的抗菌性,使其具有更加广谱的抗菌性;同时保留了中药有机酸的抗炎、抗氧化性能。
较佳地,所述壳聚糖的分子量为1万~30万;所述壳聚糖季铵盐分子的取代度为15~35%。
较佳地,所述中药有机酸的接枝率为100~200mg PAE/g。
较佳地,所述多功能中药有机酸接枝壳聚糖季铵盐广谱抗菌剂除具备抗菌性能外,还包含抗炎、抗氧化中至少一种性能。
本发明通过工艺优化,选择合适的壳聚糖分子量、壳聚糖季铵盐的取代度、中药有机酸的接枝率、HACC与中药有机酸的质量比等,能够满足共聚物在较高浓度下具有较好抗菌性能的同时,对生物体没有细胞毒性。
第二方面,本发明还提供了上述多功能中药有机酸接枝壳聚糖季铵盐广谱抗菌剂的制备方法,以中药有机酸和壳聚糖季铵盐分子作为反应底物,利用1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐(EDC)与N-羟基琥珀酰亚胺(NHS)作为反应促进剂,合成中药有机酸接枝壳聚糖季铵盐共聚物。
较佳地,所述制备方法还包括:通过透析、离心、洗涤、冷冻干燥对接枝共聚物进一步纯化,得到一种纯净的中药有机酸接枝壳聚糖季铵盐广谱抗菌剂。
较佳地,所述制备方法包括以下步骤:
(1)将中药有机酸溶于无水乙醇中,充分搅拌直到完全溶解,得到溶液A;
(2)将HACC溶解在Tris-HCl缓冲液中,得到溶液B;
(3)将上述溶液A和溶液B混合均匀后,滴加EDC和NHS水溶液,混合均匀;
(4)将步骤(3)得到的混合溶液于室温下反应8~12h;
(5)将步骤(4)所得的反应液进行透析,室温下用去离子水透析1~5天;
(6)将透析后的溶液冷冻干燥。
较佳地,所述HACC、中药有机酸的质量比为1:1~1:4。
较佳地,所述EDC和NHS在反应体系中的浓度分别为2~4mg/ml和0.25~1mg/ml。
较佳地,所述Tris-HCl缓冲液的pH为4~6。
较佳地,所述透析袋的截留分子量为2000~5000。
较佳地,所述冷冻干燥的温度为-50~-30℃,时间为3-5天。
较佳地,所述步骤(4)的反应在恒温摇床中进行,恒温摇床的转速优选为80~150r/min。
本发明中,利用改性剂EDC/NHS使得中药有机酸分子上的羧基和壳聚糖的氨基之间形成酰胺键,本身实际不参与反应,其中间物容易被清洗或者透析除去。而且其合成条件温和、易操作,交联剂无毒性,无残留,还能显著提高HACC的接枝效率和接枝率。
附图说明
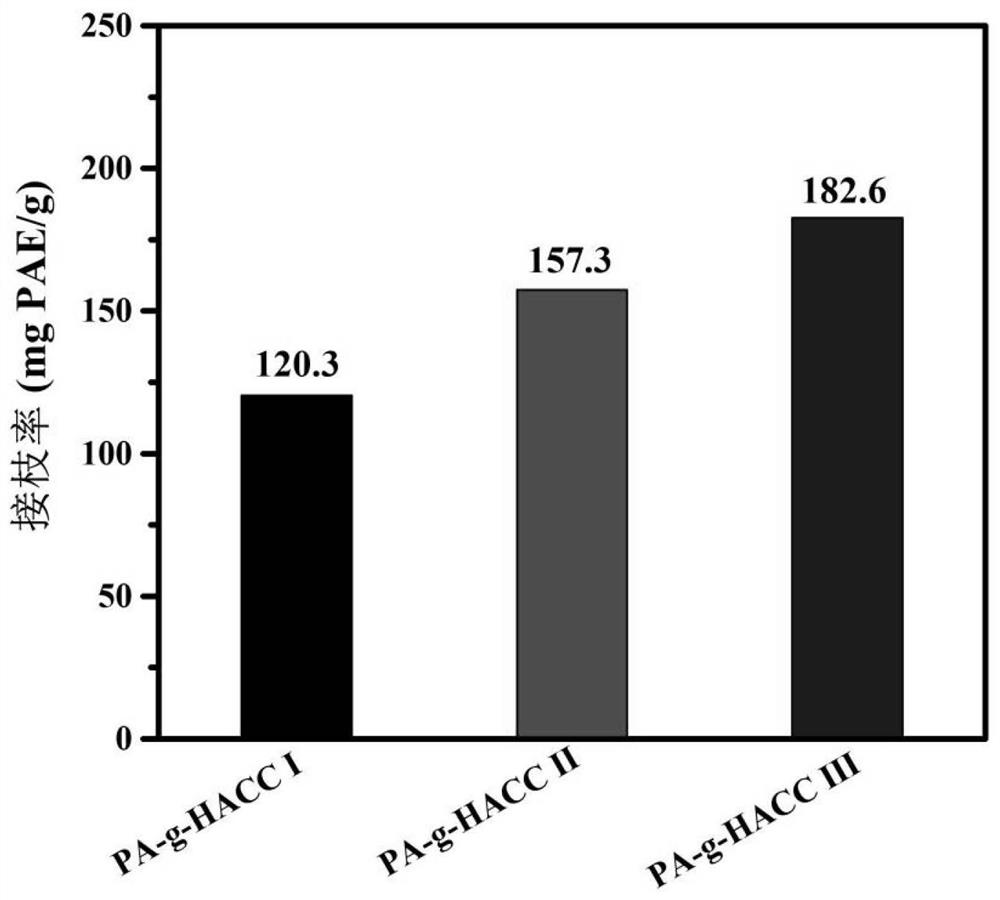
图1示出PA-g-HACC I(实施例1)、PA-g-HACCⅡ(实施例2)、PA-g-HACCⅢ(实施例3)的接枝率;
图2示出HACC、PA-g-HACCⅠ、PA-g-HACCⅡ、PA-g-HACCⅢ、原儿茶酸的FT-IR谱图;
图3示出HACC、PA、PA-g-HACCⅠ、PA-g-HACCⅡ、PA-g-HACCⅢ对DPPH自由基的清除率;
图4示出HACC(a)、PA(b)、PA-g-HACCⅠ(c)、PA-g-HACCⅡ(d)、PA-g-HACCⅢ (e)对大肠杆菌和金黄色葡萄球菌的抗菌率;
图5示出HACC(a)、PA(b)、PA-g-HACCⅠ(c)、PA-g-HACCⅡ(d)、PA-g-HACCⅢ (e)对NIH3T3细胞毒性;
图6从左至右分别示出HACC(a)、PA(b)、PA-g-HACCⅠ(c)、PA-g-HACCⅡ(d)、 PA-g-HACCⅢ(e)对巨噬细胞炎症模型中炎症因子TNF-α、IL1-α含量的影响。
具体实施方式
以下通过下述实施方式进一步说明本发明,应理解,下述实施方式仅用于说明本发明,而非限制本发明。
本发明的目的是提供一种操作简便、成本低、性能好的中药有机酸接枝HACC广谱抗菌剂及其制备方法,且该方法制备所得的中药有机酸接枝HACC广谱抗菌剂抗菌性能更好,抗菌范围得到了进一步的提升。
为实现上述目的,本发明采用如下技术方案:
本发明提供一种中药有机酸接枝HACC广谱抗菌剂的制备方法,包括以下步骤:以中药有机酸和HACC分子作为反应底物,利用EDC/NHS作为引发剂,合成中药有机酸接枝HACC共聚物。一些实施方式中,还通过透析、离心、洗涤、冷冻干燥对接枝共聚物进一步纯化。得到一种纯净的中药有机酸接枝HACC广谱抗菌剂。
可选的,其具体步骤如下:
将中药有机酸溶于无水乙醇中,充分搅拌直到完全溶解,获得中药有机酸溶液。中药有机酸添加质量可为1~4g。所述中药有机酸包括且不限于没食子酸、龙胆酸、丹参酚酸、原儿茶酸、水杨酸、咖啡酸等。
将1g HACC(壳聚糖季胺盐)溶解在Tris-HCl缓冲液中,获得壳聚糖季胺盐溶液。优选地,缓冲液的pH可为5。
将上述两种溶液混合均匀后,滴加EDC和NHS水溶液,混合均匀。一些实施方式中,HACC与中药有机酸的质量比可为1:1~1:4。一些示例中,滴加EDC和NHS以使其在反应体系中的浓度分别为2~4mg/ml和0.25~1mg/ml。其中EDC和NHS在该浓度范围内既可以有效催化反应发生,同时又可以节约原料,减少因过度引入外来试剂而产生的影响。
将上述混合溶液转移至恒温摇床,反应时间8~20h,反应温度可为室温。恒温摇床的转速可为80~150转/分钟。
将所得的反应液进行透析,室温下用去离子水透析1~5天,例如3天。使用的透析袋截留分子量可为2000~5000。
将透析后的溶液冷冻干燥。例如,冷冻干燥的温度可为-50~-30℃,时间可为3~5天。
一些实施方式中,所得中药有机酸接枝HACC广谱抗菌剂的接枝率为100~200mgPAE/g。
本发明的技术方案达到了如下的有益效果:
(a)本发明的制备工艺成熟,方法简便,且投入较少,有利于大规模生产,中间产物及其衍生物无毒无害无污染,对环境友好。与其他对HACC改性的方法相比,该方法操作更加简便,所得中药有机酸接枝HACC广谱抗菌剂原料投入更少,纯化效率更高。
(b)本发明制备方法制得的中药有机酸接枝HACC广谱抗菌剂其物化性质与机械性能稳定,接枝后的产物均保留了两种物质接枝前二者独特的化学性质,如中药有机酸的抗氧化性能、HACC良好的水溶性,同时也对二者的不足进行了相互补充,实现最后所得接枝物优势互补。
(c)本发明制备方法制得的中药有机酸接枝HACC广谱抗菌剂其抗菌性能与其广谱性得到了显著的提高。相较于HACC,中药有机酸接枝HACC广谱抗菌剂对革兰氏阴性菌的抗菌性能得到了显著的提升,同时也保留了HACC对革兰氏阳性菌良好的抗菌效果。同时接枝后的抗菌剂安全无毒,不产生明显的生物毒性,具备作为医疗、卫生等抗菌领域安全有效的抗菌材料,应用范围广泛,产生经济效益高。
本发明所用的HACC为自制的、壳聚糖和季铵盐反应合成的壳聚糖衍生物,其制备方法参考Peng(Peng ZX.Adjustment of the antibacterial activity andbiocompatibility of hydroxypropyltrimethyl ammonium chloride chitosan byvarying the degree of substitution of quaternary ammonium.CarbohydratePolymers.2010,81:275-283.)的文献报道。所述季铵盐为 2,3-环氧丙基三甲基氯化铵、十二烷基二甲基苄基氯化铵、氯丙胺三甲基氯化铵、羟丙基三甲基氯化铵中的至少一种;所述壳聚糖的分子量为1万~30万;季铵盐的取代度为15~36%,该范围取代度的HACC具有良好抗菌性能并无细胞毒性。在实施例中,选用羟丙基三甲基氯化铵作为HACC的合成原材料,壳聚糖分子量为8万,季铵盐取代度为23%。
为了阐明本发明的技术方案及技术目的,下面结合附图及具体实施方式对本发明做进一步的介绍。
实施例1
原儿茶酸接枝壳聚糖季铵盐广谱抗菌剂Ⅰ(PA-g-HACC I)的制备方法,包括以下步骤:
(1)将1g原儿茶酸(PA)溶于1ml无水乙醇中,充分搅拌直到完全溶解,制得原儿茶酸乙醇溶液;
(2)将1gHACC溶解在10ml的Tris-HCl缓冲液(pH=5);
(3)将上述两种溶液混合均匀后,滴加EDC和NHS水溶液,使其在反应体系中的浓度分别为3mg/ml和0.75mg/ml,混合均匀;
(4)将上述混合溶液转移至恒温摇床,室温反应12h,恒温摇床的转速120r/min;
(5)将步骤(4)所得的反应液进行透析,室温下用去离子水透析3天,使用的透析袋截留分子量为3000;
(6)将透析后的溶液冷冻干燥,冷冻干燥的温度为-50℃,时间为3天。
实施例2
原儿茶酸接枝壳聚糖季铵盐广谱抗菌剂Ⅱ(PA-g-HACCⅡ)的制备方法,包括以下步骤:
(1)将3g PA溶于1ml无水乙醇中,充分搅拌直到完全溶解,制得原儿茶酸乙醇溶液;
(2)将1g HACC溶解在10ml的Tris-HCl缓冲液(pH=5);
(3)将上述两种溶液混合均匀后,滴加EDC和NHS水溶液,使其在反应体系中的浓度分别为3mg/ml和0.75mg/ml,混合均匀;
(4)将上述混合溶液转移至恒温摇床,室温反应12h,恒温摇床的转速120r/min;
(5)将步骤(4)所得的反应液进行透析,室温下用去离子水透析3天,使用的透析袋截留分子量为3000;
(6)将透析后的溶液冷冻干燥,冷冻干燥的温度为-50℃,时间为3天。
实施例3
原儿茶酸接枝壳聚糖季铵盐广谱抗菌剂Ⅲ(PA-g-HACCⅢ)的制备方法,包括以下步骤:
(1)将4g PA溶于1ml无水乙醇中,充分搅拌直到完全溶解,制得原儿茶酸乙醇溶液;
(2)将1g HACC溶解在10ml的Tris-HCl缓冲液(pH=5);
(3)将上述两种溶液混合均匀后,滴加EDC和NHS水溶液,使其在反应体系中的浓度分别为3mg/ml和0.75mg/ml,混合均匀;
(4)将上述混合溶液转移至恒温摇床,室温反应12小时,恒温摇床的转速120r/min;
(5)将步骤(4)所得的反应液进行透析,室温下用去离子水透析3天,使用的透析袋截留分子量为3000;
(6)将透析后的溶液冷冻干燥,冷冻干燥的温度为-50℃,时间为3天。
实施例4
对上述实施例中三种PA-g-HACC抗菌剂的接枝率进行比较。其具体方法如下:
采用Folin-Ciocalteu法测定PA-g-HACC的接枝率。准确称取5.0mg充分溶于去离子水中,分别取1.0ml样品溶液与1.0ml Folin-Ciocalteu试剂(预先稀释10倍浓度)充分混合,于37℃下避光反应5min。然后加入5.0ml饱和碳酸氢钠溶液并充分混合,静置2h,以去离子水作为参比溶液在760nm波长处测定溶液吸光度值。实验最终以每克样品中所含原儿茶酸的毫克数(mg PAE/g)表示PA-g-HACC的接枝率。
结果如图1所示。根据绘制PA标准曲线可以得到,PA-g-HACCⅠ、PA-g-HACCⅡ、 PA-g-HACCⅢ的接枝率分别为120.3mg PAE/g、157.3mg PAE/g、182.6mg PAE/g。通过实验说明,在HACC单体质量不变的情况下,PA-g-HACC接枝共聚物的接枝率随着原儿茶酸质量的增大而增大,其可能原因是HACC主链附近的PA分子数量逐渐增大,增加了接枝上主链氨基的几率。
实施例5
对实施例1、2、3中三种PA-g-HACC广谱抗菌剂进行傅里叶红外光谱(FT-IR)分析。
结果如图2所示。HACC分子在3500-3200cm
实施例6
对实施例1、2、3中三种PA-g-HACC广谱抗菌剂的DPPH自由基清除率进行了测定和比较。其具体方法如下:
分别取各组样0.5、1.0、1.5、2.0和2.5mg平铺于24孔板中,取2ml 0.04mmol/LDPPH- 乙醇溶液加入每个孔,室温放置30min,无水乙醇调零,在517nm下测定吸光值,记作A
DPPH清除率的计算公式为:DPPH清除率(%)=[A
测定结果如图3所示,DPPH作为一种相对稳定的自由基,被广泛运用于测定抗氧化剂清除自由基的活性。在不同浓度中下样品PA-g-HACCⅠ、Ⅱ、Ⅲ的自由基清除活性均明显高于HACC(p<0.05),并且随着样品PA-g-HACCⅠ、Ⅱ、Ⅲ浓度的增加,DPPH自由基清除率也逐渐升高。当样品浓度在2.5mg/ml时,各组样品自由基清除活性大小顺序依次为:PA>PA-g-HACCⅢ>PA-g-HACCⅡ>PA-g-HACCⅠ>HACC(p<0.05)。壳聚糖季铵盐自由基清除活性本身不强,但在接枝原儿茶酸后的清除活性得到了显著提高,并且随着原儿茶酸接枝量的增加清除活性逐步增加。这说明,壳聚糖季铵盐在接枝原儿茶酸后,抗氧化活性得到了显著的提高。
实施例7
对实施例1、2、3中三种PA-g-HACC广谱抗菌剂的抑菌率进行了测定和比较。其具体方法如下:
(1)称取胰蛋白胨15g,大豆蛋白胨5g,氯化钠5g溶于1L去离子水中,搅拌至完全溶解;用氢氧化钠将该混合溶液的pH值调节至7.0~7.4之间。121℃高温灭菌30min后取出,作为菌种生长的胰大豆蛋白胨培养基(TSB);
(2)将冻存的菌株(大肠杆菌:ATCC 25922,金黄色葡萄球菌:ATCC 25923)解冻,在超净工作台中,用划线的方法接种于胰大豆蛋白胨培养板上,然后将培养板倒置于37℃细菌培养箱中静置培养;24h后,挑取单个菌落接种于含10ml TSB培养基50ml的离心管中,离心管口用棉球塞紧;将离心管放入恒温摇床进行摇菌,在150rpm、37℃、有氧条件下培养12h;取1ml细菌悬液于1.5ml的离心管中,4℃,5000rpm的条件下离心5min,取出,吸出离心管中的TSB培养基,留沉淀的菌株于离心管中,并用配制好的PBS清洗离心管中的沉淀菌株3次以去除残留的TSB培养基;清洗完成后,加入1ml的PBS将底部沉淀的菌株吹打悬浮,根据麦氏比浊法确定菌悬液的浓度;最后以无菌TSB调整细菌浓度为1×10
(3)将所得的PA-g-HACC广谱抗菌剂溶于TSB培养基,配置为终浓度为2.5mg/ml的 PA-g-HACC广谱抗菌剂溶液;
(4)取步骤(3)中所得的PA-g-HACC广谱抗菌剂溶液1ml加入到无菌的24孔板中,每孔分别接种步骤(2)中的大肠杆菌与金黄色葡萄球菌使得终浓度为200-500CFU/ml。37℃微生物培养箱中培养12h;
(5)取步骤(4)中PA-g-HACC广谱抗菌剂-细菌共混溶液1ml,用无菌PBS溶液稀释10
(6)取步骤(5)中的培养板对其单菌落进行计数。
PA-g-HACC广谱抗菌剂的抗菌率按下面公式计算:抗菌率(%)=(空白组单菌落个数-实验组单菌落个数)/空白组单菌落个数×100%。
测定结果如图4所示,HACC对大肠杆菌的抑菌率仅为14.7±13.2%,表明HACC对大肠杆菌没有抑菌作用;PA对大肠杆菌的抑菌率高达92.9±2.91%;PA-g-HACC广谱抗菌剂Ⅰ、Ⅱ、Ⅲ对大肠杆菌的抑菌率分别为74.9±4.1%、86.7±1.5%、87.6±0.9%,表明接枝 PA后,壳聚糖衍生物对革兰氏阴性菌的抗菌性能得到明显改善。PA-g-HACC广谱抗菌剂Ⅰ、Ⅱ、Ⅲ对金黄色葡萄球菌的抑菌率分别为95.4±1.6%、98.0±1.2%、98.0±0.6%,均高于HACC的92.4±2.4%和PA的87.8±4.9%,表明在PA和HACC的协同作用下,PA-g-HACC 广谱抗菌剂对革兰氏阳性菌的抗菌性能得到了显著提升。实验结果表明,相比HACC, PA-g-HACC具有更好、更广谱的抗菌性能。
实施例8
对实施例1、2、3中PA-g-HACC广谱抗菌剂的细胞毒性进行了测定和比较。其具体方法如下:
将培养好的NIH3T3消化收集并计数,而后用培养基稀释至1×10
测定结果如图5所示,相较于HACC、PA,三种PA-g-HACC广谱抗菌剂表现出良好的细胞相容性,说明在此接枝范围内,该材料对生物无毒害作用。生物毒性作为材料用于医疗、卫生等领域的一个重要指标。结果表明,通过制备一定质量比的PA-g-HACC广谱抗菌剂在抗菌的同时能够有效保护正常细胞不受到毒害,具有作为医疗、卫生等领域的抗菌剂的潜力。
实施例9
对实施例1、2、3中PA-g-HACC广谱抗菌剂对巨噬细胞炎症模型中炎症因子(TNF-α、IL1-α)的含量进行了测定和比较。其具体方法如下:
人外周血单核细胞系THP-1细胞经Phorbol-12-myristate-13-acetate(PMA)诱导1天作为巨噬细胞来源。将培养好的细胞消化收集并计数,而后用培养基稀释至1×10
测定结果如图6所示,原儿茶酸与壳聚糖季铵盐接枝以后,与壳聚糖季铵盐相比,所有PA-g-HACC组均能够显著降低炎症因子的分泌(p<0.05)。并且随着原儿茶酸接枝含量的增加,共培养中两组炎症因子含量逐级下降,并且随着时间的延长能够有效抑制新的炎症因子生成。综上所述,PA-g-HACC系列材料具有较好的抗炎能力,能够在炎症发生的情况下减轻炎症因子的分泌。
以上显示和描述了本发明的基本原理、主要特征和本发明的优点。本行业的技术人员应该了解,本发明不受上述实施例的限制,上述实施例和说明书中描述的只是说明本发明的原理,在不脱离本发明精神和范围的前提下,本发明还会有各种变化和改进,本发明要求保护范围由所附的权利要求书、说明书及其等效物界定。
- 一种多功能中药有机酸接枝壳聚糖季铵盐广谱抗菌剂及其制备方法
- 一种含有机酸盐的壳聚糖季铵盐及其制备方法和应用
