一种花鲈骨骼肌卫星细胞的体外培养方法以及鉴定方法
文献发布时间:2023-06-19 13:49:36
技术领域
本发明属于生物技术领域,尤其涉及一种花鲈骨骼肌卫星细胞的体外培养方法以及鉴定方法。
背景技术
花鲈(Lateolabrax maculatus),俗称鲈鱼、青鲈、寨花、七星鲈等,隶属鲈形目(Perciformes)、脂科(Serranidae)、花鲈属(Lateolabrax),其肉质细嫩、味道鲜美、营养价值高,广受消费者喜爱。在鱼类中,骨骼肌占整个躯体约40%-60%的重量,骨骼肌的生长对鱼类的躯体生长起到决定性的作用。骨骼肌来源于胚胎发育时期由轴旁中胚层发育而来的体节,其基本结构单位为肌纤维。骨骼肌的形成主要经历了胚胎期的肌肉发育过程及胚后期的肌肉生长过程,从肌纤维的层面来看,骨骼肌的形成过程本质上为肌纤维数目的增加(增生)及肌纤维体积的增加(肥大)。卫星细胞作为骨骼肌的祖细胞,被激活后进行增殖,分化,融合等过程,最后发育成有功能的肌纤维。骨骼肌卫星细胞是用于研究肌肉生长发育过程、肌肉损伤与修复机制等相关内容的重要基础材料。
然而,当前关于骨骼肌卫星细胞的培养的报道常见于哺乳动物,而对花鲈骨骼肌卫星细胞的培养存在研究空白。
发明内容
本发明实施例的目的在于提供一种花鲈骨骼肌卫星细胞的体外培养方法以及鉴定方法,旨在解决现有技术对花鲈骨骼肌卫星细胞的培养存在研究空白的问题。
本发明实施例是这样实现的,一种花鲈骨骼肌卫星细胞的体外培养方法,包括:
将经灭菌处理的花鲈肌肉组织块置于含有1%三抗的磷酸盐缓冲盐溶液中进行裁剪处理,并将裁剪处理后的花鲈肌肉组织块转移到第一培养瓶中加入完全培养基进行原代培养;
原代培养生长到70%丰度后进行胰酶消化处理,待90%的细胞质收缩变为圆形时,加入完全培养基终止胰酶消化后,经离心处理收集细胞沉淀,并将所述细胞沉淀与完全培养基按照1∶2的质量比混匀接种至第二培养瓶中以进行细胞传代培养;
将细胞传代培养所得的细胞悬液与冷冻保存液混合过夜后转入液氮中保存,解冻时采用37℃水浴解冻并经离心处理收集细胞沉淀,加入完全培养基重悬所述细胞沉淀,将重悬之后的细胞悬液接种到第三培养瓶中;
当细胞传代培养贴壁生长到70%丰度后,将培养基更换为分化培养基以诱导分化花鲈骨骼肌卫星细胞,对诱导分化培养的花鲈骨骼肌卫星细胞每24h更换一次分化培养基,并记录从单核细胞到融合成多核肌管的过程;
将胰酶消化之后剩余的花鲈肌肉组织块转移到第四培养瓶中,倒置所述第三培养瓶5-6h以使组织块紧密结合在所述第三培养瓶上,随后正置所述第四培养瓶并加入完全培养基进行培养。
本发明实施例的另一目的在于一种花鲈骨骼肌卫星细胞类型和阶段的确定方法,包括:
获取所述体外培养方法所得的诱导分化前骨骼肌卫星细胞和诱导分化后融合成肌管的细胞;
获取所述诱导分化前骨骼肌卫星细胞和诱导分化后融合成肌管的细胞总RNA,并通过反转录试剂盒将RNA反转录为cDNA,以cDNA为模板,以18s rRNA作为内参基因,加入pax7、myod1、myod2、myogenin上下游引物进行PCR扩增以确定细胞类型和阶段;
其中,所述18srRNA基因的特异性引物如SEQ NO.1和SEQ NO.2所示;
所述pax7a引物设计如SEQ NO.3和SEQ NO.4所示;
所述pax7b引物设计如SEQ NO.5和SEQ NO.6所示;
所述myod1引物设计如SEQ NO.7和SEQ NO.8所示;
所述myod2引物设计如SEQ NO.9和SEQ NO.10所示;
所述myogenin引物设计如SEQ NO.11和SEQ NO.12所示。
本发明实施例的另一目的在于一种花鲈骨骼肌卫星细胞分化能力的鉴定方法,包括:
将所述体外培养方法所得的诱导分化72h的骨骼肌卫星细胞经预冷PBS洗涤后,加入4%多聚甲醛固定30min后进行PBS洗涤,用含0.25%Triton X-100的PBS通透化处理20min后进行PBS洗涤,加入0.5mg/ml DAPI染色2min,置于荧光倒置显微镜下观察以确定细胞分化能力。
本发明实施例提供的花鲈骨骼肌卫星细胞的体外培养方法,成功体外分离培养花鲈骨骼肌卫星细胞,经过差速贴壁之后纯度较高,且能传代培养,除此之外能有效地被诱导分化并且融合成多核肌管,最终发育成有功能性的肌纤维。本发明可为了解海水硬骨鱼类肌肉生长发育的分子机制、相关基因的功能验证以及骨骼肌损伤修复方面的研究提供实验材料。
附图说明
图1是本发明实施例提供的原代培养不同天数细胞的生长状态;
图2是本发明实施例提供的原代培养不同代数细胞的生长状态;
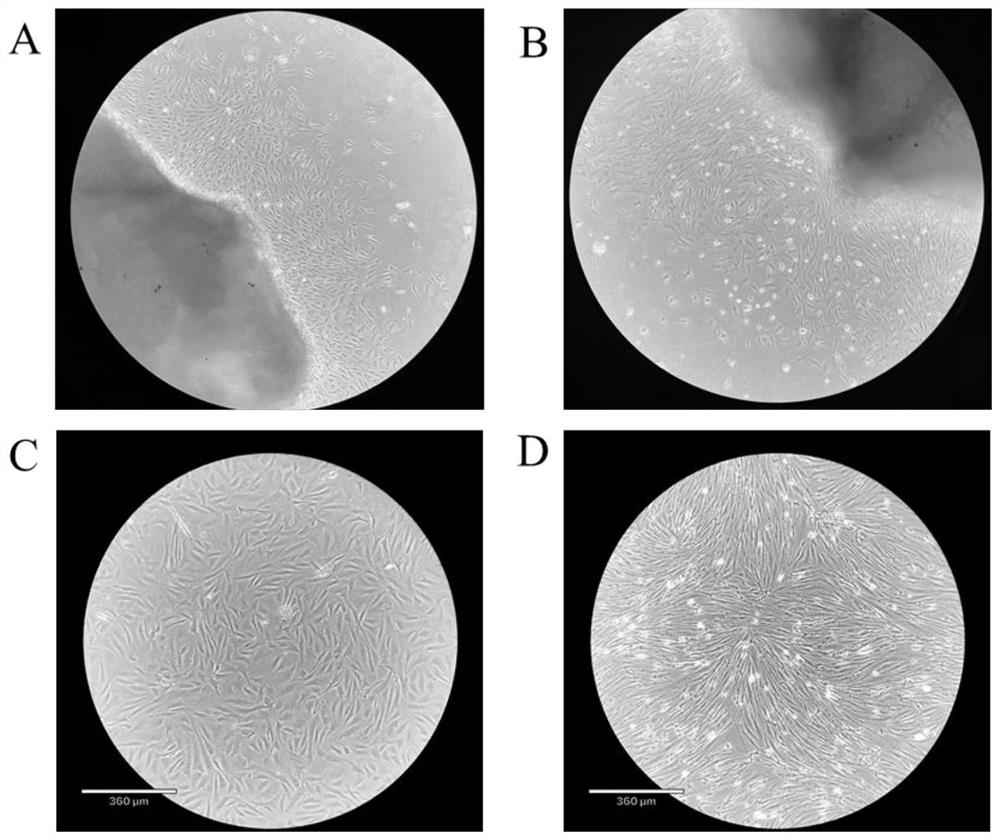
图3是本发明实施例提供的花鲈肌卫星细胞培养不同阶段的状态;
图4是本发明实施例提供的花鲈骨骼肌卫星细胞类型和阶段的鉴定结果;
图5是本发明实施例提供的花鲈肌卫星细胞分化能力的鉴定结果。
具体实施方式
为了使本发明的目的、技术方案及优点更加清楚明白,以下结合实施例,对本发明进行进一步详细说明。应当理解,此处所描述的具体实施例仅仅用以解释本发明,并不用于限定本发明。
本发明实施例为了解决现有技术对花鲈骨骼肌卫星细胞的培养存在研究空白的问题,提供了一种花鲈骨骼肌卫星细胞的体外培养方法,成功体外分离培养花鲈骨骼肌卫星细胞,经过差速贴壁之后纯度较高,且能传代培养,除此之外能有效地被诱导分化并且融合成多核肌管,最终发育成有功能性的肌纤维。本发明可为了解海水硬骨鱼类肌肉生长发育的分子机制、相关基因的功能验证以及骨骼肌损伤修复方面的研究提供实验材料。
本发明实施例提供了一种花鲈骨骼肌卫星细胞的体外培养方法,包括:
将经灭菌处理的花鲈肌肉组织块置于含有1%三抗的磷酸盐缓冲盐溶液中进行裁剪处理,并将裁剪处理后的花鲈肌肉组织块转移到第一培养瓶中加入完全培养基进行原代培养;
原代培养生长到70%丰度后进行胰酶消化处理,待90%的细胞质收缩变为圆形时,加入完全培养基终止胰酶消化后,经离心处理收集细胞沉淀,并将所述细胞沉淀与完全培养基按照1∶2的质量比混匀接种至第二培养瓶中以进行细胞传代培养;
将细胞传代培养所得的细胞悬液与冷冻保存液混合过夜后转入液氮中保存,解冻时采用37℃水浴解冻并经离心处理收集细胞沉淀,加入完全培养基重悬所述细胞沉淀,将重悬之后的细胞悬液接种到第三培养瓶中;
当细胞传代培养贴壁生长到70%丰度后,将培养基更换为分化培养基以诱导分化花鲈骨骼肌卫星细胞,对诱导分化培养的花鲈骨骼肌卫星细胞每24h更换一次分化培养基,并记录从单核细胞到融合成多核肌管的过程;
将胰酶消化之后剩余的花鲈肌肉组织块转移到第四培养瓶中,倒置所述第三培养瓶5-6h以使组织块紧密结合在所述第三培养瓶上,随后正置所述第四培养瓶并加入完全培养基进行培养。
在本发明实施例中,所述三抗是由10000units/mL青霉素、10mg/mL链霉素以及1250units/mL制霉素组成。
在本发明实施例中,所述完全培养基包括质量比1%三抗、10ng/mL bFGF、20%胎牛血清以及L-15基础培养基。
在本发明实施例中,所述分化培养基包括质量比1%三抗、2%马血清以及L-15基础培养基。
在本发明实施例中,所述胰酶的质量分数为0.25%。
在本发明实施例中,所述离心速度为2000rpm,离心时间为5min。
本发明实施例还提供了一种花鲈骨骼肌卫星细胞类型和阶段的确定方法,包括:
获取上述体外培养方法所得的诱导分化前骨骼肌卫星细胞和诱导分化后融合成肌管的细胞;
获取所述诱导分化前骨骼肌卫星细胞和诱导分化后融合成肌管的细胞总RNA,并通过反转录试剂盒将RNA反转录为cDNA,以cDNA为模板,以18s rRNA作为内参基因,加入pax7、myod1、myod2、myogenin上下游引物进行PCR扩增以确定细胞类型和阶段;
其中,所述18srRNA基因的特异性引物如SEQ NO.1和SEQ NO.2所示;
所述pax7a引物设计如SEQ NO.3和SEQ NO.4所示;
所述pax7b引物设计如SEQ NO.5和SEQ NO.6所示;
所述myod1引物设计如SEQ NO.7和SEQ NO.8所示;
所述myod2引物设计如SEQ NO.9和SEQ NO.10所示;
所述myogenin引物设计如SEQ NO.11和SEQ NO.12所示。
在本发明实施例中,所述PCR体系为5uL Mix(Vazyme,P213-01),pax7a、pax7b、myod1、myod2、myogenin上下游引物各0.4uL,1uL cDNA,加水补至10uL。
在本发明实施例中,所述扩增条件为95℃预变性3min,95℃变性15s,60℃退火20s,72℃延伸30s,循环35次,72℃延伸5min,4℃保存。
本发明实施例还提供了一种花鲈骨骼肌卫星细胞分化能力的鉴定方法,包括:
将上述体外培养方法所得的诱导分化72h的骨骼肌卫星细胞经预冷PBS洗涤后,加入4%多聚甲醛固定30min后进行PBS洗涤,用含0.25%Triton X-100的PBS通透化处理20min后进行PBS洗涤,加入0.5mg/ml DAPI染色2min,置于荧光倒置显微镜下观察以确定细胞分化能力。
以下给出本发明某些实施方式的实施例,其目的不在于对本发明的范围进行限定。
实施例1
本实施例中,花鲈骨骼肌卫星细胞的培养具体步骤如下:
1)细胞的原代培养:①将用于取样的花鲈个体浸于75%乙醇30s,随后取花鲈侧线上方,背鳍下方小块肌肉,移入装有含4%三抗(BI,no.PB180424)PBS(Biosharp,BL601A)的50ml无菌离心管中。将组织块转移到含75%乙醇的无菌50ml离心管中浸泡30s,依次过含4%、3%、2%、1%三抗PBS的50ml离心管,每次浸泡5min,期间晃动离心管,使组织块和PBS充分接触、灭菌;②将组织块移到装有含1%三抗PBS的容器中;将组织块剪为约1mm
2)细胞的传代培养:①原代细胞生长到70%丰度时即可进行传代,采用差速贴壁法纯化骨骼肌卫星细胞,分离出的细胞在培养箱中预培养2h,此时贴壁细胞主要为成纤维细胞,然后将未贴壁细胞转入新的培养瓶中培养,可重复此操作2-3次。②传代中用到的包括L-15培养基、胰酶(Gibco,no.12605-028)、血清在内的试剂应在25℃培养箱中预热;③传代具体步骤:先弃去培养瓶中的旧培养基,用预热的无菌PBS洗涤1-2次,加入1ml 0.25%的胰酶,显微镜下观察细胞的状态,待90%的细胞胞质收缩变为圆形时,用手轻拍培养瓶使大部分细胞脱落,然后加入完全培养基终止胰酶消化,用枪头反复吹打细胞悬液,2000r/min离心5min,弃上清以去除胰酶,进而消除对细胞的影响,用完全培养基重悬细胞沉淀,按照1∶2的比例接种于新的细胞培养瓶中,每次传代均利用差速贴壁法去除成纤维细胞。
3)细胞的冻存与复苏:
①细胞冷冻保存液为含20%DMSO(Solarbio,D8371)、30%胎牛血清的L-15培养基,使用前4℃预冷,细胞利用步骤2)收集之后,将细胞悬液与冻存液1∶1混合之后,于4℃保存1h,-20℃保存3h,然后于-80℃冰箱过夜,之后转入液氮中长期保存;②细胞解冻时采用37℃水浴锅快速解冻,待冻存管中冰块将要融化时停止水浴,离心收集细胞,以去除DMSO,加入新鲜完全培养基重悬细胞沉淀,将重悬之后的细胞悬液接种到细胞培养瓶中。
4)细胞的诱导分化:①肌卫星细胞传代培养贴壁生长到70%丰度后,将培养基更换为分化培养基(含2%马血清(G-CLONE,CF1020)、1%三抗的L-15培养基),诱导分化花鲈骨骼肌卫星细胞,24h后有细胞开始融合;48h有较多细胞开始融合;72h有大量细胞开始融合,出现双核肌管;96h时细胞融合程度加深,出现多核肌管。②对诱导分化培养的骨骼肌卫星细胞每24h更换一次新鲜分化培养基,记录从单核细胞到融合成多核肌管的过程。图2为组织块重新贴壁后,原代培养不同代数细胞的生长状态,即细胞增殖阶段和成肌诱导分化不同阶段的生长状态。
5)组织块的重新贴壁培养:将步骤2)消化之后剩余的组织块转移到新的培养瓶中,均匀摆放,间隔0.5cm,倒置细胞培养瓶5-6h,使组织块紧密结合在细胞培养瓶上,随后正置细胞培养瓶,加入完全培养基继续培养,2-3天即可见细胞迁出并达到70%的丰度,可进一步传代培养。将组织块重新贴壁的方法迁出卫星细胞的速度明显快于初次培养的组织块。图3为组织块重新贴壁后,花鲈肌卫星细胞培养不同阶段的状态(A:细胞增殖(P)阶段:24h、48h、72h,B:细胞诱导分化(D)阶段:24h、48h、72h、96h)。
实施例2花鲈骨骼肌卫星细胞类型和阶段的鉴定方法
实施例1所培养的细胞类型的鉴定方法,本实施例收取诱导分化前肌卫星细胞和诱导分化后融合成肌管的细胞,采用trizol法(Vazyme,R401-01),提取两个阶段细胞总RNA,通过反转录试剂盒(Vazyme,P611-01),把1ug细胞RNA反转录为cDNA,通过扩增骨骼肌卫星细胞的标志基因pax7和增殖阶段的标志基因myod1、myod2以及分化阶段的标志基因myogenin来确定细胞类型和阶段,PCR体系为5uL Mix(Vazyme,P213-01),pax7a、pax7b、myod1、myod2、myogenin上下游引物各0.4uL,1uL cDNA,加水补至10uL,随后进行PCR扩增,扩增条件为95℃预变性3min,95℃变性15s,60℃退火20s,72℃延伸30s,循环35次,72℃延伸5min,4℃保存;PCR产物电泳检测后拍照记录。18s rRNA作为内参基因。RT-PCR结果显示,在诱导分化前,肌卫星细胞静止期和增殖期标志基因pax7和myod1、myod2呈阳性表达(图4A,其中,花鲈肌卫星细胞未分化阶段标志基因RT-PCR检测标注:M,2KB DNA标志;1,pax7a基因;2,pax7b基因;3,myod1基因;4,myod2基因;5,myogenin基因;6,18s内参基因),而且pax7表达水平明显高于myod1、myod2的表达水平,这可能是由于此阶段的肌卫星细胞刚分离培养不久,大部分细胞处于静止期,少部分细胞进入了增殖期。在肌卫星细胞诱导分化72h之后,分化阶段标志基因myogenin表达水平明显高于增殖期标志基因myod1、myod2的表达水平,这说明本发明分离的骨骼肌卫星细胞具备良好的体外成肌诱导分化能力(图4B,其中,花鲈肌卫星细胞诱导分化72h之后标志基因-RT-PCR检测标注:M,2KB DNA标志;1,myod1基因;2,myod2基因;3,myogenin基因;4,18s内参基因)。
其中,所述的细胞类型鉴定所使用的引物序列如下表1所示:
表1细胞类型鉴定所使用的引物序列图表
实施例3花鲈骨骼肌卫星细胞分化能力的鉴定方法
鉴定获得的传代细胞分化能力的方法:将诱导分化72h的细胞经PBS洗1-2次后,加入4%多聚甲醛固定30min,PBS洗涤5min×3次,用含0.25%Triton X-100(Solarbio,T8200)的PBS通透化处理20min,PBS洗涤5min×3次,加入0.5mg/ml DAPI(Solarbio,C0065)染色2min,置于荧光倒置显微镜下观察。可以看到出现多核肌细胞,说明培养的肌卫星细胞具备的良好的体外成肌诱导分化能力(图5,其中,A为花鲈肌卫星细胞诱导分化72h的光镜图,B为花鲈肌卫星细胞诱导分化72h的DAPI染色图)。拍照仪器为Echo Revolve荧光显微镜。
以上所述实施例仅表达了本发明的几种实施方式,其描述较为具体和详细,但并不能因此而理解为对本发明专利范围的限制。应当指出的是,对于本领域的普通技术人员来说,在不脱离本发明构思的前提下,还可以做出若干变形和改进,这些都属于本发明的保护范围。因此,本发明专利的保护范围应以所附权利要求为准。
以上所述仅为本发明的较佳实施例而已,并不用以限制本发明,凡在本发明的精神和原则之内所作的任何修改、等同替换和改进等,均应包含在本发明的保护范围之内。
序列表
<110> 中国海洋大学
<120> 一种花鲈骨骼肌卫星细胞的体外培养方法以及鉴定方法
<141> 2021-09-23
<160> 12
<170> SIPOSequenceListing 1.0
<210> 1
<211> 25
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 1
cgcacggatg atggttcaga tgtag 25
<210> 2
<211> 27
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 2
ctggtgtaga tgtctgggta atgtgtc 27
<210> 3
<211> 18
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 3
agtcggacca cgttcaca 18
<210> 4
<211> 18
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 4
tggtagacgg aggtagcg 18
<210> 5
<211> 23
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 5
acaccagcga catgcacttc ttc 23
<210> 6
<211> 23
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 6
gaggaggagg aggaggagga agg 23
<210> 7
<211> 22
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 7
aagtcagagg accatcttca cc 22
<210> 8
<211> 19
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 8
cctcatcgtt gctgctttc 19
<210> 9
<211> 22
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 9
tccatccagc ctgtcacctc ac 22
<210> 10
<211> 24
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 10
accttcttca gacgcctctt ctcc 24
<210> 11
<211> 20
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 11
gagaaacggc taccacatcc 20
<210> 12
<211> 22
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 12
gatacgctca ttccgattac ag 22
- 一种花鲈骨骼肌卫星细胞的体外培养方法以及鉴定方法
- 山羊骨骼肌卫星细胞体外培养方法
