心电数据处理方法及装置
文献发布时间:2023-06-19 18:32:25
技术领域
本公开涉及数据处理领域,尤其涉及一种心电数据处理方法及装置。
背景技术
癫痫作为一种疾病会影响患者的生活,大部分患者可以用一种或多种药物联合治疗对癫痫发作情况加以控制,但仍然会有部分患者对药物治疗并不敏感,这些患者被称为药物难治性癫痫患者。一些特定的医学处置,例如迷走神经刺激(vagus nervestimulation,VNS)手术,可以对药物难治性癫痫患者的癫痫发作情况实现有效控制,但特定的医学处置应用于不同个体时,治疗效果的差异很大,并且治疗效果的优劣具有很高的不确定性。据统计分析结果显示,针对接受特定的医学处置的患者在治疗前后的癫痫发作情况,仅有约5%-9%的患者的癫痫发作情况得到完全控制,约10%的患者的癫痫发作情况完全没有改善,其余患者的癫痫发作情况表现为不同程度的发作频率降低。总体而言,在接受特定的医学处置后,约50%-60%的药物难治性癫痫患者可以达到癫痫发作频率降低至治疗前的一半以下的效果。
预测患者是否适合接受特定的医学处置,例如针对采用迷走神经刺激的治疗手段治疗药物难治性癫痫患者的治疗效果的不确定性和个体差异大的问题,通过术前评估手段来预测患者是否适合接受迷走神经刺激手术,成为相关领域的研究热点。
发明内容
有鉴于此,本公开提出了一种心电数据处理方法及装置,根据本申请实施例的心电数据处理方法,可以提高目标对象对特定的医学处置的适应性的预测准确度。
根据本公开的一方面,提供了一种心电数据处理方法,包括:采集目标对象的心电数据;根据所述目标对象的心电数据,确定第一特征向量,所述第一特征向量包括由所述目标对象的心电数据确定的多个心率变异性指标;将所述第一特征向量输入训练好的预测模型,得到预测结果,其中,预测结果表示所述目标对象是否适合接受特定的医学处置。
在一种可能的实现方式中,所述目标对象的心电数据包括清醒状态的心电数据和睡眠状态的心电数据,根据所述目标对象的心电数据,确定第一特征向量,包括:根据所述目标对象的心电数据,确定所述目标对象的清醒状态下的RR间期序列以及睡眠状态下的RR间期序列;根据所述目标对象的清醒状态下的RR间期序列以及睡眠状态下的RR间期序列,得到所述第一特征向量。
在一种可能的实现方式中,根据所述目标对象的清醒状态下的RR间期序列以及睡眠状态下的RR间期序列,得到所述第一特征向量,包括:确定作为所述训练好的预测模型的输入的多个指标类型;根据所述目标对象的清醒状态下的RR间期序列以及睡眠状态下的RR间期序列,确定与所述多个指标类型对应的所述多个心率变异性指标;根据所述多个心率变异性指标,得到所述第一特征向量。
在一种可能的实现方式中,所述预测模型根据样本对象的心电数据训练得到,所述方法还包括:根据所述样本对象的心电数据,确定所述样本对象的多个心率变异性指标;根据所述样本对象接受所述特定的医学处置后的效果,将所述效果满足预设条件的样本对象的多个心率变异性指标确定为正样本,将所述效果不满足预设条件的样本对象的多个心率变异性指标确定为负样本;对所述正样本和所述负样本进行差异显著性分析,得到具有显著性差异的心率变异性指标,其中正样本和负样本的具有显著性差异的心率变异指标之间的差别大于阈值;对所述具有显著性差异的心率变异性指标进行重要性排序,得到第二特征向量;根据所述样本对象的多个心率变异性指标中,与所述第二特征向量中的指标类型相同的指标,训练得到所述预测模型。
在一种可能的实现方式中,对所述具有显著性差异的心率变异性指标进行重要性排序,得到第二特征向量,包括:根据所有具有显著性差异的心率变异性指标,得到特征子集,确定预测模型对所述特征子集的预测准确率;判断当前特征子集是否为空集;在所述当前特征子集为空集时,按照预测准确率最高的一个特征子集中的心率变异性指标的重要性评分,对所述预测准确率最高的一个特征子集中的心率变异性指标进行重要性排序,得到第二特征向量。
在一种可能的实现方式中,对所述具有显著性差异的心率变异性指标进行重要性排序,得到第二特征向量,还包括:在所述当前特征子集不为空集时,重复以下操作:将所述当前特征子集输入预设的随机森林模型,得到所述当前特征子集中的每个心率变异性指标的重要性评分;消除所述当前特征子集中,至少一个重要性评分最低的心率变异性指标,所述当前特征子集中剩余的心率变异性指标的集合,作为新的当前特征子集,确定预测模型对当前特征子集的预测准确率;重新判断当前特征子集是否为空集。
在一种可能的实现方式中,根据所述样本对象的多个心率变异性指标中,与所述第二特征向量中的指标类型相同的指标,训练得到所述预测模型,包括:根据所述第二特征向量中的不同指标,排列组合得到多个第三特征向量,其中,不同的第三特征向量中的指标的组合不同,或者,不同的第三特征向量中的指标的组合以及指标在第三特征向量中的排序不同;计算分别以所述样本对象的多个心率变异性指标中,与多个第三特征向量中的指标类型相同的指标作为所述预测模型的输入时,所述预测模型的预测准确度;根据预测准确度最高的第三特征向量确定预测模型的输入指标类型,得到训练好的预测模型。
在一种可能的实现方式中,所述样本对象的心电数据包括清醒状态的心电数据和睡眠状态的心电数据,根据所述样本对象的心电数据,确定所述样本对象的多个心率变异性指标,包括:根据所述样本对象的心电数据,确定所述样本对象的清醒状态下的RR间期序列以及睡眠状态下的RR间期序列;根据所述样本对象的清醒状态下的RR间期序列以及睡眠状态下的RR间期序列,确定与预设的多个指标类型对应的所述多个心率变异性指标,所述样本对象的多个心率变异性指标包括至少一个时域心率变异性指标、至少一个频域心率变异性指标、以及至少一个非线性心率变异性指标中的一个或多个。
根据本公开的另一方面,提供了一种心电数据处理装置,包括:采集模块,用于采集目标对象的心电数据;确定模块,用于根据所述目标对象的心电数据,确定第一特征向量,所述第一特征向量包括由所述目标对象的心电数据确定的多个心率变异性指标;预测模块,用于将所述第一特征向量输入训练好的预测模型,得到预测结果,其中,预测结果表示所述目标对象是否适合接受特定的医学处置。
在一种可能的实现方式中,所述目标对象的心电数据包括清醒状态的心电数据和睡眠状态的心电数据,根据所述目标对象的心电数据,确定第一特征向量,包括:根据所述目标对象的心电数据,确定所述目标对象的清醒状态下的RR间期序列以及睡眠状态下的RR间期序列;根据所述目标对象的清醒状态下的RR间期序列以及睡眠状态下的RR间期序列,得到所述第一特征向量。
在一种可能的实现方式中,根据所述目标对象的清醒状态下的RR间期序列以及睡眠状态下的RR间期序列,得到所述第一特征向量,包括:确定作为所述训练好的预测模型的输入的多个指标类型;根据所述目标对象的清醒状态下的RR间期序列以及睡眠状态下的RR间期序列,确定与所述多个指标类型对应的所述多个心率变异性指标;根据所述多个心率变异性指标,得到所述第一特征向量。
在一种可能的实现方式中,所述预测模型根据样本对象的心电数据训练得到,所述方法还包括:根据所述样本对象的心电数据,确定所述样本对象的多个心率变异性指标;根据所述样本对象接受所述特定的医学处置后的效果,将所述效果满足预设条件的样本对象的多个心率变异性指标确定为正样本,将所述效果不满足预设条件的样本对象的多个心率变异性指标确定为负样本;对所述正样本和所述负样本进行差异显著性分析,得到具有显著性差异的心率变异性指标,其中正样本和负样本的具有显著性差异的心率变异指标之间的差别大于阈值;对所述具有显著性差异的心率变异性指标进行重要性排序,得到第二特征向量;根据所述样本对象的多个心率变异性指标中,与所述第二特征向量中的指标类型相同的指标,训练得到所述预测模型。
在一种可能的实现方式中,对所述具有显著性差异的心率变异性指标进行重要性排序,得到第二特征向量,包括:根据所有具有显著性差异的心率变异性指标,得到特征子集,确定预测模型对所述特征子集的预测准确率;判断当前特征子集是否为空集;在所述当前特征子集为空集时,按照预测准确率最高的一个特征子集中的心率变异性指标的重要性评分,对所述预测准确率最高的一个特征子集中的心率变异性指标进行重要性排序,得到第二特征向量。
在一种可能的实现方式中,对所述具有显著性差异的心率变异性指标进行重要性排序,得到第二特征向量,还包括:在所述当前特征子集不为空集时,重复以下操作:将所述当前特征子集输入预设的随机森林模型,得到所述当前特征子集中的每个心率变异性指标的重要性评分;消除所述当前特征子集中,至少一个重要性评分最低的心率变异性指标,所述当前特征子集中剩余的心率变异性指标的集合,作为新的当前特征子集,确定预测模型对当前特征子集的预测准确率;重新判断当前特征子集是否为空集。
在一种可能的实现方式中,根据所述样本对象的多个心率变异性指标中,与所述第二特征向量中的指标类型相同的指标,训练得到所述预测模型,包括:根据所述第二特征向量中的不同指标,排列组合得到多个第三特征向量,其中,不同的第三特征向量中的指标的组合不同,或者,不同的第三特征向量中的指标的组合以及指标在第三特征向量中的排序不同;计算分别以所述样本对象的多个心率变异性指标中,与多个第三特征向量中的指标类型相同的指标作为所述预测模型的输入时,所述预测模型的预测准确度;根据预测准确度最高的第三特征向量确定预测模型的输入指标类型,得到训练好的预测模型。
在一种可能的实现方式中,所述样本对象的心电数据包括清醒状态的心电数据和睡眠状态的心电数据,根据所述样本对象的心电数据,确定所述样本对象的多个心率变异性指标,包括:根据所述样本对象的心电数据,确定所述样本对象的清醒状态下的RR间期序列以及睡眠状态下的RR间期序列;根据所述样本对象的清醒状态下的RR间期序列以及睡眠状态下的RR间期序列,确定与预设的多个指标类型对应的所述多个心率变异性指标,所述样本对象的多个心率变异性指标包括至少一个时域心率变异性指标、至少一个频域心率变异性指标、以及至少一个非线性心率变异性指标中的一个或多个。
根据本公开的另一方面,提供了一种心电数据处理装置,包括:处理器;用于存储处理器可执行指令的存储器;其中,所述处理器被配置为执行上述方法。
根据本公开的另一方面,提供了一种非易失性计算机可读存储介质,其上存储有计算机程序指令,其中,所述计算机程序指令被处理器执行时实现上述方法。
根据本申请实施例的心电数据处理方法,通过采集目标对象的心电数据并处理得到第一特征向量,使得第一特征向量输入预测模型时,预测模型能够给出表示目标对象是否适合接受特定的医学处置的预测结果,从而能够在接受特定的医学处置前预先预测目标对象对于特定的医学处置的适应性。并且第一特征向量包括多个心率变异性指标,因此预测结果与多个心率变异性指标均相关,考虑了不同心率变异性指标之间的综合作用,可以提高预测结果的准确度。
根据下面参考附图对示例性实施例的详细说明,本公开的其它特征及方面将变得清楚。
附图说明
图1示出根据本申请实施例的心电数据处理方法的示例性应用场景。
图2示出根据本申请实施例的心电数据处理方法的示例性示意图。
图3示出现有技术根据心电数据获取心率变异性指标的示例性方法示意图。
图4示出根据本申请实施例的庞加莱图的一个示例。
图5示出根据本申请实施例确定心率变异性指标的重要性排序的实现方式的一个示例。
图6示出本申请实施例按照评分结果从高到低对心率变异性指标进行排序的实现方式的一个示例。
图7示出本申请实施例获得训练好的二分类预测模型的一个示例。
图8示出根据本申请实施例的心电数据处理方法的示例性示意图。
图9示出根据本申请实施例训练得到预测模型的示例性示意图。
图10示出根据本申请实施例的心电数据处理装置的示例性示意图。
图11示出根据本申请实施例的一种心电数据处理装置800的示例性框图。
图12示出根据本申请实施例的一种心电数据处理装置1900的示例性框图。
具体实施方式
以下将参考附图详细说明本公开的各种示例性实施例、特征和方面。附图中相同的附图标记表示功能相同或相似的元件。尽管在附图中示出了实施例的各种方面,但是除非特别指出,不必按比例绘制附图。
在这里专用的词“示例性”意为“用作例子、实施例或说明性”。这里作为“示例性”所说明的任何实施例不必解释为优于或好于其它实施例。
另外,为了更好的说明本公开,在下文的具体实施方式中给出了众多的具体细节。本领域技术人员应当理解,没有某些具体细节,本公开同样可以实施。在一些实例中,对于本领域技术人员熟知的方法、手段、元件和电路未作详细描述,以便于凸显本公开的主旨。
针对药物难治性患者对于特定的医学处置(例如迷走神经刺激手术)的适应性预测方面,目前尚无明确的术前评估手段应用于临床,而基于心电(electrocardiography,ECG)、脑电(electroencephalography,EEG)、核磁影像资料(magnetic resonanceimaging,MRI)、患者人口统计学特征(性别、年龄等)、临床病史(病程)、发作特征(包括发作类型、发作频率、病灶位置等)等数据,进行特定的医学处置的适应性相关因素的研究,得到的结论也不相一致,甚至相互矛盾。
目前在预测药物难治性患者对特定的医学处置的适应性方面,一种应用比较广泛的方法是基于24小时动态心电信号进行适应性预测,该方法操作简单、成本相对较低,且动态心电信号的采集设备通常是可穿戴设备,使得心电信号受患者的活动的影响较小,数据稳定性强,因此成为一种优选的特定的医学处置的适应性预测方案。具体的,该方法通过术前给样本对象佩戴一个便携式动态心电信息记录盒,在样本对象自由活动的状态下,采集样本对象的术前24小时动态心电信号,并记录样本对象进行特定的医学处置(例如迷走神经刺激手术)后较长一段时间内的癫痫发作频率。通过这种方式记录多个样本对象的术前24小时动态心电信号并统计多个样本对象的术后癫痫发作频率,按照癫痫发作频率与术前癫痫发作频率的关系将多个患者归类为多组,例如癫痫发作频率降低至术前的十分之一以下的样本对象作为一组,癫痫发作频率降低至术前的十分之一至五分之一的样本对象作为一组,等等,通过分析每组样本对象的术前24小时动态心电信号,确定每组样本对象的术前心率变异性(heart rate variability,HRV)指标,寻找不同分组的样本对象之间具有统计学显著性差异的心率变异性指标,作为特定的医学处置的适应性预测的敏感因子,采用统计检验方法(例如差异显著性检验方法)分析每个具有统计学差异的心率变异性指标与术后癫痫发作频率的关系,总结指标与癫痫发作频率之间的规律。在此基础上,对于准备接受该特定的医学处置(迷走神经刺激手术)、需要在手术之前确定对该特定的医学处置的适应性的目标对象,可以通过分析该目标对象的术前24小时动态心电信号,确定心率变异性指标,根据指标的数值以及总结得到的指标与癫痫发作频率之间的规律对该目标对象对特定的医学处置的适应性进行预测。
现有的基于24小时动态心电信号进行特定的医学处置的适应性预测的方法,其缺点在于,忽略了不同心率变异性指标之间的综合作用,导致预测结果准确度下降;且统计检验方法总结的规律存在不确定性,采用总结得到的规律重复地基于相同的心率变异性指标进行预测,每次得到的预测结果也可能不同,导致单次预测得到的预测结果准确度难以令人信服,可能需要多次预测来保证预测结果的准确度,带来数据处理成本的提高;此外,在患者处于睡眠或清醒的不同状态时,心率变异性指标的数值存在较大的差异,因此不同状态的心率变异性指标对应的特定的医学处置的适应性的预测结果可能不同,假设对不同状态下的心率变异性指标不加以区分,直接将状态未知的心率变异性指标用于进行特定的医学处置的适应性预测,也会导致预测准确率降低。
综上所述,现有技术的方法在临床应用上具有准确性低的缺陷。
有鉴于此,本申请实施例提出一种心电数据处理方法及装置,根据本申请实施例的心电数据处理方法,可以提高迷走神经刺激手术等特定的医学处置的适应性的预测的准确性。
图1示出根据本申请实施例的心电数据处理方法的示例性应用场景。如图1所示,本申请实施例的心电数据处理方法可以由服务器或终端设备执行,服务器或终端设备可以包括但不限于智能手机、个人计算机、平板电脑等多种电子设备。服务器或终端设备上可以部署有训练好的预测模型。目标对象可穿戴或佩戴有能够进行心电数据采集的可穿戴设备,服务器或终端设备可以通过有线或者无线通信方式接收来自可穿戴设备的心电数据,其中,终端设备也可以是可穿戴设备本身。在目标对象接受特定的医学处置前的任意24小时,可穿戴设备持续采集目标对象的心电数据并发送至服务器或终端设备。
根据本申请实施例的心电数据处理方法,在服务器或终端设备上,目标对象的心电数据经过一系列分析处理,可以得到一个用于输入到预测模型的特征向量,该特征向量输入到预测模型,可以得到目标对象的预测结果。根据该预测结果,可以判断目标对象对于迷走神经刺激手术等特定的医学处置的适应性。
下面结合图2-图6介绍根据本申请实施例的心电数据处理方法的示例性工作方式。图2示出根据本申请实施例的心电数据处理方法的示例性示意图。如图2所示,在一种可能的实现方式中,所述方法包括:
S11,获取样本对象的心电数据并确定样本对象的心率变异性指标。
其中,样本对象的心电数据可以是对应清醒状态和睡眠状态的两组心电数据。举例来说,由于样本对象的生理活动,体外采集的24小时心电数据可能是清醒状态和睡眠状态掺杂的,睡眠状态下的心电数据特征与清醒状态下的心电数据特征并不相同。可以观察24小时的心电数据,分析体外采集的心电数据表现出的特征,确定与睡眠状态下的心电数据特征相符合的心电数据所属的时间段,选择该时间段中连续4小时的心电数据,作为睡眠状态下的4小时心电数据。同理,可确定与清醒状态下的心电数据特征相符合的心电数据所属的时间段,选择该时间段中连续4小时的心电数据,作为清醒状态下的4小时心电数据。确定不同状态下心电数据的过程可以通过人工筛选来实现。
心率变异性是指瞬时心率或瞬时心动周期的微小变化,主要受控制心脏节律的自主神经系统(autonomic nervous system,ANS)的影响,其中自主神经系统包括交感神经和副交感神经。心率变异性指标可例如包括从心电数据中统计或计算得到的、指示心率变异性的程度的指标。图3示出现有技术根据心电数据获取心率变异性指标的示例性方法示意图。
如图3所示,步骤S11可包括步骤S111和步骤S112,在获取清醒和睡眠两种状态下各4个小时的心电数据后,可以执行下文的步骤S111和步骤S112以得到心率变异性指标。
S111,从清醒和睡眠两种状态下各4个小时的心电数据中分别得到清醒和睡眠两种状态下各4个小时的RR间期序列。
其中,RR间期在心电图上体现为心电图中相邻心跳间的时间(或距离,心电图距离1mm=时间0.04秒),由相邻RR间期组成的时间序列称为RR间期序列。可以采用现有技术的方法对心电数据进行数字化、去噪处理,针对处理后的心电数据,统计显示为心电图中心跳波形的数据的采集时间,确定相邻的心跳间的时间间隔,并根据多个时间间隔得到RR间期序列。针对清醒和睡眠两种状态下各4个小时的心电数据,可以分别得到清醒状态对应的RR间期序列和睡眠状态对应的RR间期序列。
S112,对清醒和睡眠两种状态下的RR间期序列进行心率变异性特征提取,得到心率变异性指标。
举例来说,可以采用现有技术的时域分析方法、频域分析方法、非线性分析方法等多种方式完成心率变异性特征提取。以下结合表1-3分别介绍时域分析方法、频域分析方法、非线性分析方法下确定的指标类型和具体确定方式。
时域分析方法包括统计学方法和几何学方法,能够较为简便的评估心率的变化。其中,统计学方法通过在心电数据中确定每次心跳的时间信息来确定每个RR间期的时间,进一步计算平均心率以及有关RR间期的统计量,几何学方法通过将RR间期序列转化到几何图形并计算相应的图形特征来量化RR间期的分布情况。时域分析方法能够定量地描述自主神经系统对心律的调节作用。下面结合表1介绍根据时域分析方法确定的心率变异性指标的相关信息。
如表1所示,根据时域分析方法,可例如确定多个心率变异性指标,包括Mean RR(RR间期序列均值)、RMSSD(相邻RR间期差值的均方根)、SDNN(RR间期序列的标准差)等,表1示出时域分析方法确定的多种指标的名称(例如Mean RR)、单位(例如ms)及对应的定义(例如RR间期序列均值)。
表1
表1续
其中,表1中的指标的数值计算方式,可以根据定义指示,参照现有技术中的对应方法来计算。例如,指标Mean RR定义为RR间期序列均值,现有技术中序列均值的计算方式为序列中的元素之和与元素个数的比值,指标Mean RR的数值可以根据RR间期序列中的RR间期之和与RR间期个数的比值确定。表1中的其他指标的数值计算方式的示例在此不再赘述。
频域分析方法包括功率谱密度分析(power spectral density,PSD),频域分析的结果能够指示功率随频率的分布关系。下面结合表2介绍根据频域分析方法确定的心率变异性指标的相关信息。
如表2所示,根据频域分析方法确定的频域指标,可包括超低频(ultra lowfrequency,ULF)功率、极低频(very low frequency,VLF)功率、低频(low frequency,LF)功率、高频(high frequency,HF)功率、低频与高频的功率比等等。表2示出频域分析方法确定的多种指标的名称(例如ULF)、单位(例如ms
表2
其中,根据功率谱密度分析得出的典型的心率变异性功率谱上可包括多个分离的谱峰,不同谱峰可近似看作位于不同的频段,各频段下面积可作为功率谱能量的测定值,即为频域指标的数值,超低频功率ULF、极低频功率VLF、低频功率LF、高频功率HF的数值可例如分别等于对应定义中的频段的面积。例如超低频功率ULF的数值可等于小于0.0033Hz的频段的面积。低频与高频的功率比,可例如等于低频功率LF对应定义中的频段的面积与高频功率HF对应定义中的频段的面积的比值。
本领域技术人员应理解,频域分析方法并不限于功率谱密度分析方法,频域分析方法还可包括幅度谱分析、相位谱分析等,只要能够在频域对RR间期进行分析,确定能够体现心率变异性的心率变异性指标即可,本申请对频域分析方法采用的具体特征提取方式不作限制。
心脏的生理活动决定了心率调节机制的非线性,因此除了时域、频域分析以外,可以采用非线性分析方法以更加全面地度量心率变异性的特性。下面结合表3介绍根据非线性分析方法确定的心率变异性指标的相关信息。
在一种可能的实现方式中,非线性指标可包括庞加莱图(PoincaréPlot)特征、心率不对称性(heart rate asymmetry,HRA)。其中,庞加莱图特征可包括指标SD1、SD2、CSI、CVI、GI、PI、SI、AI(参见表3),心率不对称性可包括指标SD1
表3
表3续
图4示出根据本申请实施例的庞加莱图的一个示例。如图4所示,以任意RR间期(例如RRn)作为横坐标X的值,以紧挨其后的RR间期(例如RRn+1)作为纵横坐标Y的值,X=Y的直线可例如是表3中的“标识线”。庞加莱图中包括若干散点(数量可等于表3中的n),每个点的位置都由相邻的两个RR间期确定,根据散点在图中的位置,可以分为落在标识线上方的散点(数量可等于表3中的l)、在标识线下方的散点(数量可等于表3中的b)、以及位于标识线上的散点(数量可等于表3中的n
其中,表3中“短程”可表示清醒或睡眠状态下的4小时中的连续一小段时间,以“短程”为5min为例,清醒或睡眠状态下的4小时可对应48个“短程”,每个“短程”都对应一组与“短程”相关的指标,例如上表3中的SD1
其中,一些非线性心率变异性指标也可以通过此前时域分析确定的心率变异性指标来计算,例如,参见表3,描述短期RR间期的波动的非线性心率变异性指标SD1,可以通过时域心率变异性指标SDSD(相邻RR间期之差的标准差)计算得到。除此之外,表3中的非线性心率变异性指标SD2也可以通过时域心率变异性指标计算得到。表3中的指标CSI、CVI,可以根据非线性心率变异性指标SD1、SD2计算得到,因此也可以看作根据时域心率变异性指标计算得到的非线性指标。
在一种可能的实现方式中,非线性指标还可包括心率碎片化(heart ratefragmentation,HRF)。其中,心率指正常人安静状态下每分钟心跳的次数,心率加速度由迷走神经调控窦房结的频率确定,心率碎片化表现为:心率加速度以高于迷走神经调控窦房结的频率发生频繁变化。心率碎片化可包括以下指标中的一种或多种:过零检测点(转折点)在整个RR间期序列中的百分比(percentage of inflection points of the RRintervals series,PIP)、心率加速或减速过程的平均时长的倒数(inverse of theaverage length of the acceleration/deceleration segments,IALS)、“短片段”百分比(percentage of short segments,PSS)、“交替片段”占总体RR间期序列的百分比(percentage of NN intervals in alternation segments,PAS)。其中,“短片段”百分比指标中的“短片段”,可定义为包括3个及以上RR间期的心率加速和减速过程,“交替片段”占总体RR间期序列的百分比指标中的“交替片段”,可定义为至少包括4个RR间期的RR间期序列,并且该RR间期序列中,每一次心跳前后,心率加速度都发生变号。
在一种可能的实现方式中,非线性指标还可包括心率的复杂度。心率的复杂度可以通过近似熵来分析。近似熵(ApEn)是由Pincus在1991年提出来的,可以测量时间序列的复杂性和规律性的一种无需粗粒化的复杂性测度分析方法。其物理意义是当维数变化时时间序列中产生新模式的概率的大小,产生新模式的概率越大,表示时间序列越复杂,相应的近似熵也就越大。举例来说,参见图4,每个点的位置都由相邻的两个RR间期确定,根据连续m+1个RR间期,可以确定m个点,根据m个点可以连成m-1个折线段,根据m-1个折线段的形状的形似程度,可以确定一个相互近似概率。同理,根据连续m+2个RR间期(包括上文所述的m+1个RR间期),可以确定m+1个点(包括上文所述的m个点),根据m+1个点可以连成m个折线段,根据m个折线段的形状的形似程度,可以确定一个相互近似概率。两个相互近似概率的差值可指示心率的复杂度。
本领域技术人员应理解,通过时域分析方法、频域分析方法以及非线性分析方法能够得到的心率变异性指标应不止上述示例中的指标。本申请对于根据样本对象的心电数据确定的心率变异性指标的具体类型和具体数量不作限制。
在一种可能的实现方式中,在通过多种分析方法确定样本对象的心率变异性指标后,可以执行下文的步骤S12进行心率变异性指标的排序。
S12,根据样本对象的心率变异性指标和样本对象接受特定的医学处置后的效果,确定心率变异性指标的重要性排序。
图5示出根据本申请实施例确定心率变异性指标的重要性排序的实现方式的一个示例。参见图5,步骤S12可例如包括下文的步骤S121-S123:
S121,根据样本对象接受特定的医学处置后的效果,将样本对象的心率变异性指标分类为正样本和负样本。
由上文描述可知,样本对象已经接受迷走神经刺激手术,样本对象接受特定的医学处置,例如迷走神经刺激手术后的效果,与该样本对象的心率变异性指标具有一定关联。可预设样本对象接受特定的医学处置后的效果为术后癫痫发作频率相比术前有所降低的样本对象为有效对象。可预设样本对象接受特定的医学处置后的效果为术后癫痫发作频率相比术前并无明显变化的样本对象为无效对象。在此情况下,正样本可包括有效对象对应的心率变异性指标,负样本可包括无效对象对应的心率变异性指标。
S122,对正负样本的心率变异性指标进行组间差异显著性分析,确定具有统计性显著差异的心率变异性指标。
举例来说,显著性差异(significant difference),是一个统计学名词,可用于评价数据差异性。如果某类型数据之间具有显著性差异,例如,参与比对的数据之间的差别大于或等于阈值,可认为参与比对的数据不是来自于同一总体(Population),而是来自于在一个或多个方面具有差异的两个不同总体。如果某类型数据之间不具有显著性差异,例如,参与比对的数据之间的差别小于阈值,可认为参与比对的数据是来自于同一总体。本申请实施例中,参与比对的数据已经确定来自具有差异性的两个不同总体,在此情况下,如果某类型数据之间具有显著性差异,该类型数据与可能与两个总体的差异相关联,如果某类型数据之间不具有显著性差异,该类型数据与可能与两个总体差异无关。
举例来说,两个总体可例如分别是正负样本,在数据类型为心-交感神经功能指数CSI时,总体的差异可例如是样本对象接受特定的医学处置后的效果差异,如果分析确定正样本和负样本的心-交感神经功能指数CSI差别较大,例如大于一个预设阈值,可认为用于分析的心-交感神经功能指数CSI之间具有显著性差异,心-交感神经功能指数CSI与样本对象接受特定的医学处置后的效果相关联。在数据类型为心-迷走神经功能指数CVI时,如果分析确定正样本和负样本的心-迷走神经功能指数CVI差别较小,例如小于另一个预设阈值,可认为用于分析的心-迷走神经功能指数CVI之间不具有显著性差异,心-迷走神经功能指数CVI与样本对象接受特定的医学处置后的效果无关。
步骤S122可以基于现有技术中的曼-惠特尼U检验法实现。本领域技术人员应理解,也可以采用其他方法实现步骤S122,只要能够以统计学的方法分析确定正负样本的心率变异性指标中,具有统计性显著差异的指标即可,本申请对具有统计性显著差异的心率变异性指标的具体确定方式不作限制。
S123,计算具有统计性显著差异的心率变异性指标的重要性评分,按照评分结果从高到低对心率变异性指标进行排序。
图6示出本申请实施例按照评分结果从高到低对心率变异性指标进行排序的实现方式的一个示例。参见图6,步骤S123可例如包括下文的步骤S21-S25:
S21,将初始特征子集输入到随机森林机器学习模型,得到每个指标的重要性评分;通过交叉验证方法确定初始特征子集对应的预测准确率。
其中,初始特征子集可以包括所有具有统计性显著差异的心率变异性指标,N表示集合中的指标的个数。举例来说,假设步骤S122确定的具有统计性显著差异的心率变异性指标分别是GI、PI、SI、AI,在此情况下,初始特征子集可以是S
随机森林机器学习模型以及交叉验证方法可以基于现有技术来实现。步骤S21可例如通过现有技术的随机森林学习模型得到指标GI的重要性评分0.5、指标PI的重要性评分0.2、指标SI的重要性评分0.2以及指标AI的重要性评分0.1。并且可例如通过现有技术的交叉验证方法确定初始特征子集S
S22,从当前特征子集中,移除若干个重要性评分最低的指标,根据余下的指标,得到一个新的特征子集。
其中,如果重要性评分最低的指标有多个,可以移除多个指标中的至少一个。在此情况下,步骤S22可移除初始特征子集S
S23,将新的特征子集输入到随机森林机器学习模型,得到每个指标的重要性评分;通过交叉验证方法确定新的特征子集对应的预测准确率。
其中,步骤S23使用的随机森林机器学习模型以及交叉验证方法可以与步骤S21中所使用的相同。步骤S23可例如通过现有技术的随机森林学习模型得到指标GI的重要性评分0.6、指标PI的重要性评分0.2以及指标SI的重要性评分0.2。并且可例如通过现有技术的交叉验证方法确定特征子集S
S24,判断当前特征子集是否为空集,在不为空集时,重复步骤S22-步骤S24,在为空集时,执行步骤S25。
举例来说,步骤S24判断的当前特征子集实际上是执行步骤S22得到的,由上文描述可知,当前特征子集S
又例如,步骤S24判断当前特征子集S
本领域技术人员应理解,只要能够满足每次执行S22时,从当前特征子集中,移除至少一个重要性评分最低的指标即可,本申请对于重要性评分最低的指标的具体移除方式不作限制。
S25,选择步骤S22-S24确定的全部特征子集中,预测准确率最高的一个特征子集,根据该特征子集中的各指标的重要性评分由高到低的顺序,对该特征子集中的指标进行排序,得到排序结果。
举例来说,步骤S22-S24确定的全部特征子集S
又例如,步骤S22-S24确定的全部特征子集S
步骤S123可以基于现有技术的递归特征消除特征选择法实现。本领域技术人员应理解,也可以采用其他方法实现步骤S123,只要能够完成具有统计性显著差异的心率变异性指标的排序、且排序结果中的任一指标的重要性不高于该指标的前一个指标即可,本申请对具有统计性显著差异的心率变异性指标的具体排序方式不作限制。
在一种可能的实现方式中,步骤S12确定心率变异性指标的重要性排序后,可以基于排序结果以及样本对象的心率变异性指标,执行下文的步骤S13训练得到预测模型,该模型可以用于步骤S14中对目标对象进行预测确定目标对象的预测结果。
S13,根据所述重要性的排序以及样本对象的心率变异性指标,采用随机森林机器学习分类算法,得到二分类预测模型。
举例来说,根据心率变异性指标的重要性排序,从排序第一的心率变异性指标开始逐个添加排序靠后的心率变异性指标,得到一个向量,该向量可以作为待训练的二分类预测模型的输入特征向量。根据输入特征向量可以完成二分类预测模型的训练。图7示出本申请实施例获得训练好的二分类预测模型的一个示例。
举例来说,如图7所示,待训练的二分类预测模型接收到输入特征向量后,根据该特征向量中的多个特征,进行排列组合,可以得到包括不同特征的组合的多个处理后的特征向量。例如,输入特征向量可以是{GI、PI、SI},如果对处理后的特征向量中的元素排列顺序不作限定,处理后的特征向量可以有
其中,二分类预测模型的预测准确率,可以通过将样本对象的心率变异性指标作为向量输入到二分类预测模型进行分类得到的预测结果,与样本对象接受特定的医学处置(例如迷走神经刺激手术)后的效果进行比对来确定。例如,二分类预测模型可得到预测结果为响应者的样本和预测结果为非响应者的样本,其中预测结果为响应者对应迷走神经刺激手术术后癫痫发作减少≥50%,预测结果为非响应者对应迷走神经刺激手术术后癫痫发作减少<50%。可以分别统计正样本中满足预测结果为响应者的样本数量,以及负样本中满足预测结果为非响应者的样本数量,根据二者之和得到预测结果准确的样本数量,在此情况下,预测结果准确的样本数量与样本总数(正样本和负样本的和)的比值,可以作为二分类预测模型的预测准确率。
上述二分类预测模型的预测准确率的确定方式仅为示例。本申请实施例对于二分类预测模型的预测准确率的确定方式不作限制。
S14,根据二分类预测模型和目标对象的心电数据,得到目标对象的预测结果。
其中,目标对象可以是尚未接受迷走神经刺激手术的对象。在步骤S14中,可以按照上文步骤S11的方法,先根据目标对象的心电数据获取目标对象的心率变异性指标。其中,获取的指标至少包括步骤S13确定的训练好的二分类预测模型的输入的最优特征向量所指示的指标,获取指标后,多个指标可以自由组合得到特征向量。在此情况下,将特征向量作为训练好的二分类预测模型的输入数据,二分类预测模型可以输出目标对象的预测结果。该预测结果可以用于判断目标对象对于迷走神经刺激手术等特定医学处置的适应性。
本领域技术人员应理解,除了上文所述的二分类预测模型,步骤S13也可以训练得到多分类预测模型,步骤S14可以使用多分类预测模型对特征向量进行处理,输出目标对象的预测结果。本申请对得到目标对象的预测结果使用的预测模型的具体形式不作限制。
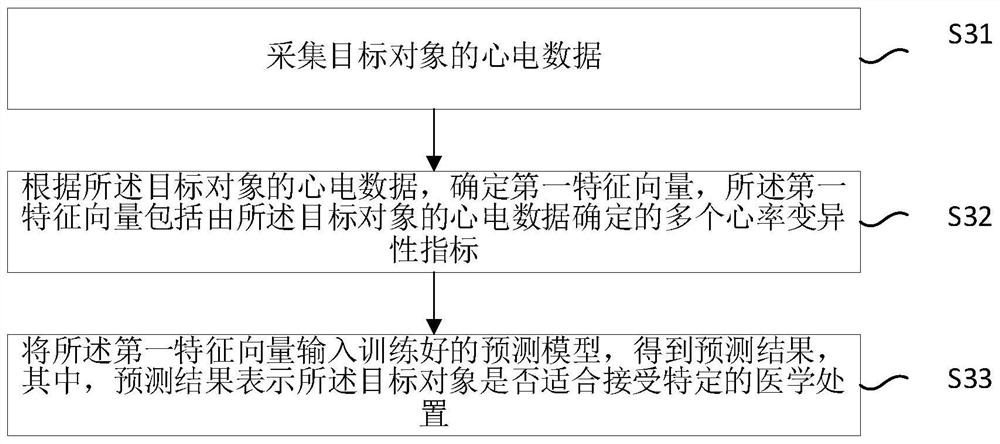
图8示出根据本申请实施例的心电数据处理方法的示例性示意图。如图8所示,本申请实施例提出一种心电数据处理方法,所述方法包括:
S31,采集目标对象的心电数据。其中,目标对象可以是迷走神经刺激手术等特定的医学处置的适应性预测对象,目标对象的心电数据的示例性采集方式,可以参照上文步骤S11的相关描述。
S32,根据所述目标对象的心电数据,确定第一特征向量,所述第一特征向量包括由所述目标对象的心电数据确定的多个心率变异性指标。心率变异性指标可以是上文表1-表3中的示例性的心率变异性指标,也可以是根据现有技术能对心电数据进行处理得到的其他指示心率变异性的指标。第一特征向量可以是上文步骤S14中的特征向量,步骤S32的示例性实现方式可以参照上文步骤S14的相关描述。
S33,将所述第一特征向量输入训练好的预测模型,得到预测结果,其中,预测结果表示所述目标对象是否适合接受特定的医学处置。其中,训练好的预测模型可以是上文中的二分类预测模型或者是多分类预测模型等。特定的医学处置可以是上文中的迷走神经刺激手术等医学处置手段。步骤S33的示例性实现方式可以参照上文步骤S14的相关描述。
根据本申请实施例的心电数据处理方法,通过采集目标对象的心电数据并处理得到第一特征向量,使得第一特征向量输入预测模型时,预测模型能够给出表示目标对象是否适合接受特定的医学处置的预测结果,从而能够在接受特定的医学处置前预先预测目标对象对于特定的医学处置的适应性。并且第一特征向量包括多个心率变异性指标,因此预测结果与多个心率变异性指标均相关,考虑了不同心率变异性指标之间的综合作用,可以提高预测结果的准确度。
在一种可能的实现方式中,所述目标对象的心电数据包括清醒状态的心电数据和睡眠状态的心电数据,步骤S31包括:根据所述目标对象的心电数据,确定所述目标对象的清醒状态下的RR间期序列以及睡眠状态下的RR间期序列;根据所述目标对象的清醒状态下的RR间期序列以及睡眠状态下的RR间期序列,得到所述第一特征向量。
其中,RR间期序列的定义以及RR间期序列的示例性确定方式可以参照上文步骤S111的相关描述。第一特征向量的示例性确定方式可以参照上文步骤S14的相关描述。
由于区分了清醒状态下和睡眠状态下的RR间期序列,使得第一特征向量中的心率变异性指标的数值与目标对象的状态相关联,采用状态已知的心率变异性指标来进行目标对象针对特定的医学处置的适应性的预测,可以进一步提高预测结果的准确度。
在一种可能的实现方式中,根据所述目标对象的清醒状态下的RR间期序列以及睡眠状态下的RR间期序列,得到所述第一特征向量,包括:确定作为所述训练好的预测模型的输入的多个指标类型;根据所述目标对象的清醒状态下的RR间期序列以及睡眠状态下的RR间期序列,确定与所述多个指标类型对应的所述多个心率变异性指标;根据所述多个心率变异性指标,得到所述第一特征向量。
其中,训练好的预测模型的输入的多个指标类型的示例性确定方式,可参照上文步骤S14中,目标对象的心率变异性指标的示例性获取方式。
通过这种方式,使得第一特征向量中的指标类型与训练好的预测模型的对应的输入的多个指标类型相符合,使得第一特征向量输入预测模型进行预测时,可以保证预测结果的准确度。
在一种可能的实现方式中,所述预测模型根据样本对象的心电数据训练得到,图9示出根据本申请实施例训练得到预测模型的示例性示意图。
如图9所示,所述方法还包括:
S41,根据所述样本对象的心电数据,确定所述样本对象的多个心率变异性指标。其示例性实现方式可以参照上文步骤S11的相关描述。
S42,根据所述样本对象接受所述特定的医学处置后的效果,将所述效果满足预设条件的样本对象的多个心率变异性指标确定为正样本,将所述效果不满足预设条件的样本对象的多个心率变异性指标确定为负样本。其中预设条件的示例可以是上文中描述的术后癫痫发作频率相比术前有所降低。步骤S42的示例性实现方式可以参照上文步骤S121的相关描述。
S43,对正样本和负样本进行差异显著性分析,得到具有显著性差异的心率变异性指标,其中正样本和负样本的具有显著性差异的心率变异指标之间的差别大于阈值。其示例性实现方式可以参照上文步骤S122的相关描述。
S44,对所述具有显著性差异的心率变异性指标进行重要性排序,得到第二特征向量。其中,第二特征向量可例如是上文步骤S123的相关描述中的排序结果。步骤S44的示例性实现方式可以参照上文步骤S123的相关描述。
S45,根据所述样本对象的多个心率变异性指标中,与所述第二特征向量中的指标类型相同的指标,训练得到所述预测模型。其示例性实现方式可以参照上文步骤S124的相关描述。
通过这种方式,可以获得训练好的预测模型。相比现有技术中先统计单个指标与预测结果的关系再进行规律总结的方法,本申请的预测模型是根据多个心率变异性指标训练得到,因此预测模型是在考虑多个指标对预测结果的综合作用下得到的,采用预测模型得到的预测结果准确度更高。
在一种可能的实现方式中,对所述具有显著性差异的心率变异性指标进行重要性排序,得到第二特征向量,包括:
根据所有具有显著性差异的心率变异性指标,得到特征子集,确定预测模型对所述特征子集的预测准确率;判断当前特征子集是否为空集;在所述当前特征子集为空集时,按照预测准确率最高的一个特征子集中的心率变异性指标的重要性评分,对所述预测准确率最高的一个特征子集中的心率变异性指标进行重要性排序,得到第二特征向量。
其中,根据所有具有显著性差异的心率变异性指标得到的特征子集,可例如是上文步骤S21中的初始特征子集。得到第二特征向量的示例性方式可以参照上文的步骤S21、S25的相关描述。
通过这种方式,可以使得第二特征向量的指标类型,与准确率最高的特征子集中的指标类型相对应,使得预测模型的预测准确率更高。
在一种可能的实现方式中,对所述具有显著性差异的心率变异性指标进行重要性排序,得到第二特征向量,还包括:
在所述当前特征子集不为空集时,重复以下操作:
将所述当前特征子集输入预设的随机森林模型,得到所述当前特征子集中的每个心率变异性指标的重要性评分;消除所述当前特征子集中,至少一个重要性评分最低的心率变异性指标,所述当前特征子集中剩余的心率变异性指标的集合,作为新的当前特征子集,确定预测模型对当前特征子集的预测准确率;重新判断当前特征子集是否为空集。
其中,当前特征子集可例如是上文描述中的初始特征子集或者新的特征子集。当前特征子集不为空集时,心电数据处理方法的示例性实现方式可以参照上文的步骤S22-S24的相关描述。
通过每次消除重要性评分最低的指标,使得消除处理后的特征子集中可以保留重要性评分较高的指标,可以在降低特征子集的维度的基础上,保证特征子集的预测准确度。
在一种可能的实现方式中,根据所述样本对象的多个心率变异性指标中,与所述第二特征向量中的指标类型相同的指标,训练得到所述预测模型,包括:
根据所述第二特征向量中的不同指标,排列组合得到多个第三特征向量,其中,不同的第三特征向量中的指标的组合不同,或者,不同的第三特征向量中的指标的组合以及指标在第三特征向量中的排序不同;计算分别以所述样本对象的多个心率变异性指标中,与多个第三特征向量中的指标类型相同的指标作为所述预测模型的输入时,所述预测模型的预测准确度;根据预测准确度最高的第三特征向量确定预测模型的输入指标类型,得到训练好的预测模型。
其中,第二特征向量可以是上文步骤S13的相关描述中的输入特征向量,第三特征向量可以是上文步骤S13的相关描述中的处理后的特征向量。步骤S45的示例性实现方式可以参照上文步骤S13的相关描述。
针对重要性排序后的第二特征向量所包括的指标进行进一步的筛选,以及对筛选结果进行排列组合,得到准确率较高的第三特征向量,使得根据第三特征向量得到预测模型时,预测模型的预测准确率进一步提高。且排列组合有多种选择方式,提高了得到预测模型的灵活性。
在一种可能的实现方式中,所述样本对象的心电数据包括清醒状态的心电数据和睡眠状态的心电数据,根据所述样本对象的心电数据,确定所述样本对象的多个心率变异性指标,包括:
根据所述样本对象的心电数据,确定所述样本对象的清醒状态下的RR间期序列以及睡眠状态下的RR间期序列;根据所述样本对象的清醒状态下的RR间期序列以及睡眠状态下的RR间期序列,确定与预设的多个指标类型对应的所述多个心率变异性指标,所述样本对象的多个心率变异性指标包括至少一个时域心率变异性指标、至少一个频域心率变异性指标、以及至少一个非线性心率变异性指标中的一个或多个。
通过这种方式,可以提升心率变异性指标的确定方式的灵活性。
图10示出根据本申请实施例的心电数据处理装置的示例性示意图。
如图10所示,本申请提供一种心电数据处理装置,包括:
采集模块100,用于采集目标对象的心电数据;
确定模块200,用于根据所述目标对象的心电数据,确定第一特征向量,所述第一特征向量包括由所述目标对象的心电数据确定的多个心率变异性指标;
预测模块300,用于将所述第一特征向量输入训练好的预测模型,得到预测结果,其中,预测结果表示所述目标对象是否适合接受特定的医学处置。
在一种可能的实现方式中,所述目标对象的心电数据包括清醒状态的心电数据和睡眠状态的心电数据,根据所述目标对象的心电数据,确定第一特征向量,包括:根据所述目标对象的心电数据,确定所述目标对象的清醒状态下的RR间期序列以及睡眠状态下的RR间期序列;根据所述目标对象的清醒状态下的RR间期序列以及睡眠状态下的RR间期序列,得到所述第一特征向量。
在一种可能的实现方式中,根据所述目标对象的清醒状态下的RR间期序列以及睡眠状态下的RR间期序列,得到所述第一特征向量,包括:确定作为所述训练好的预测模型的输入的多个指标类型;根据所述目标对象的清醒状态下的RR间期序列以及睡眠状态下的RR间期序列,确定与所述多个指标类型对应的所述多个心率变异性指标;根据所述多个心率变异性指标,得到所述第一特征向量。
在一种可能的实现方式中,所述预测模型根据样本对象的心电数据训练得到,所述方法还包括:根据所述样本对象的心电数据,确定所述样本对象的多个心率变异性指标;根据所述样本对象接受所述特定的医学处置后的效果,将所述效果满足预设条件的样本对象的多个心率变异性指标确定为正样本,将所述效果不满足预设条件的样本对象的多个心率变异性指标确定为负样本;对所述正样本和所述负样本进行差异显著性分析,得到具有显著性差异的心率变异性指标,其中正样本和负样本的具有显著性差异的心率变异指标之间的差别大于阈值;对所述具有显著性差异的心率变异性指标进行重要性排序,得到第二特征向量;根据所述样本对象的多个心率变异性指标中,与所述第二特征向量中的指标类型相同的指标,训练得到所述预测模型。
在一种可能的实现方式中,对所述具有显著性差异的心率变异性指标进行重要性排序,得到第二特征向量,包括:根据所有具有显著性差异的心率变异性指标,得到特征子集,确定预测模型对所述特征子集的预测准确率;判断当前特征子集是否为空集;在所述当前特征子集为空集时,按照预测准确率最高的一个特征子集中的心率变异性指标的重要性评分,对所述预测准确率最高的一个特征子集中的心率变异性指标进行重要性排序,得到第二特征向量。
在一种可能的实现方式中,对所述具有显著性差异的心率变异性指标进行重要性排序,得到第二特征向量,还包括:在所述当前特征子集不为空集时,重复以下操作:将所述当前特征子集输入预设的随机森林模型,得到所述当前特征子集中的每个心率变异性指标的重要性评分;消除所述当前特征子集中,至少一个重要性评分最低的心率变异性指标,所述当前特征子集中剩余的心率变异性指标的集合,作为新的当前特征子集,确定预测模型对当前特征子集的预测准确率;重新判断当前特征子集是否为空集。
在一种可能的实现方式中,根据所述样本对象的多个心率变异性指标中,与所述第二特征向量中的指标类型相同的指标,训练得到所述预测模型,包括:根据所述第二特征向量中的不同指标,排列组合得到多个第三特征向量,其中,不同的第三特征向量中的指标的组合不同,或者,不同的第三特征向量中的指标的组合以及指标在第三特征向量中的排序不同;计算分别以所述样本对象的多个心率变异性指标中,与多个第三特征向量中的指标类型相同的指标作为所述预测模型的输入时,所述预测模型的预测准确度;根据预测准确度最高的第三特征向量确定预测模型的输入指标类型,得到训练好的预测模型。
在一种可能的实现方式中,所述样本对象的心电数据包括清醒状态的心电数据和睡眠状态的心电数据,根据所述样本对象的心电数据,确定所述样本对象的多个心率变异性指标,包括:根据所述样本对象的心电数据,确定所述样本对象的清醒状态下的RR间期序列以及睡眠状态下的RR间期序列;根据所述样本对象的清醒状态下的RR间期序列以及睡眠状态下的RR间期序列,确定与预设的多个指标类型对应的所述多个心率变异性指标,所述样本对象的多个心率变异性指标包括至少一个时域心率变异性指标、至少一个频域心率变异性指标、以及至少一个非线性心率变异性指标中的一个或多个。
在一种可能的实现方式中,本申请提供一种心电数据处理装置,包括:处理器;用于存储处理器可执行指令的存储器;其中,所述处理器被配置为:调用所述存储器存储的指令,以执行上述心电数据处理方法。
在一种可能的实现方式中,本申请提供一种非易失性计算机可读存储介质,其上存储有计算机程序指令,所述计算机程序指令被处理器执行时实现上述心电数据处理方法。
图11示出根据本申请实施例的一种心电数据处理装置800的示例性框图。例如,心电数据处理装置800可以是移动电话,计算机,数字广播终端,消息收发设备,游戏控制台,平板设备,医疗设备,健身设备,个人数字助理等。
参照图11,心电数据处理装置800可以包括以下一个或多个组件:处理组件802,存储器804,电源组件806,多媒体组件808,音频组件810,输入/输出(I/O)的接口812,传感器组件814,以及通信组件816。
处理组件802通常控制心电数据处理装置800的整体操作,诸如与显示,电话呼叫,数据通信,相机操作和记录操作相关联的操作。处理组件802可以包括一个或多个处理器820来执行指令,以完成上述的方法的全部或部分步骤。此外,处理组件802可以包括一个或多个模块,便于处理组件802和其他组件之间的交互。例如,处理组件802可以包括多媒体模块,以方便多媒体组件808和处理组件802之间的交互。
存储器804被配置为存储各种类型的数据以支持在心电数据处理装置800的操作。这些数据的示例包括用于在心电数据处理装置800上操作的任何应用程序或方法的指令,联系人数据,电话簿数据,消息,图片,视频等。存储器804可以由任何类型的易失性或非易失性存储设备或者它们的组合实现,如静态随机存取存储器(SRAM),电可擦除可编程只读存储器(EEPROM),可擦除可编程只读存储器(EPROM),可编程只读存储器(PROM),只读存储器(ROM),磁存储器,快闪存储器,磁盘或光盘。
电源组件806为心电数据处理装置800的各种组件提供电力。电源组件806可以包括电源管理系统,一个或多个电源,及其他与为心电数据处理装置800生成、管理和分配电力相关联的组件。
多媒体组件808包括在所述心电数据处理装置800和用户之间的提供一个输出接口的屏幕。在一些实施例中,屏幕可以包括液晶显示器(LCD)和触摸面板(TP)。如果屏幕包括触摸面板,屏幕可以被实现为触摸屏,以接收来自用户的输入信号。触摸面板包括一个或多个触摸传感器以感测触摸、滑动和触摸面板上的手势。所述触摸传感器可以不仅感测触摸或滑动动作的边界,而且还检测与所述触摸或滑动操作相关的持续时间和压力。
在一些实施例中,多媒体组件808包括一个前置摄像头和/或后置摄像头。当心电数据处理装置800处于操作模式,如拍摄模式或视频模式时,前置摄像头和/或后置摄像头可以接收外部的多媒体数据。每个前置摄像头和后置摄像头可以是一个固定的光学透镜系统或具有焦距和光学变焦能力。
音频组件810被配置为输出和/或输入音频信号。例如,音频组件810包括一个麦克风(MIC),当心电数据处理装置800处于操作模式,如呼叫模式、记录模式和语音识别模式时,麦克风被配置为接收外部音频信号。所接收的音频信号可以被进一步存储在存储器804或经由通信组件816发送。在一些实施例中,音频组件810还包括一个扬声器,用于输出音频信号。
I/O接口812为处理组件802和外围接口模块之间提供接口,上述外围接口模块可以是键盘,点击轮,按钮等。这些按钮可包括但不限于:主页按钮、音量按钮、启动按钮和锁定按钮。
传感器组件814包括一个或多个传感器,用于为装置800提供各个方面的状态评估。例如,传感器组件814可以检测到装置800的打开/关闭状态,组件的相对定位,例如所述组件为心电数据处理装置800的显示器和小键盘,传感器组件814还可以检测心电数据处理装置800或心电数据处理装置800一个组件的位置改变,用户与心电数据处理装置800接触的存在或不存在,心电数据处理装置800方位或加速/减速和心电数据处理装置800的温度变化。传感器组件814可以包括接近传感器,被配置用来在没有任何的物理接触时检测附近物体的存在。传感器组件814还可以包括光传感器,如CMOS或CCD图像传感器,用于在成像应用中使用。在一些实施例中,该传感器组件814还可以包括加速度传感器,陀螺仪传感器,磁传感器,压力传感器或温度传感器。
通信组件816被配置为便于心电数据处理装置800和其他设备之间有线或无线方式的通信。心电数据处理装置800可以接入基于通信标准的无线网络,如WiFi,2G或3G,或它们的组合。在一个示例性实施例中,通信组件816经由广播信道接收来自外部广播管理系统的广播信号或广播相关信息。在一个示例性实施例中,所述通信组件816还包括近场通信(NFC)模块,以促进短程通信。例如,在NFC模块可基于射频识别(RFID)技术,红外数据协会(IrDA)技术,超宽带(UWB)技术,蓝牙(BT)技术和其他技术来实现。
在示例性实施例中,心电数据处理装置800可以被一个或多个应用专用集成电路(ASIC)、数字信号处理器(DSP)、数字信号处理设备(DSPD)、可编程逻辑器件(PLD)、现场可编程门阵列(FPGA)、控制器、微控制器、微处理器或其他电子元件实现,用于执行上述方法。
在示例性实施例中,还提供了一种非易失性计算机可读存储介质,例如包括计算机程序指令的存储器804,上述计算机程序指令可由心电数据处理装置800的处理器820执行以完成上述方法。
图12示出根据本申请实施例的一种心电数据处理装置1900的示例性框图。例如,心电数据处理装置1900可以被提供为一服务器。参照图12,心电数据处理装置1900包括处理组件1922,其进一步包括一个或多个处理器,以及由存储器1932所代表的存储器资源,用于存储可由处理组件1922的执行的指令,例如应用程序。存储器1932中存储的应用程序可以包括一个或一个以上的每一个对应于一组指令的模块。此外,处理组件1922被配置为执行指令,以执行上述方法。
心电数据处理装置1900还可以包括一个电源组件1926被配置为执行装置1900的电源管理,一个有线或无线网络接口1950被配置为将心电数据处理装置1900连接到网络,和一个输入输出(I/O)接口1958。心电数据处理装置1900可以操作基于存储在存储器1932的操作系统,例如Windows ServerTM,Mac OS XTM,UnixTM,LinuxTM,FreeBSDTM或类似。
在示例性实施例中,还提供了一种非易失性计算机可读存储介质,例如包括计算机程序指令的存储器1932,上述计算机程序指令可由心电数据处理装置1900的处理组件1922执行以完成上述方法。
本公开可以是系统、方法和/或计算机程序产品。计算机程序产品可以包括计算机可读存储介质,其上载有用于使处理器实现本公开的各个方面的计算机可读程序指令。
计算机可读存储介质可以是可以保持和存储由指令执行设备使用的指令的有形设备。计算机可读存储介质例如可以是――但不限于――电存储设备、磁存储设备、光存储设备、电磁存储设备、半导体存储设备或者上述的任意合适的组合。计算机可读存储介质的更具体的例子(非穷举的列表)包括:便携式计算机盘、硬盘、随机存取存储器(RAM)、只读存储器(ROM)、可擦式可编程只读存储器(EPROM或闪存)、静态随机存取存储器(SRAM)、便携式压缩盘只读存储器(CD-ROM)、数字多功能盘(DVD)、记忆棒、软盘、机械编码设备、例如其上存储有指令的打孔卡或凹槽内凸起结构、以及上述的任意合适的组合。这里所使用的计算机可读存储介质不被解释为瞬时信号本身,诸如无线电波或者其他自由传播的电磁波、通过波导或其他传输媒介传播的电磁波(例如,通过光纤电缆的光脉冲)、或者通过电线传输的电信号。
这里所描述的计算机可读程序指令可以从计算机可读存储介质下载到各个计算/处理设备,或者通过网络、例如因特网、局域网、广域网和/或无线网下载到外部计算机或外部存储设备。网络可以包括铜传输电缆、光纤传输、无线传输、路由器、防火墙、交换机、网关计算机和/或边缘服务器。每个计算/处理设备中的网络适配卡或者网络接口从网络接收计算机可读程序指令,并转发该计算机可读程序指令,以供存储在各个计算/处理设备中的计算机可读存储介质中。
用于执行本公开操作的计算机程序指令可以是汇编指令、指令集架构(ISA)指令、机器指令、机器相关指令、微代码、固件指令、状态设置数据、或者以一种或多种编程语言的任意组合编写的源代码或目标代码,所述编程语言包括面向对象的编程语言—诸如Smalltalk、C++等,以及常规的过程式编程语言—诸如“C”语言或类似的编程语言。计算机可读程序指令可以完全地在用户计算机上执行、部分地在用户计算机上执行、作为一个独立的软件包执行、部分在用户计算机上部分在远程计算机上执行、或者完全在远程计算机或服务器上执行。在涉及远程计算机的情形中,远程计算机可以通过任意种类的网络—包括局域网(LAN)或广域网(WAN)—连接到用户计算机,或者,可以连接到外部计算机(例如利用因特网服务提供商来通过因特网连接)。在一些实施例中,通过利用计算机可读程序指令的状态信息来个性化定制电子电路,例如可编程逻辑电路、现场可编程门阵列(FPGA)或可编程逻辑阵列(PLA),该电子电路可以执行计算机可读程序指令,从而实现本公开的各个方面。
这里参照根据本公开实施例的方法、装置(系统)和计算机程序产品的流程图和/或框图描述了本公开的各个方面。应当理解,流程图和/或框图的每个方框以及流程图和/或框图中各方框的组合,都可以由计算机可读程序指令实现。
这些计算机可读程序指令可以提供给通用计算机、专用计算机或其它可编程数据处理装置的处理器,从而生产出一种机器,使得这些指令在通过计算机或其它可编程数据处理装置的处理器执行时,产生了实现流程图和/或框图中的一个或多个方框中规定的功能/动作的装置。也可以把这些计算机可读程序指令存储在计算机可读存储介质中,这些指令使得计算机、可编程数据处理装置和/或其他设备以特定方式工作,从而,存储有指令的计算机可读介质则包括一个制造品,其包括实现流程图和/或框图中的一个或多个方框中规定的功能/动作的各个方面的指令。
也可以把计算机可读程序指令加载到计算机、其它可编程数据处理装置、或其它设备上,使得在计算机、其它可编程数据处理装置或其它设备上执行一系列操作步骤,以产生计算机实现的过程,从而使得在计算机、其它可编程数据处理装置、或其它设备上执行的指令实现流程图和/或框图中的一个或多个方框中规定的功能/动作。
附图中的流程图和框图显示了根据本公开的多个实施例的系统、方法和计算机程序产品的可能实现的体系架构、功能和操作。在这点上,流程图或框图中的每个方框可以代表一个模块、程序段或指令的一部分,所述模块、程序段或指令的一部分包含一个或多个用于实现规定的逻辑功能的可执行指令。在有些作为替换的实现中,方框中所标注的功能也可以以不同于附图中所标注的顺序发生。例如,两个连续的方框实际上可以基本并行地执行,它们有时也可以按相反的顺序执行,这依所涉及的功能而定。也要注意的是,框图和/或流程图中的每个方框、以及框图和/或流程图中的方框的组合,可以用执行规定的功能或动作的专用的基于硬件的系统来实现,或者可以用专用硬件与计算机指令的组合来实现。
以上已经描述了本公开的各实施例,上述说明是示例性的,并非穷尽性的,并且也不限于所披露的各实施例。在不偏离所说明的各实施例的范围的情况下,对于本技术领域的普通技术人员来说许多修改和变更都是显而易见的。本文中所用术语的选择,旨在最好地解释各实施例的原理、实际应用或对市场中的技术的改进,或者使本技术领域的其它普通技术人员能理解本文披露的各实施例。
- 心电图数据的分割处理方法、装置及可读存储介质
- 话音数据处理方法以及支持该话音数据处理方法的电子装置
- 一种数据处理方法、装置和用于数据处理的装置
- 一种数据处理方法、装置和用于数据处理的装置
- 一种数据处理方法、装置和用于数据处理的装置
- 一种无创胎儿心电检测装置及心电信号数据处理方法
- 一种无创胎儿心电检测装置及心电信号数据处理方法
