一种含外泌体衍生的丝素蛋白纳米颗粒水凝胶在治疗压疮性溃疡中的应用
文献发布时间:2023-06-19 19:20:08
技术领域
本发明涉及生物化学技术领域,更具体地说,它涉及一种含外泌体衍生的丝素蛋白纳米颗粒水凝胶在治疗压疮性溃疡中的应用。
背景技术
压疮病理机制是由于活动功能障碍,局部皮肤血管长期受压,使血液循环受阻,缺血、缺氧后导致组织溃烂坏死,出现压疮。当前治疗压疮的方法有解除压力、敷料保护、清创等,而减轻损伤、促进组织或溃疡修复主要是通过物理或手术的方式延缓压疮进展,尚没有针对压疮发生后血管缺血缺氧引起内皮细胞损伤的相关机制进行研究,也没有研究内皮细胞来源的外泌体及其携带的蛋白在抑制压疮发生发展中作用。
压疮有关的应用治疗包括清除坏死组织、保持伤口湿润、伤口敷料、压缩绷带和静电纺丝支架,主要为对症治疗和改善伤口环境促进愈合。新型三维针织面料可以使中性粒细胞弹性蛋白酶表达降低,转化生长因子水平升高促进细胞增殖;负压吸引等方法有效清除炎症分泌物及坏死物,促进组织愈合;清创、皮瓣移植及泡沫敷料刺激细胞增殖/迁移和血管生成,并促进伤口愈合和提高的伤口周围皮肤应力。与压疮发生及治疗相关的机制研究主要关注点为修复创面、实现抗菌、伤口酸化、增强微循环及细胞刺激。胚胎干细胞来源的外泌体通过激活Nrf2通路,抑制内皮细胞衰老,恢复因衰老而引起的血管功能障碍,加速小鼠的伤口愈合。冷大气压等离子体可以实现抗菌、伤口酸化、增强的微循环和细胞刺激促进组织重塑和内皮细胞增殖来促进伤口愈合。乳香标准化提取物通过协调机制发挥其促伤口愈合潜力,促进生长因子生成和抑制细胞凋亡,增加血管生成以加速压疮的伤口愈合。在压疮发生的过程中血管起到重要作用,目前尚没有研究对压疮发生过程中如何抑制缺氧引起内皮细胞发生铁死亡进行报道;在治疗研究中,也没有采用靶向性纳米颗粒抑制压疮部位血管损伤的研究报道。
研究表明,正常成熟的皮肤血管内皮不表达或低水平表达CD13分子,但本项目研究首次发现长期受压缺氧后,内皮细胞(ECs)表达CD13明显增加。NGR是含精氨酸、甘氨酸、天冬酰胺基序的多肽,而且是CD13的高亲和性配体,NGR肽含有氨基(-NH2)端,可与羧基(-COOH)端催化反应,丝素蛋白纳米颗粒表面有大量氨基(-NH2)端,也可以与羧基(-COOH)端催化反应,我们通过催化剂EDC和NSH将NGR肽与丝素蛋白纳米颗粒通过二羧酸聚乙烯醇(HOOC-PEG-COOH)交联在一起,从而使丝素蛋白纳米颗粒可以特异性靶向压疮部位血管。因此本项目中我们开发出的靶向血管的纳米颗粒,可以抑制血管内皮细胞因缺氧发生铁死亡,改善及预防压疮的形成,具有重要的临床意义和社会价值。
发明内容
本发明的目的是为了解决上述问题,提供一种含外泌体衍生的丝素蛋白纳米颗粒水凝胶在治疗压疮性溃疡中的应用,将纳米颗粒混合在丝素蛋白/胶原的水凝胶中,开发出一种靶向性治疗压疮的缓释载体,敷在受压皮肤上后,不仅可以保持压疮部位渗出液的吸收,而且NGR肽与内皮细胞表面的CD13分子结合后,MFGE8可被转运进内皮细胞,进而抑制由于缺氧引起的内皮细胞铁死亡,减少血管损伤,延缓或者抑制压疮的形成,减轻皮肤压疮的发生。
本发明的上述技术目的是通过以下技术方案得以实现的:一种外泌体衍生的丝素蛋白纳米颗粒的制备方法,包括以下步骤:
S1.丝素蛋白溶液制备;
S2.纳米颗粒的制备;
S3.外泌体中乳脂球表皮生长因子VIII(MFG-E8)的生产制备;
S4.MFGE8蛋白纯化;
S5.包被MFGE8的丝素蛋白纳米颗粒的制备;
S6.交联NGR肽的MFGE8-丝素蛋白纳米颗粒的制备。
本发明进一步设置为:丝素蛋白溶液的具体制备方法,包括以下步骤:
S1.取去除蚕蛹的家蚕蚕茧2g,放入1L水中,加入5-10gNa
S2.将去除丝胶的丝素在去离子水中洗涤3-5次,然后在60℃的烘箱中烘干;
S3.配制50ml三元溶液,配制方法:双蒸水,乙醇,氯化钙分别为30.43ml:19.57ml:24g;
S4.将蚕茧加入到三元溶液中,在60±5℃条件下溶解1-2h,直至丝素完全溶解成液体;4000rpm/min(3220g)离心10min,收集上清;
S5.将上清在截留分子量在8000-14000的透析袋中过滤48h,过滤完成后再4000rpm/min(3220g)离心10min,收集上清,并测定蛋白浓度。
本发明进一步设置为:纳米颗粒的具体制备方法,包括以下步骤:
S1.将获取的丝素蛋白溶液稀释到10mg/ml(1%),在15ml离心管中加入5ml丙酮溶液,将丙酮在涡旋混合器上涡旋,丙酮溶液与1%丝素蛋白溶液体积比为5:1,即将1ml质量分数为1%的丝素蛋白溶液滴加到丙酮中,滴加结束后,继续涡旋30-60s;
S2.涡旋结束后,离心6000rpm/min(3840g),10min,倒掉上清收集沉淀;
S3.加入双蒸水10ml洗涤,离心6000rpm/min(3840g),10min,倒掉上清收集沉淀,去除丙酮残留;
S4.重复步骤S3;
S5.在沉淀中加入5ml的双蒸水,在冰上进行超声,条件为:超声时间2min,暂停2s超声2s,振幅30%;
S6.超声结束后,6000rpm/min,离心10min,获取乳白色上清;
S7.乳白色上清继续12000rpm/min,离心10min,获得纳米粒子沉淀,冷冻干燥后,获得纳米粒子。
本发明进一步设置为:外泌体中乳脂球表皮生长因子VIII(MFG-E8)的具体生产制备方法,包括以下步骤:
S1.提取大鼠血管内皮原代细胞,进行扩增培养获得其分泌的外泌体;
S2.对外泌体进行质谱检测分析,结果表明MFGE8在在外泌体中的含量非常丰富;
S3.构建HBLV-r-MFGE8-3xFlag-Green-PURO转染慢病毒;
S4.37℃,5%CO
S5.3天后加入嘌呤霉素挑选转入MFGE8的CHO-s细胞;
S6.待含有绿色荧光的CHO-s细胞达到80%左右后进行胰酶消化,细胞消化下来后进行离心,1000rpm/min,离心5min,收集细胞沉淀,加入CHO-s细胞专用培养基在摇床上培养,摇床转速为150rpm/min,使CHO-s细胞悬浮培养;
S7.细胞在培养液生长,培养液由澄清变浑浊后进行离心1200rpm/min,离心5min,收集CHO-s细胞沉淀;
S8.将沉淀的细胞在加入蛋白酶抑制剂PMSF的细胞裂解液中进行冰上裂解30-60min,蛋白酶抑制剂PMSF体积分数为1%;
S9.裂解后进行超声,条件为:超声时间8s,暂停2s超声2s,振幅20%;
S10.4℃条件下离心12000rpm/min,离心10min;
S11.收集含有MFGE8蛋白上清。
本发明进一步设置为:MFGE8蛋白纯化的具体方法,包括以下步骤:
S1.按照500ul蛋白上清加入20ul的anti-Flag磁珠纯化MFGE8蛋白,在摇床上室温下孵育2h;
S2.磁分离,在磁力架上分离20s,去除上清;
S3.洗脱,每20ul磁珠悬浊液加入100ul的3xFlag多肽进行洗脱,室温下孵育30-60分钟;
S4.磁力架分离20s,上清为洗脱的Flag标签蛋白MFGE8;
S5.对纯化蛋白进行Westernblotting检测;
S6.MFGE8纯化蛋白的制备及检测。
本发明进一步设置为:包被MFGE8的丝素蛋白纳米颗粒的具体制备方法,包括以下步骤:
S1.将获取的丝素蛋白溶液稀释到20mg/ml(2%),并将500ul纯化MFGE8蛋白(0.93mg/ml)加入到500ul的2%丝素蛋白溶液中,使丝素蛋白浓度为1%;
S2.在15ml离心管中加入5ml丙酮溶液,将丙酮在涡旋混合器上涡旋,丙酮溶液与含有MFGE8纯化蛋白的丝素蛋白溶液体积比为5:1,即将1mlS1中的MFGE8-丝素蛋白溶液滴加到丙酮中,滴加结束后,继续涡旋30-60s;
S3.涡旋结束后,离心6000rpm/min(3840g),10min,倒掉上清收集沉淀;
S4.加入双蒸水10ml洗涤,离心6000rpm/min(3840g),10min,倒掉上清收集沉淀,去除丙酮残留;
S5.重复步骤S3;
S6.在沉淀中加入5ml的双蒸水,在冰上进行超声,条件为:超声时间3min,暂停3s超声2s,振幅30%;
S7.超声结束后,3000rpm/min,离心10min,获取乳白色上清;
S8.乳白色上清继续12000rpm/min,离心10min,获得纳米粒子沉淀,冷冻干燥后,获得包被MFGE8的丝素蛋白纳米颗粒;
S9.包被MFGE8丝素蛋白纳米颗粒检测。
本发明进一步设置为:交联NGR肽的MFGE8-丝素蛋白纳米颗粒的具体制备方法,包括以下步骤:
S1.取包被MFGE8的丝素蛋白纳米颗粒(由500ul的2%丝素蛋白溶液与500ul纯化MFGE8蛋白(0.93mg/ml)生产),加入1ml双蒸水溶解纳米颗粒;
S2.在1ml纳米颗粒溶液中加入10mgEDC,50mgHOOC-PEG-COOH及50mgNGR肽,在室温下、摇床上反应0.5-1h;
S3.再加入10mg的NSH,在室温下、摇床上反应过夜;
S4.第二天将纳米颗粒溶液在6000rpm/min条件下离心10min,丢弃上清,获得交联NGR肽的MFGE8-丝素蛋白纳米颗粒的制备沉淀纳米颗粒。
本发明还提出了一种富含交联NGR肽的MFGE8-丝素蛋白纳米颗粒的胶原/丝素蛋白水凝胶制备方法,包括以下步骤:
S1.将提取的丝素蛋白溶液在10%-15%的聚乙烯醇20000溶液浓缩48h,使丝素蛋白溶液最终浓度为8%-10%;
S2.取卡波姆0.24g,溶解到1ml的双蒸水中;
S3.取聚乙烯醇2g溶解于10ml的双蒸水中,使其质量分数为20%;
S4.取800ul的1mol/L的NaOH溶液加入到卡波姆溶液中,搅拌均匀,然后再加入800ul的20%聚乙烯醇;
S5.取8%-10%丝素蛋白溶液4ml,加入到卡波姆溶液中搅拌均匀;
S6.取2ml质量分数为1%胶原溶液,并加入1mol/L的NaOH的200ul混合均匀后,加入到卡波姆溶液中;
S7.取交联NGR肽的MFGE8-丝素蛋白纳米颗粒溶解在200ul的双蒸水中,并加入到卡波姆溶液中搅拌均匀;
S8.调节PH值至6-7之间;
S9.在湿润的环境中放置12-24h,直至其交联成胶;
S10.检测胶原/丝素蛋白水凝胶中纳米颗粒。
综上所述,本发明具有以下有益效果:
本发明的一种含外泌体衍生的丝素蛋白纳米颗粒水凝胶,作为一种无创治疗手段在临床应用中更能得到患者的认可,而且靶向纳米治疗,能针对性提高患者的治疗效果。在后续的应用研究中,我们可以在动物实验的基础上开展相应临床应用研究,应用转化后不仅可以为压疮患者提供一种新的治疗手段,还将产生巨大的社会经济价值。
附图说明
图1是本发明实施例中外泌体进行质谱检测分析图;
图2是本发明实施例中MFGE8纯化蛋白检测图;
图3是本发明实施例中包被MFGE8丝素蛋白纳米颗粒检测图;
图4是本发明实施例中交联NGR肽的MFGE8-丝素蛋白纳米颗粒检测图;
图5是本发明实施例中交联NGR肽的MFGE8-丝素蛋白纳米颗粒的细胞摄取实验图;
图6是本发明实施例中胶原水凝胶示意图;
图7是本发明实施例中胶原水凝胶电镜检测图;
图8是本发明实施例中胶原水凝胶储能模量G’和损耗模量G”检测图;
图9是本发明实施例中丝素蛋白水凝胶示意图;
图10是本发明实施例中丝素蛋白水凝胶电镜检测图;
图11是本发明实施例中丝素蛋白水凝胶储能模量G’和损耗模量G”检测图;
图12是本发明实施例中胶原/丝素蛋白水凝胶示意图;
图13是本发明实施例中胶原/丝素蛋白水凝胶电镜检测图;
图14是本发明实施例中胶原/丝素蛋白水凝胶储能模量G’和损耗模量G”检测图;
图15是本发明实施例中胶原/丝素蛋白水凝胶中纳米颗粒检测图;
图16是本发明实施例中压疮缺氧部位MFGE8和CD13表达情况免疫荧光检测图;
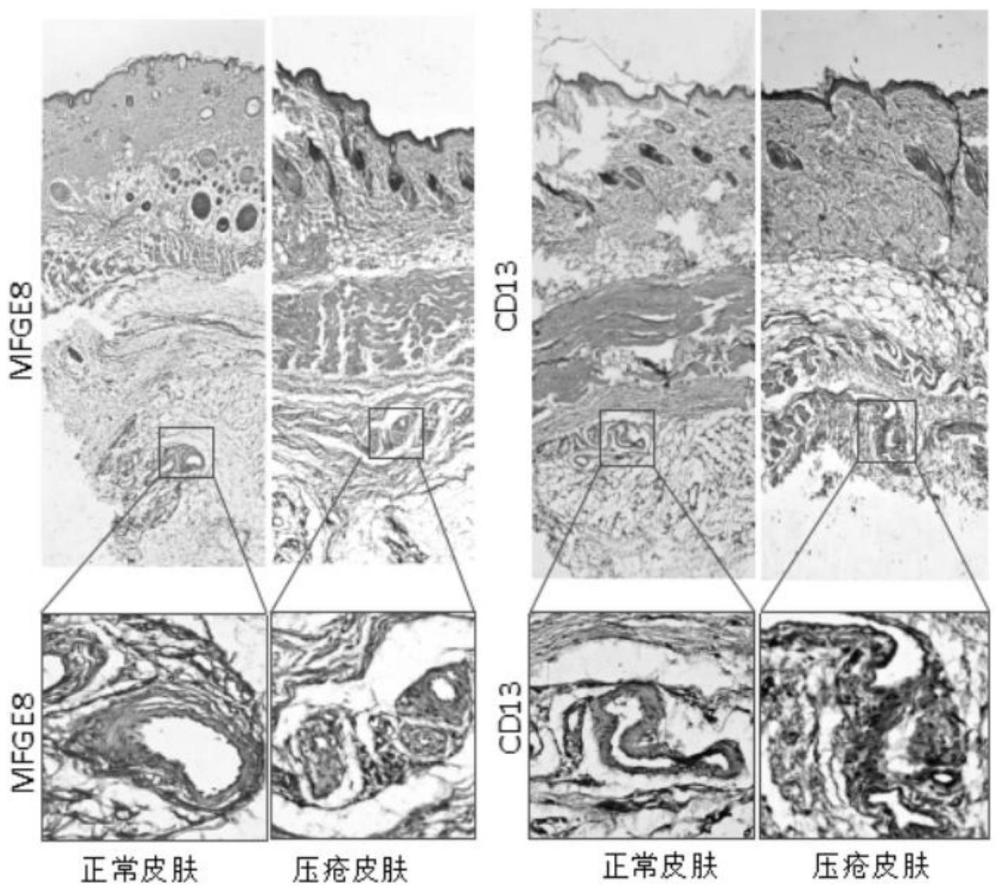
图17是本发明实施例中压疮缺氧部位MFGE8和CD13表达情况免疫组化检测图;
图18是本发明实施例中交联NGR肽的MFGE8-丝素蛋白纳米颗粒靶向组织血管检测图;
图19是本发明实施例中动物皮肤溃疡修复及统计分析图;
图20是本发明实施例中动物Masson染色检测溃疡修复情况图。
具体实施方式
为了使本技术领域的人员更好地理解本发明方案,下面将结合本发明的实施例及附图,对本发明的技术方案进行进一步详细地描述,显然,所描述的实施例仅仅是本发明一部分的实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都应当属于本发明保护的范围。
需要说明的是,在不冲突的情况下,本发明中的实施例及实施例中的特征可以相互组合。下面将结合实施例来详细说明本发明。
实施例:
如图1-20所示,一种含外泌体衍生的丝素蛋白纳米颗粒水凝胶在治疗压疮性溃疡中的应用,一种外泌体衍生的丝素蛋白纳米颗粒的制备方法,包括以下步骤:
S1.丝素蛋白溶液制备;
S2.纳米颗粒的制备;
S3.外泌体中乳脂球表皮生长因子VIII(MFG-E8)的生产制备;
S4.MFGE8蛋白纯化;
S5.包被MFGE8的丝素蛋白纳米颗粒的制备;
S6.交联NGR肽的MFGE8-丝素蛋白纳米颗粒的制备。
丝素蛋白溶液的具体制备方法,包括以下步骤:
S1.取去除蚕蛹的家蚕蚕茧2g,放入1L水中,加入5-10gNa
S2.将去除丝胶的丝素在去离子水中洗涤3-5次,然后在60℃的烘箱中烘干;
S3.配制50ml三元溶液,配制方法:双蒸水,乙醇,氯化钙分别为30.43ml:19.57ml:24g;
S4.将蚕茧加入到三元溶液中,在60±5℃条件下溶解1-2h,直至丝素完全溶解成液体;4000rpm/min(3220g)离心10min,收集上清;
S5.将上清在截留分子量在8000-14000的透析袋中过滤48h,过滤完成后再4000rpm/min(3220g)离心10min,收集上清,并测定蛋白浓度。
纳米颗粒的具体制备方法,包括以下步骤:
S1.将获取的丝素蛋白溶液稀释到10mg/ml(1%),在15ml离心管中加入5ml丙酮溶液,将丙酮在涡旋混合器上涡旋,丙酮溶液与1%丝素蛋白溶液体积比为5:1,即将1ml质量分数为1%的丝素蛋白溶液滴加到丙酮中,滴加结束后,继续涡旋30-60s;
S2.涡旋结束后,离心6000rpm/min(3840g),10min,倒掉上清收集沉淀;
S3.加入双蒸水10ml洗涤,离心6000rpm/min(3840g),10min,倒掉上清收集沉淀,去除丙酮残留;
S4.重复步骤S3;
S5.在沉淀中加入5ml的双蒸水,在冰上进行超声,条件为:超声时间2min,暂停2s超声2s,振幅30%;
S6.超声结束后,6000rpm/min,离心10min,获取乳白色上清;
S7.乳白色上清继续12000rpm/min,离心10min,获得纳米粒子沉淀,冷冻干燥后,获得纳米粒子。
外泌体中乳脂球表皮生长因子VIII(MFG-E8)的具体生产制备方法,包括以下步骤:
S1.提取大鼠血管内皮原代细胞,进行扩增培养获得其分泌的外泌体;
S2.对外泌体进行质谱检测分析,结果表明MFGE8在在外泌体中的含量非常丰富;
S3.构建HBLV-r-MFGE8-3xFlag-Green-PURO转染慢病毒;
S4.37℃,5%CO
S5.3天后加入嘌呤霉素挑选转入MFGE8的CHO-s细胞;
S6.待含有绿色荧光的CHO-s细胞达到80%左右后进行胰酶消化,细胞消化下来后进行离心,1000rpm/min,离心5min,收集细胞沉淀,加入CHO-s细胞专用培养基在摇床上培养,摇床转速为150rpm/min,使CHO-s细胞悬浮培养;
S7.细胞在培养液生长,培养液由澄清变浑浊后进行离心1200rpm/min,离心5min,收集CHO-s细胞沉淀;
S8.将沉淀的细胞在加入蛋白酶抑制剂PMSF的细胞裂解液中进行冰上裂解30-60min,蛋白酶抑制剂PMSF体积分数为1%;
S9.裂解后进行超声,条件为:超声时间8s,暂停2s超声2s,振幅20%;
S10.4℃条件下离心12000rpm/min,离心10min;
S11.收集含有MFGE8蛋白上清。
MFGE8蛋白纯化的具体方法,包括以下步骤:
S1.购买Flag标签蛋白免疫沉淀试剂盒(磁珠法)
S2.按照500ul蛋白上清加入20ul的anti-Flag磁珠纯化MFGE8蛋白,在摇床上室温下孵育2h;
S3.磁分离,在磁力架上分离20s,去除上清;
S4.洗脱,每20ul磁珠悬浊液加入100ul的3xFlag多肽进行洗脱,室温下孵育30-60分钟;
S5.磁力架分离20s,上清为洗脱的3xFlag标签蛋白MFGE8;
S6.对纯化蛋白进行Westernblotting检测;
S7.MFGE8纯化蛋白的制备及检测。
包被MFGE8的丝素蛋白纳米颗粒的具体制备方法,包括以下步骤:
S1.将获取的丝素蛋白溶液稀释到20mg/ml(2%),并将500ul纯化MFGE8蛋白加入到500ul的2%丝素蛋白溶液中,使丝素蛋白浓度为1%;
S2.在15ml离心管中加入5ml丙酮溶液,将丙酮在涡旋混合器上涡旋,丙酮溶液与含有MFGE8纯化蛋白的丝素蛋白溶液体积比为5:1,即将1mlS1的MFGE8-丝素蛋白溶液滴加到丙酮中,滴加结束后,继续涡旋30-60s;
S3.涡旋结束后,离心6000rpm/min(3840g),10min,倒掉上清收集沉淀;
S4.加入双蒸水10ml洗涤,离心6000rpm/min(3840g),10min,倒掉上清收集沉淀,去除丙酮残留;
S5.重复步骤S3;
S6.在沉淀中加入5ml的双蒸水,在冰上进行超声,条件为:超声时间3min,暂停3s超声2s,振幅30%;
S7.超声结束后,3000rpm/min,离心10min,获取乳白色上清;
S8.乳白色上清继续12000rpm/min,离心10min,获得纳米粒子沉淀,冷冻干燥后,获得包被MFGE8的丝素蛋白纳米颗粒;
S9.包被MFGE8丝素蛋白纳米颗粒检测。
交联NGR肽的MFGE8-丝素蛋白纳米颗粒的具体制备方法,包括以下步骤:
S1.购买NGR肽,二羧酸聚乙二醇(HOOC-PEG-COOH),及EDC(1-(3-二甲氨基丙基)-3-乙基碳二亚胺),NHS(N-羟基琥珀酰亚胺)
S2.取包被MFGE8的丝素蛋白纳米颗粒(由500ul的2%丝素蛋白溶液与500ul纯化MFGE8蛋白生产),加入1ml双蒸水溶解纳米颗粒;
S3.在1ml纳米颗粒溶液中加入10mgEDC,50mgHOOC-PEG-COOH及50mgNGR肽,在室温下、摇床上反应0.5-1h;
S4.再加入10mg的NSH,在室温下、摇床上反应过夜;
S5.第二天将纳米颗粒溶液在6000rpm/min条件下离心10min,丢弃上清,获得交联NGR肽的MFGE8-丝素蛋白纳米颗粒的制备沉淀纳米颗粒。
进行交联NGR肽的MFGE8-丝素蛋白纳米颗粒检测。
进行交联NGR肽的MFGE8-丝素蛋白纳米颗粒的细胞摄取实验。
胶原/丝素蛋白水凝胶制备方法,包括以下步骤:
S1.取一只大鼠,用戊巴比妥钠麻醉,然后断颈处死。
S2.取下尾部,浸泡在75%酒精中5min,然后PBS盐溶液或生理盐水洗2-3次。
S3.剥除皮肤,暴露出尾部白色胶原。
S4.取下尾部胶原,剪碎至1-3mm3大小,PBS盐溶液或生理盐水洗涤1次。
S5.离心4000rpm/min(3220g),离心5min,倒掉上清。
S6.沉淀中加入体积分数为0.5%-1%的乙酸溶液的100ml。
S7.在4℃条件下,摇床上摇动溶解48h。
S8.完全溶解后,4℃条件下8000rpm/min离心10min,收集上清。
S9.上清在10%NaCl溶液中搅拌盐析10min,可见10%NaCl溶液中有大量絮状胶原析出。
S10.将析出的胶原在4℃条件下8000rpm/min离心10min,收集胶原沉淀。
S11.加入50-100ml的0.1mmol/L的盐酸溶液进行溶解胶原沉淀。
S12.将溶解后的胶原溶液冷冻干燥,-80℃长期保存。
胶原水凝胶制备方法
取胶原粉末100-150mg,溶解到10ml的0.1mmol/L盐酸溶液中,加入适量的1mol/LNaOH,使胶原溶液的PH值为中性,在37℃条件下交联,5-10min后形成胶原水凝胶,检测水凝胶特性。
丝素蛋白水凝胶制备方法,包括以下步骤:
S1.将提取的丝素蛋白溶液在10%-15%的聚乙烯醇20000溶液浓缩48h,使丝素蛋白溶液最终浓度为8%-10%。
S2.取卡波姆0.24g,溶解到3ml的双蒸水中。
S3.取聚乙烯醇2g溶解于10ml的双蒸水中,使其质量分数为20%。
S4.取800ul的1mol/L的NaOH溶液加入到卡波姆溶液中,搅拌均匀,然后再加入800ul的20%聚乙烯醇。
S5.加8%-10%丝素蛋白溶液4ml,搅拌均匀。
S6.调节PH值至6-7之间。
S7.在湿润的环境中放置12-24h,直至其交联成胶。
S8.检测水凝胶特性。
胶原/丝素蛋白水凝胶制备方法,包括以下步骤:
S1.将提取的丝素蛋白溶液在10%-15%的聚乙烯醇20000溶液浓缩48h,使丝素蛋白溶液最终浓度为8%-10%。
S2.取卡波姆0.24g,溶解到1ml的双蒸水中。
S3.取聚乙烯醇2g溶解于10ml的双蒸水中,使其质量分数为20%。
S4.取800ul的1mol/L的NaOH溶液加入到卡波姆溶液中,搅拌均匀,然后再加入800ul的20%聚乙烯醇。
S5.加8%-10%丝素蛋白溶液4ml,搅拌均匀。
S6.取2ml质量分数为1%胶原溶液,并加入1mol/L的NaOH的200ul混合均匀后,加入到卡波姆溶液中。
S7.调节PH值至6-7之间。
S8.在湿润的环境中放置12-24h,直至其交联成胶。
S9.检测胶原/丝素蛋白水凝胶。
本发明还提出了一种富含交联NGR肽的MFGE8-丝素蛋白纳米颗粒的胶原/丝素蛋白水凝胶制备方法,包括以下步骤:
S1.将提取的丝素蛋白溶液在10%-15%的聚乙烯醇20000溶液浓缩48h,使丝素蛋白溶液最终浓度为8%-10%;
S2.取卡波姆0.24g,溶解到1ml的双蒸水中;
S3.取聚乙烯醇2g溶解于10ml的双蒸水中,使其质量分数为20%;
S4.取800ul的1mol/L的N一种含外泌体衍生的丝素蛋白纳米颗粒水凝胶在治疗压疮性溃疡中的应用OH溶液加入到卡波姆溶液中,搅拌均匀,然后再加入800ul的20%聚乙烯醇;
S5.取8%-10%丝素蛋白溶液4ml,加入到卡波姆溶液中搅拌均匀;
S6.取2ml质量分数为1%胶原溶液,并加入1mol/L的NaOH的200ul混合均匀后,加入到卡波姆溶液中;
S7.取交联NGR肽的MFGE8-丝素蛋白纳米颗粒溶解在200ul的双蒸水中,并加入到卡波姆溶液中搅拌均匀;
S8.调节PH值至6-7之间;
S9.在湿润的环境中放置12-24h,直至其交联成胶;
S10.检测胶原/丝素蛋白水凝胶中纳米颗粒。
压疮缺氧部位MFGE8和CD13表达情况检测。
交联NGR肽的MFGE8-丝素蛋白纳米颗粒靶向组织血管检测。
进行动物实验,并分析动物皮肤溃疡修复情况以及Masson染色检测溃疡修复情况。
作用机理:本发明根据外泌体中携带的关键蛋白,开发出靶向血管的纳米颗粒,抑制血管内皮细胞因缺氧引起的铁死亡,预防及改善压疮的形成。我们首先提取内皮细胞内皮细胞外泌体,质谱检测分析出其携带重要蛋白MFGE8;随后使用CH-sO细胞生产纯化MFGE8蛋白,然后制备包裹MFGE8的丝素蛋白纳米颗粒;压疮后,血管内皮细胞缺血缺氧,CD13表达增加,根据此现象,合成与血管内皮上CD13特异性结合的NGR肽;其次,NGR肽的氨基团(-NH2)和丝素蛋白纳米颗粒的氨基团(-NH2)通过与HOOC-PEG-COOH交联,合成NGR肽与丝素蛋白纳米颗粒交联的靶向性纳米颗粒,靶向缺血缺氧的血管,抑制内皮细胞线粒体自噬及铁死亡的发生。胶原水凝胶富含水,而且空隙较大,胶原蛋白促进细胞生长;丝素蛋白水凝胶强度相对较大,含水较少,而且含有的多种促进细胞增殖的氨基酸及多肽;根据胶原水凝胶和丝素蛋白水凝胶的特点,我们将两种水凝胶按照一定比例配制丝素蛋白/胶原水凝胶,较好的保存两种水凝胶的特点。构建动物模型后,将靶向性纳米颗粒与制备的丝素蛋白/胶原水凝胶混合,构建缓释载体,释放抑制线粒体自噬及铁死亡发生的丝素蛋白纳米颗粒,敷在皮肤上进行相应的靶向性治疗,并分析相应的治疗效果。
本具体实施例仅仅是对本发明的解释,其并不是对本发明的限制,本领域技术人员在阅读完本说明书后可以根据需要对本实施例做出没有创造性贡献的修改,但只要在本发明的权利要求范围内都受到专利法的保护。
- 一种检测外泌体中miRNA-1246的纳米金核酸探针及其制备方法和应用
- 一种用于捕获血液中外泌体的磁性纳米颗粒的制备方法及其应用
- 负载干细胞外泌体的丝素纳米纤维水凝胶的制作工艺
- 一种外泌体、外泌体的制备方法及其在制备治疗脓毒症药物或者制剂中的应用
