一株耐受重金属铜和锌的链霉菌HG2-8-2及其应用
文献发布时间:2023-06-19 19:28:50
技术领域
本发明涉及生物领域,具体涉及一株耐受重金属铜和锌的链霉菌HG2-8-2及其应用。
背景技术
近年来由于工农业的迅速发展,环境问题日趋严重,如采矿工与冶金工业的快速增长,导致环境重金属污染越来越严重,废弃重金属矿区污染成为全世界面临的严重环境问题之一。重金属由于具有毒性强、不能降解、易富集、能在食物链中传递且具有致癌性等特性,对生态环境和人类健康都有潜在威胁。铜污染是常见的重金属污染。铜矿的开采、尾矿的堆积、工业废水的排放、含铜农药的使用等因素都会使得土壤中铜元素积累过多。铜元素被植物吸收后停留在根部,阻碍根系对其它成分特别是对铁元素的吸收,导致植物生长不良。而且过多的铜进入人体内导致人体出现恶心、呕吐、上腹疼痛、急性溶血和肾小管变形等中毒现象。金属锌本身无毒,但如果长期饮用锌污染的水,或食用土地锌污染的农作物,或呼吸锌尘污染的空气,会导致急性和慢性锌中毒如呕吐、腹泻等胃肠道、贫血、头晕和疲劳等症状。
目前对于重金属土壤污染的修复技术包括物理修复、化学修复、植物修复、微生物修复、联合修复等。传统的物理修复方式工程量大、成本高、而且难以应用到大面积的土壤修复治理中;化学修复的操作过程相对复杂,同时会破坏土壤结构,导致土壤肥力下降,可能存在二次污染;植物修复因其成本低廉,不存在二次污染,是一种绿色环保的土壤重金属污染修复技术,但其存在生物量小、生长周期长等弊端,单一的植物修复很难达到理想的效果。采用微生物吸附去除重金属己成为一个新兴的、环境友好且不引入二次污染的技术。
放线菌作为土壤中三大微生物类群之一,种类繁多,代谢功能各异,是一类能产生活性物质且用途广泛的微生物资源,其常被用于植物促生和病虫害的生物防治等方面研究。链霉菌是最高等的放线菌,菌丝纤细、无隔、多核、分枝,革兰氏阳性,菌丝体发达,分化成基内菌丝和气生菌丝,后者成熟后发育成孢子丝,其形态多样,可裂生大量分生孢子进行散播、繁殖。菌落小而致密、干燥不透明,幼时表面光滑、边缘整齐、颜色单调、不易挑起,继而发展成绒毛状、表面起粉、色泽丰富,正反面颜色不同。已报道的放线菌有千余种,主要分布于土壤中。已知放线菌所产抗生素的90%由本属产生。孙敬组等人发现密旋链霉菌能抑制草莓土传病害,具有防病促生的功能;何斐等人发现娄彻氏链霉菌对魔芋软腐病有较强的拮抗作用,还对魔芋生长有促进作用;也有研究发现,链霉菌Streptomyces sp.)细胞壁能够结合94.7%的Cr,使CrO
本研究通过分离和筛选耐重金属铜和锌的链霉菌,探查链霉菌对重金属胁迫下的含羞草幼苗生长的影响,以丰富功能链霉菌资源。
发明内容
针对上述技术问题,本发明的首要目的是提供一株耐受重金属铜和锌的链霉菌(Streptomyces sp.)HG2-8-2,所述的链霉菌HG2-8-2于2022年10月27日保藏于广东省微生物菌种保藏中心,保藏编号为GDMCC No:62932。
本发明的第二目的是提供一种菌剂,所述的菌剂包括所述的链霉菌HG2-8-2。
本发明的第三目的是提供一种菌株发酵液,所述的发酵液是利用所述的链霉菌HG2-8-2发酵所得。
本发明的第四目的是提供所述的链霉菌HG2-8-2,或所述的菌剂,或所述的菌株发酵液在重金属铜污染土壤修复中的应用。
本发明的第五目的是提供所述的链霉菌HG2-8-2,或所述的菌剂,或所述的菌株发酵液在重金属锌污染土壤修复中的应用。
本发明的第六目的是提供所述的链霉菌HG2-8-2,或所述的菌剂,或所述的菌株发酵液在促进重金属胁迫环境下植物生长中的应用。
优选的,所述的重金属为铜和/或锌。
优选的,所述的植物为含羞草。
本发明的第七目的是提供一种植物促生剂,所述植物促生剂含有所述的链霉菌HG2-8-2。
本发明的第八目的是提供一种土壤修复剂,所述的土壤修复剂含有所述的链霉菌HG2-8-2。
本发明的有益效果是:(1)本发明提供了一株耐受重金属铜和锌的链霉菌(Streptomyces sp.)HG2-8-2,所述的链霉菌HG2-8-2于2022年10月27日保藏于广东省微生物菌种保藏中心,保藏编号为GDMCCNo:62932。(2)本发明所述的链霉菌HG2-8-2能够耐受一定浓度的铜和锌污染,并且能够有效去除环境中的铜离子和锌离子;可用于重金属铜污染土壤的修复。(3)在受铜污染的环境中,浸染链霉菌HG2-8-2的含羞草幼苗根长、茎长、幼苗鲜重均显著大于未染菌处理的,链霉菌HG2-8-2对含羞草幼苗生长的促生作用明显。(4)在受锌污染的环境中,链霉菌HG2-8-2可有效解除锌离子对含羞草幼苗的胁迫,对含羞草幼苗生长有明显促生作用。
附图说明
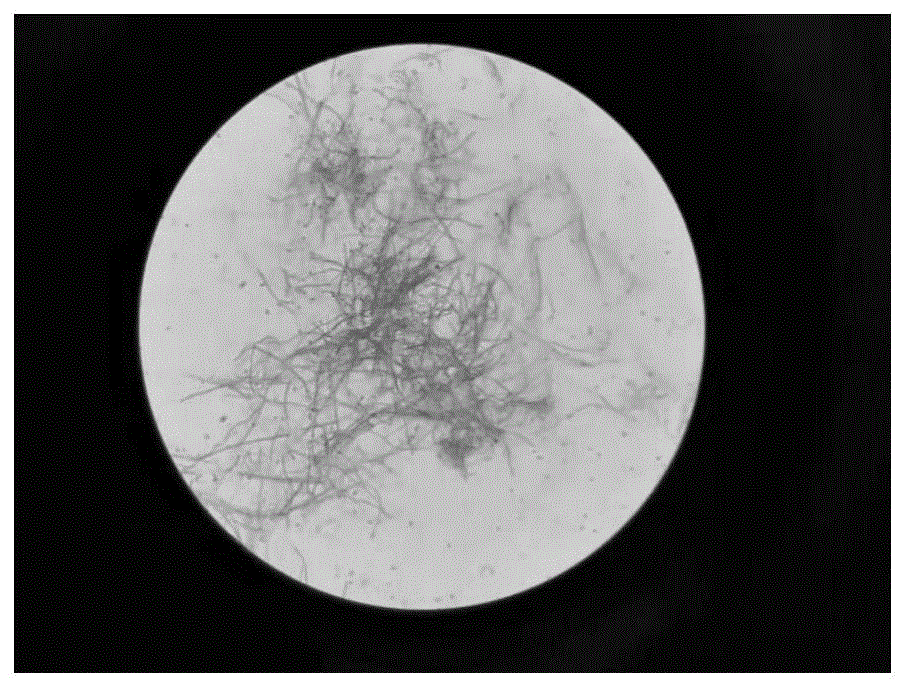
图1菌株HG2-8-2显微照片
图2琼脂糖凝胶电泳图
图3链霉菌HG2-8-2对重金属铜耐受性
图4链霉菌HG2-8-2对重金属锌耐受性
图5链霉菌HG2-8-2对重金属铜的去除率
图6链霉菌HG2-8-2对重金属锌的去除率
图7链霉菌HG2-8-2对重金属铜胁迫下含羞草根长的影响
图8链霉菌HG2-8-2对重金属铜胁迫下含羞草茎长的影响
图9链霉菌HG2-8-2对重金属铜胁迫下含羞草幼苗鲜重的影响
图10染菌组比未染菌组含羞草幼苗各指标增加的倍数
图11染菌组比未染菌组含羞草幼苗各指标增加的量
图12链霉菌HG2-8-2对重金属锌胁迫下含羞草根长的影响
图13链霉菌HG2-8-2对重金属锌胁迫下含羞草茎长的影响
图14链霉菌HG2-8-2对重金属锌胁迫下含羞草幼苗鲜重的影响
图15染菌组比未染菌组含羞草幼苗各指标增加的倍数
图16染菌组比未染菌组含羞草幼苗各指标增加的倍数
具体实施方式
下面结合具体实施例对本发明的保护范围进行详细的阐述,应当说明的是,本发明的保护范围并不受以下实施例的限制。
实施例一、菌株的分离及鉴定
1.菌株分离
1.1样品采集
供试土壤样品采自广东潮州韩钢(潮州市潮安县)周边的杂草地(116°67'E,23°64'N),在杂草地选5个取点,样点之间距离>50m。取样时,去除土壤表面枯枝落叶和杂草,取0~10cm的土壤样品,5个样点的土样充分混合均匀、过100目筛。
1.2高氏一号培养基制备
可溶性淀粉20g,NaCl 5g,KNO
称取20g可溶性淀粉于小烧杯中,加入10ml自来水调成糊状,倒入大烧杯与90ml热水混匀。分别称取其它药品,加入淀粉溶液中,搅拌使其溶解,pH调至7.2~7.4。加入琼脂粉,加热搅拌后装到锥形瓶内,于高温高压灭菌锅内121℃0.103MPa灭菌20min,培养基略冷却后倒入无菌平皿中,制成无菌平板,待用。
1.3土壤稀释样液制备
称取1.1中所述混合均匀的1g土壤样品于装有玻璃珠的锥形瓶中,加99mL无菌水,振荡10min后得10
1.4分离菌株
在超净台中取无菌平板多套,用移液枪各取0.2mL10
2菌株筛选
2.1制备菌悬液
制备高氏一号液体培养基,在高压锅进行灭菌;用接种环将1.4中所述67株放线菌分别接到50ml液体培养基中,制成菌悬液,以150r/min、28℃摇床培养3-5d。
2.2耐重金属铜的菌株筛选
(1)初筛配制含Cu
(2)复筛
将初筛中筛选出6株耐受Cu
2.3耐重金属锌的菌株筛选
(1)制备含重金属锌的高氏一号培养基
重金属Zn
(2)耐重金属锌的菌株筛选
以移液枪将2.1中所述的各种菌株菌悬液0.1ml分别接种到上述含重金属Zn
3菌株HG2-8-2菌落和细胞特征
菌株HG2-8-2菌落呈现平坦光滑的凹凸状。菌丝纤细、无隔、分枝,革兰氏阳性,菌丝体发达,气生菌丝成熟后发育成孢子丝。菌落的孢子堆为白色,属于白孢类群。其显微镜照片如图1所示。
4菌株HG2-8-2的16S rDNA测序鉴定
(1)基因组DNA提取
采用柱式法提取,具体过程如下:
1)取2ml离心管,加入200μL预处理液和少许玻璃珠,然后加入适量菌样品,放入研磨仪中研磨至充分。
2)加入20μLProteinase K,加入200μL裂解液,充分颠倒混匀,70℃放置10min。
3)加200μL无水乙醇,充分颠倒混匀,短离心以去除管盖内壁液滴。
4)过吸附柱,洗涤液洗1次,漂洗液洗2次。
5)吸附柱室温放置3~5分钟,以彻底晾干吸附材料中残余的漂洗液。
6)将吸附转入一个新离心管,向吸附膜中间位置悬空滴加50~100μL dd
H
(2)PCR扩增
16s引物序列:
Primer1(27f):AGAGTTTGATCMTGGCTCAG
Primer2(1492R):TACGGYTACCTTGTTACGACTT
Primer3(V4-515F):GTGCCAGCAGCCGCGGTAA
PCR扩增反应体系:
PCR Mix21μL;PrimerF(5P)1μL;PrimerR(5P)1μL;DNA模板(ng/μL)2μL;总体积25μL。
反应条件:
1.96℃5min
2.96℃20sec;62℃30sec;72℃30sec;35cycles
3.72℃10min
4.4℃forever
(3)PCR产物检测及纯化
3μL PCR产物进行1.0%的琼脂糖凝胶检测,观察条带性状。
电泳条件:3μL样品+1%琼脂糖凝胶,Marker条带组成:100bp,250bp,500bp,750bp,1000bp,2000bp,3000bp,5000bp。750bp条带浓度为60ng/3μL,显示为加亮带,其余条带浓度均为30ng/3μL。电泳方向从下向上。
(4)测序将纯化后的PCR产物上机测序。测序结果进行NCBI-BLAST比对。
NCBI链接:https://www.ncbi.nlm.nih.gov/。
5测序结果
(1)琼脂糖凝胶电泳图
琼脂糖凝胶电泳图如图2所示,电泳孔位1对应样品HG2-8-2菌株。目的条带清晰,无断裂,无拖尾,浓度可观;Mark清晰,能表征条带的大小。(扩增引物:27F+1492R;测序引物:V4-515F+V4-806R)。
(2)基因序列
菌株HG2-8-28的16S rDNA序列如SEQ ID No.1所示。
(3)blast结果
根据blast结果,所述菌株HG2-8-2与Streptomyces sp.KF815090.1亲源关系最近(99.51%),因此,判定HG2-8-2菌株为链霉菌属(Streptomyces sp.)菌株,其全称为链霉菌(Streptomyces sp.)HG2-8-2,并于2022年10月27日保藏于广东省微生物菌种保藏中心,保藏编号为:GDMCC No:62932,保藏地址为广州市先烈中路100号大院59号楼5楼,广东省科学院微生物研究所,联系电话为020-87137633,E-mail:gdmcc@gdim.cn。
应当说明的是,在以下实施例中,将链霉菌(Streptomyces sp.)HG2-8-2简写为链霉菌HG2-8-2,二者具有相同的含义。
实施例二、链霉菌HG2-8-2对重金属铜和锌的耐受性
1.对铜的耐受性
配制含Cu
实验结果如图3所示,随Cu
2对锌的耐受性
配制含Zn
实验结果如图4所示,Zn
实施例三、链霉菌HG2-8-2对重金属铜和锌的去除率
1.链霉菌HG2-8-2对重金属铜的去除率
(1)激活链霉菌HG2-8-2菌:首先将链霉菌HG2-8-2菌株在固体高氏一号培养基上划线接种,在温度条件为28℃的培养箱里培养5d至菌苔丰满。
(2)制备菌悬液:用接种环在培养丰满的菌苔上挑选一环菌落于50mL液体培养基中(100mL锥形瓶),以150r/min 28℃摇床培养5d,装入10ml橙色离心管中,以4000rpm/min离心10min,弃去上清液,得到菌悬液。
(3)铜标准溶液的制备:称取0、0.01、0.02、0.03、0.04g的CuSO
(4)铜与链霉菌HG2-8-2混合培养液的制备:将步骤(2)所述菌悬液吸取0.5ml加到浓度为0、50、100、150、200mg/L的铜溶液(50ml)中,摇床培养24h(转速为150r/min,温度为28℃),得到铜与链霉菌HG2-8-2混合培养液。吸取培养24h含不同浓度Cu
(5)重金属铜去除率的测定
将步骤(3)所述Cu
结果如图5所示,在Cu
2.链霉菌HG2-8-2对重金属锌的去除率
(1)激活链霉菌HG2-8-2:同上;
(2)制备链霉菌HG2-8-2菌悬液:同上;
(3)锌标准溶液的制备:称取0、0.02、0.04、0.06、0.08g的ZnSO
(4)锌与链霉菌HG2-8-2混合培养液的制备:将步骤(2)所述菌悬液吸取0.5ml加到浓度为0、400、800、1200、1600mg/L的锌溶液(50ml)中,摇床培养24h(转速为150r/min,温度为28℃),得到锌与链霉菌HG2-8-2混合培养液。吸取培养24h含不同浓度Zn
(5)重金属锌去除率的测定:
将步骤(3)所述标准溶液放入火焰原子吸收光谱仪进行测定锌的含量及绘制出标准曲线,标准曲线公式为:y=0.0121X+0.0019,得到初始浓度。将步骤(4)所述含锌的链霉菌HG2-8-2培养液(混合培养液)在火焰原子吸收光谱仪测定OD值,根据标准曲线公式及链霉菌HG2-8-2混合培养液的OD,得到培养24h后Zn
结果如图6所示,链霉菌HG2-8-2在锌溶液浓度为400-1600mg/L的范围内,随着Zn
实施例四、链霉菌HG2-8-2对受铜污染的含羞草促生作用
1.实验过程
(1)种子处理用75%酒精进行消毒3min,在超净工作台中用无菌水将种子冲洗5次,并用已灭菌的吸水纸将种子表面的水吸干。将含羞草种子置于65℃的温水浸泡15min取出,破除种子休眠。
(2)重金属胁迫实验
A.设置实验组和对照组
实验组(染菌组):在超净工作台中,将一组含羞草种子置于链霉菌HG2-8-2菌悬液中浸泡6小时,取出阴干1h待用,浸泡过程中保持与空气有接触。
对照组(未染菌组):在超净工作台中,将另一组含羞草种子置于无菌水中浸泡6小时,取出待用。浸泡过程中保持与空气有接触,之后自然阴干1h待用。
B.配制铜溶液
配制浓度为0、50、100、200、300、400、500mg/L的Cu
C.重金属铜胁迫实验
用滤纸培养皿法将实验组和对照组含羞草种子30颗放入垫有滤纸的直径为90mm培养皿中。3个重复。按照重金属:无菌水=1:1的比例混匀,等量加入实验组和对照组。为避免Cu
原始数据以SPSS 26.0软件进行处理分析数据,以最小差异显著法检验其差异性;以Origin Pro 8.0制图。
2.实验结果
如图7-9所示,随着培养液中Cu
实施例五、链霉菌HG2-8-2对受锌离子污染的含羞草促生作用
1.实验过程
(1)种子处理用75%酒精进行消毒3min,在超净工作台中用无菌水将种子冲洗5次,并用已灭菌的吸水纸将种子表面的水吸干。将含羞草种子置于65℃的温水浸泡15min取出,破除种子休眠。
(2)重金属胁迫实验
A.设置实验组和对照组
实验组(染菌组):在超净工作台中,将一组含羞草种子置于链霉菌HG2-8-2菌悬液中浸泡6小时,取出阴干1h待用,浸泡过程中保持与空气有接触。
对照组(未染菌组):在超净工作台中,将另一组含羞草种子置于无菌水中浸泡6小时,取出待用。浸泡过程中保持与空气有接触,之后自然阴干1h待用。
B.配制锌溶液
配制浓度为0、300、900、1200、1500mg/L的Zn
C.重金属锌胁迫实验
用滤纸培养皿法将实验组和对照组含羞草种子30颗放入垫有滤纸的直径为90mm培养皿中。3个重复。按照重金属:无菌水=1:1的比例混匀,等量加入实验组和对照组。为避免Zn
原始数据以SPSS 26.0软件进行处理分析数据,以最小差异显著法检验其差异性;以Origin Pro 8.0制图。
2.实验结果
如图12-14所示,随着培养液中Zn
综上所述,本发明所请求保护的链霉菌(Streptomyces sp.)HG2-8-2耐受一定浓度的铜和锌污染,能够显著解除铜和锌离子对含羞草幼苗生长的不利影响,促进含羞草幼苗生长和生物量积累。同时,本发明所请求保护的链霉菌(Streptomyces sp.)HG2-8-2菌株能够有效去除环境中的铜离子和锌离子。
- 一株高温紫链霉菌及其在纤维素降解中的应用
- 一株具有耐受重金属特性的高效解磷草酸青霉菌
- 一株具有耐受重金属特性的高效解磷草酸青霉菌
