miRNA的基因组合及其在制备用于确定膀胱癌相关疾病状态的试剂盒中的用途和试剂盒
文献发布时间:2023-06-19 19:30:30
技术领域
本申请属于生物诊断技术领域,尤其涉及一种miRNA的基因组合及其在制备用于确定个体中膀胱癌相关的疾病状态的试剂盒中的用途和试剂盒。
背景技术
膀胱癌(Bladder cancer,BC)是一种在膀胱组织中起源于尿路上皮的恶性肿瘤,由不受控制的膀胱内壁细胞异常增长造成,是泌尿系统最常见的恶性肿瘤之一。
膀胱镜检查是一种创性检查,有可能导致泌尿系感染、前列腺损伤、尿道狭窄等,有血尿、疼痛、感染等风险。且临床应用受到外科医生经验水平等因素制约,总花费较高因而导致患者依从性差,不利于肿瘤早期筛查和术后监测。因此,急需一种无创、便捷、准确的诊断标志物用于辅助和改进膀胱肿瘤的检测。
公开于本申请背景技术部分的信息仅仅旨在加深对本申请的一般背景技术的理解,而不应当被视为承认或以任何形式暗示该信息构成已为本领域技术人员所公知的现有技术。
发明内容
本申请实施例提供一种miRNA的基因组合及其在制备用于确定个体中膀胱癌相关的疾病状态的试剂盒中的用途和试剂盒,旨在提供一种满足下列效果中至少一个的诊断标志物:灵敏度更高,漏检率更少,诊疗效率更高。
第一方面,本申请提供了一种用于确定个体中膀胱癌相关的疾病状态的外泌体中miRNA的基因组合,包括基因序列hsa-miR-652-3p,还包括以下5种基因序列中的至少一种:hsa-miR-140-5p,hsa-miR-28-3p,hsa-miR-486-5p,hsa-miR-96-3p和hsa-miR-132-3p,所述hsa-miR-652-3p,hsa-miR-140-5p,hsa-miR-28-3p,hsa-miR-486-5p,hsa-miR-96-3p和hsa-miR-132-3p的基因序列依次如SEQ ID NO:1-6所示。
可选的,miRNA的基因组合包括基因序列hsa-miR-652-3p,还包括以下3种基因序列中的至少一种:hsa-miR-140-5p,hsa-miR-28-3p,hsa-miR-486-5p,hsa-miR-96-3。
可选的,miRNA的基因组合包括基因序列hsa-miR-652-3p、hsa-miR-96-3p和hsa-miR-132-3p。
可选的,miRNA的基因组合包括基因序列hsa-miR-652-3p、hsa-miR-96-3p和hsa-miR-140-5p。
可选的,miRNA的基因组合包括基因序列hsa-miR-652-3p、hsa-miR-28-3p和hsa-miR-140-5p。
第二方面,miRNA的基因组合在制备用于确定个体中膀胱癌相关的疾病状态的试剂盒中的用途,包括基因序列hsa-miR-652-3p,还包括以下5种基因序列中的至少一种:hsa-miR-140-5p,hsa-miR-28-3p,hsa-miR-486-5p,hsa-miR-96-3p和hsa-miR-132-3p,所述hsa-miR-652-3p,hsa-miR-140-5p,hsa-miR-28-3p,hsa-miR-486-5p,hsa-miR-96-3p和hsa-miR-132-3p的基因序列依次如SEQ ID NO:1-6所示,其中,miRNA的基因组合来源于尿液外泌体。
第二方面,本申请提供了一种miRNA的基因组合在制备用于确定个体中膀胱癌相关的疾病状态的试剂盒中的用途,包括以下至少两种基因序列:hsa-miR-140-5p,hsa-miR-652-3p,hsa-miR-28-3p,hsa-miR-486-5p,hsa-miR-96-3p和hsa-miR-132-3p,所述hsa-miR-140-5p,hsa-miR-652-3p,hsa-miR-28-3p,hsa-miR-486-5p,hsa-miR-96-3p和hsa-miR-132-3p的基因序列依次如SEQ ID NO:1-6所示,其中,miRNA的基因组合来源于尿液外泌体。
第三方面,本申请提供了一种通过miRNA的基因组合确定个体中膀胱癌相关的疾病状态的试剂盒,包括检测所述miRNA的基因组合的引物对,其hsa-miR-652-3p,hsa-miR-140-5p,hsa-miR-28-3p,hsa-miR-486-5p,hsa-miR-96-3p和hsa-miR-132-3p的基因序列的正向引物的序列依次如SEQ ID NO:7-12所示,反向引物的序列均为SEQ ID NO:13所示。
可选的,所述试剂盒还包括获取装置,用于从待测样本中获取miRNA的基因组合。
可选的,所述获取装置包括:
蛋白过滤组件,用于去除待测样本中蛋白干扰;
外泌体磁珠捕获元件,与所述蛋白过滤组件连通,用于富集和捕获所述miRNA的基因组合;
裂解元件,与所述外泌体磁珠捕获元件连通,用于从混合液中过滤获得含所述miRNA的基因组合的外泌体磁珠捕获元件。
本申请实施例的用于确定个体中膀胱癌相关的疾病状态的miRNA的基因组合,包括基因序列hsa-miR-652-3p,还包括以下5种基因序列中的至少一种:hsa-miR-140-5p,hsa-miR-28-3p,hsa-miR-486-5p,hsa-miR-96-3p和hsa-miR-132-3p,所述hsa-miR-652-3p,hsa-miR-140-5p,hsa-miR-28-3p,hsa-miR-486-5p,hsa-miR-96-3p和hsa-miR-132-3p的基因序列依次如SEQ IDNO:1-6所示。本申请提供了全新的诊断标志物,使检测膀胱癌相关的疾病状态的灵敏度更高,漏检率更少,诊疗效率更高,可以更简单、高效、准确的确定患者是否患有膀胱癌。
附图说明
图1示出了本申请实施例的miRNAs基因序列引物扩增的熔解曲线;
图2示出了本申请实施例的唾液或者尿液中外泌体miRNAs获取装置;
图3示出了本申请实施例的miRNA在样本中荧光定量PCR典型扩增图;
图4示出了本申请实施例的单一miRNA基因序列用于膀胱癌筛查的ROC曲线图;
图5示出了本申请实施例的hsa-miR-652-3p和hsa-miR-486-5p两基因序列联合用于膀胱癌筛查的ROC曲线图;
图6示出了本申请实施例的hsa-miR-652-3p、hsa-miR-96-3p和hsa-miR-132-3p三个基因序列联合用于膀胱癌筛查的ROC曲线图;
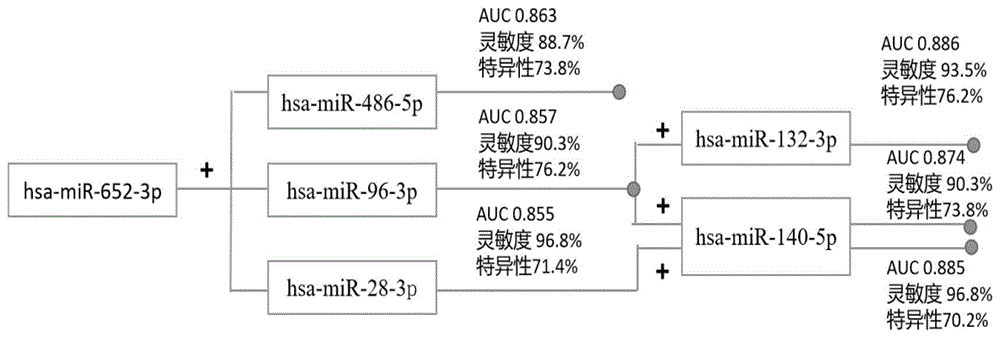
图7示出了本申请实施例的基于miRNAs基因序列联检对于膀胱癌筛查诊断性能;
图8示出了本申请实施例的无创尿液外泌体miRNAs基因序列检测和尿液镜检联合策略;
图9示出了本申请实施例的miRNA基因序列和镜检联合诊断性能。
具体实施方式
为使本公开实施例的目的、技术方案和优点更加清楚,下面将结合本公开实施例中的附图,对本公开实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本公开一部分实施例,而不是全部的实施例。基于本公开中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本公开保护的范围。
本公开的说明书和权利要求书及上述附图中的术语“第一”、“第二”、“第三”“第四”等(如果存在)是用于区别类似的对象,而不必用于描述特定的顺序或先后次序。应该理解这样使用的数据在适当情况下可以互换,以便这里描述的本公开的实施例能够以除了在这里图示或描述的那些以外的顺序实施。
应当理解,在本公开的各种实施例中,各过程的序号的大小并不意味着执行顺序的先后,各过程的执行顺序应以其功能和内在逻辑确定,而不应对本公开实施例的实施过程构成任何限定。
应当理解,在本公开中,“包括”和“具有”以及他们的任何变形,意图在于覆盖不排他的包含,例如,包含了一系列步骤或单元的过程、方法、系统、产品或设备不必限于清楚地列出的那些步骤或单元,而是可包括没有清楚地列出的或对于这些过程、方法、产品或设备固有的其它步骤或单元。
应当理解,在本公开中,“多个”是指两个或两个以上。“和/或”仅仅是一种描述关联对象的关联关系,表示可以存在三种关系,例如,和/或B,可以表示:单独存在A,同时存在A和B,单独存在B这三种情况。字符“/”一般表示前后关联对象是一种“或”的关系。“包含A、B和C”、“包含A、B、C”是指A、B、C三者都包含,“包含A、B或C”是指包含A、B、C三者之一,“包含A、B和/或C”是指包含A、B、C三者中任1个或任2个或3个。
应当理解,在本公开中,“与A对应的B”、“与A相对应的B”、“A与B相对应”或者“B与A相对应”,表示B与A相关联,根据A可以确定B。根据A确定B并不意味着仅仅根据A确定B,还可以根据A和/或其他信息确定B。A与B的匹配,是A与B的相似度大于或等于预设的阈值。
取决于语境,如在此所使用的“若”可以被解释成为“在……时”或“当……时”或“响应于确定”或“响应于检测”。
下面以具体地实施例对本公开的技术方案进行详细说明。下面这几个具体的实施例可以相互结合,对于相同或相似的概念或过程可能在某些实施例不再赘述。
膀胱癌(Bladder cancer,BC)是一种在膀胱组织中起源于尿路上皮的恶性肿瘤,由不受控制的膀胱内壁细胞异常增长造成,是泌尿系统最常见的恶性肿瘤之一。
其中,尿路上皮癌(Urothelial carcinoma,简称UC)为最常见的是泌尿系统中起源于尿路上皮的一种多源性的恶性肿瘤,占膀胱癌的90%以上;另有鳞状细胞癌(3%-7%)、腺癌(<2%)、小细胞癌、混合型癌、癌肉瘤等少见的组织学类型。多数诊断为UC的患者,大部分罹患浅表性UC的临床病例经积极治疗后预后良好,但易复发,晚期膀胱癌治疗效果欠佳、生存率低。因此通过肿瘤早诊、和实时监测复发可明显改善患者预后及生存质量。
然而,传统技术中,膀胱癌相关早诊、和实时监测复发可明显改善患者预后及生存质量的标志物有限,且效果仍有待提高。
例如,血尿,一种膀胱癌,对于膀胱癌的阳性预测值仅有8%。《膀胱癌诊疗指南(2022版)》(以下简称,指南)推荐对血尿患者首先进行泌尿系超声和/或CT检查,膀胱镜检查和活检是初发诊断和术后复发监测的“金标准”。NMIBC通常行经尿道膀胱肿物电切术(TURBt)后5年内有31%~78%患者出现膀胱肿瘤复发需再次或多次行TURBt手术,有0.8%~45%患者因未及早发现肿瘤复发而进展为肌层浸润性膀胱癌。因此,NMIBC患者TURBt术后每3~6个月需做一次膀胱镜检查。但膀胱镜检查为有创性检查,有可能导致泌尿系感染、前列腺损伤、尿道狭窄等,有血尿、疼痛、感染等风险,且临床应用受到外科医生经验水平等因素制约,总花费较高因而导致患者依从性差,不利于肿瘤早期筛查和术后监测。
经发明人研究发现,基于尿液检测技术寻求无创、便捷、准确的诊断方法辅助和改进膀胱肿瘤的检测,以期最终补充甚至取代膀胱镜检查。
基于尿液检测技术在膀胱癌无创诊断中的研究进展主要为:1)尿细胞学。从尿液或膀胱冲洗液标本中检测脱落癌细胞是首个广泛应用于临床的膀胱癌无创诊断方法。指南中指明,这一方法检测膀胱癌的敏感性为13%~75%,特异度高达99%(95% CI:83%~99.7%)。其敏感性与肿瘤分级呈正相,高级别肿瘤(包括原位癌)阳性率达84%;G1和低级别肿瘤的敏感性为16%。炎症、上皮不典型增生以及放化疗后组织改变等因素,导致其存在12%的假阳性率。指南推荐尿液细胞学仅作为膀胱镜的辅助手段来更准确地检测高级别肿瘤。此外,由于尿脱落细胞学检测灵敏度低,且阅片依赖于病理医生的主观经验和技术水平影响,不能广泛推广。2)尿液生物标志物检测方法,美国食品和药物管理(FDA)认证了6种尿液生物标志物检查方法,用以诊断或监测膀胱癌:定量NMP22,定性NMP22,定量BTA,定性BTA,荧光原位杂交FISH,荧光免疫组化(uCyt+/ImmunoCyt)。与尿液细胞学相比,NMP22和BAT检测低级别肿瘤(G1)的敏感性较高66%-83%,总体特异性较低(NPM22:65%-68%),同时,假阳性较高约18%。引起假阳性的原因主要有以下几种:泌尿系感染、尿路结石、近期留置尿管、肠代膀胱、其他泌尿生殖系统肿瘤和接受器械检查等。较低的特异性及较高的假阳性率成为了限制这两者独立应用于临床的原因。
发明人经研究,发现通过本申请的miRNA的基因组合提高了其特异性检测,也得到了较低的假阳性率,可以应用于临床诊断。
miRNA的基因组合
本申请第一方面提供了一种用于确定个体中膀胱癌相关的疾病状态的miRNA的基因组合,第一方面,本申请提供了一种用于确定个体中膀胱癌相关的疾病状态的miRNA的基因组合,包括基因序列hsa-miR-652-3p,还包括以下5种基因序列中的至少一种:hsa-miR-140-5p,hsa-miR-28-3p,hsa-miR-486-5p,hsa-miR-96-3p和hsa-miR-132-3p,所述hsa-miR-652-3p,hsa-miR-140-5p,hsa-miR-28-3p,hsa-miR-486-5p,hsa-miR-96-3p和hsa-miR-132-3p的基因序列依次如SEQ ID NO:1-6所示。
上述miRNA的基因组合从5'端到3'端的序列组成如下:
SEQ ID NO.1:AAUGGCGCCACUAGGGUUGUG
SEQ ID NO.2:CAGUGGUUUUACCCUAUGGUAG
SEQ ID NO.3:CACUAGAUUGUGAGCUCCUGGA
SEQ ID NO.4:UCCUGUACUGAGCUGCCCCGAG
SEQ ID NO.5:AAUCAUGUGCAGUGCCAAUAUG
SEQ ID NO.6:UAACAGUCUACAGCCAUGGUCG
在本申请实施例中,miRNA单独或者组合实施诊断的临床性能,在尿液中外泌体中miRNAs进行筛查可以实现较好的筛查效果(所有组别P<0.0001),其中灵敏度(88.7%~96.8%)、特异性在66.7%~76.2%。
上述miRNA的基因组合可以来源于尿液外泌体中,可以判断生物样本的受试者是否患有膀胱癌或者判断受试者是否存在患有膀胱癌的疾病状态。上述尿液中的外泌体,具有双层脂质膜结构的直径分布在30-150nm之间的细胞外囊泡,它可将蛋白质、脂质和核酸(miRNA、lncRNA、circRNA)等生物活性分子转移到受体细胞,广泛分布在血液、唾液、母乳或尿液等体液中。因此,本申请中的miRNA的基因组合基于尿液中外泌体miRNAs表达谱变化,可以反映膀胱癌疾病信号信息。
在本实施例中,上述miRNA的基因组合,两两组合或者合并组合均具有高敏感性(灵敏度88.7%~96.8%),特异性为69%~81%。基于上述miRNA的基因组合的检测结果,配合检测指标,由于其无创易于反复获取尿液,检测效能不受实验人员主观经验影响,检测成本低于FISH等检测方法,灵敏度高,因此可以成为目前临床手段一个有效弥补,大大提高灵敏度,减少漏检率,提高医院诊疗效率。
经发明人研究发现,上述6种miRNAs基因序列的显著性效果的作用机理如下:
据报道,hsa-miR-652-3p在正常尿液中表达很高(Expression RPM~420),有和乳腺癌,非小细胞肺癌和胃癌,以及非肿瘤疾病的生物标志物的报道,目前未见和膀胱癌相关报道。但其与其他基因序列的组合,可以提高检测结果的准确性。
基因序列hsa-miR-140-5p在正常尿液中表达中等(Expression RPM~100),主要报道功能和信号通路可能和TP53信号通路相关,与一些肿瘤发生发展相关,例如前列腺癌,胰腺癌,结肠癌,血液肿瘤等,可能TP63的3'-UTR中的SNP rs35592567的T等位基因与膀胱癌风险显著相关,且T等位基因通过干扰miR-140-5p的结合效率降低了TP63的转录后水平,提示miR-140-5p和膀胱癌风险间接相关,从而可以用于检测膀胱癌的疾病状态。
hsa-miR-28-3p在正常尿液中表达中等(Expression RPM~140),报道功能和信号通路有TP53,EGFR,KRAS等,与一些肿瘤发生发展相关,例如胶质瘤,黑色素瘤等,目前未见和膀胱癌相关报道。但经临床试验,可以用于检测膀胱癌。
hsa-miR-486-5p在正常尿液中表达较低(Expression RPM~55),报道功能相关有宫颈癌,骨肉瘤,汞中毒,食管癌等。目前未见和膀胱癌相关报道。但经临床试验,可以用于检测膀胱癌。
hsa-miR-96-3p在正常尿液中表达极低(Expression RPM~10),报道功能相关有肺癌、肾癌、前列腺癌、膀胱癌、肝癌、骨代谢等,和膀胱癌的相关报道为体外实验中miR-96(非hsa-miR-96-3p)可能通过靶向HERG1,或者靶向FOXO1,作为膀胱癌患者治疗靶点,亦或可能通过上调IRS1和MAP4K1水平来影响膀胱癌细胞的生长,成为膀胱尿路上皮癌的潜在诊断标志物。目前未见和膀胱癌相关报道。但经临床试验,可以用于检测膀胱癌。但其与其他基因序列的组合,可以提高检测结果的准确性。
hsa-miR-132-3p在正常尿液中表达极高(Expression RPM~850),报道功能相关有抗炎、免疫、胰腺癌、肝癌、乳腺癌、神经退行性疾病等相关,和膀胱癌的相关报道为血清中三个miRNA组合(miR-132-3p、miR-7-5p和miR-148b-3p)可作为BC筛查和诊断的非侵入性和方便的诊断工具但其与其他基因序列的组合,可以提高检测结果的准确性。
在一些实施例中,miRNA的基因组合包括基因序列hsa-miR-652-3p,还包括以下3种基因序列中的至少一种:hsa-miR-140-5p,hsa-miR-28-3p,hsa-miR-486-5p,hsa-miR-96-3。
在一些实施例中,miRNA的基因组合包括基因序列hsa-miR-652-3p、hsa-miR-96-3p和hsa-miR-132-3p。
在一些实施例中,miRNA的基因组合包括基因序列hsa-miR-652-3p、hsa-miR-96-3p和hsa-miR-140-5p。
在一些实施例中,miRNA的基因组合包括基因序列hsa-miR-652-3p、hsa-miR-28-3p和hsa-miR-140-5p。
上述基因组合进一步提高了检测结果的准确性和灵敏度。
第二方面,miRNA的基因组合在制备用于确定个体中膀胱癌相关的疾病状态的试剂盒中的用途,包括基因序列hsa-miR-652-3p,还包括以下5种基因序列中的至少一种:hsa-miR-140-5p,hsa-miR-28-3p,hsa-miR-486-5p,hsa-miR-96-3p和hsa-miR-132-3p,所述hsa-miR-652-3p,hsa-miR-140-5p,hsa-miR-28-3p,hsa-miR-486-5p,hsa-miR-96-3p和hsa-miR-132-3p的基因序列依次如SEQ ID NO:1-6所示,其中,miRNA的基因组合来源于尿液外泌体。
在一些实施例中,miRNA的基因组合的快捷提取和扩增,可以包括以下步骤:
(1)从尿液原液中,利用磁性四氧化三铁-氧化物纳米颗粒富集法进行富集外泌体;
(2)通过外泌体磁珠法富集纯化内含miRNAs靶标的外泌体;
(3)在逆转录的时候通过加尾法或者茎环法增加miRNAs逆转录产物的长度,从而达到定量聚合酶链扩增实验。
在本申请实施例中,由于成熟的miRNA的长度只有20nt左右,利用成熟的加A法进行反转录-定量聚合酶链扩增实验,实现靶miRNA的检测;本申请的方法通过疾病对应性,锁定一组关键靶标,在尿液中对其检测,与尿液镜检结果进行对比,可以显著提高检测灵敏度。
在一些实施例中,所述用途包括对个体中膀胱癌进行早筛和/或复发检测。
在一些实施例中,所述膀胱癌相关的疾病状态是临床上有意义的膀胱癌发生的可能性。
在一些实施例中,所述膀胱癌相关的疾病状态是膀胱癌的存在或不存在。
第三方面,本申请提供了一种通过miRNA的基因组合确定个体中膀胱癌相关的疾病状态的试剂盒,包括检测所述miRNA的基因组合的引物对,其hsa-miR-652-3p,hsa-miR-140-5p,hsa-miR-28-3p,hsa-miR-486-5p,hsa-miR-96-3p和hsa-miR-132-3p的基因序列的正向引物的序列依次如SEQ ID NO:7-12所示,反向引物的序列均为SEQ ID NO:13所示。
在本申请实施例中,miRNAs扩增的基因组合的引物对,可以来自sRNAPrimerDB软件给出的若干候选组合,通过实验进行熔解曲线分析筛选特异性Tm值的引物对,获得可以特异性扩增(排除在空白对照NTC中无因碱基错配或者引物二聚体等原因引起的非特异性扩增)目的miRNA的序列引物,进行后续实验,确保信号全部来自miRNAs基因序列,如图1所示。图1中ABCD四幅图为熔解曲线导数图谱,证明引物序列扩增特异性的示意图。熔解曲线导数图谱,是指利用荧光信号变化的负一次导数(dR/dT)(纵坐标)与温度(横坐标)作图得到导数图谱,导数图谱会出现特征峰,更直观地反映PCR产物的解链情况。在导数图谱中,特征峰对应的温度就是Tm值,根据特征峰的位置和形态,可以区分特异性产物和非特异性产物。特异性扩增得到的熔解曲线只有一个紧密的单峰。ABC分别为hsa-miR-140-5p、hsa-miR-652-3p、hsa-miR-28-3p的熔解曲线示意图,图1D说明Tm值对于hsa-miR-486-5p和hsa-miR-96-3p特异性扩增的区分。
在一些实施例中,所述试剂盒还包括获取装置,用于从待测样本中获取miRNA的基因组合。
在一些实施例中,参见图2,获取装置包括:
蛋白过滤组件,用于去除待测样本中蛋白干扰;具体地,一般为脱脂棉。
外泌体磁珠捕获元件,与所述蛋白过滤组件连通,用于富集和捕获所述包裹miRNA的外泌体;具体地,一般为金属氧化物,例如TiO2,Fe3O4,TiO2,ZrO2,Y2O3,ITO,In2O3和Mn2O3等,用于捕获外泌体囊泡。
裂解元件,与所述外泌体磁珠捕获元件连通,用于裂解外泌体获得所述目标miRNAs的混合物。具体地,一般为浸润裂解液(TE缓冲液,pH8.0)后封干的脱脂棉。
装置使用说明:将装置底部用塞头堵住,采集的尿液或者唾液直接适量(1-2mL)加入装置顶部静置5分钟,取出塞头利用顶部压力方式将液体推至底部膜处浸润再静置5分钟,最后底部留出的液体作为模板,进行后续检测。
在上述获取装置中,提取流程简单易操作,适用于无创采集的体液,能够更好更快速得到外泌体及其内含稳定的miRNA生物标志物,针对临床和大健康市场上的刚需和痛点,适用于筛查大样本调查的液体诊断监控技术。其中,蛋白过滤组件为棉纤维,以过滤掉作为待测样本的唾液中唾液黏蛋白,或者过滤掉作为待测样本的尿液中其他蛋白的干扰。外泌体磁珠捕获元件为TiO2磁珠,填充于蛋白过滤组件和过滤元件之间,用以捕获包裹miRNAs的外泌体囊泡。裂解元件为膜被裂解液浸泡后封干,用于裂解外泌体囊泡,释放miRNAs。
本申请提供的通过miRNA的基因组合确定个体中膀胱癌相关的疾病状态的试剂盒,弥补尿液镜检灵敏度低的不足,联合镜检提高尿液筛查阳性率,适合于吸烟、中老年、化工接触等尿路上皮癌高危人群筛查;尿路上皮癌术后监控。
实施例
下述实施例更具体地描述了本申请公开的内容,这些实施例仅仅用于阐述性说明,因为在本申请公开内容的范围内进行各种修改和变化对本领域技术人员来说是明显的。除非另有声明,以下实施例中所报道的所有份、百分比、和比值都是基于重量计,而且实施例中使用的所有试剂都可商购获得或是按照常规方法进行合成获得,并且可直接使用而无需进一步处理,以及实施例中使用的仪器均可商购获得。
实施例1可用于筛查正常人和膀胱癌患者的差异性miRNAs获得
一、收集50例正常志愿者尿液,80例已经确认为膀胱癌/低级别尿路上皮癌术前尿液(来源于中国科学院肿瘤医院)。使用纳米颗粒技术捕获UC患者尿液中外泌体,进行miRNAs差异性分析,筛选出能区分正常人和膀胱癌患者的miRNAs。
二、实验过程:氧化物富集法进行外泌体富集和RNA的提取
1、实验试剂
洗涤缓冲液:20mM Tris-HCl,150mM NaCl,10mM CaCl2,余量为水;
清洗收集液:0.01mM PBS,PH 7.2。
用化学共沉淀法制备二氧化锆包覆的四氧化三铁磁珠,方法如下:将FeSO4·7H2O(0.18mol/L)和FeCl3·6H2O(0.12mol/L)溶解于水-无水乙醇(体积比=5:1)混合液中,以800rpm速度搅拌并通氮气30min。随后加热升温到70℃,在搅拌状态下加入体积百分比25%氨水溶液使混合液pH达到10~11。继续搅拌15min,然后缓慢滴加质量体积比为8.5%的八水氧氯化锆。加热到80℃恒温反应90min。反应液静置降温到30℃后,用外加磁场吸附磁性颗粒,去掉上清,用去离子水清洗3次,真空冷冻干燥获得磁珠。
预处理液:70%乙醇水溶液;
上样缓冲液/平衡缓冲液:10mM的柠檬酸(pH=6)缓冲液(溶剂为水);
洗脱缓冲液:0.01%(体积百分含量)氨水,pH=10
2、尿液中的外泌体内涵miRNAs提取实验步骤:
样本量推荐范围:唾液原液、尿液1mL-2mL;血清500μl(需用洗涤缓冲液2倍稀释后上样)。
(1)磁珠悬液:自制四氧化三铁-二氧化钛磁珠用20%乙醇水溶液(体积百分比)配成50mg/ml的磁珠悬液。
(2)平衡磁珠:
①每个样本取500μl(25mg)的磁珠悬液,将离心管放置在磁分离器上,放置30s,遗弃上清。500μl的70%乙醇水溶液(预处理液)温和洗涤磁珠5min,将离心管放置在磁分离器上,放置30s,遗弃上清。重复一次洗涤。
②用500μl的洗脱缓冲液洗涤磁珠10min,将离心管放置在磁分离器上,放置30s,遗弃上清。
③500μl上样缓冲液平衡磁珠60s,将离心管放置在磁分离器上,放置30s,遗弃上清。共3次平衡。
(3)捕获外泌体
①将样本对应加入到平衡好的磁珠中,混悬,室温孵育20min。将离心管放置在磁分离器上,放置30s,遗弃上清。
②使用100μl洗脱缓冲液孵育40min,磁性分离,移取上清液至新的离心管中,得到外泌体溶液。
(4)捕获RNA
①上一步得到的外泌体溶液中加入200μl RNA捕获磁珠(诺唯赞生物科技股份有限公司,N412-01)吹打混匀后室温孵育5min。将离心管放置在磁分离器上,放置30秒,遗弃上清,保留RNA捕获磁珠。
②加入500μl新鲜配制的80%乙醇水溶液漂洗磁珠,室温孵育30秒后小心移除上清,重复漂洗1次。
③磁珠暴露在空气中自然干燥后加入适量体积的Nuclease-free H2O,吹打混匀室温孵育5min,得到磁珠悬浮液。
将磁珠悬浮液置于磁力架5min后转移上清至新的离心管中,得到RNA。
三、miRNA芯片筛选
首先,获得可能具备区分正常人和疾病的尿液样本的候选miRNAs,因此将RNAs用miRNA芯片检测。miRNA芯片(Agilent Human miRNA(8*60K)array)由上海伯豪生物技术有限公司分析完成。芯片筛选结果挑选显著统计学差异如下所示:hsa-miR-7、hsa-miR-15、hsa-miR-16、hsa-miR-21、hsa-miR-22、hsa-miR-28、hsa-miR-29、hsa-miR-31、hsa-miR-34、hsa-miR-92、hsa-miR-93、hsa-miR-96、hsa-miR-126、hsa-miR-132、hsa-miR-140、hsa-miR-155、hsa-miR-191、hsa-miR-199、hsa-miR-200、hsa-miR-205、hsa-miR-221、hsa-miR-361、hsa-miR-375、hsa-miR-423、hsa-miR-486、hsa-miR-619、hsa-miR-652、hsa-miR-940、hsa-miR-4454、hsa-miR-let7b。
四、可用于筛查正常人和膀胱癌患者的差异性miRNAs
80例已经确认为膀胱癌/低级别尿路上皮癌患者的初诊未治疗尿液和50例正常志愿者尿液,针对上述芯片结果获得的候选miRNAs,基于反转录荧光定量PCR进行验证和进一步筛选。具体实验过程如下:
1、实验过程同实施例1中氧化物富集法进行外泌体富集和RNA的提取,RNA反转录过程如下:
2、尿液中的外泌体内涵miRNAs反转录
将上述一得到的RNA按照如下反转录得到cDNA:使用poly(a)聚合酶和ATP进行poly(a)-尾反应,对miRNA进行反转录。使用miRcute增强型miRNA cDNA第一链合成试剂盒(KR211,天根生物),可保证miRNA 3’末端的Poly(A)修饰过程和逆转录过程同时高效进行。miRNA反转录体系的配制:2XRT buffer 5μl,RTmix(酶和反转录引物)1μl,RNA模板4μl,共10μl体系。内含通用反转录引物:CAGTGCAGGGTCCGAGGTCAGAGCCACCTGGGCAATTTTTTTTTTTVN(VN=V:A、C、G;N:A、C、G和T);
反转录程序如下:42℃60min进行miRNA加A尾反应和逆转录反应;95℃3min酶失活反应。
3、QPCR检测
以上述cDNA为模板,用如下引物和检测体系进行QPCR检测:
在进行下游荧光定量检测时,为避免逆转录体系对定量PCR反应的抑制,得到合适的Ct值(15-28之间),可将cDNA反应液稀释10倍后使用。
采用
研发中使用
上述QPCR检测体系如下:2×AceQ qPCR SYBR Green Master Mix 10μl;F(miRNA上游引物)0.4μl;Rp(通用QPCR下游引物)0.4μl;反转录cDNA模板4μl;ddH2O 5.2μl,共20μl体系。
miRNAs和对应QPCR正向引物序列如下:
miRNA ID正向引物(5'-->3')
hsa-miR-140-5p AACACGCCAGTGGTTTTACCC
hsa-miR-652-3p AACAAGAATGGCGCCACTAGG
hsa-miR-28-3p AACAGACACTAGATTGTGAGCTCCT
hsa-miR-486-5p AACACGTGTCCTGTACTGAGCT
hsa-miR-96-3p AACAAGAATCATGTGCAGTGCCAAT
hsa-miR-132-3p AACACGTGTAACAGTCTACAGCCA
通用反向(下游)引物(5'-->3'):CAGTGCAGGGTCCGAGGT
上述各个基因和通用反向(下游)引物分别组成引物对,进行扩增。
上述QPCR程序:95℃ 15min,5个预扩增(94℃for 20s,63℃for 30s,and 72℃for34s,)35个循环(94℃for 20s,and 60℃for 34s)plate read;Melting curve analysis;END。
使用Applied Biosystems 7500Real Time PCR System进行实时荧光定量PCR检测,根据每个miRNA在样本中扩增的阈值循环数(Ct值)进行统计分析,Ct值与模板的起始拷贝数的对数存在线性关系,起始模板浓度越高,Ct值越小;起始模板量浓度越低,Ct值越大,检测结果典型扩增图,如图3所示,横坐标为扩增循环数(Ct值),纵坐标为荧光信号强度ΔRn值(实时荧光强度-基线荧光强度)。左图为通过对一个样本中hsa-miR-96-3p的重复检测获得的Ct值,右图为通过对疾病组和正常组不同样本中的hsa-miR-96-3p检测获得的Ct值。
上述采用prism 9.0软件对数据进行处理,组间数据比较采用独立样本t检验,P<0.05有差异即有统计学意义。从芯片筛选结果针对荧光定量PCR进行验证,发现靶基因hsa-miR-140-5p、hsa-miR-652-3p、hsa-miR-28-3p、hsa-miR-486-5p、hsa-miR-96-3p、hsa-miR-132-3p在50例正常志愿者尿液、和80例患者中分别具有统计学差异(如表1所示),获得的具有筛查正常人和膀胱癌患者的6个miRNAs基因序列的受试者工作特征曲线(receiveroperating characteristic curve,ROC,反映敏感性和特异性连续变量的综合指标),ROC曲线如下图4和表1。两个miRNAs基因序列:hsa-miR-652-3p和hsa-miR-486-5p联合用于膀胱癌筛查的ROC曲线图,如图5所示,联检可以进一步将AUC提高至0.86以上,灵敏度最高可达96.8%。三个miRNAs基因序列:sa-miR-652-3p、hsa-miR-96-3p和hsa-miR-132-3p三个miRNAs基因序列联合用于膀胱癌筛查的ROC曲线图,如图6.各miRNAs基因序列的联合使用如图7所示。
上述结果肯定了尿液外泌体中miRNAs对于膀胱癌筛查具有临床性能,准确率和灵敏度较高。
表1单一miRNAmiRNAs基因序列用于膀胱癌筛查的统计学差异
实施例2miRNAs对于监测膀胱癌患者术后复发的监测效果
80例已经确认为膀胱癌/低级别尿路上皮癌(膀胱低级别UC 12例、膀胱高级别UC30例、肾盂高级别UC12例、输尿管低级别UC 6例、输尿管高级别UC 13例、输尿管尿路上皮原位癌7例)。术后3-6月随访尿液镜检结果分组如下:1)A组13例:未见肿瘤细胞、少数非典型细胞、未见高级别尿路上皮癌细胞(TPS II,NHGUC),均界定为“阴性”。2)B组15例:发现非典型细胞(TPS III,AUC);C组6例:有少许可疑癌细胞,部分细胞伴鳞状分化特征(TPS IV,SHGUC);D组35例:有高级别尿路上皮癌细胞(TPS V,HGUC);E组11例:有尿路上皮肿瘤细胞(TPS VI,LGUN)和有腺癌细胞(TPS VII,Other Malignancy),上述B-E均界定为“阳性”。
此外,为了进一步验证上述6个miRNAs单独或者联检是否对于术后复发具有监测作用,因此,跟进随访这80例初诊患者的3-6个月的尿液镜检结果。实验步骤同实施例1中的提取、逆转录和QPCR过程。选取细胞学诊断为不明确(包括A组阴性、B组非典型上皮细胞、C组可疑癌细胞三个诊断级别)的患者尿液样本共34例进行统计学分析,结果表明镜检阴性样本的miRNA检测结果26例为阳性,即,在尿液镜检显示为“阴性”的样本中,检测到了阳性结果,这些样本中检测灵敏度从0%提高到71%,说明尿液中外泌体miRNAs可以提高膀胱癌术后监测复发的灵敏度,减小单纯尿液细胞学诊断的漏检率,使得患者及时得到诊疗。
综上,对膀胱癌筛查和术后监测进行无创尿液外泌体miRNAs检测+尿液镜检联合策略(图8和图9)。miRNA和镜检联合的灵敏度可以高达71.0%,特异性高达100%,与单独使用miRNA相比,总体诊断效能ROC曲线的AUC值增加至0.935(单独miRNAs组合联检为0.886);更可以使得镜检的灵敏度在更早期和低级别人群从16%左右提高至71%,因此可以更大规模、便捷地进行分级诊疗。
结论,miNRAs可以针对已确诊患者人群,在复发过程中尿液镜检阴性(含阳性)的样本,对应阳性指标,相对于正常人群阴性指标,进行筛选分析。目的在于弥补尿液镜检灵敏度低的不足,联合镜检提高尿液筛查阳性率。本申请保护的6种miRNAs单独或者组合,既可以对正常人进行筛查,也可以针对术后人群复发状态进行定期监测。
还需要说明的是,本申请中提及的示例性实施例,基于一系列的步骤或者装置描述一些方法或系统。但是,本申请不局限于上述步骤的顺序,也就是说,可以按照实施例中提及的顺序执行步骤,也可以不同于实施例中的顺序,或者若干步骤同时执行。
以上所述,仅为本申请的具体实施方式,所属领域的技术人员可以清楚地了解到,为了描述的方便和简洁,上述描述的系统、模块和单元的具体工作过程,可以参考前述方法实施例中的对应过程,在此不再赘述。应理解,本申请的保护范围并不局限于此,任何熟悉本技术领域的技术人员在本申请揭露的技术范围内,可轻易想到各种等效的修改或替换,这些修改或替换都应涵盖在本申请的保护范围之内。
- 一种基因序列组合物及其在制备分枝杆菌肺病检测试剂盒中的应用
- 一组蛋白作为肿瘤标志物在制备恶性肿瘤诊断试剂和试剂盒中的用途
- miRNA在制备高级浆液性上皮性卵巢癌化疗耐药性评价试剂盒中的应用
- D-丝氨酸作为标志物在制备抑郁症诊断试剂盒中的应用及抑郁症诊断试剂盒
- 与抗精神疾病药相关的试剂盒、目标基因及其制备、SNP标记、SNP识别和应用
- 抗原组合在制备用于肺癌相关自身抗体检测的试剂盒中的用途以及相应的试剂盒和检测方法
- miRNA在制备用于检测KSHV潜伏感染的试剂盒中的用途
