人源化抗EMAPII治疗性抗体
文献发布时间:2023-06-19 19:30:30
相关申请的交叉引用
本申请依据35U.S.C.§119(e)要求于2020年6月29日提交的第63/045,687号美国临时申请的优先权,所有该临时申请的全部内容均通过引用方式并入本文。
背景技术
内皮单核细胞激活多肽II(EMAPII)是一种促凋亡和单核细胞趋化性细胞因子,涉及多种多样的病变,总体而言对人类健康具有巨大影响。尤其是,已显示EMAPII是香烟烟雾诱发的肺气肿的介导物。本领域需要靶向EMAPII的新型疗法。本公开解决了这一需求。
发明内容
在一方面,本发明提供了一种人源化抗内皮单核细胞激活多肽II(抗EMAPII)抗体,包含:重链可变结构域,其具有与SEQ ID NO:1至SEQ ID NO:5中任一项有90%或更高的序列同一性的氨基酸序列;以及轻链可变结构域,其具有与SEQ ID NO:6至SEQ ID NO:9中任一项有90%或更高的序列同一性的氨基酸序列。
在另一方面,本发明提供了一种人源化抗内皮单核细胞激活多肽II(抗EMAPII)抗体,包含重链可变结构域,该重链可变结构域具有与SEQ ID NO:1至SEQ ID NO:5中任一项有90%或更高的序列同一性的氨基酸序列。
在又一方面,本发明提供了一种人源化抗内皮单核细胞激活多肽II(抗EMAPII)抗体,包含轻链可变结构域,该轻链可变结构域具有与SEQ ID NO:6至SEQ ID NO:9中任一项有90%或更高的序列同一性的氨基酸序列。
在又一方面,本发明提供了一种嵌合的抗内皮单核细胞激活多肽II(抗EMAPII)抗体,包含与SEQ ID NO:10具有90%或更高序列同一性的重链可变结构域和与SEQ ID NO:11具有90%或更高序列同一性的轻链可变结构域。
在又一方面,本发明提供了一种重组载体,其包含编码在SEQ ID NO:1至SEQ IDNO:11中任一项所示氨基酸序列的核酸。
在又一方面,本发明提供了一种用本文别处描述的重组载体转化的细胞。
在又一方面,本发明提供了一种产生抗体的方法,其包括在表达抗体的条件下培养本文别处描述的转化的细胞。
在又一方面,本发明提供了一种药物组合物,其包含如本文别处描述的抗体和至少一种药学上可接受的赋形剂。
在又一方面,本发明提供了一种在有此需要的受试者中治疗慢性阻塞性肺病(COPD)的方法,该方法包括向受试者施用本文别处描述的药物组合物。
在又一方面,本发明提供了一种在有此需要的受试者中治疗肺气肿的方法,该方法包括向受试者施用本文别处描述的药物组合物。
在又一方面,本发明提供了一种在有此需要的受试者中治疗支气管肺发育异常的方法,该方法包括向受试者施用本文别处描述的药物组合物。
在又一方面,本发明提供了一种在有此需要的受试者中治疗内皮单核细胞激活多肽II(EMAPII)介导的疾病的方法,该方法包括向受试者施用如本文别处描述的药物组合物。
在某些实施方案中,重链可变结构域具有与SEQ ID NO:1至SEQ ID NO:5中任一项有95%或更高的序列同一性的氨基酸序列;并且轻链可变结构域具有与SEQ ID NO:6至SEQID NO:9中任一项有95%或更高的序列同一性的氨基酸序列。
在某些实施方案中,重链可变结构域具有与SEQ ID NO:2或SEQ ID NO:3中任一项有99%或更高的序列同一性的氨基酸序列;并且轻链可变结构域具有与SEQ ID NO:6或SEQID NO:9中任一项有99%或更高的序列同一性的氨基酸序列。
在某些实施方案中,重链可变结构域具有与SEQ ID NO:2或SEQ ID NO:3中任一项有95%或更高的序列同一性的氨基酸序列。
在某些实施方案中,轻链可变结构域具有与SEQ ID NO:6或SEQ ID NO:9中任一项有95%或更高的序列同一性的氨基酸序列。
在某些实施方案中,重链可变结构域与SEQ ID NO:10具有95%或更高的序列同一性,并且轻链可变结构域与SEQ ID NO:11具有95%或更高的序列同一性。
附图说明
当结合附图阅读时,将会更好地理解以下对本发明具体实施方案的详细描述。为了说明本发明,附图示出了具体实施方案。然而,应该理解的是,本发明不限于附图中所示实施方案的精确布置和手段。
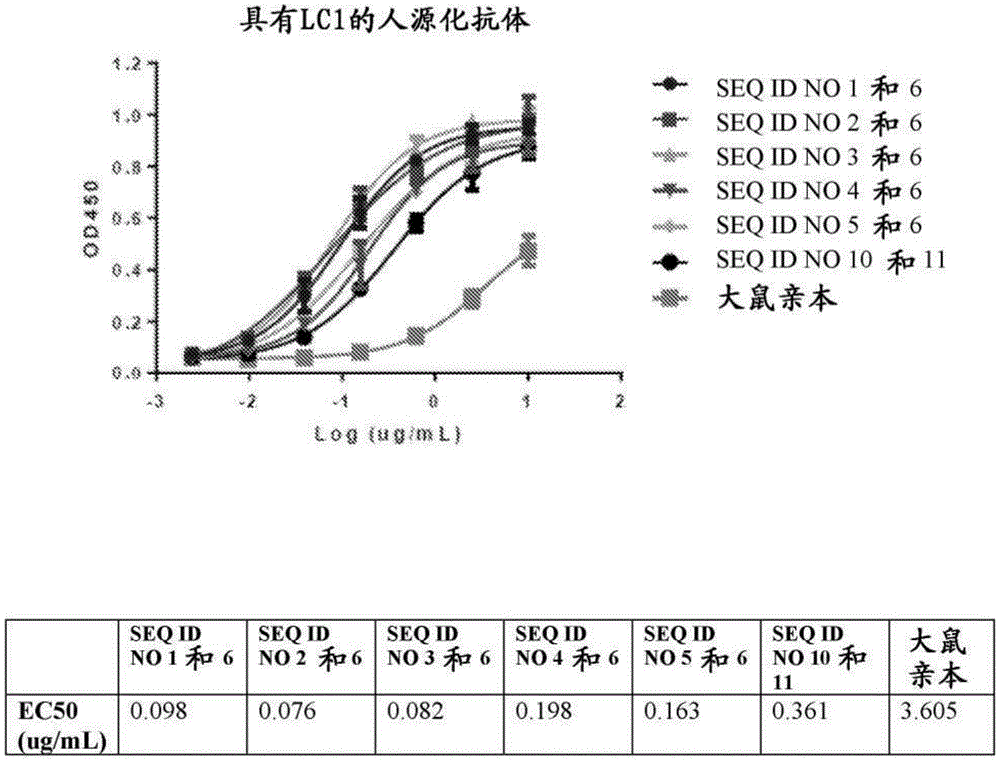
图1描绘了具有LC1(SEQ ID NO.6)的人源化抗体针对人前体EMAPII(proEMAPII)的酶联免疫吸附测定(ELISA)。
图2描绘了具有LC2(SEQ ID NO.7)的人源化抗体针对人proEMAPII的酶联免疫吸附测定(ELISA)。
图3描绘了具有LC3(SEQ ID NO.8)的人源化抗体针对人proEMAPII的酶联免疫吸附测定(ELISA)。
图4描绘了具有LC4(SEQ ID NO.9)的人源化抗体针对人proEMAPII的酶联免疫吸附测定(ELISA)。
图5描绘了8种抗体针对人proEMAPII的ELISA筛选。
图6描绘了8种抗体针对人成熟EMAPII的ELISA筛选。
图7描绘了8种抗体针对小鼠proEMAPII的ELISA筛选。
图8描绘了8种抗体针对小鼠成熟EMAPII的ELISA筛选。
发明详述
定义
除非另有定义,否则本文所用的所有技术和科学术语具有与本发明所属领域普通技术人员通常理解的相同含义。尽管在实施过程中可以使用与本文所述方法和材料类似或等同的任何方法和材料来测试本发明,但是本文描述了优选的材料和方法。在描述和要求保护本发明时,将使用以下术语。还应当理解的是,本文使用的术语仅仅是为了描述特定的实施方案,而并非意在进行限制。
如本文所用的,以下每个术语在本节中均具有与之相关的含义。
除非另有定义,否则本文所用的所有技术和科学术语一般具有与本发明所属领域普通技术人员通常理解的相同含义。总体来说,本文使用的命名和细胞培养、分子遗传学、分析化学、免疫学以及核酸化学和杂交、单克隆抗体合成以及生物学和生物物理学表征中的实验室程序都是本领域众所周知和常用的那些。对于化学合成和化学分析使用标准技术或对其进行的改进。
本文所用的冠词“一个”和“一种”指的是该冠词的一个/种或多于一个/种(即,至少一个/种)的语法客体。举例来说,“一种要素”意指一个/种要素或多于一个/种要素。
如本文所用的,术语“内皮单核细胞激活多肽II”或“EMAPII”指的是促炎细胞因子。EMAPII以34kD的前体形式(“前体EMAPII”)或者在经蛋白酶的蛋白水解切割后以18kD的成熟蛋白(“成熟EMAPII”)从细胞中释放出来。成熟EMAPII的人类同源物包含序列SEQ IDNO:12:
SKPIDVSRLDLRIGCIITARKHPDADSLYVEEVDVGEIAPRTVVSGLVNHVPLEQMQNRMVILLCNLKPAKMRGVLSQAMVMCASSPEKIEILAPPNGSVPGDRITFDAFPGEPDKELNPKKKIWEQIQPDLHTNDECVATYKGVPFEVKGKGVCRAQTMSNSGIK。
除非另有说明,否则术语“EMAPII”可用于指该蛋白质的前体和成熟形式两者。
如本文所用的,术语“约”将由本领域普通技术人员理解,并且将在一定程度上根据其使用的上下文而变化。如本文所用的术语“约”,在提及可测量值诸如量、浓度、持续时间等时,意在包括与指定值相差±20%或±10%,更优选±5%,甚至更优选±1%,以及还更优选±0.1%,因为这样的变化适于执行所公开的方法。
如本文所用的,术语一个分子对另一个分子的“亲和力”指的是两个分子之间结合的程度(或紧密度)。更高的亲和力意味着两个分子之间的结合更紧密。可以根据解离常数(或K
如本文所用的“氨基酸”意在包括天然和人工合成氨基酸,以及D-和L-氨基酸。“标准氨基酸”意指天然存在的肽中常见的20种L-氨基酸中的任何一种。“非标准氨基酸残基”意指除标准氨基酸之外的任何氨基酸,无论它是以合成方式制备的还是源自天然来源的。如本文所用的,“合成氨基酸”还包括化学修饰的氨基酸,包括但不限于盐类、氨基酸衍生物(如酰胺类)和取代物。肽中所含的氨基酸,特别是位于羧基或氨基末端的氨基酸,可以通过甲基化、酰胺化、乙酰化或用其他化学基团取代来进行修饰,这些修饰可以改变肽的循环半衰期,而不会对肽的活性产生不利影响。另外,肽中可能存在或不存在二硫键。
如本文所用的术语“抗体”,指的是一种能够与抗原上特定表位特异性结合的免疫球蛋白分子。抗体可以是源自天然来源或重组来源的完整免疫球蛋白,并且可以是完整免疫球蛋白的免疫反应性部分。抗体通常是免疫球蛋白分子的四聚体。本发明中的抗体可以以多种形式存在,包括例如多克隆抗体、单克隆抗体、细胞内抗体(“内抗体”)、Fv、Fab和F(ab)
如本文所用的“抗体重链”,指的是所有抗体分子在其天然存在的构象中具有的两种类型多肽链中较大的一种。
如本文所用的“抗体轻链”,指的是所有抗体分子在其天然存在的构象中具有的两种类型多肽链中较小的一种。α和β轻链指的是两种主要的抗体轻链同种型。
如本文所用的术语“抗原”或“Ag”,被定义为引发免疫应答的分子。这种免疫应答可能涉及抗体产生或特异性免疫活性细胞的激活,或者二者兼而有之。熟练的技术人员将会理解,任何大分子,包括几乎所有的蛋白质或肽,都可以作为抗原。此外,抗原可以来源于重组或基因组DNA。熟练的技术人员将会理解,任何DNA,包括编码引发免疫应答的蛋白质的核苷酸序列或部分核苷酸序列,因此编码如本文所用的该术语“抗原”。此外,本领域技术人员将会理解,抗原不需要仅由基因的全长核苷酸序列来编码。十分明显的是,本发明包括但不限于使用多于一种基因的部分核苷酸序列,并且这些核苷酸序列以各种组合排列以引发所需的免疫应答。而且,熟练的技术人员将会理解,抗原根本不需要由“基因”来编码。十分明显的是,抗原可以生成或合成,或者可以来源于生物样品。这种生物样品可以包括但不限于组织样品、肿瘤样品、细胞或生物流体。
基因的“编码区”由基因编码链的核苷酸残基和基因非编码链的核苷酸组成,它们分别与由基因转录产生的mRNA分子的编码区同源或互补。
mRNA分子的“编码区”还由mRNA分子的核苷酸残基组成,这些核苷酸残基在mRNA分子的翻译过程中与转运RNA分子的反密码子区匹配或者编码终止密码子。因此,编码区可以包括对应于由mRNA分子编码的成熟蛋白质中不存在的氨基酸残基(例如,蛋白质输出信号序列中的氨基酸残基)的核苷酸残基。
如在本文中用于指核酸的“互补的”,指的是两条核酸链的区域之间或者同一条核酸链的两个区域之间序列互补性的广义概念。已知第一核酸区域的腺嘌呤残基能够与和该第一区域反向平行的第二核酸区域的残基形成特定氢键(“碱基配对”),如果该残基是胸腺嘧啶或尿嘧啶。类似地,已知第一核酸链的胞嘧啶残基能够与和该第一链反向平行的第二核酸链的残基碱基配对,如果该残基是鸟嘌呤。核酸的第一区域与相同或不同核酸的第二区域互补,前提是如果当两个区域以反向平行方式排列时,第一区域的至少一个核苷酸残基能够与第二区域的残基形成碱基配对。优选地,第一区域包含第一部分,并且第二区域包含第二部分,由此当第一和第二部分以反向平行方式排列时,第一部分至少约50%,优选至少约75%、至少约90%或至少约95%的核苷酸残基能够与第二部分中的核苷酸残基碱基配对。更优选地,第一部分的所有核苷酸残基都能够与第二部分中的核苷酸残基碱基配对。
如本文所用的,术语“保守性变异”或“保守性取代”指的是将一个氨基酸残基用另一个生物学上相似的残基替换。保守性变异或取代不太可能改变肽链的形状。保守性变异或取代的示例包括将一个疏水性残基如异亮氨酸、缬氨酸、亮氨酸或蛋氨酸替换另一个疏水性残基,或者用一个极性残基取代另一个极性残基,如用精氨酸取代赖氨酸、用谷氨酸取代天冬氨酸或用谷氨酰胺取代天冬酰胺等。
术语“递送媒介物”在本文中用作泛指能够将化合物递送至受试者的任何递送媒介物,包括但不限于胃肠外递送媒介物。
如本文所用的术语“DNA”被定义为脱氧核糖核酸。
“有效量”或“治疗有效量”在本文中可互换使用,并且指的是如本文所述的化合物、配制品、材料或组合物有效实现特定生物学结果的量。这种结果可以包括但不限于,通过本领域任何合适的手段确定的疾病或病况的治疗。
“编码”指的是多核苷酸如基因、cDNA或mRNA中特定核苷酸序列用作在生物过程中合成其它聚合物和大分子的模板的固有性质,所述聚合物和大分子具有确定的核苷酸序列(即,rRNA、tRNA和mRNA)或确定的氨基酸序列以及由此产生的生物学特性。因此,如果与基因相对应的mRNA的转录和翻译在细胞或其他生物系统中产生蛋白质,则该基因编码该蛋白质。编码链(其核苷酸序列与mRNA序列相同且通常在序列表中提供)和非编码链(其用作基因或cDNA转录的模板)都可以称为编码蛋白质或该基因或cDNA的其他产物。
如本文所用的,术语“EMAPII介导的疾病”意指受试者中EMAPII的水平过高发挥作用的任何疾病,其中通过降低受试者中EMAPII的水平来影响治疗。
非人(例如,鼠类)抗体的“人源化”形式是嵌合的免疫球蛋白、免疫球蛋白链或其片段(诸如Fv、Fab、Fab'、F(ab')2或抗体的其他抗原结合子序列),其含有源自非人免疫球蛋白的极少序列。在大多数情况下,人源化抗体是以下人免疫球蛋白(接受体抗体),其中来自接受体的互补决定区(CDR)的残基替换为来自非人类物种如小鼠、大鼠或兔(供体抗体)的CDR的残基,后者具有所需特异性、亲和力和能力。在一些情况下,人免疫球蛋白的Fv框架区(FR)残基替换为相应的非人残基。而且,人源化抗体可包含既不存在于接受体抗体中,也不存在于导入的CDR或框架序列中的残基。进行这些修饰是为了进一步完善和优化抗体性能。一般来说,人源化抗体将包含基本上所有的至少一个、通常是两个可变结构域,其中所有或基本上所有的CDR区对应于非人免疫球蛋白的那些CDR区,并且所有或基本上所有的FR区是人免疫球蛋白序列的那些FR区。人源化抗体最好还包含免疫球蛋白恒定区(Fc)的至少一部分,通常是人免疫球蛋白的恒定区。有关进一步详细信息,参见Jones等人,Nature,321:522-525,1986;Reichmann等人,Nature,332:323-329,1988;Presta,Curr.Op.Struct.Biol.,2:593-596,1992。
如本文所用的“同一性”指的是两个聚合分子之间,特别是两个氨基酸分子之间,例如两个多肽分子之间的亚基序列同一性。当两个氨基酸序列在相同位置具有相同的残基时;例如,如果两个多肽分子中的每一个中的一个位置均被精氨酸占据时,那么它们在该位置具有同一性。在比对中,两个氨基酸序列在相同位置具有相同残基的同一性或程度经常表示为百分比。两个氨基酸序列之间的同一性是匹配或相同位置数量的直接函数;例如,如果两个序列中有一半的(如,长度为10个氨基酸的聚合物中的5个位置)位置是相同的,那么这两个序列具有50%同一性;如果90%的位置(如,10个中的9个)是匹配或相同的,则这两个氨基酸序列具有90%同一性。
如本文所用的术语“个体”、“患者”或“受试者”,包括任何动物种类的成员,包括但不限于鸟类、人类和其他灵长类动物,以及其他哺乳动物,包括在商业上相关的哺乳动物,诸如牛、猪、马、羊、猫和狗。优选地,受试者是人。
如本文所用的术语“说明材料”,包括出版物、录像、图解或任何其他表达介质,其可用于传达试剂盒中本发明的组合物和/或化合物的有用性。例如,试剂盒的说明材料可以附于含有本发明化合物和/或组合物的容器上,或者与含有该化合物和/或组合物的容器一起装运。备选地,可以将说明材料与容器分开装运,目的是让接收者以协作方式使用说明材料和化合物。说明材料的递送可以是例如通过出版物的物理递送或传达试剂盒的有用性的其他表达介质,或者可以备选地通过电子传输来实现,例如借助于计算机,如通过电子邮件,或从网站下载。
“分离的”意指从天然状态中改变或者移出。例如,活的动物中天然存在的核酸或肽不是“分离的”,但是从其天然状态的共存物质部分或完全脱离的相同核酸或肽是“分离的”。分离的核酸或蛋白质可以以基本上纯化的形式存在,或者可以存在于非天然环境如例如宿主细胞中。
“分离的核酸”指的是一种核酸区段或片段,它们已从天然存在状态下其侧翼序列中分离出来,即一种DNA片段,其已从通常与该片段相邻的序列中移出,这些序列即为在该片段天然存在的基因组中与其相邻的序列。该术语还适用于已从天然伴随核酸的其他组分,即在细胞中天然伴随核酸的RNA或DNA或蛋白质中基本上纯化出的核酸。因此,该术语包括,例如,引入载体、引入自主复制质粒或病毒,或者引入原核生物或真核生物的基因组DNA中的重组DNA,或者作为独立于其他序列的单独分子(即,作为通过PCR或限制性酶消化产生的cDNA或者基因组或cDNA片段)而存在的重组DNA。它还包括作为编码其他多肽序列的杂合基因的一部分的重组DNA。
在本发明的上下文中,使用了下列常见核酸碱基的缩写。“A”指的是腺苷,“C”指的是胞嘧啶,“G”指的是鸟苷,“T”指的是胸苷,并且“U”指的是尿苷。
所谓“核酸”是指任何核酸,无论是由脱氧核糖核苷还是由核糖核苷构成,也无论是由磷酸二酯连接还是由经修饰的连接构成,这些经修饰的连接诸如磷酸三酯、氨基磷酸酯、硅氧烷、碳酸酯、羧甲基酯、乙酰胺酯、氨基甲酸酯、硫醚、桥接氨基磷酸酯(phosphoramidate)、桥接亚甲基膦酸酯(methylene phosphonate)、硫代磷酸酯、甲基膦酸酯、二硫代磷酸酯、桥接硫代磷酸酯或砜连接,以及此类连接的组合。术语“核酸”还具体包括由除了五种生物学上存在的碱基(腺嘌呤、鸟嘌呤、胸腺嘧啶、胞嘧啶和尿嘧啶)之外的碱基构成的核酸。
除非另有说明,否则“编码氨基酸序列的核苷酸序列”包括所有彼此为简并形式且编码相同氨基酸序列的核苷酸序列。短语编码蛋白质或RNA的核苷酸序列也可能包括内含子,就编码蛋白质的核苷酸序列在某些形式中可能包含一个或多个内含子而言。
本文使用常规表示法来描述多核苷酸序列:单链多核苷酸序列的左手端是5'端;双链多核苷酸序列的左手方向称为5'方向。
核苷酸到新生RNA转录本的5'到3'方向添加称为转录方向。与mRNA具有相同序列的DNA链称为“编码链”;DNA链上位于DNA上参考点5'处的序列称为“上游序列”;DNA链上位于DNA上参考点3'处的序列称为“下游序列”。
术语“寡核苷酸”通常指的是短多核苷酸,一般不超过约60个核苷酸。应当理解的是,当核苷酸序列由DNA序列(即A、T、G、C)表示时,这也包括RNA序列(即A、U、G、C),其中“U”替换了“T”。
术语“可操作地连接”指的是调节序列和异源核酸序列之间的功能性连接,其结果是表达后者。例如,当第一核酸序列与第二核酸序列处于功能关系时,则该第一核酸序列与该第二核酸序列可操作地连接。例如,如果启动子影响编码序列的转录或表达,则该启动子与编码序列可操作地连接。总体来说,可操作地连接的DNA序列是接近的,并且在必要时在同一阅读框中连接两个蛋白质编码区。
如本文所用的术语“启动子”被定义为启动多核苷酸序列特异性转录所需的由细胞的合成机制或所引入的合成机制识别的DNA序列。
如本文所用的,术语“启动子/调节序列”意指与启动子/调节序列可操作地连接的基因产物表达所需的核酸序列。在一些情况下,该序列可以是核心启动子序列,在其他情况下,该序列还可以包括增强子序列和基因产物表达所需的其他调节元件。例如,启动子/调节序列可以是一种以组织特异性方式表达基因产物的启动子/调节序列。
如本文所用的,术语“药物组合物”指的是至少一种本发明的化合物与其他化学成分,如载剂、稳定剂、稀释剂、分散剂、悬浮剂、增稠剂和/或赋形剂的混合物。该药物组合物有助于将化合物施用于生物体。本领域存在多种施用化合物的技术,包括但不限于静脉内、经口、气雾剂、胃肠外、眼部、肺部和局部施用。
“药学上可接受的”指的是从药理学/毒理学角度来看,患者可接受的,以及从物理/化学角度来看,药物生产化学家可接受的关于组成、配方、稳定性、患者接受度和生物利用度的那些性质和/或物质。“药学上可接受的载剂”指的是一种不干扰活性成分(一种或多种)的生物活性的有效性且对接受其施用的宿主无毒的介质。
如本文所用的术语“多核苷酸”被定义为核苷酸的链。此外,核酸是核苷酸的聚合物。因此,如本文所用的核酸和多核苷酸是可以互换的。本领域技术人员一般都知道核酸是多核苷酸,它们可以水解成单体“核苷酸”。单体核苷酸可以水解成核苷。如本文所用的多核苷酸,包括但不限于通过本领域现有的任何手段获得的所有核酸序列,这些手段包括但不限于重组手段,即,利用普通克隆技术和PCR
如本文所用的,术语“蛋白质”、“肽”和“多肽”可互换使用,并且指的是由肽键共价连接的氨基酸残基构成的化合物。术语“肽键”意指由一个氨基酸的羧基和第二氨基酸的氨基之间失去一分子水而形成的共价酰胺键。蛋白质或肽必须包含至少两个氨基酸,并且对可构成蛋白质或肽序列的氨基酸最大数量没有限制。多肽包括包含两个或更多个通过肽键彼此连接的氨基酸的任何肽或蛋白质。如本文所用的,该术语既指短链,也指较长链,短链在本领域中通常也被称为例如肽、寡肽和寡聚物,较长链在本领域中通常被称为蛋白质,蛋白质中有许多类型。“蛋白质”包括,例如生物活性片段、基本上同源的蛋白质、寡肽、同二聚体、异二聚体、蛋白质变体、修饰的蛋白质、衍生物、类似物和融合蛋白等。蛋白质包括天然蛋白质、重组蛋白质、合成蛋白质或其组合。蛋白质可以是受体或非受体。
如本文所用的术语“重组DNA”被定义为通过连接来自不同来源的DNA片段而产生的DNA。
如本文所用的术语“重组多肽”被定义为通过使用重组DNA方法产生的多肽。
如本文所用的术语“RNA”被定义为核糖核酸。
如本文所用的术语“治疗性”意指治疗和/或预防。
如本文所用的术语“治疗/处理”意指降低受试者出现症状的频率,或者施用药剂或化合物以降低出现症状的频率和/或严重程度。如本文所用的,“缓解”可与术语“治疗/处理”互换使用。
如本文所用的,“治疗疾病、病症或病况”意指降低受试者出现疾病、病症或病况的症状的频率或严重程度。治疗疾病、病症或病况可包括也可不包括完全根除或消除症状。
“表达载体”指的是一种包含重组多核苷酸的载体,该重组多核苷酸包含与待表达的核苷酸序列可操作性连接的表达调控序列。表达载体包含足够用于表达的顺式作用元件;用于表达的其他元件可由宿主细胞提供或在体外表达系统中提供。表达载体包括本领域已知的所有载体,诸如并入了重组多核苷酸的粘粒、质粒(例如,裸质粒或包含在脂质体中的质粒)和病毒(例如,逆转录病毒、腺病毒和腺相关病毒)。
“载体”是一种包含基因的物质组成,并可用于将基因递送至细胞内部。载体指的是任何含有该基因的质粒,它能够将外来序列转移到靶生物体或靶细胞的基因组中。
如本文所用的,术语“片段”应用于核酸时,小于整体。
本文使用了以下缩写:V
范围:在整个本公开中,本发明的各个方面都可以用范围形式来表示。应当理解,范围形式的描述只是为了方便和简明,而不应被解释为对本发明范围的硬性限制。相应地,对范围的描述应被视为已明确公开了所有可能的子范围以及该范围内的单个数值。例如,对一个范围诸如从1至6的描述应被认为已经明确公开了子范围诸如从1至3、从1至4、从1至5、从2至4、从2至6、从3至6等,以及该范围内的单个数字,例如,1、2、2.7、3、4、5、5.3和6。无论范围的宽度如何,这都是适用的。
描述
本发明提供了一种识别前体和成熟EMAPII的人源化单克隆抗体。该抗体包含四种轻链可变区之一和五种重链可变区之一。本发明还提供了一种嵌合的抗EMAPII抗体。进一步公开了用于递送抗体的药物组合物以及通过用本发明的抗体靶向EMAPII来治疗疾病的方法。
抗体、载体和包含抗体的组合物
一方面,本发明提供了一种人源化抗EMAPII抗体。该抗体包括重链可变结构域和轻链可变结构域,该重链可变结构域包含与SEQ ID NO:1至SEQ ID NO:5中任一项具有90%或更高序列同一性的氨基酸序列,该轻链可变结构域包含与SEQ ID NO:6至SEQ ID NO:9中任一项具有90%或更高序列同一性的氨基酸序列。如图1-8和实施例1所示,本文公开的抗体结合前体EMAPII和成熟EMAPII。
H4424(人源化HC1)SEQ ID NO:1
MDPKGSLSWRILLFLSLAFELSYGEVQLVESGGGLVQPGGSLKLSCAASGFTFSDAAMYWVRQASGKGLEWVGRIRTKPNNYATYYAASVKGRFTISRDDSKNTAYLQMNSLKTEDTAVYYCTSWSYDFDYWGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPG
H4425(人源化HC2)SEQ ID NO:2
MDPKGSLSWRILLFLSLAFELSYGAVQLVESGGGLVQPGGSLKLSCAASGFTFSDAAMYWVRQASGKGLEWVARIRTKPNNYATYYAASVKGRFTISRDDSKNTVYLQMNSLKTEDTAVYYCTSWSYDFDYWGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPG
H4426(人源化HC3)SEQ ID NO:3
MDPKGSLSWRILLFLSLAFELSYGAVHLVESGGGLVQPGGSLKLSCAASGFTFSDAAMYWVRQASGKGLEWVARIRTKPNNYATYYAASVKGRFTISRDDSKNTVYLQMNSLKTEDTAVYYCTSWSYDFDYWGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPG
H4427(人源化HC4)SEQ ID NO:4
MDPKGSLSWRILLFLSLAFELSYGEVQLVESGGGLVQPGGSLKLSCAASGFTFSDAAIYWVRQASGKGLEWVARIRTKPNNYATYYAASVKGRFTISRDDSNSTAYLQMNSLKTEDTAVYYCTSWSYDFDYWGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPG
H4428(人源化HC5)SEQ ID NO:5
MDPKGSLSWRILLFLSLAFELSYGAVQLVESGGGLVQPGGSLKLSCAASGFTFSDAAMYWVRQASGKGLEWVARIRTKPNNYATYYAASVKGRFTISRDDSNSTAYLQMNSLKTEDTAVYYCTSWSYDFDYWGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPG
L4424(人源化LC1)SEQ ID NO:6
METDTLLLWVLLLWVPGSTGDIVMTQSPLSLPVTPGEPASISCRSSKSLLHSSGKTYLNWYLQKPGQSPQLLIYWMSNRASGVPDRFSGSGSGTDFTLKISRVEAEDVGVYYCQQFLEYPLTFGQGTKLEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
L4425(人源化LC2)SEQ ID NO:7
METDTLLLWVLLLWVPGSTGDIVMTQSPLSLPVTPGEPASISCRSSKSLLHSSGKTYLNWYLQKPGQSPQLLIYWMSTRASGVPDRFSGSGSGTDFTLKISRVEAEDVGVYYCQQFLEYPLTFGQGTKLEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
L4426(人源化LC3)SEQ ID NO:8
METDTLLLWVLLLWVPGSTGDIVMTQSPLSLPVTPGEPASISCRSSKSLLHSSGKTYLNWYLQKPGQSPQLLIYWMSTRASGVPDRFSGSGSGTDFTLKISRVEAEDVGVYYCQQFLEYPLTFGGGTKVEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
L4427(人源化LC4)SEQ ID NO:9
METDTLLLWVLLLWVPGSTGDIQMTQSPLSLPVTPGEPASISCRSSKSLLHSSGKTYLNWYLQKPGQSPQLLIYWMSTRASGVPDRFSGSGSGTDFTLKISRVEAEDVGVYYCQQFLEYPLTFGGGTKVEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
在多个实施方案中,人源化抗EMAPII抗体的重链和轻链可变区之一或两者包含分别与SEQ ID NO:1至SEQ ID NO:5和SEQ ID NO:6至SEQ ID NO:9具有95%或更高、96%或更高、97%或更高、98%或更高、99%或更高或者100%序列同一性的氨基酸序列。
另一方面,本发明提供了一种嵌合的抗EMAPII抗体,其包含与SEQ ID NO:10具有90%或更高序列同一性的重链可变结构域和与SEQ ID NO:11具有90%或更高序列同一性的轻链可变结构域。
MHC1309HC.4SEQ ID NO:10
AVHLVESGGGFVQPTESLKISCAASGFTFSDAAMYWVRQAPGKGLEWVARIRTKPNNYATYYADSVKGRFTISRDDSKSMVYLQMDNLKTEDTAMYYCTSWSYDFDYWGQGVMVTVSS
MHC1309LC.1SEQ ID NO:11
DIVMTQGALPNPVPSGESASITCQSSKSLLHSSGKTYLNWYLQRPGQSPHLLIYWMSTRASGVSDRLSGSGSGTDFTLKISSVEAEDVGVYYCQQFLEYPLTFGSGTKLEIK
在多个实施方案中,嵌合的抗EMAPII抗体的重链和轻链可变区之一或两者包含分别与SEQ ID NO:10和SEQ ID NO:11具有95%或更高、96%或更高、97%或更高、98%或更高、99%或更高或者100%序列同一性的氨基酸序列。
另一方面,本发明提供了一种重组载体,其包含编码SEQ ID NO:1至SEQ ID NO:11中任一项所示氨基酸序列的核酸。在多个实施方案中,该载体包含编码如SEQ ID NO:1至SEQ ID NO:5中任一项所示的人源化抗EMAPII抗体重链的核酸。在多个实施方案中,该载体包含编码如SEQ ID NO:6至SEQ ID NO:11中任一项所示的人源化抗EMAPII抗体轻链的核酸。在多个实施方案中,该载体包含编码如SEQ ID NO:1至SEQ ID NO:5中任一项所示的人源化抗EMAPII抗体重链和如SEQ ID NO:6至SEQ ID NO:9中任一项所示的人源化抗EMAPII抗体轻链的核酸。在多个实施方案中,该核酸与启动子可操作地连接。在多个实施方案中,本发明提供了一种用该重组载体转化的细胞。本发明进一步提供了一种产生如SEQ ID NO:1至SEQ ID NO:5中任一项所示的人源化抗EMAPII抗体重链和如SEQ ID NO:6至SEQ ID NO:9中任一项所示的人源化抗EMAPII抗体轻链的方法,包括在表达抗体的条件下培养用该载体转化的细胞。
简单汇总来说,通常通过将编码抗体多肽或其部分的核酸可操作地连接至启动子并将该构建体引入表达载体中,来实现编码抗体的天然或合成核酸的表达。该载体可适用于在真核生物中复制和整合。典型的克隆载体包含转录和翻译终止子、起始序列和启动子,可用于调节所需核酸序列的表达。
可以将核酸克隆到许多类型的载体中。例如,可以将核酸克隆到包括但不限于质粒、噬菌粒、噬菌体衍生物、动物病毒和粘粒的载体中。特别感兴趣的载体包括表达载体、复制载体、探针生成载体和测序载体。
此外,可以将表达载体以病毒载体的形式提供给细胞。病毒载体技术在本领域中是众所周知的,并且在例如下列中进行了描述,即Sambrook等人,Molecular Cloning:ALaboratory Manual,1-3卷(第3版,Cold Spring Harbor Press,NY 2001),以及其他病毒学和分子生物学手册。可用作载体的病毒包括但不限于逆转录病毒、腺病毒、腺相关病毒、疱疹病毒和慢病毒。一般来说,合适的载体包含在至少一种生物体中功能性的复制起点、启动子序列、实用的限制性内切核酸酶位点以及一种或多种可筛选标志物(例如,WO 01/96584;WO 01/29058;和第6,326,193号美国专利)。
额外的启动子元件,例如增强子,调节转录起始的频率。通常情况下,这些位于起始位点上游30-110bp的区域,尽管最近证明一些启动子也含有起始位点下游的功能性元件。启动子元件之间的间距经常是灵活的,因此当元件相对于彼此反转或移动时,启动子功能得以保留。在胸苷激酶(tk)启动子中,启动子元件之间的间距可增加到50bp,然后活性才开始下降。根据启动子的不同,似乎单个元件可以协同或独立地发挥作用以激活转录。
启动子的一个示例是EF1α启动子。另一个示例包括立即早期巨细胞病毒(CMV)启动子序列。该启动子序列是一个强组成型启动子序列,能够驱动与其可操作性连接的任何多核苷酸序列的高水平表达。然而,也可以使用其他组成型启动子序列,包括但不限于猿猴病毒40(SV40)早期启动子、小鼠乳腺肿瘤病毒(MMTV)、人类免疫缺陷病毒(HIV)长末端重复(LTR)启动子、MoMuLV启动子、禽白血病病毒启动子、EB病毒(Epstein-Barr virus)立即早期启动子、劳斯肉瘤病毒启动子以及人类基因启动子,诸如但不限于肌动蛋白启动子、肌球蛋白启动子、血红蛋白启动子和肌酸激酶启动子。此外,本发明不应局限于使用组成型启动子。还涵盖了将诱导型启动子作为本发明的一部分。诱导型启动子的使用提供了一种分子开关,当需要与其可操作地连接的多核苷酸序列的表达时,该分子开关能够开启多核苷酸序列的这种表达,或者当不需要该表达时,该分子开关能够关闭表达。诱导型启动子的示例包括但不限于金属硫蛋白启动子、糖皮质激素启动子、孕酮启动子和四环素启动子。
为了评估抗体多肽或其部分的表达,待导入细胞内的表达载体还可包含可选择的标志物基因或报告基因或两者,以便于从试图通过病毒载体转染或感染的细胞群体中鉴定和选择表达细胞。在其它方面,可以在不同的DNA片段上携带可选择标志物,并用于共转染程序。可以在可选择标志物和报告基因的侧翼都加上适当的调节序列,以实现在宿主细胞中的表达。有用的可选择标志物包括例如抗生素抗性基因,如neo等。
报告基因用于鉴定可能转染的细胞并用于评估调节序列的功能性。一般来说,报告基因是接受体生物体或组织中不存在或者不由其表达的基因,并且它编码多肽,该多肽的表达表现为一些易于检测的特性,例如酶活性。在将DNA导入接受体细胞后的适当时间测定报告基因的表达。合适的报告基因可包括编码下列的基因:萤光素酶、β-半乳糖苷酶、氯霉素乙酰转移酶、分泌型碱性磷酸酶或绿色荧光蛋白基因(例如,Ui-Tei等人,2000FEBSLetters 479:79-82)。合适的表达系统是众所周知的,并且可以使用已知技术制备或从市场上获得。一般来说,显示出报告基因的最高表达水平的具有最小5'侧翼区的构建体被鉴定为启动子。这种启动子区域可以与报告基因相连,并用于评估作用剂调节启动子驱动转录的能力。
将基因导入细胞并在细胞中表达的方法是本领域已知的。在表达载体的情况下,可以通过本领域的任何方法将载体轻易地导入宿主细胞,例如哺乳动物、细菌、酵母或昆虫细胞。例如,可以通过物理、化学或生物手段将表达载体转移到宿主细胞中。
将多核苷酸导入宿主细胞的物理方法包括磷酸钙沉淀、脂质转染、粒子轰击、显微注射、电穿孔等。用于产生包含载体和/或外源核酸的细胞的方法在本领域是众所周知的。参见,例如,Sambrook等人,Molecular Cloning:A Laboratory Manual,1-3卷(第3版,ColdSpring Harbor Press,NY 2001)。
将感兴趣的多核苷酸导入宿主细胞的生物学方法包括使用DNA和RNA载体。病毒载体,尤其是逆转录病毒载体,已经成为将基因插入哺乳动物细胞例如人类细胞的最广泛使用的方法。其他病毒载体可以来源于慢病毒、痘病毒、单纯疱疹病毒I型、腺病毒和腺相关病毒等。参见,例如,第5,350,674号和第5,585,362号美国专利。
用于将多核苷酸导入宿主细胞的化学手段包括胶体分散系统,诸如大分子复合物、纳米胶囊、微球、珠和基于脂质的系统,包括水包油乳液、胶束体、混合胶束体和脂质体。用作体外和体内递送媒介物的示例性胶体系统是脂质体(例如,人工膜囊泡)。
在利用非病毒递送系统的情况下,示例性递送媒介物是脂质体。涵盖使用脂质配制品将核酸导入宿主细胞(体外、离体或体内)。在另一方面,核酸可以与脂质缔合。可以将与脂质缔合的核酸封装在脂质体的水相内部、散布在脂质体的脂质双层内、通过连接分子(与脂质体和寡核苷酸都缔合)附着在脂质体上、包封于脂质体中、与脂质体形成复合物、分散在含有脂质的溶液中、与脂质混合、与脂质组合、作为悬浮液包含在脂质中、包含在胶束体中或与胶束体形成复合物,或者以其他方式与脂质缔合。脂质、脂质/DNA或脂质/表达载体相关组合物不限于溶液中的任何特定结构。例如,它们可能存在于双层结构中,作为胶束体或具有“塌陷”结构。它们也可能简单地散布在溶液中,可能形成大小或形状不均一的聚集体。脂质是脂肪物质,其可以是天然存在的或合成的脂质。例如,脂质包括天然存在于细胞质中的脂肪液滴以及含有长链脂肪烃及其衍生物的一类化合物,例如脂肪酸类、醇类、胺类、氨基醇类和醛类。
适用的脂质可从商业来源获得。例如,二肉豆蔻酰磷脂酰胆喊(“DMPC”)可以获自Sigma,St.Louis,MO;磷酸二鲸蜡脂(“DCP”)可以获自K&K Laboratories(Plainview,NY);胆固醇(“Choi”)可以获自Calbiochem-Behring;二肉豆蔻酰磷脂酰甘油(“DMPG”)和其他脂质可以获自Avanti Polar Lipids,Inc.(Birmingham,AL.)。氯仿或氯仿/甲醇中的脂质储备溶液可在约-20℃储存。将氯仿用作唯一的溶剂,因为它比甲醇更容易蒸发。“脂质体”是一个通用术语,包括通过产生封闭的脂质双层或聚集体而形成的各种单层和多层脂质媒介物。脂质体的特征在于具有囊泡结构,带有磷脂双层膜和内部水性介质。多层脂质体具有由水性介质分隔的多个脂质层。当磷脂悬浮在过量的水溶液中时,它们会自发形成。脂质成分进行自重排,然后形成封闭式结构,并将水和溶解的溶质捕获在脂质双层之间(Ghosh等人,1991 Glycobiology 5:505-10)。然而,还包括在溶液中具有不同于正常囊泡结构的结构的组合物。例如,脂质可能呈现出胶束结构或仅作为脂质分子的非均一聚集体存在。还涵盖lipofectamine-核酸复合物。
在多个实施方案中,本发明提供了一种药物组合物,其包含所述抗体和至少一种药学上可接受的赋形剂。药物组合物可以是适于向患者递送抗体的任何形式,并且该药物组合物的具体情况将根据提供该药物组合物所针对的适应证而变化。合适的药用赋形剂的实例在本文别处公开。
治疗疾病的方法
EMAPII与香烟烟雾诱发的肺部损伤以及一般性肺部损伤有关。如图1-8所示,本发明的抗体结合前体EMAPII和成熟EMAPII两者。相应地,在多个实施方案中,本发明提供了一种在有此需要的受试者中治疗慢性阻塞性肺病(COPD)特别是肺气肿的方法,该方法包括以药物组合物的形式向受试者施用如本文公开的人源化抗EMAPII抗体。
在多个实施方案中,本发明提供了一种在有此需要的受试者中治疗肺气肿的方法,该方法包括以药物组合物的形式向受试者施用如本文公开的人源化抗EMAPII抗体。
在多个实施方案中,本发明提供了一种在有此需要的受试者中治疗急性肺部损伤的方法,该方法包括以药物组合物的形式向受试者施用如本文公开的人源化抗EMAPII抗体。
在多个实施方案中,本发明提供了一种在有此需要的受试者中治疗支气管肺发育异常的方法,该方法包括以药物组合物的形式向受试者施用如本文公开的人源化抗EMAPII抗体。
本文公开的抗EMAPII抗体结合EMAPII并降低可用于与靶细胞相互作用的EMAPII的水平。相应地,在多个实施方案中,本发明提供了一种在有此需要的受试者中治疗EMAPII介导的疾病的方法,该方法包括以药物组合物的形式向受试者施用如本文公开的人源化抗EMAPII抗体。
施用/剂量/配制品
将本发明的化合物和/或组合物施用于患者,优选哺乳动物,更优选人类,可以使用已知的程序、以有效治疗拟用疾病的剂量和时间段来进行。治疗拟用疾病所必需的治疗性化合物的有效量可根据下列因素而变化,诸如患者的疾病或病症状态;患者的年龄、性别和体重;以及用于检测本发明化合物的设备。本领域普通技术人员将能够研究相关因素并确定治疗性化合物的有效量,而无需进行过度实验。
本发明所述的药物组合物中活性成分的实际剂量水平可能变化,以获得一定量的活性成分,对于特定的患者、组合物和施用方式,这样的量有效地实现治疗,而不会对患者产生毒性。
在某些实施方案中,使用一种或多种药学上可接受的赋形剂或载剂来配制本发明的组合物。在某些实施方案中,本发明的药物组合物包含有效量的本发明化合物和药学上可接受的载剂。
载剂可以是溶剂或分散介质,其包含例如水、乙醇、多元醇(例如,甘油、丙二醇和液态聚乙二醇等)、它们的合适混合物以及植物油。例如,可以通过使用包衣如卵磷脂、通过在分散的情况下保持所需的粒径以及通过使用表面活性剂来维持适当的流动性。可以通过各种抗细菌剂和抗真菌剂,例如对羟基苯甲酸酯、氯丁醇、酚、抗坏血酸、硫柳汞等,来实现预防微生物的作用。在许多情况下,优选在组合物中包括等渗剂,例如糖类、氯化钠或多元醇如甘露醇和山梨糖醇。可通过在组合物中包含延迟吸收的作用剂,例如单硬脂酸铝或明胶,来实现注射用组合物的吸收时间延长。
用于施用的本发明化合物可以在下列范围中:约1μg至约10,000mg、约20μg至约9,500mg、约40μg至约9,000mg、约75μg至约8,500mg、约150μg至约7,500mg、约200μg至约7,000mg、约350μg至约6,000mg、约500μg至约5,000mg、约750μg至约4,000mg、约1mg至约3,000mg、约10mg至约2,500mg、约20mg至约2,000mg、约25mg至约1,500mg、约30mg至约1,000mg、约40mg至约900mg、约50mg至约800mg、约60mg至约750mg、约70mg至约600mg、约80mg至约500mg,以及其间的任何和所有整体或部分增量。
在某些实施方案中,本发明化合物的剂量为约1mg至约2,500mg。在某些实施方案中,用于本文所述组合物的本发明化合物的剂量小于约10,000mg、或小于约8,000mg、或小于约6,000mg、或小于约5,000mg、或小于约3,000mg、或小于约2,000mg、或小于约1,000mg、或小于约500mg、或小于约200mg、或小于约50mg。类似地,在某些实施方案中,如本文所述的第二化合物的剂量小于约1,000mg、或小于约800mg、或小于约600mg、或小于约500mg、或小于约400mg、或小于约300mg、或小于约200mg、或小于约100mg、或小于约50mg、或小于约40mg、或小于约30mg、或小于约25mg、或小于约20mg、或小于约15mg、或小于约10mg、或小于约5mg、或小于约2mg、或小于约1mg、或小于约0.5mg,以及其任何和所有整体或部分增量。
配制品可以采用与常规赋形剂的混合物,这些常规赋形剂即为适用于经口、胃肠外、鼻腔、静脉内、皮下、肠内或本领域已知的任何其他合适施用方式的药学上可接受的有机或无机载剂物质。可以对药物制备物进行灭菌,并且如果期望的话,可以将其与助剂混合,例如润滑剂、防腐剂、稳定剂、润湿剂、乳化剂、用于影响渗透压的盐类、缓冲剂、着色剂、矫味剂和/或芳香物质等。
本发明的任何组合物的施用途径包括经口、鼻腔、直肠、阴道内、胃肠外、颊部、舌下或局部。可以将用于本发明的化合物配制为用于通过任何合适的途径施用,诸如用于经口或胃肠外,例如经皮、跨粘膜(如,舌下、舌、(经)颊部、(经)尿道、阴道(如,经阴道和阴道周)、鼻腔(内)和(经)直肠)、膀胱内、肺内、十二指肠内、胃内、鞘内、皮下、肌内、皮内、动脉内、静脉内、支气管内、吸入以及局部施用。
合适的组合物和剂型包括例如片剂、胶囊剂、囊片、丸剂、凝胶囊(gel caps)、锭剂(troche)、分散剂、混悬剂、溶液剂、糖浆剂、颗粒剂、珠剂、透皮贴剂、凝胶剂、散剂、小球剂(pellets)、乳浆剂、锭剂(lozenge)、乳膏剂、糊剂、硬膏剂、洗剂、薄片剂(discs)、栓剂、用于鼻腔或经口施用的液体喷雾剂、用于吸入的干粉或雾化配制品以及用于膀胱内施用的组合物和配制品等。应该理解的是,可用于本发明的配制品和组合物不限于本文所述的特定配制品和组合物。
胃肠外施用
如本文所用的,药物组合物的“胃肠外施用”包括特征在于物理性裂开受试者的组织并通过组织中的裂口施用药物组合物的任何施用途径。因此,胃肠外施用包括但不限于通过注射组合物、通过手术切口应用组合物、通过组织穿透性非手术伤口应用组合物等来施用药物组合物。具体而言,涵盖胃肠外施用包括但不限于皮下、静脉内、腹膜内、肌内、胸骨内注射和肾透析输注技术。
适用于胃肠外施用的药物组合物的配制品包含活性成分和与其组合的药学上可接受的载剂,例如无菌水或无菌等渗盐水。此类配制品可以以适于推注施用或连续施用的形式制备、包装或销售。注射用配制品可以以单位剂型制备、包装或销售,例如在安瓿中,或者在含有防腐剂的多剂量容器中。用于胃肠外施用的配制品包括但不限于混悬剂、溶液剂、油性或水性媒介物中的乳剂、糊剂和植入式缓释或可生物降解的配制品。此类配制品还可包含一种或多种附加成分,包括但不限于悬浮剂、稳定剂或分散剂。在用于胃肠外施用的配制品的某些实施方案中,活性成分以干燥(即,粉状物或粒状物)形式提供,用于在胃肠外施用重构组合物之前用合适的媒介物(例如,灭菌无热原水)进行重构。
药物组合物可以以无菌注射用水性或油性混悬剂或溶液剂的形式制备、包装或销售。这种混悬剂或溶液剂可以根据已知技术配制,并且除了活性成分之外,它们还可以包含附加成分,例如本文所述的分散剂、润湿剂或悬浮剂。这种无菌注射用配制品可以使用无毒的胃肠外可接受的稀释剂或溶剂,例如水或1,3-丁二醇来制备。其他可接受的稀释剂和溶剂包括但不限于林格氏液、等渗氯化钠溶液和不挥发油,如合成的甘油单酯类或甘油二酯类。其他有用的胃肠外可施用配制品包括那些含有微晶形式、脂质体制剂形式或作为可生物降解聚合物系统组分的活性成分的配制品。用于缓释或植入的组合物可以包含药学上可接受的聚合或疏水性材料,例如乳液、离子交换树脂、略溶性聚合物或略溶性盐。
其他施用形式
本发明的其他剂型包括如在下列中描述的剂型:第6,340,475号;第6,488,962号;第6,451,808号;第5,972,389号;第5,582,837号;和第5,007,790号美国专利。本发明的其他剂型还包括如在下列中描述的剂型:第2003/0147952号;第2003/0104062号;第2003/0104053号;第2003/0044466号;第2003/0039688号;和第2002/0051820号美国专利申请。本发明的其他剂型还包括如在下列中描述的剂型:PCT申请号为WO 03/35041;WO03/35040;WO03/35029;WO 03/35177;WO 03/35039;WO 02/96404;WO02/32416;WO 01/97783;WO 01/56544;WO 01/32217;WO 98/55107;WO98/11879;WO 97/47285;WO 93/18755;和WO 90/11757的申请。
实验性实施例
通过参考以下实验性实施例,对本发明作进一步详细描述。除非另有说明,所提供的这些实施例仅用于说明的目的,而并非意在进行限制。因此,本发明决不应理解为仅限于以下实施例,而应理解为涵盖由于本文提供的教导而变得明显的任何和所有变化。
无需进一步描述,相信本领域普通技术人员可以使用前面的描述和下面的说明性实施例来实施本发明所要求保护的方法。因此,以下工作实施例具体指出了本发明的优选实施方案,并且不应理解为以任何方式限制本公开的其余部分。
实施例1:
大鼠杂交瘤IgG可变区和恒定区的克隆和测序
进行cDNA末端快速扩增(RACE)以扩增V
使用计算机模拟分析进行亲本抗体的人源化设计。人源化过程始于生成同源性建模的抗体3D结构,并基于结构建模创建亲本抗体的轮廓。根据整个框架的总体序列同一性、匹配的界面位置、相似分类的CDR典型位置以及必须要去除的N-糖基化位点的存在,鉴定了要采用的接受体框架。选定两个轻链(LC)和两个重链(HC)框架进行人源化设计。
通过创建多个杂合序列来设计人源化抗体,这些杂合序列将亲本抗体序列的选定部分与人框架序列相融合。使用3D模型,通过肉眼和计算机建模对这些人源化序列进行系统分析,以分离出最有可能保留抗原结合的序列。目标是在保留原始抗体特异性的同时,最大限度地提高最终人源化抗体中人类序列的量。
基于两种不同的重链和轻链人类接受体框架,设计了三种人源化轻链和五种人源化重链(参见表1)。HC1和LC1利用第一种各自的框架,并含有最多的人类序列和最少的亲本抗体框架序列。HC2、HC3和LC2使用与之前相同的框架,但含有额外的亲本序列。HC4、HC5、LC3和LC4利用第二种各自的框架,并且还包含与人类框架融合的额外亲本序列。
表1:人源化链信息表
人源化链的人源性分数的计算
单克隆抗体的人源性分数是根据下列来计算的,即Gao,S.H.,Huang,K.,Tu,H.和Adler,A.S.2013,Monoclonal antibody humanness score and its applications.BMCBiotechnology,13:55。该分数表示在人类中的抗原性降低方面,抗体可变区序列与人类的相似程度,这是在对抗体进行人源化时的一个重要因素。亲本抗体和人源化抗体的人源性分数如下所示。根据这种方法,对于重链来说,79或更高的分数表明就其抗原性而言是类人抗体;对于κ轻链来说,86或更高的分数表明就其抗原性而言是类人抗体。
表2:重链的人源性分数
/>
表3:轻链的人源性分数
人源化抗体的构建
通过首先合成可变区序列来构建全长抗体基因。为了在哺乳动物细胞中表达,对序列进行了优化。然后将这些可变区序列克隆到已经含有人Fc结构域的表达载体中。此外,为了进行比较,使用相同的主链Fc序列将亲本重链和轻链的可变区构建为全长嵌合链。
小规模生产
人源化抗体的产量为0.03升。还对嵌合性亲本抗体进行了规模放大,以进行直接比较。在不存在血清的情况下,使用化学成分确定的培养基将所示重链和轻链的质粒转染到悬浮的HEK293细胞中,以制备抗体。具体而言,对抗体序列进行基因合成,并克隆到专有表达载体pLEV123中。使用MabSelect SuRe蛋白A介质(GE Healthcare)纯化条件培养基中的全部抗体。
表3:在HEK293细胞中瞬时产生的抗体
/>
人源化抗体的结合ELISA
对20种人源化抗体、嵌合性亲本抗体和大鼠亲本抗体进行了剂量依赖性结合ELISA。用磷酸盐缓冲盐水(PBS)中的人前体EMAPII以2μg/mL的浓度将ELISA板在4℃包被过夜。所有抗体均用0.05%的含吐温磷酸盐缓冲盐水(PBST)以7点、4倍连续稀释法稀释,从10μg/mL开始,最后一点是单独的PBST。将抗体在预先封闭的ELISA板上孵育1.5小时,然后用0.05% PBST洗涤3次。用HRP测定稀释剂将二级抗体(辣根过氧化物酶(HRP)-抗人IgG Fc或HRP-抗大鼠IgG Fc)稀释5000倍,并在室温孵育1小时。然后将板洗涤4次,并加入TMB底物。在室温显色5分钟,然后用1N HCl终止反应。结合曲线见图1-4。
与前体和成熟EMAPII的结合
对20种抗体进行了剂量依赖性结合ELISA,结果如图5-8所示。抗原包被为2μg/mL,在4℃过夜。用PBS中的2% BSA封闭,室温1.5小时。在室温以10μg/mL、1:4稀释度进行1小时的一抗孵育。对于人源化和嵌合抗体,检测抗体是山羊抗人抗体;对于大鼠亲本抗体,检测抗体是山羊抗大鼠抗体。室温1小时(1:10000的稀释度)。
列举的实施方案列表
实施方案1.一种人源化抗内皮单核细胞激活多肽II(抗EMAPII)抗体,包含:
重链可变结构域,其具有与SEQ ID NO:1至SEQ ID NO:5中任一项有90%或更高的序列同一性的氨基酸序列;以及
轻链可变结构域,其具有与SEQ ID NO:6至SEQ ID NO:9中任一项有90%或更高的序列同一性的氨基酸序列。
实施方案2.根据实施方案1所述的抗体,其中重链可变结构域具有与SEQ ID NO:1至SEQ ID NO:5中任一项有95%或更高的序列同一性的氨基酸序列;并且
轻链可变结构域具有与SEQ ID NO:6至SEQ ID NO:9中任一项有95%或更高的序列同一性的氨基酸序列。
实施方案3.根据实施方案1所述的抗体,其中重链可变结构域具有与SEQ ID NO:2或SEQ ID NO:3中任一项有99%或更高的序列同一性的氨基酸序列;并且
轻链可变结构域具有与SEQ ID NO:6或SEQ ID NO:9中任一项有99%或更高的序列同一性的氨基酸序列。
实施方案4.一种人源化抗内皮单核细胞激活多肽II(抗EMAPII)抗体,包含重链可变结构域,该重链可变结构域具有与SEQ ID NO:1至SEQ ID NO:5中任一项有90%或更高的序列同一性的氨基酸序列。
实施方案5.根据实施方案4所述的抗体,其中重链可变结构域具有与SEQ ID NO:2或SEQ ID NO:3中任一项有95%或更高的序列同一性的氨基酸序列。
实施方案6.一种人源化抗内皮单核细胞激活多肽II(抗EMAPII)抗体,包含轻链可变结构域,该轻链可变结构域具有与SEQ ID NO:6至SEQ ID NO:9中任一项有90%或更高的序列同一性的氨基酸序列。
实施方案7.根据实施方案6所述的抗体,其中轻链可变结构域具有与SEQ ID NO:6或SEQ ID NO:9中任一项有95%或更高的序列同一性的氨基酸序列。
实施方案8.一种嵌合性抗内皮单核细胞激活多肽II(抗EMAPII)抗体,包含与SEQID NO:10具有90%或更高序列同一性的重链可变结构域和与SEQ ID NO:11具有90%或更高序列同一性的轻链可变结构域。
实施方案9.根据实施方案8所述的抗体,其中重链可变结构域与SEQ ID NO:10具有95%或更高的序列同一性,并且轻链可变结构域与SEQ IDNO:11具有95%或更高的序列同一性。
实施方案10.一种重组载体,包含编码SEQ ID NO:1至SEQ ID NO:11中任一项所示氨基酸序列的核酸。
实施方案11.一种用根据实施方案10所述的重组载体转化的细胞。
实施方案12.一种产生抗体的方法,包括在表达抗体的条件下培养实施方案11所述的转化的细胞。
实施方案13.一种药物组合物,其包含根据实施方案1-9中任一项所述的抗体和至少一种药学上可接受的赋形剂。
实施方案14.一种在有此需要的受试者中治疗慢性阻塞性肺病(COPD)的方法,该方法包括向受试者施用根据实施方案13所述的药物组合物。
实施方案15.一种在有此需要的受试者中治疗肺气肿的方法,该方法包括向受试者施用根据实施方案13所述的药物组合物。
实施方案16.一种在有此需要的受试者中治疗支气管肺发育异常的方法,该方法包括向受试者施用根据实施方案13所述的药物组合物。
实施方案17.一种在有此需要的受试者中治疗内皮单核细胞激活多肽II(EMAPII)介导的疾病的方法,该方法包括向受试者施用根据实施方案13所述的药物组合物。
其他实施方案
本文中对变量的任何定义中列举的要素列表包括将该变量定义为任何单个要素或所列要素的组合(或子组合)。本文中对实施方案的列举包括将该实施方案作为任何单个实施方案或者将该实施方案与任何其他实施方案或其部分进行组合。
本文引用的每项和各项专利、专利申请和出版物的公开内容在此均通过引用方式整体并入本文。虽然已经参照具体实施方案公开了本发明,但是显而易见的是,在不脱离本发明的真实精神和范围的情况下,本领域的其他技术人员可以设计出本发明的其他实施方案和变型。所附权利要求意在理解为包括所有此类实施方案和等同变型。
序列表
<110>Allinaire Therapeutics, LLC
Hay, Doughlas W.P.
Berezovsky, Suzanne E.
Knight, David
Huang, Kexin
Wang, Jordon K. K
<120>人源化抗EMAP II治疗性抗体
<130>206009-7004WO1(00093)
<150>US63045687
<151>2020-06-29
<160>12
<170>PatentIn version 3.5
<210>1
<211>471
<212>PRT
<213>人工序列
<220>
<223>人源化HC1
<400>1
Met Asp Pro Lys Gly Ser Leu Ser Trp Arg Ile Leu Leu Phe Leu Ser
1 5 1015
Leu Ala Phe Glu Leu Ser Tyr Gly Glu Val Gln Leu Val Glu Ser Gly
202530
Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Lys Leu Ser Cys Ala Ala
354045
Ser Gly Phe Thr Phe Ser Asp Ala Ala Met Tyr Trp Val Arg Gln Ala
505560
Ser Gly Lys Gly Leu Glu Trp Val Gly Arg Ile Arg Thr Lys Pro Asn
65707580
Asn Tyr Ala Thr Tyr Tyr Ala Ala Ser Val Lys Gly Arg Phe Thr Ile
859095
Ser Arg Asp Asp Ser Lys Asn Thr Ala Tyr Leu Gln Met Asn Ser Leu
100 105 110
Lys Thr Glu Asp Thr Ala Val Tyr Tyr Cys Thr Ser Trp Ser Tyr Asp
115 120 125
Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser
130 135 140
Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr
145 150 155 160
Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro
165 170 175
Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val
180 185 190
His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser
195 200 205
Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile
210 215 220
Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val
225 230 235 240
Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
245 250 255
Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro
260 265 270
Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val
275 280 285
Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val
290 295 300
Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln
305 310 315 320
Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln
325 330 335
Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala
340 345 350
Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro
355 360 365
Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr
370 375 380
Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser
385 390 395 400
Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr
405 410 415
Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr
420 425 430
Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe
435 440 445
Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys
450 455 460
Ser Leu Ser Leu Ser Pro Gly
465 470
<210>2
<211>471
<212>PRT
<213>人工序列
<220>
<223>人源化HC2
<400>2
Met Asp Pro Lys Gly Ser Leu Ser Trp Arg Ile Leu Leu Phe Leu Ser
1 5 1015
Leu Ala Phe Glu Leu Ser Tyr Gly Ala Val Gln Leu Val Glu Ser Gly
202530
Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Lys Leu Ser Cys Ala Ala
354045
Ser Gly Phe Thr Phe Ser Asp Ala Ala Met Tyr Trp Val Arg Gln Ala
505560
Ser Gly Lys Gly Leu Glu Trp Val Ala Arg Ile Arg Thr Lys Pro Asn
65707580
Asn Tyr Ala Thr Tyr Tyr Ala Ala Ser Val Lys Gly Arg Phe Thr Ile
859095
Ser Arg Asp Asp Ser Lys Asn Thr Val Tyr Leu Gln Met Asn Ser Leu
100 105 110
Lys Thr Glu Asp Thr Ala Val Tyr Tyr Cys Thr Ser Trp Ser Tyr Asp
115 120 125
Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser
130 135 140
Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr
145 150 155 160
Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro
165 170 175
Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val
180 185 190
His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser
195 200 205
Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile
210 215 220
Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val
225 230 235 240
Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
245 250 255
Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro
260 265 270
Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val
275 280 285
Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val
290 295 300
Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln
305 310 315 320
Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln
325 330 335
Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala
340 345 350
Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro
355 360 365
Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr
370 375 380
Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser
385 390 395 400
Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr
405 410 415
Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr
420 425 430
Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe
435 440 445
Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys
450 455 460
Ser Leu Ser Leu Ser Pro Gly
465 470
<210>3
<211>471
<212>PRT
<213>人工序列
<220>
<223>人源化HC3
<400>3
Met Asp Pro Lys Gly Ser Leu Ser Trp Arg Ile Leu Leu Phe Leu Ser
1 5 1015
Leu Ala Phe Glu Leu Ser Tyr Gly Ala Val His Leu Val Glu Ser Gly
202530
Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Lys Leu Ser Cys Ala Ala
354045
Ser Gly Phe Thr Phe Ser Asp Ala Ala Met Tyr Trp Val Arg Gln Ala
505560
Ser Gly Lys Gly Leu Glu Trp Val Ala Arg Ile Arg Thr Lys Pro Asn
65707580
Asn Tyr Ala Thr Tyr Tyr Ala Ala Ser Val Lys Gly Arg Phe Thr Ile
859095
Ser Arg Asp Asp Ser Lys Asn Thr Val Tyr Leu Gln Met Asn Ser Leu
100 105 110
Lys Thr Glu Asp Thr Ala Val Tyr Tyr Cys Thr Ser Trp Ser Tyr Asp
115 120 125
Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser
130 135 140
Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr
145 150 155 160
Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro
165 170 175
Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val
180 185 190
His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser
195 200 205
Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile
210 215 220
Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val
225 230 235 240
Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
245 250 255
Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro
260 265 270
Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val
275 280 285
Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val
290 295 300
Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln
305 310 315 320
Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln
325 330 335
Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala
340 345 350
Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro
355 360 365
Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr
370 375 380
Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser
385 390 395 400
Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr
405 410 415
Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr
420 425 430
Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe
435 440 445
Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys
450 455 460
Ser Leu Ser Leu Ser Pro Gly
465 470
<210>4
<211>471
<212>PRT
<213>人工序列
<220>
<223>人源化HC4
<400>4
Met Asp Pro Lys Gly Ser Leu Ser Trp Arg Ile Leu Leu Phe Leu Ser
1 5 1015
Leu Ala Phe Glu Leu Ser Tyr Gly Glu Val Gln Leu Val Glu Ser Gly
202530
Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Lys Leu Ser Cys Ala Ala
354045
Ser Gly Phe Thr Phe Ser Asp Ala Ala Ile Tyr Trp Val Arg Gln Ala
505560
Ser Gly Lys Gly Leu Glu Trp Val Ala Arg Ile Arg Thr Lys Pro Asn
65707580
Asn Tyr Ala Thr Tyr Tyr Ala Ala Ser Val Lys Gly Arg Phe Thr Ile
859095
Ser Arg Asp Asp Ser Asn Ser Thr Ala Tyr Leu Gln Met Asn Ser Leu
100 105 110
Lys Thr Glu Asp Thr Ala Val Tyr Tyr Cys Thr Ser Trp Ser Tyr Asp
115 120 125
Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser
130 135 140
Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr
145 150 155 160
Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro
165 170 175
Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val
180 185 190
His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser
195 200 205
Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile
210 215 220
Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val
225 230 235 240
Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
245 250 255
Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro
260 265 270
Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val
275 280 285
Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val
290 295 300
Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln
305 310 315 320
Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln
325 330 335
Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala
340 345 350
Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro
355 360 365
Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr
370 375 380
Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser
385 390 395 400
Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr
405 410 415
Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr
420 425 430
Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe
435 440 445
Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys
450 455 460
Ser Leu Ser Leu Ser Pro Gly
465 470
<210>5
<211>471
<212>PRT
<213>人工序列
<220>
<223>人源化HC5
<400>5
Met Asp Pro Lys Gly Ser Leu Ser Trp Arg Ile Leu Leu Phe Leu Ser
1 5 1015
Leu Ala Phe Glu Leu Ser Tyr Gly Ala Val Gln Leu Val Glu Ser Gly
202530
Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Lys Leu Ser Cys Ala Ala
354045
Ser Gly Phe Thr Phe Ser Asp Ala Ala Met Tyr Trp Val Arg Gln Ala
505560
Ser Gly Lys Gly Leu Glu Trp Val Ala Arg Ile Arg Thr Lys Pro Asn
65707580
Asn Tyr Ala Thr Tyr Tyr Ala Ala Ser Val Lys Gly Arg Phe Thr Ile
859095
Ser Arg Asp Asp Ser Asn Ser Thr Ala Tyr Leu Gln Met Asn Ser Leu
100 105 110
Lys Thr Glu Asp Thr Ala Val Tyr Tyr Cys Thr Ser Trp Ser Tyr Asp
115 120 125
Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser
130 135 140
Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr
145 150 155 160
Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro
165 170 175
Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val
180 185 190
His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser
195 200 205
Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile
210 215 220
Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val
225 230 235 240
Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
245 250 255
Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro
260 265 270
Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val
275 280 285
Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val
290 295 300
Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln
305 310 315 320
Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln
325 330 335
Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala
340 345 350
Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro
355 360 365
Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr
370 375 380
Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser
385 390 395 400
Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr
405 410 415
Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr
420 425 430
Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe
435 440 445
Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys
450 455 460
Ser Leu Ser Leu Ser Pro Gly
465 470
<210>6
<211>239
<212>PRT
<213>人工序列
<220>
<223>人源化LC1
<400>6
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 1015
Gly Ser Thr Gly Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro
202530
Val Thr Pro Gly Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Lys Ser
354045
Leu Leu His Ser Ser Gly Lys Thr Tyr Leu Asn Trp Tyr Leu Gln Lys
505560
Pro Gly Gln Ser Pro Gln Leu Leu Ile Tyr Trp Met Ser Asn Arg Ala
65707580
Ser Gly Val Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe
859095
Thr Leu Lys Ile Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr
100 105 110
Cys Gln Gln Phe Leu Glu Tyr Pro Leu Thr Phe Gly Gln Gly Thr Lys
115 120 125
Leu Glu Ile Lys Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro
130 135 140
Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu
145 150 155 160
Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp
165 170 175
Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp
180 185 190
Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys
195 200 205
Ala Asp Tyr Glu Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln
210 215 220
Gly Leu Ser Ser Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
225 230 235
<210>7
<211>239
<212>PRT
<213>人工序列
<220>
<223>人源化LC2
<400>7
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 1015
Gly Ser Thr Gly Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro
202530
Val Thr Pro Gly Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Lys Ser
354045
Leu Leu His Ser Ser Gly Lys Thr Tyr Leu Asn Trp Tyr Leu Gln Lys
505560
Pro Gly Gln Ser Pro Gln Leu Leu Ile Tyr Trp Met Ser Thr Arg Ala
65707580
Ser Gly Val Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe
859095
Thr Leu Lys Ile Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr
100 105 110
Cys Gln Gln Phe Leu Glu Tyr Pro Leu Thr Phe Gly Gln Gly Thr Lys
115 120 125
Leu Glu Ile Lys Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro
130 135 140
Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu
145 150 155 160
Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp
165 170 175
Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp
180 185 190
Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys
195 200 205
Ala Asp Tyr Glu Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln
210 215 220
Gly Leu Ser Ser Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
225 230 235
<210>8
<211>239
<212>PRT
<213>人工序列
<220>
<223>人源化LC3
<400>8
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 1015
Gly Ser Thr Gly Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro
202530
Val Thr Pro Gly Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Lys Ser
354045
Leu Leu His Ser Ser Gly Lys Thr Tyr Leu Asn Trp Tyr Leu Gln Lys
505560
Pro Gly Gln Ser Pro Gln Leu Leu Ile Tyr Trp Met Ser Thr Arg Ala
65707580
Ser Gly Val Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe
859095
Thr Leu Lys Ile Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr
100 105 110
Cys Gln Gln Phe Leu Glu Tyr Pro Leu Thr Phe Gly Gly Gly Thr Lys
115 120 125
Val Glu Ile Lys Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro
130 135 140
Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu
145 150 155 160
Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp
165 170 175
Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp
180 185 190
Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys
195 200 205
Ala Asp Tyr Glu Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln
210 215 220
Gly Leu Ser Ser Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
225 230 235
<210>9
<211>239
<212>PRT
<213>人工序列
<220>
<223>人源化LC4
<400>9
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 1015
Gly Ser Thr Gly Asp Ile Gln Met Thr Gln Ser Pro Leu Ser Leu Pro
202530
Val Thr Pro Gly Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Lys Ser
354045
Leu Leu His Ser Ser Gly Lys Thr Tyr Leu Asn Trp Tyr Leu Gln Lys
505560
Pro Gly Gln Ser Pro Gln Leu Leu Ile Tyr Trp Met Ser Thr Arg Ala
65707580
Ser Gly Val Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe
859095
Thr Leu Lys Ile Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr
100 105 110
Cys Gln Gln Phe Leu Glu Tyr Pro Leu Thr Phe Gly Gly Gly Thr Lys
115 120 125
Val Glu Ile Lys Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro
130 135 140
Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu
145 150 155 160
Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp
165 170 175
Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp
180 185 190
Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys
195 200 205
Ala Asp Tyr Glu Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln
210 215 220
Gly Leu Ser Ser Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
225 230 235
<210>10
<211>118
<212>PRT
<213>人工序列
<220>
<223>MHC1309HC.4
<400>10
Ala Val His Leu Val Glu Ser Gly Gly Gly Phe Val Gln Pro Thr Glu
1 5 1015
Ser Leu Lys Ile Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asp Ala
202530
Ala Met Tyr Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
354045
Ala Arg Ile Arg Thr Lys Pro Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp
505560
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Ser Met
65707580
Val Tyr Leu Gln Met Asp Asn Leu Lys Thr Glu Asp Thr Ala Met Tyr
859095
Tyr Cys Thr Ser Trp Ser Tyr Asp Phe Asp Tyr Trp Gly Gln Gly Val
100 105 110
Met Val Thr Val Ser Ser
115
<210>11
<211>112
<212>PRT
<213>人工序列
<220>
<223>MHC1309LC.1
<400>11
Asp Ile Val Met Thr Gln Gly Ala Leu Pro Asn Pro Val Pro Ser Gly
1 5 1015
Glu Ser Ala Ser Ile Thr Cys Gln Ser Ser Lys Ser Leu Leu His Ser
202530
Ser Gly Lys Thr Tyr Leu Asn Trp Tyr Leu Gln Arg Pro Gly Gln Ser
354045
Pro His Leu Leu Ile Tyr Trp Met Ser Thr Arg Ala Ser Gly Val Ser
505560
Asp Arg Leu Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65707580
Ser Ser Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gln Gln Phe
859095
Leu Glu Tyr Pro Leu Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210>12
<211>166
<212>PRT
<213>人
<400>12
Ser Lys Pro Ile Asp Val Ser Arg Leu Asp Leu Arg Ile Gly Cys Ile
1 5 1015
Ile Thr Ala Arg Lys His Pro Asp Ala Asp Ser Leu Tyr Val Glu Glu
202530
Val Asp Val Gly Glu Ile Ala Pro Arg Thr Val Val Ser Gly Leu Val
354045
Asn His Val Pro Leu Glu Gln Met Gln Asn Arg Met Val Ile Leu Leu
505560
Cys Asn Leu Lys Pro Ala Lys Met Arg Gly Val Leu Ser Gln Ala Met
65707580
Val Met Cys Ala Ser Ser Pro Glu Lys Ile Glu Ile Leu Ala Pro Pro
859095
Asn Gly Ser Val Pro Gly Asp Arg Ile Thr Phe Asp Ala Phe Pro Gly
100 105 110
Glu Pro Asp Lys Glu Leu Asn Pro Lys Lys Lys Ile Trp Glu Gln Ile
115 120 125
Gln Pro Asp Leu His Thr Asn Asp Glu Cys Val Ala Thr Tyr Lys Gly
130 135 140
Val Pro Phe Glu Val Lys Gly Lys Gly Val Cys Arg Ala Gln Thr Met
145 150 155 160
Ser Asn Ser Gly Ile Lys
165
- 抗人gp39的人源化抗体、包含所述人源化抗体的组合物及其治疗用途
- 高亲和力的、配体阻断性、人源化的抗T细胞免疫球蛋白结构域和粘蛋白结构域3(TIM-3)IgG4抗体用于治疗骨髓纤维化的用途
