肿瘤微酸-谷胱甘肽级联响应型超灵敏纳米探针及其制备方法与应用
文献发布时间:2024-04-18 19:52:40
技术领域
本发明属于分子影像技术领域,尤其涉及一种肿瘤微酸和谷胱甘肽(GSH)级联响应型超灵敏纳米探针及其制备方法和应用。
背景技术
分子影像技术运用影像学手段显示组织水平、细胞和亚细胞水平的特定分子,反映活体状态下分子水平变化,实现在体生理、病理的实时、无创、动态成像,可用于研究活体疾病或肿瘤的发生、发展及转移等过程。近红外荧光成像由于具有无创、无辐射、快速成像、高灵敏等优点,在肿瘤诊断领域展现出巨大的潜力。
分子影像技术的核心是分子影像探针。然而目前的近红外荧光探针多为一直发光型(always-ON),探针进入体内后会随着血液循环遍布全身,产生较强的背景信号,不仅成像信噪比低,而且容易产生假阳性信号。而响应型(OFF-ON)探针在正常组织和血液中不发光,只有在到达肿瘤部位时才被点亮,产生荧光信号,能显著地降低来自探针自身的背景信号,从而提高成像灵敏度和分辨率,减少假阳性信号的产生。因此,通过构建响应型近红外荧光成像探针,使其荧光信号能够被特定的肿瘤相关标志物激活,就可以实现目标组织的高灵敏、高特异性地可视化跟踪检测。然而大多数病理参数、生物靶标通常由多种类型的细胞共享,这些标志物不仅在病灶组织过表达,在正常细胞及血液中也有表达。目前的单靶标激活探针在复杂的生理病理环境下,可能会存在非特异性激活的问题,导致成像呈现假阳性信号。
由于以上这些原因,开发多靶标协同激活的成像探针可以有效避免非特异性激活产生的假阳性信号。构建满足肿瘤检测所需求的高特异成像探针,既是目前临床的迫切需求,也是生物医学领域的研究热点。
发明内容
为改善上述技术问题,本发明提供一种纳米探针,包括微酸响应基质和GSH激活近红外花菁染料;
根据本发明的实施方案,所述GSH激活近红外花菁染料为Cy7SS(Heptamethinecyanine dyes-disulfide,七甲川花菁染料-二硫化合物),所述Cy7SS具有通式Cy7SS-I或Cy7SS-II所示的结构:
其中:X为C(CH
根据本发明的实施方案,所述X优选为C(CH
根据本发明的实施方案,所述Cy7SS的结构如下所示:
根据本发明的实施方案,所述微酸响应基质为磷酸钙(简写为CaP);在一些实施方案中,所述磷酸钙为无定型形式;优选的,所述无定型为Ca
根据本发明的实施方案,所述磷酸钙可以通过如下反应得到:通过使用聚丙烯酸和钙盐在异丙醇中自组装后在磷酸盐的作用下矿化沉积形成;所述钙盐可以为氢氧化钙;所述磷酸盐可以为磷酸氢二铵。其中,聚丙烯酸的羧基能够与钙盐中的钙离子配位,进一步在磷酸盐的作用下矿化沉积形成所述磷酸钙。
根据本发明的实施方案,所述GSH激活近红外花菁染料包覆于所述微酸响应基质。
根据本发明的实施方案,所述微酸响应基质具有匹配肿瘤微酸环境的超灵敏响应范围,响应的pH的范围为7.2~6.5,例如响应的pH的范围为7.05~6.75;ΔpH可以小于0.3,例如为0.2;响应的pH示例性为7.0、6.9、6.8、6.5、6.25。
本发明还提供所述纳米探针(Cy7SS@CaP)的制备方法,包括如下步骤:
(1)GSH激活近红外花菁染料Cy7SS-I或Cy7SS-II的制备:化合物Cy7SS-Ia与R
(2)将步骤(1)得到的Cy7SS-I或Cy7SS-II通过组装包覆于微酸响应基质中合成Cy7SS@CaP纳米成像探针;
其中,X、Y、R
根据本发明的实施方案,步骤(1)中,R
根据本发明的实施方案,步骤(1)中,所述R
根据本发明的实施方案,步骤(1)中,所述反应可以在有机溶剂存在下进行,所述溶剂为N,N-二甲基甲酰胺(DMF)、二甲基亚砜(DMSO)、乙腈(MeCN)、二氯甲烷(DCM)、氯仿中的至少一种,优选为DMF;
根据本发明的实施方案,步骤(1)中,所述反应可以在催化剂作用下进行,所述催化剂可以为有机碱或无机碱,例如为三乙胺、二异丙基乙胺(DIPEA)、吡啶、哌啶、碳酸钠、碳酸钾、碳酸氢钠,优选三乙胺;
根据本发明的实施方案,步骤(1)中,所述反应的温度为25-45℃,示例性为40℃;所述反应的时间为12-36h,例如为24h。
根据本发明的实施方案,步骤(2)中,所述组装包覆的方法为:将聚丙烯酸钙、Cy7SS和磷酸氢二铵在溶剂中混合得到所述纳米探针;
根据本发明的实施方案,所述溶剂可以为水和有机溶剂的混合溶剂,所述有机溶剂可以为甲醇、乙醇、异丙醇中的至少一种;
根据本发明的实施方案,步骤(2)中,所述组装包覆的方法为:将20%聚丙烯酸溶于去离子水中,加入氢氧化钙,搅拌溶解,将Cy7SS溶于DMSO滴入上述反应液中,再加入异丙醇和磷酸氢二铵,搅拌8-24h,得到所述纳米探针。
根据本发明示例性的实施方案,步骤(2)中,所述组装包覆的方法为:将50-90μL20%聚丙烯酸(PAA,分子量为2000-5000)溶于10mL去离子水中,加入5-8mg氢氧化钙,搅拌溶解,将不同染料Cy7SS溶于100-500μL DMSO,滴入上述液体搅拌30min,向上述反应液缓慢加入10-50mL异丙醇,加入5-10mg磷酸氢二铵,搅拌8-24h,离心并水洗3次,分散于去离子水中,得到所述纳米探针。
本发明还提供所述纳米探针在肿瘤检测中的应用,例如用于活体肿瘤成像。根据本发明的实施方案,所述肿瘤选自乳腺癌。
本发明还提供所述纳米探针用于活体肿瘤成像的方法:尾静脉将探针注射进入小鼠,探针通过EPR(enhanced permeability and retention effect,高渗透长滞留效应)在肿瘤部位聚集。在正常组织和血液中,纳米粒子由于被双重锁定呈淬灭状态;肿瘤部位微酸代谢引起微酸响应基质材料(即CaP)解体,随后染料Cy7SS进入细胞被GSH激活,荧光信号经肿瘤微酸、GSH连续激活后级联放大,实现肿瘤高灵敏准确检测。
有益效果
通过以上技术方案,本发明供一种肿瘤微酸、GSH级联响应型超灵敏纳米探针及其制备方法和应用,与现有技术对比,其技术优势在于:
1.本发明结合肿瘤微酸激活型基质和GSH激活型染料,利用双重锁定淬灭荧光,赋予纳米探针更加优异的性能。所述纳米成像探针通过染料修饰淬灭近红外发光,再通过组装聚集形成CaP纳米粒子进一步淬灭,双重淬灭极大降低背景荧光,有助于肿瘤高信噪比成像。
2.本发明提供的纳米探针受微酸、GSH双标志物依序响应级联放大,有效改善现有荧光成像探针生物成像时特异性差、信噪比低的问题,提高肿瘤检测特异性,减少单靶向造影剂带来成像过程的假阳性。
3.本发明提供的纳米探针具有微酸、GSH级联放大效应,检测灵敏度提高,合成简单、光学性能优良、生物相容性好,可用于肿瘤在体超灵敏检测。
4.本发明提供的纳米探针具有匹配肿瘤微酸环境的超灵敏响应范围,响应的pH的范围为7.2~6.5,极大的扩展了肿瘤检测探针的响应范围;且可以灵敏的响应微弱的pH变化,ΔpH的变化范围至少为0.2。
附图说明
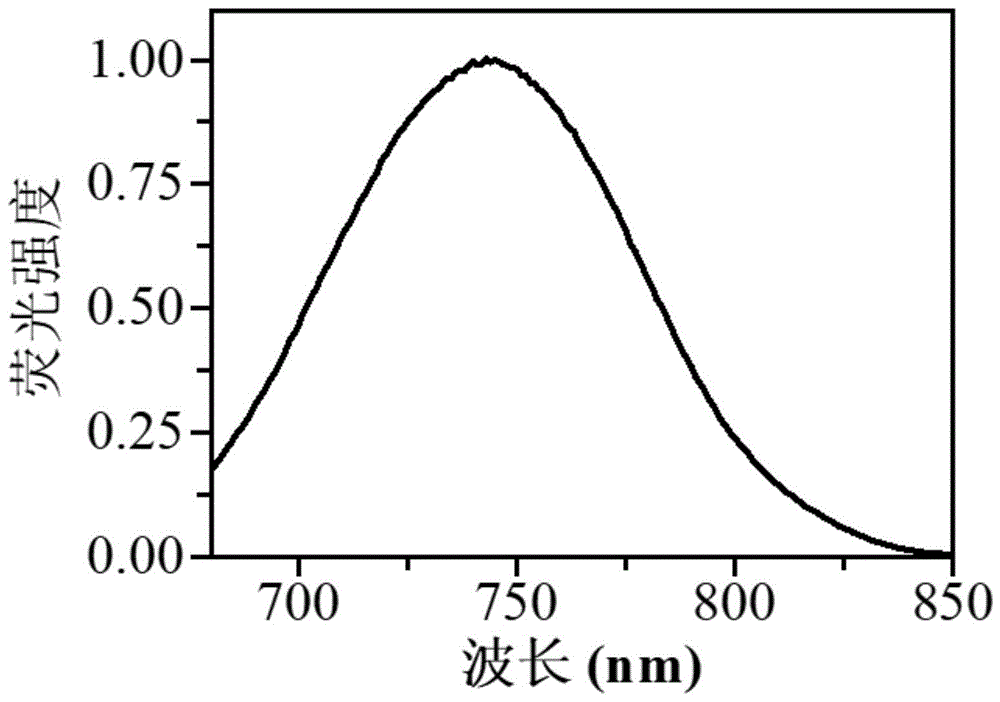
图1为实施案例1所述Cy7SS荧光光谱
图2为实施案例2所述Cy7SS响应性荧光光谱
图3为实施案例3所述Cy7SS@CaP TEM图
图4为实施案例4所述Cy7SS@CaP酸响应性曲线
图5为实施案例4所述Cy7SS@CaP级联响应性光谱
图6为实施案例5所述纳米成像探针细胞毒性
图7为实施案例6所述纳米成像探针用于乳腺癌检测
术语定义与说明
除非另有说明,本申请说明书和权利要求书中记载的基团和术语定义,包括其作为实例的定义、优选地定义、实施例中具体化合物的定义等,可以彼此之间任意组合和结合。这样的组合和结合后的基团定义及化合物结构,应当属于本申请记载的范围。
除非另有说明,本申请中基团的下标一般指该基团的个数。
本申请说明书和权利要求书记载的数值范围,当该数值范围被定义为“整数”时,应当理解为记载了该范围的两个端点以及该范围内的每一个整数。例如,“0~6的整数”应当理解为记载了0、1、2、3、4、5和6的每一个整数。当该数值范围被定义为“数”时,应当理解为记载了该范围的两个端点、该范围内的每一个整数以及该范围内的每一个小数。
术语“卤素”指F、Cl、Br和I。换言之,F、Cl、Br和I在本说明书中可描述为“卤素”。
本发明单独使用或用作后缀或前缀的“C
具体实施方式
下文将结合具体实施例对本发明的技术方案做更进一步的详细说明。应当理解,下列实施例仅为示例性地说明和解释本发明,而不应被解释为对本发明保护范围的限制。凡基于本发明上述内容所实现的技术均涵盖在本发明旨在保护的范围内。
除非另有说明,以下实施例中使用的原料和试剂均为市售商品,或者可以通过已知方法制备。
为解决现有技术存在的信噪比低、特异性差的问题,本发明采取的具体技术方案是:利用肿瘤弱酸性微环境及肿瘤细胞内高表达的GSH为双靶点,通过将GSH可激活的近红外花菁染料包覆于微酸响应的基质材料中进一步淬灭,设计合成微酸、GSH级联响应型荧光成像探针。本发明所述纳米成像探针通过微酸与GSH双靶向提高检测特异性,通过连续激活级联响应将成像信号放大,提高检测灵敏度,从而满足肿瘤检测需求。
实施案例1
级联响应型近红外纳米成像探针中荧光染料部分采用七甲川花菁染料进行修饰改造,通式为Cy7SS-I和Cy7SS-II,以如下反应方程式为例,介绍制备过程。
步骤一:Cy7和胱胺二盐酸盐制备Cy7SS的反应:称取200.0mg Cy7、337.68mg胱胺二盐酸盐、207.315mg碳酸钾,溶于5mL DMF,在氩气保护下40℃反应24h,溶液变为深蓝色。
步骤二:Cy7SS-1的分离纯化:将步骤一所得的产物用乙醚析出,调整展开剂比例,采用柱层析分离法将其分离,收集蓝色段,用旋转蒸发仪旋干即得化合物Cy7SS-1。
Cy7SS-1的荧光光谱测试:
取1mg Cy7SS-1溶于1mL DMSO中配制成母液,浓度为1.25×10
实施案例2
为考察Cy7SS-I和Cy7SS-II的GSH响应性能,以Cy7SS-1为例测试吸收光谱、发射光谱与GSH浓度的关系。
步骤一:配置母液:取1mg Cy7SS-1溶于1mL DMSO中配制染料母液,浓度为1.25×10
步骤二:配置工作溶液:取21个2mL离心管,分别编号1-7,3组平行样品,分别加入1.7mL、1.8mL、1.86mL、1.7mL、1.8mL、1.86mL、1.9mL溶剂DMSO,200μL、100μL、40μL的10mMGSH母液,200μL、100μL、40μL、0μL的1mM GSH母液,分别加入100μL Cy7SS-1母液,使得工作溶液染料浓度为6.25×10
测定结果如图2所示,随着GSH浓度从0μM增加到1mM,820nm处荧光从无到有逐渐增强,具有非常好的响应性能。实验结果表明Cy7SS-1对GSH响应敏感,且与浓度变化相关,检测限至少达20μM,可以很好的匹配肿瘤区域GSH浓度,能够用于肿瘤高灵敏度检测。
实施案例3:
为了实现本发明双重淬灭的效果,将得到的Cy7SS-1通过自组装包覆于微酸响应基质中,实现荧光信号的进一步淬灭。GSH激活型染料以Cy7SS-1为例,微酸响应基质以CaP为例,介绍级联响应纳米成像探针制备过程。
用移液枪准确量取50μL 20%PAA(Mw=2000),在超声条件下将其溶解于10mL去离子水,并加入7.5mg氢氧化钙超声溶解后置于磁力搅拌器,氩气保护下加入1mg Cy7SS-1,室温搅拌30min。缓慢滴入50mL异丙醇,形成乳白色溶液,30min滴加完毕。准确称取9.6mg磷酸氢二铵加入上述反应液,室温搅拌24h。反应结束,离心收集产物,用50mL去离子水洗涤3次,收集离心产物分散于5mL去离子水中,即为级联响应型纳米成像探针Cy7SS@CaP。
参照上述步骤,将Cy7SS-1替换为Cy7,可制备得到微酸响应对照探针Cy7S@CaP。
为考察纳米成像探针的大小和形貌,分别通过透射电子显微镜(TransmissionElectron Microscope,简称TEM)对Cy7SS@CaP纳米探针进行表征,结果如图3所示,纳米探针大小均一分散性好,直径约为100nm。
实施案例4:
为考察级联响应纳米探针的响应敏感性,以Cy7SS@CaP为例测试其在不同pH中的荧光发射光谱以及在微酸、GSH依序激活下的光谱变化。
步骤一:配置母液:将制得Cy7SS@CaP分散在1mL去离子水中,浓度为50mg/mL。
步骤二:配置工作溶液,测试微酸响应性:取27个2mL离心管,分别编号1-9,3组平行样品,分别加入1.8mL pH为7.4、7.25、7.05、6.9、6.8、6.5、6.25、6.05、5.85的柠檬酸钠缓冲溶液,各加入200μL Cy7SS@CaP母液,测定其荧光发射光谱(通道1),结果如图4所示,荧光信号可以灵敏的响应微弱的pH变化,ΔpH为0.2。
步骤三:配置工作溶液,测试级联响应性:取9个2mL离心管,分别编号1-3,分为3组平行组,分别将200μL Cy7SS@CaP母液稀释于2.0mL pH为7.4的柠檬酸钠缓冲溶液、2.0mLpH为6.8的柠檬酸钠缓冲溶液和1.8mL pH为6.8的柠檬酸钠缓冲溶液,然后分别继续加入200μL浓度为10mM GSH母液,震荡;分别测试测试荧光光谱,结果如图5所示,820nm处荧光信号经历pH、GSH双标志物连续激活,信号级联放大。
实施案例5:
良好的生物相容性是纳米成像探针活体成像检测的基础,为此以Cy7SS@CaP为例,验证其对乳腺癌细胞系的细胞毒性。
采用4T1细胞系,含10%胎牛血清、100U/mL青霉素、0.1mg/mL链霉素的DMEM培养37℃、5%二氧化碳的培养箱培养细胞。将4T1细胞培养培养至对数生长期,以1×10
实施案例6:
为了考察级联响应纳米成像探针在活体水平对肿瘤的检测性能,以Cy7SS@CaP为例,选取响应的单响应探针及always on对照探针对乳腺癌小鼠模型成像。
选取生理状态与肿瘤体积大小接近的荷瘤小鼠若干只,平均分为4组,尾静脉注射纳米成像探针,分别为级联响应探针Cy7SS@CaP、微酸响应对照探针Cy7S@CaP、GSH响应对照探针SiO
以上,对本发明的实施方式进行了说明。但是,本发明不限定于上述实施方式。凡在本发明的精神和原则之内,所做的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
- 一种pH响应型自辅因子DNAzyme ZnO纳米探针及其制备方法与应用
- 肿瘤基质微酸环境响应的两亲性高分子前药胶束及其制备方法和应用
- 一种温度响应型发光金纳米胶束及其制备方法与在可视化温度检测中的应用
- 一种pH响应型超灵敏纳米荧光探针及制备方法
- 一种高灵敏度硫化氢响应型纳米探针及其制备方法和应用
