一种基于寡糖链检测胰腺癌的检测试剂、制备方法及应用
文献发布时间:2024-04-18 19:52:40
技术领域
本发明属于生物医药技术领域,涉及一种胰腺癌的检测方法,具体涉及一种基于血清寡糖链G-Test特异指纹图谱的胰腺癌检测方法。
背景技术
胰腺癌是一种恶性程度很高,诊断和治疗都很困难的消化道恶性肿瘤,约90%为起源于腺管上皮的导管腺癌。胰腺癌早期的确诊率不高,手术死亡率较高,而治愈率很低,也是预后最差的恶性肿瘤之一,5年生存率低于5%。胰腺癌起病隐匿,早期症状不典型,常表现为上腹部不适、腰背部痛、消化不良或腹泻等,易与其他消化系统疾病相混淆,出现症状时大多已属中晚期。胰腺癌的病理分型是以组织形态结构和细胞生物学特性为基础,不同类型的胰腺癌,其形态结构和生物学行为各异,流行病学和分子机制亦不同,因此现有的胰腺癌病理分型系统众多。在所有类型的胰腺癌中,胰腺导管腺癌(PDAC)是最为常见的,占85%-90%,而患者总体的5年生存率低于5%,这一数字在近50年来都没有改善。其它各类胰腺肿瘤约占胰腺肿瘤的10%-15%。由于胰腺癌早期转移、生长迅速且位置较深,症状及体征均缺乏典型性,临床上容易漏诊或误诊。
胰腺癌的临床诊断主要有影像学检测和肿瘤标志物检测。影像学检查包括CT、MRI等作为辅助检查进行胰腺癌的诊断,其特异性有待进一步提高。目前出现的胰腺癌诊断试剂盒都是检测一些常见的肿瘤标记物,如C19-9、癌胚抗原CEA等,灵敏性及准确性都偏低。单项检测往往有很大的局限性,难以满足快速诊断的要求。上述诊断方法都有自身的局限性,目前急需探索出用于辅助诊断胰腺癌并同时具有较高灵敏度和特异度的新型无创性方法。
糖蛋白是通过蛋白质的翻译后修饰即糖基化后形成的一类结合蛋白。蛋白质的糖基化(Glycosylation)是一种最常见的蛋白翻译后修饰,是在糖基转移酶作用下将糖类转移至蛋白质和蛋白质上特殊的氨基酸残基形成糖苷键的过程。大多数的糖蛋白都是分泌蛋白,广泛存在于细胞膜、细胞间质、血浆以及粘液中。蛋白质上N-糖链通过加工修饰来调控蛋白质的结构,稳定性和活性,所以糖蛋白中糖链对于维持机体生物学功能起重要作用,从而赋予糖蛋白具有多种生物功能。因此了解糖链的改变有助于阐明炎症、肿瘤细胞对周围组织侵袭及转移等异常生物行为学的分子机理。
目前己经在多种肿瘤中发现了蛋白质N-糖链的异常改变,而N-糖链的末端唾液酸修饰改变是其中之一。唾液酸是一类带负电荷的9碳糖化合物,广泛存在于生物体内,常位于聚糖链末端;其在唾液酸酶的作用下通过α-2,3或α-2,6糖苷键与糖链上的半乳糖或N-乙酰半乳糖胺连接形成聚唾液酸链。研究发现聚糖链末端的唾液酸在调控细胞的相互识别、分子相互作用、病毒感染、免疫响应以及信号传导起到重要的功能,且细胞表面糖蛋白质唾液酸修饰具有组织和细胞特异性。众多研究表明唾液酸修饰异常参与了疾病的发生发展,且与多种疾病如感染性疾病以及肿瘤的浸润和转移有着密切关系。因此检测唾液酸相关的寡糖基的改变对于疾病的诊断和作为靶点开发治疗的药物具有潜在的临床价值。
发明内容
针对目前临床上使用的胰腺癌检测中存在的问题,如血液检查和影像学检测特异性和准确度不高,病理检查有创伤性,患者依存性差等,本发明提供一种胰腺癌检测试剂,通过该试剂测定血清中的天然寡糖N-糖组图谱,再将峰值量化并进行统计学分析,从而提供一种胰腺癌的血清天然寡糖N-糖组图谱模型的建立方法,通过测定生理病理状态下蛋白质的天然糖基化修饰的改变来检测胰腺癌。
本发明采用的技术方案如下:
一种基于寡糖链检测胰腺癌的检测试剂,由以下试剂组成:
试剂A:浓度为10mM、pH为8.3的碳酸氢铵溶液中加入质量浓度1~5%的SDS配制而成;
试剂B:由0.05~10单位/10μl糖胺酰酶、质量浓度10%的NP-40和浓度为10mM、pH为8.3的碳酸氢铵溶液混合配制而成,混合溶液pH值为5~9;
试剂C:由8-氨基芘-1,3,6-三磺酸溶于DMSO中配制成浓度为0.02mM~1M有机物还原剂;
试剂D:终止液。
优选的,所述试剂A、试剂B与试剂C的体积比是1:1:1。
优选的,所述试剂A、试剂B与试剂C的体积都为5μl。
优选的,所述试剂D为超纯水。
一种基于寡糖链检测胰腺癌检测试剂的制备方法,包括以下步骤:
步骤一寡糖链的制备
在经过灭活处理的5μl血清样品中加入5μl试剂A,进行变性,冷却至室温后,加入5μl试剂B,37℃反应3h,然后进行干燥;
步骤二寡糖链的标记
在步骤一干燥后得到的样品中加入5μl试剂C,60℃反应1h后进行荧光标记,然后加入100μl试剂D终止标记反应;
步骤三寡糖链分离分析
取10μl寡糖链标记后的液体,用分析仪进行N-寡糖链分离检测,得到天然寡糖N-糖组图谱;
步骤四数据处理分析
N-糖组图谱的峰值量化:将每个峰的峰高值除以所有峰的高度的总和,计算得到每个峰的相对含量。
一种组合物在制备寡糖链胰腺癌检测试剂中的应用,所述组合物由血清中的G4S4、G3S3、G2S2、G2S2F、G2S1、G2S1F、G1F和G2F2组成,所述组合物通过G2S2/G3S3+G2S2/G2S2F的值来检测胰腺癌。
所述G1F为同分异构体。
本发明提供一种胰腺癌的血清天然寡糖N-糖组图谱模型的建立方法,通过测定血清天然寡糖链G-Test特异指纹图谱,进行统计学分析。
材料和方法:
一、检测样本:胰腺癌患者和健康人的血清。
二、实验设备:毛细管电泳分析仪,PCR,离心机。
三、试剂制备:
1、试剂A:浓度为10mM、pH为8.3的碳酸氢铵溶液中加入质量浓度1~5%的SDS配制而成;
2、试剂B:由0.05~10单位/10μl糖胺酰酶、质量浓度10%的NP-40和浓度为10mM、pH为8.3的碳酸氢铵溶液混合配制而成,混合溶液pH值为5~9;
3、试剂C:由8-氨基芘-1,3,6-三磺酸溶于DMSO中配制成浓度为0.02mM~1M有机物还原剂;
4、试剂D:终止液。
四、N-糖组图谱检测
1、寡糖链的制备
在经过灭活处理的5μl血清样品中加入5μl试剂A,进行变性;待冷却至室温后,加入5μl试剂B,37℃反应3h,然后进行干燥。
2、寡糖链的标记
(1)干燥后的样品中加入5μl试剂C,60℃反应1h,进行荧光标记;
(2)荧光标记完成后,加入100μl试剂D终止标记反应。
3、寡糖链分离分析
取10μl寡糖链标记后的液体,在ABI3500dx仪器下进行N-寡糖链分离检测,从而得到天然寡糖N-糖组图谱。
4、数据处理分析
(1)N-糖组图谱的峰值量化:将每个峰的峰高值除以所有峰的高度的总和,计算得到每个峰的相对含量。
(2)胰腺癌患者与健康人群N-糖组数据分析:将胰腺癌患者与健康人N-糖组数据进行对比分析。将每个峰峰高值除以所有峰高度的总和,定量计算得到每个峰的相对含量,即N-糖组图谱的峰值量化,然后对量化后的胰腺癌组和健康对照组N-糖组图谱中9个N-寡糖链峰进行比对统计分析。N-糖组图谱的组合物由G4S4、G3S3、G2S2、G2S2F、G2S1、G2S1F、G1F和G2F2组成,其中G1F为同分异构体;通过组合物G2S2/G3S3+G2S2/G2S2F值来检测胰腺癌。
与现有技术相比,本发明的有益效果:
(1)将G-Test指纹图谱的各个峰值进行量化,然后将胰腺癌患者(152例)和健康人(143例)各峰相对含量结果进行对比分析,发现N-聚糖组合物G2S2、G3S3以及G2S2F在两组间存在显著的统计学差异(p<0.05);因此,基于组合物G2S2/G3S3+G2S2/G2S2F建立的模型在区分胰腺癌患者时ROC曲线下AUC值达到0.875(图2),该G2S2/G3S3+G2S2/G2S2F模型检测的cutoff值为4.57时,对胰腺癌的检测有82.30%的灵敏度和81.20%的特异性,表明血清中的N-聚糖组合物G2S2/G3S3+G2S2/G2S2F可以作为辅助诊断胰腺癌的标志物。
(2)本发明提出的G-Test检测法是基于DNA测序仪的毛细管微电泳技术(DSA-FACE),将血清样本中糖蛋白N-糖链进行荧光标记后,用毛细管微电泳进行分离,通过测量荧光信号得到的糖蛋白的含量即天然寡糖N-糖组图谱。本发明通过检测生理病理状态下唾液酸寡糖链的变化与疾病状态的相关性,可以根据这些变化,建立N-聚糖组合物的预测模型来辅助诊断胰腺癌状态。
(3)基于本发明方法构建的G-Test天然N-糖组图谱模型,能够让众多患者接受常规、无创检测,帮助医生及患者及时监测胰腺癌的发生和疾病进展,本发明的检测技术具有灵敏度高、操作简单、微量(5μl血清)、重复性高、稳定性好、高通量(96-孔板)等优点,可在临床中推广使用。
附图说明
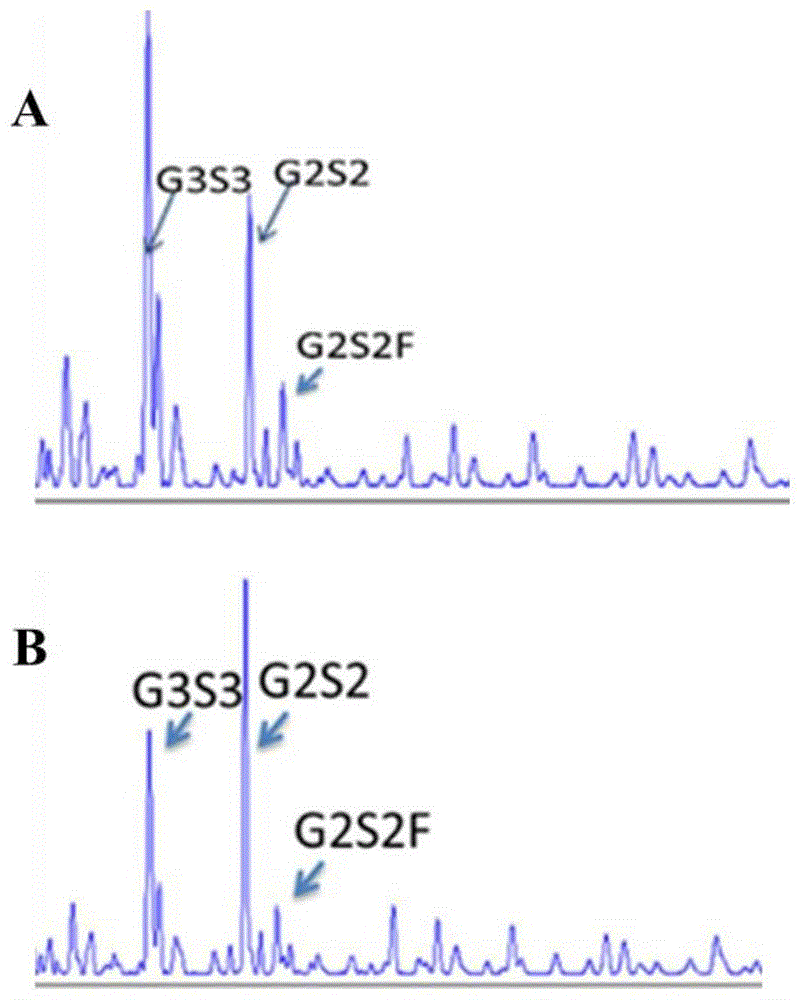
图1是胰腺癌患者和健康人的血清天然寡糖N-糖组图谱;
图2是基于N-糖组合物G2S2/G3S3+G2S2/G2S2F建立的鉴别胰腺癌状态模型ROC曲线图;检测样本总数为295例,其中胰腺癌患者血清样本152例,健康人血清样本143例,得到ROC曲线下面积AUC=0.875。
具体实施方式
下面结合实施例和附图对本发明作进一步详述。需要说明的是,下列实施例仅用于说明本发明而不用于限制本发明的范围。下列实施例中未注明具体条件的实验方法,通常按照常规条件试验,或按照制造厂商建议的条件。
检测胰腺癌状态,通过测定血清天然寡糖N-糖组图谱,进行统计学分析,采用的材料和方法如下列实施例。
实施例一
1.检测样本:胰腺癌患者和健康人的血清。
2.实验设备:毛细管电泳分析仪,PCR,离心机。
3.试剂制备:
1)试剂A:浓度为10mM的碳酸氢铵溶液中加入质量浓度2.5%的SDS配制而成;
2)试剂B:由3单位/10μl糖胺酰酶、质量浓度10%的NP-40和浓度为10mM、pH为8.3的碳酸氢铵溶液混合配制而成,溶液pH值为7;
3)试剂C:由8-氨基芘-1,3,6-三磺酸溶于DMSO中配制而成浓度为10mM有机物还原剂;
4)试剂D:超纯水。
4.N-糖组图谱检测:
(1)寡糖链的制备
在经过灭活处理的5μl血清样品中加入5μl试剂A,进行变性;待冷却至室温后,加入5μl试剂B,37℃反应3h,然后进行干燥。
(2)寡糖链的标记
1)干燥后的样品中加入5μl试剂C,60℃反应1h,进行荧光标记;
2)荧光标记完成后,加入100μl试剂D终止标记反应。
(3)寡糖链分离分析
取10μl寡糖链标记后的液体,在ABI3500dx仪器下进行N-寡糖链分离检测,从而得到天然寡糖N-糖组图谱。
(4)数据处理分析
1)N-糖组图谱的峰值量化:将每个峰的峰高值除以所有峰的高度的总和,计算得到每个峰的相对含量。
2)胰腺癌患者与健康人群N-糖组数据分析:将胰腺癌患者与健康人N-糖组数据进行对比分析。如图1所示,人血清的N-糖组图谱显示出近9个N-寡糖链峰,不同寡糖链因所带电荷以及分子大小的不同而表现出不同的迁移率,即表现在N-糖组图谱上的不同的峰则代表了不同的寡糖链,其峰高代表了寡糖链的相对含量。图1中A为健康人血清N-聚糖图谱,B为胰腺癌患者血清N-聚糖图谱。N-糖组图谱的组合物由G4S4、G3S3、G2S2、G2S2F、G2S1、G2S1F、G1F和G2F2组成,其中G1F为同分异构体;通过计算组合物G2S2/G3S3+G2S2/G2S2F值来辅助判断胰腺癌状态。
基于组合物G2S2/G3S3+G2S2/G2S2F建立的模型在区分胰腺癌患者时ROC曲线下AUC值达到0.875(图2),该G2S2/G3S3+G2S2/G2S2F模型检测的cutoff值为4.57时,对胰腺癌的检测有82.30%的灵敏度和81.20%的特异性,表明血清中的N-聚糖组合物G2S2/G3S3+G2S2/G2S2F能作为辅助诊断胰腺癌的标志物。
实施例二
1)试剂A:浓度为10mM的碳酸氢铵溶液中加入质量浓度1%的SDS配制而成;
2)试剂B:由0.05单位/10μl糖胺酰酶、质量浓度10%的NP-40和浓度为10mM、pH为8.3的碳酸氢铵溶液混合配制而成,溶液pH值为5;
3)试剂C:由8-氨基芘-1,3,6-三磺酸溶于DMSO中配制而成浓度为0.02mM有机物还原剂;
4)试剂D:超纯水。
4.N-糖组图谱检测同实施例一。
实施例三
1)试剂A:浓度为10mM的碳酸氢铵溶液中加入质量浓度5%的SDS配制而成;
2)试剂B:由10单位/10μl糖胺酰酶、质量浓度10%的NP-40和浓度为10mM、pH为8.3的碳酸氢铵溶液混合配制而成,溶液pH值为9;
3)试剂C:由8-氨基芘-1,3,6-三磺酸溶于DMSO中配制而成浓度为1M有机物还原剂;
4)试剂D:超纯水。
4.N-糖组图谱检测同实施例一。
本检测技术与现有技术相比,通过检测生理病理状态下唾液酸寡糖链的变化与疾病状态的相关性,可以根据这些变化,建立N-聚糖组合物的预测模型来辅助判断胰腺癌状态。基于本发明方法构建的G-Test天然N-糖组图谱模型,能够让众多患者接受常规、无创检测,帮助医生及患者及时监测胰腺癌的发生和疾病进展,可在临床中推广使用。
以上结合附图所述的具体实施例,对本发明的目的、技术方案和有益效果进行了进一步详细说明,所应理解的是,以上所述仅为本发明的具体实施例而已,但并非对本发明保护范围的限制,所属领域技术人员应该明白,凡在本发明的精神和原则之内,不需要付出创造性劳动即可做出的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
- 一种NSE检测试纸条的制备方法、试纸条、检测卡及NSE检测试剂盒
- 一种能快速定性检测猪瘟病毒的检测试剂的制备方法
- 一种快速检测尿液对羟基苯丙氨酸的检测试剂及其制备方法
- 一种莲藕潜隐病毒双抗体夹心酶联免疫检测试剂盒及制备与检测方法
- 一种用于检测羧酸酯酶的荧光探针及其制备方法与专用检测试剂盒
- 一种基于寡糖链检测胃癌的检测试剂、制备方法及应用
- 一种基于寡糖链检测慢性乙型肝炎患者肝纤维化的检测试剂、制备方法及应用
