一种乙酰-L-高丝氨酸内酯的制备方法
文献发布时间:2024-04-18 19:58:30
技术领域
本发明属于精细化学品制备技术领域,更具体地,涉及一种精草铵膦合成关键中间体的制备方法,该制备方法是以L-高丝氨酸内酯衍生物和乙酰氯为原料制备乙酰-L-高丝氨酸内酯。
背景技术
草铵膦除草剂目前是全球第二大灭生性除草剂,市售草铵膦是外消旋混合物,有两种对映异构体,其两种对映异构体的化学结构式如下所示;虽然草铵膦具有两种对用异构体,但是在除草中起作用的仅仅只有L-构型的草铵膦,而D-对映异构体则无除草活性除草剂,使用精草铵膦与草铵膦相比的优势是,其除草活性增加2倍,生物亲和性更优异,植物吸收利用更快速,其有效成分用量可降低50%,从而可减少进入环境的无效体,降低对环境的危害和操作人员的接触剂量,同时在达到相同防效的情况下,可大大节省使用成本,对提高经济性和减轻环境压力都是极为有利的。
L-草铵膦和D-草铵膦的化学结构式
近年来,国内企业和科研院所通过技术攻关,以生物催化法制备的L-高丝氨酸为原料合成精草铵膦工艺突飞猛进,目前利尔化学和山东绿霸等公司环评公示已具备万吨级产能。传统的L-高丝氨酸路线合成精草铵膦均需要对L-高丝氨酸内酯衍生物的氨基进行保护,氨基保护基通常为MocCl或EocCl(Chinese Journal of Pesticides,2006,45,1;Tehahedron.Letters.1992,33,2669;J.Wuhan Univ.2010,56,11;Chinese ChemicalLetters,2006,17,177)。然而,MocCl和EocCl为剧毒管制品,其运输保存和工业化大生产均存在较大安全隐患。因此,当前工业界亟需寻找一种操作步骤简单兼具高反应收率的L-高丝氨酸内酯衍生物的氨基保护方法。
发明内容
针对现有技术的以上缺陷或改进需求,本发明的目的在于提供一种乙酰-L-高丝氨酸内酯的制备方法,其中通过对关键制备工艺的整体流程以及各个反应步骤的参数条件(包括碱催化剂的种类与物料配比,反应温度与时间等)进行改进,与传统L-高丝氨酸内酯衍生物的氨基保护方法相比,乙酰氯作为氨基保护基,具有反应选择性高、成本低廉、操作简单、工业应用价值高等优点。
为实现上述目的,按照本发明,提供了一种乙酰-L-高丝氨酸内酯的制备方法,包括以下步骤:
将L-高丝氨酸内酯衍生物和碱催化剂在溶剂中进行反应后,滴加乙酰氯后继续反应,监测反应完全后,中和、萃取、干燥、浓缩、重结晶得到乙酰-L-高丝氨酸内酯。
作为本发明的进一步优选,所述步骤中,所述L-高丝氨酸内酯衍生物为L-高丝氨酸内酯盐酸盐、L-高丝氨酸内酯氢溴酸盐和L-高丝氨酸内酯硫酸盐中的任意一种。
作为本发明的进一步优选,所述步骤中,所述碱催化剂为三乙胺、二乙胺、N,N-二异丙基乙胺、甲醇钠、乙醇钠、氧化钙、氢氧化钠、氢氧化钾碳酸钠和碳酸氢钠中的任意一种。
作为本发明的进一步优选,所述步骤中,所述溶剂为二氯甲烷、1,2-二氯乙烷、丙酮、四氢呋喃、1,4-二氧六环和水中的任意一种或两种混合溶剂。
酸内酯衍生物和碱催化剂进行反应的温度为0-10℃,反应时间10min-60min。
作为本发明的进一步优选,所述步骤中,所述L-高丝氨酸内酯衍生物和乙酰氯的摩尔比为1:3~3:1。
滴加乙酰氯后在20-100℃下反应1-10h。
作为本发明的进一步优选,所述步骤中,所述乙酰-L-高丝氨酸内酯的制备方法,其特征在于,所述步骤中,L-高丝氨酸内酯衍生物和所述碱的摩尔比为1:1~1:5。
通过本发明所构思的以上技术方案,与传统的L-高丝氨酸内酯衍生物氨基保护合成路线相比,提供了精草铵膦中间体合成新方法。该方法不涉及剧毒品MocCl和EocCl,反应选择性更好,乙酰氯是廉价的市售大宗化学品,目前市场价格为7000-8000元/吨。因此,本发明中的制备方法使用的原料廉价易得,工业化前景巨大,通过对反应条件进行优化(尤其是针对反应物的配比、碱催化剂种类、反应温度及时间等),使得反应选择性好,乙酰-L-高丝氨酸内酯产率高。
本发明是从L-高丝氨酸内酯衍生物和乙酰氯为原料制备得到乙酰-L-高丝氨酸内酯,与现有的技术相比具有合成效率高、成本较低、操作简单不需要使用剧毒管制化学品的特点,涉及的主要反应如下:
该合成反应能保证较高的产率,所需氨基保护试剂廉价易得,合成步骤操作简单。综上所述,本发明与传统L-高丝氨酸内酯衍生物的氨基保护方法相比,具有反应选择性高、成本较低、操作简单、工业应用价值大且避免了剧毒化学品的使用等优点。
为了使本发明的目的、技术方案及优点更加清楚明白,以下结合实施例,对本发明进行进一步详细说明。应当理解,此处所描述的具体实施例仅仅用以解释本发明,并不用于限定本发明。此外,下面所描述的本发明各个实施方式中所涉及到的技术特征只要彼此之间未构成冲突就可以相互组合。
本发明中乙酰-L-高丝氨酸内酯的制备方法主要是通过以下步骤实现的:
步骤:在配有机械搅拌的反应器中投入L-高丝氨酸内酯衍生物、乙酰氯、溶剂以及碱催化剂,上述物料混合后于0-80℃下搅拌反应1-10小时;反应结束后以酸中和碱性反应体系到中性;用乙酸乙酯或二氯甲烷液-液萃取得有机相;有机相合并干燥后减压浓缩;异丙醇/乙醇/甲醇和石油醚/乙醚重结晶分离得到乙酰-L-高丝氨酸内酯,为白色固体。
下面以不同的反应条件对上述方案进行详细说明。
附图说明
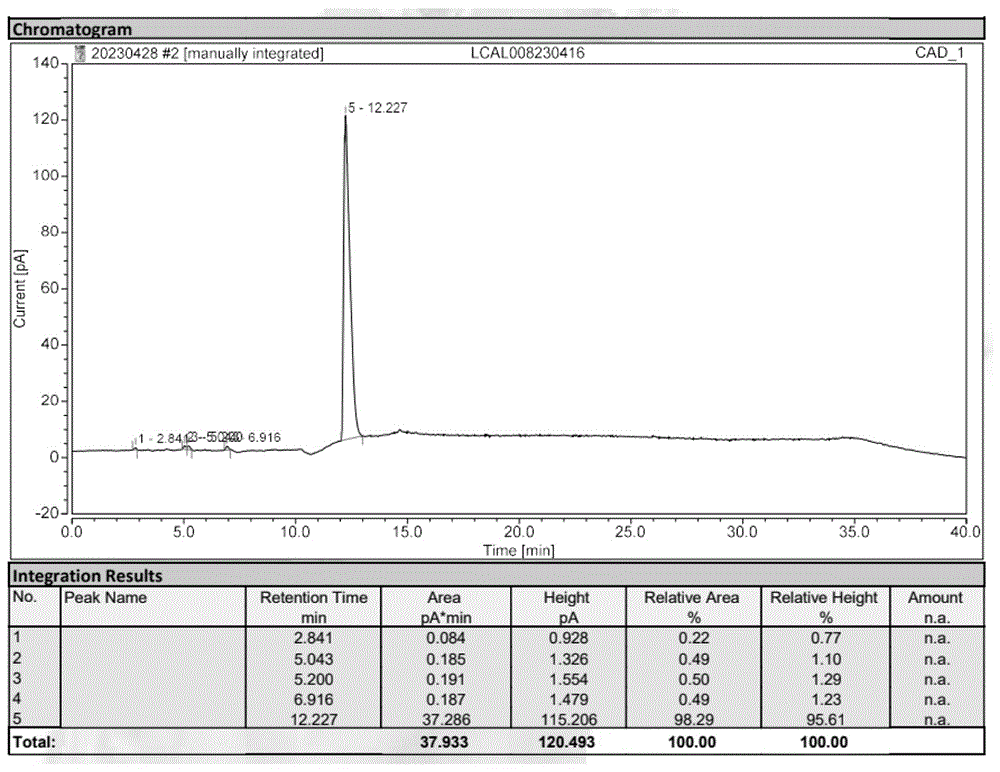
图1为实施例1中分离得到的乙酰-L-高丝氨酸内酯液相图。
图2为实施例2中分离得到的乙酰-L-高丝氨酸内酯液相图。
图3为实施例3中分离得到的乙酰-L-高丝氨酸内酯液相图。
图4为实施例4中分离得到的乙酰-L-高丝氨酸内酯液相图。
具体实施方式
实施例1:乙酰-L-高丝氨酸内酯的制备步骤:取L-高丝氨酸内酯氢溴酸盐1mol(180.9g)溶于有机溶剂四氢呋喃(1L)中,再加入有机碱三乙胺1.2mol(121.4g),将上述反应液于配有磁力搅拌的反应器中0℃下保温0.5小时,通过滴液漏斗向体系中缓慢滴加乙酰氯1.1mol(86.4g),升温至20℃反应3h,液相监测原料消耗毕,反应结束后以饱和氯化铵中和碱性反应体系至中性;用乙酸乙酯液-液萃取得有机相;有机相合并经无水硫酸钠干燥后减压浓缩;异丙醇和石油醚重结晶分离得到乙酰-L-高丝氨酸内酯121.6g,收率85%,液相纯度98.29%,分离得到的乙酰-L-高丝氨酸内酯液相图如图1所示。
实施例2:乙酰-L-高丝氨酸内酯的制备
L-高丝氨酸内酯盐酸盐1mol(137.6g)溶于有机溶剂二氯甲烷和水混合溶剂中(V
实施例3:乙酰-L-高丝氨酸内酯的制备
L-高丝氨酸内酯盐酸盐1mol(137.6g)溶于有机溶剂丙酮和水混合溶剂中(V
实施例4:乙酰-L-高丝氨酸内酯的制备
L-高丝氨酸内酯硫酸盐1mol(199.0g)溶于水中(1L),再加入碱甲醇钠1.5mol(81.03g),将上述反应液于配有磁力搅拌的反应器中5℃下保温2小时,通过滴液漏斗向体系中缓慢滴加乙酰氯2.0mol(157.0g),升温至100℃反应4h,液相监测原料消耗毕,反应结束后以稀盐酸中和碱性反应体系至中性;用乙酸乙酯液-液萃取得有机相;有机相合并经无水硫酸钠干燥后减压浓缩;甲醇和乙醚重结晶分离得到乙酰-L-高丝氨酸内酯126.2g,收率88.19%,液相纯度95.98%,分离得到的乙酰-L-高丝氨酸内酯液相图如图4所示。
本领域的技术人员容易理解,以上所述仅为本发明的较佳实施例而已,并不用以限制本发明,凡在本发明的精神和原则之内所作的任何修改、等同替换和改进等,均应包含在本发明的保护范围之内。
- 一种N-乙酰-L-半胱氨酸的制备方法
- 一种N-苯乙酰基-L-脯氨酸的制备方法
- 一种Nα-(9H-芴-9-基甲氧基)羰基-Nε-乙酰基-L-赖氨酸的制备方法
- 一种制备L-丙氨酰-L-谷氨酰胺的方法
- 一种利用有机溶剂转化N-乙酰神经氨酸水合物制备N-乙酰神经氨酸的方法
- N-苯乙酰-L-脯氨酸和 N-1-(苯基乙酰基)-L-脯氨酰甘氨酸乙酯的制备方法
- 一种高光学纯度的L-或D-高丝氨酸内酯氢溴酸盐的制备方法
