在两相体系中使用碱对含有不饱和侧链的苯醌进行闭环
文献发布时间:2024-04-18 19:58:30
技术领域
本发明涉及色烷和色烯的合成领域,特别是3,4-脱氢生育酚、3,4-脱氢生育三烯酚、生育酚和生育三烯酚的合成。
背景技术
维生素E及其酯是一类重要的色烷化合物。色烷的合成途径是通过相应的色烯。
色烯的形成有不同的途径。
Schudel,Mayer,Isler,Helv.Chim.Acta 46,2517-2526(1963)公开了在以吡啶为反应介质通过闭环的色烯形成过程中,通过香叶基-香叶基三甲基苯醌的闭环反应形成3,4-脱氢生育三烯酚。得到的反应混合物是一种复杂的混合物,要分离出所需的产物需要经过复杂的衍生化过程,形成脱氢生育三烯酚对苯偶氮苯甲酸酯用于分离,并且通过结晶进行纯化。在这一过程中,使用非常昂贵且剧毒的化学品4-(苯基偶氮)苯甲酰氯,因此非常不利。
WO 2015/028643 A1公开了通过Au(I)或Ag(I)催化手性芳基炔的分子内加氢形成色烯。金和银催化剂非常昂贵。
Kabbe和Heitzer,Synthesis 1978,12,888-889公开了,使用由TMHQ和异植醇合成维生素E(即α-生育酚)的已知合成途径不适用于合成生育三烯酚(即由TMHQ和香叶基芳樟醇合成生育三烯酚),因为类异戊二烯侧链会发生酸催化的二级闭环反应。
发明内容
因此,本发明要解决的问题是提供一种提供色烯和色烷的方法,这种方法要比涉及复杂的衍生化、纯化和化学转化的工艺简单得多,最终可以得到所需的产品。
根据权利要求1的方法解决了这一问题。令人惊奇的是,在碱存在的情况下,两相体系非常适用于这一目的,并且可以很容易地分离出所需的式(I)化合物。特别发现,强碱性催化剂特别适合作为所述闭环反应的碱。
该方法为权利要求11或12所述的式(III)或(IV)的色烷提供了非常有利的合成途径。
本发明的其它方面属于其它独立权利要求的主题。特别优选的实施方式是从属权利要求的主题。
具体实施方式
在第一方面,本发明涉及制备式(I)化合物的方法,
所述方法包括在两相体系中在碱存在下式(II)化合物的闭环步骤,产生式(I)化合物,
其中
n=0或1或2或3或4或5或6或7或8或9或10或11或12;
R
R
要么彼此独立地表示氢或甲基或甲氧基
要么共同表示-CH-CH-CH-并形成芳香基团;
任何带有虚线
任何波浪线彼此独立地表示碳-碳键,并且当连接至碳-碳双键时处于Z构型或E构型中。
为清楚起见,本文中使用的一些术语定义如下:
在本文中,"C
在本文中,如果多个式子中存在相同的符号或基团标记,则在一个特定式子中对所述基团或符号所下的定义也适用于包含相同标记的其他式子。
本文中,术语"彼此独立地"是指,在取代基、分子或基团的上下文中,相同指定的取代基、分子或基团可以以不同的含义同时出现在同一分子中。
在本文中,式子中的任何虚线表示取代基与分子其余部分结合的键。
在本文中,化学式中任何带有虚线
在本文中任何化学式中,波浪线都代表碳碳键,当连接至碳碳双键时处于Z构型或E构型中。在所有分子中,碳碳双键优选处于E构型中。
“pK
式(II)化合物
式(II)化合物是本领域技术人员已知的物质,并且其合成方法也是已知的。
在一个优选的实施方式中,取代基R
泛醌是本实施方式的重要代表。根据侧链中类异戊二烯基团的数目泛醌表示为泛醌-2(n=0)、泛醌-3(n=1)、泛醌-4(n=2)、泛醌-5(n=3)、泛醌-6(n=4)、泛醌-7(n=5)、泛醌-8(n=8)、泛醌-9(n=9)、泛醌-4(n=2)、泛醌-5(n=3)、泛醌-6(n=4)、泛醌-7(n=5)、泛醌-8(n=6)、泛醌-9(n=7)和泛醌-10(n=8)。泛醌也以旧称辅酶Q而闻名。泛醌-10(n=8)(=辅酶Q10)是本实施方式中特别优选的物种。
在另一个优选的实施方式中,取代基R
特别优选R
优选地n=2。进一步优选的是,式(II)中所有带有虚线
在本实施方式中,优选地式(II)化合物为式(II-BB)化合物
=香叶基香叶基三甲基苯醌
在另一个优选的实施方式中,取代基R
在本实施方式中,R
维生素K1(叶绿醌)是本实施方式的一个例子。
甲基萘醌(MK),又称维生素K2,是本实施方式的另一个重要代表。
任何带有虚线
根据侧链中类异戊二烯基团的数目,甲基萘醌表示为MK-2(n=0)、MK-3(n=1)、MK4(n=2)、MK-5(n=3)、MK-6(n=4)、MK-7(n=5)、MK-8(n=6)、MK-9(n=7)、MK-10(n=8)、MK-11(n=9)、MK-12(n=10)和MK-13(n=11)。
MK-4(n=2)是本实施方式中特别优选的物种。
如果任何带有虚线
碱
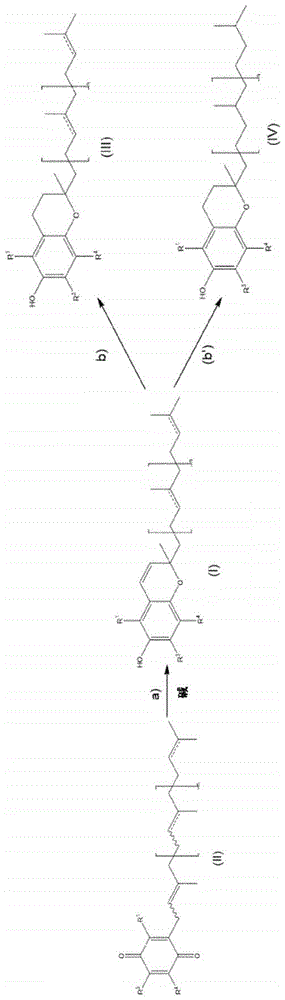
所述方法包括式(I)化合物在碱("碱")存在下的闭环步骤,以产生式(I)化合物,如图1反应方案中步骤a)所示。
碱优选地是碱金属或碱土金属的氢氧化物或碳酸盐,尤其是碱金属氢氧化物。
此外,优选地碱为有机胺,特别是有机叔胺。
并非所有的碱对本发明都同样有效。优选地所述碱不是吡啶。事实证明,所述碱的共轭酸在水中测定的pK
相应酸的pk
1
2
https://organicchemistrydata.org/hansreich/resources/pka/pka_data/
3
4
在一个实施方式中,所述碱是有机胺,特别是选自由以下组成的组:4-二甲基氨基吡啶(=DMAP)、1,8-二氮杂双环[5.4.0]十一碳-7-烯(=DBU)、1,5-二氮杂双环[4.3.0]壬-5-烯(=DBN)、1,4-二氮杂双环[2.2.2]辛烷(=DABCO)、1-氮杂双环[2.2.2]辛烷(=奎宁环)和金雀花碱(sparteine),优选地选自由4-二甲基氨基吡啶(=DMAP)、1,8-二氮杂双环[5.4.0]十一碳-7-烯(=DBU)和1-氮杂双环[2.2.2]辛烷(=奎宁环)组成的组。
碱尤其不能是氢化物,如氢化钠,因为氢化物与式(II)化合物接触时会形成分子氢。氢的形成会在闭环步骤和一般处理过程中造成重大的安全隐患。
在另一个实施方式中,碱优选地是碱金属或碱土金属的氢氧化物或碳酸盐,优选地是碱金属或碱土金属的氢氧化物,特别是碱金属氢氧化物。在本实施方式中,优选的碱是NaOH或KOH。
在另一个实施方式中,碱是氧化铝上的氟化钾(KF/Al
两相体系
式(II)化合物的闭环步骤是在碱存在下的两相体系中进行的。
所述两相体系是一种具有两种不同相的反应体系。两相体系特别由一个液相和一个固相或另一个液相组成。
优选地两相中有一相包括烃,优选地甲苯。
式(II)化合物尤其溶解在所述烃中,优选地甲苯中。
碱优选地与式(II)化合物处于不同的相中。
在其中一个实施方式中,所述两相体系由两个液相组成,优选地由一个水相和一个与水相不混溶的有机相组成。所述有机相尤其包括烃,优选地甲苯。
所述水相优选地包含碱。
在另一个实施方式中,所述两相体系由液相和固相组成。
碱优选地为固体形式。因此,固相具体地为碱或包括碱。碱可以由固体载体支撑。碱可以被吸收或吸附,或化学结合至固体载体如氧化铝、二氧化硅、碳、碳酸盐或硅酸盐或其他矿物。
本实施方式中的液相可以是式(II)化合物,也可以是包含有机溶剂的液态有机相。有机溶剂具体地为烃,最好是甲苯。
因此,作为固相,可以使用碱金属或碱土金属的固体氢氧化物或碳酸盐,优选地碱金属或碱土金属的氢氧化物,特别是碱金属氢氧化物。所述固体氢氧化物或碳酸盐优选地以具有高比表面积的固体形式使用,特别通过机械工艺,如研磨、碾磨或粉碎,或物理化学工艺,如适当的沉淀或结晶获得。研究发现,固体碱的表面积越大(例如以m
在一个特别优选的实施方式中,所述固体碱为氧化铝上的氟化钾(KF/Al
当碱以固体形式使用时,优选地使用相转移剂,特别是季铵盐,尤其是式[NR
据观察,尤其是由液相和固相组成的两相体系显示非常高的产率以及高转化率。因此,由液相和固体组成的两相体系是优选的。
在闭环反应中使用两相体系是非常有利的,因为两相可以很容易地相互分离,这样不仅可以更好地分离起始原料,还可以更好地分离反应产物。因此,使用这种两相体系进行相关反应有利于分别分离反应产物。此外,它还简化了起始原料的循环利用,有利于连续反应模式,而连续反应模式是工业化生产式(I)化合物的优选方式。当碱以固相形式提供时,可以很容易地以较大物体的形式提供,通常是以结构填充物元件的形式提供,这种填充物元件可以是进行还原反应的反应器的一部分,也可以是插入所述反应器的一个元件。这种结构填充物元件可以是堆积的填充物、编织物、开孔泡沫结构(优选由塑料(例如聚氨酯或三聚氰胺树脂)或陶瓷制成),或从蒸馏和萃取技术中原理上已知的结构填充物元件,即通过其几何形状已知。固体碱也可以由具有多孔壁的容器组成,例如具有适当孔径或网孔直径的网或网眼,以允许反应介质的传输,但避免固体碱这样做。有用的结构填充物元件尤其是金属织物填充物和金属线织物填充物,例如Montz A3、Sulzer BX、DX和EX的设计。也可以使用其他机织、针织或毛毡材料制成的结构填充物来代替金属织物填充物。更多有用的结构填充物是扁平状或波纹状片状物,优选地没有穿孔或其他相对较大的孔,例如相当于Montz BI或Sulzer Mellapak的设计的那些。由膨胀金属制成的结构填充物(例如MontzBSH的结构填充物)也很有优势。在这种情况下,特别是当反应在连续反应模式的反应器中进行时,可以很容易地从反应器中取出碱,并用新的碱替换。
已经证明,碱可以用于闭环步骤,特别地以碱/式(II)化合物的摩尔比大于1,特别地在2和1.1之间的量。
然而,令人惊奇地发现,碱也可以催化量使用,即相对于式(II)化合物,碱
闭环步骤通常在搅拌下,优选地在40至200℃之间,优选地在90至150℃之间的温度下,更优选地如果使用有机溶剂在有机溶剂的回流温度下,并且/或者在1bara至10bara之间的压力下进行。此外,该反应优选地在惰性气氛下进行,优选地在氮气下。
已表明,上述方法可以顺利地产生了式(I)化合物。
特别地,上述方法可以简单地分离出所需的式(I)化合物,即无需进行任何复杂的衍生化,以及随后的通过结晶的纯化和最后的化学转化衍生物至所需的化合物,如无需像Schudel,Mayer,Isler,Helv.Chim.Acta 46,2517-2526(1963)中所公开的方法那样。
式(I)化合物特别优选的实施方式是式(I-A)、(I-B)和(I-C)化合物,优选地式(I-AA)、(I-BB)、(I-CC1)和(I-CC2)化合物:
n=0-9,特别地n=8
n=0-9,特别地n=8
n=0-9,特别地n=2
n=0-12
n=0-12,特别地n=2
非常优选的化合物是式(I-As)化合物。
n=3-9,特别地n=8。
非常优选的化合物是式(I-Cis)化合物,
n=1-12,特别地n=2-5。
如上所述得到的式(I)化合物可以借助氢化剂进行氢化。
在一个实施方式中,氢化时仅环中的碳碳双键被氢化了,而烯烃碳碳双键未被氢化("部分氢化"),这样氢化得到式(III)化合物,如图1所示。
式(III)化合物的特别优选实施方式是式(III-A)、(III-B)和(III-C)化合物,优选地式(III-AA)、(III-BB)、(III-CC1)和(III-CC2)化合物:
n=0-9,特别地n=8
n=0-9,特别地n=8
n=0-9,特别地n=2
n=0-12
n=0-12,特别地n=2
非常优选的化合物是式(III-Cis)化合物,
n=3-6,特别地n=5。
在另一个实施方式中,在这种氢化反应中,所有的烯烃碳碳双键都被氢化("完全氢化"),从而氢化得到式(IV)化合物,如图1所示。
式(IV)化合物的特别优选实施方式是式(IV-A)、(IV-B)和(IV-C)化合物,优选地式(IV-A)、(IV-BB)和(IV-CC)化合物:
n=0-9,特别地n=8
n=0-9,特别地n=2
非常优选的化合物是式(IV-Cs)化合物,
n=3-12,特别地n=3-5。
因此,在另一方面,本发明还涉及一种方法,制备式(III)化合物的方法,
所述方法包括以下步骤:
a)通过如上详述的方法制备式(I)化合物;
其中任何带有虚线
任何波浪线彼此独立地表示碳-碳键,并且当连接到碳-碳双键时处于Z构型或E构型中;
b)借助适用于部分氢化的氢化剂对式(I)化合物进行部分氢化,产生式(III)化合物。
步骤b)中使用的氢化剂是仅氢化式(I)中环的碳碳双键的氢化剂。特别适合用作氢化剂的是钠/乙醇,如Schudel,Mayer,Isler,Helv.Chim.Acta 46,2517-2526(1963),特别是第2524页最后一段中所述。
因此,在另一方面中,本发明还涉及一种制备式(IV)化合物的方法,
所述方法包括以下步骤:
a)通过如上详述的方法制备式(I)化合物;
其中任何带有虚线
任何波浪线彼此独立地表示碳-碳键,并且当连接至碳-碳双键时
处于Z构型或E构型中;
b')借助氢化剂对式(I)化合物进行氢化,产生式(IV)化合物。
在步骤b')中使用的氢化剂是这样的氢化剂,它能氢化式(I)的环中所有的烯烃碳碳双键。特别适合作为氢化剂的是在7、8、9或10族过渡金属存在下的氢气,特别地选自Pd、Pt、Rh、Ru、Mn、Fe、Co和Ni组成的组,更优选地Pd。
非均相过渡金属催化剂优选地是非均相担载型过渡金属催化剂。
在本实施方式中,过渡金属担载在载体上,即,钯附着在/或沉积在载体上。载体是一种固体材料。
所述载体优选地是碳或无机载体。优选的无机载体是氧化物或碳酸盐。优选的氧化物是Si、Al、Ce、Ti或Zr的氧化物,特别地是Al或Si的氧化物。特别优选的是二氧化硅、氧化铝、二氧化钛和氧化铈。
如果支撑物是Ce,则优选的氧化物是CeO
优选地氢化在压力下进行,特别是在2-20巴的氢气压力下。进一步优选地,氢化在0℃至100℃的温度下进行。
由式(II)化合物和碱本身组成的双相组合物也是本发明的目的。
因此,在另一方面中,本发明涉及一种双相组合物,其包含:
i)式(II)化合物
其中
n=0或1或2或3或4或5或6或7或8或9或10或11或12;
R
R
要么彼此独立地表示氢或甲基或甲氧基
要么共同表示-CH-CH-CH-并形成芳香基团;
任何带有虚线
以及
任何波浪线彼此独立地表示碳-碳键,并且当连接到碳-碳双键时
处于Z构型或E构型中;
和
ii)与式(II)化合物处于不同相的碱。
式(II)化合物和碱及其优选实施方式已在上文针对方法详细讨论过。
在本发明中,发现基于两相的反应体系可用于上述闭环步骤中的有效闭环。
因此,在另一方面,本发明涉及与式(II)化合物处于不同相的碱用于式(II)化合物的闭环反应以产生式(I)化合物的用途,
其中
n=0或1或2或3或4或5或6或7或8或9或10或11或12;
R
R
要么彼此独立地表示氢或甲基或甲氧基
要么共同表示-CH-CH-CH-并形成芳香基团;
任何带有虚线
任何波浪线彼此独立地表示碳-碳键,并且当连接到碳-碳双键时处于Z构型或E构型中。
上文针对方法已详细讨论了式(II)化合物、碱、两相和闭环步骤及其优选实施方式。
进一步发现,式(I-A)或(I-C)或(III-A)或(III-C)或(IV-A)或(IV-C)的化合物具有抗氧化性。
因此,在另一方面,本发明涉及式(I-A)或(I-C)或(III-A)或(III-C)或(IV-A)或(IV-C)的化合物作为抗氧化剂的用途,
其中n=0-9,特别地n=8
其中n=0-12
其中n=0-9,特别地n=8
其中n=0-12
其中n=0-9,特别地n=8
n=0-12
其中
R
式(I-A)或(I-C)或(III-A)或(III-C)或(IV-A)或(IV-C)的化合物以及它们的优选实施方式已在上文针对方法详细讨论过。
本文中公开的几种化合物是新的。由于这些化合物适用于所公开的方法和用途,因此它们不仅是新颖的,而且具有创造性。
因此,在另一方面中,本发明尤其涉及式(I-As)或(I-Cis)或(III-Cis)或(IV-Cs)的化合物,
其中n=3-9,特别地n=8
其中n=1-12,特别地n=2-5;
其中n=3-6,特别地n=5;
/>
其中n=3-12,特别地n=3-5。
并且其中
R
任何带有虚线
任何波浪线彼此独立地表示碳-碳键,并且当连接至碳-碳双键时处于Z构型或E构型中。
实施例
下面的实验进一步说明了本发明。
实验系列1:液体/固体双相体系:甲苯/固体NaOH
在第一个系列中,在3.5mg四丁基溴化铵(1mol%(相对于香叶基香叶基三甲基苯醌))的存在下,加入0.46g(1.098mmol)香叶基香叶基三甲基苯醌(纯度97%)和6ml甲苯以及4.7mg研磨过的固体NaOH(0.1098mmol,10mol%(相对于香叶基香叶基三甲基苯醌))并在回流(110℃)条件下搅拌,反应时间如表1所示,得到2,5,7,8-四甲基-2-(4,8,12-三甲基十三碳-3,7,11-三烯-1-基)-2H-色烯-6-醇(3,4-脱氢-α-生育三烯酚),转化率和产率如表1所示。
表1.固体NaOH用作固/液两相体系中的固相碱。
实验系列2:液/固两相体系:甲苯/氧化铝上的氟化钾(KF/Al
在第二个系列中,加入0.46g(1.098mmol)香叶基香叶基三甲苯醌(纯度97%)和6ml甲苯以及46mg碱氧化铝上的氟化钾(KF:40重量%)和四丁基溴化铵(1mol%(相对于香叶基香叶基三甲基苯醌)),并在回流(110℃)下搅拌48小时,得到2,5,7,8-四甲基-2-(4,8,12-三甲基十三碳-3,7,11-三烯-1-基)-2H-色烯-6-醇(3,4-脱氢-α-生育三烯酚),转化率和产率如表2所示。
表2.氧化铝上的氟化钾(KF/Al
实验系列3:液/液两相体系:甲苯/碱水溶液
在第三个系列中,在3.5mg四丁基溴化铵(1mol%(相对于香叶基香叶基三甲基苯醌))的存在下,加入0.46g(1.098mmol)香叶基香叶基三甲基苯醌(纯度97%)和6ml甲苯以及6ml浓度如表3所示的相应碱的水溶液,并且在回流(110℃)下搅拌,时间如表3所示,得到2,5,7,8-四甲基-2-(4,8,12-三甲基十三碳-3,7,11-三烯-1-基)-2H-色烯-6-醇(3,4-脱氢-α-生育三烯酚),转化率和产率如表3所示。
表3.不同碱的水溶液作为液相碱和甲苯形成液/液两相体系。
部分氢化
根据Schudel,Mayer,Isler,Helv.Chim.Acta 46,2517-2526(1963)在2524页最后一段公开的过程,将上述制备的3,4-脱氢-α-生育三烯酚(=2,5,7,8-四甲基-2-(4,8,12-三甲基十三碳-3,7,11-三烯-1-基)-2H-色烯-6-醇)定量氢化为α-生育三烯酚(=2,5,7,8-四甲基-2-(4,8,12-三甲基十三碳-3,7,11-三烯-1-基)色烷-6-醇),其特征可通过核磁共振进行验证。
完全氢化
根据Kabbe and Heitzer,Synthesis 1978;12,888-889的888页的最后一段,将上述制备的3,4-脱氢-α-生育三烯酚(=2,5,7,8-四甲基-2-(4,8,12-三甲基十三碳-3,7,11-三烯-1-基)-2H-色烯-6-醇)定量氢化为α-生育酚(=2,5,7,8-四甲基-2-(4,8,12-三甲基十三烷基)-色满-6-醇),其特征可通过核磁共振验证。
- 一种在水介质中制备侧链含有不饱和碳-碳双键的聚苯醚的方法
- 一种在水介质中制备侧链含有不饱和碳-碳双键的聚苯醚的方法
