分离芯片
文献发布时间:2024-04-18 20:02:18
技术领域
本发明属于生物技术领域,具体涉及一种分离芯片。
背景技术
核酸是有机生命一切活动的基础,人体内的细胞活动都是按照一定的规律进行的,其中基因在整个细胞生命活动调节起着关键性的作用。而人体内疾病的产生往往都是和基因组的异常或表达异常相关,因此,分析人体内的核酸序列及异常有助于对疾病的治病机理进行研究,从而更有效、更精准的进行治疗。分子诊断是指从核酸分子层面对疾病进行诊断分析的一种方法,相比于传统的诊断方法,其更精准,更接近疾病产生的根源。
核酸提取是所有分子诊断技术能够有效地进行检测分析的基础前提,核酸提取质量会直接影响后续检测分析结果,因此,如何实现快速、高效的核酸提取技术至关重要。目前,常用的核酸提取技术主要有磁珠法、柱提法和溶液法三种,其中,磁珠法可以与自动化提取仪兼容,从而慢慢成为主流的提取手段。但目前基于磁珠法的提取方式基本都是在离心管中操作,对于提取样本量有一定需求,对于小样本量提取则无法实现,如需要对少量几个细胞或者单个细胞进行提取,这种管式的方法无法满足。现有提取技术的通量低,样品的需要量大,对于微量样品不易提取。
发明内容
本发明实施例的目的是提供一种分离芯片,用以解决现有提取技术通量低,样品的需要量大,对于微量样品不易提取的问题。
本发明实施例提供了一种分离芯片,包括:
基板,所述基板上具有多个分离腔,所述分离腔具有进口和出口,每个所述分离腔中包括多个容纳腔且相邻容纳腔连通;
每个所述分离腔中相邻容纳腔之间分布有第一流道并通过所述第一流道连通,和/或相邻分离腔之间分布有第二流道并通过所述第二流道连通;
所述容纳腔的内侧壁具有亲水层,所述第一流道与所述第二流道的内侧壁具有疏水层。
其中,所述第一流道与所述第二流道连通。
其中,多个所述分离腔中的所述容纳腔呈阵列分布,相邻列中的容纳腔之间分布有所述第一流道,同一行中相邻容纳腔之间通过第三流道连通,所述第三流道的内侧壁具有亲水层,所述第一流道与所述第三流道连通。
其中,多个所述分离腔中的容纳腔呈阵列分布,相邻行中的容纳腔之间分布有所述第二流道,同一列中相邻容纳腔之间通过第四流道连通,所述第四流道的内侧壁具有亲水层,所述第二流道与所述第四流道连通。
其中,位于最外侧的两行中,一行的容纳腔具有进口,另一行的容纳腔具有出口。
其中,所述基板上具有多个同心分布的环形区,每个所述环形区分布有环形腔,所述第二流道的数量为多个,所述第二流道沿所述环形区的径向方向延伸,且所述第二流道分别与每个所述环形腔连通,每个所述环形腔位于相邻所述第二流道之间的部分限定为所述容纳腔,位于相邻所述第二流道之间的多个所述容纳腔之间连通构成所述分离腔。
其中,多个所述第二流道之间相互连通。
其中,位于相邻环形腔之间的区域分别具有容纳腔的进口,位于最外侧环形腔的容纳腔设有出口。
其中,所述第二流道的进口位于所述环形区的环心位置。
其中,多个所述分离腔中的所述容纳腔呈阵列分布,每个所述分离腔中相邻容纳腔之间分布有第一流道并通过所述第一流道连通,相邻分离腔之间分布有第二流道,所述第一流道与所述第二流道连通,所述第一流道与所述第二流道连接成一条弯曲流道。
其中,所述基板包括:
第一基板,所述第一基板上具有多个第一分离腔,所述第一分离腔具有进口和出口,每个所述第一分离腔中包括多个第一容纳腔且相邻第一容纳腔连通;
每个所述第一分离腔中相邻第一容纳腔之间分布有第一凹槽并通过所述第一凹槽连通,和/或相邻第一分离腔之间分布有第二凹槽并通过所述第二凹槽连通;
第二基板,所述第二基板设置于所述第一基板上,所述第二基板上与所述第一容纳腔对应的位置设有第二容纳腔,所述第一容纳腔与所述第二容纳腔构成所述容纳腔,所述第一凹槽与所述第二基板围绕构成所述第一流道,所述第二凹槽与所述第二基板围绕构成所述第二流道。
其中,所述第一容纳腔和/或第二容纳腔的内侧壁具有亲水层,所述第二基板的表面上与所述第一凹槽、所述第二凹槽对应的区域具有疏水层。
其中,每个所述分离腔包括三个所述容纳腔。
在本发明实施例的分离芯片中,所述基板上具有多个分离腔,所述分离腔具有进口和出口,每个所述分离腔中包括多个容纳腔且相邻容纳腔连通;每个所述分离腔中相邻容纳腔之间分布有第一流道并通过所述第一流道连通,和/或相邻分离腔之间分布有第二流道并通过所述第二流道连通;所述容纳腔的内侧壁具有亲水层,所述第一流道与所述第二流道的内侧壁具有疏水层。在提取过程中,由于所述第一流道与所述第二流道的内侧壁具有疏水层,可以向第一流道与所述第二流道中注入液封油,通过液封油可以将相邻的容纳腔或分离腔隔离开,由于容纳腔的内侧壁具有亲水层,样品液可以集聚在容纳腔中,可以将样品液加入分离腔的容纳腔中使其在不同的容纳腔中停留后流经下一个容纳腔中进行处理,比如,在第一个容纳腔中加入样品液进行裂解,裂解后的样品液进入第二个容纳腔进行清洗,清洗后再进入第三个容纳腔中进行洗脱,洗脱后的液体从出口流出,可以进行后续的处理分析。通过分离腔中容纳腔以及流道的设置,可以同时进行多个样品的提取处理,需要的样品量较少,微量即可满足提取需要,减少样品用量,通过该芯片提取核酸具有高通量,易于微量样品提取,提高提取的效率。
附图说明
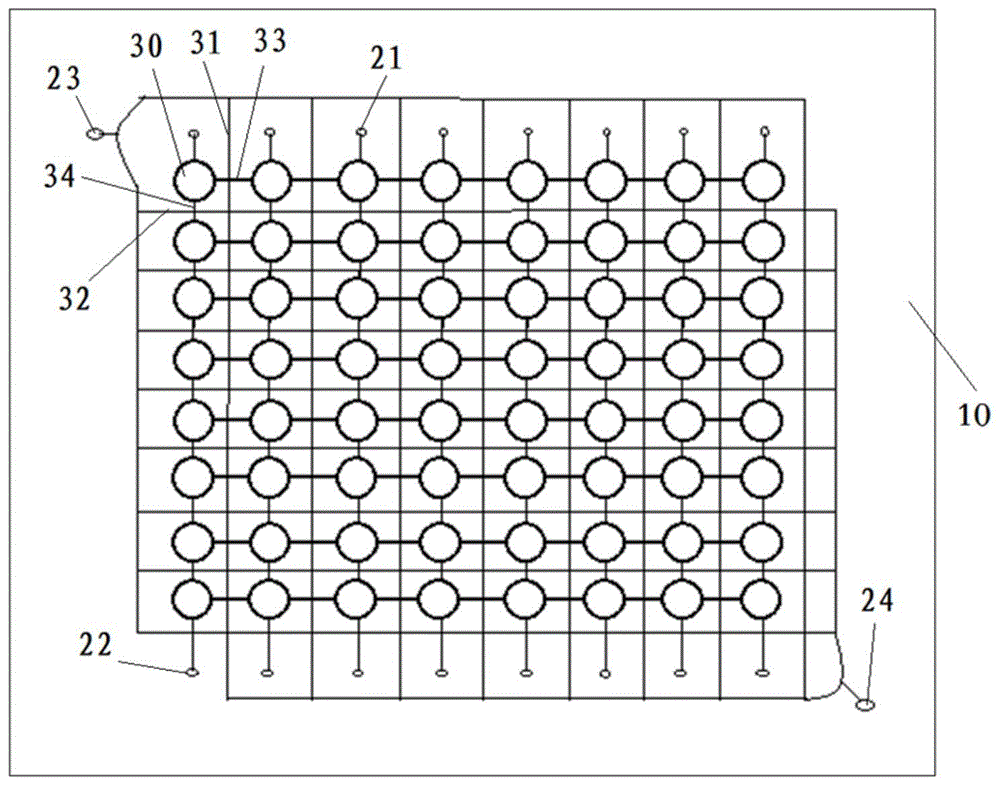
图1为容纳腔在分离芯片上的一个分布示意图;
图2为图1中第一基板与第二基板配合的一个局部示意图;
图3为在第二基板上形成亲水层、疏水层的一个示意图;
图4为提取过程的一个示意图;
图5为容纳腔在分离芯片上的另一个分布示意图;
图6为图5中线A位置的一个剖视图;
图7为容纳腔在分离芯片上的又一个分布示意图;
图8为图7中线B位置的一个剖视图。
附图标记
基板10;亲水层11;疏水层12;
分离腔20;进口21;出口22;
容纳腔30;
第一流道31;第二流道32;第三流道33;第四流道34;
第一基板40;
第二基板50;
第一容纳腔41;第一凹槽42;
第二容纳腔51;第二凹槽52;
混匀磁块60;条形磁铁61;吸附磁块62。
具体实施方式
下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有作出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
本发明的说明书和权利要求书中的术语“第一”、“第二”等是用于区别类似的对象,而不用于描述特定的顺序或先后次序。应该理解这样使用的数据在适当情况下可以互换,以便本发明的实施例能够以除了在这里图示或描述的那些以外的顺序实施。此外,说明书以及权利要求中“和/或”表示所连接对象的至少其中之一,字符“/”,一般表示前后关联对象是一种“或”的关系。
下面结合附图1至图8所示,通过具体的实施例及其应用场景对本发明实施例提供的分离芯片进行详细地说明。
如图1至图8所示,本发明实施例的分离芯片,包括:基板10,基板10上具有多个分离腔20,分离腔20具有进口和出口,可以将裂解液和结合液从进口加入分离腔中,经过清洗和洗脱后的溶液可以从出口流出。每个分离腔20中包括多个容纳腔30且相邻容纳腔30连通;比如,每个分离腔20中可以包括三个容纳腔30,三个容纳腔30中相邻的两个容纳腔30之间连通,第一个容纳腔30与第二个容纳腔30之间连通,第二个容纳腔30与第三个容纳腔30之间连通,第一个容纳腔30、第二个容纳腔30与第三个容纳腔30可以均设置有进口,第一个容纳腔30、第二个容纳腔30与第三个容纳腔30中的至少一个可以设置出口,比如,第三个容纳腔30可以设置出口,具体开口的位置、形状和数量可以根据实际情况选择。在提取过程中,可以将裂解液和结合液从进口加入第一个容纳腔30中,将清洗液加入第二个容纳腔30中,将洗脱液加入第三个容纳腔30中,洗脱后的溶液可以从出口流出。
如图1、图5和图7所示,每个分离腔20中相邻容纳腔30之间分布有第一流道31并通过第一流道31连通,相邻容纳腔30之间可以通过第一流道31使得溶液在不同的容纳腔30之间流动或使得磁珠在不同的容纳腔30之间移动。和/或,相邻分离腔20之间分布有第二流道32并通过第二流道32连通,相邻分离腔20之间可以通过第二流道32,使得溶液在不同的分离腔20之间流动,在使用过程中,可以根据实际的需要使得溶液在不同的分离腔20之间流动,也可以根据实际的需要使得磁珠在不同的分离腔20或容纳腔30之间流动。
容纳腔30的内侧壁可以具有亲水层11,亲水性液体可以集聚在容纳腔30中,第一流道31与第二流道32的内侧壁可以具有疏水层12,疏水性液体可以集聚在第一流道31与第二流道32中,比如,液封油可以集聚在第一流道31与第二流道32中,通过第一流道31与第二流道32中的液封油可以将相邻的容纳腔30进行隔离开或者将相邻的分离腔20进行隔离开,由于通过液封油进行隔离,在提取过程中,磁珠在外部磁体的磁力作用下可以从一个容纳腔30穿过液封油进入相邻的容纳腔30,磁珠在外部磁体的磁力作用下可以从一个分离腔20中的容纳腔30穿过液封油进入相邻分离腔20中的容纳腔30。
在提取过程中,如图1、图5和图7所示,可以将裂解液和结合液从进口加入第一个容纳腔30中,将清洗液加入第二个容纳腔30中,将洗脱液加入第三个容纳腔30中,洗脱后的溶液可以从出口流出。比如,如图4所示,利用一个分离腔20进行提取过程的说明,左侧的第一个容纳腔30可以作为裂解液腔,可以将细胞样本溶液通过裂第一个容纳腔30的进口注入到第一个容纳腔30中,通过来回反复抽取注入充分混匀样本液和裂解液,保持裂解反应3分钟;将磁珠溶液通过第一个容纳腔30的进口注入到第一个容纳腔30中,将磁珠混匀,可以在芯片上方通过条形磁铁61进行上下混匀,反应结合3分钟后,释放混匀磁块60;通过基板下方的吸附磁块62将磁珠吸附到容纳腔30的下侧壁,之后移动吸附磁块62将磁珠移动到第二个容纳腔30中,第二个容纳腔30可以作为清洗液腔,释放吸附磁块62,并通过混匀磁块60充分清洗混匀1分钟,释放混匀磁块60;将上述磁珠通过吸附磁块62转移到清洗液中,释放吸附磁块62,用混匀磁块混匀2分钟,释放混匀磁块60,用吸附磁块62将磁珠吸附到第二个容纳腔30的下侧壁上;第三个容纳腔30可以作为洗脱液腔,将样本洗脱液从第三个容纳腔30中吸出,可以用于下一步测试。
在本发明实施例的分离芯片中,在提取过程中,由于第一流道31与第二流道32的内侧壁具有疏水层,可以向第一流道31与所述第二流道32中注入液封油,通过液封油可以将相邻的容纳腔30或分离腔20隔离开,由于容纳腔30的内侧壁具有亲水层,样品液可以集聚在容纳腔30中,可以将样品液加入分离腔20的容纳腔30中使其在不同的容纳腔30中停留后流经下一个容纳腔30中进行处理,比如,在第一个容纳腔30中加入样品液进行裂解,裂解后的样品液进入第二个容纳腔30进行清洗,清洗后再进入第三个容纳腔30中进行洗脱,洗脱后的液体从出口流出,可以进行后续的处理分析。
通过分离腔20中的容纳腔30以及流道的设置,可以同时进行多个样品的提取处理,需要的样品量较少,微量即可满足提取需要,减少样品用量,通过该芯片提取核酸具有高通量,易于微量样品提取,提高提取的效率。利用本发明中的芯片可以进行高通量微量核酸提取,通过腔室流道设计,可以使核酸提取各步骤在单独隔绝的腔室内进行,通过磁力控制微磁珠在不同腔室中进行移动,以实现提取。在提取过程中,通过优化试剂体系,可以实现裂解和结合液在同一步骤实现。此外,清洗液可以采用无醇清洗液,通过采用无醇清洗液可以解决提取芯片中无法消除乙醇对于后续扩增反应的影响,采用磁力吸附控制的方法,可以实现自动磁珠混匀和移动,通过这种芯片结构及反应步骤优化设计,可以在一张芯片上实现快速高通量微量核酸提取整个流程,可以用来将来稀有微量样本、单细胞等少量样本的核酸提取。
在一些实施例中,第一流道31与第二流道32可以连通,通过第一流道31与第二流道32的连通可以将不同的分离腔20或容纳腔30进行连通,在液封过程中,可以通过液封油将相邻的分离腔20或容纳腔30隔离开,便于快速液封,同时,便于样品液的快速进样,提高提取速度。
在另一些实施例中,如图1所示,多个分离腔20中的容纳腔30可以呈阵列分布,相邻列中的容纳腔30之间可以分布有第一流道31,同一行中相邻容纳腔30之间可以通过第三流道33连通,第三流道33的内侧壁可以具有亲水层,第一流道31与第三流道33可以连通。多个分离腔20中的所有容纳腔30可以呈阵列分布,相邻列中的容纳腔30之间可以分布有第一流道31,可以向第一流道31中注入液封油,通过液封油将相邻列中的容纳腔30之间进行油封。同一行中相邻容纳腔30之间可以通过第三流道33连通,第三流道33的内侧壁可以具有亲水层,便于样品液的集聚,防止液封油进入。第一流道31与第三流道33可以连通,第一流道31与第三流道33可以交叉连通,比如,第一流道31与第三流道33可以垂直交叉连通。
在本发明的实施例中,如图1所示,多个分离腔20中的容纳腔30可以呈阵列分布,相邻行中的容纳腔30之间分布有第二流道32,同一列中相邻容纳腔30之间通过第四流道34连通,第四流道34的内侧壁具有亲水层,第二流道32与第四流道34连通。多个分离腔20中的容纳腔30可以呈阵列分布,相邻行中的容纳腔30之间分布有第二流道32,可以向第二流道32中注入液封油,通过液封油将同一列中相邻容纳腔30之间进行油封。同一列中相邻容纳腔30之间通过第四流道34连通,第四流道34的内侧壁具有亲水层,第二流道32与第四流道34连通。第二流道32与第四流道34可以交叉连通,比如,第二流道32与第四流道34可以垂直交叉连通。多个分离腔20中的所有容纳腔30可以呈阵列分布,通过设置不同的流道进行油封,可以通过液封油将同一列中的相邻容纳腔30之间进行油封,可以将同一行中相邻容纳腔30之间进行油封。在提取过程中,可以根据需要将多个容纳腔30分成一组构成一个分离腔20。
比如,如图1所示,每个分离腔20中可以包括三个容纳腔30,位于最左侧的第一列中的容纳腔30可以作为裂解液腔,位于左侧的第二列中的容纳腔30可以作为清洗液腔,位于左侧的第三列中的容纳腔30可以作为洗脱液腔;位于最侧的第四列中的容纳腔30可以作为裂解液腔,位于左侧的第五列中的容纳腔30可以作为清洗液腔,位于左侧的第六列中的容纳腔30可以作为洗脱液腔;从左向右依次类推可以构成很多组的分离腔20。在提取过程中,可以通过液封油将同一列中相邻容纳腔30之间进行油封,可以将同一行中相邻容纳腔30之间进行油封。可以向位于最左侧的第一列的容纳腔30加入裂解液和结合液,可以向位于左侧的第二列的容纳腔30加入清洗液,可以向位于左侧的第三列的容纳腔30加入洗脱液,由于相邻容纳腔30之间连通,可以使得溶液的加入速度加快,可以同时进行很多组的样品提取,提高通量,需要的样品量少,可以实现微量样品的提取。
可选地,位于最外侧的两行中,一行的容纳腔30可以具有进口,另一行的容纳腔30可以具有出口,可以通过进口加入样品液,可以从出口吸出洗脱液。另外,根据实际的情况,还可以在其他行或列中的容纳腔30上设置进口或出口,以便满足不同的提取需要。
在本发明的实施例中,如图5所示,基板10上可以具有多个同心分布的环形区,每个所述环形区可以分布有环形腔,每个环形区的环形腔可以同心设置,每个环形腔的腔室的截面尺寸可以相同或不同。第二流道32的数量可以为多个,第二流道32可以沿所述环形区的径向方向延伸,且第二流道32分别与每个所述环形腔连通,每个所述环形腔位于相邻第二流道32之间的部分限定为容纳腔30,也即是,通过第二流道32可以将每个环形腔分隔成多个容纳腔30,第二流道32可以注入液封油,通过液封油可以将每个环形腔中相邻容纳腔30之间进行油封。位于相邻第二流道32之间的多个容纳腔30之间连通构成分离腔20,使得磁珠可以在相邻第二流道32之间的多个容纳腔30之间进行移动。
比如,基板10上可以具有三个同心分布的环形区,每个环形区可以分布有环形腔,每个环形腔位于相邻第二流道32之间的部分限定为容纳腔30,相邻两个第二流道32之间具有三个容纳腔30,位于相邻第二流道32之间的三个容纳腔30之间连通构成一个分离腔20,可以通过相邻第二流道32之间的三个容纳腔30之间连通构成的分离腔20进行提取分离,比如,位于最内侧的一个容纳腔30可以作为裂解液腔,位于中间的一个容纳腔30可以作为清洗液腔,位于最外侧的一个容纳腔30可以作为洗脱液腔,位于最内侧的一个容纳腔30可以具有样品液的进口,样品液的进口可以位于最内侧与中间的环形腔之间,样品液和磁珠溶液可以经过进口进入;位于中间的清洗液腔可以具有清洗液的进口,清洗液的进口可以位于最外侧与中间的环形腔之间,清洗液可以经过该进口进入;位于最外侧的洗脱液腔可以具有洗脱液的出口,洗脱液的出口可以位于最外侧的环形腔的外周,洗脱液可以经过该出口进入。可以根据实际情况设置容纳腔30的进口或出口,具体的位置、形状和数量等可以根据实际情况设置。
可选地,多个第二流道32之间相互连通,便于第二流道32中的液封油可以相互流动,可以快速将液封油注入第二流道32中。
可选地,位于相邻环形腔之间的区域可以分别具有容纳腔30的进口21,位于最外侧环形腔的容纳腔30设有出口22。比如,在一个分离腔20中,位于最内侧的一个容纳腔30可以作为裂解液腔,位于最内侧的容纳腔30可以具有进口21,位于中间的一个容纳腔30可以作为清洗液腔,位于中间的容纳腔30可以具有进口21,位于最外侧的一个容纳腔30可以作为洗脱液腔,位于最外侧的容纳腔30可以具有出口22,在提取过程中,位于最外侧的洗脱液腔可以具有洗脱液的出口,便于洗脱液的吸取或流出。
可选地,第二流道32的进口23可以位于所述环形区的环心位置,多个第二流道32的一端可以在环形区的环心位置连通,多个第二流道32可以共用一个进口23,以便于快速均匀地向多个第二流道32中注入液封油。多个第二流道32的另一端可以连通,多个第二流道32的另一端可以均与环形流道连通,使得多个第二流道之间可以相互连通,以便于液封油可以在不同的第二流道32之间流动。
在本发明的实施例中,如图7所示,多个分离腔20中的容纳腔30可以呈阵列分布,每个分离腔20中相邻容纳腔30之间分布有第一流道31并通过第一流道31连通,相邻分离腔20之间分布有第二流道32,第一流道31与第二流道32连通,第一流道31与第二流道32连接成一条弯曲流道,弯曲流道的一端具有进口23,弯曲流道的另一端具有出口24。通过第一流道31与第二流道32中注入液封油,可以将每个分离腔20中相邻容纳腔30之间进行油封。第一流道31与第二流道32连接成一条弯曲流道,便于液封油的注入。
比如,如图7所示,每个分离腔20中可以包括三个容纳腔30,位于最左侧的第一列中的容纳腔30可以作为裂解液腔,第一列中的容纳腔30可以具有进口21,位于左侧的第二列中的容纳腔30可以作为清洗液腔,位于左侧的第三列中的容纳腔30可以作为洗脱液腔,位于左侧的第三列中的容纳腔30可以具有出口22;位于最侧的第四列中的容纳腔30可以作为裂解液腔,位于左侧的第五列中的容纳腔30可以作为清洗液腔,位于左侧的第六列中的容纳腔30可以作为洗脱液腔。在提取过程中,可以通过液封油将同一行中相邻容纳腔30之间进行油封,使得同一个分离腔20中的相邻容纳腔30之间进行油封。可以向位于最左侧的第一列的容纳腔30加入裂解液和结合液,可以向位于左侧的第二列的容纳腔30加入清洗液,可以向位于左侧的第三列的容纳腔30加入洗脱液,可以同时进行很多组的样品提取,提高通量,需要样品量少,可以实现微量样品的提取。
在一些实施例中,如图2、图6和图8所示,基板10可以包括:第一基板40与第二基板50,第一基板40上可以具有多个第一分离腔,第一分离腔具有进口21和出口22,每个第一分离腔中包括多个第一容纳腔41且相邻第一容纳腔41连通;每个第一分离腔中相邻第一容纳腔41之间分布有第一凹槽42并通过第一凹槽42连通,和/或相邻第一分离腔之间分布有第二凹槽52并通过第二凹槽52连通。
第二基板50设置于第一基板40上,第二基板50上与第一容纳腔41对应的位置设有第二容纳腔51,第一容纳腔41与所述第二容纳腔51构成容纳腔30,第一凹槽42与第二基板50围绕构成第一流道31,第二凹槽52与第二基板50围绕构成第二流道32。第二基板50与第一基板40的边缘之间可以密封胶连接和密封。在制备过程中,可制备第一基板40与第二基板50,可以在第一基板40上形成第一容纳腔41、第一凹槽42、第二凹槽52,在第二基板50上形成第二容纳腔51,然后将第二基板50覆盖在第一基板40上进行连接,使得第一容纳腔41与所述第二容纳腔51构成容纳腔30,第一凹槽42与第二基板50围绕构成第一流道31,第二凹槽52与第二基板50围绕构成第二流道32。还可以根据实际的情况选择不同的制备方法。
在一些实施例中,第一容纳腔41和/或第二容纳腔51的内侧壁可以具有亲水层11,第二基板50的表面上与第一凹槽42、第二凹槽52对应的区域可以具有疏水层12。第一容纳腔41和/或第二容纳腔51的内侧壁具有亲水层11,可以使得容纳腔30的内侧壁可以具有亲水层11,亲水性液体可以集聚在容纳腔30中。第二基板50的表面上与第一凹槽42、第二凹槽52对应的区域具有疏水层12,可以使得构成的第一流道31与第二流道32的内侧壁可以具有疏水层12,疏水性液体可以集聚在第一流道31与第二流道32中。液封油可以集聚在第一流道31与第二流道32中,通过第一流道31与第二流道32中的液封油可以将相邻的容纳腔30进行隔离开或者将相邻的分离腔20进行隔离开。
在一些实施例中,如图1、图5和图7所示,每个分离腔20可以包括三个容纳腔30。三个容纳腔30中相邻的两个容纳腔30之间连通,比如,第一个容纳腔30与第二个容纳腔30之间连通,第二个容纳腔30与第三个容纳腔30之间连通,第一个容纳腔30、第二个容纳腔30与第三个容纳腔30可以均设置有进口21,第一个容纳腔30、第二个容纳腔30与第三个容纳腔30中的至少一个可以设置出口22,比如,第三个容纳腔30可以设置出口22,具体开口的位置、形状和数量可以根据实际情况选择。在提取过程中,可以将裂解液和结合液从进口21加入第一个容纳腔30中,将清洗液加入第二个容纳腔30中,将洗脱液加入第三个容纳腔30中,洗脱后的溶液可以从出口22吸出,以便进行后续测试。
第二基板上的结构制备可以通过不同的方法制备,具体的制备过程可以包括:
可以在第二基板50的表层先沉积一层二氧化硅层,之后将二氧化硅层用氧plasma(等离子体)处理5分钟,在表面形成羟基键,形成亲水层11。
具体制备流程可以如下:
1、在第二基板50上通过化学气相沉积法(PECVD)沉积一层100纳米的二氧化硅层;第二基板50可以为玻璃基底;
2、将上述1中的玻璃基底通过plasma处理5分钟,表面会形成一定羟基或羧基,其表面亲疏水性能通过测试水相接触角进行验证,水相接触角≤5°;
3、在玻璃基底上4000rpm旋涂60秒,旋涂光刻胶AR-N430,厚度为1.4微米;
4、将旋涂后的基底置于90℃热板上面1分钟,之后置于85℃热风烘箱中软退火25分钟;
5、通过光刻法制备点阵,点阵尺寸为边长5mm的正方形,紫外波长365nm、405nm、436nm,能量40mJ/cm
6、在95℃热台烘干2分钟;
7、在90℃热风烘箱中固化25分钟;
8、利用25℃去离子水显影30秒;
9、曝光固化150mJ/cm
10、上述基底在转速5000rpm,30秒条件下旋涂一层特氟龙层54,膜层厚度为100~150nm;
11、将旋涂后基底涂布一层pH 8.5的TE缓冲液,置于培养皿中反应半小时,之后用氮气枪吹干;
12、将上述基底在AR 300-76剥离液中剥离30秒,去除残胶,在第二基板50上形成第二容纳腔51、亲水层11和疏水层12。亲水层11和疏水层12的厚度可以根据实际选择,比如,亲水层11和疏水层12的厚度可以为100nm。
芯片的第一基板40可以通过热塑聚丙烯(PP)材料制备,其中,流道、腔室可以通过光刻制备热塑膜具,再通过热压法制备出相应的流道和腔室,PP第二基板的开口可以通过微机械加工实现,第一基板40与第二基板50可以通过热固化胶进行对位贴合。
下面通过一些具体的实施例对本发明进一步说明。
实施例1
实施例1中芯片的结构可以如图1所示,可以通过上述基板的制备方法制备,并制备成芯片。
裂解液腔室中的裂解液组分:3.5M GITC(异硫氰酸胍),1%Tween 20,50mM TrispH 8.0,25mM EDTA,20mg/mL Proteinase K,5%glycerol(甘油,丙三醇)v/v35%isopropanol(异丙醇);
磁珠溶液为纳微磁珠20mg/mL;
清洗液组分:10%聚乙二醇,100mM氯化钠,10mM 3-吗啉丙磺酸;
洗脱液组分:无酶水;
油相组分可以为矿物油、全氟烷、有机长链烷烃中的任意一种。
细胞样本:MSC细胞,浓度10
具体操作如下:
将上述油相通过注射方式注射到基板的油相液封流道中,之后利用亲疏水差异,将裂解液注射到裂解液腔中,把多余的油相挤出,之后同理将清洗液和洗脱液分别注入到清洗液腔和洗脱液腔中;
将细胞样本溶液通过裂解液腔注射口注入到裂解液腔中,通过来回反复抽取注入充分混匀样本液和裂解液,保持裂解反应3分钟;
将磁珠溶液通过裂解液注射口注入到上述裂解液腔中,磁珠混匀方式可根据图4所示,在基板上方可以通过条形磁铁61进行上下混匀,反应结合3分钟后,释放混匀磁块60,可以通过基板下方的吸附磁块62将磁珠吸附到基板上容纳腔的下侧壁,之后移动吸附磁块62将磁珠移动到清洗液腔中,释放吸附磁块62,并通过混匀磁块60充分清洗混匀1分钟,释放混匀磁块60;将上述磁珠通过吸附磁块62转移到清洗液中,释放吸附磁块62,用混匀磁块60混匀2分钟,释放混匀磁块60,用吸附磁块62将磁珠吸附到基板上容纳腔的下侧壁;
将样本洗脱液从洗脱液腔中吸出,用于下一步测试。
测试部分:DNA样本浓度测试取1uL用Qubit 4.0进行测试,测试结果显示在表1中,DNA样本纯度取1uL通过nanodrop one进行测试,A230/280的吸光度值越接近1.8,则纯度越高,具体结果在表1中。
实施例2
实施例2中芯片的结构可以如图5所示,基板中第一基板的制备工艺与实施例1类似,溶液组分和操作步骤也和实施例1中类似。芯片的第二基板可以选用可透气且亲水的热塑性材料,如聚二甲基硅氧烷(PDMS)或聚对苯二甲酸乙二醇酯(PET)材料,并通过臭氧plasma处理,使其表面成为亲水性。相比于实施例1的结构,实施例2中采用的液封流道比较简单,其通量可以同时操作8个不同的样本。DNA提取产物的浓度测试和纯度测试结果在表1中给出。
实施例3
实施例3的芯片可以如图7所示,实施例3相比于实施例1油相液封管路只需一条,管路设计比较简单,相比于实施例2中的圆盘式结构,实施例3中长方形结构方便试用产线量产工艺制备第一基板,通过微加工可做成上万的通量数。第二基板可以采用材质可以为PDMS或其他透气可穿刺材料PET,其中裂解液、清洗液和洗脱液都可以通过穿刺预填充到腔室中,其他流程和实施例2类似。DNA提取产物的测试结果在表1中给出。
表1不同实施例的提取结果
从表1可知,通过本发明实施例中的芯片提取核酸的效果好,提取时间短,有利于提高核酸的提取效率。
上面结合附图对本发明的实施例进行了描述,但是本发明并不局限于上述的具体实施方式,上述的具体实施方式仅仅是示意性的,而不是限制性的,本领域的普通技术人员在本发明的启示下,在不脱离本发明宗旨和权利要求所保护的范围情况下,还可做出很多形式,均属于本发明的保护之内。
- 微流控芯片、干细胞分离方法及微流控芯片的制备方法
- 分离芯片和分离方法
- 驱动芯片封装结构及其分离方法、分离设备
- 裸芯片分离器和包括该裸芯片分离器的裸芯片供应设备
- 分离芯片及该分离芯片的制作方法
