给予治疗的方法
文献发布时间:2023-06-19 10:22:47
本发明涉及施用化合物1的疗法的改进方法,其涉及通过避免或禁忌联合CYP3A4/P-gp诱导剂例如利福平来增加化合物1的有效性。
化合物1是处于研究中的具有结构式I的小分子药物。
结构、名称和合成是已知的,并描述于WO 2014/139882中。化合物1正被开发为自分泌运动因子抑制剂,并被研究用于治疗肺纤维化,特别是特发性肺纤维化(MaherTM等人,“Safety,tolerability,pharmacokinetics,and pharmacodynamics of GLPG1690,anovel autotaxin inhibitor,to treat idiopathic pulmonary fibrosis(FLORA):aphase 2a randomised placebo-controlled trial”,Lancet Respiratory Medicine,2018年5月)。
利福平是一种用于治疗细菌感染的抗生素,在治疗结核病(TB)中具有特别作用。
本文所述的发明基于在还施用利福平的患者中观察到的化合物1的全身性暴露减少。
因此,本发明第一个方面提供化合物1,其用于治疗需要化合物1的疗法的患者,其特征在于该治疗包括避免、禁忌或中断:联合CYP3A4/P-gp诱导剂的伴随使用或共同施用。
在第二个方面,本发明还提供了化合物1在制备用于治疗需要使用化合物1的疗法的患者的药物中的用途,其特征在于该治疗包括避免、禁忌或中断:联合CYP3A4/P-gp诱导剂的伴随使用或共同施用。
在另一个方面,本发明提供了使用化合物1向需要使用化合物1的疗法的患者给予治疗的方法,其包括向患者给予治疗有效量的化合物1,并避免、禁忌或中断:联合CYP3A4/P-gp诱导剂的伴随使用或共同施用。
在具体实施方案中,联合CYP3A4/P-gp诱导剂是利福平。从以下详细描述中,进一步的实施方案是显而易见的。
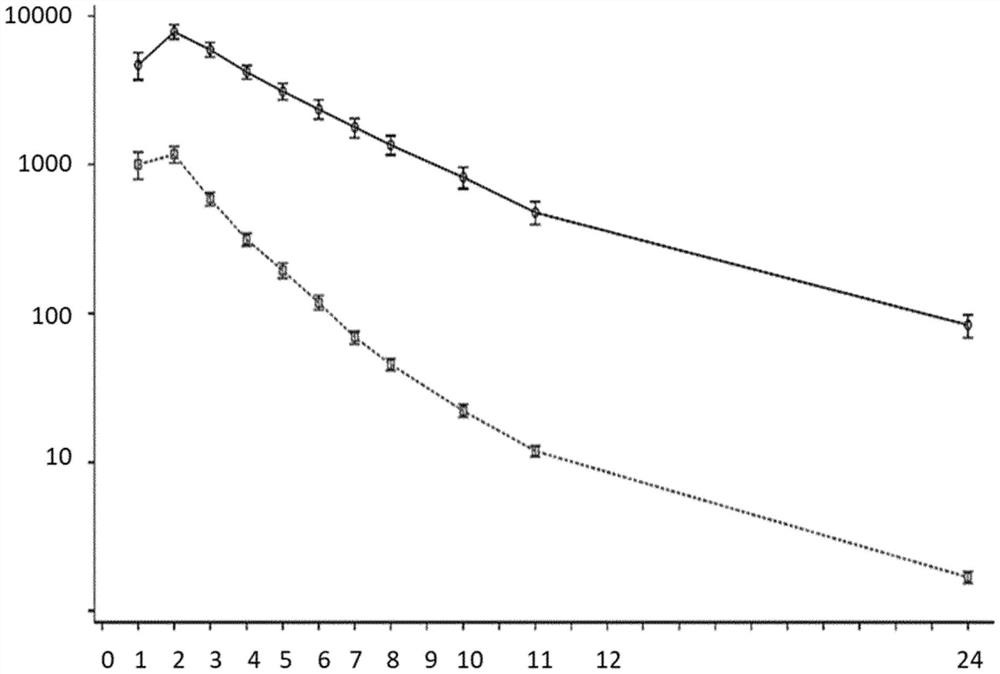
图1:随时间推移的平均值(±SE)化合物1血浆浓度(ng/mL)(Log-线性标度):实线代表在第1天获得的数据,虚线代表在第12天获得的数据。
化合物1是具有结构式I的小分子自分泌运动因子(ATX)抑制剂。
结构、名称和合成是已知的,并描述于WO 2014/139882中。化合物1正在被研究作为人用药物的口服活性剂。
如本文所用,“需要化合物1的疗法”或“需要化合物1的治疗”的患者是将受益于化合物1的施用的患者,所述患者可患有化合物1治疗可用于改善症状的任何疾病或病状。在实施方案中,需要化合物1的疗法或治疗的患者是患有疾病或具有得益于自分泌运动因子抑制的病症的患者。所述疾病或病症包括纤维化疾病、增殖性疾病、炎性疾病、自身免疫性疾病、呼吸系统疾病、心血管疾病、神经变性疾病、皮肤病和/或异常血管发生相关疾病。
在实施方案中,需要化合物1的疗法或治疗的患者是患有纤维化疾病的患者。在一个具体的实施方案中,纤维变性疾病选自特发性肺纤维化(IPF)、囊性纤维化、不同病因的其他弥漫性实质肺病、包括医源性药物诱导的纤维变性、职业性和/或环境诱导的纤维变性、肉芽肿病(肉样瘤病、超敏性肺炎)、胶原血管病、肺泡蛋白沉积症、朗格汉斯细胞肉芽肿病、淋巴管肌瘤病、遗传性疾病(Hermansky-Pudlak综合征、结节性硬化、神经纤维瘤病、代谢性贮积病、家族性间质性肺病)、辐射诱导的纤维变性、慢性阻塞性肺病(COPD)、硬皮病、博来霉素诱导的肺纤维化、慢性哮喘、硅肺、石棉诱导的肺纤维化、急性呼吸窘迫综合征(ARDS)、肾纤维化、肾小管间质纤维化、肾小球肾炎、局灶节段性肾小球硬化、IgA肾病、高血压、Alport、肠纤维变性、肝纤维化、肝硬化、酒精诱导的肝纤维化、毒性/药物诱导的肝纤维化、血色素沉着病、非酒精性脂肪性肝炎(NASH)、胆管损伤、原发性胆汁性肝硬化、感染诱导的肝纤维化、病毒诱导的肝纤维化,和自身免疫性肝炎、角膜瘢痕形成、肥厚性瘢痕、Dupuytren病、瘢痕瘤、皮肤纤维化、皮肤硬皮病、系统性硬化病、脊髓损伤/纤维变性、骨髓纤维化、血管再狭窄、动脉粥样硬化、动脉硬化、韦格纳肉芽肿病、佩罗尼氏病或慢性淋巴细胞性。更特别地,纤维化疾病是特发性肺纤维化(IPF)。
在实施方案中,需要化合物1的疗法或治疗的患者是患有增殖性疾病的患者。在一个具体实施方案中,增殖性疾病选自癌症、白血病、多发性骨髓瘤和银屑病。
在实施方案中,需要化合物1的疗法或治疗的患者是患有炎性疾病的患者。在一个具体实施方案中,炎性疾病选自类风湿性关节炎、骨关节炎、变应性气道疾病(例如哮喘)、慢性阻塞性肺病(COPD)和炎性肠病(例如克罗恩病和溃疡性结肠炎)。更特别地,所述炎性疾病选自类风湿性关节炎和慢性阻塞性肺病(COPD)。
在实施方案中,需要化合物1的疗法或治疗的患者是患有自身免疫性疾病的患者。在一个具体实施方案中,自身免疫性疾病选自COPD、哮喘(例如内源性哮喘、外源性哮喘、粉尘性哮喘、婴儿性哮喘),特别是慢性或顽固性哮喘(例如晚期哮喘和气道高反应性)、支气管炎,包括支气管哮喘、系统性红斑狼疮(SLE)、皮肤红斑狼疮、狼疮肾炎、皮肌炎、干燥综合征、多发性硬化、银屑病、干眼病、I型糖尿病及其相关并发症、特应性湿疹(特应性皮炎)、甲状腺炎(桥本病和自身免疫性甲状腺炎)、接触性皮炎和进一步的湿疹性皮炎、炎性肠病(例如克罗恩病和溃疡性结肠炎)、动脉粥样硬化和肌萎缩性侧索硬化。特别地,所述自身免疫性疾病选自COPD、哮喘、系统性红斑狼疮、I型糖尿病和炎性肠病。
在一个具体实施方案中,需要化合物1的疗法或治疗的患者是患有呼吸系统疾病的患者。在一个具体实施方案中,呼吸系统疾病选自哮喘、成人呼吸窘迫综合征和过敏性(外源性)哮喘、非过敏性(内源性)哮喘、急性重度哮喘、慢性哮喘、临床哮喘、夜间哮喘、过敏原诱导的哮喘、阿司匹林敏感型哮喘、运动诱导的哮喘、等二氧化碳过度通气、儿童发作型哮喘、成人发作型哮喘、咳嗽变异性哮喘、职业性哮喘、类固醇耐受性哮喘、季节性哮喘、季节性过敏性鼻炎、常年性过敏性鼻炎、慢性阻塞性肺病(包括慢性支气管炎或肺气肿)、肺动脉高压、间质性肺纤维化和/或气道炎症和囊性纤维化、以及缺氧。
在一个具体实施方案中,需要化合物1的疗法或治疗的患者是患有心血管疾病的患者。在一个具体实施方案中,心血管疾病选自心律失常(心房或心室或两者)、动脉粥样硬化及其后遗症、心绞痛、心律紊乱、心肌缺血、心肌梗死、心脏或血管动脉瘤、血管炎、中风、肢体、器官或组织的外周阻塞性动脉病、脑、心脏、肾或其他器官或组织缺血后的再灌注损伤、内毒素性、手术或创伤性休克、高血压、瓣膜性心脏病、心力衰竭、血压异常、休克、血管收缩(包括与偏头痛相关的血管收缩)、血管异常、炎症、限于单一器官或组织的功能不全。
在一个具体实施方案中,需要化合物1的疗法或治疗的患者是患有神经变性疾病的患者。在一个具体实施方案中,神经变性疾病选自阿尔茨海默病和其他痴呆、脑癌、变性神经疾病、脑炎、癫痫、遗传性脑病、头和脑畸形、脑积水、中风、帕金森病、多发性硬化、肌萎缩性侧索硬化(ALS或Lou Gehrig病)、亨廷顿病和朊病毒病。
在一个具体实施方案中,需要化合物1的疗法或治疗的患者是患有皮肤病的患者。在一个具体的实施方案中,所述皮肤病选自特应性皮炎、大疱病(bullous disorders)、胶原性疾病、银屑病、银屑病病损、皮炎、接触性皮炎、湿疹、瘙痒、荨麻疹、酒渣鼻、硬皮病、伤口愈合、瘢痕形成、肥厚性瘢痕形成、瘢痕瘤、川崎病、酒渣鼻或Sjogren-Larsso综合征。在一个特定实施例中,需要化合物1的疗法或治疗的患者是患有硬皮病的患者。
在一个具体实施方案中,需要化合物1的疗法或治疗的患者是患有异常血管发生相关疾病的患者。在一个具体实施方案中,所述异常血管生成相关疾病选自动脉粥样硬化、高血压、肿瘤生长、炎症、类风湿性关节炎、湿性黄斑变性、脉络膜新血管形成、视网膜新血管形成、糖尿病性视网膜病和多形性成胶质细胞瘤。
细胞色素P4503A4,也称为其基因名“CYP3A4”,是单加氧酶细胞色素P450家族的成员。CYP3A4蛋白位于内质网,主要在肝脏和肠中表达,并参与所选药物的代谢。
P-糖蛋白(P-gp)也被称为“多药耐药蛋白(MDR1)”,也称之为其基因名为“ABCB1”。P-糖蛋白是一类称为“ATP结合盒”转运蛋白或简称为“ABC”转运蛋白的转运分子的成员。P-糖蛋白位于各种组织的细胞膜中,例如肠、肾、肝和血脑屏障。P-糖蛋白将施用于个体的物质如药物(未改变或在它们被代谢后)转运出细胞(流出),从而使它们可以从体内清除。
联合CYP3A4/P-gp诱导剂是在对个体给药时可提高CYP3A4和P-gp介导的活性的物质。降低化合物1利用度的联合CYP3A4/P-gp诱导剂可选自苯妥英、卡马西平、利福平、地塞米松和圣约翰草(St John’s wort)。在一个具体实施方案中,CYP3A4/P-gp诱导剂选自苯妥英、卡马西平和利福平。在一个具体实施方案中,CYP3A4/P-gp诱导剂是利福平。
利福平(也称为利福平(rifampin)或利福定(rifadin))是一种抗生素。“利福平适应证”(预防性和/或治疗性),即利福平的应用适应证,包括结核病、脑膜炎球菌性脑膜炎、麻风病、流感嗜血杆菌病、普鲁斯病、军团病和严重的葡萄球菌感染。
在一个实施方案中,利福平指明用于治疗所有形式的结核病,包括新发、晚期、慢性和耐药性病例,即使与其他活性抗结核病药物组合使用。利福平也能有效对抗大多数非典型分枝杆菌菌株。
在一个实施方案中,利福平指明用于治疗脑膜炎球菌性脑膜炎,特别是预防脑膜炎球菌性脑膜炎,用于治疗脑膜炎奈瑟氏球菌(N.meningitides)无症状携带者,例如鼻咽中。
在一个实施方案中,利福平指明用于治疗流感嗜血杆菌感染(Haemophilusinfluenzae),特别是用于治疗流感嗜血杆菌(H.influenza)的无症状携带者。
在一个实施方案中,利福平指明用于治疗麻风病,通常与至少一种其他活性抗麻风病药物组合用于多菌型麻风和少菌型麻风的处理,以实现感染状态向非感染状态的转化。
需要利福平治疗的患者是将受益于利福平施用的患者。这样的患者可能患有利福平治疗可用于改善症状的任何疾病或病症。这样的疾病或病症包括由对利福平敏感的生物体感染引起的那些,例如利福平适应证。
如本文所用,术语“避免”及其其他形式是作为术语放弃、停止、克制和制止及其其他形式的替代术语。
在一个具体的实施方案中,术语“避免使用或施用利福平”包括或涉及通过在需要利福平治疗的患者中寻找使用利福平的替代品来避免使用利福平。类似地,对于预期用于需要化合物1的疗法的患者的任何其他P-gp诱导剂,情况可能如此。
如本文所使用的,术语“中断”及其其他形式是作为术语中止、停止、暂停和脱离及其其他形式的替代。
如本文所用,术语“禁忌”及其其他形式,例如“禁忌”涉及包括不输入禁忌的活性的说明。
本文描述了(参见实施例1)关于利福平联合施用对化合物1全身性暴露的影响的人类临床研究。利福平是CYP3A4和P-糖蛋白诱导剂。该研究揭示了对吸收速率和吸收程度的影响,从而明显降低化合物1的生物利用度。因此,提供了涉及在需要化合物1治疗的患者中避免、禁忌和/或中断使用CYP3A4/P-gp诱导剂的方面和实施方案。在本文所述的实施方案中,在需要化合物1治疗的患者中,例如在使用或正在施用化合物1的患者中,避免或禁忌CYP3A4/P-gp诱导剂如利福平的伴随使用或共同施用,或者中断施用CYP3A4/P-gp诱导剂如利福平,以避免不利的药物相互作用,例如避免化合物1的全身性暴露减少,这潜在地导致并也因此避免所述患者中化合物1的功效(治疗)降低。
在一些方面,提供了将化合物1施用于需要化合物1的疗法的患者的方法,其涉及向患者施用治疗有效量的化合物1,且避免在也需要用CYP3A4/P-gp诱导剂治疗的患者中使用或施用(例如,伴随使用或共同施用)所述CYP3A4/P-gp诱导剂。在一个实施方案中,提供了向需要化合物1的疗法的患者施用化合物1的所述方法,其涉及向所述患者施用治疗有效量的化合物1,且避免使用或施用(例如,伴随使用或共同施用)利福平。在另一个实施方案中,通过选择使用或施用CYP3A4/P-gp诱导剂如利福平的替代疗法,避免了CYP3A4/P-gp诱导剂如利福平的使用或施用。
在一些方面,提供了将化合物1施用于需要化合物1的疗法的患者的方法,其涉及向患者施用治疗有效量的化合物1,且中断在也需要用CYP3A4/P-gp诱导剂治疗的患者中使用或施用(例如,同时使用或共同施用)所述CYP3A4/P-gp诱导剂。在一个实施方案中,提供了向需要化合物1的疗法的患者施用化合物1的所述方法,其涉及向所述患者施用治疗有效量的化合物1,且中断使用或施用(例如,伴随使用或共同施用)利福平。
在一些实施方案中,CYP3A4/P-gp诱导剂如利福平的使用或施用在化合物1的开始施用或开始使用的同时中断。在其他实施方案中,CYP3A4/P-gp诱导剂如利福平在开始使用或施用化合物1之前至少1天、至少2天或至少3天中断。在另外的实施方案中,CYP3A4/P-gp诱导剂如利福平在开始使用或施用化合物1之前至少1周、至少2周或至少3周中断。
在另一个实施方案中,CYP3A4/P-gp诱导剂如利福平,在开始使用或施用化合物1后1天内、2天内或3天内中断。这些时间段可提供足够的时间使CYP3A4/P-gp诱导剂逐渐减少和停药而没有副作用,例如当CYP3A4/P-gp诱导剂是地塞米松时。因此,中断CYP3A4/P-gp诱导剂前的时间应与CYP3A4/P-gp诱导剂的安全停药一致。在一些实施方案中,CYP3A4/P-gp诱导剂在化合物1的疗法开始后不迟于一个月、3周、2周或1周被中断。
在一些方面,提供了向需要化合物1的疗法的患者施用化合物1的方法,其涉及向该患者施用治疗有效量的化合物1,且禁忌在也需要用CYP3A4/P-gp诱导剂治疗的患者中使用或施用(例如,伴随使用或共同施用)所述CYP3A4/P-gp诱导剂。在一个实施方案中,提供了向需要化合物1的疗法的患者施用化合物1的所述方法,其涉及向所述患者施用治疗有效量的化合物1,且禁忌使用或施用(例如,伴随使用或共同施用)利福平。
在另一个方面,提供了包装产品或药盒,其包含化合物1,所述化合物1任选地处于容器中,以及包装插页、包装标签、说明书或其他标签,其包括关于以下的信息、建议或说明:避免或中断或禁忌并行使用化合物1和利福平或一般CYP3A4/P-gp诱导剂,如本文的不同方面和实施方案中所述。例如,诸如包装插页、包装标签、说明书或其他标签可以包括以下信息、建议或说明中的任何一个或多个:
-告知或建议患者应避免并行使用CYP3A4/P-gp诱导剂,例如利福平;
-告知或建议所述患者禁忌并行使用CYP3A4/P-gp诱导剂,例如利福平;
-告知或建议所述患者应中断并行使用CYP3A4/P-gp诱导剂,例如利福平,例如在化合物1治疗之前至少1周、至少两周、至少3周或至少4周中断;
-告知或建议患者并行使用CYP3A4/P-gp诱导剂,例如利福平,可改变化合物1的治疗效果,例如降低化合物1的治疗效果,在这种情况下,说明书可进一步指出因此并行使用是禁忌的;
-指导所述患者中断并行使用CYP3A4/P-gp诱导剂,例如利福平;
-指导需要化合物1的疗法的患者不并行使用或施用CYP3A4/P-gp诱导剂,例如利福平;
-禁忌并行使用或施用CYP3A4/P-gp诱导剂,例如利福平。
说明或建议还可包括使用替代疗法代替使用CYP3A4/P-gp诱导剂如利福平的建议。
应理解,包括在包装插页、包装标签、说明书或其他标签中的明确措词可根据包装被授权上市的管辖区而变化,且因此涵盖涉及在需要化合物1的疗法的患者中避免、中断或禁忌并行使用或施用P-gp诱导剂(例如利福平)的任何措词。
在一个相关方面或实施方案中,提供了制备或包装化合物1药物的方法,其包括包装化合物1(任选地将其包装在容器中),连同包装插页、包装标签、说明书或其他标签(包括前述说明、建议或推荐中的任何一个、两个、三个或更多个)。
在健康男性受试者中进行I期、开放标签、非随机化、药物-药物相互作用研究,以评价利福平重复剂量对化合物1的单剂量药代动力学(PK)的影响,以及评价在利福平口服剂量之前或之后施用的单剂量化合物1的安全性和耐受性。
十八名健康男性受试者在第1天接受600mg化合物1的单次口服剂量。从第2天至第11天,将600mg利福平每天一次(q.d.)施用给所有受试者,连续10天。在第12天,受试者接受600mg化合物1的单次口服剂量(参见表1)。在第15天和第18天之间进行随访。
表1化合物1和利福平施用方案
用于测定化合物1的样品
在第1、2、12、13天(即在第1天和第12天施用化合物1后1、2、3、4、5、6、7、8、12和24小时)和在随访时,采集用于化合物1的PK评价的血液样品。通过臂中静脉穿刺(或留置导管)将用于测定血浆中化合物1水平的2mL血液样品收集到含有肝素锂的真空管中,并立即冷却(冰浴)。
在血液收集后30分钟内,通过在4℃以大约1,500g离心10分钟来分离血浆,并转移到2个聚丙烯管中,其中第一等分试样中具有至少400μL血浆,第二等分试样中具有剩余体积。在适当标记后,将血浆样品在离心后2小时内储存在-20℃±10℃的临床中心中,并且保护其免受直射日光。
药物动力学评估
使用经确证的串联质谱液相色谱(LC/MS-MS)波谱测定法测定血浆浓度,其中化合物1的定量限为1.00ng/mL,胆固醇为20.0mg/mL,4β羟基胆固醇为5.00ng/mL。使用Phoenix
从血浆中的各浓度-时间曲线确定化合物1的以下参数:
C
t
AUC
AUC
C
利福平对CYP3A4的诱导作用是用4-β-羟基胆固醇/胆固醇的比例作为标记物来评价的,并证明是有效的。
药物动力学分析
每名受试者以天列出化合物1的血浆浓度和PK参数(第1天:利福平多剂量前的化合物1;第12天:利福平多剂量后的化合物1)。按天计算血浆浓度和PK参数的描述性统计。平均值(±SE)浓度-时间曲线是按天产生的。
药物相互作用的评估
对化合物1的以下自然log(ln)变换的PK参数进行混合效应模型,其中以天数作为固定效应,受试者作为随机效应:C
由于t
药物动力学结果
化合物1血浆浓度
平均值(±SE)图示于图1(对数线性标度)。
在第1和12天,在施用后2小时达到化合物1的平均最大浓度,其值分别是7,870ng/mL和1,180ng/mL。
化合物1的消除在多次利福平摄入之前和之后表现为双相的(图1)。当比较第12天和第1天时,对数-线性平均浓度-时间曲线的目视检查显示表观消除速率的微小差异,表明对化合物1消除速率没有影响,因此对化合物1清除没有影响。
化合物1药代动力学参数
单个化合物1PK参数与描述性统计和药物-药物相互作用评估的统计学分析结果总结在表2中。
表2:化合物1药代动力学参数和药物-药物相互作用评估的统计学分析的总结
PE=点估计值
N=具有数据的受试者的数目
对于C
统计分析显示C
如点估计值(PE)所示,多次利福平摄入导致化合物1的生物利用度显著降低:C
化合物1PK参数(C
本研究的目的是研究利福平的多个口服剂量对化合物1的单剂量PK的影响。
在单次600mg口服剂量后,快速(2小时)达到化合物1的最大血浆浓度,相关平均值为7,870ng/mL。
每天一次用利福平(600mg,每日)给药10天导致化合物1的生物利用度降低(C
- 包括给予维生素D化合物和另外的治疗剂的治疗癌症的方法
- 治疗剂的组合和给予方式以及联合治疗
