一种检测SARS-CoV-2的引物组合物及其应用
文献发布时间:2023-06-19 11:30:53
技术领域
本发明属于基因工程技术领域,涉及一种检测SARS-CoV-2的引物组合物及其应用。
背景技术
冠状病毒属于套式病毒目、冠状病毒科、冠状病毒属,是一类具有囊膜、基因组为线性单股正链的RNA病毒,是自然界广泛存在的一类病毒。某些冠状病毒会感染人类并引起疾病,比如中东呼吸综合征(MERS)、严重急性呼吸综合征(SARS)和SARS-CoV-2引起的肺炎,其症状可从普通感冒到重症肺部感染。
SARS-CoV-2引起的肺炎主要以发热、乏力和干咳为主要表现。少数患者伴有鼻塞、流涕、腹泻等症状。对SARS-CoV-2感染的肺炎疑似案例、疑似聚集性病例患者及接触物等进行SARS-CoV-2检测,并采取适当措施,可以有效地鉴别感染病源,阻断疫情传播。
SARS-CoV-2基因组为一条完整的单股正链RNA,长约30Kb。利用NCBI上的ORFfinder工具进行该病毒的基因组注释分析发现SARS-CoV-2基因组中共有14个开放阅读框(具有编码基因的能力),ORF1a、ORF1ab和4种结构蛋白:刺突蛋白(Spike protein,S蛋白),膜蛋白(membrane protein,M蛋白),包膜蛋白(envelope protein,E蛋白),核壳蛋白(nucleocapsid,N蛋白)。
易发生突变是多数RNA病毒的一种固有性质,已有报道揭示了SARS-CoV-2突变株的出现,SARS-CoV-2具有校对功能的聚合酶(proofreading polymerase),其可使SARS-CoV-2发生碱基置换(substitutions)突变的机率较低,但SARS-CoV-2较易发生缺失(deletions)突变,这种突变多发生在S蛋白的重复缺失区(recurrent deletion regions,RDRs),作为抗体识别表位,RDRs的缺失突变可能导致SARS-CoV-2抗体的结合特异性发生变化,使其发生抗原进化(antigenic evolution),进而逃逸由突变前SARS-CoV 2诱生的中和抗体。
目前,国内外对SARS-CoV-2进行检测的方法主要集中在以靶序列PCR扩增为基础的检测和测序技术(Sanger测序、NGS测序)两方面,SARS-CoV-2核酸的定性检测主要包括逆转录+实时荧光定量PCR(Real-time PCR)等,其中荧光PCR技术简单、快速且灵敏,如CN111270021A公开了一种用于检测新型冠状病毒SARS-CoV-2的引物对、探针、组合物、试剂盒及应用,该荧光RT-RAA引物和荧光探针可以快速、定性检测患者样本中的新型冠状病毒SARS-CoV-2,但由于病毒发现时间较短,科学认知不足,用于鉴别诊断的基因位点未经大规模临床验证,可能存在假阴性或假阳性,准确性和分析特异性风险。
综上所述,提供一种准确检测SARS-CoV-2的引物及检测方法,发现新的变异位点,对于SARS-CoV-2防控具有重要意义。
发明内容
针对现有技术的不足和实际需求,本发明提供一种检测SARS-CoV-2的引物组合物及其应用,利用所述引物组合物进行逆转录巢式PCR,并结合测序,能够快速、准确地获取SARS-CoV-2基因信息,从而能够实现快速检测SARS-CoV-2以及判断SARS-CoV-2突变株。
为达上述目的,本发明采用以下技术方案:
第一方面,本发明提供一种检测SARS-CoV-2的引物组合物,所述引物组合物包括SEQ ID NO:1~SEQ ID NO:12所示的核酸序列。
SEQ ID No.1:CAGTGTGTTAATCTTACAACCAGAAC。
SEQ ID No.2:CAGACTTTAATAACAACATTAGTAGCGTT。
SEQ ID No.3:GAACAGGAAGAGAATCAGCAAC。
SEQ ID No.4:ACTCAGTAAGAACACCTGTGCCT。
SEQ ID No.5:GTTTCTGCCTTTCCAACAATTTGGC。
SEQ ID No.6:CTGCATTCAGTTGAATCACCAC。
SEQ ID No.7:TCTTTCACACGTGGTGTTTATTAC。
SEQ ID No.8:ACAATAAGTAGGGACTGGGTCTTC。
SEQ ID No.9:CTGTGTTGCTGATTATTCTGTCCTATAT。
SEQ ID No.10:AACCATTGAAGTTGAAATTGACAC。
SEQ ID No.11:GACATTGCTGACACTACTGATGCT。
SEQ ID No.12:CTGGTAGAATTTCTGTGGTAACACTAAT。
本发明中,设计引物组合物时首先通过进化树分析,发现与SARS-CoV-2亲缘最近的为蝙蝠bat-SL-CoVZC45病毒,其次为SARS-CoV病毒,为提高扩增特异性,选择的目标序列均与bat-SL-CoVZC45和SARS-CoV序列有5%以上的碱基差异的序列,并通过Blast比对,确保与人类基因组、常见人体或环境微生物之间无交叉反应。
因此,本发明的引物组合物能够针对SARS-CoV-2的S蛋白特定区域g.21765_21770del(p.HV 69_70del)、g.A22812C(p.K417T)、g.G22813C/T(p.K417N)、g.G23012A(p.E484K)、g.A23063T(p.N501Y)、g.A23403G(p.D614G)和g.C23604A(p.P681H)进行高度特异性扩增。
优选地,所述引物组合物还包括内参引物。
优选地,所述内参引物为B2M内参引物。
优选地,所述B2M内参引物包括SEQ ID NO:13和SEQ ID NO:14所示的核酸序列。
SEQ ID No.13:TCATGAGGAGTATGCAGACTCT。
SEQ ID No.14:TCCACATCTGTGGATTCAGCA。
本发明中,内参引物可作为监控提取与反转录过程的指标。
第二方面,本发明提供第一方面所述的检测SARS-CoV-2的引物组合物在制备SARS-CoV-2检测产品中的应用。
第三方面,本发明提供一种检测SARS-CoV-2的试剂盒,所述试剂盒包括第一方面所述的检测SARS-CoV-2的引物组合物。
优选地,所述试剂盒还包括PCR反应液、测序引物和测序试剂。
优选地,所述PCR反应液包括DNA聚合酶、Mg
优选地,所述PCR反应液还包括逆转录扩增Mix、10×QIAGEN buffer和5Qsolution。
优选地,所述测序引物包括SEQ ID NO:7、SEQ ID NO:9和SEQ ID NO:11所示的核酸序列。
优选地,所述测序试剂包括BigDye Terminator v3.1 Cycle Sequencing Kit。
第四方面,本发明提供一种第三方面所述的检测SARS-CoV-2的试剂盒以非疾病治疗和/或诊断为目的的使用方法,所述方法包括:
以样本中核酸为模板,利用第一方面所述的检测SARS-CoV-2的引物组合物进行逆转录巢式PCR,对逆转录巢式PCR的产物进行测序,并对测序结果进行分析。
本发明中,采用所述引物组合物能够对SARS-CoV-2进行高度特异性逆转录巢式PCR,对逆转录巢式PCR的产物进行测序,可准确获取SARS-CoV-2基因信息,从而进行SARS-CoV-2检测以及突变株分析。
本发明中,样本可以为人体样本,亦可以为接触物、食品等环境样本。
优选地,所述逆转录巢式PCR包括一步法逆转录巢式PCR。
优选地,所述测序包括Sanger测序。
本发明中使用Sanger测序法获取SARS-CoV-2核酸序列,可直接读取DNA的序列,测序长度较长,可发现新的变异位点,包括新的、罕见的突变形式及突变的确切类型,如点突变、片段缺失等。
优选地,所述一步法逆转录巢式PCR包括第一轮扩增和第二轮扩增。
优选地,所述第一轮扩增的引物包括SEQ ID NO:1~6、SEQ ID NO:13和SEQ ID NO:14所示的核酸序列。
优选地,所述第一轮扩增的反应体系如表1所示,其中,混合酶包括热启动Taq酶、逆转录酶和UNG酶。
表1
优选地,所述第一轮扩增的程序如表2所示。
表2
优选地,所述第二轮扩增的引物包括SEQ ID NO:7~12、SEQ ID NO:13和SEQ IDNO:14所示的核酸序列。
优选地,所述第二轮扩增的反应体系如表3所示。
表3
优选地,所述第二轮扩增的程序如表4所示。
表4
优选地,引物对应关系如表5所示。
表5
优选地,所述方法还包括回收扩增产物的步骤;
优选地,所述回收扩增产物的方法包括通过琼脂糖凝胶电泳回收扩增产物。
优选地,所述琼脂糖凝胶的质量百分比为1~3%(w/w)。
优选地,所述电泳的电压为80~120 V。
优选地,所述电泳的时间为15~25 min。
优选地,所述Sanger测序包括:
采用BigDye Terminator试剂盒进行测序PCR,将测序PCR产物用酒精纯化,加入Hi-Di甲酰胺,上样,按照ABI 3500XL Dx的仪器说明书进行设置开始运行程序,下机后进行结果分析。
作为优选的技术方案,所述检测SARS-CoV-2的试剂盒以非疾病治疗和/或诊断为目的的使用方法包括以下步骤:
(1)提取样本中核酸;
(2)以样本中核酸为模板,利用SEQ ID NO:1~6、SEQ ID NO:13和SEQ ID NO:14所示引物,按扩增程序:53~57℃,14~16 min;93~96℃,28~32 sec;93~96℃,9~11 sec,58~62℃,58~62 sec,13~17个循环;36~40℃,28~32 sec,进行第一轮扩增,使用1~3%(w/w)的琼脂糖凝胶于80~120 V进行电泳15~25 min,回收第一轮扩增产物;
(3)以所述第一轮扩增产物为模板,利用SEQ ID NO:7~12、SEQ ID NO:13和SEQ IDNO:14所示的引物按扩增程序:93~97℃,14~16 min;93~95℃,28~32 sec,58~62℃,58~62sec,70~74℃,58~62 sec,33~37个循环;70~74℃,9~11 min;36~40℃,28~32 sec,进行第二轮扩增,使用1~3%(w/w)的琼脂糖凝胶于80~120 V进行电泳15~25 min,回收第二轮扩增产物;
(4)利用SEQ ID NO:7、SEQ ID NO:9和SEQ ID NO:11所示的测序引物,对所述第二轮扩增产物进行Sanger测序,并对测序结果进行分析。
与现有技术相比,本发明具有以下有益效果:
(1)本发明的引物组合物具备高特异性,能够针对SARS-CoV-2的S蛋白特定区域进行高特异逆转录巢式PCR;
(2)本发明利用所述引物组合物行逆转录巢式PCR,并结合Sanger测序,能够快速、准确地获取SARS-CoV-2基因信息,从而能够实现快速检测SARS-CoV-2以及判断SARS-CoV-2突变株,且具备良好的准确性、灵敏度、特异性以及重复性。
附图说明
图1为实施例2中第二轮扩增产物琼脂糖凝胶电泳图;
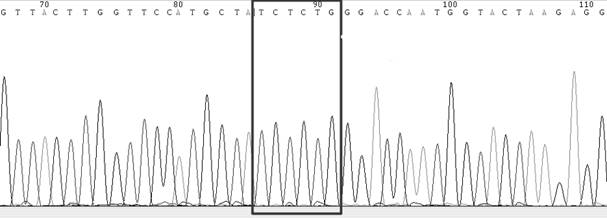
图2为实施例2中1号扩增产物测序结果图,图中矩形标记处为突变起始位置,g.21765_21770 del(p. HV 69_70del)突变;
图3为实施例2中2号扩增产物测序结果图,图中矩形标记处为突变区域,g.G22813T(p. K417N)突变;
图4为实施例2中2号扩增产物测序结果图,图中矩形标记处为突变区域,g.G23012A(p. E484K)无突变;
图5为实施例2中2号扩增产物测序结果图,图中矩形标记处为突变区域,g.A23063T(p. N501Y)无突变;
图6为实施例2中3号扩增产物测序结果图,图中矩形标记处为突变区域,g.A23403G(p. D614G)突变;
图7为实施例2中3号扩增产物测序结果图,图中矩形标记处为突变区域,g.C23604A(p. P681H)无突变;
图8为实施例3中第二轮扩增产物琼脂糖凝胶电泳图;
图9为实施例3中1号扩增产物测序结果图,图中矩形标记处为突变起始位置,g.21765_21770 del(p. HV 69_70del)突变;
图10为实施例3中2号扩增产物测序结果图,图中矩形标记处为突变区域,g.G22813T(p. K417N)突变;
图11为实施例3中2号扩增产物测序结果图,图中矩形标记处为突变区域,g.G23012A(p. E484K)突变;
图12为实施例3中2号扩增产物测序结果图,图中矩形标记处为突变区域,g.A23063T(p. N501Y)无突变;
图13为实施例3中3号扩增产物测序结果图,图中矩形标记处为突变区域,g.A23403G(p. D614G)无突变;
图14为实施例3中3号扩增产物测序结果图,图中矩形标记处为突变区域,g.C23604A(p. P681H)无突变。
具体实施方式
为进一步阐述本发明所采取的技术手段及其效果,以下结合实施例和附图对本发明作进一步地说明。可以理解的是,此处所描述的具体实施方式仅仅用于解释本发明,而非对本发明的限定。
实施例中未注明具体技术或条件者,按照本领域内的文献所描述的技术或条件,或者按照产品说明书进行。所用试剂或仪器未注明生产厂商者,均为可通过正规渠道商购获得的常规产品。
实施例1
本实施例提供一种SARS-CoV-2检测试剂盒及其使用方法,所述试剂盒包括SEQ IDNo.1~12所示的引物组合物、SEQ ID No.7,9,11所示的测序引物、PCR反应的试剂和Sanger测序的试剂,其中PCR反应的试剂包括宝瑞生物的逆转录扩增Mix、宝瑞生物的混合酶(包含热启动Taq酶、逆转录酶、UNG酶)、QIAGEN的10×buffer、QIAGEN的5Q solution、QIAGEN的25mM Mg
所述使用方法包括:
(1)采集鼻咽拭子样本;
(2)采用磁珠法提取核酸;
(3)使用核苷酸序列如SEQ ID No.1~12所示的引物组合进行扩增反应,
第一轮扩增反应的体系为30 μL,Primers由SEQ ID No.1~6所示的引物组合混合而成,反应体系如表6所示。
表6
第一轮扩增反应程序如表7所示。
表7
第二轮扩增反应的体系为50 μL,Primers为SEQ ID No.7-12所示的引物组合,反应体系如表8所示。
表8
第二轮扩增反应程序如表9所示。
表9
(3)扩增产物的琼脂糖凝胶电泳及回收
用2%(w/w)的琼脂糖凝胶进行电泳,电泳条件为100 V,20 min,采用离心柱型普通琼脂糖凝胶DNA回收试剂盒(天根,Cat NO. DP209-03)回收扩增产物;
(4)Sanger测序
以第二轮扩增产物为模板,使用核苷酸序列如SEQ ID No.7,9,11所示的测序引物进行Sanger测序,采用BigDye Terminator试剂盒进行测序PCR,将测序PCR产物用酒精纯化,加入Hi-Di甲酰胺,上样,按照ABI 3500XL Dx的仪器说明书进行设置开始运行程序,下机后进行结果分析。
其中,测序PCR反应的体系为10 μL,具体体系如表10所示。
表10
测序PCR反应的程序如表11所示。
表11
实施例2
本实施例使用实施例1所述试剂盒及使用方法对SARS-CoV-2(样本来源:凯普医学检验所检测人源标本的剩余核酸样本)进行检测,具体对SARS-CoV-2 S蛋白基因突变g.21765_21770 del(p.HV 69_70del)、g.A22812C(p.K417T)、g.G22813C/T(p.K417N)、g.G23012A(p.E484K)、g.A23063T(p.N501Y)、g.A23403G(p.D614G)和g.C23604A(p.P681H)进行检测。
如表5所示,SEQ ID NO:1、2和SEQ ID NO:7、8分别为g.21765_21770 del(p.HV69_70del)区段的第一轮扩增和第二轮扩增的引物,首先以SEQ ID NO:1、2所示引物进行第一轮扩增,并以SEQ ID NO:7、8所示引物进行第二轮扩增,得到1号扩增产物,同理,以SEQID NO:3、4所示引物进行第一轮扩增,并以SEQ ID NO:9、10所示引物进行第二轮扩增,得到2号扩增产物;以SEQ ID NO:5、6所示引物进行第一轮扩增,并以SEQ ID NO:11、12所示引物进行第二轮扩增,得到3号扩增产物,进行琼脂糖凝胶电泳,结果如图1所示,左侧第一泳道为DNA marker(条带大小由上至下分别为1000 bp,700 bp,500 bp,400 bp,300 bp,200 bp和100 bp),左数第2-5泳道分别为1~3号第二轮扩增产物以及内参扩增产物,回收各扩增产物,并进行Sanger测序,结果如图2-图7所示,样本检测结果为g.21765_21770 del(p.HV69_70del)、g.G22813T(p.K417N)和g.A23403G(p. D614G)突变。
实施例3
本实施例使用实施例1所述试剂盒及使用方法对SARS-CoV-2(样本来源:假病毒的RNA样本,假病毒购买于广州艾基生物技术有限公司)进行检测,具体对SARS-CoV-2 S蛋白基因突变g.21765_21770 del(p.HV 69_70del)、g.A22812C(p.K417T)、g.G22813C/T(p.K417N)、g.G23012A(p.E484K)、g.A23063T(p.N501Y)、g.A23403G(p.D614G)和g.C23604A(p.P681H)进行检测。
如表5所示,SEQ ID NO:1、2和SEQ ID NO:7、8分别为g.21765_21770 del(p.HV69_70del)区段的第一轮扩增和第二轮扩增的引物,首先以SEQ ID NO:1、2所示引物进行第一轮扩增,并以SEQ ID NO:7、8所示引物进行第二轮扩增,得到1号扩增产物,同理,以SEQID NO:3、4所示引物进行第一轮扩增,并以SEQ ID NO:9、10所示引物进行第二轮扩增,得到2号扩增产物;以SEQ ID NO:5、6所示引物进行第一轮扩增,并以SEQ ID NO:11、12所示引物进行第二轮扩增,得到3号扩增产物,进行琼脂糖凝胶电泳,结果如图8所示,左侧第一泳道为DNA marker(条带大小由上至下分别为1000 bp,700 bp,500 bp,400 bp,300 bp,200 bp和100 bp),左数第2-5泳道分别为1~3号第二轮扩增产物以及内参扩增产物,回收各扩增产物,并进行Sanger测序,结果如图9-图14所示,样本检测结果为g.21765_21770 del(p.HV69_70del)、g.G22813T(p.K417N)、g.G23012A(p.E484K)突变。
实施例4
本实施例使用实施例1所述试剂盒及使用方法对已知突变情况的SARS-CoV-2样本进行检测,从而对本发明检测试剂盒及使用方法进行性能验证,验证性能分为四部分:准确度验证、灵敏度与特异性验证、最低检出量验证、重复性验证。
准确度验证结果如表12所示。
表12
灵敏度检测结果如表13所示。
表13
特异性检测结果如表14所示。
表14
最低检出量检测结果如表15所示。
表15
重复性检测结果如表16和表17所示。
表16
表17
综上所述,本发明采用所述引物组合物具备高特异性,能够针对SARS-CoV-2的S蛋白特定区域进行高特异逆转录巢式PCR,本发明利用所述引物组合物行逆转录巢式PCR,并结合Sanger测序,能够快速、准确地获取SARS-CoV-2基因信息,从而能够实现快速检测SARS-CoV-2以及判断SARS-CoV-2突变株,且具备良好的准确性、灵敏度、特异性以及重复性。
申请人声明,本发明通过上述实施例来说明本发明的详细方法,但本发明并不局限于上述详细方法,即不意味着本发明必须依赖上述详细方法才能实施。所属技术领域的技术人员应该明了,对本发明的任何改进,对本发明产品各原料的等效替换及辅助成分的添加、具体方式的选择等,均落在本发明的保护范围和公开范围之内。
SEQUENCE LISTING
<110> 广东凯普生物科技股份有限公司,北京凯普医学检验实验室有限公司,郑州凯普医学检验所(有限合伙),广州凯普医药科技有限公司
<120> 一种检测SARS-CoV-2的引物组合物及其应用
<130> 20210428
<160> 14
<170> PatentIn version 3.3
<210> 1
<211> 26
<212> DNA
<213> 人工序列
<400> 1
cagtgtgtta atcttacaac cagaac 26
<210> 2
<211> 29
<212> DNA
<213> 人工序列
<400> 2
cagactttaa taacaacatt agtagcgtt 29
<210> 3
<211> 22
<212> DNA
<213> 人工序列
<400> 3
gaacaggaag agaatcagca ac 22
<210> 4
<211> 23
<212> DNA
<213> 人工序列
<400> 4
actcagtaag aacacctgtg cct 23
<210> 5
<211> 25
<212> DNA
<213> 人工序列
<400> 5
gtttctgcct ttccaacaat ttggc 25
<210> 6
<211> 22
<212> DNA
<213> 人工序列
<400> 6
ctgcattcag ttgaatcacc ac 22
<210> 7
<211> 24
<212> DNA
<213> 人工序列
<400> 7
tctttcacac gtggtgttta ttac 24
<210> 8
<211> 24
<212> DNA
<213> 人工序列
<400> 8
acaataagta gggactgggt cttc 24
<210> 9
<211> 28
<212> DNA
<213> 人工序列
<400> 9
ctgtgttgct gattattctg tcctatat 28
<210> 10
<211> 24
<212> DNA
<213> 人工序列
<400> 10
aaccattgaa gttgaaattg acac 24
<210> 11
<211> 24
<212> DNA
<213> 人工序列
<400> 11
gacattgctg acactactga tgct 24
<210> 12
<211> 28
<212> DNA
<213> 人工序列
<400> 12
ctggtagaat ttctgtggta acactaat 28
<210> 13
<211> 22
<212> DNA
<213> 人工序列
<400> 13
tcatgaggag tatgcagact ct 22
<210> 14
<211> 21
<212> DNA
<213> 人工序列
<400> 14
tccacatctg tggattcagc a 21
- 一种检测SARS-CoV-2的引物组合物及其应用
- 一种用于检测新型冠状病毒SARS-CoV-2的引物对、探针、组合物、试剂盒及应用
