一种低分子量醛的分离鉴定方法和应用
文献发布时间:2023-06-19 11:35:49
技术领域
本发明涉及分析化学技术领域,特别是涉及一种低分子量醛的分离鉴定方法和应用。
背景技术
乙醛、丙醛和丁醛等低分子量醛是化学工业的重要原料,可用于染色助剂、抗皱整理剂和印花黏合剂等的制备或生产,但这些低分子量醛都具有较强的刺激性,有一定的毒性,残留的少量低分子量醛可通过呼吸或皮肤接触引发呼吸道和皮肤的炎症,产生中毒现象,并存在致敏、致癌和致突变等潜在危害。因此开展低分子量醛残留的检测方法研究,对保障人体健康具有十分重要的现实意义。
低分子量醛在酸性条件下与酚试剂(3-甲基-2-苯并噻唑酮腙盐酸盐,MBTH)反应可生成有色的具有C=N双键的MBTH-醛衍生物,具有Z型和E型两种异构体(见图1),可以采用分光光度法、液相色谱法或液相色谱-串联质谱法等测定。但由于反应条件(如MBTH浓度、反应溶液pH值、反应时间和反应温度等)的差异,导致生成的MBTH-醛衍生物的Z型和E型两种异构体的比例随着反应条件的差异而变化较大。当采用分光光度法测定时,因其不能分离Z型和E型两种异构体,也不能分离MBTH–乙醛衍生物、MBTH–丙醛衍生物和MBTH–丁醛衍生物,测定的是各种低分子量醛的总量,而且灵敏度低,准确度差。高效液相色谱法或液相色谱-串联质谱法具有较好的分离能力,但MBTH-醛衍生物异构体较难分离,如果分离条件稍有不当,就会造成色谱峰的重叠,同时由于分子结构的异构现象,导致质谱裂解获得的碎片离子的峰强度比也存在较大的差异,在质谱MRM法检测时,定量结果的准确度低、重复性差,目前既无MBTH–醛衍生物Z型和E型两种异构体的分离文献报道,也无测定文献报道。因此,很有必要提供一种能够分离鉴定MBTH-醛衍生物的Z型和E型两种异构体的方法。
发明内容
本发明的目的是提供一种能够分离鉴定MBTH-醛衍生物的Z型和E型两种异构体的方法,以解决上述现有技术存在的问题。
为实现上述目的,本发明提供了如下方案:
本发明提供一种低分子量醛的分离鉴定方法,以MBTH溶液为衍生化试剂,将待测物质进行衍生化处理,得到MBTH-醛衍生物,加入碱性溶液调节pH至6~9,过滤,采用液相色谱串联质谱法测定MBTH-醛衍生物的Z型和E型异构体,采用MRM法分别定量,Z型和E型两种异构体的定量结果分别通过各自的标准曲线计算,然后合并Z型和E型两种异构体的量获得乙醛、丙醛、丁醛的总量。
进一步地,所述衍生化处理,包括以下步骤:将待测物置于反应容器中,加入体积浓度为2.0%的磷酸溶液后超声萃取10~15min,离心沉淀后,吸取上清液于一个反应容器中,加入衍生化试剂,所述上清液与所述衍生化试剂的体积比为4:1,摇匀后置于5~35℃水浴中进行衍生化反应5~30min。
进一步地,所述碱性溶液包括氨水、氢氧化钠、碳酸钠、乙二胺或三乙胺中的一种。
进一步地,色谱及质谱条件如下:
色谱柱:C18色谱柱;流动相:A相为酸溶液或碱溶液,B相为乙腈,梯度洗脱程序:0~2min,30%B~85%B;2.0~5.5min,85%B;5.5~6.5min,85%B~30%B;6.5~7.5min,30%B,流速:0.2~0.4mL/min;进样量:10.0~20.0μL;柱温:30~50℃;
电离源:电喷雾正离子模式;离子喷雾电压4.0kV;离子源温度450℃;采集方式:多反应监测正离子模式;雾化器压力50.0psi;辅助气压力50.0psi;气帘气压力35.0psi;碰撞气压力7.0psi;扫描时间50ms;碰撞室出口电压10.0V;碰撞室入口电压10.0V;Q1/Q3离子对、碰撞能量及去簇电压见表1,
表1 6种MBTH-醛衍生物的多反应监测正离子模式质谱参数
注:MBTH:3-甲基-2-苯并噻唑酮腙盐酸盐;(1)定量离子。
进一步地,所述C18色谱柱包括Diamonsil C18,150×2.1mm,2.2μm;PlatisilODS,150×4.6mm,5μm;Xbridge C18柱,100mm×2.1mm,3.5μm;Zorbax SB C18柱,150mm×2.1mm,2.1μm;Shim-pack XR-ODSII柱,150mm×2.0mm,2.2μm或Zorbax Extend-C18柱,150mm×2.1mm,2.1μm中的一种。
进一步地,所述A相包括水、三氟乙酸水溶液、乙酸铵水溶液、乙酸铵-甲酸水溶液或氨水溶液中的一种。
进一步地,所述三氟乙酸的体积浓度为0.1%、0.2%、0.5%、1.0%、1.5%或2.0%。
本发明以改性C18的色谱柱为分离色谱柱,乙腈-0.5%三氟乙酸混合液为流动相,通过液相色谱串联质谱法对乙醛、丙醛和丁醛的MBTH–醛衍生物Z型和E型异构体进行分离鉴定。本发明所述分离检测方法能将乙醛、丙醛和丁醛的MBTH–醛衍生物的Z型和E型异构体进行有效的分离,进而准确的控制纺织品中乙醛、丙醛和丁醛的残留量和纺织产品的质量。本检测方法具有高准确度和高精密度的特性,可用于纺织领域中低分子量醛的检测。
本发明还提供所述的低分子量醛的分离鉴定方法在分离鉴别乙醛、丙醛和丁醛的MBTH衍生物的Z型和E型异构体中的应用。
本发明公开了以下技术效果:
一是解决了Z型和E型的乙醛、丙醛和丁醛-MBTH衍生物异构体的基线分离问题,本发明采用普通C18柱,在乙腈-水的流动相中添加体积浓度为0.5%的三氟乙酸作为流动相改进剂,不但改善了峰形,减轻了色谱峰拖尾的现象,而且大大改善了分离度,使乙醛、丙醛和丁醛的MBTH衍生物的Z型和E型均达到了基线分离。
二是选择了适宜的反应终止剂。在醛与酚试剂反应时,加入了反应终止剂氨水。醛与酚试剂反应需在较强的酸性环境(pH约为1)下进行,而且受反应物浓度、反应温度和反应时间等反应条件的制约,在规定的反应时间内的反应效率可能没有达到100%,存在衍生不完全的问题,如不终止反应,不同时间下测定的溶液的反应效率会存在显著的差异,后测定的溶液的反应效率会比早测定溶液的反应效率高,给乙醛、丙醛和丁醛的定量检测结果带来误差。本发明在反应10min时,加入适量的反应终止剂氨水至反应溶液中,调节pH约为8,终止反应。保证了反应溶液在进入液相色谱分离测定时的反应时间和反应效率的一致性。
三是检测结果更准确和可靠。由于本发明采用液相色谱法分离,串联质谱法测定,使乙醛、丙醛和丁醛的MBTH衍生物的Z型和E型异构体达到了基线分离,并分别采用标准曲线法进行准确定量测定,避免了文献方法报道的Z型和E型异构体同时测定时由于质谱响应强度差异引起的测定误差。
附图说明
为了更清楚地说明本发明实施例或现有技术中的技术方案,下面将对实施例中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本发明的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动性的前提下,还可以根据这些附图获得其他的附图。
图1为低分子量醛在酸性条件下与MBTH反应生成Z型和E型两种异构体的反应过程图;
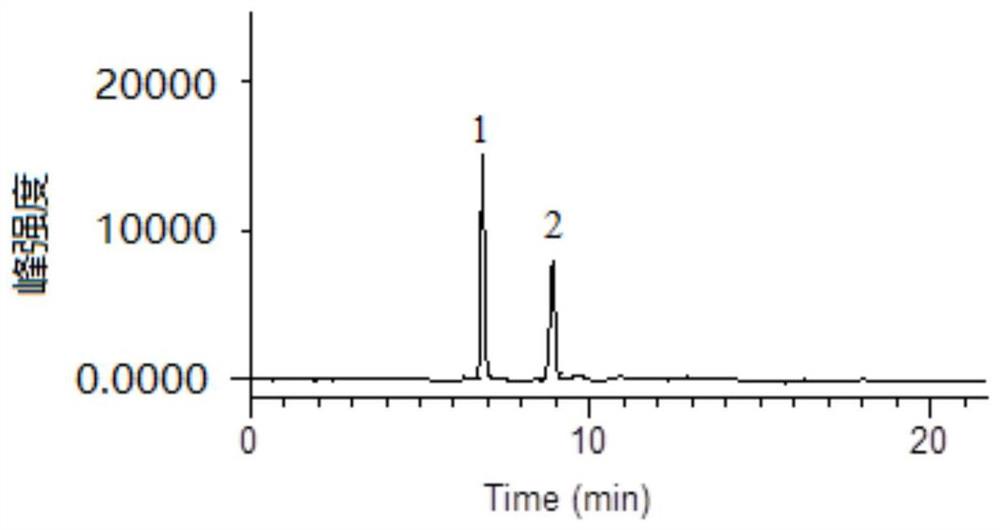
图2为实施例1中MBTH-乙醛衍生物的Z型和E型异构体的MRM图,其中峰1为Z型-MBTH-乙醛衍生物,峰2为E型-MBTH-乙醛衍生物;
图3为实施例1中MBTH-丙醛衍生物的Z型和E型异构体的MRM图,其中峰3为Z型-MBTH-丙醛衍生物,峰4为E型-MBTH-丙醛衍生物;
图4为实施例1中MBTH-丁醛衍生物的Z型和E型异构体的MRM图,其中峰5为Z型-MBTH-丁醛衍生物,峰6为E型-MBTH-丁醛衍生物。
图5为实施例2中MBTH-乙醛衍生物的Z型和E型异构体的MRM图,其中峰1为Z型-MBTH-乙醛衍生物,峰2为E型-MBTH-乙醛衍生物;
图6为实施例2中MBTH-丙醛衍生物的Z型和E型异构体的MRM图,其中峰3为Z型-MBTH-丙醛衍生物,峰4为E型-MBTH-丙醛衍生物;
图7为实施例2中MBTH-丁醛衍生物的Z型和E型异构体的MRM图,其中峰5为Z型-MBTH-丁醛衍生物,峰6为E型-MBTH-丁醛衍生物;
图8为实施例3中MBTH-乙醛衍生物的MRM图,其中峰1为Z型-MBTH-乙醛衍生物,峰2为E型-MBTH-乙醛衍生物;
图9为实施例3中MBTH-丙醛衍生物的MRM图,其中峰3为MBTH-丙醛衍生物;
图10为实施例3中MBTH-丁醛衍生物的MRM图,其中峰4为MBTH-丁醛衍生物;
图11为实施例4中MBTH-乙醛衍生物的MRM图,其中峰1为Z型-MBTH-乙醛衍生物,峰2为E型-MBTH-乙醛衍生物;
图12为实施例4中MBTH-丙醛衍生物的MRM图,其中峰3为MBTH-丙醛衍生物;
图13为实施例4中MBTH-丁醛衍生物的MRM图,其中峰4为MBTH-丁醛衍生物;
图14为实施例5中MBTH-乙醛衍生物的MRM图,其中峰1为Z型-MBTH-乙醛衍生物,峰2为E型-MBTH-乙醛衍生物;
图15为实施例5中MBTH-丙醛衍生物的MRM图,其中峰3为MBTH-丙醛衍生物;
图16为实施例5中MBTH-丁醛衍生物的MRM图,其中峰4为MBTH-丁醛衍生物;
图17为实施例6中MBTH-乙醛衍生物的MRM图,其中峰1为Z型-MBTH-乙醛衍生物,峰2为E型-MBTH-乙醛衍生物;
图18为实施例6中MBTH-丙醛衍生物的MRM图,其中峰3为MBTH-丙醛衍生物;
图19为实施例6中MBTH-丁醛衍生物的MRM图,其中峰4为MBTH-丁醛衍生物;
图20为实施例7中MBTH-醛衍生物的MRM图,其中峰1为Z型-MBTH-乙醛衍生物,峰2为E型-MBTH-乙醛衍生物,峰3为Z型-MBTH-丙醛衍生物,峰4为E型-MBTH-丙醛衍生物,峰5为Z型-MBTH-丁醛衍生物,峰6为E型-MBTH-丁醛衍生物;
图21为实施例8中MBTH-醛衍生物的MRM图,其中峰1为Z型-MBTH-乙醛衍生物,峰2为E型-MBTH-乙醛衍生物,峰3为Z型-MBTH-丙醛衍生物,峰4为E型-MBTH-丙醛衍生物,峰5为Z型-MBTH-丁醛衍生物,峰6为E型-MBTH-丁醛衍生物;
图22为实施例9中MBTH-醛衍生物的MRM图,其中峰1为Z型-MBTH-乙醛衍生物,峰2为E型-MBTH-乙醛衍生物,峰3为Z型-MBTH-丙醛衍生物,峰4为E型-MBTH-丙醛衍生物,峰5为Z型-MBTH-丁醛衍生物,峰6为E型-MBTH-丁醛衍生物;
图23为实施例10中MBTH-醛衍生物的MRM图,其中峰1为Z型-MBTH-乙醛衍生物,峰2为E型-MBTH-乙醛衍生物,峰3为Z型-MBTH-丙醛衍生物,峰4为E型-MBTH-丙醛衍生物,峰5为Z型-MBTH-丁醛衍生物,峰6为E型-MBTH-丁醛衍生物;
图24为实施例11中MBTH-醛衍生物的MRM图,其中峰1为Z型-MBTH-乙醛衍生物,峰2为E型-MBTH-乙醛衍生物,峰3为Z型-MBTH-丙醛衍生物,峰4为E型-MBTH-丙醛衍生物,峰5为Z型-MBTH-丁醛衍生物,峰6为E型-MBTH-丁醛衍生物;
图25为实施例12中MBTH-醛衍生物的MRM图,其中峰1为Z型-MBTH-乙醛衍生物,峰2为E型-MBTH-乙醛衍生物,峰3为Z型-MBTH-丙醛衍生物,峰4为E型-MBTH-丙醛衍生物,峰5为Z型-MBTH-丁醛衍生物,峰6为E型-MBTH-丁醛衍生物;
图26为实施例13中MBTH-醛衍生物的MRM图,其中峰1为Z型-MBTH-乙醛衍生物,峰2为E型-MBTH-乙醛衍生物,峰3为Z型-MBTH-丙醛衍生物,峰4为E型-MBTH-丙醛衍生物,峰5为Z型-MBTH-丁醛衍生物,峰6为E型-MBTH-丁醛衍生物;
图27为实施例14中MBTH-醛衍生物的MRM图,其中峰1为Z型-MBTH-乙醛衍生物,峰2为E型-MBTH-乙醛衍生物,峰3为Z型-MBTH-丙醛衍生物,峰4为E型-MBTH-丙醛衍生物,峰5为Z型-MBTH-丁醛衍生物,峰6为E型-MBTH-丁醛衍生物;
图28为实施例15中MBTH-醛衍生物的MRM图,其中峰1为Z型-MBTH-乙醛衍生物,峰2为E型-MBTH-乙醛衍生物,峰3为Z型-MBTH-丙醛衍生物,峰4为E型-MBTH-丙醛衍生物,峰5为Z型-MBTH-丁醛衍生物,峰6为E型-MBTH-丁醛衍生物;
图29为实施例16-19中不同反应终止剂对乙醛、丙醛和丁醛的衍生物的质谱测定基质效应的影响;
图30为实施例28-34中衍生化反应时间对乙醛、丙醛和丁醛的衍生化效率的影响;
图31为实施例35-37中衍生化反应温度对乙醛、丙醛和丁醛的衍生化效率的影响;
图32为实施例1中放置时间对乙醛、丙醛和丁醛的衍生化反应产物稳定性的影响。
具体实施方式
现详细说明本发明的多种示例性实施方式,该详细说明不应认为是对本发明的限制,而应理解为是对本发明的某些方面、特性和实施方案的更详细的描述。
应理解本发明中所述的术语仅仅是为描述特别的实施方式,并非用于限制本发明。另外,对于本发明中的数值范围,应理解为还具体公开了该范围的上限和下限之间的每个中间值。在任何陈述值或陈述范围内的中间值以及任何其他陈述值或在所述范围内的中间值之间的每个较小的范围也包括在本发明内。这些较小范围的上限和下限可独立地包括或排除在范围内。
除非另有说明,否则本文使用的所有技术和科学术语具有本发明所述领域的常规技术人员通常理解的相同含义。虽然本发明仅描述了优选的方法和材料,但是在本发明的实施或测试中也可以使用与本文所述相似或等同的任何方法和材料。本说明书中提到的所有文献通过引用并入,用以公开和描述与所述文献相关的方法和/或材料。在与任何并入的文献冲突时,以本说明书的内容为准。
在不背离本发明的范围或精神的情况下,可对本发明说明书的具体实施方式做多种改进和变化,这对本领域技术人员而言是显而易见的。由本发明的说明书得到的其他实施方式对技术人员而言是显而易见得的。本发明说明书和实施例仅是示例性的。
关于本文中所使用的“包含”、“包括”、“具有”、“含有”等等,均为开放性的用语,即意指包含但不限于。
本发明中AB SCIEX 4500系列三重四极杆串联质谱仪(美国AB SCIEX公司)和Analyst 1.6.2数据处理系统,UltiMate3000标准型液相色谱仪(美国DIONEX公司);SHZ-88B水浴恒温振荡器(太仓文尔惠金仪器),DQS-200E超声波清洗器(昆山市超声仪器有限公司),XE240梅特勒-托利多万分之一电子分析天平(瑞士梅特勒-托利多公司)。Milli-Q纯水系统(美国Millipore公司);具塞刻度试管(10mL)。
甲醇、三氟乙酸、三乙胺、乙腈(色谱纯)购于德国Merck公司,盐酸和氨水(优级纯)购于上海国药试剂集团公司。乙醛、丙醛和丁醛标准溶液(1.00mg/mL)购自Chem Service公司,Z型和E型的乙醛、丙醛和丁醛的MBTH衍生物标准贮备液(1.00mg/mL,以醛计)。
溶液的配制过程如下:
乙醛、丙醛和丁醛混合标准溶液(10.0mg/L):分别准确吸取1.00mL的甲醛、乙醛和丙醛标准贮备液(1.00mg/mL)于一个100mL容量瓶中,用水稀释并定容至刻度。
Z型和E型的乙醛、丙醛和丁醛的MBTH衍生物混合标准溶液(10.0mg/L,以醛计):准确吸取1.00mL的乙醛、丙醛和丁醛的MBTH衍生物标准贮备液(1.00mg/mL)于一个100mL容量瓶中,用水稀释并定容至刻度。
MBTH溶液(1.0g/L):准确称取0.10g酚试剂用水溶解后加入10mL浓盐酸,并用水定容至100mL,储存于棕色容器中,在4℃冰箱内冷藏保存。
MBTH溶液(10.0mg/L):取10.0mL酚试剂溶液于一个1000mL容量瓶中,然后加入100mL水后加入10mL浓盐酸,再用水稀释并定容至刻度。
标准溶液系列的配制:分别移取适量的Z型和E型的乙醛、丙醛和丁醛的MBTH衍生物混合标准溶液(10.0mg/L,以醛计)于7个10mL容量瓶中,配成浓度分别相当于乙醛、丙醛和丁醛为1.0μg/L、2.0μg/L、5.0μg/L、10.0μg/L、50.0μg/L、100.0μg/L和200.0μg/L的标准系列溶液。
实施例1
准确称取1.0g剪碎的纺织品样品于50mL具塞比色管中,加入体积浓度为2.0%的磷酸溶液10mL后超声萃取10min。离心沉淀后,吸取上清液4.0mL于一个10mL具塞比色管中,加入1.0mL的MBTH溶液(10.0mg/L)作为衍生化试剂,摇匀后置于15℃水浴中进行衍生化反应10.0min,然后加入体积浓度为5%的氨水调节pH至8.0,用蒸馏水稀释至刻度,用0.22μm水相微孔滤膜过滤,吸取10μL进样分析。试样在C18色谱柱上,采用乙腈-0.5%三氟乙酸水溶液为流动相,进行梯度洗脱,然后采用串联质谱法测定MBTH-醛衍生物的Z型和E型异构体,采用MRM法分别定量,Z型和E型两种异构体的定量结果分别通过各自的标准曲线计算,然后合并Z型和E型两种异构体的量获得乙醛、丙醛、丁醛的总量。色谱质谱条件如下:
色谱柱:Diamonsil C18(150×2.1mm,2.2μm);流动相:A相为0.5%(V/V)三氟乙酸水溶液,B相为乙腈。梯度洗脱程序:0~2min,30%B~85%B;2.0~5.5min,85%B;5.5~6.5min,85%B~30%B;6.5~7.5min,30%B。流速:0.35mL/min;进样量:10.0μL;柱温:40℃。
电离源:电喷雾正离子模式;离子喷雾电压4.0kV;离子源温度450℃;采集方式:多反应监测(multi-reaction monitoring,MRM)正离子模式;雾化器压力50.0psi;辅助气压力50.0psi;气帘气压力35.0psi;碰撞气压力7.0psi;扫描时间50ms;碰撞室出口电压10.0V;碰撞室入口电压10.0V。碰撞室入口电压:10.0V;Q1/Q3离子对、碰撞能量及去簇电压见表1。
表1 6种MBTH-醛衍生物的多反应监测正离子模式质谱参数
注:MBTH:3-甲基-2-苯并噻唑酮腙盐酸盐;(1)定量离子
本实施例的乙醛、丙醛和丁醛的Z型的检出限均为0.05μg/kg,E型异构体检出限均为0.07μg/kg,Z型的定量限均为0.2μg/kg,E型异构体定量限均为0.3μg/kg。本实施例的乙醛、丙醛和丁醛的平均回收率分别为93.4%、93.5%和93.6%。不分离法的乙醛、丙醛和丁醛的平均回收率分别为87.7%、89.7%和87.4%,本发明的乙醛、丙醛和丁醛的平均精密度分别为4.8%、5.1%和5.8%,不分离法的乙醛、丙醛和丁醛的平均精密度分别为4.8%、5.3%和6.8%。
实施例2
同实施例1,不同之处仅在于色谱柱为Platisil ODS(150×4.6mm,5μm)。
实施例3
同实施例1,不同之处仅在于色谱柱为Xbridge C18柱(100mm×2.1mm,3.5μm)。
实施例4
同实施例1,不同之处仅在于色谱柱为Zorbax SB C18柱(150mm×2.1mm,2.1μm),
实施例5
同实施例1,不同之处仅在于色谱柱为Shim-pack XR-ODSII柱(150mm×2.0mm,2.2μm)。
实施例6
同实施例1,不同之处仅在于色谱柱为Zorbax Extend-C18柱(150mm×2.1mm,2.1μm)。
上述实施例不同色谱柱条件下的分离鉴定结果见图5~图19。乙醛、丙醛和丁醛的MBTH衍生物的Z型和E型异构体在Diamonsil C18(150×2.1mm,2.2μm)柱上能获得较好的基线分离,在Platisil ODS上丁醛的异构体色谱峰重叠,在Xbridge C18柱(100mm×2.1mm,3.5μm)、Zorbax SB C18柱(150mm×2.1mm,2.1μm)、Shim-pack XR-ODSII柱(150mm×2.0mm,2.2μm)和Zorbax Extend-C18柱(150mm×2.1mm,2.1μm)上丙醛和丁醛的异构体色谱峰重叠。在本发明的方法中Diamonsil C18柱(150×2.1mm,2.2μm)作为最优分析柱。实施例1中乙醛、丙醛和丁醛的酚试剂衍生物的分离色谱图如图2~4所示。
实施例7
同实施例1,不同之处仅在于流动相为乙腈-水。
实施例8
同实施例1,不同之处仅在于流动相为乙腈-5mmol/L乙酸铵水溶液。
实施例9
同实施例1,不同之处仅在于流动相为乙腈-5mmol/L乙酸铵-0.1%甲酸水溶液。
实施例10
同实施例1,不同之处仅在于流动相为乙腈-0.5%氨水溶液。
实施例11
同实施例1,不同之处仅在于流动相中三氟乙酸的体积浓度为0.1%。
实施例12
同实施例1,不同之处仅在于流动相中三氟乙酸的体积浓度为0.2%。
实施例13
同实施例1,不同之处仅在于流动相中三氟乙酸的体积浓度为1.0%。
实施例14
同实施例1,不同之处仅在于流动相中三氟乙酸的体积浓度为1.5%。
实施例15
同实施例1,不同之处仅在于流动相中三氟乙酸的体积浓度为2.0%。
不同流动相改进剂的分离鉴定效果见图20~图28。本发明验证了碱性的氨水、三乙胺和酸性的甲酸、乙酸和三氟乙酸以及乙酸铵的分离鉴定效果。结果表明,加入氨水、三乙胺和乙酸铵后,各异构体之间的分离度反而下降,甲酸和乙酸均提高分离的效果,但没有三氟乙酸明显。故在本发明的方法中三氟乙酸作为最优流动相改性剂。
不同流动相的分离鉴定效果见图20~图28。本发明验证了不同品种的流动相对乙醛、丙醛和丁醛的MBTH衍生物的Z型和E型异构体的色谱分离的影响,本发明主要对5种流动相进行了试验(乙腈-水、乙腈-0.5%三氟乙酸水溶液、乙腈-5mmol/L乙酸铵水溶液、乙腈-5mmol/L乙酸铵-0.1%甲酸水溶液、乙腈-0.5%氨水溶液)。由上述实施例可知,对于本发明针对的乙醛、丙醛和丁醛的MBTH衍生物的Z型和E型异构体而言,这5种流动相只有乙腈-0.5%三氟乙酸水溶液在选择适宜的梯度后能获得较好的Z型和E型异构体的基线分离,并且具有较好的质谱响应灵敏度,乙腈-0.5%三氟乙酸水溶液总体效果更佳。
不同的三氟乙酸浓度(0.1%、0.2%、0.5%、1.0%、1.5%和2.0%)对乙醛、丙醛和丁醛的MBTH衍生物的Z型和E型异构体分离度的影响结果见图2~图4和图24~图28。结果表明,0.5%的三氟乙酸的分离度最好,而且灵敏度适中。0.1%和0.2%的三氟乙酸,无法达到基线分离。1.0%、1.5%和2.0%的三氟乙酸,会引起质谱响应灵敏度的降低,相比0.5%的三氟乙酸的质谱灵敏度,灵敏度分别降低10.3%、15.8%和38.2%。
实施例16
同实施例1,不同之处仅在于加入1.0mol/L氢氧化钠调节pH。
实施例17
同实施例1,不同之处仅在于加入质量浓度为5%的碳酸钠溶液调节pH。
实施例18
同实施例1,不同之处仅在于加入体积浓度为5%的乙二胺水溶液调节pH。
实施例19
同实施例1,不同之处仅在于加入体积浓度为5%的三乙胺水溶液调节pH。
酚试剂与低分子量醛反应须在较强的酸性条件下(pH<2)才能较好地快速反应,改变溶液的酸度可以改变反应速度。本发明验证了不同品种的碱性物质作为反应终止剂,如体积浓度为5%的氨水、1.0mol/L氢氧化钠、质量浓度为5%的碳酸钠溶液、体积浓度为5%的乙二胺溶液或体积浓度为5%的三乙胺溶液,分别考察了它们与酚试剂的互溶性、操作的便捷性及质谱检测的匹配性等,不同反应终止剂的基质效应结果见图29。结果表明,上述5种碱性物质均能终止衍生化反应,但氢氧化钠由于碱性较强,采用浓溶液加入,在量上不易控制,且过量后易产生溶液的混浊,主要原因是氢氧化钠的碱性太强,而且由于钠盐的不挥发性,容易造成液相色谱和质谱的管路和离子源的堵塞。碳酸钠尽管靠气泡就可容易判断终点,加入量也容易掌握,但因钠盐的不挥发性,易致管路和离子源堵塞的局限。乙二胺、三乙胺的碱性适中,与酚试剂也互溶,但反应物中多余的乙二胺或三乙胺存在一定的基质效应,使醛-MBTH衍生物的质谱响应灵敏度受到制约。氨水的碱性适中,与酚试剂溶液中的盐酸反应生成高温下易挥发的氯化铵,并且没有基质效应,又容易获得,价格低廉。本发明的方法中体积浓度为5%的氨水为最优反应终止剂。
实施例20
同实施例1,不同之处仅在于调节pH至1.0。
实施例21
同实施例1,不同之处仅在于调节pH至2.0。
实施例22
同实施例1,不同之处仅在于调节pH至3.0。
实施例23
同实施例1,不同之处仅在于调节pH至4.0。
实施例24
同实施例1,不同之处仅在于调节pH至5.0。
实施例25
同实施例1,不同之处仅在于调节pH至6.0。
实施例26
同实施例1,不同之处仅在于调节pH至7.0。
实施例27
同实施例1,不同之处仅在于调节pH至9.0。
准确吸取MBTH溶液(1.0mg/L)5mL于7个50mL具塞试管中,分别加入不同量的5%氨水,调节溶液的pH值为1.0、2.0、3.0、4.0、5.0、6.0、7.0、8.0、9.0(即实施例1、20~27),然后加入100ng的乙醛、丙醛和丁醛,反应10min后采用液相色谱串联质谱法测定生成的6种醛-MBTH衍生物及其异构体的峰高,结果见表2。由表2可知,不同pH值下各衍生物的峰高随着pH值的增大而峰高降低,当pH=8.0时,峰高接近于0。结果表明,当pH值=8.0时,乙醛、丙醛和丁醛与酚试剂几乎不反应,本发明选择pH=8.0为溶液终止反应的pH值,也即加入氨水调节至pH=8.0。
表2不同pH值下的MBTH-醛衍生物的MRM色谱峰高(n=3)
实施例28
同实施例1,不同之处仅在于衍生化时间为1.0min。
实施例29
同实施例1,不同之处仅在于衍生化时间为5.0min。
实施例30
同实施例1,不同之处仅在于衍生化时间为15.0min。
实施例31
同实施例1,不同之处仅在于衍生化时间为20.0min。
实施例32
同实施例1,不同之处仅在于衍生化时间为30.0min。
实施例33
同实施例1,不同之处仅在于衍生化时间为45.0min。
实施例34
同实施例1,不同之处仅在于衍生化时间为60.0min。
采用5.0mL的1.0mg/L的酚试剂溶液对5.0mL浓度为20.0μg/L的乙醛、丙醛和丁醛进行衍生化反应,在不同衍生化时间(1.0、5.0、10.0、15.0、20.0、30.0、45.0、60.0min,即实施例1、28~34)测定其衍生化反应的效率,结果见图30。结果表明,乙醛、丙醛和丁醛与酚试剂的衍生化反应,在适宜的条件下能在10.0min内达到95%以上。
实施例35
同实施例1,不同之处仅在于衍生化温度为5℃。
实施例36
同实施例1,不同之处仅在于衍生化温度为25℃。
实施例37
同实施例1,不同之处仅在于衍生化温度为35℃。
测定不同衍生化温度(5、15、25、35℃,即实施例1、35~37)对乙醛、丙烯和丁醛衍生化效率的影响,结果见图31。结果表明,在pH=1的溶液中,温度越高衍生化反应越快,5℃时的衍生化反应相对较慢,在15℃时,衍生化反应能在10min达到90%以上。
验证例1MBTH-醛衍生物的稳定性
乙醛、丙醛和丁醛与酚试剂衍生完成后,衍生物的稳定性直接影响测定结果的准确性。本发明验证了在室温下放置不同时间(0、1、3、6、12、24、36、72h)对实施例1制备的乙醛、丙醛和丁醛的MBTH-醛衍生物稳定性的影响,结果见图32。结果表明,室温下,乙醛、丙醛和丁醛的MBTH-醛衍生物在放置72h后,其测定结果没有变化。表明MBTH-醛衍生物在本发明条件下可保持至少72h内稳定。
验证例2线性范围、检出限及定量限
采用实施例1的Z型和E型的乙醛、丙醛和丁醛的MBTH衍生物混合标准溶液(10.0mg/L,以醛计),以乙腈为溶剂,配制一系列标准工作溶液。使得乙醛、丙醛和丁醛的浓度范围为0.1~100μg/L(0.1,0.2,0.5,1.0,5.0,10.0,50.0和100.0μg/L)。在实施例1的仪器条件下进样检测。以样品浓度为横坐标、仪器响应值为纵坐标绘制标准工作曲线,外标法定量。结果如表3所示,乙醛、丙醛和丁醛在各自的测定范围内线性关系良好(r≥0.9990),以信噪比S/N=3计算方法检出限,S/N=10计算定量限,得乙醛、丙醛和丁醛的方法检出限为0.05~0.07μg/kg,其方法定量限为0.2~0.3μg/kg。
表3线性方程、相关系数、线性范围、检出限和定量限
验证例3方法的精密度和准确度
在MBTH溶液(1.0mg/L)中添加不同量的乙醛、丙醛和丁醛标准贮备液,配制成低、中、高3个浓度(分别为0.2、5.0、80.0μg/L)的质量控制(QC)样品,分别采用本发明方法和异构体色谱峰重叠的液质联用法进行6次的重复测定,计算其回收率和精密度。本发明的测定结果以2个异构体的测定量的和计算。结果表明,本发明的回收率在90.0~98.4%,不分离法的回收率在82.5~93.2%,本发明的精密度3.5~7.6%,不分离法的精密度3.4~9.0%。结果见表4。
表4加标回收率和精密度试验结果(n=3)
*不分离法是指异构体不进行色谱基线分离的液相色谱-串联质谱法,即异构体色谱峰重叠的液相色谱-串联质谱法。色谱柱为Shim-pack XR-ODS II(100mm×2.0mm,2.5μm);流动相A相为水,B相为甲醇;梯度洗脱程序为:0-2min,35%B-90%B,2.0-5.5min,90%B,5.5-6.5min,90%B-35%B,6.5-7.5min,35%B;洗脱流速度为0.3mL/min;柱温为40℃。
以上所述的实施例仅是对本发明的优选方式进行描述,并非对本发明的范围进行限定,在不脱离本发明设计精神的前提下,本领域普通技术人员对本发明的技术方案做出的各种变形和改进,均应落入本发明权利要求书确定的保护范围内。
- 一种低分子量醛的分离鉴定方法和应用
- 一种超高分子量、低蠕变聚乙烯纤维的制备方法及应用
