利用酪氨酸激酶抑制剂的组合物和方法
文献发布时间:2023-06-19 12:14:58
本申请是分案申请,原申请的申请日为2016年1月26日,申请号为201680018121.6,发明名称为“利用酪氨酸激酶抑制剂的组合物和方法”。
相关申请的交叉引用
本申请要求2015年11月3日提交的美国临时申请序列号62/250,052和2015年1月26日提交的美国临时申请序列号62/107,553的优先权,其内容以其全部通过引用并入本文。
关于联邦资助研究或进展的声明
本发明是利用国家卫生研究院(National Institute of Health)授予的GM099801下的政府支持进行的。政府对发明有一定的权利。
技术领域
本申请涉及利用酪氨酸激酶抑制剂的组合物和方法。
背景技术
心血管疾病是全世界男性和女性死亡的主要原因,尽管有重大进展。根据世界卫生组织(WHO)的报告,估计到2030年每年有2360万人将死于心血管疾病。
RAS-MAPK途径对人类生长发育至关重要。该信号级联的不同步骤的异常导致神经-心脏-面部-皮肤综合征、或RASopathies,一组具有重叠但不同表型的病症。RASopathy患者具有不同程度的智力障碍、生长不良、相对大头、外胚层异常、畸形特征以及某些恶性肿瘤的风险增加。许多RASopathy存在显著的基因座异质性。
先天性心脏病(CHD)是新生儿中发现的最常见的缺陷,发生在约1%的活产(livebirth)中。在美国有超过一百万人患有某种形式的CHD,其中大多数人需要持续监测和治疗以防止心脏功能的恶化。AVCD包括房室瓣和心房和心室隔膜的不同异常。在完整的形式中,发现单一的共同房室瓣和房间隔缺损(原中隔口)与室隔入口部分的后室间隔缺损融合。在部分形式中,有两个独立的右和左房室瓣,具有二尖瓣瓣裂、房间隔缺损(原中隔口)和无室间隔通讯。二尖瓣瓣裂被认为是较不严重的AVCD形式。AVCD也是唐氏综合征儿童中最常见的CHD,也是与染色体和孟德尔病症背景中的心外异常最常相关的结构性心脏缺陷之一。在与NS相关的AVCD中发现了独特的解剖特征。事实上,一般而言,由于附属纤维组织和/或二尖瓣与左心室异常乳头肌的异常插入,这种缺陷具有部分类型,最终与主动脉下狭窄有关。
先天性心脏病(CHD)发生在约60-86%的受RASopathy——具有RAS-MAPK途径中异常的一组病症——影响的患者。肺动脉瓣狭窄(PVS)和肥大性心肌病是显示与RASopathies有明显关联的最常见缺陷。具有多发性着色斑的诺南综合征(Noonan sydrome)(NSML)中CHD谱(spectrum)较宽,并且房室管缺损(AVCD)家族是第三常见的心脏缺陷。
大多数患有心血管疾病和RASopathy相关的先天性心脏病的患者需要治疗多年。特别是RASopathy相关的先天性心脏病通常与低死亡率相关。因此,存在以对心脏病具有最大效果的低风险疗法治疗患者中的心血管疾病的需要。
发明内容
如下所述,本发明包括异常地抑制蛋白质酪氨酸磷酸化如Src家族酪氨酸激酶及其底物的磷酸化的组合物和方法。
一方面,本发明包括治疗受试者中具有异常蛋白质酪氨酸磷酸化的心血管疾病或状况的方法,包括向需要其的受试者施用低剂量的酪氨酸激酶抑制剂,其中所述酪氨酸激酶抑制剂在受试者中降低酪氨酸磷酸化的异常水平并改善至少一种心脏功能。
另一方面,本发明包括治疗先天性心脏病的方法,包括向需要其的受试者施用低剂量的酪氨酸激酶抑制剂,其中所述酪氨酸激酶抑制剂在受试者中降低酪氨酸磷酸化的异常水平并改善至少一种心脏功能。
再一方面,本发明包括治疗与具有异常蛋白质酪氨酸磷酸化的RASopathy相关的心血管疾病或状况的方法,包括向需要其的受试者施用低剂量的酪氨酸激酶抑制剂,其中所述酪氨酸激酶抑制剂在受试者中降低酪氨酸磷酸化的异常水平并改善至少一种心脏功能。
又一方面,本发明包括包含低剂量酪氨酸激酶抑制剂的组合物,其中所述低剂量酪氨酸激酶抑制剂能够在需要其的受试者中减少酪氨酸磷酸化并改善至少一种心脏功能。
另一方面,本发明包括药物组合物,其包含如本文所述的组合物和药学上可接受的载体。
再一方面,本发明包括如本文所述的组合物在制备用于治疗受试者中的心血管疾病或状况的药物中的用途。
在本文描述的本发明的上述方面或任何其它方面的各种实施方式中,先天性心脏病与RASopathy相关,如选自以下的RASopathy:神经纤维瘤病1型、诺南综合征、具有多发性着色斑的诺南综合征(豹斑综合征(Leopard syndrome))、毛细血管畸形-动静脉畸形综合征、克斯提洛氏弹性蛋白缺陷症(Costello综合征)、心脏-面部-皮肤综合征和Legius综合征。在一个实施方式中,心血管疾病或状况是先天性心脏病。
在另一个实施方式中,低剂量在酪氨酸激酶抑制剂的化学治疗剂量的约1/250至约1/175(about 175 fold to about 250 fold lower than)的范围内。
在另一个实施方式中,心脏功能选自肌原纤维组构(organization)、心肌细胞收缩性、SERCA2A表达和心脏纤维化。
在另一个实施方式中,酪氨酸激酶抑制剂选自阿法替尼、阿西替尼、伯舒替尼、卡博替尼、西地尼布、色瑞替尼、克唑替尼、达拉非尼、达沙替尼、厄洛替尼、依维莫司、吉非替尼、依鲁替尼、伊马替尼、拉帕替尼、乐伐替尼、来他替尼(lestaurtinib)、尼洛替尼、尼达尼布、帕博西尼、帕唑帕尼、帕纳替尼、瑞格非尼(regorafenib)、鲁索替尼(ruxolitinib)、塞马纳尼(semananib)、西罗莫司、索拉非尼、舒尼替尼、替西罗莫司、托法替尼、曲美替尼、凡德他尼和威罗菲尼。在再一个实施方式中,酪氨酸激酶抑制剂是Src家族酪氨酸激酶抑制剂,如选自下列的Src家族酪氨酸激酶抑制剂:A419259、AP23451、AP23464、AP23485、AP23588、AZD0424、AZM475271、BMS354825、CGP77675、CU201、ENMD 2076、KB SRC 4、KX2361、KX2-391、MLR 1023、MNS、PCI-32765、PD166285、PD180970、PKC-412、PKI166、PP1、PP2、SRN004、SU6656、TC-S7003、TG100435、TG100948、TX-1123、VAL 201、WH-4-023、XL 228、细格菌素、博舒替尼、虎刺醛、达沙替尼、除草霉素A、靛玉红、来那替尼(neratinib)、薰草菌素A、培利替尼(pelitinib)、白皮杉醇(四羟反式茋,piceatannol)、塞卡替尼(saracatinib)、SrcI1及其类似物。
在另一个实施方式中,受试者是儿科患者,如小于12岁的儿科受试者。在再一个实施方式中,受试者大于18岁。
在另一个实施方式中,酪氨酸磷酸化的异常水平包括酪氨酸磷酸化P0相关蛋白(P0蛋白相关,Protein Zero-Related)(PZR)的异常水平。在这样的实施方式中,低剂量酪氨酸激酶抑制剂降低PZR酪氨酸磷酸化。在再一个实施方式中,低剂量酪氨酸激酶抑制剂在心脏组织中向受试者提供抗纤维化作用。在又一个实施方式中,低剂量酪氨酸激酶抑制剂降低跨膜糖蛋白,如跨膜糖蛋白P0相关蛋白(PZR)的异常酪氨酸磷酸化。在另一个实施方式中,低剂量酪氨酸激酶抑制剂在心脏组织中提供抗纤维化作用。
附图说明
当结合附图阅读时,将更好地理解本发明的优选实施方式的以下详细描述。为了说明本发明的目的,在附图中示出了目前优选的实施方式。然而,应当理解,本发明不限于附图中所示的实施方式的精确排列和手段。
图1A是Ptpn11
图1B是显示野生型和Ptpn11
图1C是差异性高酪氨酰磷酸化肽的热图(磷酸化位点由括号中的MS鉴定)。
图1D是通过差异蛋白质组学的含酪氨酸242(上图)和酪氨酸264(下图)的PZR的提取的离子色谱图和肽序列的一组图像。
图1E显示不同脊椎动物中P0相关蛋白(PZR)C末端的氨基酸序列。基于免疫受体酪氨酸的抑制基序的共有序列(ITIM;S/I/V/LXYXXI/V/L)用黑体字表示,酪氨酸残基用适当的氨基酸编号标记为红色。序列显示为来自智人(homo sapiens)、小家鼠、褐鼠(rattusnorvegicus)、欧洲牛(Bos taurus)、家犬(Canis lupus familiaris)、鮐、原鸡的PZR C末端。
图2A是显示PZR酪氨酰磷酸化表征的一组印迹。用空载体或活化的谷胱甘肽S-转移酶(GST)-Shp2E76A和空载体(载体)、野生型人PZR(WT)或在酪氨酸241(Y241F)、酪氨酸263(Y263F)或两者(2YF)处突变的PZR共转染C2C12细胞。细胞裂解物用抗pPZR(Y241或Y263)、抗PZR或抗Shp2抗体进行免疫印迹。
图2B是显示PZR酪氨酰磷酸化表征的一组印迹。用空载体(Vec)或活化的Shp2E76A和空载体(载体)、野生型斑马鱼PZR(WT)或在酪氨酸236(Y241F)、酪氨酸258(Y263F)或二者(2YF)处突变的PZR共转染HEK-293细胞。细胞裂解物用抗pPZR(Y241或Y263)、PZR或Shp2抗体进行免疫印迹。使用ERK1/2作为加载对照。
图2C是显示PZR酪氨酰磷酸化表征的一组印迹。用表达作为对照的GFP、野生型Shp2或Shp2E76A的腺病毒感染HUVEC。细胞裂解物用抗pPZR(Y241或Y263)、抗总PZR和抗Shp2抗体进行免疫印迹。
图2D是显示PZR酪氨酰磷酸化表征的一组印迹。用空载体、野生型Shp2(WT)或指示的Shp2突变体(活化的Shp2,E76A;诺南综合征(NS)突变体,N308D;或具有多发性着色斑的诺南综合征(NSML)突变体,Y279C和T468M)瞬时转染HEK-293细胞。细胞裂解物用抗pPZR(Y241或Y263)、抗PZR和抗Shp2抗体进行免疫印迹。使用ERK1/2作为加载对照。
图2E是显示PZR酪氨酰磷酸化表征的一组印迹。用HA标记的斑马鱼PZR和空载体、野生型Shp2、Shp2D61G(NS突变体)或Shp2A462T(NSML突变体)转染HEK-293T细胞。细胞裂解物用抗HA抗体进行免疫沉淀,免疫复合物用抗Shp2和抗HA抗体进行免疫印迹。全细胞裂解物(WCL)用抗pPZR(Y241和Y263)、抗Shp2和抗HA抗体印迹。
图3A显示Ptpn11
图3B显示Ptpn11
图3C显示Ptpn11
图3D显示Ptpn11
图4A显示Ptpn11
图4B是显示Ptpn11
图4C是Ptpn11
图5A是显示Ptpn11
图5B是显示Ptpn11
图5C是显示Ptpn11
图5D是显示Ptpn11
图6A是显示Src家族激酶对PZR Y241和Y263磷酸化的影响的一组印迹。HEK-293细胞用指示的Shp2突变体瞬时转染,并用二甲基亚砜(DMSO)作为对照或5μM SU6656处理。细胞裂解物用抗Shp2、pSrc(Y416)、Src、pPZR(Y241或Y263)和总PZR抗体免疫印迹。使用ERK1/2作为加载对照。
图6B是显示Src家族激酶对PZR Y241和Y263磷酸化的影响的一组印迹。在指示浓度的DMSO、PP2或SU6656存在下,用表达作为对照的GFP或组成型活性Shp2E76A的腺病毒感染NIH 3T3细胞。细胞裂解物用抗Shp2、pSrc(Y416)、Src、pPZR(Y241或Y263)和总PZR抗体免疫印迹。ERK1/2用作加载对照。
图7A是显示Src激酶介导NS-或NSML-Shp2诱导的PZR高酪氨酰磷酸化的印迹。用表达GFP或Shp2E76A的腺病毒感染SYF细胞(Src
图7B是显示Src激酶介导NS-或NSML-Shp2诱导的PZR高酪氨酰磷酸化的印迹。SYF细胞用野生型c-Src或激酶死(激酶失活,kinase dead)c-SrcK295R/Y527F(KR/YF)瞬时转染,并用表达GFP、野生型Shp2或Shp2E76A的腺病毒感染。细胞裂解物用抗Shp2、pSrc(Y416)、pPZR(Y241或Y263)、PZR和Src抗体免疫印迹。ERK1/2用作加载对照。
图7C是显示Src激酶诱导PZR高酪氨酰磷酸化的印迹。用加Flag标记的人PZR转染HEK-293细胞。细胞裂解物用抗Flag抗体免疫沉淀。免疫沉淀物用Src重组蛋白进行体外Src激酶测定。反应产物用抗pPZR(Y241或Y263)抗体免疫印迹。
图7D是显示Src家族激酶诱导PZR高酪氨酰磷酸化的印迹。用组成型活性Src突变体和加HA标记的野生型斑马鱼PZR(WT)、在酪氨酸236(Y241F)、酪氨酸258(Y263F)或两者(2YF)处突变的PZR共转染FIEK-293细胞。细胞裂解物用抗pPZR(Y241或Y263)和HA抗体免疫印迹。
图8A是显示具有NS/NSML相关的Shp2突变体的增强的Src复合物形成的印迹和图。用Shp2 WT和指示的Shp2突变体瞬时转染HEK-293细胞。细胞裂解物用抗c-Src抗体免疫沉淀(IP),免疫复合物用抗Shp2和抗Src抗体免疫印迹(IB)。该图表示来自三个独立实验的密度分析的平均值±SEM。统计显著性使用比较Shp2突变体与WT的邓奈特检验得出。*,P<0.05;**,P<0.01。
图8B是显示具有NS/NSML相关的Shp2突变体和PZR的增强的Src复合物形成的印迹的图像。用Shp2 WT或E76A或Y279C突变体和空载体(载体)、WT人PZR或PZR 2YF突变体共转染HEK-293细胞。细胞裂解物用抗pPZR(Y241或Y263)或Shp2抗体免疫印迹。ERK1/2用作加载对照。免疫复合物用抗Src、抗Shp2和抗PZR抗体免疫印迹。
图9是NS和NSML突变体对PZR酪氨酰磷酸化的影响的模型的图解。
图10是显示达沙替尼给药剂量的一组图像。雄性Ptpn11D61G/+小鼠腹腔注射以指示剂量的达沙替尼或DMSO对照,24小时后处死小鼠,收集心脏组织并使用指示的抗体免疫印迹。
图11A是显示NS小鼠模型中达沙替尼的出生前给药方案的图解。在动物在子宫中在E7.5直到出生后9天(P9)之间的时间,达沙替尼每天施用给怀孕的母亲。在出生后第10天(P10),小鼠通过每日注射直接接受达沙替尼46天(P56)。评估小鼠在P42和P56的心脏功能。
图11B是显示NS小鼠模型中达沙替尼的出生后给药方案的图解。达沙替尼在P10开始每天施用给小鼠持续32天(P42),停药14天(P56)。评估小鼠在P42和P56的心脏功能。
图12A是显示在NS小鼠中出生前达沙替尼治疗改善心脏功能的一组图。根据本文所述的方案给怀孕小鼠腹腔注射达沙替尼(0.1mg/kg)。指示每组的小鼠数。统计显著性由*;P<0.05,**;P<0.01,***;P<0.001通过双因素ANOVA检验指示。LV vol;s–心缩期左心室容积,LV vol;d–心舒期左心室容积,FS–缩短分数和EF–射血分数。
图12B是显示在出生后NS小鼠中达沙替尼治疗改善心脏功能的一组图。根据本文所述的方案在P10开始给NS小鼠腹腔注射达沙替尼(Disatinib)(0.1mg/kg)。治疗32天后评估小鼠的心脏功能。指示每组的小鼠数。统计显著性由*;P<0.05,**;P<0.01,***;P<0.001通过双因素ANOVA检验指示。LV vol;s–心缩期左心室容积,LV vol;d–心舒期左心室容积,FS–缩短分数和EF–射血分数。
图12C是显示停止达沙替尼治疗后心脏功能保持改善的一组图。根据图1B所示的方案在P10开始给NS小鼠腹腔注射达沙替尼(0.1mg/kg)。接受达沙替尼32天的小鼠在两周后被重新评估心脏功能。指示每组的小鼠数。统计显著性由*;P<0.05,**;P<0.01,***;P<0.001通过双因素ANOVA检验指示。LV vol;s–心缩期左心室容积,LV vol;d–心舒期左心室容积,FS–缩短分数和EF–射血分数。
图13,包括图13a-13l,是显示c-Src激酶是诺南综合征的推定靶标的一组图像。图13a是人Shp2野生型全长、N+C-SH2和PTP结构域构建体的示意图。图13b是显示与Flag-Shp2全长、N+C或PTP结构域共转染到HEK-293T细胞中的Myc-Src全长的检测的图像。通过免疫沉淀测定蛋白质-蛋白质相互作用。图13c是显示在4℃下用纯化的加His标记的Shp2的PTP结构域温育过夜的纯化的c-Src的GST-SH3结构域的检测的图像。蛋白质用GST-琼脂糖珠固定并通过SDS-PAGE分离。通过用抗His抗体的免疫印迹检测GST复合物中的His-PTP结构域。图13d是显示Src(Y416)的磷酸化水平的图像。来自Ptpn11
图14,包括图14a-14n,是显示达沙替尼改善Ptpn11
图15,包括图15a-15j,是显示由达沙替尼拯救(rescued)的Ptpn11
图16,包括图16a-图16g,是显示来自达沙替尼处理的Ptpn11
图17a-17g,包括图17a-17g,是显示达沙替尼在体外对NS信号传导的作用的一组图像。将来自Ptpn11
图18,包括图18a-18f,是显示达沙替尼对体内NS信号传导的作用的一组图像。3周龄的WT和Ptpn11
图19,包含图19a-19e,是显示出生后达沙替尼施用没有在Ptpn11
图20,包括图20a-20k,是显示在达沙替尼处理的Ptpn11
图21,包括图21a-21e,是显示出生后达沙替尼处理没有拯救Ptpn11
图22,包括图22a-22c,是显示达沙替尼不诱发肝损伤的一组图像。图22a是来自出生后载体或达沙替尼处理的8周龄WT和Ptpn11
图23是显示Src的SH3结构域和Shp2的PTP结构域之间的分子相互作用的图像。将纯化的c-Src的加GST标记的SH3结构域与纯化的Shp2的加His-标记的PTP结构域在4℃温育过夜。蛋白质用GST-琼脂糖珠固定并通过SDS-PAGE分离。通过用抗His抗体的免疫印迹在GST复合物中检测His-PTP结构域。
图24,包括图24a-24b,是显示由NS-Shp2诱导的PZR高磷酸化不依赖Shp2磷酸酶或c-Abl激酶活性的一组图像。将来自Ptpn11
图25,包括图25a-25f,是显示达沙替尼处理之后NSML(Y279C/+)小鼠中心肌病和纤维化的分子标记改善的图。从出生后载体或达沙替尼处理的(0.1mg/kg/天)WT和Ptpn11
具体实施方式
定义
除非另有定义,本文使用的所有技术和科学术语具有与本发明所属领域的普通技术人员通常理解的相同的含义。尽管与本文所述类似或等同的任何方法和材料可用于本发明的测试实践中,但是本文描述了优选的材料和方法。在描述和要求保护本发明时,将使用以下术语。
还应当理解,本文使用的术语仅用于描述特定实施方式的目的,而不是意欲是限制性的。
如本文所用,冠词“一(a)”和“一(an)”用于指一个或多于一个(即,至少一个)的冠词的语法对象。通过实例,“一要素(要素,an element)”指一个要素或多于一个要素。
如本文所用,当提到可测量的值如量、持续时间(时距,temporal duration)等时,术语“约”意在包括指定值的±20%或在10%、9%、8%、7%、6%、5%、4%、3%、2%、1%、0.5%、0.1%、0.05%、或0.01%内的变化,因为这些变化适合进行所公开的方法。除非从上下文另外是清楚的,否则本文中提供的所有数值均由术语约修饰。
短语“异常蛋白质酪氨酸磷酸化”是指一种或多种靶蛋白的高磷酸化或低磷酸化和/或异常的蛋白激酶活性。在一个实施方式中,将异常的蛋白质酪氨酸磷酸化与对照比较。
术语“心血管疾病或状况”是指影响心血管系统的任何疾病或状况,包括但不限于神经传导障碍、血栓形成、动脉粥样硬化、心绞痛、高血压、动脉硬化、心肌梗塞、充血性心力衰竭、心肌病、高血压、动脉和静脉狭窄、瓣膜疾病、心肌炎和心律失常。心血管疾病的状况还包括但不限于,与心脏和中央或外周动脉和静脉脉管系统相关的疾病状态的任何临床表现。例如,所述临床表现包括但不限于疼痛、虚弱、高血压、升高的血浆胆固醇、升高的血浆脂肪酸、心动过速、心动过缓、异常心电图、外部或内部出血、头痛、头晕、恶心和呕吐。
术语“心脏功能”是指心脏的活动或心脏中进行活动的细胞或组织的相互作用。心脏功能的实例包括但不限于肌原纤维组构、心肌细胞收缩性、血液和营养物足够递送到需要的组织。异常的心脏功能(血液和营养物向组织递送不足)可导致问题,诸如但不限于,血压变化、血栓形成、心电图变化、心律失常、心肌炎、心包炎、心肌梗塞、心肌病、肥大、萎缩、心力衰竭(心室衰竭(左或右))、充血性心力衰竭和心脏骤停。心脏功能的改善可以包括改善、消除或预防至少一种异常的心脏功能,例如但不限于,肌原纤维解体、异常心肌细胞收缩性、心脏纤维化、异常血压、过度的血压变化、血栓形成、心电图变化、心律失常、心肌炎、心包炎、心肌梗死、心肌病和充血性心力衰竭。
在本公开中,“包含(comprises)”、“包含(comprising)”、“含有(containing)”和“具有”等可以具有美国专利法赋予它们的含义,并且可指“包括(includes)”、“包括(including)”等等;“基本上由......组成”或“基本上组成”同样具有美国专利法中赋予的含义,并且该术语是开放式的,允许多于所叙述的存在,只要所叙述的基本或新颖特征不因多于所叙述的存在而改变,但是排除了现有技术实施方式。
“先天性心脏病”是指一种心脏病类别,其包括在出生前发生的心血管结构的异常。
“有效量”是指相对于未经治疗的患者减少或改善疾病的至少一种症状所需的量。用于疾病的治疗性处理的活性化合物(一种或或多种)的有效量根据受试者的施用方式、年龄、体重和一般健康状况而变化。
如本文所用的术语“表达”定义为由其启动子驱动的特定核苷酸序列的转录和/或翻译。
“片段”是指多核苷酸或核酸分子的一部分。该部分优选包含参考核酸的整个长度的至少10%、20%、30%、40%、50%、60%、70%、80%或90%。片段可以包含10、20、30、40、50、60、70、80、90或100、200、300、400、500、600、700、800、900、1000、1500、2000或2500(和之间的任何整数值)个核苷酸。应用于核酸分子的片段是指较大核酸的亚序列。核酸分子的“片段”可以是至少约15个核苷酸长度;例如,至少约50个核苷酸至约100个核苷酸;至少约100至约500个核苷酸,至少约500至约1000个核苷酸,至少约1000个核苷酸至约1500个核苷酸;或约1500个核苷酸至约2500个核苷酸;或约2500个核苷酸(和之间的任何整数)。
“低剂量”是指治疗有效剂量低于针对除了心脏病、先天性心脏病、心力衰竭或类似状况以外的适应症通常规定的剂量。在一个实施方式中,低剂量低于化学治疗剂量。在另一个实施方式中,低剂量在酪氨酸激酶抑制剂的化学治疗剂量的约约1/200的范围中。在另一个实施方式中,低剂量酪氨酸激酶抑制剂改善至少一种心脏功能。已经显示达沙替尼以约20mg/kg的剂量在预防小鼠的肿瘤发生中是有效的(Kantarjian,H.et al.Dasatinibversus imatinib in newly diagnosed chronic-phase chronic myeloid leukemia.NEngl J Med362,2260-2270(2010))。据报道,达沙替尼在人类中的治疗效果为约2mg/kg,小鼠中约24mg/kg的等效剂量(Yu,E.Y.et al.Phase II study of dasatinib in patientswith metastatic castration-resistant prostate cancer.Clinical cancerresearch:an official journal of the American Association for Cancer Research15,7421-7428(2009)和Apperley,J.F.et al.Dasatinib in the treatment of chronicmyeloid leukemia in accelerated phase after imatinib failure:the START atrial.J Clin Oncol 27,3472-3479,doi:10.1200/JCO.2007.14.3339(2009)。低至0.1mg/kg的达沙替尼的剂量(治疗剂量的约1/200)足以治疗CHD相关的心脏病。
术语“分离的”、“纯化的”或“生物纯的”是指在不同程度上不含与其天然状态中发现的通常伴随其的组分的物质。“分离”表示与原始来源或环境分离的程度。“纯化”表示高于分离的分离程度。“纯化的”或“生物纯的”蛋白质充分地不含其它物质,使得任何杂质都不会实质上影响蛋白质的生物学性质或引起其它不良后果。也就是说,如果当通过重组DNA技术产生时,其基本上不含细胞物质、病毒物质或培养基,或当化学合成时,其基本上不含化学前体或其它化学物质,则核酸或肽被纯化。纯度和均匀性通常使用分析化学技术,例如,聚丙烯酰胺凝胶电泳或高效液相色谱来测定。术语“纯化的”可以表示核酸或蛋白质在电泳凝胶中产生基本上一条带。对于可以进行修饰(例如磷酸化或糖基化)的蛋白质,不同的修饰可产生不同的分离的蛋白质,其可以被分别纯化。
“药学上可接受的”是指这样的性质和/或物质,其从药理/毒理学观点来看,对于患者是可接受的,以及从物理/化学观点来看,关于组合物、制剂、稳定性、患者接受和生物利用度,对于制造药剂师可接受的。“药学上可接受的载体”是指这样的介质,其不干扰活性成分(一种或多种)的生物活性的效力,并且对其所施用的宿主无毒性。
如本文所用,术语“药物组合物”或“药学上可接受组合物”是指在本发明中有用的至少一种化合物或分子与药学上可接受的载体的混合物。药物组合物有助于给患者施用化合物或分子。本领域中存在多种施用化合物或分子的技术,包括但不限于静脉内、口服、气雾剂、肠胃外、眼、肺和局部施用。
如本文所用,术语“药学上可接受的载体”是指在患者内或向患者运送或运输在本发明中有用的化合物或分子使得其可以执行其预期功能所涉及的药学上可接受的材料、组合物或载体,如液体或固体填料、稳定剂、分散剂、悬浮剂、稀释剂、赋形剂、增稠剂、溶剂或包封材料。通常,这样的构建体从一个器官、或身体的部分运送或运输到另一个器官或身体的部分。在与制剂的其他成分相容的意义上,每种载体必须是“可接受的”,包括本发明中有用的化合物,并且对患者无害。可以充当药学上可接受的载体的材料的一些实例包括:糖,如乳糖、葡萄糖和蔗糖;淀粉,如玉米淀粉和马铃薯淀粉;纤维素及其衍生物,如羧甲基纤维素钠、乙基纤维素和乙酸纤维素;粉状黄蓍胶;麦芽;明胶;滑石;赋形剂,如可可脂和栓剂蜡;油,如花生油、棉籽油、红花油、芝麻油、橄榄油、玉米油和大豆油;二醇,如丙二醇;多元醇,如甘油、山梨糖醇、甘露醇和聚乙二醇;酯,如油酸乙酯和月桂酸乙酯;琼脂;缓冲剂,如氢氧化镁和氢氧化铝;表面活性剂;海藻酸;无热原水;等渗盐水;林格溶液;乙醇;磷酸盐缓冲溶液;和药物制剂中使用的其他无毒相容物质。如本文所用,“药学上可接受的载体”还包括与本发明中有用的化合物的活性相容并且对患者生理学上可接受的任何和全部包衣、抗细菌和抗真菌剂、和吸收延迟剂等。补充的活性化合物也可以并入组合物中。“药学上可接受的载体”可进一步包括可用于本发明的化合物或分子的药学上可接受的盐。可以包括在本发明实践中使用的药物组合物中的其它另外的成分是本领域已知的,并在例如Remington's Pharmaceutical Sciences(Genaro,Ed.,Mack Publishing Co.,1985,Easton,PA)中描述,其通过引用并入本文。
也称为“髓鞘蛋白P0样蛋白1(myelin protein zero-like protein 1)”或“MPZL1”的“P0相关蛋白”或“PZR”是指为免疫球蛋白超家族细胞表面蛋白的蛋白质。PZR含有两个免疫受体酪氨酸基抑制基序(ITIMs),其负责与Shp2结合。当磷酸化时,PZR可以特异性结合Shp2,导致Shp2酪氨酸磷酸酶活性的激活。一旦被激活,Shp2的酪氨酸磷酸酶活性用于使传播细胞信号的下游底物去磷酸化。Shp2还可以通过充当支架或衔接蛋白发信号,借此其募集其它分子/活性至特定复合物。Shp2可以以催化依赖和不依赖的方式控制信号传导。
PZR的一种同种型,称为PZR1b,缺乏ITIMs,对全长PZR和其Shp2的募集具有显性负调控作用。示例性PZR序列包括在GenBank登录号NM_001146191和NP_001139663中发现的人PZR,或其片段,以及在NM_001001880或NP_001001880中发现的小鼠PZR序列,或其片段。关于PZR已知的大部分信息涉及其在粘附介导的细胞信号传导和细胞迁移中的作用。然而,PZR是否参与病理生理细胞信号传导仍然是未知的,以及随后PZR作为任何人类疾病的靶标的有效性尚未实现。
“RASopathy”是指由编码Ras/分裂原活化蛋白激酶(MAPK)途径的组分或调节物的基因中的种系突变引起的一组遗传综合征。这些综合征包括1型神经纤维瘤病、诺南综合征、具有多发性着色斑的诺南综合征、毛细血管畸形-动静脉畸形综合征、克斯提洛氏弹性蛋白缺陷症、心脏-面部-皮肤综合征和Legius综合征。Ras/MAPK通路在调节细胞周期和细胞生长、分化和衰老中起必不可少的作用,所有这些都对正常发育至关重要。由于共同的基础Ras/MAPK途径失调,RASopathies表现出许多重叠的表型特征。这些重叠表型在某些情况下可存在或由独立于MAPK本身操作的机制引起。本文所述的PZR/Shp2复合物位于Ras的上游。
诺南综合征(NS)是常染色体显性疾病,其在美国以约1:1,000-2,500活产的发病率发生。NS中最常见的心脏缺陷是肺动脉瓣狭窄、房间隔缺损和肥厚性心肌病,其中每个的严重程度从轻度到危及生命。具有多发性着色斑(NSML)的诺南综合征是具有与NS相似表型的罕见常染色体显性疾病,包括“诺南样”外观以及多发性着色斑、电导异常、眼距过宽、肺动脉瓣狭窄、异常的生殖器、生长迟缓和耳聋。NS相关的突变导致增加的磷酸酶活性。NSML相关的突变导致降低的磷酸酶活性。
“参考”是指标准或对照。“参考”是用作比较依据的定义的标准或对照。
如本文所用,“样品”或“生物样品”是指可以包含筛选方法或治疗期望的感兴趣细胞(例如,其癌症或肿瘤细胞)的任何物质。样品可以是生物样品,如生物流体或生物组织。在一个实施方式中,生物样品是包括肺动脉内皮细胞的组织样品。这样的样品可以包括种类不同的细胞、蛋白质和遗传物质。生物组织的实例还包括器官、肿瘤、淋巴结、动脉和个体细胞(一个或多个)。生物流体的实例包括尿、血、血浆、血清、唾液、精液、粪便、痰、脑脊髓液、眼泪、粘液、羊水等。
“酪氨酸激酶的Src家族”或“SFKs”是这样的酶家族,其催化磷酸基团加入到蛋白质底物的酪氨酸残基上。c-Src代表SFK家族的一员。
“Src家族酪氨酸激酶抑制剂”是指降低或阻止Src家族蛋白质底物上酪氨酸残基磷酸化的分子。Src家族酪氨酸激酶抑制剂可以破坏酪氨酰磷酸化,结合酪氨酸激酶或酪氨酸残基,可能具有比酪氨酸激酶或磷酸基团更高的缔合效率,和/或阻止磷酸基与酪氨酸残基的有效结合以减少或阻止磷酸化。Src家族酪氨酸激酶抑制剂包括但不限于,小分子Src家族酪氨酸激酶抑制剂、Src家族酪氨酸激酶拮抗剂、中和抗体和抑制肽和/或寡核苷酸。小分子Src家族酪氨酸激酶抑制剂的实例包括但不限于A419259、AP23451、AP23464、AP23485、AP23588、AZD0424、AZM475271、BMS354825、CGP77675、CU201、ENMD 2076、KB SRC 4、KX2361、KX2-391、MLR 1023、MNS、PCI-32765、PD166285、PD180970、PKC-412、PKI166、PP1、PP2、SRN004、SU6656、TC-S7003、TG100435、TG100948、TX-1123、VAL 201、WH-4-023、XL 228、细格菌素、伯舒替尼、虎刺醛、达沙替尼、除草霉素A、靛玉红、来那替尼、薰草菌素A、培利替尼、四羟反式茋、塞卡替尼、SrcI1、及其类似物。
“含有Src同源性2(SH2)结构域的(SH2)蛋白质酪氨酸磷酸酶-2”或“Shp2”是蛋白质酪氨酸磷酸酶(PTPs)的酪氨酸特异性家族的成员。Shp2是催化蛋白质的酪氨酸去磷酸化的酪氨酸磷酸酶。人类基因突变,PTPN11,已被发现引起约一半的诺南综合征病例和约十分之一的NSML病例。
“受试者”或“患者”,如本文所用,可以是人或非人哺乳动物。非人哺乳动物包括,例如,家畜和宠物,例如羊、牛、猪、犬、猫和鼠哺乳动物。优选地,受试者是人。
术语“跨膜糖蛋白”是指跨越细胞膜的膜蛋白。在一个实施方式中,跨膜糖蛋白包括免疫球蛋白超家族细胞表面蛋白,例如PZR。
如本文所用,术语“治疗(treat)”、“治疗(treating)”、“治疗(treatment)”等是指减少或改善与其相关的病症和/或症状。应当理解,尽管不被排除,治疗病症或状况不要求与其相关的病症、状况或症状完全减轻或消除。
“酪氨酸激酶抑制剂”是指降低或阻止蛋白质底物上的酪氨酸残基磷酸化的分子。酪氨酸激酶抑制剂可以破坏酪氨酰磷酸化,结合酪氨酸激酶或酪氨酸残基,可能具有比酪氨酸激酶或磷酸基更高的缔合效率,和/或阻止磷酸基与酪氨酸残基的有效结合以减少或阻止磷酸化。酪氨酸激酶抑制剂包括但不限于,小分子酪氨酸激酶抑制剂、酪氨酸激酶拮抗剂、中和抗体和抑制肽和/或寡核苷酸。小分子酪氨酸激酶抑制剂的实例包括但不限于阿法替尼、阿西替尼、伯舒替尼、卡博替尼、西地尼布、色瑞替尼、克唑替尼、达拉非尼、达沙替尼、厄洛替尼、依维莫司、吉非替尼、依鲁替尼、伊马替尼、拉帕替尼、乐伐替尼、来他替尼、尼洛替尼、尼达尼布、帕博西尼、帕唑帕尼、帕纳替尼、瑞格非尼、鲁索替尼、塞马纳尼、西罗莫司、索拉非尼、舒尼替尼、替西罗莫司、托法替尼、曲美替尼、凡德他尼和威罗菲尼。
本文提供的范围被理解为在该范围内的所有值的速记。例如,1至50的范围被理解为包括1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、31、32、33、34、35、36、37、38、39、40、41、42、43、44、45、46、47、48、49或50的任何数字、数字组合或子范围。
本文中的变量或方面的实施方式的叙述包括作为任何单个实施方式的该实施方式,或与任何其它实施方式或其部分的组合。
本文提供的任何组合物或方法可以与本文提供的任何其它组合物和方法中的一种或多种组合。
组合物
已经发现异常蛋白质酪氨酸磷酸化,如Src家族酪氨酸激酶及其底物的磷酸化,在具有心血管疾病的受试者中改变。还发现异常蛋白质酪氨酸磷酸化在具有某些疾病如RASopathies的受试者中改变。抑制酪氨酸激酶活性治疗心脏病并改善至少一种心脏功能。抑制也可改善具有与RASopathy相关的先天性心脏缺损的受试者的心血管功能。本发明包括抑制酪氨酸激酶,如Src家族酪氨酸激酶以改善至少一种心脏功能从而阻止或减少酪氨酸磷酸化的组合物。本发明在一个方面包括含有低剂量酪氨酸激酶抑制剂的组合物,其中低剂量酪氨酸激酶抑制剂降低酪氨酸磷酸化并改善需要其的受试者中的至少一种心脏功能。
在一个实施方式中,低剂量酪氨酸激酶抑制剂降低跨膜糖蛋白如Src家族酪氨酸激酶和P0相关蛋白(PZR)的异常酪氨酸磷酸化。
在一个实施方式中,低剂量酪氨酸激酶抑制剂的量在酪氨酸激酶抑制剂的化学治疗剂量的约1/500至约1/25的范围内。在另一个实施方式中,低剂量酪氨酸激酶抑制剂的量在酪氨酸激酶抑制剂的化学治疗剂量的约1/400至约1/25的范围内。在另一个实施方式中,低剂量酪氨酸激酶抑制剂的量在酪氨酸激酶抑制剂的化学治疗剂量的约1/300至约1/25的范围内。在另一个实施方式中,低剂量酪氨酸激酶抑制剂的量在酪氨酸激酶抑制剂的化学治疗剂量的约1/300至约1/35的范围内。在另一个实施方式中,低剂量酪氨酸激酶抑制剂的量在酪氨酸激酶抑制剂的化学治疗剂量的约1/300至约1/50的范围内。在另一个实施方式中,低剂量酪氨酸激酶抑制剂的量在酪氨酸激酶抑制剂的化学治疗剂量的约1/300至约1/100的范围内。在另一个实施方式中,低剂量酪氨酸激酶抑制剂的量在酪氨酸激酶抑制剂的化学治疗剂量的约1/250至约1/150的范围内。在另一个实施方式中,低剂量酪氨酸激酶抑制剂的量在酪氨酸激酶抑制剂的化学治疗剂量的约1/250至约1/175的范围内。低剂量酪氨酸激酶抑制剂可以是酪氨酸激酶抑制剂的化学治疗剂量的约1/25、1/30、1/35、1/40、1/45、1/50、1/55、1/60、1/65、1/70、1/75、1/80、1/85、1/90、1/95、1/100、1/105、1/110倍、1/115、1/120、1/125、1/130、1/135、1/140、1/145、1/150、1/155、1/160、1/165、1/170、1/175、1/180、1/185、1/190、1/195、1/200、1/205、1/210、1/215、1/220、1/225、1/230、1/235、1/240、1/245、1/250、1/255、1/260、1/265、1/270、1/275、1/280、1/285、1/290、1/295、1/300、和它们之间的任何倍率变化。在一些实施方式中,对于70kg成年人,酪氨酸激酶抑制剂的化学治疗剂量在约75至约170mg/天或约1.1至约2.4的范围内。
在另一个实施方式中,低剂量酪氨酸激酶抑制剂选自阿法替尼、阿西替尼、伯舒替尼、卡博替尼、西地尼布、色瑞替尼、克唑替尼、达拉非尼、达沙替尼、厄洛替尼、依维莫司、吉非替尼、依鲁替尼、伊马替尼、拉帕替尼、乐伐替尼、来他替尼、尼洛替尼、尼达尼布、帕博西尼、帕唑帕尼、帕纳替尼、瑞格非尼、鲁索替尼、塞马纳尼、西罗莫司、索拉非尼、舒尼替尼、替西罗莫司、托法替尼、曲美替尼、凡德他尼和威罗菲尼。在另一个实施方式中,组合物包含多于一种的本文公开的酪氨酸激酶抑制剂。
在又一个实施方式中,低剂量酪氨酸激酶抑制剂是Src家族酪氨酸激酶抑制剂,例如但不限于选自以下的抑制剂:A419259、AP23451、AP23464、AP23485、AP23588、AZD0424、AZM475271、BMS354825、CGP77675、CU201、ENMD 2076、KB SRC 4、KX2361、KX2-391、MLR1023、MNS、PCI-32765、PD166285、PD180970、PKC-412、PKI166、PP1、PP2、SRN 004、SU6656、TC-S7003、TG100435、TG100948、TX-1123、VAL 201、WH-4-023、XL 228、细格菌素、博舒替尼、虎刺醛、达沙替尼、除草霉素A、靛玉红、来那替尼、薰草菌素A、培利替尼、四羟反式茋、塞卡替尼、SrcI1及其类似物。在另一个实施方式中,组合物包含至少一种Src家族酪氨酸激酶抑制剂。
在另一个实施方式中,低剂量酪氨酸激酶抑制剂改善至少一种心脏功能。心脏功能可包括但不限于,肌原纤维组构、心肌细胞收缩性、SERCA2A表达和心脏纤维化。异常的心脏功能可导致问题,如但不限于血压变化、血栓形成、心电图变化、心律失常、心肌炎、心包炎、心肌梗塞、心肌病、心力衰竭(心室衰竭)、充血性心力衰竭和心脏骤停。心脏功能的改善可以包括改善、消除或预防至少一种异常的心脏功能,如但不限于肌原纤维解体、异常心肌细胞收缩性、失调的SERCA2A表达、心脏纤维化、异常血压、过度的血压变化、血栓形成、心电图变化、心律失常、心肌炎、心包炎、心肌梗死、心肌病和充血性心力衰竭。
在再一个实施方式中,低剂量酪氨酸激酶抑制剂提供抗纤维化作用。心肌中增加的纤维化组分水平已与心力衰竭的进展有关。低剂量的酪氨酸激酶抑制降低了心肌中纤维化组分的积累。
减少异常蛋白质酪氨酸磷酸化的组合物也包括在本发明中。某些疾病,如心血管疾病或状况像先天性心脏病由异常的蛋白质酪氨酸磷酸化表征。因此,本发明包括阻止或减少一种或多种跨膜糖蛋白如P0相关蛋白或PZR的酪氨酸磷酸化的治疗。另一方面,本发明包括能够降低与心血管疾病或状况相关的异常蛋白质酪氨酸磷酸化的组合物。在再一方面,本发明包括能够降低与先天性心脏病相关的异常蛋白质酪氨酸磷酸化的组合物。再又一方面,本发明包括能够降低与RASopathy相关的心血管疾病或状况相关的异常蛋白质酪氨酸磷酸化的组合物。
方法
本发明还包括在需要其的受试者中预防或治疗心血管疾病或状况的方法。如本文所述,异常酪氨酸磷酸化的抑制预防和/或治疗心血管疾病或状况。向需要其的受试者如儿科受试者施用包括低剂量的酪氨酸激酶抑制剂的组合物以降低酪氨酸磷酸化的异常水平用于预防或治疗心血管疾病或状况。
一方面,本发明包括治疗受试者中具有异常蛋白质酪氨酸磷酸化的心血管疾病或状况的方法,包括向需要其的受试者施用低剂量的酪氨酸激酶抑制剂,其中所述酪氨酸激酶抑制剂降低酪氨酸磷酸化的异常水平并改善受试者中的至少一种心脏功能。
在另一方面,本发明包括治疗先天性心脏病的方法,其包括向需要其的受试者施用低剂量的酪氨酸激酶抑制剂,其中所述酪氨酸激酶抑制剂降低酪氨酸磷酸化的异常水平并改善受试者中的至少一种心脏功能。
在再一方面,本发明包括治疗与具有异常蛋白质酪氨酸磷酸化的RASopathy相关的心血管疾病或状况的方法,包括向需要其的受试者施用低剂量的酪氨酸激酶抑制剂,其中所述酪氨酸激酶抑制剂在受试者中降低P0相关蛋白(PZR)酪氨酸磷酸化的异常水平并改善至少一种心脏功能。
在一个实施方式中,本文所述方法中的心血管疾病或状况是与RASopathy例如但不限于选自以下的RASopathy相关的先天性心脏病或心血管疾病或状况:神经纤维瘤病1型、诺南综合征、具有多发性着色斑的诺南综合征(豹斑综合征)、毛细血管畸形-动静脉畸形综合征、克斯提洛氏弹性蛋白缺陷症、心脏-面部-皮肤综合征和Legius综合征。
在另一个实施方式中,方法包括向为儿科患者的受试者施用酪氨酸激酶抑制剂。儿科受试者可以小于18岁。儿科受试者可以小于12岁。儿科受试者可以小于10、9、8、7、6、5、4、3、2和1岁。在另一个实施方式中,受试者是小于12岁的儿科患者。在可选的实施方式中,方法包括向大于18岁的受试者施用酪氨酸激酶抑制剂。
在一个实施方式中,方法包括施用低剂量酪氨酸激酶抑制剂,所述酪氨酸激酶抑制剂降低跨膜糖蛋白如Src家族酪氨酸激酶和P0相关蛋白(PZR)的异常酪氨酸磷酸化。在一个实施方式中,酪氨酸磷酸化的异常水平包括酪氨酸磷酸化的P0相关蛋白(PZR)的异常水平。
在另一个实施方式中,施用低剂量酪氨酸激酶抑制剂改善心脏功能,如但不限于肌原纤维组构、心肌细胞收缩性、SERCA2A表达和心脏纤维化。在另一个实施方式中,心脏功能的改善可以包括改善、消除或预防至少一种异常的心脏功能,如但不限于肌原纤维解体、异常心肌细胞收缩性、失调的SERCA2A表达、心脏纤维化、异常血压、过度的血压变化、血栓形成、心电图变化、心律失常、心肌炎、心包炎、心肌梗死、心肌病和充血性心力衰竭。在再一个实施方式中,施用低剂量酪氨酸激酶抑制剂为受试者提供抗纤维化作用。
在一个实施方式中,本文所述方法中使用的低剂量酪氨酸激酶抑制剂的剂量在酪氨酸激酶抑制剂的化学治疗剂量的约1/500至约1/25的范围内。在另一个实施方式中,低剂量酪氨酸激酶抑制剂的量在酪氨酸激酶抑制剂的化学治疗剂量的约1/400至约1/25的范围内。在另一个实施方式中,低剂量酪氨酸激酶抑制剂的量在酪氨酸激酶抑制剂的化学治疗剂量的约1/300至约1/25的范围内。在另一个实施方式中,低剂量酪氨酸激酶抑制剂的量在酪氨酸激酶抑制剂的化学治疗剂量的约1/300至约1/35的范围内。在另一个实施方式中,低剂量酪氨酸激酶抑制剂的量在酪氨酸激酶抑制剂的化学治疗剂量的约1/300至约1/50的范围内。在另一个实施方式中,低剂量酪氨酸激酶抑制剂的量在酪氨酸激酶抑制剂的化学治疗剂量的约1/300至约1/100的范围内。在另一个实施方式中,低剂量酪氨酸激酶抑制剂的量在酪氨酸激酶抑制剂的化学治疗剂量的约1/250至约1/150的范围内。在另一个实施方式中,低剂量酪氨酸激酶抑制剂的量在酪氨酸激酶抑制剂的化学治疗剂量的约1/250至约1/175的范围内。低剂量酪氨酸激酶抑制剂可以是酪氨酸激酶抑制剂的化学治疗剂量的约1/25、1/30、1/35、1/40、1/45、1/50、1/55、1/60、1/65、1/70、1/75、1/80、1/85、1/90、1/95、1/100、1/105、1/110、1/115、1/120、1/125、1/130、1/135、1/140、1/145、1/150、1/155、1/160、1/165、1/170、1/175、1/180、1/185、1/190、1/195、1/200、1/205、1/210、1/215、1/220、1/225、1/230、1/235、1/240、1/245、1/250、1/255、1/260、1/265、1/270、1/275、1/280、1/285、1/290、1/295、1/300、和它们之间的任何倍率变化。在一些实施方式中,对于70kg的成年人,酪氨酸激酶抑制剂的化学治疗剂量在约75至约170mg/天或约1.1至约2.4的范围内。
在再一个实施方式中,低剂量酪氨酸激酶抑制剂选自阿法替尼、阿西替尼、伯舒替尼、卡博替尼、西地尼布、色瑞替尼、克唑替尼、达拉非尼、达沙替尼、厄洛替尼、依维莫司、吉非替尼、依鲁替尼、伊马替尼、拉帕替尼、乐伐替尼、来他替尼、尼洛替尼、尼达尼布、帕博西尼、帕唑帕尼、帕纳替尼、瑞格非尼、鲁索替尼、塞马纳尼、西罗莫司、索拉非尼、舒尼替尼、替西罗莫司、托法替尼、曲美替尼、凡德他尼和威罗菲尼。在另一个实施方式中,酪氨酸激酶抑制剂是Src家族酪氨酸激酶抑制剂,例如但不限于A419259、AP23451、AP23464、AP23485、AP23588、AZD0424、AZM475271、BMS354825、CGP77675、CU201、ENMD 2076、KB SRC 4、KX2361、KX2-391、MLR 1023、MNS、PCI-32765、PD166285、PD180970、PKC-412、PKI166、PP1、PP2、SRN004、SU6656、TC-S7003、TG100435、TG100948、TX-1123、VAL 201、WH-4-023、XL 228、细格菌素、博舒替尼、虎刺醛、达沙替尼、除草霉素A、靛玉红、来那替尼、薰草菌素A、培利替尼、四羟反式茋、塞卡替尼、SrcI1及其类似物。在另一个实施方式中,组合物包含多于一种本文公开的酪氨酸激酶抑制剂。在再一个实施方式中,组合物包含至少一种Src家族酪氨酸激酶抑制剂。在这样的实施方式中,酪氨酸激酶抑制剂可以通过不同的给药途径,或在相同或不同的药物组合物中,一起或依次施用。
本文公开的方法和组合物还可用作具有以异常蛋白质酪氨酸磷酸化为特征的心血管疾病或状况的受试者中的心血管疾病或状况的治疗。
药物组合物
本发明还包括本发明的药物组合物实施本发明的方法的用途。一方面,本发明包括药物组合物,所述药物组合物包含本文所述的组合物和药学上可接受的载体。在另一方面,本文所述的组合物用于制备用于治疗需要其的受试者的心血管疾病或状况的药物。在再一方面,本发明包括药物组合物,其包含本文所述的组合物组合用于治疗心血管疾病或状况的另一治疗剂。这样的药物组合物可以以适于施用给受试者的形式提供,并且可以包含一种或多种药学上可接受的载体、一种或多种另外的成分、或这些的一些组合。本文所述的组合物可以包含生理学上可接受的盐,如本发明中考虑的化合物组合生理学上可接受的阳离子或阴离子,其在本领域中是公知的。
可用于本发明方法的药物组合物可被适当地开发用于吸入、口服、直肠、阴道、肠胃外、局部、经皮、肺、鼻内、颊、眼、鞘内、静脉内或其它给药途径。其它预期的制剂包括设计的纳米颗粒、脂质体制剂、含有活性成分的再密封的红细胞和基于免疫的制剂。给药途径(一种或多种)对于本领域技术人员将是显而易见的,并且将取决于任何数量的因素,包括被治疗的疾病的类型和严重性、被治疗的兽医学或人类患者的类型和年龄等。
本文所述的药物组合物的制剂可以通过药理学领域中已知或之后开发的任何方法制备。通常,这种制备方法包括使活性成分与载体或一种或多种其它辅助成分(accessory ingredients)结合的步骤,然后如果需要或想要,将产品成型或包装成想要的单剂量或多剂量单位。
在一个实施方式中,使用一种或多种药学上可接受的赋形剂或载体配制本发明的组合物。在一个实施方式中,本发明的药物组合物包含治疗有效量的至少一种本发明的化合物和药学上可接受的载体。可用的药学上可接受的载体包括但不限于甘油、水、盐水、乙醇和其它药学上可接受的盐溶液如磷酸盐和有机酸的盐。这些和其它药学上可接受的载体的实例描述于Remington’s Pharmaceutical Sciences(1991,Mack Publication Co.,NewJersey)中。
除非另有说明,本发明的实施应用在本领域技术人员的范围内适宜的分子生物学(包括重组技术)、微生物学、细胞生物学、生物化学和免疫学的常规技术。这些技术在文献,如“Molecular Cloning:A Laboratory Manual”,第4版(Sambrook,2012);“Oligonucleotide Synthesis”(Gait,1984);“Culture of Animal Cells”(Freshney,2010);“Methods in Enzymology”“Handbook of Experimental Immunology”(Weir,1997);“Gene Transfer Vectors for Mammalian Cells”(Miller and Calos,1987);“Short Protocols in Molecular Biology”(Ausubel,2002);“Polymerase ChainReaction:Principles,Applications and Troubleshooting”,(Babar,2011);“CurrentProtocols in Immunology”(Coligan,2002)中被充分说明。这些技术适用于本发明的多核苷酸和多肽的生产,并且,因此,可以在制备和实施本发明时考虑。特定实施方式的特别有用的技术将在以下部分中讨论。
实施例
通过参考以下实验实施例进一步详细描述本发明。这些实施例仅是为了说明的目的而提供的,除非另有说明,否则不意欲是限制性的。因此,本发明绝不应被解释为限于以下实施例,而应被解释为包括由于本文提供的教导而变得明显的任何和所有变化。
在没有进一步描述的情况下,相信本领域普通技术人员可以使用前述描述和以下说明性实施例来制备和利用本发明的化合物并实施所要求保护的方法。因此,以下工作实施例具体指出了本发明的实施方式,并且不被解释为以任何方式限制。
诺南综合征(NS)是由激活编码Shp2的PTPN11基因中的突变引起的常染色体显性疾病,其表现为先天性心脏病、身材矮小症和面部畸形。Shp2信号传导的复杂性通过这样的观察例证:具有多发性着色斑的诺南综合征(NSML)患者具有失活的PTPN11突变,但显示与NS相似的症状。“P0相关蛋白”(PZR)——与胞外基质接合(关联,interface)以促进细胞迁移的跨膜糖蛋白——被鉴定为NS和NSML的小鼠模型中主要的高酪氨酰磷酸化蛋白质。通过增强募集Src到NS和NSML Shp2,以不依赖磷酸酶的方式促进PZR高酪氨酰磷酸化。因此,PZR被确定为NS和NSML靶标。增强的PZR介导的Shp2的膜募集充当引导这些PTPN11突变的重叠病理生理学特征的常见机制。
现在描述在本文公开的实验操作中使用的材料和方法。
抗体、化学品、细胞系和表达试剂。与Cell Signaling合作生成兔单克隆磷酸-PZR(Y241)和兔单克隆磷酸-PZR(Y263)抗体。小鼠单克隆Src抗体、兔多克隆Src抗体、兔多克隆磷酸-ERK1/2(T202Y204)、小鼠单克隆ERK1/2抗体、兔多克隆磷酸-Akt(S473)抗体和小鼠单克隆Akt抗体购自Cell Signaling。兔多克隆Shp2抗体和兔多克隆ERK1/2抗体购自SantaCruz Biotechnology。小鼠单克隆Shp2抗体购自BD Bioscience。小鼠抗磷酸酪氨酸抗体4G10(05-321)来自Merck Millipore,兔抗GFP(TP401)来自Acris,小鼠抗HA.11克隆16B12来自Covance。兔多克隆PZR(105-6)由Z.J.Zhao慷慨提供。Src家族激酶抑制剂PP2和SU6656购自Calbiochem。HEK-293、NIH 3T3、SYF(Src
MS分析。如前所述进行磷酸扫描(PhosphoScan)方法(Rikova,K.,et al.,Cell,131:1190-1203)。将野生型和Shp2突变体(诺南综合征)小鼠心脏匀浆、超声处理并离心以除去细胞碎片。使用ProteinPlus考马斯(Coomassie)试剂(Pierce)对每个组织的总蛋白进行标准化,并使用胰蛋白酶(Worthington)将蛋白质还原、烷基化和消化过夜。通过具有Sep-Pak经典C
动物处理——Ptpn11
达沙替尼治疗——N-(2-氯-6-甲基苯基)-2-[[6-[4-(2-羟基乙基)-1-哌嗪基]-2-甲基-4-嘧啶基]氨基]-5-噻唑甲酰胺一水合物(达沙替尼,BMS-354825))购自Biovision。将达沙替尼以10mg/ml的浓度溶于DMSO中,然后以200μg/ml的浓度重悬于载体(1×Dulbecco’s PBS)中。WT和Ptpn11
超声心动图研究——使用Vevo 770控制台通过超声心动图分析心脏尺寸和功能。用吸入的异氟醚(在O
统计分析——统计学值呈现为平均值±s.e.m。使用双因素ANOVA(Tukey的多重比较)检验来计算P值。所有统计分析均用GraphPad Prism 5进行。对于所有研究,P值小于0.05被认为是显著的。
现在描述用于进行本文公开的实施例2中的实验的材料和方法。
抗体、化学药品、细胞系和质粒——如下所示,以下抗体用于免疫印迹(IB)或免疫沉淀(IP)。小鼠单克隆Flag(F1804,IP-1:100,IB-1:1,000)和小鼠单克隆生物素化Flag(F9291,IB-1:1,000)抗体来自Sigma。小鼠单克隆Myc(sc-40,IP-1:100,IB-1:1,000)、小鼠单克隆生物素化Myc(sc-40B,IB-1:1,000)、兔多克隆Shp2(sc-280,IB-1:1,000)、小鼠单克隆p38(sc-535,IB-1:1,000)、小鼠单克隆GST(sc-138,IB-1:1,000)抗体来自Santa CruzBiotechnology。兔单克隆磷酸-PZR(Y241;#8181,IB-1:1,000)、兔单克隆磷酸-PZR(Y263;#8088,IB-1:1,000)、兔多克隆磷酸-Src(Y416;#2101,IB-1:1000)、小鼠单克隆Src(#2110,IB-1:1,000)、小鼠单克隆Raf1(#12552,IB-1:1,000)、兔多克隆磷酸-MEK1/2(S217/221;#9154,IB-1:1000)小鼠单克隆MEK1/2(#4694,IB-1:1,000)、兔多克隆磷酸-ERK1/2(T202/Y204;#9101,IB-1:1,000)、小鼠单克隆ERK(#9107,1:1,000)、兔多克隆磷酸-p38(T180/Y182;#9215,IB-1:1,000)、兔多克隆磷酸-JNK(T183/Y185;#4668,IB-1:1,000)、小鼠单克隆JNK(#3708,IB-1:1,000)、兔多克隆磷酸-Akt(S473;#9271,IB-1:1,000)、小鼠单克隆Akt(#2967,IB-1:1,000)、兔多克隆SERCA2A(#9580,1:1,000)、兔多克隆肌钙蛋白I(#4002,IB-1:1,000)抗体购自Cell Signaling。从Abcam获得兔多克隆磷酸-Raf1(Y341;ab192820,IB-1:1,000)和兔多克隆α微管蛋白(ab4074,IB-1:1,000)抗体。小鼠单克隆Shp2(#610622,IB-1:1,000)抗体购自BD Biosciences。小鼠单克隆His(#11922416,IB-1:1,000)抗体来自Roche。兔多克隆肌钙蛋白T(MS-295,IB-1:1,000)来自Thermo Scientific。兔多克隆PZR抗体(IB-1:1,000)由Z.J.Zhao慷慨提供。达沙替尼购自Biovision,STI-571获自LKT实验室。Shp2磷酸酶抑制剂由Z.-Y.Zhang(Indiana University)慷慨提供。HEK-293T细胞购自ATCC,从WT和Ptpn11
免疫沉淀和免疫印迹——将细胞或心脏组织在裂解缓冲液(25mM Tris-HCl,pH7.4、136mM NaCl、1mM CaCl
体外GST拉下(GST-pull down)测定——Src的细菌纯化GST-SH3和Shp2的His-PTP由T.Boggon(耶鲁大学)提供。在含有Src蛋白的GST-SH3与Shp2的His-PTP或标记Flag的Shp2过表达HEK-293细胞裂解物的1ml裂解缓冲液中在4℃下进行拉下测定过夜。通过BSA包被的GST-琼脂糖珠在4℃下亲和纯化SH3结合的Shp2蛋白1小时。使用用抗His或抗Flag和抗-GST抗体的免疫印迹检查Src的SH3和Shp2蛋白之间的相互作用。
动物处理——Ptpn11
组织学——从载体或达沙替尼处理的野生型和NS小鼠中分离心脏、肝和脾。将组织在磷酸盐缓冲盐水(PBS)中的4%多聚甲醛中固定,处理以用于石蜡切片,并用苏木精和伊红(H&E)或Masson’s Trichrome染色。在明视野显微镜下获得组织图像(Olympus BX51,耶鲁肝中心(Yale Liver Center))。
超声心动图——将小鼠在具有氧气中1%异氟醚的密封塑料室中麻醉,直到不动,然后转移到加热的程序板(37℃)上。在整个程序中,用与异氟醚蒸发器连接的鼻锥供应的1%异氟醚将动物保持麻醉。将扫描头放置在小鼠的胸部,获得稳定的图像信号(B模式和M模式),并用Vevo 770(VisualSonics)分析数据。收缩和舒张的左心室外周壁厚度、室直径和室间壁厚度用M模式图像测量。计算射血分数(EF)和缩短分数(FS)的百分比。
血液动力学研究——通过腹膜内注射氯胺酮(100mg/kg)和赛拉嗪(5mg/kg)引起麻醉。将动物放在温垫上,并在颈部上进行切口。暴露右侧颈动脉,将1.9French顶端有换能器的导管(Millar Inc.,Houston,TX)插入动脉,然后进入左心室。在基础条件下测量包括高保真阳性、阴性dp/dt的左心室压力和心率。使用LabChart软件记录和分析数据。
RNA提取和定量实时PCR分析——根据制造商的说明,使用RNeasy试剂盒(Qiagen,CA)从小鼠心脏分离RNA。使用逆转录酶PCR试剂盒(Applied Biosystems,CA)将总共1μgRNA逆转录以产生cDNA。使用Applied Biosytems 7500Fast实时PCR系统和具有以下引物对的SYBR绿色基因表达反应混合物(master mix)一式三份进行实时定量PCR。
18S rRNA,5’-ACCGCAGCTAGGAATAATGGA-3’SEQ ID NO:1,5’-ACCAAAAGCCTTGACTCCG-3’SEQ ID NO:2;
ANF,5’-CCTGGAGGAGAAGATGCCGGTAGAA-3’SEQ ID NO:3,5’-CCCCAGTCCAGGGAGGCACCTCGG-3’SEQ ID NO:4;
BNP,5’-CACTTCAAAGGTGGTCCCAGAGCTGC-3’SEQ ID NO:5,5’-GACCGGATCGGATCCGTCAGTCG-3’SEQ ID NO:6;
MHC,5’-GTCCCGGACACTGGACCAGGCC-3’SEQ ID NO:7,5’-CTCCTTTTCTTCCAGTTGCCTAGCCAA-3’SEQ ID NO:8;
MHC,5’-GAGCAAGGCCGAGGAGACGCAGCGT-3’SEQ ID NO:9,5’-GAGCCTCCTTCTCGTCCAGCTGCCGG-3’SEQ ID NO:10;
Col1a2,5’-AGGTCTTCCTGGAGCTGATG-3’SEQ ID NO:11,5’-ACCCACAGGGCCTTCTTTAC-3’SEQ ID NO:12;
Col3a1,5’-ACAGCAAATTCACTTACACAGTTC-3’SEQ ID NO:13,5’-CTCATTGCCTTGCGTGTTT-3’SEQ ID NO:14。
所有的相对基因表达水平使用ΔC
用于单细胞分析的心脏组织的酶消化——来自8周龄小鼠的心肌细胞通过Langendorff程序——从Xianghua Xu,et al.J Vis Exp.2009;(28):1308修改——分离。简言之,将心脏快速切除并插管至Langendorff装置,在那里用37℃无Ca
心肌细胞功能表征——心肌细胞在Tyrodes溶液(150mM:NaCl:140,KCl:5.4,CaCl2:1.8,MgCl
统计分析——所有数据表示平均值±平均值的标准误差(SEM)。使用方差分析(ANOVA)和利用GraphPad Prism 6统计软件程序的Tukey多重比较来评估组之间的差异。
现在描述本文公开的实验结果。
实施例1:用酪氨酸激酶干预靶向RASopathy介导的心脏病。
图1A是Ptpn11
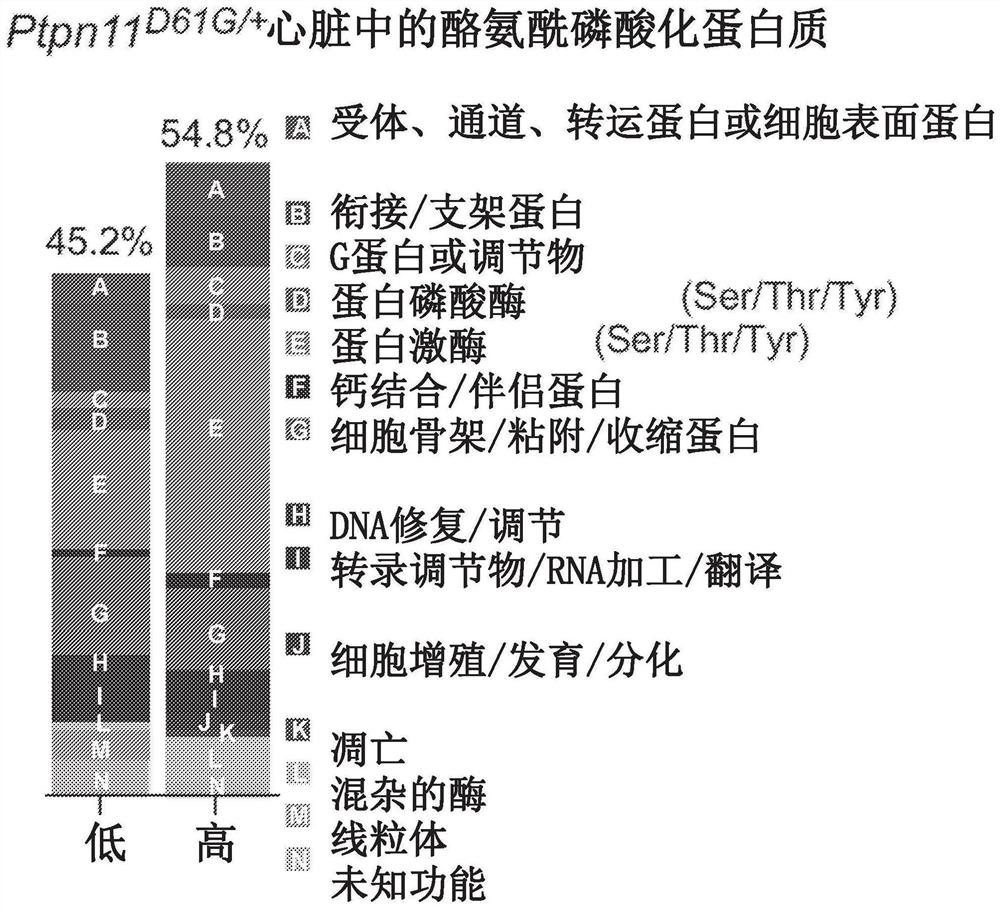
图1B是显示野生型和Ptpn11
图2A-2E显示免疫印迹——显示PZR酪氨酰磷酸化的表征。NS和NSML突变体引起的PZR高酪氨酰磷酸化位点的构象。在小鼠中发现的酪氨酰磷酸化位点(一个或多个)的PZR磷酸化抗性突变体的表达损害其在培养细胞中被磷酸化的能力,也如使用磷酸特异性抗PZR(Y242)和抗PZR(Y263)所检测到的。代表在NS或NSML患者中发现的那些的Shp2的突变体能够在Y241和Y263处诱导PZR高酪氨酰磷酸化。类似地,斑马鱼PZR表现出能够在可比较的残基处被酪氨酰磷酸化的相同属性。这些结果表明NS或豹斑综合征相关的Shp2突变体在各种细胞系中诱导PZR高度磷酸化。
图3A-3D显示了Ptpn11
图4A-4C显示Ptpn11
图5A-5D显示在Ptpn11
图6A-6B是显示Src家族激酶对NS/NMLS-Shp2介导的PZR Y241和Y263磷酸化的影响的印迹。NS和NMLS相关突变体诱导PZR高酪氨酰,其可以在用SFK抑制剂SU6656预处理细胞后被抑制。这些结果表明SFK能够在Y241和Y263上磷酸化PZR。这些结果进一步显示NS和NSML-Shp2突变诱导的PZR高酪氨酰磷酸化是Src家族激酶依赖性的。
图7A-7B是显示Src激酶介导的NS/LS-Shp2诱导的PZR高酪氨酰磷酸化的印迹。图7C-7D是显示Src激酶介导的PZR高酪氨酰磷酸化的印迹。这些图显示了酪氨酸激酶抑制效能对PZR酪氨酰磷酸化的作用的比较。将酪氨酸激酶抑制剂PP2和SU6656施用于表达活化的Shp2(Shp2-E76A)突变体的细胞。虽然PP2和SU6656均能抑制Shp2-E76A诱导的PZR高酪氨酰磷酸化,但是SU6656更有效。与PP2相比,PZR高酪氨酰磷酸化在1μMSU6656被完全抑制,其在5μM PP2被抑制。这些结果支持Src家族激酶负责PZR磷酸化的观念。重要的是,通过Src的PZR磷酸化产生Shp2与PZR相互作用的结合位点(pY241/pY263)。这些结果暗示c-Src在Shp2结合位点直接磷酸化PZR。
在诺南综合征中,由Src引起的Y241和Y263的磷酸化增加导致有害地高水平的PZR/Shp2复合物,这被认为是推进这些患者中先天性心脏病发展的机制。
图8A-8B显示具有NS/NSML相关的Shp2突变体和PZR的增强的Src复合物形成。图8A显示,与野生型Shp2相比,已知引起NS或NSML的Shp2的突变体形式可以以增加的亲和力与c-Src结合。这些结果进一步表明c-Src在Shp2结合位点直接磷酸化PZR。
图9是NS-和NSML-Shp2突变体对PZR酪氨酰磷酸化影响的模型的图解。该模型基于实验数据,从中PZR被观察为在NS和NSML小鼠模型的心脏中在Shp2结合位点上高酪氨酰磷酸化。增加的PZR酪氨酰磷酸化促进Shp2与PZR的结合增加。该图提出,增强的PZR酪氨酰磷酸化导致Shp2向PZR的募集增加,以促进进一步的PZR酪氨酸磷酸化,以及其他在附近的潜在Src底物。
此外,NS和NSML突变体与酪氨酸激酶Src以增加的亲和力相互作用。总之,这些混杂的相互作用导致了来自PZR的功能失调的下游信号传导,其促进了先天性心脏病的发展。提出通过干扰Src酪氨酸激酶活性,PZR/Shp2复合物减少,来自PZR和可能的其他靶标的改变的信号传导被纠正。
图10是显示达沙替尼给药剂量的一组图像。雄性Ptpn11D61G/+小鼠腹腔注射以指示剂量的达沙替尼或DMSO对照。24小时后处死小鼠,心脏组织被收集并使用PZR和pY(263)-PZR抗体免疫印迹。这些结果显示,在NS小鼠中注射达沙替尼有效减少PZR酪氨酰磷酸化。
图11A是显示NS小鼠模型中达沙替尼的出生前给药方案的图解。在E7.5动物在子宫中时直到出生后9天(P9)之间的时间,每天施用达沙替尼给怀孕的母亲。在出生后第10天(P10),NS小鼠通过每日注射(腹腔)直接接受达沙替尼6周(P42)和8周(P56)。
图11B是显示NS小鼠模型中达沙替尼的出生后给药方案的图解。达沙替尼在出生后第10天(P10)开始每天施用给NS小鼠持续6周(P42),6周之后,治疗停止,并测量心脏功能。然后在从达沙替尼治疗中撤出2周后评估同一组小鼠。
在图11A和11B中,在6周和8周评估小鼠的心脏功能。这些图解描述了NS小鼠中出生前或出生后达沙替尼治疗策略。本文描述的给药方案被设计以测试达沙替尼用于NS相关心脏病的治疗性干预的有效性的三个方面。因为NS是发育障碍,所以图11A所示的第一给药方案测试了当施用于发育中的胚胎时,达沙替尼在发挥治疗效果上的有效性。第二评估确定了达沙替尼在出生后施用时治疗NS相关心脏病的有效性。这一策略与心脏病的结果更密切相关,因为已经意识到患者可以在出生后施用治疗剂量的达沙替尼。这种给药策略将减轻子宫并发症的风险。最后,第三测试是确定在治疗的心脏功能改善后,达沙替尼施用对维持治疗是必需的。
图12A是显示在NS小鼠中出生前达沙替尼治疗改善心脏功能的一组图(P42,图11A中所见)。图12B是显示在出生后NS小鼠中达沙替尼治疗改善心脏功能的一组图(P42)。图12C是显示停止达沙替尼治疗后心脏功能保持的改善的一组图(P56,图11B中所见)。这些结果提供了Src信号传导参与NS发病机制的证据。
这些实验的结果表明,低剂量的达沙替尼——在此被定义为低于被认为对治疗癌症有效的剂量——对于改善NS小鼠中的心脏功能是有效的。在图12A中,结果表明,当将达沙替尼注射入怀孕小鼠时,通过射血分数(EF)和缩短分数(FS)测量的心脏功能完全恢复到野生型参数。在图11B中,达沙替尼即使在发育后施用时也被显示是有效的。该治疗仍然在NS小鼠的心脏功能中发挥完整的矫正功能。这些结果表明,达沙替尼用于治疗RASopathy患者中先天性心脏病的治疗性施用可以通过发育后施用而以基本上较低的风险发生。最后,图12C显示,在已达到有效心脏功能后2周停止达沙替尼导致持续保持心脏功能。这些结果表明,一旦获得了有效的治疗并恢复了心脏功能,就不必继续暴露于达沙替尼。
实施例2:通过达沙替尼选择性拯救诺南综合征(NS)小鼠模型中的心脏缺陷。
Shp2由两个Src同源2(SH2)结构域、蛋白质酪氨酸磷酸酶(PTP)结构域和羧基末端尾构成。NS相关的Shp2(NS-Shp2)突变通常发生在占据氨基末端SH2和PTP结构域之间的界面的氨基酸残基中。所得到的突变破坏在SH2和PTP结构域之间发生的自我抑制性“关闭”构象,有利于促进催化的更“开放”构型。
P0相关蛋白(PZR)——跨膜糖蛋白,其在其C-末端含有两个基于免疫受体酪氨酸的抑制基序(ITIMs)——充当c-Src底物,并构成NS小鼠模型的心脏中主要的高酪氨酰磷酸化蛋白和Shp2结合靶。NS-Shp2突变体以增强亲和力与c-Src相互作用,赋予这些突变体通过PZR复合物形成而混合地靶向c-Src的能力。使用斑马鱼作为NS介导的CHD的模型,提出PZR-Shp2-Src复合物形成驱动NS介导的CHD中的异常信号传导。
这个推测的关键是NS-Shp2突变体显示与c-Src增强的相互作用而导致增加的c-Src介导的信号传导的能力。Shp2和c-Src之间增强的相互作用的性质可能作为Shp2的PTP结构域中另外在“关闭”构象中未被暴露的结合表面的暴露增加的结果发生。虽然Shp2已显示通过其SH3结构域与c-Src形成复合物,但是尚未定义c-Src与之相互作用的Shp2上的区域。
为了解决这个问题,设计了一系列Shp2缺失突变体(图13a),共转染到HEK-293T细胞中,通过共免疫沉淀检查复合物的形成(图23)。如所预期的,在具有c-Src的复合物中检测到全长Shp2,而缺乏PTP结构域的Shp2的缺失突变体没有相互作用(图13b)。体外结合测定进一步确定了Shp2的PTP结构域和c-Src的SH3结构域直接相互作用(图13c)。
由于这种相互作用发生在Shp2的PTP结构域内,所以与野生型Shp2相比,NS-Shp2突变体的“开放”构象被认为准备与c-Src的SH3结构域建立更稳定的相互作用。因此,NS-Shp2突变体通过PZR在膜上与c-Src更稳定地复合,其先前已被提出是异常c-Src介导的信号传导的推定机制。重要的是,这些观察结果暗示c-Src或Src家族激酶(SFK)成员作为Shp2介导的NS发病机制中的候选物(一个或多个)。
为了测试SFK是否参与NS发病机制,c-Src在药理学上被抑制以测试其抑制是否改善Shp2-NS信号传导。为了抑制c-Src,使用了达沙替尼
达沙替尼抑制PZR酪氨酰磷酸化也导致PZR/Shp2复合物形成的破坏(图13d)。另外,达沙替尼在NS衍生的MEFs中抑制Raf-1、MEK1、JNK和Akt(图17)。
BCR-Abl激酶抑制剂STI-571
为了检查达沙替尼在体内对NS介导的c-Src和PZR酪氨酰磷酸化的作用,将达沙替尼注射入含有Asp61至Gly61(D61G)的Shp2敲入突变的小鼠(Araki et al Nat Med 10,849-857(2004))。对PtpN11
已经显示达沙替尼以约20mg/kg的剂量在预防小鼠的肿瘤发生中有效(Shah etal.,Science 305,399-401(2004))。据报道,达沙替尼的治疗效果在人体中为约2mg/kg——在小鼠中约24mg/kg的等效剂量(Kantarjianet al.,N Engl J Med 362,2260-2270(2010),Yu et al.,Clinical Cancer Research 15,7421-7428(2009),Apperley J ClinOncol 27,3472-3479(2009))。低至0.5mg/kg的达沙替尼的剂量足以显著抑制3周龄NS小鼠心脏中的c-Src和PZR酪氨酰磷酸化(图13i-13l)。值得注意的是,在这些达沙替尼的剂量(0.1-0.5mg/kg)下,ERK1/2磷酸化(图13i-13l)、Raf-1、MEK1、p38MAPK和JNK在3周龄NS小鼠的心脏中都不受影响(图18)。这些结果表明,达沙替尼在低至有效化疗剂量的1/250的剂量(对于慢性髓性白血病成人患者约100-140mg/天或约1.4-2.0mg/kg/天)下可以抑制NS小鼠心脏中的PZR酪氨酰磷酸化。
此外,在NS小鼠的心脏中,达沙替尼介导的PZR酪氨酰磷酸化的抑制与ERK1/2磷酸化的抑制分离(图13)。因此,独立于ERK1/2途径,低剂量的达沙替尼干扰NS-Shp2信号传导。
将达沙替尼施用于怀孕的母亲,并评估NS小鼠中心脏缺陷的改善。达沙替尼以0.1、0.5或1.0mg/kg每日腹膜内施用于与NS小鼠杂交的野生型怀孕小鼠,从胚胎第7天开始直到出生后第9天(在护理雌性中)。出生后第10天(P10),达沙替尼注射直接重新开始每天到个体幼仔中,直到出生后8周(P56)(图14a)。尽管以0.5和1.0mg/kg/天的达沙替尼治疗显示胚胎致死率,但是以0.1mg/kg/天的达沙替尼治疗没有可观察到的不良反应(表1)。
在6周和8周时通过超声心动图和侵入性血液动力学检查NS小鼠的心脏功能。与载体处理的野生型小鼠相比,未治疗的NS小鼠的射血分数(EF)和缩短分数(FS)显著降低了35%(P<0.01)。然而,与载体处理的NS小鼠相比,达沙替尼治疗的NS小鼠在P42显示完全恢复心脏功能(图14b和14c和表2)。然而,持续施用达沙替尼另外2周在野生型和达沙替尼治疗的NS小鼠中均引起心力衰竭(图14d-14e和表3)。这些数据表明,在子宫内达沙替尼治疗可以拯救在NS小鼠中观察到的受损的心脏功能。因此,c-Src活性有助于Shp2-NS CHD的表现。
表1:来自出生前达沙替尼治疗的Ptpn11
表2:出生前载体或达沙替尼治疗的WT和Ptpn11D
数据代表平均值±SEM。*,P<0.05;**,P<0.01表示与载体处理的WT小鼠相比的显著性。
表3:出生前载体或达沙替尼治疗的WT和Ptpn11D
数据代表平均值±SEM。*,P<0.05;***,P<0.001表示与载体处理的WT小鼠相比的显著性。所有p值都使用双因素ANOVA(Tukey多重比较)得出。IVS,室间隔壁厚度;LVID,左心室内部尺寸;LVPW,左室后壁厚度;LV vol,左心室容积;EF,射血分数;FS,缩短分数;d,舒张;s,收缩。
达沙替尼有效地减少了对发育后的CHD的NS-Shp2效应。NS小鼠用达沙替尼(0.1mg/kg/天)治疗从P10直至P42(图14f)。除了CHD的呈现之外,NS人和小鼠显示与人类疾病相似的生长迟缓、面部畸形和脾肿大。尽管发现NS小鼠显示减少的生长、面部畸形和脾肿大,但是达沙替尼治疗没有改善这些NS相关的病状的任一种(图19-21)。此外,在用达沙替尼治疗的野生型或NS小鼠中都没有检测到肝损伤的证据(图22)。
然而,通过检查心脏参数,达沙替尼治疗的NS小鼠(P42)完全恢复了心脏功能性,如通过EF和FS的测量所确定的(图14g和14h和表4-5)。值得注意的是,当在随后的时间点在NS小鼠中评估心脏功能时,其后,达沙替尼治疗已停止2周,观察到与载体处理的野生型对照相比类似水平的心脏功能改善(图14i和14j)。另外的心脏参数也通过侵入性血液动力学评估,这些结果显示达沙替尼治疗的NS小鼠主动脉血压和左心室压得到显著恢复(图14k-14n和表6)。
综合来看,这些数据表明,当以用作CML治疗的亚治疗(sub-therapeutic)的剂量的施用给发育后NS小鼠时,达沙替尼提供了对预防NS小鼠心力衰竭的选择性效力。有趣的是,心脏功能的改善似乎不是短暂的,因为去除达沙替尼并没有逆转NS小鼠中心脏功能的恢复。
表4:出生后载体或达沙替尼治疗的WT和Ptpn11D
数据代表平均值±SEM。*,P<0.05;**,P<0.01表示与载体处理的WT小鼠相比的显著性。
表5:出生后载体或达沙替尼治疗的WT和Ptpn11D
数据代表平均值±SEM。***,P<0.001表示与载体处理的WT小鼠相比的显著性。
表6:出生后载体或达沙替尼治疗的WT和Ptpn11D
数据代表平均值±S EM。**,P<0.01;***,P<0.001表示与载体处理的WT小鼠相比的显著性。
为了进一步了解在达沙替尼治疗的NS小鼠中显示的心脏表型的性质,进行这些心脏的总体形态学和组织学检查。NS小鼠与野生型小鼠相比具有较低的心脏重量(图15a)。NS小鼠中心脏重量与体重的比显著增加(图15b)。组织学分析还显示,NS小鼠具有扩张型心肌病(DCM),显示为左室间隔壁厚度明显减少,收缩期左心室腔尺寸增加(图15c和表4)。
如所预期的,心脏组织的组织学检查显示载体处理的NS小鼠的左心室壁中解体的肌纤维结构(图15d)。相比之下,达沙替尼治疗的NS小鼠显示所有这些病理性心脏表型显著逆转到与载体处理的野生型小鼠基本上相似的水平(图15a-15d)。
衰竭的心脏的另一个标志是获得心脏纤维化。与达沙替尼治疗赋予NS心脏中心力衰竭保护的观念一致,达沙替尼治疗的NS小鼠心脏中的纤维化与载体处理的野生型小鼠相比在组织学水平上显著减低,与纤维化基因Col1a2和Col3a1的mRNA表达水平降低一致(图15d-15f)。纤维化成分如胶原——由Col1a2和Col3a1基因编码——的沉积与心力衰竭有关。因此,Col1a2和Col3a1表达的降低与低剂量达沙替尼治疗引起的心力衰竭的矫正相一致。
心脏结构蛋白如α肌球蛋白重链(MYH6)和β肌球蛋白重链(MYH7)基因的重新表达指示心肌病。特别地,MYH6的失活和MYH7的激活代表支持心肌病发展的心脏重新编程的特征(Morita et al.,J Clin Invest115(2005))。与野生型小鼠相比,载体处理的NS小鼠中MYH6表达显著下调。达沙替尼治疗在野生型和NS型小鼠中产生了相当水平的MYH6表达(图15g)。MYH7在载体处理的NS小鼠中显著地重新表达,并且这在达沙替尼治疗后完全标准化返回到载体野生型治疗的水平(图15h)。
通过评估心房利钠肽(Anp)和脑利钠肽(Bnp),进一步支持了达沙替尼改善NS小鼠中心力衰竭的效果。与载体处理的野生型对照相比,NS小鼠中Anp和Bnp mRNA表达水平均显著上调(图15i和15j)。相比之下,达沙替尼治疗的NS小鼠从Anp和Bnp升高的mRNA表达水平被完全挽救(图15i和15j)。总的来说,这些结果支持Src家族激酶活性在NS相关的CHD发展中起不可或缺作用的结论。
为了确定达沙替尼对NS心脏功能的影响是否是心肌内在的,在来自载体和达沙替尼治疗的野生型和NS小鼠的分离的心肌细胞中测量钙(Ca
来自载体处理的NS小鼠的心肌细胞显示收缩性不足,其缩短峰值比载体处理的野生型小鼠小22%(图16a和16c)。鉴于在这些相同的心肌细胞中观察到的Ca
通过对肌浆(内质)网Ca
引人注目的是,与野生型相比,载体处理的NS小鼠心脏显示SERCA2A蛋白表达显著降低,TnI和TnT表达增加(图16d-16g)。与达沙替尼治疗的NS小鼠心脏功能的恢复一致,从达沙替尼治疗的NS小鼠分离的心脏组织表现出完全正常化的SERCA2A表达水平(图16d和16e)。
心力衰竭期间由于保留收缩性的补偿性机制而发生的正在进行的重塑导致收缩蛋白、肌钙蛋白T(TnT)和肌钙蛋白I(Tnl)的上调。与载体处理的野生型小鼠相比,载体处理的NS小鼠中TnT和TnI均显著升高(图16d、16f和16g)。达沙替尼治疗的NS小鼠显示了衰竭心脏表型的完全逆转,这是因为TnT和TnI表达水平都恢复到与载体处理的野生型小鼠相当的那些水平(图16d、16f和16g)。总的来说,这些发现清楚地表明,用达沙替尼对NS小鼠模型的发育后治疗减轻了心肌的收缩功能障碍。
表7:分离自出生后载体或达沙替尼治疗的WT和Ptpn11D
数据代表平均值±SEM。*,P<0.05;***,P<0.001表示与载体处理的WT心肌细胞相比的显著性。
先前,确定了跨膜糖蛋白PZR是NS小鼠心脏中的最异常高酪氨酰磷酸化的蛋白质(Eminagaet al.,J Biol Chem283,15328-15338(2008))。PZR是Shp2结合蛋白和SFK底物。PZR高酪氨酰磷酸化是增强的NS介导的Src信号传导的直接结果。这些数据表明,c-Src在NS相关的CHD的传播中起作用。
图25a-25f中呈现的数据表示在野生型(WT)和NSML(Ptpn11
如所显示的,6周龄的载体处理的Ptpn11
这是c-Src信号传导参与NS发病机制的第一个证据。其他组已报道Shp2以磷酸酶依赖的方式位于SFK的上游(Zhanget al.,Mol Cell13,341-355(2004))。这里证明了产生(引起,invoke)NS-Shp2突变体的“开放”构象提供增强的PTP-Shp2/Src-SH3结合和定位以促进c-Src信号传导的独特机制。以CML治疗所需的亚治疗剂量的达沙替尼的发育后施用足以恢复心脏的收缩性和功能。这些数据强烈地暗示c-Src作为NS介导的发病机制的中心介质。在低剂量的达沙替尼,Src途径似乎被选择性地影响,而至少在心肌中,ERK1/2信号传导被极小地抑制。然而,可以想象的是ERK1/2存在于受达沙替尼治疗影响的心脏中特异的细胞亚组中。
重要的是,从达沙替尼治疗的NS小鼠中分离的心肌细胞的钙介导的收缩偶联的分析清楚地表明,这些细胞是一种作用位点,通过该位点,c-Src的达沙替尼抑制对收缩机制发挥作用。与以前的观察一致,NS-Shp2突变体在心肌中增加Ca
总之,本文描述了用于治疗PTPN11介导的CHD的新颖且不曾预料的治疗策略。这些数据将Src激酶家族识别为一类介导PTPN11相关的CHD的靶标。“低剂量”达沙替尼或其他c-Src抑制剂的治疗策略可能开辟治疗心脏病的新途径。
其他实施方式
本文的变量的任何定义中要素的列表的叙述包括作为列出的要素的任何单个要素或组合(或亚组合)的变量的定义。本文的实施方式的叙述包括作为任何单个实施方式或与任何其它实施方式或其部分组合的实施方式。
本文引用的每个专利、专利申请和出版物的公开内容在此以其全部通过引用并入本文。虽然已经参考具体实施方式公开了本发明,但是显然本领域技术人员可以想出本发明的其它实施方式和变化,而不脱离本发明的真实精神和范围。所附权利要求意在被解释为包括所有这样的实施方式和等同变化。
序列表
<110> 耶鲁大学
<120> 利用酪氨酸激酶抑制剂的组合物和方法
<130> 047162-7053WO1(00378)
<150> 62/250,052
<151> 2015-11-03
<150> 62/107,553
<151> 2015-01-26
<160> 14
<170> PatentIn 版本3.5
<210> 1
<211> 21
<212> DNA
<213> 人工序列
<220>
<223> 合成序列
<400> 1
accgcagcta ggaataatgg a 21
<210> 2
<211> 19
<212> DNA
<213> 人工序列
<220>
<223> 合成序列
<400> 2
accaaaagcc ttgactccg 19
<210> 3
<211> 25
<212> DNA
<213> 人工序列
<220>
<223> 合成序列
<400> 3
cctggaggag aagatgccgg tagaa 25
<210> 4
<211> 24
<212> DNA
<213> 人工序列
<220>
<223> 合成序列
<400> 4
ccccagtcca gggaggcacc tcgg 24
<210> 5
<211> 26
<212> DNA
<213> 人工序列
<220>
<223> 合成序列
<400> 5
cacttcaaag gtggtcccag agctgc 26
<210> 6
<211> 23
<212> DNA
<213> 人工序列
<220>
<223> 合成序列
<400> 6
gaccggatcg gatccgtcag tcg 23
<210> 7
<211> 22
<212> DNA
<213> 人工序列
<220>
<223> 合成序列
<400> 7
gtcccggaca ctggaccagg cc 22
<210> 8
<211> 27
<212> DNA
<213> 人工序列
<220>
<223> 合成序列
<400> 8
ctccttttct tccagttgcc tagccaa 27
<210> 9
<211> 25
<212> DNA
<213> 人工序列
<220>
<223> 合成序列
<400> 9
gagcaaggcc gaggagacgc agcgt 25
<210> 10
<211> 26
<212> DNA
<213> 人工序列
<220>
<223> 合成序列
<400> 10
gagcctcctt ctcgtccagc tgccgg 26
<210> 11
<211> 20
<212> DNA
<213> 人工序列
<220>
<223> 合成序列
<400> 11
aggtcttcct ggagctgatg 20
<210> 12
<211> 20
<212> DNA
<213> 人工序列
<220>
<223> 合成序列
<400> 12
acccacaggg ccttctttac 20
<210> 13
<211> 24
<212> DNA
<213> 人工序列
<220>
<223> 合成序列
<400> 13
acagcaaatt cacttacaca gttc 24
<210> 14
<211> 19
<212> DNA
<213> 人工序列
<220>
<223> 合成序列
<400> 14
ctcattgcct tgcgtgttt 19
- 酪氨酸激酶抑制剂及包含该酪氨酸激酶抑制剂的药物组合物
- 酪氨酸激酶抑制剂及包含该酪氨酸激酶抑制剂的药物组合物
