一种可聚合的维生素B2类似物及其制备方法
文献发布时间:2023-06-19 18:37:28
技术领域
本发明涉及材料科学技术领域,具体涉及一种可聚合的维生素B2类似物及其制备方法。
背景技术
上世纪60年代,Clark和Lyons首次制备酶电极,提出了酶生物传感器的概念。随着生物、物理学、化学、医学和电子技术等多种学科的快速发展和学科交叉的推进,酶传感器凭借其分析速度快、选择性高、成本低廉且操作方便等其它生物传感器所无法比拟的优势而发展成为现代分析科学中重要的研究领域之一。
虽然酶生物传感器的研究已经取得了长足的发展,但是酶与电极之间的电子转移速率仍然限制着酶生物传感器的性能。酶生物传感器所要解决的中心问题就是使反应能够在恒电位下快速进行,将电子从酶的活性中心快速转移到电极表面,形成响应电流。所以电子转移的难易和速度决定着这类传感器的性能。由于酶的电活性中心一般深埋在蛋白质的内部,使得酶和电极间难以直接进行电子的转移。电子介体是指能将酶反应过程中产生的电子从酶的活性中心转移到电极表面,从而使电极产生相应电流变化的一类物质。因此,寻求适合的电子介体是构建酶生物传感器成功的关键。
第一代酶生物传感器是以天然氧为电子介体的,这类传感器具有响应特性差、易受环境中氧浓度的影响和其它电活性物质干扰等缺点。第二代酶生物传感器是利用人工合成的电子介体代替氧在酶和电极之间传递电子,加强了酶与电极间的电子转移,加速了电极反应,排除了环境中氧浓度对测量的影响,克服了第一代酶生物传感器的上述缺点,在酶生物传感器的研究中备受关注。发明人所在的上海交通大学朱新远课题组参照葡萄糖氧化酶活性中心(FAD)的结构,设计合成了一系列含有可聚合基团乙烯基改性的异咯嗪衍生物,并以其为电子介体应用于酶生物传感器,显著改善了酶生物传感器的性能(Xinyuan Zhu,et al,Biosensors and Bioelectronics,2021,174,112805;Xinyuan Zhu,et al,ACSApplied Energy Materials,2021,4,5034–5042)。根据结构与性能的关系,可通过优化含有可聚合基团乙烯基改性的异咯嗪衍生物的结构,可进一步提高传感器的灵敏度和抗干扰性能。
发明内容
本发明针对现有技术中可聚合的维生素B2类似物在实际应用过程中电子传输能力较低和溶解性较差的问题,提供一种可聚合的维生素B2类似物及其制备方法和应用,可用于构建灵敏度高和抗干扰能力强的酶生物传感器。
本发明第一个目的是提供一种可聚合的维生素B2类似物,其结构如通式(I)所示:
其中,R
进一步地,所述可聚合的维生素B2类似物为如下式(II)化合物:
进一步地,所述可聚合的维生素B2类似物包括以下化合物:
本发明第二个目的是式(II)所示化合物的制备方法,合成路线如下:
其中X为卤素。
进一步地,所述式(II)所示化合物的制备方法,包括以下步骤:
S1.将维生素B2加入到稀硫酸中搅拌,冰浴,缓慢滴加氧化剂溶液;待滴加结束后,移除冰浴,室温反应,待反应结束,经提纯,真空干燥得中间体FMF,其结构式为:
S2.将步骤S1中的FMF加入溶剂1中,搅拌,加入还原剂,室温反应,待反应结束,经提纯,真空干燥得中间体7,8-二甲基-10-羟基-异咯嗪(HEF),其结构式为:
S3.将
其中,m=2~7。
S4.将HEF和中间体A加入溶剂3中,加入碱2,加热反应,待反应结束,经提纯,真空干燥获得式(II)可聚合的维生素B2类似物。
式(I)化合物是采用相应取代基的维生素B2衍生物,或者在式(II)基础上进行基团的取代得到。其方法和条件为本领域所熟知。
进一步地,所述氧化剂为高碘酸、高碘酸钠或高碘酸钾中的至少一种;维生素B2与强氧化剂的摩尔比为1:2~1:6,优选1:3-4。
进一步地,所述还原剂为硼氢化钠或者氰基硼氢化钠,FMF和还原剂的摩尔比为1:1~1:3,优选1:1.5-2。
进一步地,步骤S3中,
进一步地,步骤S2中所述溶剂1为乙醇、甲醇、二甲基亚砜、N,N-二甲基甲酰胺、N,N-二甲基乙酰胺或四氢呋喃中的一种或几种;步骤S3中所述溶剂2为乙酸乙酯、二氯甲烷、二甲基亚砜、N,N-二甲基甲酰胺、N,N-二甲基乙酰胺、四氢呋喃、1,4二氧六环、丙酮或乙腈中的一种或几种;步骤S4中所述溶剂3为二甲基亚砜、N,N-二甲基甲酰胺、N,N-二甲基乙酰胺、四氢呋喃、1,4二氧六环或丙酮中的一种或几种。
进一步地,步骤S1、S2、S3和S4中所述提纯方式为硅胶层析法,所述真空干燥温度40~120℃,所述真空干燥时间为6~30h。
优选地,步骤S1、S2、S3和S4中所述干燥温度60~80℃,所述干燥时间为18~24h。
本发明第三个目的是提供一种酶修饰电极,是混合酶溶液滴加在电极上表面干燥得到,所述混合酶溶液的溶质包括氧化还原共聚物和葡萄糖氧化酶,所述氧化还原共聚物的单体包括上述可聚合的维生素B2类似物。
进一步地,所述氧化还原共聚物的单体包括维生素B2类似物,丙烯酰胺,N-丙烯酰氧基琥珀酰亚胺;更进一步地,维生素B2类似物,丙烯酰胺,N-丙烯酰氧基琥珀酰亚胺的摩尔比为3-5:10-15:1-1.5。
进一步地,混合酶溶液是氧化还原共聚物和葡萄糖氧化酶按照质量比为1-2:1-2溶于缓冲溶液得到,混合酶溶液中氧化还原共聚物的质量浓度为5-50mg/mL,优选10-20mg/mL。
进一步地所述电极是羧基化碳纳米管修饰的玻碳电极。
进一步地,所述酶修饰电极是通过包括以下步骤的制备方法得到:
(1)将可聚合的维生素B2类似物、丙烯酰胺(AAm)和N-丙烯酰氧基琥珀酰亚胺(NAS)聚合得到氧化还原聚合物;
(2)氧化还原聚合物和葡萄糖氧化酶溶于缓冲溶液中,得到混合酶溶液;
(3)羧基化碳纳米管(cMWCNTs)分散液滴加在玻碳电极上,干燥,再滴加混合酶溶液,在2-5℃下干燥,得到葡萄糖氧化酶修饰电极。
进一步地,步骤(1)中,聚合反应条件是是在DMSO中,惰性气氛下,加入引发剂升温反应;所述升温是升温至50-60℃,聚合反应时间2-4h,所述引发剂为过硫酸钠,过硫酸钾,过硫酸铵中的至少一种;聚合反应结束后用截留分子量为10000-13000的透析袋进行透析,2 -4h换一次透析液,除去未反应的单体、副产物以及部分低聚物;最终冷冻干燥得到氧化还原聚合物。
进一步地,步骤(2)中,所述缓冲溶液是pH为7.2-7.4的PBS缓冲溶液。
与现有技术相比,本发明具有以下有益效果:
本发明在异咯嗪环的结构上引入烯基,合成了一种含有可聚合基团乙烯基改性的异咯嗪衍生物。此类化合物可与其他单体共聚制备可用作电子介体的氧化还原聚合物。发明人预料不到地发现,异咯嗪环与烯基之间的连接链段采用了低聚乙二醇链段(重复单元数m为2~7),能够明显提高传感器的抗干扰能力。本发明所提出的含有可聚合基团乙烯基改性的异咯嗪衍生物所需原材料组分简单,合成工艺反应条件温和,简单易控,绿色环保。制备的产品易纯化,杂质较少,产率较高,因而适于大规模工业生产。
附图说明
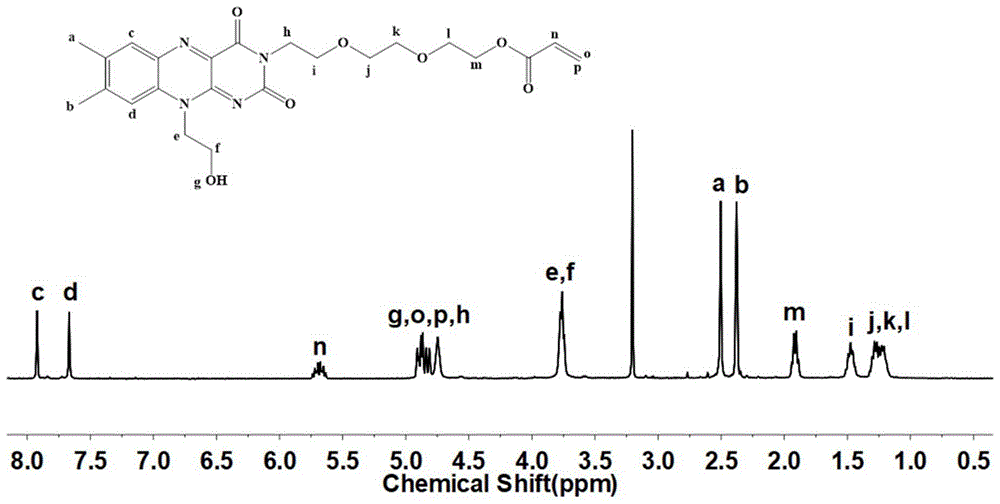
图1是实施例2中HEF-PEG-3的核磁氢谱图;
图2是实施例2中酶修饰电极在电解液(pH=7.4的PBS缓冲液)中加入葡萄糖前后酶修饰电极的CV曲线;
图3是实施例4中酶修饰电极在电解液(pH=7.4的PBS缓冲液)中加入葡萄糖前后酶修饰电极的CV曲线。
具体实施方式
下面结合附图和具体实施例进一步详细说明本发明。除非特别说明,本发明实施例使用的各种原料均可以通过常规市购得到,或根据本领域的常规方法制备得到,所用设备为实验常用设备。除非另有定义或说明,本文中所使用的所有专业与科学用语与本领域技术熟练人员所熟悉的意义相同。
实施例1
本实施例提供一种可聚合的维生素B2类似物及其制备方法和应用,具体步骤包括:
S1.HEF-PEG-2的合成:
S11.合成中间体7,8-二甲基-10-乙醛基-异咯嗪(FMF):
将5.6g(14.9mmoL,1eq)维生素B2添加到140mL的稀硫酸(1:35(v/v))中,0℃搅拌成悬浮液。接着,通过恒压滴液漏斗缓慢滴加90mL高碘酸水溶液(12.50g,54.8mmoL,3.7eq);待溶液滴加完成后,室温过夜反应。待反应结束后,加入2g活性炭,缓慢搅拌30分钟。随后,将反应液过滤,收集滤液,用饱和的Na
S12.合成中间体7,8-二甲基-10-羟乙基-异咯嗪(HEF)
具体合成过程如下:将284.3mg(1mmol)FMF和100mL甲醇加入到250mL两口瓶中,磁力搅拌,待HEF在甲醇中分散均匀,然后加入57mg(1.5mmol)NaBH
S13.合成Br-PEG-2:
具体合成过程如下:将338.4mg(2mmol)溴二乙二醇、303.6mg(3mmol)三乙胺和10mL超干的THF加入到25mL的单口瓶中,冰浴磁力搅拌,通过恒压滴液漏斗缓慢滴加362mg(3mmol)丙烯酰氯,滴加完毕后,室温反应24h。TLC跟踪反应,待反应结束后,抽滤得到滤液;接着将反应液减压蒸去溶剂,产物以石油醚∶乙酸乙酯=20∶1(体积比)为流动相,以硅胶为固定相作柱色谱提纯,收集产物并旋干得到无色液体,油泵抽干,得到334.6mg产物,产率为75%。该中间体Br-PEG-2结构如下:
S14.合成HEF-PEG-2:
具体合成过程如下:将286.3mg(1mmol)HEF、691mg(5mmol)碳酸钾和60mL DMF加入到150mL的单口瓶中,磁力搅拌,油浴加热至65℃后,加入1115.4mg(5mmol)Br-PEG-2,避光反应8h。TLC跟踪反应,待反应结束后,加入100mL DMF,抽滤得到滤液,接着将反应液减压蒸去溶剂,产物以石油醚∶乙酸乙酯=1∶3(体积比)为流动、以硅胶为固定相作柱色谱提纯,收集产物并旋干得到黄色固体,在80℃真空中干燥24h,得到265.6mg产物,产率为62%。
S2.共聚物poly(HEF-PEG-2-AM)的合成
将HEF-PEG-2、丙烯酰胺(AAm)和N-丙烯酰氧基琥珀酰亚胺(NAS)加入二甲基亚砜(DMSO)中,将反应液混合均匀,持续氮气鼓泡30min,尽可能排除溶液中氧气;缓慢加入四甲基乙二胺(TEMED)后,迅速加入过硫酸铵(APS),将混合物加热至50℃反应2小时;待反应结束后,采用截留分子量为10000的透析袋在DMSO中透析,2h换一次透析液,除去未反应的单体、副产物以及部分低聚物;接着在去离子水中透析,完成溶剂置换,待置换完成后,将共聚物的水溶液冷冻干燥得到共聚物poly(HEF-PEG-2-AM)。聚合反应中各个反应物的摩尔比参照表1。
表1共聚物poly(HEF-PEG-2-AM)的合成参数
*所有数字均表示摩尔比
S3.酶修饰电极的制备
取10mg poly(HEF-PEG-2-AM)和10mg葡萄糖氧化酶溶于1mL pH=7.4的PBS缓冲液,混合均匀,反应1小时。同时,将玻碳电极(GCE)(直径3mm)依次用300nm和50nm粒径的氧化铝浆料进行打磨,然后依次用超纯水和乙醇进行清洗。接着将10μL羧基化碳纳米管(cMWCNTs)分散液(1mg/mL)滴加在抛光的GCE表面,并将电极在室温下干燥,所得电极表示为cMWCNT/GCE。接着,取10μl混合酶溶液滴加到cMWCNT/GCE表面,在4℃下干燥,得到葡萄糖氧化酶修饰电极1。
S4.酶修饰电极的葡萄糖响应性:
选用Ag/AgCl作为参比电极,铂丝作为对电极和上述自制酶修饰电极作为工作电极构建三电极体系,使用循环伏安法测试20mM glucose溶液(pH=7.4的PBS缓冲液)对应的响应电流。
实施例2
本实施例提供一种可聚合的维生素B2类似物及其制备方法和应用,具体步骤包括:
S1.HEF-PEG-3的合成:
S11.合成Br-PEG-3:
具体合成过程如下:将338.4mg(2mmol)溴-三聚乙二醇、303.6mg(3mmol)三乙胺和10mL超干的THF加入到25mL的单口瓶中,冰浴磁力搅拌,通过恒压滴液漏斗缓慢滴加362mg(3mmol)丙烯酰氯,滴加完毕后,室温反应24h。TLC跟踪反应,待反应结束后,抽滤得到滤液;接着将反应液减压蒸去溶剂,产物以石油醚∶乙酸乙酯=40∶3(体积比)为流动相,以硅胶为固定相作柱色谱提纯,收集产物并旋干得到无色液体,油泵抽干,得到374mg产物,产率为70%。
S12.合成HEF-PEG-3:
具体合成过程如下:将286.3mg(1mmol)HEF、691mg(5mmol)碳酸钾和60mL DMF加入到150mL的单口瓶中,磁力搅拌,油浴加热至65℃后,加入1336mg(5mmol)Br-PEG-3,避光反应8h。TLC跟踪反应,待反应结束后,加入100mL DMF,抽滤得到滤液,接着将反应液减压蒸去溶剂,产物以石油醚∶乙酸乙酯=1∶4(体积比)为流动、以硅胶为固定相作柱色谱提纯,收集产物并旋干得到黄色固体,在60℃真空中干燥24h,得到283.5mg产物,产率为60%。
S2.共聚物poly(HEF-PEG-3-AM)的合成
将HEF-PEG-3、丙烯酰胺(AAm)和N-丙烯酰氧基琥珀酰亚胺(NAS)加入二甲基亚砜(DMSO)中,将反应液混合均匀,持续氮气鼓泡30min,尽可能排除溶液中氧气;缓慢加入四甲基乙二胺(TEMED)后,迅速加入过硫酸铵(APS),将混合物加热至50℃反应2小时;待反应结束后,采用截留分子量为10000的透析袋在DMSO中透析,2h换一次透析液,除去未反应的单体、副产物以及部分低聚物;接着在去离子水中透析,完成溶剂置换,待置换完成后,将共聚物的水溶液冷冻干燥得到共聚物poly(HEF-PEG-3-AM)。聚合反应中各个反应物的摩尔比参照表2。
表2共聚物poly(HEF-PEG-3-AM)的合成参数
*所有数字均表示摩尔比
S3.酶修饰电极的制备
取10mg poly(HEF-PEG-3-AM)和10mg葡萄糖氧化酶溶于1mL pH=7.4的PBS缓冲液,混合均匀,反应1小时。同时,将玻碳电极(GCE)(直径3mm)依次用300nm和50nm粒径的氧化铝浆料进行打磨,然后依次用超纯水和乙醇进行清洗。接着将10μL cMWCNTs分散液(1mg/mL)滴加在抛光的GCE表面,并将电极在室温下干燥,所得电极表示为cMWCNT/GCE。接着,取10μl混合酶溶液滴加到cMWCNT/GCE表面,在4℃下干燥,得到葡萄糖氧化酶修饰电极2。
S4.酶修饰电极的葡萄糖响应性:
选用Ag/AgCl作为参比电极,铂丝作为对电极和上述自制酶修饰电极作为工作电极构建三电极体系,使用循环伏安法测试20mM glucose溶液(pH=7.4的PBS缓冲液)对应的响应电流。
实施例3
本实施例提供一种可聚合的维生素B2类似物及其制备方法和应用,具体步骤包括:
S1.HEF-PEG-4的合成:
S11.合成Br-PEG-4:
具体合成过程如下:将514.2mg(2mmol)溴代-四聚乙二醇、252mg(3mmol)碳酸氢钠和10mL超干的乙酸乙酯加入到25mL的单口瓶中,冰浴磁力搅拌,通过恒压滴液漏斗缓慢滴加362mg(3mmol)丙烯酰氯,滴加完毕后,室温反应24h。TLC跟踪反应,待反应结束后,抽滤得到滤液;接着将反应液减压蒸去溶剂,产物以石油醚∶乙酸乙酯=40∶3(体积比)为流动相,以硅胶为固定相作柱色谱提纯,收集产物并旋干得到无色液体,油泵抽干,得到485.4mg产物,产率为78%。该中间体结构如下:
S12.合成HEF-PEG-4:
具体合成过程如下:将286.3mg(1mmol)HEF、691mg(5mmol)碳酸钾和60mL DMF加入到150mL的单口瓶中,磁力搅拌,油浴加热至65℃后,加入1555.9mg(5mmol)Br-PEG-4,避光反应10h。TLC跟踪反应,待反应结束后,加入100mL DMF,抽滤得到滤液,接着将反应液减压蒸去溶剂,产物以石油醚∶乙酸乙酯=1∶4(体积比)为流动、以硅胶为固定相作柱色谱提纯,收集产物并旋干得到黄色固体,在80℃真空中干燥24h,得到372mg产物,产率为72%。
S2.共聚物poly(HEF-PEG-4-AM)的合成
将HEF-PEG-4、丙烯酰胺(AAm)和N-丙烯酰氧基琥珀酰亚胺(NAS)加入二甲基亚砜(DMSO)中,将反应液混合均匀,持续氮气鼓泡30min,尽可能排除溶液中氧气;缓慢加入四甲基乙二胺(TEMED)后,迅速加入过硫酸铵(APS),将混合物加热至50℃反应2小时;待反应结束后,采用截留分子量为10000的透析袋在DMSO中透析,2h换一次透析液,除去未反应的单体、副产物以及部分低聚物;接着在去离子水中透析,完成溶剂置换,待置换完成后,将共聚物的水溶液冷冻干燥得到共聚物poly(HEF-PEG-4-AM)。聚合反应中各个反应物的摩尔比参照表3。
表3共聚物poly(HEF-PEG-4-AM)的合成参数
*所有数字均表示摩尔比
S3.酶修饰电极的制备
取1mg poly(HEF-PEG-4-AM)和10mg葡萄糖氧化酶溶于1mL pH=7.4的PBS缓冲液,混合均匀,反应1小时。同时,将玻碳电极(GCE)(直径3mm)依次用300nm和50nm粒径的氧化铝浆料进行打磨,然后依次用超纯水和乙醇进行清洗。接着将10μL cMWCNTs分散液(1mg/mL)滴加在抛光的GCE表面,并将电极在室温下干燥,所得电极表示为cMWCNT/GCE。接着,取10μl混合酶溶液滴加到cMWCNT/GCE表面,在4℃下干燥,得到葡萄糖氧化酶修饰电极3。
S4.酶修饰电极的葡萄糖响应性:
选用Ag/AgCl作为参比电极,铂丝作为对电极和上述自制酶修饰电极作为工作电极构建三电极体系,使用循环伏安法测试20mM glucose溶液(pH=7.4的PBS缓冲液)对应的响应电流。
实施例4
本实施例提供一种可聚合的维生素B2类似物及其制备方法和应用,具体步骤包括:
S1.HEF-PEG-7的合成:
S11.合成Br-PEG-7:
具体合成过程如下:将778.6mg(2mmol)溴代-七聚乙二醇、252mg(3mmol)碳酸氢钠和10mL超干的四氢呋喃加入到25mL的单口瓶中,冰浴磁力搅拌,通过恒压滴液漏斗缓慢滴加362mg(3mmol)丙烯酰氯,滴加完毕后,室温反应24h。TLC跟踪反应,待反应结束后,抽滤得到滤液;接着将反应液减压蒸去溶剂,产物以石油醚∶乙酸乙酯=5∶1(体积比)为流动相,以硅胶为固定相作柱色谱提纯,收集产物并旋干得到无色液体,油泵抽干,得到532mg产物,产率为60%。该中间体结构如下:
S12.合成HEF-PEG-7:
具体合成过程如下:将286.3mg(1mmol)HEF、691mg(5mmol)碳酸钾和60mL DMF加入到150mL的单口瓶中,磁力搅拌,油浴加热至65℃后,加入2216.7mg(5mmol)Br-PEG-7,避光反应8h。TLC跟踪反应,待反应结束后,加入100mL DMF,抽滤得到滤液,接着将反应液减压蒸去溶剂,产物以石油醚∶乙酸乙酯=1:2(体积比)为流动、以硅胶为固定相作柱色谱提纯,收集产物并旋干得到黄色固体,在60℃真空中干燥24h,得到356.8mg产物,产率为55%。
S2.共聚物poly(HEF-PEG-7-AM)的合成
将HEF-PEG-7、丙烯酰胺(AAm)和N-丙烯酰氧基琥珀酰亚胺(NAS)加入二甲基亚砜(DMSO)中,将反应液混合均匀,持续氮气鼓泡30min,尽可能排除溶液中氧气;缓慢加入四甲基乙二胺(TEMED)后,迅速加入过硫酸铵(APS),将混合物加热至50℃反应2小时;待反应结束后,采用截留分子量为10000的透析袋在DMSO中透析,2h换一次透析液,除去未反应的单体、副产物以及部分低聚物;接着在去离子水中透析,完成溶剂置换,待置换完成后,将共聚物的水溶液冷冻干燥得到共聚物poly(HEF-PEG-7-AM)。聚合反应中各个反应物的摩尔比参照表4。
表4共聚物poly(HEF-PEG-7-AM)的合成参数
*所有数字均表示摩尔比
S3.酶修饰电极的制备
取10mg poly(HEF-PEG-7-AM)和10mg葡萄糖氧化酶溶于1mL pH=7.4的PBS缓冲液,混合均匀,反应1小时。同时,将玻碳电极(GCE)(直径3mm)依次用300nm和50nm粒径的氧化铝浆料进行打磨,然后依次用超纯水和乙醇进行清洗。接着将10μL cMWCNTs分散液(1mg/mL)滴加在抛光的GCE表面,并将电极在室温下干燥,所得电极表示为cMWCNT/GCE。接着,取10μl混合酶溶液滴加到cMWCNT/GCE表面,在4℃下干燥,得到葡萄糖氧化酶修饰电极4。
S4.酶修饰电极的葡萄糖响应性:
选用Ag/AgCl作为参比电极,铂丝作为对电极和上述自制酶修饰电极作为工作电极构建三电极体系,使用循环伏安法测试20mM glucose溶液(pH=7.4的PBS缓冲液)对应的响应电流。
对比例1
S1.HEF-C-13的合成
S11.合成11-溴丙烯酸癸酯:
具体合成过程如下:将502.4mg(2mmol)11-溴-1-十一醇、303.6mg(3mmol)三乙胺和10mL超干的THF加入到25mL的单口瓶中,冰浴磁力搅拌,通过恒压滴液漏斗缓慢滴加362mg(4mmol)丙烯酰氯,滴加完毕后,室温反应24h。TLC跟踪反应,待反应结束后,抽滤得到滤液;接着将反应液减压蒸去溶剂,产物以石油醚∶乙酸乙酯=20:1(体积比)为流动相,以硅胶为固定相作柱色谱提纯,收集产物并旋干得到无色液体,油泵抽干,得到427mg产物,产率为70%。11-溴丙烯酸癸酯的结构如下:
S2.合成HEF-C-13:
具体合成过程如下:将286.3mg(1mmol)HEF、691mg(5mmol)碳酸钾和60mL DMF加入到150mL的单口瓶中,磁力搅拌,油浴加热至60℃后,加入1526.3mg(5mmol)11-bromoundecyl acrylate,避光反应18h。TLC跟踪反应,待反应结束后,加入100mL DMF,抽滤得到滤液;接着将反应液减压蒸去溶剂,产物以石油醚∶乙酸乙酯=1:10(体积比)为流动相,以硅胶为固定相作柱色谱提纯,收集产物并旋干得到黄色固体,在60℃真空中干燥24h,得到306mg产物,产率为60%。
S2.共聚物poly(HEF-C-13-AM)的合成
将HEF-C-13、丙烯酰胺(AAm)和N-丙烯酰氧基琥珀酰亚胺(NAS)加入二甲基亚砜(DMSO)中,将反应液混合均匀,持续氮气鼓泡30min,尽可能排除溶液中氧气;缓慢加入四甲基乙二胺(TEMED)后,迅速加入过硫酸铵(APS),将混合物加热至50℃反应2小时;待反应结束后,采用截留分子量为10000的透析袋在DMSO中透析,2h换一次透析液,除去未反应的单体、副产物以及部分低聚物;接着在去离子水中透析,完成溶剂置换,待置换完成后,将共聚物的水溶液冷冻干燥得到共聚物poly(HEF-C-13-AM)。聚合反应中各个反应物的摩尔比参照表5。
表5共聚物poly(HEF-C-13-AM)的合成参数
*所有数字均表示摩尔比
S3.酶修饰电极的制备
取10mg poly(HEF-C-13-AM)和10mg葡萄糖氧化酶溶于1mL pH=7.4的PBS缓冲液,混合均匀(poly(HEF-C-13-AM)在1mL pH=7.4的PBS缓冲液中只能溶解0.5g),反应1小时。同时,将玻碳电极(GCE)(直径3mm)依次用300nm和50nm粒径的氧化铝浆料进行打磨,然后依次用超纯水和乙醇进行清洗。接着将10μL cMWCNTs分散液(1mg/mL)滴加在抛光的GCE表面,并将电极在室温下干燥,所得电极表示为cMWCNT/GCE。接着,取10μl混合酶溶液滴加到cMWCNT/GCE表面,在4℃下干燥,得到葡萄糖氧化酶修饰电极5。
S4.酶修饰电极的葡萄糖响应性:
使用电化学工作站测试在电解液(pH=7.4的PBS缓冲液)中加入葡萄糖前后酶修饰电极的CV曲线。
对比例2
S1.酶修饰电极的制备
取10mg葡萄糖氧化酶溶于1mL pH=7.4的PBS缓冲液,混合均匀,反应1小时;取10μl酶溶液滴加到cMWCNT/GCE表面,在4℃下干燥,得到葡萄糖氧化酶修饰电极6。
S2.酶修饰电极的葡萄糖响应性:
使用电化学工作站测试在电解液(pH=7.4的PBS缓冲液)中加入葡萄糖前后酶修饰电极的CV曲线。将前后CV曲线中氧化峰电流密度的增加定义为催化电流(ΔIp),并从CV曲线中读取各个酶修饰电极的氧化还原电位,结果如下表6所示:
表6
由图2和图3可知,以含异咯嗪环的氧化还原聚合物为电子介体构建的酶修饰电极具有优异的葡萄糖响应性和较低的氧化还原电位。由表6可知,本发明制备的酶修饰电极对葡萄糖都具有优异的响应性,且实施例均优于对比例1,并且随着PEG链长度的增加,催化电流也随之增加,由于PEG链长度是容易进行调控的,说明本发明引入聚乙二醇链段改善酶生物传感器的灵敏度的策略是成功的。
