一种甲硫氨酸循环关键代谢物的绝对定量分析方法及应用
文献发布时间:2023-06-19 18:46:07
技术领域
本发明属于分析检测技术领域,具体涉及一种甲硫氨酸循环关键代谢物的绝对定量分析方法及应用。
背景技术
甲硫氨酸分子中含有S-甲基,可通过各种转甲基作用生成富含甲基的多种生理活性物质,甲硫氨酸在腺苷转移酶的催化下与ATP反应,生成S-腺苷甲硫氨酸(SAM),S-腺苷甲硫氨酸中的甲基为活性甲基,经甲基转移酶催化后,可将甲基转移至其他物质,使其甲基化,而S-腺苷甲硫氨酸去甲基化后生成S-腺苷同型半胱氨酸(SAH),S-腺苷同型半胱氨酸脱去腺苷生成同型半胱氨酸(HCY),同型半胱氨酸再接受5-甲基四氢叶酸上的甲基,重新生成甲硫氨酸,形成一个循环。在甲硫氨酸循环中,同型半胱氨酸在胱硫醚-β-合成酶催化下生成胱硫醚,胱硫醚会进一步生成半胱氨酸,约50%的同型半胱氨酸在胱硫醚β合成酶的作用下,最终生成半胱氨酸(CYS),半胱氨酸在γ-谷氨酰胺半胱氨酸合成酶的作用下生成还原型谷胱甘肽(GSH)。此外,甜菜碱(BET)是胆碱(CHO)氧化代谢的终产物,是一种重要的甲基化剂,通过甜菜碱高半胱氨酸-S-甲基转移酶参与甲硫氨酸的生物合成(甲硫氨酸循环关键代谢物体内转化示意图见附图1)。
正常血浆总同型半胱氨酸浓度一般在5-15μmol/L,平均浓度大约为10μmol/L。血浆总同型半胱氨酸浓度越高,患心脑血管疾病(如冠心病,动脉粥样硬化),肾功能障碍和糖尿病等糖脂代谢紊乱相关疾病的风险越高。当人体的新陈代谢出现障碍时,同型半胱氨酸会由于无法降解而在体内聚集。高浓度的同型半胱氨酸会对血管内壁造成损害,使血管内膜增厚、粗糙,形成斑块,进而使管腔狭窄甚至阻塞,动脉供血不全,导致动脉粥样硬化和冠心病的发生。由此可知,在一种或多种因素的影响下,人体同型半胱氨酸升高,使得细胞、组织及器官发生病变,从而对人体健康造成严重影响。同型半胱氨酸升高是人体代谢异常的结果,其代谢通路上涉及9种重要代谢物包括甲硫氨酸(MET)、同型半胱氨酸(HCY)、半胱氨酸(CYS)、胆碱(CHO)、甜菜碱(BET)、还原型谷胱甘肽(GSH)、S-腺苷同型半胱氨酸(SAH)、S-腺苷甲硫氨酸(SAM)、谷氨酸(GLU),它们的含量变化,可在一定程度上反应甲硫氨酸循环代谢水平的变化,把它们作为检测指标,通过检测并控制这些代谢物处于合适的水平范围内,可有效预防疾病发生或控制高同型半胱氨酸血症病情发展。
针对以同型半胱氨酸为代表的甲硫氨酸代谢途径标志物的检测方法包括高效液相色谱法、光谱法、化学发光法、放射酶免疫法以及酶比色法等。上述的传统检测方法操作过程繁琐复杂,且灵敏度和特异性不足,尤其是对基质复杂且含量较低的内源性物质,检测效果不理想,无法满足检测需要。如中文文献“基于HPLC-MS的早期胃癌血清和尿液代谢组学研究”报道了通过高效液相色谱-质谱联用技术比较早期胃癌组,慢性浅表性胃炎组,正常人群组血清和尿液小分子代谢产物的差异,其中包括对血清中的二氢胆固醇,胆固醇,酪氨酸,乳酸,酪胺,3-羟基丙酸,丙酮酸,丙氨酸,溶血磷脂酰胆碱(18:0)等9种代谢物的筛选和鉴定,(刘通.基于HPLC-MS的早期胃癌血清和尿液代谢组学研究[D].右江民族医学院,2017.),但该文献并未对甲硫氨酸的循环代谢物进行全面分析和鉴定;再如中文文献“血样中含硫醇类氨基酸代谢产物的分离及定量研究”报道了利用液相色谱-三级四级杆质谱联用对同型半胱氨酸代谢途径的相关物质进行同时检测:包括甲硫氨酸(MET),S-腺苷甲硫氨酸(SAM),同型半胱氨酸(HCY),S-腺苷同型半胱氨酸(SAH),胱硫醚(Cysta),半胱氨基甘氨酸(Cys-Gly),谷胱甘肽(GSH)。建立了一种同时对人血样中7种含硫醇类氨基酸代谢产物进行定量的HPLC-MS/MS方法,但该文献针对叶酸缺乏小鼠、高血压患者的血浆进行检测,且采用的是高效液相色谱-荧光检测方法以及高效液相色谱-紫外吸收检测,该方法对于甲硫氨酸循环代谢产物的定量检测并不理想(江芝婷.血样中含硫醇类氨基酸代谢产物的分离及定量研究.)。因此,目前能够同时检测同型半胱氨酸、甲硫氨酸、半胱氨酸、胆碱、甜菜碱、还原型谷胱甘肽、S-腺苷同型半胱氨酸、S-腺苷甲硫氨酸、谷氨酸等9种物质的HPLC-MS/MS方法未有报道,且由于血清基质复杂,与待测物理化性质相似的内源性物质非常多,会影响结果的灵敏度和准确性,因此,亟需开发一种甲硫氨酸代谢途径标志物的全面的分析方法。
发明内容
针对现有技术中存在的问题,本发明提出了一种甲硫氨酸循环关键代谢物的绝对定量分析方法,基于高效还原-巯基衍生化策略与HPLC-MS/MS检测平台相结合的甲硫氨酸循环关键代谢物的绝对定量分析方法,可同时对ng-μg级别的不同水平物质同时检测,检测范围广,不受结构类似物的影响,并且样品用量少、分析时间短。
第一方面,本发明提供了一种甲硫氨酸循环关键代谢物的绝对定量分析方法,其特征在于,所述方法包括如下步骤:
S1、标本预处理:将血清标本进行高效还原-巯基衍生化预处理并去除干扰蛋白质;
S2、色谱分离:将经过步骤S1处理过的标本注入到高效液相色谱柱中完成标本的初步分离;
S3、质谱鉴定:将步骤S2初步分离后的标本通过质谱仪完成定量分析离子碎片的强度分析和质谱图的采集。
进一步地,本发明提供了所述步骤S1标本预处理的步骤:
1)配制含有氘代苯丙氨酸的甲醇溶液,作为储备溶液备用;
2)配制含有N-乙基马来酰亚胺溶液,充分溶解,备用;
3)配制含有三(2-羰基乙基)磷盐酸盐的溶液,充分溶解,备用;
4)预处理去除干扰蛋白前的前处理;
更进一步地,所述步骤4)的前处理包括以下步骤:
a)配制标准曲线样品溶液:称取甲硫氨酸、胆碱、甜菜碱、S-腺苷同型半胱氨酸、S-腺苷甲硫氨酸、谷氨酸的标准品,用甲醇溶液分别配置成储备溶液,称取同型半胱氨酸、半胱氨酸、还原型谷胱甘肽的标准品,用N-乙基马来酰亚胺溶液配置成储备溶液,分别得到甲硫氨酸、胆碱、甜菜碱、S-腺苷同型半胱氨酸、S-腺苷甲硫氨酸、同型半胱氨酸、谷氨酸和半胱氨酸和还原型谷胱甘肽的系列标准品溶液;
b)配制标本:取血清至EP管内,充分涡旋均匀即得一份标本,进行以下步骤处理;
①高效还原-巯基衍生化:先向96孔蛋白沉淀板中加入血清,加入三(2-羰基乙基)磷盐酸盐溶液,使用96孔板振荡器混合均匀后静置,随后加入N-乙基马来酰亚胺,再加入含有氘代苯丙氨酸的甲醇溶液,使用96孔板振荡器混合均匀后室温静置;
②预处理去除干扰蛋白:使用生物样品前处理仪将经过步骤①后获得的溶液收集到洁净的收集板中备用,所得溶液即为去除干扰蛋白的待测物溶液;
③预处理样品干燥及复溶:将收集板里的溶液用氮气吹干,吹干后标本在甲醇-水溶液中复溶,然后在涡旋器上混合均匀后即可进行后续测试。
进一步地,本发明提供了所述步骤S2色谱分离的高效液相色谱流速设定为300μL/min,柱温固定在30℃,进样量设定为10μL。
进一步地,本发明还提供了所述步骤S2色谱分离的高效液相色谱流动程序为:
0min时,0.1%甲酸-水溶液的占比为95%,0.1%甲酸-甲醇溶液或0.1%甲酸-80%甲醇-20%乙腈溶液的占比为5%;
1min时,0.1%甲酸-水溶液的占比为5%,0.1%甲酸-甲醇溶液或0.1%甲酸-80%甲醇-20%乙腈溶液的占比为95%;
2min时,0.1%甲酸-水溶液的占比为80%,0.1%甲酸-甲醇溶液或0.1%甲酸-80%甲醇-20%乙腈溶液的占比为20%;
3min时,0.1%甲酸-水溶液的占比为80%,0.1%甲酸-甲醇溶液或0.1%甲酸-80%甲醇-20%乙腈溶液的占比为20%;
5min时,0.1%甲酸-水溶液的占比为90%,0.1%甲酸-甲醇溶液或0.1%甲酸-80%甲醇-20%乙腈溶液的占比为10%;
7min时,0.1%甲酸-水溶液的占比为95%,0.1%甲酸-甲醇溶液或0.1%甲酸-80%甲醇-20%乙腈溶液的占比为5%;
10min时,停止;
进一步地,本发明提供了所述步骤S3使用的质谱仪采用了Turbo VTM离子源和帘气的设计、电离模式是电喷雾电离、质量分析器是三重四级杆,所述三重四级杆采用的是多反应检测模式进行扫描检测。
进一步地,本发明提供了所述甲硫氨酸循环关键代谢物包括甲硫氨酸、同型半胱氨酸、半胱氨酸、胆碱、甜菜碱、还原型谷胱甘肽、S-腺苷同型半胱氨酸、S-腺苷甲硫氨酸和/或谷氨酸。
第二方面,本发明提供了一种甲硫氨酸循环关键代谢物的绝对定量分析方法在制备同型半胱氨酸血症试剂盒中的应用。
第三方面,本发明提供了一种甲硫氨酸循环关键代谢物绝对定量分析的HPLC-MS/MS检测平台构建方法,其特征在于,所述检测平台包括如下系统:
1)色谱分离系统
所述色谱分离系统中色谱柱采用Waters
2)质谱鉴定系统
所述质谱鉴定系统中质谱仪采用了Turbo VTM离子源和帘气的设计、电离模式是电喷雾电离、质量分析器是三重四级杆,所述三重四级杆采用的是多反应检测模式进行扫描检测。
第四方面,本发明提供了利用上述方法构建的HPLC-MS/MS检测平台在制备同型半胱氨酸血症试剂盒中的应用。
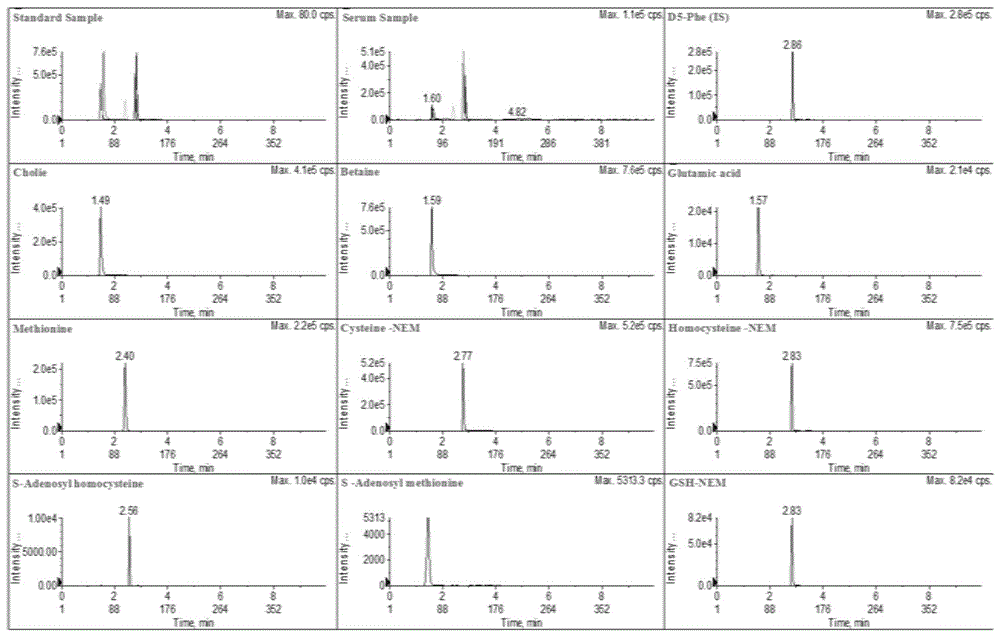
本研究利用HPLC-MS/MS分析平台,以三(2-羰基乙基)磷盐酸盐(TECP)为高效还原剂,以N-乙基马来酰亚胺(NEM)为巯基保护试剂,以氘代苯丙氨酸(D5-Phe)为内标物质,构建了绝对定量分析检测血清中甲硫氨酸(MET)、同型半胱氨酸(HCY)、半胱氨酸(CYS)、胆碱(CHO)、甜菜碱(BET)、还原型谷胱甘肽(GSH)、S-腺苷同型半胱氨酸(SAH)、S-腺苷甲硫氨酸(SAM)、谷氨酸(GLU)的方法,绘制每种目标甲硫氨酸代谢物对应的标准曲线;并进一步验证了该方法平台的定量限、线性范围,通过加标回收实验评价其准确性和血清基质对结果的影响,分析计算该平台检测的偏倚以评价其精密度,最终成功建立了一个稳定的、灵敏而可靠的定量检测人血清中同型半胱氨酸、甲硫氨酸、半胱氨酸、胆碱、甜菜碱、还原型谷胱甘肽、S-腺苷同型半胱氨酸、S-腺苷甲硫氨酸、谷氨酸等9种物质的检测平台(具体见附图2)。
本发明通过预处理、色谱参数和质谱条件的选择优化,建立了HPLC-MS/MS液质联用平台,并对该技术的性能进行验证。
首先是标准曲线的绘制和线性相关性的验证,由于血清中含有甲硫氨酸、胆碱、甜菜碱、S-腺苷同型半胱氨酸、S-腺苷甲硫氨酸、同型半胱氨酸、半胱氨酸、还原型谷胱甘和谷氨酸等9种物质,因此需对血清进行剔除内源性物质的处理,本研究采用活性炭吸附法,处理血清样品,具体方法为:在20mL血清中加入1.5g活性炭,37℃下剧烈旋转3h,并在21380×g离心15min。上清液依次通过0.45μm和0.22μm滤膜后使用HPLC-MS/MS确认其不含或仅含有少量甲硫氨酸、胆碱、甜菜碱、S-腺苷同型半胱氨酸、S-腺苷甲硫氨酸、同型半胱氨酸、半胱氨酸、还原型谷胱甘和谷氨酸等9种物质,以活性炭吸附处理的血清作为血清基质。使用经活性炭吸附处理的血清为基质配制不同浓度梯度的甲硫氨酸、胆碱、甜菜碱、S-腺苷同型半胱氨酸、S-腺苷甲硫氨酸、同型半胱氨酸、半胱氨酸、谷氨酸和还原型谷胱甘肽等9种化合物的标准曲线样品溶液,分析9种化合物的实测浓度和配制浓度之间的r值分别为0.9999,0.9997,0.9999,0.9996,0.9995,0.9995,0.9999,0.9998和0.9995,相关系数R
然后经过HPLC-MS/MS技术平台准确度的验证,本发明以高(C)、中(E)、低(J)三个浓度水平加样回收率试验,结果显示9种甲硫氨酸循环关键代谢物在PBS为基质的高、中、低三个浓度水平均具有满意的回收率,在85%至115%范围内。证明该方法平台能够以高准确度定量分析以血清为基质的溶液中的甲硫氨酸、胆碱、甜菜碱、S-腺苷同型半胱氨酸、S-腺苷甲硫氨酸、同型半胱氨酸、半胱氨酸、谷氨酸和还原型谷胱甘肽等9种化合物。
而本发明是对血清中的9种甲硫氨酸循环关键代谢物进行检测和分析,故而本发明以血清为基质进行加标回收率实验以确定基质效应的大小,结果显示以血清为基质时,加标回收率也可控制在85%~115%范围内,说明该平台性能稳定,受人血清基质效应影响较小,适用于对人血清中甲硫氨酸、胆碱、甜菜碱、S-腺苷同型半胱氨酸、S-腺苷甲硫氨酸、同型半胱氨酸、半胱氨酸、谷氨酸和还原型谷胱甘肽等9种化合物的定量检测分析。
最后,本发明对HPLC-MS/MS检测平台的精密度进行验证,先后6次应用本发明的HPLC-MS/MS检测平台定量检测高浓度水平、中浓度水平和低浓度水平的9种蛋氨酸循环关键代谢物(具体见附图3~5),分析6次检测结果的批内偏倚值大小,以此来评估HPLC-MS/MS平台的精密度大小,分析结果提示,高、中、低三个浓度水平的CV值均小于15%,符合仪器精密度的要求。
与现有技术相比,本发明的有益效果如下:
(1)本发明选用氘代苯丙氨酸作为定量检测9种待测甲硫氨酸循环关键代谢物类物质的内标物,分子量以及结构等特性与所要检测的代谢物相近,所以设定的质谱仪参数既适用于内标物氘代苯丙氨酸的电离和检测,也满足待检的甲硫氨酸循环关键代谢物类类物质的定量分析,因此,同位素标记的化合物是作为内标的最佳选择。
(2)本发明的方法在标本预处理时采用三(2-羰基乙基)磷盐酸盐为高效还原试剂,极大地保护了血清样本中易被氧化的同型半胱氨酸、半胱氨酸以及还原型谷胱甘肽,以N-乙基马来酰亚胺为巯基保护试剂,使用N-乙基马来酰亚胺与同型半胱氨酸、半胱氨酸以及还原型谷胱甘肽的巯基结合,形成稳定的同型半胱氨酸、半胱氨酸以及还原型谷胱甘肽衍生物,大大地提高了这三种物质的检测灵敏度。同型半胱氨酸、半胱氨酸、还原型谷胱甘肽,检测灵敏度分别提高了14.44倍、5.08倍、3.41倍,此外,同型半胱氨酸、半胱氨酸以及还原型谷胱甘肽衍生物的稳定性亦显著优于原性化合物。
(3)本发明的方法中采用三重四级杆的多反应检测模式(Multi-reactiionmonitoring,MRM)进行扫描检测,限定母离子和子离子两个参数,选择性极高,提高了灵敏度。
(4)本发明通过优化前处理方法,从而实现对同型半胱氨酸、甲硫氨酸、半胱氨酸、胆碱、甜菜碱、还原型谷胱甘肽、S-腺苷同型半胱氨酸、S-腺苷甲硫氨酸、谷氨酸等9种物质的准确检测,可用于制备同型半胱氨酸血症等试剂盒中,具有良好的实际应用之价值。
附图说明
图1为甲硫氨酸循环关键代谢物代谢体内转化示意图。
图2为甲硫氨酸循环关键代谢物MRM谱图。
图3为显示QCH浓度的标准曲线样品溶液的MRM谱图。
图4为显示QCM浓度的标准曲线样品溶液的MRM谱图。
图5为显示QCL浓度的标准曲线样品溶液的MRM谱图。
图6为甲硫氨酸(MET)的标准曲线图。
图7为同型半胱氨酸(HCY)的标准曲线图。
图8为半胱氨酸(CYS)的标准曲线图。
图9为胆碱(CHO)的标准曲线图。
图10为甜菜碱(BET)的标准曲线图。
图11为还原型谷胱甘肽(GSH)的标准曲线图。
图12为S-腺苷同型半胱氨酸(SAH)的标准曲线图。
图13为谷氨酸(GLU)的标准曲线图。
图14为S-腺苷甲硫氨酸(SAM)的标准曲线图。
图15为同型半胱氨酸、半胱氨酸、还原型谷胱甘肽在高效还原-巯基衍生化前后的灵敏度。
图16为同型半胱氨酸、半胱氨酸、还原型谷胱甘肽在高效还原-巯基衍生化前后的稳定性。
图17为急性心肌梗死患者和健康对照者的血清甲硫氨酸循环关键代谢物水平
图18为急性心肌梗死患者和健康对照者的血清甲硫氨酸循环关键代谢物得分图
(A)PCA-X评分图,R2X(CUM)=1,Q2(CUM)=0.977;OPLS-DA得分图(B),R2X(CUM)=1,R2Y(CUM)=0.824,Q2(CUM)=0.782。
图19为血清甲硫氨酸循环关键代谢物对急性心肌梗死的预测能力。
图20为NASH模型小鼠和正常对照小鼠的血清甲硫氨酸循环关键代谢物水平。
图21为NASH模型小鼠和正常对照小鼠的血清甲硫氨酸循环关键代谢物得分图,
(A)PCA-X评分图,R2X(CUM)=1,Q2(CUM)=0.996;OPLS-DA得分图(B),R2X(CUM)=797,R2Y(CUM)=0.967,Q2(CUM)=0.93。
图22为血清甲硫氨酸循环关键代谢物对非酒精性脂肪肝炎的预测能力。
具体实施方式
本发明下列实施例中未注明具体条件的实验方法,通常按照常规条件,或按照制造厂商所建议的条件。实施例中所用到的各种常用化学试剂,均为市售产品。
除非另有定义,本发明所使用的所有的技术和科学术语与属于本发明的技术领域的技术人员通常理解的含义相同。本发明的说明书中所使用的术语只是为了描述具体的实施例的目的,不用于限制本发明。
本发明的术语“包括”和“具有”以及它们任何变形,意图在于覆盖不排他的包含。例如包含了一系列步骤的过程、方法、装置、产品或设备没有限定于已列出的步骤或模块,而是可选地还包括没有列出的步骤,或可选地还包括对于这些过程、方法、产品或设备固有的其它步骤。
为使本发明的目的、技术方案和优点更加清楚明了,下面结合具体实施方式,对本发明进一步详细说明。应该理解,这些描述只是示例性的,而并非要限制本发明的范围。此外,在以下说明中,省略了对公知结构和技术的描述,以避免不必要地混淆本发明的概念。
以下实施例对本发明做进一步的描述,但该实施例并非用于限制本发明的保护范围。
实施例1HPLC-MS/MS方法学建立
第一部分、试剂和仪器
标本分析过程主要涉及标本还原、衍生化、去除蛋白预处理、色谱分离、质谱鉴定,所使用的试剂和仪器如下:
1、标本预处理所需试剂及仪器
试剂:甲醇(Merk公司生产,纯度为LC-MS级)、乙腈(Merk公司生产,纯度为LC-MS级)、甲酸(Merk公司生产,纯度为LC-MS级)。
仪器:Cleanert PPT 96孔蛋白沉淀板,货号96CD2025Q;Cleanert M96生物样品前处理仪;Cleanert V96样品氮吹浓缩仪和96孔收集板,以上仪器均来自天津博纳艾杰尔科技有限公司。
2、色谱分离所需试剂及仪器
试剂:0.1%甲酸(体积比)-水溶液和0.1%甲酸(体积比)-80%甲醇(体积比)-20%乙腈(体积比)溶液,甲酸、甲醇和乙腈均由Merk公司生产,纯度均是HPLC级,纯度为LC-MS级。
仪器:Waters
3、质谱鉴定所需仪器
仪器:AB 4000Q-Trap质谱仪(美国应用生物系统(Appliedbio systems)公司下属的AB/SCIEX生产部门制造),质谱仪中使用TurboV离子源,三重四级杆(Triple quadruple)作为串联质谱的质量分析装置。
4、其他试剂
甲硫氨酸(MET,>98%,S1230AS),半胱氨酸(CYS,>98%,S0118AS),S-腺苷甲硫氨酸(SAM,>96%,N0911A),甜菜碱(BET,>98%,J0310AS),谷氨酸(GLU,>99%,A0226A)购自大连美仑生物技术有限公司;S-腺苷同型半胱氨酸(SAH,97.2%,R089M0)购自USP(Twinbrook,Canada),胆碱(CHO,47-50%in Water,FFJVM-BC),DL-Homocysteine(HCY,>90%,PSGPG-HD)购自日本TCI(Tokyo,Japan),L-phenylalanine-d5(D5-Phe,SDHA-013)购自美国CIL(Andover,USA),N-乙基马来酰亚胺(NEM,≥99.0%,BCBZ7317),三(2-羰基乙基)磷盐酸盐(TECP,≥98.0%,SLBZ2552)购自默克西格玛(St.Louis,MO,USA)。
第二部分、方法
S1、标本预处理:将血清标本进行高效还原-巯基衍生化预处理并去除干扰蛋白质;
S2、色谱分离:将经过步骤S1处理过的标本注入到高效液相色谱柱中完成标本的初步分离;
S3、质谱鉴定:将步骤S2初步分离后的标本通过质谱仪完成定量分析离子碎片的强度分析和质谱图的采集;所述方法使用氘代苯丙氨酸作为蛋氨酸循环关键代谢物定量检测的内标物。
上述步骤S1~S3具体如下:
(1)标本预处理
血清标本中的同型半胱氨酸、半胱氨酸以及还原型谷胱甘肽极易被氧化,且检测灵敏度低,需要进行高效还原-巯基衍生化保护,提高其稳定性及检测灵敏度,此外血清中含有大量的蛋白质,影响对检测甲硫氨酸类物质的定量检测,需要对标本进行预处理除去干扰蛋白质,具体步骤如下:
1)配制含有D5-Phe(100ng/mL)的甲醇溶液:200mL甲醇溶液加入20μL浓度为1mg/mL的D5-Phe储备溶液,充分混匀备用;
2)配制含有N-乙基马来酰亚胺(NEM,69mM)的溶液:50mL超纯水中加431.66mg N-乙基马来酰亚胺,充分溶解;
3)配制含有三(2-羰基乙基)磷盐酸盐(TECP,51mM)的溶液:10mL超纯水中加146.19mg N-三(2-羰基乙基)磷盐酸盐,充分溶解;
4)预处理去除干扰蛋白前的前处理:
a)配制标准曲线样品溶液:标准曲线样品溶液共有A至J的10个浓度水平,具体如表1所示,称取甲硫氨酸(MET)、胆碱(CHO)、甜菜碱(BET)、S-腺苷同型半胱氨酸(SAH)、S-腺苷甲硫氨酸(SAM)、谷氨酸(GLU)的标准品,用10%甲醇溶液(MeOH)分别配置成浓度为5mg/mL、5mg/mL、20mg/mL、0.1mg/mL、2.5mg/mL、1mg/mL的储备溶液,称取同型半胱氨酸(HCY)、半胱氨酸(CYS)、还原型谷胱甘肽(GSH)的标准品,用50mM的N-乙基马来酰亚胺(NEM)溶液分别配置成浓度为5mg/mL的储备溶液,得到甲硫氨酸、胆碱、甜菜碱、S-腺苷同型半胱氨酸、S-腺苷甲硫氨酸、同型半胱氨酸、半胱氨酸、谷氨酸和还原型谷胱甘肽的系列标准品溶液。
表1甲硫氨酸循环关键代谢物定量分析的标准曲线浓度
b)配制标本:取100μL人血清至EP管内,充分涡旋均匀即得一份标本,进行如下步骤处理;
①高效还原-巯基衍生化:先向Cleanert PPT 96孔蛋白沉淀板中加入50μL血清,然后加入10μL浓度为69mM的TECP溶液,使用96孔板振荡器于600rpm涡旋1min混合均匀后静置13min,随后加入50μL浓度为51mM的NEM,再加入300μL含有D5-Phe(100ng/mL)的甲醇溶液,使用96孔板振荡器于600rpm涡旋5min混合均匀后室温静置21min。
②预处理去除干扰蛋白:使用Cleanert M 96生物样品前处理仪将经过步骤①后得到的溶液收集到洁净的收集板中备用,所得溶液即为去除干扰蛋白的待测物溶液;
③预处理样品干燥及复溶:将收集板里的溶液在Cleanert 96样品氮吹浓缩仪中用氮气吹干,温度设定为30℃,吹干后标本再置于0.1mL 10%甲醇-水溶液中复溶,涡旋器上混合均匀后即可进行后续测试。
(2)色谱分离
将经过预处理的标本注入到高效液相色谱柱中,HPLC流动相程序见表2,流速设定为300μL/min,柱温固定在30℃,进样量设定为10μL,。
表2HPLC分离的流动相程序
(3)质谱分析
经HPLC分离后的标本进入质谱仪进行鉴定和定量分析,质谱仪的参数设置见表3;
表3甲硫氨酸循环关键代谢物定量分析的质谱参数
表中“Q1 Mass”指母离子,“Q3 Mass”指子离子,单位均为质荷比m/z;DP”表示去簇电压,单位是伏特;“EP”表示入口电压,单位是伏特,CE””表示碰撞电压,单位是伏特;“CXP”表示碰撞室出口电压,单位是伏特。
实施例2HPLC-MS/MS方法学验证
由于难以获得完全不含甲硫氨酸(MET)、同型半胱氨酸(HCY)、半胱氨酸(CYS)、胆碱(CHO)、甜菜碱(BET)、还原型谷胱甘肽(GSH)、S-腺苷同型半胱氨酸(SAH)、S-腺苷甲硫氨酸(SAM)和谷氨酸(GLU)的基质,所以本发明首先采用活性炭吸附处理的血清进行方法学评估和性能验证。
1、验证方法
(1)线性关系和灵敏度的评估
称取甲硫氨酸(MET)、胆碱(CHO)、甜菜碱(BET)、S-腺苷同型半胱氨酸(SAH)、S-腺苷甲硫氨酸(SAM)、谷氨酸(GLU)的标准品,用10%甲醇溶液分别配置成浓度为5mg/mL、5mg/mL、20mg/mL、0.1mg/mL、2.5mg/mL、1mg/mL的储备溶液,称取同型半胱氨酸(HCY)、半胱氨酸(CYS)、还原型谷胱甘肽(GSH)的标准品,用50mM的N-乙基马来酰亚胺(NEM)溶液分别配置成浓度为5mg/mL的储备溶液,得到含甲硫氨酸、胆碱、甜菜碱、S-腺苷同型半胱氨酸、S-腺苷甲硫氨酸、同型半胱氨酸、半胱氨酸、还原型谷胱甘和谷氨酸的系列混合标准品溶液A-J,具体见表4。
将J浓度的标准曲线样品稀释至更低浓度梯度上机检测,测定信噪比(S/N),直至S/N为10:1,再平行处理五个样本,满足CV值小于20%,则此时的标准曲线样品浓度即为仪器的最低定量限(Limit of Quantitation,LOQ),用最低定量限(LOQ)值表示本发明HPLC-MS/MS技术平台的灵敏度。
表4甲硫氨酸循环关键代谢物定量分析的标准曲线浓度
此外,本研究重点考察、比较了在执行高效还原-巯基衍生化前后,同型半胱氨酸(HCY)、半胱氨酸(CYS)、还原型谷胱甘肽(GSH)三种物质得的检测灵敏度。分别配置10ng/mL的同型半胱氨酸(HCY)或同型半胱氨酸衍生化物(HCY-NEM)、100ng/mL的半胱氨酸(CYS)或半胱氨酸衍生化物(CYS-NEM)、100ng/mL的还原型谷胱甘肽(GSH)或还原型谷胱甘肽衍生化物(GSH-NEM)溶液。比较相同浓度下,执行高效还原-巯基衍生化前后,同型半胱氨酸(HCY)、半胱氨酸(CYS)、还原型谷胱甘肽(GSH)三种物质的峰面积情况,表明执行高效还原-巯基衍生化后,同型半胱氨酸(HCY)、半胱氨酸(CYS)、还原型谷胱甘肽(GSH)的峰面积相比执行高效还原-巯基衍生化前分别提高了14.44倍、5.08倍、3.41倍,表明检测灵敏度有了较显著的提高,具体见附图15。
(2)高效还原-巯基衍生化对3种关键代谢物稳定性的影响
为了考察、比较在执行高效还原-巯基衍生化前后,同型半胱氨酸(HCY)、半胱氨酸(CYS)、还原型谷胱甘肽(GSH)三种物质得的检测灵敏度。分别配置10ng/mL的同型半胱氨酸(HCY)或同型半胱氨酸衍生化物(HCY-NEM)、100ng/mL的半胱氨酸(CYS)半胱氨酸衍生化物(CYS-NEM)、100ng/mL的还原型谷胱甘肽(GSH)或还原型谷胱甘肽衍生化物(GSH-NEM)溶液。比较相同浓度下,执行高效还原-巯基衍生化前后,同型半胱氨酸(HCY)、半胱氨酸(CYS)、还原型谷胱甘肽(GSH)三种物质在4℃以及25℃条件下,分别放置12h、24h、48h、72h、96h、120h的峰面积变化情况。由附图16结果可见,在执行高效还原-巯基衍生化后,同型半胱氨酸(HCY)、半胱氨酸(CYS)、还原型谷胱甘肽(GSH)三种物质的稳定性明显提高。
(3)方法精密度和准确度确定
以QCH,QCM和QCL三个浓度水平的标准样品对本研究的分析方法进行准确度和精密度的评价,具体见表5。
表5甲硫氨酸循环关键代谢物的日内准确度、精密度和日间准确度、精密度
由表5结果表明,9种化合物在样品中的日内准确度、精密度和日间准确度、精密度良好,RSD小于15%,表明本方法适用于血清样本中甲硫氨酸循环关键代谢物的定量检测。
(4)方法稳定性考察
以QCH,QCM和QCL三个浓度水平的标准样品进行稳定性的评价,具体见表6。
表6甲硫氨酸循环关键代谢物的血浆稳定性
表6结果表明,9种化合物在样品中稳定性良好,准确度在85%~115%范围内,表明本方法适用于血清样本中甲硫氨酸循环关键代谢物的定量检测。
(5)血清为基质进行的加标回收与基质效应实验
以QCH,QCM和QCL三个浓度水平的标准样品进行加标回收与基质效应的评价,具体见表7。
表7甲硫氨酸循环关键代谢物的血浆回收率及基质效应
表7结果表明,本方法对血清中9种化合物的回收率良好,且无明显的基质效应,表明本方法适用于血清样本中甲硫氨酸循环关键代谢物的定量检测。
实施例3基于高效还原-巯基衍生化的HPLC-MS/MS检测用于甲硫氨酸循环关键代谢物的绝对定量分析方法用于临床样本检测
第一部分、试剂和仪器
标本分析过程主要涉及标本还原、衍生化、去除蛋白预处理、色谱分离、质谱鉴定,所使用的试剂和仪器同实施例1。
第二部分、方法
样本收集经广州医科大学附属第三医院医学伦理学委员会批准。急性心肌梗死人血清样本(n=40)和健康人血清样本(n=25)取自广州医科大学附属第三医院,均获得所有患者及健康志愿者知情同意(伦理批准批号:2021#026)
S1、标本预处理:将血清标本进行高效还原-巯基衍生化预处理并去除干扰蛋白质;
S2、色谱分离:将经过步骤S1处理过的标本注入到高效液相色谱柱中完成标本的初步分离;
S3、质谱鉴定:将步骤S2初步分离后的标本通过质谱仪完成定量分析离子碎片的强度分析和质谱图的采集;所述方法使用氘代苯丙氨酸作为蛋氨酸循环关键代谢物定量检测的内标物。
上述步骤S1~S3具体如下:
(1)标本预处理
对标本进行预处理除去干扰蛋白质,主要步骤如下:
1)配制含有D5-Phe(100ng/mL)的甲醇溶液:200mL甲醇溶液加入20μL浓度为1mg/mL的D5-Phe储备溶液,充分混匀备用;
2)配制含有N-乙基马来酰亚胺(NEM,69mM)的溶液:50mL超纯水中加431.66mg N-乙基马来酰亚胺,充分溶解;
3)配制含有三(2-羰基乙基)磷盐酸盐(TECP,51mM)的溶液:10mL超纯水中加146.19mg N-三(2-羰基乙基)磷盐酸盐,充分溶解;
4)预处理去除干扰蛋白前的前处理:
a)配制标准曲线样品溶液:标准曲线样品溶液共有A至J的10个浓度水平,具体如表8所示,称取甲硫氨酸(MET)、胆碱(CHO)、甜菜碱(BET)、S-腺苷同型半胱氨酸(SAH)、S-腺苷甲硫氨酸(SAM)、谷氨酸的标准品,用10%甲醇溶液分别配置成浓度为5mg/mL、5mg/mL、20mg/mL、0.1mg/mL、2.5mg/mL、1mg/mL的储备溶液,称取同型半胱氨酸(HCY)、半胱氨酸(CYS)、还原型谷胱甘肽(GSH)的标准品,用50mM的N-乙基马来酰亚胺(NEM)分别溶液配置成浓度为5mg/mL的储备溶液,得到甲硫氨酸、胆碱、甜菜碱、S-腺苷同型半胱氨酸、S-腺苷甲硫氨酸、同型半胱氨酸、半胱氨酸、谷氨酸和还原型谷胱甘肽的系列标准品溶液。
表8甲硫氨酸循环关键代谢物定量分析的标准曲线浓度
b)配制标本:取100μL人血清至EP管内,充分涡旋均匀即得一份标本,进行如下步骤处理;
①高效还原-巯基衍生化:先向Cleanert PPT 96孔蛋白沉淀板中加入50μL人血清,然后加入10μL浓度为69mM的TECP溶液,使用96孔板振荡器于600rpm涡旋1min混合均匀后静置13min,随后加入50μL浓度为51mM的NEM,再加入300μL含有D5-Phe(100ng/mL)的甲醇溶液,使用96孔板振荡器于600rpm涡旋5min混合均匀后室温静置21min。
②预处理去除干扰蛋白:使用Cleanert M96生物样品前处理仪将经过步骤①后得到的溶液收集到洁净的收集板中备用;所得溶液即为去除干扰蛋白的待测物溶液;
③预处理样品干燥及复溶:将收集板里的溶液在Cleanert 96样品氮吹浓缩仪中用氮气吹干,温度设定为30℃;吹干后标本再于0.1mL 10%甲醇-水溶液中复溶,涡旋器上混合均匀后即可进行后续测试。
(2)色谱分离
将经过预处理的标本注入到高效液相色谱柱中,HPLC流动相参数见表9,流速设定为300μL/min,柱温固定在30℃,进样量设定为10μL。
表9HPLC分离的流动相条件
(3)质谱分析
经HPLC分离后的标本进入质谱仪进行鉴定和定量分析,质谱仪的参数设置见表10。
表10甲硫氨酸循环关键代谢物定量分析的质谱参数
表中“Q1 Mass”指母离子,“Q3 Mass”指子离子,单位均为质荷比m/z;DP”表示去簇电压,单位是伏特;“EP”表示入口电压,单位是伏特,CE””表示碰撞电压,单位是伏特;“CXP”表示碰撞室出口电压,单位是伏特。
第三部分、结果分析
(1)不同人群血清中甲硫氨酸循环关键代谢物的含量
比较了健康志愿者(Normal)和急性心肌梗死(AMI)患者的血清甲硫氨酸循环关键代谢物水平。由附图17结果显示,AMI患者的血清甲硫氨酸循环关键代谢物水平与健康志愿者相比有显著差异。其中,甜菜碱,胆碱,S-腺苷同型半胱氨酸,同型半胱氨酸,谷氨酸的水平在AMI患者中显著升高。S-腺苷甲硫氨酸,谷胱甘肽水平在AMI患者中明显降低;两组之间的半胱氨酸水平无显著差异。基于血清甲硫氨酸循环关键代谢物构建的PCA-X和OPLS-DA模型结果显示,甲硫氨酸循环关键代谢物可以明显区分健康志愿者和AMI患者(见图18)。
(2)甲硫氨酸循环关键代谢物对急性心肌梗死的诊断能力
ROC曲线分析用于研究甲硫氨酸循环关键代谢物,并采用曲线下面积(AUC)进行定量分析。AUCs>0.5表明该方法具有诊断价值,AUCs在0.7~0.9表示有一定的准确性,AUCs>0.9表示准确性高。由附图19结果发现了可以区分健康志愿者、AMI患者的甲硫氨酸循环关键代谢物,包括同型半胱氨酸(AUC=0.994),S-腺苷甲硫氨酸(AUC=0.962),甲硫氨酸(AUC=0.928),谷胱甘肽(AUC=0.894),谷氨酸(AUC=0.798),胆碱(AUC=0.758),S-腺苷同型半胱氨酸(AUC=0.754),甜菜碱(AUC=0.746),半胱氨酸(AUC=0.574)。其中,同型半胱氨酸(HCY),S-腺苷甲硫氨酸(SAM),甲硫氨酸(MET),谷胱甘肽(GSH),谷氨酸(GLU),胆碱(CHO),S-腺苷同型半胱氨酸(SAH),甜菜碱(BET)指标的综合预测能力超过0.7。其中,同型半胱氨酸(HCY),S-腺苷甲硫氨酸(SAM),甲硫氨酸(MET)的AUC值大于0.9,表明这些代谢物对心肌梗死的预测能力最佳,适用于心肌梗死患者的诊断。
实施例4基于高效还原-巯基衍生化的HPLC-MS/MS检测用于甲硫氨酸循环关键代谢物的绝对定量分析方法用于代谢性疾病基础实验研究
第一部分、试剂和仪器
标本分析过程主要涉及标本还原、衍生化、去除蛋白预处理、色谱分离、质谱鉴定,所使用的试剂和仪器同实施例1。
第二部分、方法
(1)样本
C57 BL/6J(18–20g)小鼠购自南方医科大学医学实验动物中心(实验动物生产许可证号:SCXK(粤)2016-0041;实验动物许可证号:NO.44002100016098),本研究经广州医科大学实验动物伦理委员会批准(伦理编号:2018-051)。正常对照组实验动物给予正常饲料,模型组动物给予高脂高胆固醇饲料(20180117,广东省医学实验动物中心),造模24周后,所有实验动物禁食不禁水12h,麻醉动物后,经腹主动脉取血,3000rpm离心10min,分离血清,保存于-80℃冰箱待测。
(2)标本预处理
血清标本中的同型半胱氨酸、半胱氨酸以及还原型谷胱甘肽极易被氧化,且检测灵敏度低,需要进行高效还原-巯基衍生化保护,提高其稳定性及检测灵敏度,此外血清中含有大量的蛋白质,影响对检测甲硫氨酸类物质的定量检测,需要对标本进行预处理除去干扰蛋白质。主要步骤如下:
1)配制含有D5-Phe(100ng/mL)的甲醇溶液:200mL甲醇溶液加入20μL浓度为1mg/mL的D5-Phe储备溶液,充分混匀备用;
2)配制含有N-乙基马来酰亚胺(NEM,69mM)的溶液:50mL超纯水中加431.66mg N-乙基马来酰亚胺,充分溶解;
3)配制含有三(2-羰基乙基)磷盐酸盐(TECP,51mM)的溶液:10mL超纯水中加146.19mg N-三(2-羰基乙基)磷盐酸盐,充分溶解;
4)预处理去除干扰蛋白前的前处理:
a)配制标准曲线样品溶液:标准曲线样品溶液共有A至J的10个浓度水平,具体如表11所示,称取甲硫氨酸(MET)、胆碱(CHO)、甜菜碱(BET)、S-腺苷同型半胱氨酸(SAH)、S-腺苷甲硫氨酸(SAM)、谷氨酸的标准品,用10%甲醇溶液分别配置成浓度为5mg/mL、5mg/mL、20mg/mL、0.1mg/mL、2.5mg/mL、1mg/mL的储备溶液,称取同型半胱氨酸(HCY)、半胱氨酸(CYS)、还原型谷胱甘肽(GSH)的标准品,用50mM的N-乙基马来酰亚胺(NEM)分别溶液配置成浓度为5mg/mL的储备溶液,得到甲硫氨酸、胆碱、甜菜碱、S-腺苷同型半胱氨酸、S-腺苷甲硫氨酸、同型半胱氨酸、半胱氨酸、谷氨酸和还原型谷胱甘肽的系列标准品溶液。
表11甲硫氨酸循环关键代谢物定量分析的标准曲线浓度
b)配制标本:取100μL空白小鼠血清至EP管内,充分涡旋均匀即得一份标本,进行如下步骤处理;
①高效还原-巯基衍生化:先向Cleanert PPT 96孔蛋白沉淀板中加入50μL空白小鼠血清,然后加入10μL浓度为69mM的TECP溶液,使用96孔板振荡器于600rpm涡旋1min混合均匀后静置13min,随后加入50μL浓度为51mM的NEM,再加入300μL含有D5-Phe(100ng/mL)的甲醇溶液,使用96孔板振荡器于600rpm涡旋5min混合均匀后室温静置21min。
②预处理去除干扰蛋白:使用Cleanert M96生物样品前处理仪将经过步骤①后得到的溶液收集到洁净的收集板中备用;所得溶液即为去除干扰蛋白的待测物溶液;
③预处理样品干燥及复溶:将收集板里的溶液在Cleanert 96样品氮吹浓缩仪中用氮气吹干,温度设定为30℃;吹干后标本再于0.1mL 10%甲醇-水溶液中复溶,涡旋器上混合均匀后即可进行后续测试。
(3)色谱分离
将经过预处理的标本注入到高效液相色谱柱中,HPLC流动相参数见表12,流速设定为300μL/min,柱温固定在30℃,进样量设定为10μL。
表12HPLC分离的流动相条件
(4)质谱分析
经HPLC分离后的标本进入质谱仪进行鉴定和定量分析,质谱仪的参数设置见表2。
表16.甲硫氨酸循环关键代谢物定量分析的质谱参数
表中“Q1 Mass”指母离子,“Q3 Mass”指子离子,单位均为质荷比m/z;DP”表示去簇电压,单位是伏特;“EP”表示入口电压,单位是伏特,CE””表示碰撞电压,单位是伏特;“CXP”表示碰撞室出口电压,单位是伏特。
第三部分、结果分析
(1)实验小鼠血清中甲硫氨酸循环关键代谢物的含量
比较了正常对照组小鼠(Normal)和非酒精性脂肪肝炎模型小鼠(NASH)的血清甲硫氨酸循环关键代谢物水平。由附图20结果显示,NASH模型小鼠的血清甲硫氨酸循环关键代谢物水平与正常组相比有显著差异。其中,甜菜碱,胆碱,S-腺苷同型半胱氨酸,同型半胱氨酸,谷氨酸,半胱氨酸,甲硫氨酸的水平在NASH模型小鼠中显著升高。S-腺苷甲硫氨酸,谷胱甘肽水平在NASH模型小鼠中明显降低;基于血清甲硫氨酸循环关键代谢物构建的PCA-X和OPLS-DA模型结果显示,使用检测到的甲硫氨酸循环关键代谢物可以明显区分正常对照组小鼠和NASH模型小鼠(见附图21)。
(2)甲硫氨酸循环关键代谢物对非酒精性脂肪肝炎的诊断和预测能力
ROC曲线分析用于研究甲硫氨酸循环关键代谢物,并采用曲线下面积(AUC)进行定量分析。AUCs>0.5表明该方法具有诊断价值,AUCs在0.7~0.9表示有一定的准确性,AUCs>0.9表示准确性高。由附图22结果发现了可以区分正常对照组小鼠(Normal)和非酒精性脂肪肝炎模型小鼠(NASH)的甲硫氨酸循环关键代谢物,包括同型半胱氨酸(AUC=1),S-腺苷甲硫氨酸(AUC=1),谷胱甘肽(AUC=1),谷氨酸(AUC=0.99),S-腺苷同型半胱氨酸(AUC=0.99),甲硫氨酸(AUC=0.97),胆碱(AUC=0.9),半胱氨酸(AUC=0.87),甜菜碱(AUC=0.83)。其中,同型半胱氨酸(HCY),S-腺苷甲硫氨酸(SAM),甲硫氨酸(MET),谷胱甘肽(GSH),谷氨酸(GLU),胆碱(CHO),S-腺苷同型半胱氨酸(SAH),甜菜碱(BET)和半胱氨酸(CYS)指标的综合预测能力均超过0.7。其中,同型半胱氨酸(HCY),S-腺苷甲硫氨酸(SAM),甲硫氨酸(MET),谷胱甘肽(GSH),谷氨酸(GLU),S-腺苷同型半胱氨酸(SAH),胆碱(CHO)的AUC值大于0.9,表明这些代谢物对NASH的预测能力最佳,适用于NASH患者及动物模型的诊断和预测。
需要说明的是,本说明书中描述的具体特征、结构、材料或者特点可以进行任意的组合,为使描述简洁,未对上述实施例中的各个技术特征所有可能的组合都进行描述,在不相互矛盾的情况下,本领域的技术人员可以将本说明书中描述的不同实施例以及不同实施例的特征进行结合和组合。
以上所述实施例仅表达了本发明的几种实施方式,其描述较为具体和详细,但并不能因此而理解为对发明专利范围的限制。应当指出的是,对于本领域的普通技术人员来说,在不脱离本发明构思的前提下,还可以做出若干变形和改进,这些都属于本发明的保护范围。因此,本发明专利的保护范围应以所附权利要求为准。
