胶质瘤免疫逃逸分子标志物在胶质瘤辅助诊断和治疗中的应用
文献发布时间:2024-04-18 19:52:40
技术领域
本发明涉及一种胶质瘤免疫逃逸标志物及其应用,特别涉及一种长链非编码RNA作为胶质瘤免疫逃逸标志物及其在胶质瘤辅助诊断和治疗中的应用。本发明属于医药技术领域。
背景技术
胶质瘤是最常见的侵袭性原发性脑肿瘤,也是最致命的中枢神经系统肿瘤,具有高增殖率、高侵袭性、高度异质性的免疫抑制微环境以及对化疗和靶向治疗的耐药等特点。免疫检查点封锁(ICB)疗法在改善某些类型肿瘤的治疗方面取得了显著的成就。然而,大脑独特的免疫微环境使免疫治疗在胶质瘤的应用中极具挑战性。在肿瘤发生发展过程中,免疫细胞浸润肿瘤组织形成肿瘤免疫微环境,帮助肿瘤细胞实现免疫逃逸,促进肿瘤恶性发展,并与免疫治疗的应答密切相关。
长链非编码RNA(lncRNA)是一种转录本长度大于200bp的非编码RNA分子,在肿瘤免疫调控中发挥着重要功能。此外,DNA甲基化是影响lncRNA表达的表观遗传调控因子,它们之间存在着复杂的调控关系。然而目前关于胶质瘤中DNA甲基化,lncRNA以及免疫逃逸之间的调控机制尚不明确,本发明发明人基于lncRNA的DNA甲基化识别胶质瘤免疫亚型,进而识别免疫逃逸相关lncRNA标志物,为胶质瘤免疫疗法的应用提供潜在的治疗靶点。
发明内容
本发明的目的在于提供一种能够识别胶质瘤免疫亚型,进而能够辅助诊断和治疗胶质瘤免疫亚型的分子标志物。
为了达到上述目的,本发明采用了以下技术手段:
本发明技术方案中,基于lncRNA的DNA甲基化数据对胶质瘤患者进行一致性聚类,确定胶质瘤免疫逃逸亚型,并识别免疫逃逸亚型中关键的lncRNA。经研究发现,胶质瘤免疫逃逸亚型中免疫细胞浸润及免疫逃逸指标升高,并且患者预后较差。LINC02447以及AL590428.1(又名CD109-AS1)在胶质瘤免疫逃逸亚型中甲基化水平降低,表达升高,并且LINC02447以及AL590428.1的表达和甲基化水平皆与胶质瘤预后相关。在抗PD1免疫治疗中,LINC02447以及AL590428.1在对药物治疗有反应的患者中低表达,而无反应的患者中高表达,并且LINC02447以及AL590428.1的高表达是胶质瘤患者预后的风险因素。
因此,在上述的研究基础上,本发明提出了胶质瘤免疫逃逸分子标志物在制备胶质瘤辅助诊断和治疗试剂中的应用,所述的胶质瘤免疫逃逸分子标志物选自长链非编码RNALINC02447以及AL590428.1中的至少一种。
其中,优选的,长链非编码RNALINC02447转录本的核酸序列如SEQ IDNO:1-4任一所示,所述的该长链非编码RNAAL590428.1转录本的核酸序列如SEQ ID NO:5所示。
其中,根据LINC02447以及AL590428.1中的至少一种的检测结果,若LINC02447以及AL590428.1中的至少一种发生低甲基化或者表达较高时,认为该胶质瘤患者具有免疫逃逸特征并且预后较差,若LINC02447以及AL590428.1中的至少一种发生高甲基化或者表达较低时,认为该胶质瘤患者预后较好。
其中,根据LINC02447以及AL590428.1中的至少一种的检测结果,若LINC02447以及AL590428.1中的至少一种发生低甲基化或者表达较高时,认为该患者不适合接受免疫治疗,需对LINC02447以及AL590428.1中的至少一种进行抑制之后,再进行免疫治疗;若LINC02447以及AL590428.1中的至少一种发生高甲基化或者表达较低时,认为该胶质瘤患者能够从免疫治疗中受益。
进一步的,本发明还提出了用于检测胶质瘤免疫逃逸分子标志物甲基化水平以及表达水平的试剂在制备胶质瘤辅助诊断和治疗试剂中的应用,所述的胶质瘤免疫逃逸分子标志物选自长链非编码RNALINC02447以及AL590428.1中的至少一种。
其中,优选的,用于检测胶质瘤免疫逃逸分子标志物甲基化水平的试剂为针对LINC02447以及AL590428.1中的至少一种设计的甲基化特异性的PCR引物,用于检测胶质瘤免疫逃逸分子标志物表达水平的试剂为针对LINC02447以及AL590428.1中的至少一种设计的qRT-PCR引物。
用于检测胶质瘤免疫逃逸分子标志物甲基化水平以及表达水平的试剂为本领域已知的检测试剂,例如用于检测胶质瘤免疫逃逸分子标志物甲基化水平的试剂可以是甲基化特异性的PCR(Methylation-specific PCR,MSP)引物,用亚硫酸氢盐处理基因组DNA,所有未发生甲基化的胞嘧啶被转化为尿嘧啶,而甲基化的胞嘧啶不变;随后设计针对甲基化和非甲基化序列的引物进行PCR。通过电泳检测MSP扩增产物,如果用针对处理后甲基化DNA链的引物能得到扩增片段,则说明该位点存在甲基化;反之,说明被检测的位点不存在甲基化。或是亚硫酸氢盐测序(Bisulfite sequencing PCR,BSP)引物,通过BSP引物,用亚硫酸氢盐处理基因组DNA,则未发生甲基化的胞嘧啶被转化为尿嘧啶,而甲基化的胞嘧啶不变。随后设计BSP引物进行PCR,在扩增过程中尿嘧啶全部转化为胸腺嘧啶,最后对PCR产物进行测序就可以判断CpG位点是否发生甲基化称为BSP-直接测序方法。亦或是一对针对亚硫酸氢盐修饰后的DNA双链的引物,采用高分辨率熔解曲线法(High Resolution Melting,HRM),在非CpG岛位置设计一对针对亚硫酸氢盐修饰后的DNA双链的引物,这对引物中间的片段包含感兴趣的CpG岛。若这些CpG岛发生了甲基化,用亚硫酸氢盐处理后,未甲基化的胞嘧啶经PCR扩增后转变成胸腺嘧啶,而甲基化的胞嘧啶不变,样品中的GC含量发生改变,从而导致熔解温度的变化。
用于检测上述胶质瘤免疫逃逸分子标志物表达水平的试剂包括实时荧光定量PCR引物等。
其他本领域已知的可用于检测上述胶质瘤免疫逃逸分子标志物甲基化水平以及表达水平的试剂也在本发明的保护范围之内,在此不再赘述。
其中,优选的,用于检测LINC02447甲基化水平的试剂为针对LINC02447设计的甲基化特异性的PCR引物,序列如下所示:
Forward:AGCGAATATTAGGAGAGGGTC
Reverse:ACGCTACCTCTAATTCCCG
用于检测AL590428.1甲基化水平的试剂为针对AL590428.1设计的甲基化特异性的PCR引物,序列如下所示:
Forward:GGTGGGTTTTGTATTTCGAC
Reverse:TACTATTAAACGCGCCCATT。
其中,优选的,用于检测LINC02447表达水平的试剂为针对LINC02447设计的qRT-PCR引物,序列如下所示:Forward:CTGGTTGCTCCCCAGAAACA
Reverse:TCTCTCCAGACGCCTAGTCC
用于检测AL590428.1表达水平的试剂为针对AL590428.1设计的qRT-PCR引物,序列如下所示:
Forward:TAGCGCTCTACCAACGATGC
Reverse:AGAGCCAACCCAACCCTAAC。
其中,优选的,根据LINC02447以及AL590428.1中的至少一种的检测结果,若LINC02447以及AL590428.1中的至少一种发生低甲基化或者表达较高时,认为该胶质瘤患者具有免疫逃逸特征并且预后较差,若LINC02447以及AL590428.1中的至少一种发生高甲基化或者表达较低时,认为该胶质瘤患者预后较好。
其中,优选的,根据LINC02447以及AL590428.1中的至少一种的检测结果,若LINC02447以及AL590428.1中的至少一种发生低甲基化或者表达较高时,认为该患者不适合接受免疫治疗,需对LINC02447以及AL590428.1中的至少一种进行抑制之后,再进行免疫治疗;若LINC02447以及AL590428.1中的至少一种发生高甲基化或者表达较低时,认为该胶质瘤患者能够从免疫治疗中受益。
相较于现有技术,本发明的有益效果是:
本发明提出了一种胶质瘤的新型免疫逃逸标志物,研究结果表明LINC02447以及AL590428.1是胶质瘤的新型免疫逃逸标志物,LINC02447以及AL590428.1的甲基化水平以及表达水平与胶质瘤的免疫逃逸以及预后相关。当LINC02447、以及AL590428.1的至少一种发生低甲基化或者表达较高时,认为该胶质瘤患者具有免疫逃逸特征并且预后较差,当LINC02447以及AL590428.1的至少一种发生高甲基化或者表达较低时,认为该胶质瘤患者预后较好。此外,本发明的提出还为胶质瘤患者是否适宜接受免疫治疗提供了指导,根据LINC02447以及AL590428.1的检测结果,当LINC02447以及AL590428.1的至少一种发生低甲基化或者表达较高时,认为该患者不适合接受免疫治疗,需对相应lncRNA进行抑制之后,再进行免疫治疗;当LINC02447以及AL590428.1的至少一种发生高甲基化或者表达较低时,认为该胶质瘤患者能够从免疫治疗中受益。本发明的提出为胶质瘤的免疫治疗提供了一种辅助诊断的方法,并且为胶质瘤的免疫治疗提供了新的治疗靶点。
附图说明
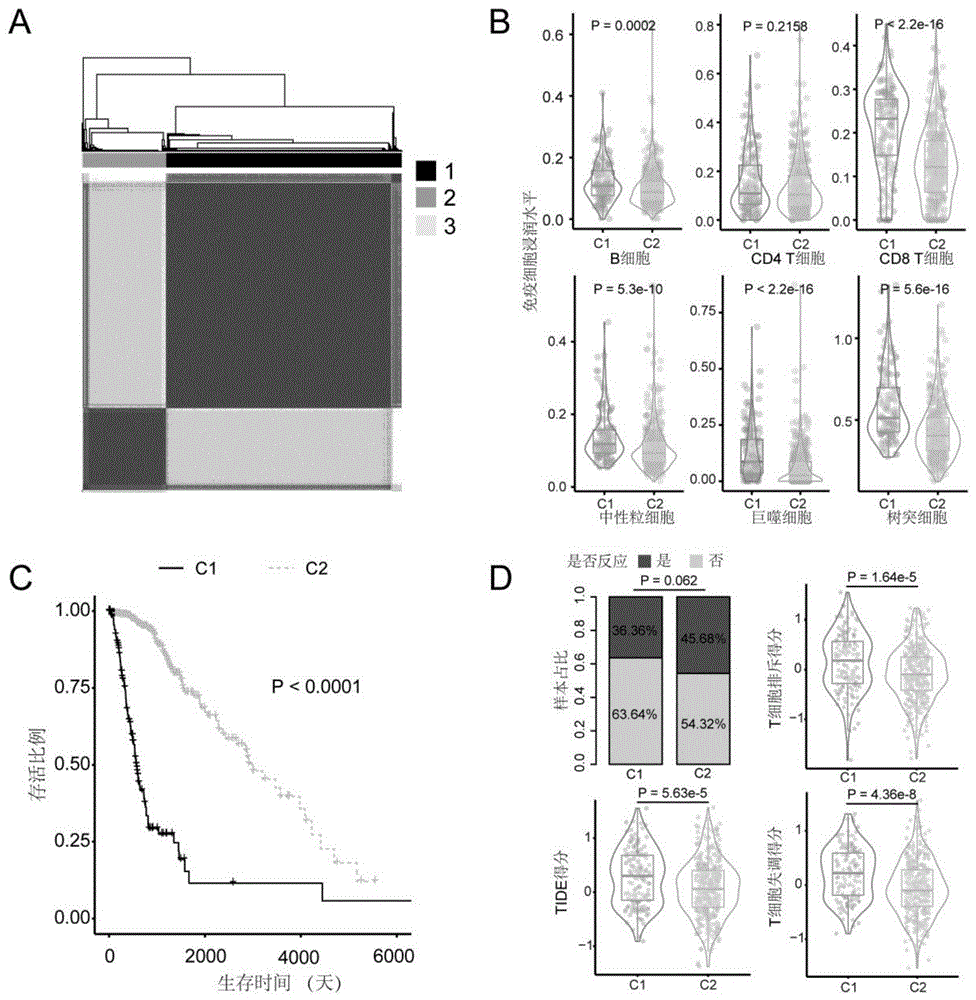
图1为胶质瘤免疫逃逸亚型识别;
其中,A.胶质瘤一致性聚类分析。B.胶质瘤亚型中免疫浸润水平分布。C.胶质瘤亚型预后分析。D.胶质瘤亚型免疫逃逸指标比较。
图2为LINC02447对于胶质瘤免疫逃逸的影响;
其中,A.LINC02447在胶质瘤亚型中的甲基化和表达水平分布。B.LINC02447在胶质瘤免疫治疗患者中的表达水平。C.LINC02447的表达水平对于胶质瘤预后的影响。D.LINC02447的甲基化水平对于胶质瘤预后的影响。
图3为AL590428.1对于胶质瘤免疫逃逸的影响。
其中,A.AL590428.1在胶质瘤亚型中的甲基化和表达水平分布。B.AL590428.1在胶质瘤免疫治疗患者中的表达水平。C.AL590428.1的表达水平对于胶质瘤预后的影响。D.AL590428.1的甲基化水平对于胶质瘤预后的影响。
图4为分子生物学实验证明LINC02447为胶质瘤新型免疫逃逸标记;
其中,A.qRT-PCR检测siRNA转染后LINC02447在U251细胞系中的表达。B.CCK-8实验检测LINC02447干扰后U251细胞系增殖能力下降。C.Westernblot检测LINC02447干扰后FOXP3、PD-L1以及CTLA4在U251细胞系中的蛋白含量,使用GAPDH作为内参。D.细胞划痕实验表明LINC02447干扰后U251细胞迁移能力减弱。E.小室实验表明LINC02447干扰后U251细胞侵袭能力减弱。*代表P小于0.05,**代表P小于0.01,***代表P小于0.001。
图5为分子生物学实验证明AL590428.1为胶质瘤新型免疫逃逸标记;
其中,A.qRT-PCR检测siRNA转染后AL590428.1在U251细胞系中的表达。B.CCK-8实验检测AL590428.1干扰后U251细胞系增殖能力下降。C.Westernblot检测AL590428.1干扰后FOXP3、PD-L1以及CTLA4在U251细胞系中的蛋白含量,使用GAPDH作为内参。D.细胞划痕实验表明AL590428.1干扰后U251细胞迁移能力减弱。E.小室实验表明AL590428.1干扰后U251细胞侵袭能力减弱。*代表P小于0.05,**代表P小于0.01,***代表P小于0.001。
具体实施方式
下面结合具体实施例来进一步描述本发明,本发明的优点和特点将会随具体实施例的描述而更为清楚。但实施例仅是范例性的,并不对本发明的范围构成任何限制。本领域技术人员应该理解的是,在不偏离本发明的精神和范围下可以对本发明技术方案的细节和形式进行修改或替换,但这些修改和替换均落入本发明的保护范围内。
实施例1胶质瘤新型免疫逃逸标志物的确定
1.基于DNA甲基化识别胶质瘤免疫亚型
实验所用的胶质瘤高通量DNA甲基化组及转录组数据均收集于癌症基因组图谱(TCGA,https://portal.gdc.cancer.gov/)数据库。基于人类基因组位置信息及甲基化芯片探针信息,首先将甲基化450K芯片探针映射至lncRNA启动子区域(转录起始位点上下游2kb),基于探针的平均甲基化水平对lncRNA甲基化水平进行定量。以标准差前5%的lncRNA甲基化作为特征运用ConsensusClusterPlus R包进行一致性聚类,选择样本数目大于5的C1和C2亚型进行后续分析(图1A)。并通过肿瘤免疫评估平台(Timer)算法评估胶质瘤亚型中的免疫细胞浸润水平(图1B),发现C1亚型中B细胞、CD8T细胞、中性粒细胞、巨噬细胞以及树突细胞浸软水平显著高于C2亚型,说明C1亚型是个免疫热亚型。
2.胶质瘤免疫逃逸亚型的确认
虽然C1是个免疫热亚型,但是通过生存分析发现C1亚型预后较差(Log-rank P值小于0.05,图1C),因此推断C1亚型中的胶质瘤患者可能发生了免疫逃逸现象。因此进一步利用肿瘤免疫功能障碍与排斥(TIDE,http://tide.dfci.harvard.edu/)算法评估免疫亚型中对于免疫治疗反应患者的占比,利用Wilcox秩和检验比较不同亚型患者对于免疫治疗受益、T细胞排斥以及T细胞失调得分的差异。发现C1亚型中对于免疫治疗受益的患者数目较少,并且TIDE得分以及T细胞排斥和T细胞失调得分显著高于C2亚型(图1D),表明C1亚型患者发生了免疫逃逸现象。因此定义C1为免疫逃逸亚型,C2为其他亚型。
3.确认lncRNA对于肿瘤免疫逃逸的影响
通过Wilcox秩和检验比较免疫逃逸亚型和其他亚型中lncRNA的表达和甲基化水平的差异。发现LINC02447以及AL590428.1在免疫逃逸亚型中甲基化水平降低(变化的甲基化水平大于-0.2,P值小于0.05),表达升高(变化倍数大于2,P值小于0.05)(图2A、图3A)。使用Tophat以及Cufflinks流程对胶质瘤抗PD1免疫治疗数据进行转录组lncRNA表达定量(PRJNA482620)。Wilcox秩和检验发现LINC02447以及AL590428.1在对于免疫治疗有反应的患者中表达显著下调(P值小于0.05,图2B、图3B)。通过Kaplan-Meier检验进行生存分析发现LINC02447和AL590428.1的高表达及低甲基化水平是胶质瘤的预后风险因素(图2C和D、图3C和D,Log-rank P值小于0.05)。因此,LINC02447以及AL590428.1在免疫逃逸亚型中发生低甲基化,导致表达升高,lncRNA的高表达和低甲基化是胶质瘤患者预后的风险因素,并且LINC02447以及AL590428.1在胶质瘤免疫治疗应答患者中低表达。综上所述表明LINC02447以及AL590428.1是新型的胶质瘤免疫逃逸标志物。
4.分子生物学实验证明lncRNA为新型胶质瘤免疫逃逸标志物
对于LINC02447和AL590428.1,首先使用siRNA干扰技术在U251细胞系中敲低其表达,与对照组相比LINC02447和AL590428.1的表达显著降低,揭示慢病毒转染siRNA序列的有效性(图4A、图5A)。通过CCK8实验探究LINC02447和AL590428.1对于胶质瘤细胞增殖的影响,发现lncRNA敲低后,U251增殖能力显著降低(图4B、图5B)。WB和qRT-PCR结果表明LINC02447和AL590428.1敲低后经典的免疫逃逸标记FOXP3、PD-L1和CTLA4在胶质瘤细胞系中蛋白水平皆显著下调,表明lncRNA与免疫逃逸存在关联(图4C、图5C)。此外,细胞划痕和小室实验结果同样发现了lncRNA敲低后胶质瘤细胞迁移和侵袭能力显著减弱(图4D和E、图5D和E)。以上结果表明,LINC02447和AL590428.1在胶质瘤中发挥促癌作用,并且能够作为一种新型的胶质瘤免疫逃逸标志物。
实施例2胶质瘤临床辅助诊断及预后判断
在临床上通过检测LINC02447以及AL590428.1至少一种的甲基化或者表达水平,可以对胶质瘤患者免疫特征及预后情况进行判断。
检测LINC02447以及AL590428.1表达水平的方法如下:
1、RNA提取
细胞样品:胶质瘤细胞。缓慢将培养瓶中的培养液弃去,用2mL PBS轻轻清洗细胞表面,注意清洗力度不要将细胞洗掉,PBS被吸净后,每瓶细胞加1mL Trizol,室温放置5min,使其充分裂解,将Trizol吸至1.5mL离心管中,加入200μL氯仿,剧烈震动30s,冰上放置5min,4℃,13500转/秒,离心15min,轻轻取出1.5mL的离心管,此时RNA存在于上层水相中,吸取上层水相,至另一离心管中,按0.5mL异丙醇/mL Trizol加入异丙醇混匀,冰浴放置10min,4℃,13500转/秒,离心10min,弃上清,RNA沉于管底,按1mL 75%乙醇/mL Trizol加入75%乙醇,温和振荡离心管,悬浮沉淀,4℃,10600转/秒,离心5min,尽量弃上清,室温晾干或真空干燥5-10min(RNA样品不要过于干燥,否则很难溶解),可用20μLDEPC水溶解RNA沉淀,最后采用紫外分光光度计检测RNA浓度,RNA样品于-80℃保存。
2、RNA浓度测定
取1μLRNA溶液滴加于紫外分光光度计的点样孔中,测定RNA浓度和纯度,RNA的OD260/OD280在1.80-2.20之间为纯度较高。
3、逆转录及qRT-PCR
采用TOYOBO的逆转录试剂盒进行逆转录,10μL的体系包括5×RT-buffer 2μL,RTenzyme mix 0.5μL,primer mix 0.5μL,RNA 500ng,用去RNA酶水补齐至10μL。逆转录的反应程序为37℃,15min(逆转录反应);98℃,5min(酶失活反应);4℃保持。将逆转录好的cDNA放于-20℃冰箱保存。qRT-PCR采用SYBR染料法进行,反应体系20μL:SYBR 10μL,上游引物1μL,下游引物1μL,去离子水7μL,cDNA样本1μL。根据扩增基因的不同配置好不同的共有反应体系,先将共有反应体系加入到PCR 96孔板中,再将cDNA加入,最后用封口膜封好后离心,1000r/min,1min。将96孔板放置到PCR仪上进行扩增反应,反应步骤为:95℃10min,(95℃15s,60℃30s,72℃30s)×40。qRT-PCR所用引物如下表,使用该引物可实现对LINC02447四个转录本(SEQ ID NO.1-4所示)、LINC01765转录本(SEQ ID NO.5所示)、AC131097.3转录本(SEQ ID NO.6所示)以及AL590428.1转录本(SEQ ID NO.7所示)的检测:
表1.引物序列
检测LINC02447以及AL590428.1甲基化水平的方法如下:
1、DNA抽提
1)样品加氯仿分层后,移去上层水相,用乙醇沉淀中间层和有机相中的DNA。每使用1mlTRIzol加0.3ml无水乙醇混匀。室温放置3分钟
2)4℃不超过2000×g离心5分钟。
3)移去上清,(如需分离蛋白质,可保留,进一步操作见后)用含10%乙醇的0.1M柠檬酸钠洗涤DNA沉淀。每用1mlTRIzol加入1ml柠檬酸钠,室温放置30分钟,4℃2000×g离心5分钟,弃上清,重复一次。
4)用75%乙醇再洗一遍DNA沉淀,每用1ml TRIzol加入1.5~2ml75%乙醇,室温放置10~20分钟(不时颠倒混合)4℃2000×g离心5分钟,弃上清。
5)室温放置晾干DNA5~15分钟,用8mM NaOH溶解DNA。从50~70mg组织或107细胞中分离的DNA溶于500μl 8mM NaOH,DNA的浓度通常为0.2-0.3μg/μl。
提取的DNA沉淀不易溶于水和Tris缓冲液中,建议用弱碱溶解,8mMNaOH的pH值为9,溶解DNA后可用TE,HEPES调节pH。从某些样品(尤其是组织)中提取的DNA中可能包含一些胶状不溶物可>12000×g离心10分钟除去。
6)上清可以在4℃存放过夜。长时间保存需要用HEPES加1Mm EDTA调整pH至7-8
2、使用基因甲基化特异性PCR扩增(MSP)试剂盒进行甲基化监测
1)实验开始前,从-20℃冰箱中取出试剂,放进冰槽里融化。然后进行下列操作:
针对一个样本,每次移出15微升扩增液(ReagentA)到PCR管加入1微升DNA样品(总量100纳克),分别加入1微升甲基化特异性的引物F和引物R(各350纳克或25微摩尔),再加入7微升补充液(ReagentB)(反应总量为25微升),即刻放进微型台式离心机瞬时离心5秒,速度为500g(或2000RPM;例如eppendorf5415),加入50微升PCR级矿物油,即刻进行热启动PCR反应。
2)反应完毕后,移取5微升进行1.8%琼脂糖凝胶电泳或15%聚丙烯酰胺凝胶,如果进行测序鉴定,胶回收PCR产物(建议使用高质纯化一步法胶回收试剂盒;20051.1),分别移出2微升反应液到2个不同的新的1.5毫升离心管(每微升100纳克),加入1微升甲基化特异性的巢式引物F(每微升350纳克)到其中一个1.5毫升离心管,作好标记,加入1微升甲基化特异性的巢式引物R(每微升350纳克)到另一个1.5毫升离心管,作好标记,进行后续的直接测序反应。
MSP所用甲基化特异性引物如下表2,使用该引物可实现对LINC02447四个转录本(SEQ ID NO.1-4所示)、LINC01765转录本(SEQ ID NO.5所示)、AC131097.3转录本(SEQ IDNO.6所示)以及AL590428.1转录本(SEQ ID NO.7所示)的甲基化检测:
表2.甲基化特异性引物序列
当LINC02447以及AL590428.1至少其中之一发生低甲基化或者表达较高时,认为该胶质瘤患者具有免疫逃逸特征并且预后较差。若LINC02447以及AL590428.1至少其中之一发生高甲基化或者表达较低时,认为该胶质瘤患者预后较好。
实施例3胶质瘤免疫治疗疗效预测
在临床上通过检测LINC02447以及AL590428.1至少其中之一的甲基化或者表达水平,可以对胶质瘤患者免疫治疗疗效进行判断。LINC02447以及AL590428.1的甲基化或者表达水平方法同实施例2。
当LINC02447以及AL590428.1至少其中之一发生低甲基化或者表达较高时,认为该患者不适合接受免疫治疗,需对相应lncRNA进行抑制之后,再进行免疫治疗。若LINC02447以及AL590428.1至少其中之一发生高甲基化或者表达较低时,认为该胶质瘤患者能够从免疫治疗中受益。
