一种检测HEK293细胞残留DNA的方法
文献发布时间:2024-04-18 19:58:21
技术领域
本发明涉及生物技术领域,具体涉及一种qPCR扩增法测量HEK293细胞残留DNA的方法,以及相应的引物和探针。
背景技术
HEK293细胞即人胚胎肾细胞293(ATCC CRL-1573),其具有转染效率高、可悬浮培养的特点,且HEK293细胞在培养体系中能够快速增长,实现高密度培养用于大规模表达,因此被广泛的用于生产蛋白、疫苗、抗癌试剂及重组腺病毒包被等。宿主细胞残留DNA是指可能出现于生物制品中的来自宿主细胞的DNA片段。用传代细胞株生产的生物制品,其宿主细胞残留DNA可能会传递肿瘤或病毒相关基因,存在潜在的危险性。由于残余DNA的潜在致病风险性,各国药品监督管理机构对宿主细胞DNA的残留量有着严格的限度控制,同时各国药典也提供数种经典的检测方法。WHO和欧盟规定每人份的生物制剂产品中DNA的残留量需控制在10ng以下;美国FDA则规定每人份生物制剂产品中DNA的残留量在100pg以内。
建立合适的宿主细胞残留DNA检测方法有助于监测生产工艺,确保生物制品的安全性和质量。目前以实时定量聚合酶链式反应(qPCR)方法为最优。qPCR法是具有序列特异性以及高灵敏度等优点的检测方法,它通过同时加入一对引物和探针,在PCR扩增时产物的增加可以通过荧光信号的强弱指示,最后通过实时监控体系中的荧光信号强弱,可以对样本进行定量分析。现在qPCR法因其高特异性、高灵敏度等特点而得到广泛的应用。
通过qPCR法检测HEK293细胞内残留的DNA已经有了部分报道,如CN115747344公开了一种qPCR法HEK293细胞残留DNA检测试剂盒,以上提到的文献以全文引入本申请。基于研发人员更高的需求,如何设计出一种更精确、检测下限更低的DNA残留的检测方法,仍然是本领域亟待解决的问题。
发明内容
在一方面,本发明提供一种qPCR扩增法测量HEK293细胞残留DNA的方法,其特征在于,所述qPCR扩增所用特异性引物及探针如下所示:
HEK293 qPCR 上游引物:5'-CGGGTTCACGCCATTCTCC-3' (SEQ ID NO:1);
HEK293 qPCR下游引物:5'-TAAAAATTAGCCGGGCGTAGTGG-3' (SEQ ID NO:2);以及
HEK293 qPCR探针:5'-TGCCTCAGCCTCCCGAGT -3' (SEQ ID NO:7)。
引物的设计位置为人源RP11-279F15序列位置。人源RP11-279F15位于人13号染色体,设计引物扩增的片段大小为81bp,具体序列如下所示:
CGGGTTCACGCCATTCTCCTGCCTCAGCCTCCCGAGTAGCTGGGACTGCAGGCGCTCACCACTACGCCCGGCTAATTTTTA (SEQ ID NO:8)。
进一步地,DNAprobe为包括荧光基团和荧光淬灭基团的单链DNA探针,荧光基团为FAM,荧光淬灭基团为BHQ1。
进一步地,还包括样品的前置处理,样品处理为一种基于磁珠的样本前置处理。
进一步地,qPCR扩增的反应体系中的上游引物的浓度为10 μM,下游引物的浓度为10 μM,探针的浓度为10 μM。
在一些实施方式中,qPCR扩增的反应体系中的上游引物的浓度为10 μM;在一些实施方式中,下游引物的浓度为10 μM;在一些实施方式中,探针的浓度为10 μM。
进一步地,qPCR扩增的反应体系为20 μl,其组成为:qPCR MIX 10 μl,上游引物0.4 μl,下游引物 0.4 μl,探针 0.2 μl,DNA 5 μl,ddH
在一些实施方式中,qPCR MIX为ACeQ Universal U+ Probe Master Mix V2,购自南京诺唯赞生物科技股份有限公司。
进一步地,qPCR扩增的反应程序为37 ℃恒温2 min,95 ℃预变性5 min,然后95℃ 10 sec,60 ℃ 30 sec,40个循环。
在另一方面,本申请还提供一种qPCR扩增法检测HEK293细胞残留DNA的试剂盒,试剂盒包括如下所示qPCR扩增所用特异性引物及探针:
HEK293 qPCR 上游引物:5'-CGGGTTCACGCCATTCTCC-3' (SEQ ID NO:1);
HEK293 qPCR下游引物:5'-TAAAAATTAGCCGGGCGTAGTGG-3' (SEQ ID NO:2);
HEK293 qPCR探针:5'-TGCCTCAGCCTCCCGAGT -3' (SEQ ID NO:7)。
进一步地,该试剂盒在qPCR扩增的过程中上游引物的浓度为10 μM,所述下游引物的浓度为10 μM,所述探针的浓度为10 μM。
进一步地,该试剂盒在qPCR扩增过程中的反应程序为37 ℃恒温2 min,95 ℃预变性5min,然后95 ℃ 10 sec,60 ℃ 30 sec,40个循环。
本发明提供的qPCR扩增法测量HEK293宿主细胞残留的DNA的方法,其qPCR扩增所用上游引物为5'-CGGGTTCACGCCATTCTCC-3' (SEQ ID NO:1),其qPCR扩增所用下游引物为5'-TAAAA ATTAGCCGGGCGTAGTGG-3' (SEQ ID NO:2),qPCR扩增所用探针为5'-TGCCTCAGCCTCCCGAGT -3' (SEQ ID NO:7),其定量限可以达到1 fg,其检测限能够更低,具有高效、快速、准确、重复性好的优点。
附图说明
为了更好地理解本发明并更清楚地展示出如何实现本发明,现通过示例的方式并参考附图阐述了根据本发明的实施方式的特征,其中:
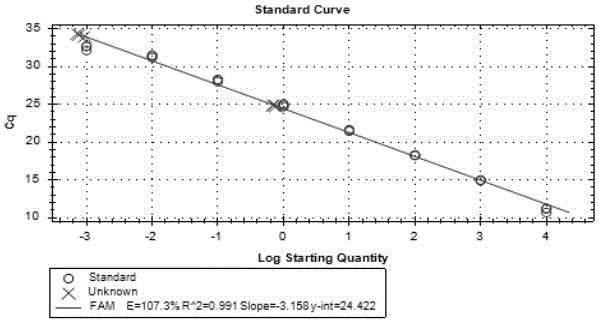
图1:实施例3中线性关系标准曲线1的示意图。
图2:实施例3中线性关系标准曲线2的示意图。
图3:实施例3中线性关系标准曲线3的示意图。
图4:实施例4中准确度标准曲线1的示意图。
图5:实施例4中准确度标准曲线2的示意图。
图6:实施例4中准确度标准曲线3的示意图。
图7:实施例5中专属性标准曲线1的示意图。
图8:实施例5中专属性标准曲线2的示意图。
图9:实施例5中专属性标准曲线3的示意图。
图10:实施例6中重复性标准曲线1的示意图。
图11:实施例6中重复性标准曲线2的示意图。
图12:实施例6中重复性标准曲线3的示意图。
具体实施方式
除非另有定义或上下文另有明确规定,本文使用的所有技术和科学术语具有与本发明所属领域的普通技术人员通常理解的相同的含义。应当理解,与本文所述类似或等同的任何方法和材料可用于本发明的实践或测试。
除非另有定义或上下文另有明确规定,本发明使用的所有材料或仪器均来自商业购买。
主要仪器和材料
。
实施例
通过参考以下实施例将更容易理解本发明,所述实施例用于说明本发明,而不应被解释为以任何方式限制本发明的范围。
尽管参照本发明的实施例详细描述了本发明,但提供这些实施例是为了说明而不是限制本发明。根据本发明原理能够得到的其它实施例均属于本发明权利要求所界定的范畴。
实施例1 引物、探针设计及优化
基于Genebank数据库及国内外文献的发掘分析,根据引物、探针设计的基本原则,以位于人13号染色体的81bp的人源RP11-279F15作为模板对设计的多对引物和探针进行筛选;得到特异性、灵敏度和重复性好的最适引物探针组合,筛选出的三组引物(N1、N2和N3)序列如下:
N1
HEK293 qPCR 上游引物:5'-CGGGTTCACGCCATTCTCC-3' (SEQ ID NO:1);
HEK293 qPCR下游引物:5'-TAAAAATTAGCCGGGCGTAGTGG-3' (SEQ ID NO:2);
N2
293HCD-F1:ATTCTCCTGCCTCAGCCT (SEQ ID NO:3);
293HCD-R1:AAATTAGCCGGGCGTAGT (SEQ ID NO:4);
N3
293HCD-F2:ACGCCATTCTCCTGCCTC (SEQ ID NO:5);
293HCD-R2:ATTAGCCGGGCGTAGTGG (SEQ ID NO:6);
探针序列如下:
HEK293 qPCR探针:5'-TGCCTCAGCCTCCCGAGT -3' (SEQ ID NO:7)。
实施例2 荧光定量PCR反应体系的优化
结合实施例1筛选出的三组引物探针组合,在荧光定量PCR反应体系中其它组分不变的情况下,将引物和探针的浓度分别设定为1μM,2 μM,5 μM,10 μM和12 μM进行PCR反应。多次重复试验结果表明,最佳的引物浓度为10 μM,最佳的探针浓度为10 μM。
结合实施例1筛选出的最适引物探针组合,在反应体系中其它组分不变的情况下,将退火延伸温度分别设定为65 ℃,75 ℃,85 ℃,95 ℃进行PCR反应。多次重复试验结果表明,最佳退火延伸温度为95 ℃。实验的反应程序为:37 ℃恒温2 min,95 ℃预变性5 min,然后95 ℃ 10 sec,60 ℃ 30 sec,40个循环。
实施例3 标准曲线的绘制
取出保存于-80℃冰箱中的定量参考标准品293 HCD(Host cell DNA,宿主细胞DNA),其浓度为50ng/μl ,记为STD0,配置293 HCD各个梯度浓度的稀释液,其具体稀释情况如表1所示:
表1 293 HCD标准品梯度浓度配置
。
配制qPCR的反应混合物溶液,按照优化后的实验条件,反应体系为20 μl,根据所用孔数按照表2的比例进行配置混合液:
表2 qPCR的反应混合物溶液
。
将不含待测样品的qPCR的15 μl反应混合物溶液分装到白色八连管中后,分别取按表1稀释后的标准品(STD1-STD8)各5 μl作为模板样品,加入分装后的白色八连管中。设置qPCR反应程序:37 ℃恒温2 min,95 ℃预变性5 min,然后95 ℃ 10 sec,60 ℃ 30 sec,40个循环;反应体积20 μl,PCR扩增反应的具体参数如表3所示。
表3 qPCR扩增反应程序
。
为了确定起始DNA浓度的对数和阈值循环数之间是否存在的线性关系,根据表1中STD1~STD8的样品以及不含标准品的制剂液空白对照组STD9对分别对N1、N2、N3引物对进行三次检测。得到的N1引物对对应线性关系标准曲线如图1、图2和图3所示,其具体的检测数据如表4所示。
表4 N1引物对标准曲线结果汇总表
。
得到的N2引物对对应线性关系,其具体的检测数据如表5所示。
表5 N2引物对标准曲线结果汇总表
。
得到的N3引物对对应线性关系,其具体的检测数据如表6所示。
表6 N3引物对标准曲线结果汇总表
。
由表4、表5、表6数据可知,N2、N3引物对对应的标准曲线,当标准品浓度在1 fg/ug时,其对应CT值出现了大于不含标准品的空白对照组的情况,即所测结果会受到制剂液的干扰,而N1引物对对应的标准曲线,当标准品浓度在1 fg/ug时,其对应CT值均小于不含标准品的空白对照组,不受制剂液的影响,因此,N1引物对检测体系显著优于N2、N3引物对监测体系,且其RSD 及相关系数(R
实施例4 准确度检测
为了确认本发明提供的使用qPCR法检测HEK293细胞残留DNA的方法进行的测定的平均结果与作为真值的偏差是否在可接受的范围内,采用赛默飞磁珠法提取试剂盒(货号:4400793)提取未知浓度的待测样品,然后未知浓度的待测样品记为序号1,未知浓度的待测样品加已知浓度的标准品记为序号2,对未知浓度的待测样品进行加标回收率的检测,如果加标回收率的值在50-150 %的范围内;RSD值均小于20 %,则认为准确度成立。加标回收率的计算公式:加标回收率=(待测样品加标后测定值(pg/μl) -待测样品未加标时检测值(pg/μl))/理论加标值(pg/μl)×100 %。制备样品及加标样品,如表7所示:
表7 准确度样品制备
。
准确度标准曲线绘制,根据实施例3提供的反应条件,以表7提供的序号1以及序号2样品作为模板,进行三次检测,得到的准确度标准曲线如图4、图5和图6所示,通过标准曲线得到的检测数据如表8所示;
表8 准确度检测数据
。
由以上数据可知,本发明所提供的方法,待测样品的RSD为7.76,加标样品,即待测样品与标准品的混合物,其RSD为9.15,RSD值均小于20 %;待测样品的加标回收率为77.71,在50-150 %的范围内,本发明提供的检测方法具有较高的准确度。
实施例5 专属性检测
专属性指样品中可能存在其他成分的情况下,所用分析方法能够准确地、选择性地检识被测组分的能力,又称为选择性或专一性。主要是考察杂质及其他成分对待检成分测定结果的影响,可通过空白试验来考察。为了确认qPCR法检测HEK293细胞残留DNA的专属性,以AAV为例,准备两种样品,分别是含有293细胞残留DNA的AAV作为样品1,以及不含293细胞残留DNA的AAV制剂液作为样品2,AAV制剂液包含氯化钠、磷酸氢二钠、磷酸二氢钠以及P-188,然后根据实施例3提供的反应条件进行三次检测,得到的专属性标准曲线如图7、图8和图9所示,通过标准曲线得到的检测数据如表9所示;
表9:专属性样品数据
。
通过表6数据发现,含HEK293 DNA的样品1能被检测出,不含HEK293 DNA的制剂液样品2其检测的CT值低于标准曲线最低点,不会对本发明检测范围内的HEK293 DNA检测结果造成影响,表明该方法的专属性良好,符合验证要求。
实施例6 重复性检测
为确认qPCR法检测HEK293细胞残留DNA方法具有较好的重复性,制备重复性验证样品。重复性指标的评估结果RSD<20%时,重复性指标的评估结果符合验收标准。制备方案照表4序号1的待测样品进行制备,对待测样品进行三次检测,得到重复性标准曲线如图10、图11和图12所示,通过重复性标准曲线得到的数据如表10所示;
表10 重复性样品数据
。
根据表10中的数据可以得出,3次重复性实验中样本检测浓度对应的RSD值为7.76%,重复性指标的评估结果RSD<20%,符合验收标准,本发明提供的方法具有较好的重复性。
实施例7 检测限
为确认qPCR法检测HEK293细胞残留DNA方法的检测限,每次进行测定的样品平均CT值结果低于无模板对照平均CT值结果,RSD值小于20%,则可确定检测限。制备检测限验证样品,制备方案照表11进行制备,对不同浓度样品进行三次检测,得到检测限标准曲线如图1~图3所示,通过标准曲线得到的数据如表12所示;
表11 检测限样品制备
。
表12 检测限样品数据
。
根据表12可以得出,3次重复性实验中,每次实验的0. 8 pg/μl和0.5 pg/μl样本检测CT值皆小于对应的无模板对照检测CT值,3次检测限实验中0.8 pg/μl样本检测CT值对应的RSD值为0.93 %,0.5 pg/μl样本检测CT值对应的RSD值为0.92 %,综上可确定检测限为0.5 fg/μl,检测限指标的评估结果符合验收标准。
目前,HEK293细胞宿主DNA残留检测的商业化的试剂盒的检测下限一般是30 fg/μl,对于一些对检测灵敏度要求比较高的样品,商业试剂盒达不到要求,CN115747344公开的一种qPCR法HEK293细胞残留DNA检测试剂盒,其定量限为10 fg/μl,检测限为3 fg/μl,也无法满足一些更低浓度的残留DNA的定量检测。本发明定量能够达到1 fg/μl,具有高效、快速、准确、特异性强的优点。
本申请提供的qPCR扩增法测量HEK293细胞残留DNA的方法,其定量限可以达到1fg/μl,检测限能够达到更低的范围,具有高效、快速、准确、特异性强的优点。
尽管参照本发明的实施例详细描述了本发明,但提供这些实施例是为了说明而不是限制本发明。根据本发明原理能够得到的其它实施例均属于本发明权利要求所界定的范畴。
- qPCR法HEK293细胞残留DNA检测试剂盒
- 一种用于定量检测CHO宿主细胞DNA残留量的引物对及检测方法
