连续细胞培养方法
文献发布时间:2023-06-19 12:16:29
相关申请的交叉引用
本申请要求2018年9月6日提交的美国临时申请号62/727,976的权益,所述临时申请特此以引用的方式整体并入。
背景技术
连续细胞培养方法和系统在生物制造中越来越受欢迎。然而,连续细胞培养方法和系统与许多警告和并发症相关。因此,仍然需要改进的连续细胞培养方法和系统。
发明内容
本公开尤其提供了用于生产(例如,制造)细胞产物,例如重组蛋白,例如糖蛋白,例如抗体剂或融合蛋白的连续培养方法。在一些实例中,本文的方法允许使用连续培养方法(例如,灌注培养方法)来大规模生产重组蛋白。本公开鉴定并解决了现有连续细胞培养技术(例如,灌注细胞培养)的问题,所述问题在于在大规模培养(例如,至少25L,例如,至少100L)下,某些细胞具有不足的活细胞浓度和受损的细胞活力。本公开部分提供了用于剪切敏感性细胞的大规模(例如,至少25L,例如,至少100L)连续培养的方法和系统。
本公开提供了以下见解:可通过控制生物反应器系统的气体出口速度来实现剪切敏感性细胞的大规模培养。例如,在气体出口速度被控制和/或维持在限定量和/或范围内(例如,使得气体出口速度为至多20m/s)的生物反应器系统(例如,灌注生物反应器系统)中剪切敏感性细胞的大规模培养可产生在约20x10
在一些实例中,提供了方法,所述方法包括在生物反应器系统(例如,灌注生物反应器系统)中培养包含剪切敏感性细胞或由剪切敏感性细胞组成的细胞群体以达到稳态活细胞浓度,其中所述稳态活细胞浓度在20x10
在一些实例中,提供了方法,所述方法包括在包括至少25L培养基的生物反应器系统(例如,灌注生物反应器系统)中培养剪切敏感性细胞,其中所述生物反应器系统具有至多20m/s的气体出口速度,并且其中所述剪切敏感性细胞以在约20x10
在一些实例中,提供了在具有至少25L(例如,至少200L)培养基和至多20m/s(例如,至多10m/s)的气体出口速度的生物反应器系统中培养由剪切敏感性细胞组成的细胞群体,以在所述培养基中达到在20x10
在一些实例中,提供了用于培养由剪切敏感性细胞组成的细胞群体的连续培养工艺,所述工艺包括控制生物反应器系统的气体出口速度,以使得所述气体出口速度不超过20m/s的速率,其中所述生物反应器系统包括至少25L的培养基,并且其中所述细胞群体达到在20x10
在一些实施方案中,在培养剪切敏感性细胞的持续时间的至少一部分期间控制气体出口速度。在一些实施方案中,当将细胞群体(例如,剪切敏感性细胞群体,例如接种物)添加至生物反应器系统时(例如,当细胞群体与生物反应器系统的培养基组合时),开始气体出口速度的控制。在一些实施方案中,在将细胞群体(例如,剪切敏感性细胞群体,例如接种物)添加至生物反应器系统之后约2小时、6小时、12小时、24小时或48小时(例如,当细胞群体与生物反应器系统的培养基组合时),开始气体出口速度的控制。
在一些实施方案中,当正在培养的细胞达到特定密度时,在培养过程期间开始气体出口速度的控制。在一些实施方案中,当生物反应器系统具有至少1x10
在一些实施方案中,控制气体出口速度,至少直到所述生物反应器系统达到稳态条件。在一些实施方案中,稳态条件包括具有在5天的时间段内改变至多20%的活细胞浓度。在一些实施方案中,从将细胞群体(例如,剪切敏感性细胞群体,例如接种物)添加至生物反应器系统的这样的时间(例如,当细胞群体与生物反应器系统的培养基组合时)控制气体出口速度,直到培养物达到稳态条件(例如,具有在5天的时间段内改变至多20%的活细胞浓度)。在一些实施方案中,从生物反应器系统具有至少1x10
在一些实施方案中,在整个培养步骤中控制气体出口速度。在一些实施方案中,控制气体出口速度持续至少约10天、至少约15天、至少约20天、至少约25天、至少约30天、至少约40天、至少约50天或至少约60天的培养。在一些实施方案中,从将细胞群体(例如,剪切敏感性细胞群体,例如接种物)添加至生物反应器系统(例如,当细胞群体与生物反应器系统的培养基组合时)的这样的时间控制气体出口速度,并且持续至少约10天、至少约15天、至少约20天、至少约25天、至少约30天、至少约40天、至少约50天或至少约60天的培养。在一些实施方案中,从生物反应器系统具有至少1x10
在一些实例中,提供了用于培养剪切敏感性细胞的灌注培养工艺,所述灌注培养工艺包括控制灌注生物反应器系统的气体出口速度,以使得所述气体出口速度不超过20m/s的速率,其中所述灌注生物反应器系统包括至少25L的培养基,其中所述培养基包含剪切敏感性细胞,并且其中所述剪切敏感性细胞以在约20x10
在一些实施方案中,剪切敏感性细胞的稳态活细胞浓度处于由下限和上限限定的范围内的量,所述上限大于所述下限。在一些实施方案中,所述下限可以是约20x10
在一些实施方案中,灌注生物反应器系统具有受控水平的溶解二氧化碳。在一些实施方案中,培养基包含120mmHg或更低、115mmHg或更低、110mmHg或更低、105mmHg或更低、100mmHg或更低、95mmHg或更低、90mmHg或更低、85mmHg或更低或80mm Hg或更低的溶解二氧化碳水平。
在一些某些实施方案中,灌注生物反应器系统具有10m/s或更低的气体出口速度;并且包括80mmHg或更低的溶解二氧化碳水平。
在一些实施方案中,细胞培养系统具有120mmHg或更低的溶解二氧化碳水平。在一些实施方案中,连续细胞培养系统(例如,灌注细胞培养系统)具有在约20mmHg至约120mmHg范围内的溶解二氧化碳水平。在一些实施方案中,溶解二氧化碳以在由下限和上限限定的范围内的量存在于连续细胞培养基中,所述上限大于所述下限。在一些实施方案中,所述下限可以是约20mmHg、约30mmHg、约40mmHg、约50mmHg、约60mmHg或约70mmHg。在一些实施方案中,所述上限可以是约50mmHg、约60mmHg、约70mmHg、约80mmHg、约90mmHg、约100mmHg、约110mmHg或约120mmHg。
在一些实施方案中,灌注生物反应器系统包括至少50L、至少100L、至少200L、至少500L、至少1,000L或至少2,000L的培养基。
在一些实施方案中,剪切敏感性细胞的连续培养进行至少10天的持续时间。在一些实施方案中,剪切敏感性细胞的连续培养进行约30天至约60天的持续时间。
在一些实施方案中,剪切敏感性细胞的连续培养进行在10天至180天范围内的持续时间。在一些实施方案中,剪切敏感性细胞的连续培养进行在由下限和上限限定的范围内的时间量,所述上限大于所述下限。在一些实施方案中,所述下限可以是约10天、约15天、约20天、约25天、约30天、约35天、约40天、约50天或约60天。在一些实施方案中,所述上限可以是约30天、约35天、约40天、约50天、约60天、约70天、约80天、约90天、约100天、约120天、约140天、约160天或约180天。
在一些实施方案中,本公开的连续培养方法包括测量活细胞浓度的步骤。在一些实施方案中,所测量的活细胞浓度是至少30x10
在一些实施方案中,用于根据本公开培养的剪切敏感性细胞是哺乳动物细胞。
在一些实施方案中,剪切敏感性细胞是哺乳动物细胞。在一些实施方案中,剪切敏感性细胞是鼠类细胞。在一些实施方案中,剪切敏感性细胞是来自小鼠细胞系。在一些实施方案中,剪切敏感性细胞系是小鼠骨髓瘤细胞系。在一些某些实施方案中,剪切敏感性细胞选自:NS0细胞和SP 2/0细胞。在一些某些实施方案中,根据本公开使用的剪切敏感性细胞是SP 2/0细胞。
在一些实施方案中,剪切敏感性细胞是人类细胞。在一些实施方案中,人剪切敏感性细胞系选自:HEK 293:人胚肾293;HT-1080:来自具有上皮样表型的纤维肉瘤;PER.C6:经由用腺病毒E1基因转染而永生化的人胚胎视网膜细胞;CAP:来自通过腺病毒5型E1基因永生化的人羊膜细胞;HKB-11:通过HEK293-S与人B细胞系的聚乙二醇融合而产生;以及HuH-7:来自人肝细胞癌。在一些某些实施方案中,剪切敏感性细胞选自:HEK 293细胞、纤维肉瘤HT 1080细胞、PER.C6细胞、CAP细胞、HKB-11细胞和HuH-7细胞。
在一些实施方案中,将根据本公开使用的剪切敏感性细胞工程化以包含或表达细胞产物。在一些实施方案中,培养的剪切敏感性细胞包括或表达细胞产物。在一些实施方案中,细胞产物是或包括核酸、脂质、肽和/或蛋白质。在一些实施方案中,细胞产物是重组蛋白。在一些实施方案中,重组蛋白是糖蛋白。在一些实施方案中,糖蛋白是含Fc的糖蛋白。在一些实施方案中,糖蛋白是抗体剂。在一些实施方案中,抗体剂是单克隆抗体。在一些某些实施方案中,单克隆抗体是优特克单抗。
在一些实施方案中,本公开的剪切敏感性细胞包含编码抗体剂的核酸,所述抗体剂已例如在二次批准流程中被批准用于人或动物中的治疗或诊断用途。在一些某些实施方案中,本公开的剪切敏感性细胞包含编码优特克单抗的核酸。
在一些实施方案中,本公开的方法和/或工艺包括从所述细胞的至少一部分中分离细胞产物和/或从所述培养基的至少一部分中分离细胞产物。在一些实施方案中,细胞产物是重组蛋白,例如糖蛋白,例如含Fc的糖蛋白,例如抗体剂,例如单克隆抗体。
在一些实施方案中,细胞培养基还包含浓度在1ppm至500ppm范围内的消泡剂(例如,消泡剂C)。在一些实施方案中,在包含剪切力保护剂(例如,Pluronic F-68)的细胞培养基中培养剪切敏感性细胞。在一些实施方案中,在包含浓度在1g/L至15g/L范围内的Pluronic F-68的细胞培养基中培养剪切敏感性细胞(例如,剪切敏感性细胞群体)。在一些实施方案中,在包含浓度在1ppm至500ppm范围内的消泡剂(例如,消泡剂C)和浓度在1g/L至15g/L范围内的剪切力保护剂(例如,Pluronic F-68)的培养基中培养剪切敏感性细胞群体。
在一些实施方案中,灌注生物反应器系统包括生物反应器槽。在一些实施方案中,生物反应器槽是搅拌生物反应器槽。在一些实施方案中,生物反应器槽具有至少50L、100L、200L、250L、400L、500L、600L、800L、1,000L或2,000L的容量。在一些某些实施方案中,生物反应器槽具有约200L、约250L或更高的容量。
在一些实施方案中,生物反应器系统(例如,灌注生物反应器系统)包括细胞截留装置。在一些实施方案中,细胞截留装置是或包括连续离心机、交替切向流过滤器(ATF)、切向流膜过滤器(TFF)、动态过滤器、自旋过滤器、超声和介电泳分离器或重力沉降器。在一些某些实施方案中,细胞截留装置是或包括ATF。
在一些实施方案中,生物反应器系统包括搅拌槽生物反应器、细胞截留装置、培养基供应和排出废物收集。
在一些实施方案中,生物反应器系统(例如,灌注生物反应器系统)包括喷射器。在一些实施方案中,生物反应器系统包括钻孔喷射器。在一些实施方案中,生物反应器系统包括开管喷射器。在一些实施方案中,生物反应器系统包括烧结喷射器。
在一些实例中,提供了剪切敏感性细胞的大规模(例如,至少25L,例如,至少100L)连续培养的方法,所述方法包括:提供或获得包含编码重组蛋白的核酸的剪切敏感性细胞,以及在具有受控气体出口速度的生物反应器系统中并在足以表达所述重组蛋白的条件下培养细胞。在一些实施方案中,生物反应器系统具有控制在至多20m/s(例如,约5m/s至约10m/s)的速率下的气体出口速度,直到所述系统达到稳态条件。在一些实施方案中,生物反应器系统在整个培养过程中具有控制在至多20m/s(例如,约5m/s至约10m/s)的速率下的气体出口速度。在一些实施方案中,稳态条件下的活细胞浓度在约20x10
在一些实例中,提供了产生剪切敏感性细胞的蛋白质制剂连续培养的方法,所述方法包括:在具有受控气体出口速度的生物反应器系统中连续培养所述剪切敏感性细胞。在一些实施方案中,生物反应器系统包括容量为至少25L、至少100L或至少200L的生物反应器槽。在一些实施方案中,所述气体出口速度控制在至多20m/s(例如,约5m/s至约10m/s)的速率下,直到所述系统达到稳态条件。在一些实施方案中,所述生物反应器系统在整个培养过程中具有控制在至多20m/s(例如,约5m/s至约10m/s)的速率的气体出口速度。在一些实施方案中,稳态条件下的活细胞浓度在约20x10
本发明的这些方面和其它方面在下文和权利要求书中更详细地描述。
附图说明
由以下附图组成的本文所包含的附图仅用于说明目的,而非限制性的。
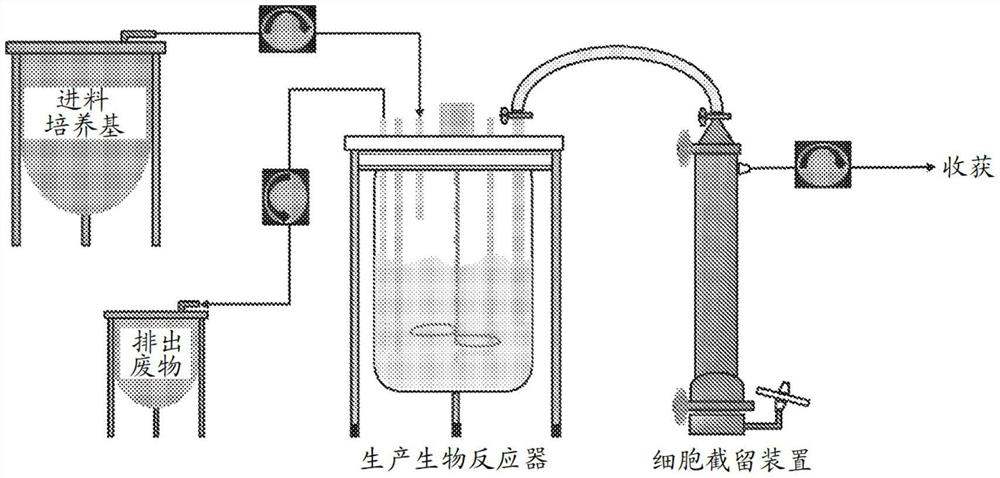
图1描绘具有示例性交替切向流作为细胞截留装置的灌注培养系统的示例性示意图。如所示,示例性灌注培养系统可包括生产生物反应器(例如,搅拌生物反应器槽)、细胞截留装置(例如,交替切向流)、进料培养基供应和排出废物。
图2描绘通过灌注培养以3L至100L的规模培养的示例性剪切敏感性细胞(例如,SP2/0细胞)的活细胞浓度(以10
图3描绘通过灌注培养以3L至200L的规模培养的示例性剪切敏感性细胞(例如,SP2/0细胞)的活细胞浓度(以10
图4描绘通过灌注培养以不同规模和不同气体出口速度培养的示例性剪切敏感性细胞(例如,SP2/0细胞)的活细胞浓度(以10
图5描绘使用3L灌注生物反应器的数个连续细胞培养运行以各种气体出口速度(GEV)进行。上图示出随时间推移的活细胞浓度(VCC),并且下图示出随时间推移的活力百分比。FU27(菱形)代表对照样品。FU28(空心正方形)代表GEV为10m/s直到第9天,然后从此为16m/s。FU29(空心三角形)代表GEV为13m/s,并且培养物在第12天崩溃。FU30(X's)代表GEV为16m/s直到第9天,然后从此下降至10m/s。
图6描绘在具有不同溶解CO
图7A和图7B描绘在控制GEV和溶解CO
图8提供总结对于不同参数,250L培养物(例如,使用SUB250生物反应器系统)的预测模型的表。
图9描绘在不同规模下剪切敏感性细胞的连续细胞培养物的总聚糖水平(上图)和唾液酸含量(下图)。每个的最左边条代表3L培养工艺,每个的中间条代表100L培养工艺,并且最右边的条代表250L培养工艺。
图10描绘相对于所证实的250L(由三角形表示)和100L(由圆圈表示)培养工艺,剪切敏感性细胞的1000L连续培养物(黑色实线)的预测的溶解CO
图11提供总结对于不同参数,1000L培养物(例如,使用SUB1000生物反应器系统)的预测模型的表。
图12提供用于确定气体出口速度的示例性等式。
一般来说,除非另外明确指明,否则本文所使用的术语是根据其在本领域中所理解的含义。某些术语的明确定义在下文提供;在整个本说明书中,在特定情况下,这些和其它术语的含义对于本领域技术人员而言将是显而易见的。
本说明书中引用的参考文献或其相关部分以引用的方式并入本文。
为了使本发明可更容易理解,在下文首先定义某些术语。以下术语和其它术语的另外的定义在整个说明书中阐述。
如本文所用,在应用于一个或多个目标值时,术语“约”或“大约”是指类似于所陈述的参考值的值。在某些实施方案中,术语“约”或“大约”是指落在所陈述的参考值的25%、20%、19%、18%、17%、16%、15%、14%、13%、12%、11%、10%、9%、8%、7%、6%、5%、4%、3%、2%、1%或更低内的值范围。
如本文所用,术语“抗体”具有其本领域所理解的含义,并且是指与特定抗原特异性地结合的免疫球蛋白(Ig)。如本领域普通技术人员所已知,在自然界中产生的抗体通常包含四条多肽链,两条重(H)链和两条轻(L)链。每条重链和轻链由可变区(分别在本文中缩写为HCVR或V
如本文所用,术语“抗体剂”是指与特定抗原特异性地结合的剂。在一些实施方案中,所述术语涵盖具有足以赋予特异性结合的免疫球蛋白结构元件的任何多肽。在各种实施方案中,合适的抗体剂可包括但不限于单克隆抗体、多克隆抗体、人源化抗体、灵长类化抗体、嵌合抗体、人抗体、双特异性抗体或多特异性抗体、单结构域抗体(例如,鲨鱼单结构域抗体(例如,IgNAR或其片段))、缀合抗体(即,与其它蛋白质、放射性标记、细胞毒素等缀合或融合的抗体)、小模块免疫药物(“SMIP
如本文所用,术语“生物制剂”、“生物治疗剂”和“生物产物”可互换地用于指多肽和蛋白质产物。例如,本文的生物制剂包括在细胞中表达的天然来源的或重组的产物,例如像蛋白质、糖蛋白、融合蛋白、生长因子、疫苗、血液因子、溶栓剂、激素、干扰素、基于白介素的产物、抗体剂(例如,单克隆抗体、双特异性抗体等)和治疗性酶。一些生物制剂是根据公共卫生署(PHS)法案的第351(a)条,根据“生物制剂许可申请”或“BLA”批准的,而参考BLA作为参考产品的生物仿制药和可互换生物制剂则根据PHS法案的第351(k)条获得许可。PHS法案的第351条编纂为42U.S.C.262。其它生物制剂可根据联邦食品和化妆品法案的第505(b)(1)条获得批准,或根据哈奇维克斯曼法案的第505(b)(2)和505(j)条批准为简化申请,其中第505条被编纂为21U.S.C.355。
如本文所用,“气体出口速度”是指从生物反应器系统的气体源,例如用于对培养基进行通气(例如,供应空气和/或氧气)的气体源离开的气体的速率。在一些实施方案中,气体出口速度是指气体从一个或多个气体源开口(例如,孔)离开并进入培养基的速率。在一些实施方案中,使用如图12中提供的等式来计算气体出口速度。在一些实施方案中,生物反应器系统包括喷射器,并且气体出口速度是指从一个或多个喷射器开口(例如,孔)离开的气体的速率。在一些实施方案中,生物反应器系统包括喷射器,并且气体出口速度是指从所述喷射器的开口离开的气体的速率的平均值。
如本文所用,“糖蛋白”是指包含共价附接于其上的一个或多个寡糖链(例如,聚糖)的氨基酸序列。示例性氨基酸序列包括肽、多肽和蛋白质。示例性糖蛋白包括糖基化抗体、抗体剂和抗体样分子(例如,Fc融合蛋白)。示例性抗体包括单克隆抗体和/或其片段、多克隆抗体和/或其片段以及含有Fc结构域的融合蛋白(例如,含有IgG1的Fc区或其糖基化部分的融合蛋白)。
如本文所用的术语“分离的”是指物质和/或实体已(1)与它在最初产生时(无论在自然界中和/或在实验环境中)与其缔合的至少一些组分分离,和/或(2)手动设计、产生、制备和/或制造。分离的物质和/或实体可与约10%、约20%、约30%、约40%、约50%、约60%、约70%、约80%、约90%、约91%、约92%、约93%、约94%、约95%、约96%、约97%、约98%、约99%或多于约99%的它们最初与其缔合的其它组分分离。在一些实施方案中,分离的剂是约80%、约85%、约90%、约91%、约92%、约93%、约94%、约95%、约96%、约97%、约98%、约99%或高于约99%纯。如本文所用,如果物质基本上不含其它组分,则所述物质为“纯的”。在一些实施方案中,如本领域技术人员将理解的,在与某些其它组分例如像一种或多种载体或赋形剂(例如,缓冲剂、溶剂、水等)组合后,物质仍可被认为是“分离的”或甚至“纯的”;在此类实施方案中,在不包括此类载体或赋形剂的情况下计算物质的分离百分比或纯度。仅举一个实例,在一些实施方案中,当在自然界中存在的生物聚合物,如多肽或多核苷酸a)根据其来源或衍生源不与在自然界中在其天然状态中伴随其的一些或全部组分缔合;b)其基本上不含来自在自然界中产生其的物种的相同物种的其它多肽或核酸;c)由来自细胞或其它表达系统的组分表达或以其它方式与来自细胞或其它表达系统的组分缔合(所述细胞或其它表达系统不是在自然界中产生其的物种)时,所述生物聚合物被认为是“分离的”。因此,例如,在一些实施方案中,化学合成的或在不同于在自然界中产生其的细胞系统的细胞系统中合成的多肽被认为是“分离的”多肽。或者地或另外地,在一些实施方案中,已经经历一种或多种纯化技术的多肽在其已经与a)在自然界中与其缔合;和/或b)在最初生产时与其缔合的其它组分分离的程度上可被认为是“分离的”多肽。
如本文所用,“回收”是指例如通过分离,例如使用本领域已知的纯化技术使剂或实体基本上不含其它先前相关的组分的过程。在一些实施方案中,从天然来源和/或包含细胞的来源回收剂或实体。
一般来说,如本文所用的“蛋白质”是多肽(即,通过肽键彼此连接的至少两个氨基酸的串)。蛋白质可包含除了氨基酸以外的部分(例如,可以是糖蛋白)并且/或者可以其它方式进行加工或修饰。本领域的普通技术人员将理解,“蛋白质”可以是由细胞产生的完整多肽链(含或不含信号序列),或者可以是其特征部分。本领域的普通技术人员将进一步理解,蛋白质有时可包含例如通过一个或多个二硫键连接或通过其它方式缔合的多于一个多肽链。
如本文所用,术语“蛋白质制剂”是指根据特定生产方法获得的蛋白质的混合物。蛋白质制剂中的蛋白质可相同或不同,即蛋白质制剂可包含同一蛋白质的多个拷贝和/或不同蛋白质的混合物。在一些实施方案中,蛋白质制剂包括糖蛋白制剂。糖蛋白制剂是包含至少一种糖蛋白的组合物或混合物。在一些实例中,糖蛋白制剂包含同一蛋白质的多个拷贝(即,具有相同的氨基酸序列),但是具有与所述蛋白质相关的聚糖的混合物。在一些实例中,使用如本文提供的方法和/或系统制备糖蛋白制剂。生产方法可包括使用经培养的细胞的重组制备步骤,所述经培养的细胞已被工程化以表达蛋白质制剂中的蛋白质(或以相关水平或在相关条件下表达所述蛋白质)。在一些实施方案中,生产方法可包括分离步骤,其中从工程化的细胞的某些组分中分离蛋白质(例如,通过裂解细胞并通过离心使蛋白质组分沉淀)。在一些实施方案中,生产方法还可包括纯化步骤,其中将蛋白质制剂中的蛋白质与其它细胞组分,例如较早步骤中使用的其它蛋白质或有机组分分离(例如,通过色谱法)。应当理解,这些步骤是非限制性的,并且可包括任何数量的另外生产步骤。可通过相同的生产方法,但在不同的场合(例如,不同的运行或制备)来制备不同的蛋白质制剂。或者,可通过不同的生产方法来制备不同的蛋白质制剂。两种生产方法可在任何方面(例如表达载体、工程化的细胞类型、培养条件、分离程序、纯化条件等)有所不同。
如本文所用,“样品”是指单独采购的样品。在一些实施方案中,分离样品的评估包括来自相同培养运行(例如,在制备期间的不同时间点)或来自不同培养运行(例如,不同轮次的培养)的样品的评估。
如本文所用,“喷射”或“气体喷射”是指将气体(例如,空气和/或O
如本文所用,如关于细胞培养系统或工艺的“稳态”或“稳态条件”是指细胞培养物具有在至少5天的时间段(例如,5天至约60天)内改变至多20%的活细胞浓度。在一些实施方案中,细胞培养系统具有在5天的时间段内改变至多20%的活细胞浓度。在一些实施方案中,细胞培养系统具有在至少5天(例如,5天、10天、15天、20天、25天、30天、40天、50天、60天)的时间段内改变至多15%、至多10%或至多5%的活细胞浓度。在一些实施方案中,细胞培养系统具有在5天的时间段内改变至多15%、至多10%或至多5%的活细胞浓度。在一些实施方案中,细胞培养系统具有在至少5天(例如,5天、10天、15天、20天、25天、30天、40天、50天、60天)的时间段内改变至多10%(即,在加或减10%的范围内)的剪切敏感性细胞的活细胞浓度。在一些实施方案中,细胞培养系统具有在5天的时间段内改变至多10%(即,在加或减10%的范围内)的剪切敏感性细胞的活细胞浓度。在一些实施方案中,通过使生物反应器系统排出(例如,除去过量细胞)来达到和/或维持稳态活细胞浓度。
在本申请中引用的所有文献和类似材料(包括但不限于专利、专利申请、文章、书籍、论文以及网页)明确地以引用的方式整体并入,无论此类文献和类似材料的格式如何。在一篇或多篇并入的文献和类似材料与本申请(包括但不限于定义的术语、术语用法、描述的技术等)不同或矛盾的情况下,以本申请为准。本文使用的章节标题仅是出于组构目的,并且不应解释为以任何方式限制所描述的主题。
具体实施方式
本公开鉴定并部分解决了现有连续细胞培养技术(例如,灌注细胞培养)的问题,所述问题在于在大培养体积(例如,至少100L,例如,至少200L)下,某些细胞具有不足的活细胞浓度和受损的细胞活力。本公开涵盖以下认识:由于其对氧供应和溶解二氧化碳(pCO
本公开涵盖以下认识:通气的重要性随生物反应器体积和细胞浓度而增加。特别地,本公开提供了以下见解:控制生物反应器系统的气体出口速度可改善某些细胞(例如像,剪切敏感性细胞)的大规模连续培养的性能。
在一些实施方案中,本公开提供了用于剪切敏感性细胞的大规模(例如,至少100L,例如,至少200L)连续培养(例如,灌注培养)的方法和工艺,其中生物反应器系统的气体出口速度被控制和/或维持在限定的量和/或范围内。例如,提供了在气体出口速度为至多20m/s(例如,至多10m/s)的生物反应器系统(例如,灌注生物反应器系统)中剪切敏感性细胞的大规模培养的方法。所提供的方法允许产生高密度细胞培养物(例如,具有在20x10
本公开部分提供了用于剪切敏感性细胞(例如,包含剪切敏感性细胞的细胞群体,例如由剪切敏感性细胞组成的细胞群体)的大规模(例如,至少25L,例如,至少100L,例如,至少200L)连续培养(例如,灌注细胞培养)的方法、工艺和/或系统。在一些实施方案中,大规模培养是25L至3,000L。在一些实施方案中,大规模培养是25L、50L、100L、200L、250L、400L、500L、600L、800L、1000L、1200L、1500L、2000L、3000L或更大。在一些实施方案中,大规模培养是100L或更大。在一些某些实施方案中,大规模培养是200L或更大。在一些某些实施方案中,大规模培养是250L或更大。
在一些实例中,连续细胞培养系统(例如,灌注细胞培养系统)是可产生高密度的剪切敏感性细胞(例如,稳态活细胞浓度为例如至少20x10
在一些实例中,连续细胞培养的方法、工艺和/或系统具有和/或达到在约20x10
一般来说,本公开的细胞培养方法包括在25℃至40℃范围内的温度下并且在地球上遇到的重力下进行培养。
在一些实施方案中,连续细胞培养系统(例如,灌注细胞培养系统)具有在约1m/s至约20m/s范围内的气体出口速度。在一些实施方案中,连续细胞培养系统(例如,灌注细胞培养系统)具有在约1m/s至约10m/s范围内的气体出口速度。在一些实施方案中,连续细胞培养系统(例如,灌注细胞培养系统)具有不超过20m/s的气体出口速度。在一些实施方案中,连续细胞培养系统(例如,灌注细胞培养系统)具有不超过10m/s的气体出口速度。
在一些实施方案中,连续细胞培养系统(例如,灌注细胞培养系统)具有在由下限和上限限定的范围内的速率下的气体出口速度,所述上限大于所述下限。在一些实施方案中,下限可以是约1m/s、约2m/s、约3m/s、约4m/s、约5m/s、约6m/s、约7m/s、约8m/s、约9m/s或约10m/s。在一些实施方案中,上限可以是约5m/s、约6m/s、约7m/s、约8m/s、约9m/s、约10m/s、约11m/s、约12m/s、约13m/s、约14m/s、约15m/s、约16m/s、约18m/s或约20m/s。
在一些实施方案中,连续细胞培养系统(例如,灌注细胞培养系统)具有不超过120mmHg的溶解二氧化碳水平。在一些实施方案中,连续细胞培养系统(例如,灌注细胞培养系统)具有在约20mmHg至约120mmHg范围内的溶解二氧化碳水平。在一些实施方案中,溶解二氧化碳以在由下限和上限限定的范围内的量存在于连续细胞培养基中,所述上限大于所述下限。在一些实施方案中,所述下限可以是约20mmHg、约30mmHg、约40mmHg、约50mmHg、约60mmHg或约70mmHg。在一些实施方案中,所述上限可以是约50mmHg、约60mmHg、约70mmHg、约80mmHg、约90mmHg、约100mmHg、约110mmHg或约120mmHg。
在一些实施方案中,剪切敏感性细胞(例如,包含剪切敏感性细胞的细胞群体,例如,由剪切敏感性细胞组成的细胞群体)的连续培养进行约10天至约180天范围内的持续时间。在一些实施方案中,剪切敏感性细胞(例如,包含剪切敏感性细胞的细胞群体,例如,由剪切敏感性细胞组成的细胞群体)的连续培养进行在由下限和上限限定的范围内的时间量,所述上限大于所述下限。在一些实施方案中,所述下限可以是约10天、约15天、约20天、约25天、约30天、约35天、约40天、约50天或约60天。在一些实施方案中,所述上限可以是约30天、约35天、约40天、约50天、约60天、约70天、约80天、约90天、约100天、约120天、约140天、约160天或约180天。
在一些实施方案中,剪切敏感性细胞(例如,包含剪切敏感性细胞的细胞群体,例如,由剪切敏感性细胞组成的细胞群体)的连续培养进行至少10天的持续时间。在一些实施方案中,剪切敏感性细胞(例如,包含剪切敏感性细胞的细胞群体,例如,由剪切敏感性细胞组成的细胞群体)的连续培养进行约30至约60天的持续时间。
本公开提供了用于大规模连续细胞培养,如用于培养剪切敏感性细胞(例如,包含剪切敏感性细胞的细胞群体,例如,由剪切敏感性细胞组成的细胞群体)的生物反应器系统。本公开的生物反应器系统适用于连续培养方法。在一些实施方案中,本公开的生物反应器系统适用于灌注培养。在图1中描绘了适用于本公开的培养方法的生物反应器系统的示例性示意图。在一些实施方案中,生物反应器系统包括生物反应器槽和细胞截留装置。在一些实施方案中,生物反应器系统包括生物反应器槽、细胞截留装置、培养基供应和排出废物收集。在一些实施方案中,生物反应器系统还包括细胞群体(例如,由剪切敏感性细胞,例如接种物组成的细胞群体)和细胞培养基。
在一些实施方案中,生物反应器系统包括搅拌槽生物反应器。在一些实施方案中,生物反应器槽(例如,搅拌槽生物反应器的生物反应器槽)具有在25L至3,000L范围内的容量。在一些实施方案中,生物反应器槽(例如,搅拌槽生物反应器的生物反应器槽)具有至少25L、50L、100L、200L、250L、300L、400L、500L、600L、800L、1000L、1200L、1400L、1500L、1600L、1800L、2000L、2400L、2500L、2600L、2800L或3000L的容量。在一些实施方案中,搅拌槽生物反应器具有至少100L的容量。在一些实施方案中,搅拌槽生物反应器具有至少200L的容量。在一些实施方案中,搅拌槽生物反应器具有至少250L的容量。在一些实施方案中,搅拌槽生物反应器具有至少500L的容量。在一些实施方案中,搅拌槽生物反应器具有至少1000L的容量。
在一些实施方案中,生物反应器系统包括喷射器。一般来说,喷射器可用于将空气和/或氧气引入细胞培养基中。本公开涵盖以下认识,喷射器选择可影响通气的速率和程度,并且还可用于使起泡最小化。在一些实施方案中,生物反应器系统包括开管喷射器和/或钻孔喷射器。
在一些实施方案中,生物反应器系统包括钻孔喷射器。在一些实施方案中,钻孔喷射器具有尺寸在0.05mm至5.0mm范围内的孔。在一些实施方案中,钻孔喷射器具有0.1mm至1.0mm的孔。在一些实施方案中,钻孔喷射器具有尺寸在由下限和上限限定的范围内的孔,所述上限大于所述下限。在一些实施方案中,下限可以是约0.05mm、约0.06mm、约0.07mm、约0.08mm、约0.09mm、约0.1mm、约0.2mm、约0.3mm、约0.4mm、约0.5mm、约0.6mm、约0.7mm、约0.8mm、约0.9mm或约1.0mm。在一些实施方案中,上限可以是约0.2mm、约0.3mm、约0.4mm、约0.5mm、约0.6mm、约0.7mm、约0.8mm、约0.9mm、约1.0mm、约1.25mm、约1.5mm、约1.75mm、约2.0mm、约2.25mm、约2.5mm、约2.75mm、约3.0mm、约3.5mm、约4.0mm、约4.5mm或约5.0mm。
在一些实施方案中,生物反应器系统包括烧结喷射器。在一些实施方案中,生物反应器系统包括位于生物反应器槽的底部的喷射器。在一些实施方案中,生物反应器系统包括大致位于生物反应器槽内的中心的喷射器。
在一些实施方案中,生物反应器系统包括细胞截留装置。适用于本公开的生物反应器系统的细胞截留装置包括连续离心机、交替切向流过滤器(ATF)、切向流膜过滤器(TFF)、动态过滤器、自旋过滤器、超声和介电泳分离器以及重力沉降器。在一些实施方案中,本公开的生物反应器系统包括细胞交替切向流(ATF)装置。在一些实施方案中,生物反应器系统包括细胞截留装置,所述细胞截留装置包括一个或多个ATF。在一些实施方案中,生物反应器系统包括细胞截留装置,所述细胞截留装置包括两个ATF。在一些实施方案中,生物反应器系统包括细胞截留装置,所述细胞截留装置包括三个或更多个ATF。
在一些实施方案中,生物反应器系统包括叶轮装置。在一些实施方案中,叶轮是安装在生物反应器槽内的底部。在一些实施方案中,叶轮大致位于生物反应器槽内的中心。在一些实施方案中,叶轮装置是磁驱动的。在一些实施方案中,生物反应器系统具有输送约5W/m
在一些实例中,本公开的培养的方法、工艺和系统用于剪切敏感性细胞的连续培养。本公开涵盖以下认识:没有细胞壁的动物细胞可能对在搅拌槽生物反应器中培养的流体机械应力(例如像通过叶轮进行的搅拌以及来自气泡的上升和破裂)敏感,所述流体机械应力在搅拌槽中的培养基内产生以为细胞提供氧气。如果过多,这些流体机械应力可导致动物细胞的损伤/死亡。此外,本公开涵盖以下认识:某些动物细胞对机械应力引起的剪切比其它动物细胞更敏感。例如,小鼠骨髓瘤细胞可能比某些CHO细胞株更具剪切敏感性。本公开提供适合于剪切敏感性细胞的大规模高密度培养的方法、工艺和系统。
某些细胞(例如动物细胞)在本领域中已知对培养期间的某些机械和/或通气条件敏感(参见例如,Gooch等人,Curr.Opin.Biotech.4:193-196(1993))。如本文所用,剪切敏感性细胞是在常规培养条件(例如,常规大规模培养条件)下表现出对剪切的一定水平的敏感性(例如,表现出降低的细胞活力)的任何动物细胞。如本文所论述,在某些实例中,当在本文所述的条件下培养此类剪切敏感性细胞时,此类细胞表现出提高的活力水平。
在一些实施方案中,剪切敏感性细胞是哺乳动物细胞。在一些实施方案中,剪切敏感性细胞是鼠类细胞。在一些实施方案中,剪切敏感性细胞是来自小鼠细胞系。鼠类(例如小鼠)剪切敏感性细胞系包括例如小鼠骨髓瘤细胞系。在一些某些实施方案中,剪切敏感性细胞选自:NS0细胞和SP 2/0细胞。
在一些实施方案中,剪切敏感性细胞是人类细胞。在一些实施方案中,人剪切敏感性细胞系包括例如,HEK 293:人胚肾293;HT-1080:来自具有上皮样表型的纤维肉瘤;PER.C6:经由用腺病毒E1基因转染而永生化的人胚胎视网膜细胞;CAP:来自通过腺病毒5型E1基因永生化的人羊膜细胞;HKB-11:通过HEK293-S与人B细胞系的聚乙二醇融合而产生;以及HuH-7:来自人肝细胞癌。在一些某些实施方案中,剪切敏感性细胞选自:HEK 293细胞、纤维肉瘤HT 1080细胞、PER.C6细胞、CAP细胞、HKB-11细胞和HuH-7细胞。
在一些某些实施方案中,根据本公开使用的剪切敏感性细胞是SP 2/0细胞。在一些实施方案中,将根据本公开使用的剪切敏感性细胞工程化以包含或表达细胞产物。
根据本公开,可使用本领域技能范围内的常规分子生物学、微生物学和重组DNA技术。此类技术描述于文献(参见例如,Sambrook,Fritsch和Maniatis,Molecular Cloning:ALaboratory Manual,第二版(1989)Cold Spring Harbor Laboratory Press,Cold SpringHarbor,N.Y.;DNA Cloning:A Practical Approach,第I和II卷(D.N.Glover编辑1985);Oligonucleotide Synthesis(M.J.Gait编辑1984);Nucleic Acid Hybridization(B.D.Hames和S.J.Higgins编辑(1985));Transcription And Translation(B.D.Hames和S.J.Higgins,编辑(1984));Animal Cell Culture(R.I.Freshney,编辑(1986));Immobilized Cells and Enzymes(IRL Press,(1986));B.Perbal,A Practical Guide ToMolecular Cloning(1984);F.M.Ausubel等人(编辑),Current Protocols in MolecularBiology,John Wiley&Sons,Inc.(1994)。
在一些实施方案中,使用重组方法生产表达如本文所述的细胞产物的剪切敏感性细胞。基因,如编码多肽(如本文所述的抗体剂)的基因的重组表达可包括构建含有编码所述多肽的多核苷酸的表达载体。一旦已经获得多核苷酸,用于产生多肽的载体就可使用本领域已知的技术通过重组DNA技术来产生。已知的方法可用于构建含有多肽编码序列和适当的转录和翻译控制信号的表达载体。这些方法包括,例如,体外重组DNA技术、合成技术和体内遗传重组。
可通过常规技术将表达载体转移至剪切敏感性细胞,然后可通过如本文所述的方法培养转染的细胞以产生细胞产物(例如,蛋白制剂,例如重组蛋白,例如糖蛋白,例如融合蛋白,例如抗体剂)。
本公开提供了用于在足以表达细胞产物的培养基中连续细胞培养(例如,剪切敏感性细胞,例如,包含剪切敏感性细胞的细胞群体,例如,由剪切敏感性细胞组成的细胞群体的连续细胞培养)的方法、工艺和系统。细胞培养基通常包含适当的能量源和调控细胞周期的化合物。一般来说,培养基包括例如本领域技术人员已知的氨基酸、维生素、无机盐和葡萄糖。在一些实施方案中,细胞培养基具有6至8的pH。用于动物细胞培养的培养基在本领域中是完善建立的,并且针对特定目的和/或细胞类型由熟练的技术人员进行常规优化。
在一些实施方案中,细胞培养基还包含在1ppm至约500ppm范围内的消泡剂(例如,消泡剂C)。在一些实施方案中,在包含剪切力保护剂(例如,Pluronic F-68)的细胞培养基中培养剪切敏感性细胞。在一些实施方案中,在包含Pluronic F-68的细胞培养基中以1g/L至15g/L范围内的浓度培养剪切敏感性细胞。在一些某些实施方案中,可在包含血清(例如,胎牛血清)的细胞培养基中培养剪切敏感性细胞群体。
在一些实例中,使用本公开的方法、工艺和/或系统连续培养剪切敏感性细胞或由剪切敏感性细胞组成的细胞群体以表达细胞产物。在一些实施方案中,细胞产物是或包括核酸、脂质、肽和/或蛋白质。
在一些实施方案中,细胞产物是重组蛋白。在一些实施方案中,本公开的剪切敏感性细胞包括编码重组蛋白的核酸。在一些实施方案中,细胞产物是糖蛋白。在一些实施方案中,重组蛋白是融合蛋白。在一些实施方案中,本公开的剪切敏感性细胞包括编码融合蛋白的核酸。在一些实施方案中,重组蛋白是Fc融合蛋白。在一些实施方案中,本公开的剪切敏感性细胞包括编码Fc融合蛋白的核酸。
在一些实施方案中,细胞产物是抗体剂。在一些实施方案中,本公开的剪切敏感性细胞包括编码抗体剂的核酸。在一些实施方案中,细胞产物是单克隆抗体。
在一些实施方案中,本公开的剪切敏感性细胞包括编码糖蛋白缀合物(例如,缀合或融合至一个或多个异源部分的Fc区或其含有一个或多个N-糖基化位点的Fc片段)的核酸。异源部分包括但不限于,肽、多肽、蛋白质、融合蛋白、核酸分子、小分子、模拟剂、合成药物、无机分子以及有机分子。在一些实例中,糖蛋白缀合物是融合蛋白,所述融合蛋白包括肽、多肽、蛋白质支架、scFv、dsFv、双抗体、Tandab或融合至Fc区(如糖基化Fc区)的抗体模拟物。融合蛋白可包括将Fc区连接至异源部分的接头区(参见例如,Hallewell等人(1989),J.Biol.Chem.264,5260-5268;Alfthan等人(1995),Protein Eng.8,725-731;Robinson和Sauer(1996)。)
在一些实施方案中,本公开的剪切敏感性细胞包含编码蛋白质的核酸,所述蛋白质已例如在二次批准流程中被批准用于人或动物中的治疗或诊断用途。
在一些实施方案中,本公开的剪切敏感性细胞包含编码蛋白质的核酸,所述蛋白质与已例如在二次批准流程中被批准用于人或动物中的治疗或诊断用途的蛋白质具有相同的一级氨基酸序列。在一些实施方案中,本公开的剪切敏感性细胞包含编码蛋白质的核酸,所述蛋白质与经批准的治疗性或诊断性蛋白质相差不超过1、2、3、4、5、10、15、20、25或30个残基。在一些实施方案中,本公开的剪切敏感性细胞包含编码蛋白质的核酸,所述蛋白质与经批准的治疗性或诊断性蛋白质的序列具有至少90%、95%、98%、99%或100%序列同一性。术语“相同的一级氨基酸序列”、“相差不超过1、2、3、4、5、10、15、20、25或30个残基的一级氨基酸序列”、“具有至少98%或更高序列同一性的序列”或类似术语涉及一级氨基酸序列之间的同一性水平。在一些实施方案中,蛋白质制剂或产物包含氨基酸变体,例如在末端残基,例如在一个或两个末端残基上不同的种类。在此类情况的一些实施方案中,所比较的序列同一性是所比较的每种产物中最丰富(例如,活性最丰富)种类的一级氨基酸序列之间的同一性。在一些实施方案中,序列同一性是指由可用于制备产物的核酸编码的氨基酸序列。
在一些实施方案中,本公开的剪切敏感性细胞包括编码尚未被批准用于人或动物中的治疗或诊断用途的蛋白质的核酸。
非限制性的示例性重组蛋白可包括阿巴西普(
在一些某些实施方案中,细胞产物是优特克单抗。在一些实施方案中,剪切敏感性细胞包含编码优特克单抗的核酸。
在一些实施方案中,剪切敏感性细胞包含编码抗体剂的核酸,所述抗体剂包含如SEQ ID NO.:1中列出的重链可变结构域和如SEQ ID NO.:2中列出的轻链可变结构域。在一些实施方案中,剪切敏感性细胞包含编码抗体剂的核酸,所述抗体剂包含重链,所述重链包含SEQ ID NO.:1的序列;和轻链,所述轻链包含SEQ ID NO.:2的序列。在一些实施方案中,剪切敏感性细胞包含编码抗体剂的核酸,所述抗体剂包含如SEQ ID NO.:1中列出的HCDR1、HCDR2和HCDR3序列以及如SEQ ID NO.:2中列出的LCDR1、LCDR2和LCDR3序列。
SEQ ID NO.:1–优特克单抗重链序列(粗体表示可变结构域序列,其中CDR序列加下划线)
SEQ ID NO.:2–优特克单抗轻链序列(粗体表示可变结构域序列,其中CDR序列加下划线)
可将使用本文所述的任何方法、系统和/或工艺生产或制造的细胞产物(例如重组蛋白,例如糖蛋白,例如抗体剂)掺入药物组合物中。这样的药物组合物可用于预防和/或治疗疾病。可通过本领域技术人员已知的方法配制包含重组蛋白(例如糖蛋白,例如抗体剂)的药物组合物(参见例如,Remington’s Pharmaceutical Sciences,第20版,LippincottWilliams&Wilkins,2000)。所述药物组合物可以可注射制剂的形式肠胃外施用,所述可注射制剂包含在水中或在另一种药学上可接受的液体中的无菌溶液或悬浮液。例如,所述药物组合物可通过适当地将细胞产物(例如重组蛋白,例如糖蛋白,例如抗体剂)与药学上可接受的媒介物或介质(如无菌水和生理盐水、植物油、乳化剂、悬浮剂、表面活性剂、稳定剂、调味赋形剂、稀释剂、媒介物、防腐剂、粘合剂)组合,随后以通常可接受的药物实践所需的单位剂量形式混合而进行配制。包含在药物制品中的活性成分的量是使得提供在指定范围内的合适的剂量。
施用途径可以是肠胃外,例如通过注射施用、经鼻施用、经肺施用或经皮施用。施用可以是通过静脉内注射、肌内注射、腹膜内注射、皮下注射的全身性或局部施用。
合适的施用方式可基于患者的年龄和疾患来选择。含有细胞产物(例如重组蛋白,例如糖蛋白,例如抗体剂)的药物组合物的单剂量可选自0.001mg/kg体重至1000mg/kg体重的范围。在一些实施方案中,剂量可在0.001mg至100,000mg的范围内选择,但是本公开不限于此类范围。施用的剂量和方法根据有需要的患者的体重、年龄、疾患等而变化,并且可适当地由本领域技术人员按需选择。
通过以下实施例进一步说明本公开。仅出于说明性目的提供实施例。所述实施例不应解释为以任何方式限制本公开的范围或内容。
此实施例描述了鉴定剪切敏感性细胞的连续培养的规模扩大问题。特别地,本实施例描述了以下发现:在不控制气体出口速度的情况下剪切敏感性细胞的大规模(例如,200L)灌注培养具有受损的细胞活力和对于生物制造而言不足的活细胞浓度。具体而言,本实施例描述了示例性剪切敏感性细胞系SP2/0的灌注培养方法的规模扩大,所述细胞系已被工程化为包含编码示例性细胞产物(例如抗体剂,例如单克隆抗体)的核酸。
用小规模连续培养系统(例如,至多100L)评估了表达示例性抗体剂的示例性剪切敏感性细胞(例如,SP2/0)的连续细胞培养(例如,灌注细胞培养)的常规条件,结果描绘在图2中。具体而言,在3L玻璃反应器、5L玻璃反应器、15L玻璃反应器和100L SUB100一次性反应器系统中生长的剪切敏感性细胞表现出可比的细胞生长和稳态活细胞浓度。以3L、5L、15L和100L培养的剪切敏感性细胞也具有可比的生产率和产品质量(数据未示出)。
尝试将示例性剪切敏感性细胞SP2/0的连续细胞培养(例如,灌注细胞培养)的规模扩大至200L,并且结果描绘在图3中。具体而言,采用了以下示例性搅拌槽生物反应器系统:
尽管在所有样品中都观察到了初始生长,然而,如图3中所描绘,从第4天开始,利用GE/Xcellerex XDR200一次性反应器系统的200L培养工艺表现出剪切敏感性细胞的细胞生长受损(活细胞浓度(以10
本实施例鉴定了在实施例1中描述的大规模(例如,200L或更大)下剪切敏感性细胞SP2/0细胞的细胞生长和活力受损的原因,并且提供了大规模连续细胞培养(例如,灌注细胞培养)的方法,所述方法生产高密度的剪切敏感性细胞(例如,具有例如至少20x10
为了了解剪切敏感性细胞的细胞生长和活力在200L连续培养系统中受损的原因,因此对各种参数进行了分析。审查了方案和条件,以确保原料(例如,培养基、培养基制备过滤器、消泡剂、接种物等)不存在问题。诸如溶解氧(DO)、pH和温度的参数在小规模培养与大规模培养之间是一致的(数据未示出)。
在>20m/s速率下的气体出口速度(GEV)被鉴定为生长和活力受损的潜在促成因素。为了评估这种假设,在培养8天后,将一部分培养液(具体而言,2L的细胞培养液)从200L生物反应器(XDR200生物反应器)转移至具有3m/s的最大GEV的台式3L生物反应器中。监测剩余200L培养系统和3L台式生物反应器的活细胞浓度。如图4所示,在3L台式生物反应器中,活细胞浓度迅速恢复。同时,从培养的第9天至第13天,随后将200L生物反应器中的喷射器气体出口速度控制(降低)到至多或等于10m/s的速率。在此期间,活细胞浓度恢复。此外,当然后在第13天使GEV增加到至少20m/s的水平时,活细胞浓度迅速下降。这些结果表明,GEV控制在至多或等于10m/s的水平可促进细胞活力以成功扩大规模(例如,达到中试规模)。
用各种气体出口速度(GEV)进行具有3L灌注生物反应器的连续细胞培养运行,以确定GEV阈值,其描绘于图5中。具体而言,GEV从10m/s增加至16m/s导致活细胞浓度迅速降低。同样,将GEV维持在13m/s也导致培养12天后活细胞浓度最终暴跌。同时,将GEV从16m/s降低至10m/s使活细胞浓度增加。
因此,本实施例证明,通过将喷射器气体出口速度控制在20m/s以下(例如,在10m/s以下),可将剪切敏感性细胞的连续培养成功地扩大至大规模培养(例如,200L或更大,例如250L或更大),并且生产高密度的剪切敏感性细胞(例如,稳态浓度为例如至少20x10
还评估了溶解CO2对剪切敏感性细胞的细胞培养活力的影响,并且结果示于图6中。具体而言,发现示例性剪切敏感性细胞(SP2/0细胞)对溶解二氧化碳(pCO2)敏感。当pCO
此实施例证明,通过控制气体出口速度(例如,在10m/s以下),可恢复大规模连续培养物的剪切敏感性细胞的细胞生长和活力。此外,此实施例还表明,控制pCO
本实施例利用对实施例1和2的理解描述了剪切敏感性细胞的成功大规模连续培养。具体而言,250L灌注反应器(SUB250)的连续细胞培养运行在GEV和pCO
图9示出在3L、100L和250L下剪切敏感性细胞的这些连续培养物都显示出可比较的总聚糖水平(上图)和可比较的唾液酸含量(下图)。因此,本实施例证明通过灌注培养工艺成功地将高细胞密度剪切敏感性细胞(SP2/0)规模扩大至250L规模(例如,使用ThermoFisher/HyClone SUB250(250L)搅拌槽生物反应器)(图7A、图7B和图9)。
因此,本实施例还证明,控制pCO
因此,本实施例支持将来自喷射器的GEV控制在<10m/s的速率下,同时保持pCO
此实施例描述了对用于生产规模(例如,1000L或更大)下剪切敏感性细胞的大规模连续培养的不同参数进行建模。如图10所示,剪切敏感性细胞的1000L连续培养物的溶解CO
应理解,虽然本公开已结合其具体实施方式进行了描述,但前述描述意图说明且并非限制本发明的范围,本发明的范围由所附权利要求书来限定。其它方面、优点和修改在以下权利要求书的范围内。
序列表
<110> 动量制药公司(Momenta Pharmaceuticals, Inc.)
<120> 连续细胞培养方法
<130> 2010403-0533(M0161PCT)
<150> 62/727,976
<151> 2018-09-06
<160> 2
<170> SIPOSequenceListing 1.0
<210> 1
<211> 449
<212> PRT
<213> 智人(Homo sapiens)
<400> 1
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Lys Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Thr Thr Tyr
20 25 30
Trp Leu Gly Trp Val Arg Gln Met Pro Gly Lys Gly Leu Asp Trp Ile
35 40 45
Gly Ile Met Ser Pro Val Asp Ser Asp Ile Arg Tyr Ser Pro Ser Phe
50 55 60
Gln Gly Gln Val Thr Met Ser Val Asp Lys Ser Ile Thr Thr Ala Tyr
65 70 75 80
Leu Gln Trp Asn Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Arg Arg Pro Gly Gln Gly Tyr Phe Asp Phe Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ser Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr
355 360 365
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
Lys
<210> 2
<211> 214
<212> PRT
<213> 智人(Homo sapiens)
<400> 2
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Glu Lys Ala Pro Lys Ser Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Asn Ile Tyr Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
- 用于细胞连续三维培养的全自动化系统及其细胞培养方法
- 用于细胞连续三维培养的全自动化系统及其细胞培养方法
