一种生物活性可降解涂层多孔引导骨再生膜及其应用
文献发布时间:2024-05-24 17:48:49
技术领域
本发明属于口腔医疗器械技术领域,具体涉及一种生物活性可降解涂层多孔引导骨再生膜及其应用。
背景技术
牙列缺损和牙列缺失是口腔科诊疗中的常见病及多发病,第四次全国口腔流行病学调查数据显示,35-44岁年龄组缺失牙患者占比32.3%,而在65-74岁人群中该比例高达81.7%。自骨结合理论提出以来,口腔种植技术得到了突飞猛进的发展,种植义齿凭借其优良的美学效果、咀嚼效能和舒适度,已逐渐成为医生和患者的首选治疗方案。
近年来牙周疾病的患病率持续升高,由于牙槽骨骨量不足而无法进行种植手术的患者不在少数,因此对于牙槽骨重度吸收的患者,需要首先重建牙槽骨缺损区域,才能获得良好的种植修复效果。针对牙槽骨骨量不足的情况,通过引导骨再生技术(guided boneregeneration,GBR)以实现骨增量是切实可行的解决办法。
引导骨再生技术主要依据各类组织细胞迁移速度不同的特点,将一层屏障膜覆盖于骨缺损区域,阻挡快速增殖的上皮和结缔组织,为骨修复提供足够的时间和空间。引导骨再生技术常用于重建牙槽骨和治疗种植体周围骨缺损,其中GBR膜是决定临床效果的关键因素之一。随着口腔材料学和加工技术的不断发展,研发性能更加优异的GBR膜已成为目前的研究热点。
理想的GBR膜应具备较高的生物相容性、良好的骨诱导性、一定的抗菌能力、足够的支撑能力和屏障阻隔功能。根据膜在体内是否吸收,目前临床上用于GBR的膜性材料可以分为两类:不可吸收性膜和可吸收性膜。不可吸收性膜有钛网膜、微孔滤膜、聚四氟乙烯膜和加强型聚四氟乙烯膜等,是当前骨组织修复中最常用的材料。该类膜具备较高的机械稳定性和可塑性,能够有效维持骨缺损重建所需的空间和形状,但是其缺点是不具有骨诱导性,且需要二次手术取出,增加了患者的痛苦和细菌感染的风险。可吸收性膜主要有聚乳酸膜、聚乙烯酯膜、共聚物膜以及胶原膜等。该类膜的优点是具有较高的生物相容性,不需要二次手术取出,可以减少术后感染的风险,但是其降解速度与骨再生周期不匹配,强度较差,难以为骨组织再生提供持久稳定的空间。
考虑到GBR膜上下两面分别对应着软组织和骨缺损区,且二者的生长特点各不相同,因此研发出具有屏障作用、支撑强度、抗菌能力并可以分别满足软硬组织不同再生需求的引导骨再生膜具有重要意义。锌作为人体中第二丰富的微量金属,具有以下优点:强度高,可以为骨缺损重建提供稳定的空间;生物相容性好,对人体无毒无害;可以完全降解吸收,且释放的锌离子具有优异的骨诱导性、抗菌性能和调控免疫细胞的作用,这些优点使锌成为目前最为理想的引导骨组织再生的基体材料。研究显示铜离子具有优良的抗菌效果和促进血管生成的能力,以及相对令人满意的生物相容性,可以辅助软组织修复,并在一定程度上减少术后细菌感染的风险。钙离子作为细胞内的第二信使,也是骨组织的主要成分,具有促进骨再生的作用,通过调控骨修复阶段中各种细胞的增殖分化、促进新血管的生成和生长因子的释放来加速骨愈合。
因此,针对软组织和骨缺损区的不同再生需求,综合利用锌、铜、钙各自的突出优势,研发同时具有支撑屏障功能、体内降解性能和诱导软硬组织再生特性的GBR膜具有重要意义。
发明内容
为解决上述技术问题,本发明的技术方案如下:
一种引导骨再生膜,所述引导骨再生膜包括:基体,软组织面和/或骨组织面;所述软组织面和/或骨组织面位于所述基体的表面。
根据本发明的实施方案,所述基体选自含有锌、镁、铁等中至少一种或两种或三种的金属,例如为纯锌、纯镁或纯铁。
根据本发明的实施方案,所述软组织面至少含有铜和/或银。
根据本发明的实施方案,所述骨组织面至少含有钙和/或锶。
根据本发明的实施方案,所述引导骨再生膜包括:基体、软组织面和骨组织面;所述软组织面和骨组织面分别位于所述基体的两个表面。
根据本发明的实施方案,所述引导骨再生膜的厚度为0.03~0.60mm,例如为0.02mm、0.03mm、0.04mm、0.05mm、0.06mm、0.07mm、0.08mm、0.09mm、0.10mm、0.20mm、0.30mm、0.40mm、0.50mm、0.60mm。
根据本发明的实施方案,所述引导骨再生膜中,所述基体的厚度为0.02~0.50mm,例如为0.02mm、0.03mm、0.04mm、0.05mm、0.06mm、0.07mm、0.08mm、0.09mm、0.10mm、0.20mm、0.30mm、0.40mm、0.50mm。
根据本发明的实施方案,所述引导骨再生膜中,所述软组织面的厚度为0.003~0.06mm,例如为0.003mm、0.004mm、0.005mm、0.006mm、0.007mm、0.008mm、0.009mm、0.01mm、0.02mm、0.03mm、0.04mm、0.05mm、0.06mm。
根据本发明的实施方案,所述引导骨再生膜中,所述骨组织面的厚度为0.003~0.06mm,例如为0.003mm、0.004mm、0.005mm、0.006mm、0.007mm、0.008mm、0.009mm、0.01mm、0.02mm、0.03mm、0.04mm、0.05mm、0.06mm。
根据本发明的实施方案,所述引导骨再生膜、软组织面和骨组织面的厚度比为0.03~0.60:0.003~0.06:0.003~0.06,例如为0.1:0.05:0.05、0.3:0.05:0.05、0.5:0.05:0.05、0.1:0.01:0.01、0.1:0.01:0.01。
根据本发明的实施方案,所述软组织面选自含有铜和/或银的涂层,其中铜和/或银的质量含量为0.001%~2%,例如为0.001%、0.002%、0.003%、0.004%、0.005%、0.006%、0.007%、0.008%、0.009%、0.01%、0.02%、0.03%、0.04%、0.05%、0.06%、0.07%、0.08%、0.09%、0.1%、0.2%、0.3%、0.4%、0.5%、0.6%、0.7%、0.8%、0.9%、1%、1.1%、1.2%、1.3%、1.4%、1.5%、1.6%、1.7%、1.8%、1.9%、2%。
优选地,所述含有铜和/或银的涂层选自锌铜合金、锌银合金、镁铜合金、镁银合金、铁铜合金、铁银合金中的至少一种。
根据本发明的实施方案,所述骨组织面选自含有钙和/或锶的涂层,其中钙和/或锶的质量含量为0.01%~3%,例如为0.01%、0.02%、0.03%、0.04%、0.05%、0.06%、0.07%、0.08%、0.09%、0.1%、0.2%、0.5%、0.8%、1%、1.5%、2%、2.5%、3%。
优选地,所述含有钙和/或锶的涂层选自锌钙合金、锌锶合金、镁钙合金、镁锶合金、铁钙合金、铁锶合金中的至少一种。
根据本发明的实施方案,所述软组织面中铜和/或银与骨组织面中钙和/或锶的含量比为0.001~2:0.01~3,例如为0.01:0.1、0.01:1、0.01:2、0.1:0.01、0.1:1、0.1:2。
根据本发明的实施方案,所述引导骨再生膜上还设置有通孔,所述通孔为至少1个及1个以上。
根据本发明的实施方案,所述通孔的形状可选用本领域已知的形状,例如为圆形、方形、三角形、梯形等。
根据本发明的实施方案,所述通孔的孔径为0.1~1mm,优选为0.2~0.7mm,例如为0.1mm、0.2mm、0.3mm、0.4mm、0.5mm、0.6mm、0.7mm、0.8mm、0.9mm、1mm。需要说明的是,本发明中所述通孔的孔径是指圆形的直径、或者是长方形的长边的边长、或者是菱形的长的对角线的长度、或者是三角形的长的高线的长度、或者是梯形的长的高线的长度。
根据本发明的实施方案,相邻的两个通孔之间的间距为0.1~2mm,优选为0.8~1.6mm,例如为0.1mm、0.2mm、0.3mm、0.4mm、0.5mm、0.6mm、0.7mm、0.8mm、0.9mm、1mm、1.1mm、1.2mm、1.3mm、1.4mm、1.5mm、1.6mm、1.7mm、1.8mm、1.9mm、2mm。
根据本发明的实施方案,通孔的孔径与两个通孔之间的间距的比值为0.1~1:0.1~2,优选为0.2~0.7:0.8~1.6,例如为0.1:0.1、0.1:1.2、0.1:1.6、0.3:0.1、0.3:1.2、0.3:1.6、0.8:0.1、0.8:1.2、0.8:1.6。
根据本发明的实施方案,所述引导骨再生膜的膜厚与通孔的孔径的比值为0.03~0.60:0.1~1,优选为0.03~0.60:0.8~1.6,例如为0.3:0.8、0.3:1.2、0.3:1.6。
根据本发明的实施方案,通过调整通孔的孔径并调整相邻的两个通孔之间的间距使所述引导骨再生膜的降解周期与骨再生周期相匹配。需要说明的是,本发明中相邻的两个通孔之间的间距是指相邻的两个通孔的中心点之间的距离,如图2~4所示。
根据本发明的实施方案,所述引导骨再生膜上还设置有固定孔。
优选地,所述固定孔位于所述引导骨再生膜的边缘。优选地,所述固定孔可选用本领域已知的固定孔,只要能将所述引导骨再生膜固定即可,例如所述固定孔为小螺孔。示例性地,所述小螺孔位于所述引导骨再生膜的边缘,例如为四个。示例性地,所述小螺孔的直径为1~2mm,例如为1mm、1.5mm、2mm。
根据本发明的实施方案,所述软组织面和骨组织面通过电纺丝的方法或3D打印的方法设置在所述基体的表面,所述电纺丝的方法或3D打印的方法可选用本领域已知的条件,本发明中不做具体限定。
本发明还提供上述引导骨再生膜在生物医学中的应用。
根据本发明的实施方案,所述生物医学包括但不限于种植区骨缺损增量手术、牙周治疗和根分叉病变等。
本发明还提供上述引导骨再生膜在制备修复骨组织缺损制品中的应用。
根据本发明的实施方案,所述修复骨组织缺损制品包括引导骨再生膜。
根据本发明的实施方案,所述修复骨组织缺损制品可用于促进种植区牙槽骨修复、根分叉区牙槽骨修复、由于牙周炎引起的牙槽骨缺损的修复中的至少一种。
与现有技术相比,本发明具有以下有益效果:
本发明提供一种具有支撑、屏障、抗菌和诱导成骨能力的生物活性可降解涂层多孔引导骨再生膜,所述引导骨再生膜具有良好的机械强度,能够维持骨缺损区的空间;所述引导骨再生膜降解周期与骨再生周期相匹配,在体内自然降解无需二次手术取出;所述引导骨再生的多孔结构既满足骨缺损区物质交换的需求,又可有效阻挡软组织的早期长入,且具有良好的生物相容性。
本发明的引导骨再生膜具有优良的塑性形和机械性能,能够根据实际应用情况将其弯曲与裁剪成合适的形状与规格,维持骨再生所需空间;所述引导骨再生膜的多孔结构具有屏障作用,既可以阻碍早期软组织长入骨缺损区,又可以透过红细胞、营养物质等。
本发明的引导骨再生膜优选为其两个表面分别设计锌铜涂层作为软组织面和锌钙涂层作为骨组织面,其中,软组织面释放的铜离子具有抗菌性和促进血管生成的能力,可抵抗术后细菌感染,辅助软组织修复;骨组织面释放的钙离子具有诱导成骨的作用,可加速缺损区骨组织修复。本发明的引导骨再生膜的可分别满足软组织和骨组织的不同再生需求,而且具有抗菌和促进骨组织再生的能力。
附图说明
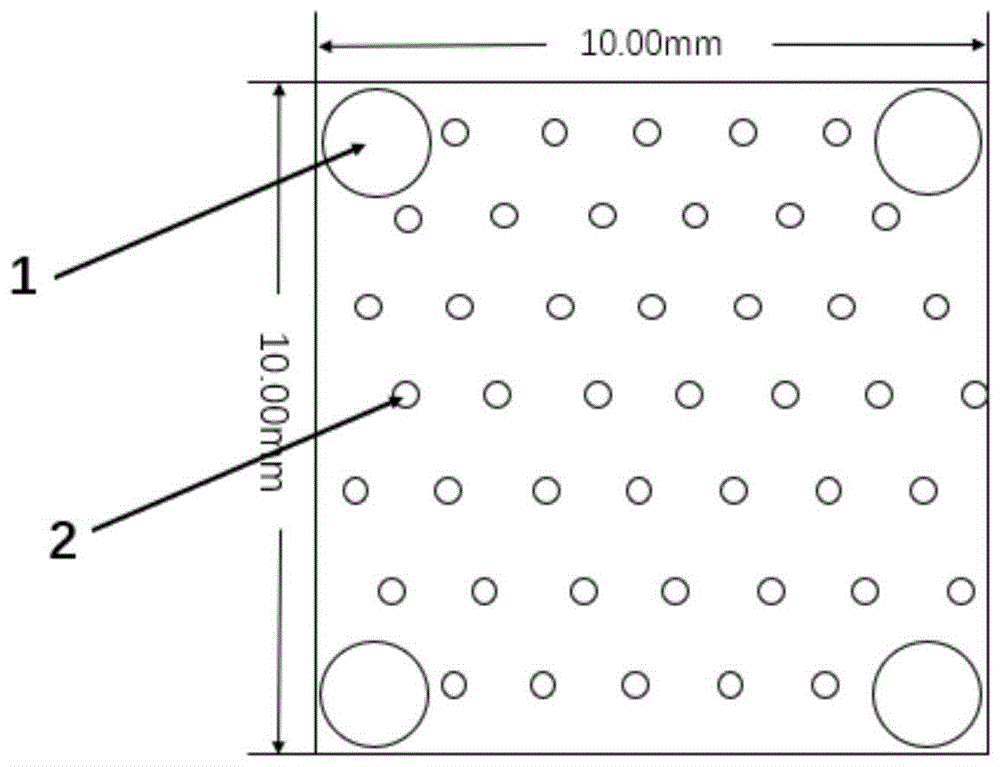
图1为本发明的引导骨再生膜的示意图;附图标记:1-小螺孔;2-通孔。
图2为通孔的直径为0.1mm的引导骨再生膜示意图。
图3为通孔的直径为0.3mm的引导骨再生膜示意图。
图4为通孔的直径为0.8mm的引导骨再生膜示意图。
图5为本发明的引导骨再生膜的剖面示意图。
图6为仅含骨组织面的引导骨再生膜的示意图。
图7为仅含软组织面的引导骨再生膜的示意图。
具体实施方式
下文将结合具体实施例对本发明的技术方案做更进一步的详细说明。应当理解,下列实施例仅为示例性地说明和解释本发明,而不应被解释为对本发明保护范围的限制。凡基于本发明上述内容所实现的技术均涵盖在本发明旨在保护的范围内。
除非另有说明,以下实施例中使用的原料和试剂均为市售商品,或者可以通过已知方法制备。
本发明的引导骨再生膜(以下简称GBR膜)的形状和规格如图1所示(单位mm)。所述引导骨再生膜包括:基体,软组织面和/或骨组织面;所述软组织面和/或骨组织面位于所述基体的表面。
根据本发明的具体实施方式,所述基体选自含有锌、镁、铁等中至少一种或两种或三种的金属,例如为纯锌、纯镁或纯铁。
根据本发明的具体实施方式,所述软组织面至少含有铜和/或银。
根据本发明的具体实施方式,所述骨组织面至少含有钙和/或锶。
根据本发明的具体实施方式,所述引导骨再生膜包括:基体、软组织面和骨组织面;所述软组织面和骨组织面分别位于所述基体的两个表面。
根据本发明的具体实施方式,所述GBR膜的厚度为0.03~0.60mm,例如为0.02mm、0.03mm、0.04mm、0.05mm、0.06mm、0.07mm、0.08mm、0.09mm、0.10mm、0.20mm、0.30mm、0.40mm、0.50mm、0.60mm。
根据本发明的具体实施方式,所述引导骨再生膜中,所述基体的厚度为0.02~0.50mm,例如为0.02mm、0.03mm、0.04mm、0.05mm、0.06mm、0.07mm、0.08mm、0.09mm、0.10mm、0.20mm、0.30mm、0.40mm、0.50mm。
根据本发明的具体实施方式,所述引导骨再生膜中,所述软组织面的厚度为0.003~0.06mm,例如为0.003mm、0.004mm、0.005mm、0.006mm、0.007mm、0.008mm、0.009mm、0.01mm、0.02mm、0.03mm、0.04mm、0.05mm、0.06mm。
根据本发明的具体实施方式,所述引导骨再生膜中,所述骨组织面的厚度为0.003~0.06mm,例如为0.003mm、0.004mm、0.005mm、0.006mm、0.007mm、0.008mm、0.009mm、0.01mm、0.02mm、0.03mm、0.04mm、0.05mm、0.06mm。
根据本发明的具体实施方式,所述软组织面选自含有铜和/或银的涂层。优选地,所述含有铜和/或银的涂层中,铜和/或银的质量含量为0.001%~2%,例如为0.001%、0.002%、0.003%、0.004%、0.005%、0.006%、0.007%、0.008%、0.009%、0.01%、0.02%、0.03%、0.04%、0.05%、0.06%、0.07%、0.08%、0.09%、0.1%、0.2%、0.3%、0.4%、0.5%、0.6%、0.7%、0.8%、0.9%、1%、1.1%、1.2%、1.3%、1.4%、1.5%、1.6%、1.7%、1.8%、1.9%、2%。
根据本发明的一个具体实施方式,所述含有铜和/或银的涂层选自锌铜合金、锌银合金、镁铜合金、镁银合金、铁铜合金、铁银合金中的至少一种。
根据本发明的具体实施方式,所述骨组织面选自含有钙和/或锶的涂层。优选地,所述含有钙和/或锶的涂层中,钙和/或锶的质量含量为0.01%~3%,例如为0.01%、0.02%、0.03%、0.04%、0.05%、0.06%、0.07%、0.08%、0.09%、0.1%、0.2%、0.5%、0.8%、1%、1.5%、2%、2.5%、3%。
根据本发明的一个具体实施方式,所述含有钙和/或锶的涂层选自锌钙合金、锌锶合金、镁钙合金、镁锶合金、铁钙合金、铁锶合金中的至少一种。
根据本发明的具体实施方式,所述GBR膜上还设置有通孔,所述通孔为至少1个及1个以上。
优选地,所述通孔均匀分布在所述GBR膜上。优选地,所述通孔的形状可选用本领域已知的形状,例如为圆形、方形、三角形、梯形等。
优选地,所述通孔的孔径为0.1~1mm,优选为0.2~0.7mm,例如为0.1mm、0.2mm、0.3mm、0.4mm、0.5mm、0.6mm、0.7mm、0.8mm、0.9mm、1mm。
优选地,相邻的两个通孔之间的间距为0.1~2mm,优选为0.8~1.6mm,例如为0.1mm、0.2mm、0.3mm、0.4mm、0.5mm、0.6mm、0.7mm、0.8mm、0.9mm、1mm、1.1mm、1.2mm、1.3mm、1.4mm、1.5mm、1.6mm、1.7mm、1.8mm、1.9mm、2mm。
根据本发明的具体实施方式,通过调整通孔的孔径并调整相邻的两个通孔之间的间距使所述引导骨再生膜的降解周期与骨再生周期相匹配。需要说明的是,本发明中相邻的两个通孔之间的间距是指相邻的两个通孔的中心点之间的距离,如图2~4所示。
根据本发明的具体实施方式,所述引导骨再生膜上还设置有固定孔。
优选地,所述固定孔位于所述引导骨再生膜的边缘。优选地,所述固定孔可选用本领域已知的固定孔,只要能将所述引导骨再生膜固定即可,例如所述固定孔为小螺孔。示例性地,所述小螺孔位于所述引导骨再生膜的边缘,例如为四个。示例性地,所述小螺孔的直径为1~2mm,例如为1mm、1.5mm、2mm。
根据本发明的具体实施方式,在实际操作中,可根据骨缺损的大小及骨的形状(例如为牙槽骨),对GBR膜进行裁剪和适当塑型,做到最佳适应和匹配。
根据本发明的一个具体实施方式,所述GBR膜包括基体、及分别位于基体两侧面的软组织面和骨组织面,如图5所示。优选地,所述骨组织面选自含有Ca和/或锶的涂层,其朝向植骨材料区从而促进成骨,软组织面选自含有Cu和/或银的涂层,其朝向软组织起到抗炎效果。
示例性地,所述GBR膜包括纯锌基体、及分别位于基体两侧面的软组织面和骨组织面,其中,所述GBR膜的厚度为0.3mm,骨组织面选自锌钙合金、镁锶合金或铁锶合金,其厚度为0.05mm;软组织面为锌铜合金、镁铜合金或铁铜合金,其厚度为0.05mm。
根据本发明的具体实施方式,所述软组织面和骨组织面通过电纺丝的方法或3D打印的方法设置在所述基体的表面。
实施例1
根据SD大鼠颅骨缺损模型的构建要求,通过3D打印技术制备得到GBR膜。
本实施例制备得到的GBR膜的尺寸为直径8mm大小的圆盘,膜的厚度为0.3mm,膜上设置有圆形通孔,通孔的直径为0.1mm,通孔均匀分布在GBR膜上,相邻的两个通孔之间的间距为1.2mm,GBR膜的两个表面分别为含Ca的涂层和含Cu的涂层,其中,含Ca的涂层为锌钙合金,其厚度为0.05mm,合金中Ca的质量含量为0.1%;含Cu的涂层为锌铜合金,其厚度为0.05mm,合金中铜的质量含量为0.01%;基体为纯锌,其厚度为0.2mm。
实施例2
本实施例与实施例1相同,不同之处在于,GBR膜上,通孔的直径为0.3mm。
实施例3
本实施例与实施例1相同,不同之处在于,GBR膜上,通孔的直径为0.8mm。
实施例1-1
本实施例与实施例1相同,不同之处在于,GBR膜的表面仅一面设置了含Ca的涂层,如图6所示。
实施例1-2
本对比例与实施例1相同,不同之处在于GBR膜的表面仅一面设置了含Cu的涂层,如图7所示。
实施例4
本实施例与实施例2相同,不同之处在于,任意相邻的两个通孔之间的间距为1.6mm。
实施例5
本实施例与实施例2相同,不同之处在于,任意相邻的两个通孔之间的间距为0.8mm。
对比例1
本对比例基本与实施例2相同,不同在于,GBR膜中,任意相邻的两个通孔之间的间距为3mm。
对比例2
本对比例基本与实施例2相同,不同在于,GBR膜中,任意相邻的两个通孔之间的间距为0.2mm。
实施例6
本实施例基本与实施例2相同,不同在于,GBR膜中,基体为纯镁,GBR膜的两个表面分别为含锶的涂层和含银的涂层,其中,含锶的涂层为镁锶合金,合金中,锶的质量含量为0.1%;含银的涂层为镁银合金,合金中银的质量含量为0.01%。
实施例7
本实施例基本与实施例2相同,不同在于,GBR膜中,基体为纯铁,GBR膜的两个表面分别为含锶的涂层和含银的涂层,其中,含锶的涂层为铁锶合金,合金中,锶的质量含量为0.1%;含银的涂层为铁银合金,合金中银的质量含量为0.01%。
对比例3
本对比例采用标准的钛网作为GBR膜。
应用例
将上述实施例和对比例中制备得到的GBR膜植入SD大鼠颅骨的骨缺损处。统计植入体内3个月后的降解情况、成骨效果及软组织的阻隔效果。
经过对比分析实验结果,可以得到:
(1)通过实施例1和实施例1-1、实施例1-2可知,双涂层的GBR膜修复骨缺损效果和抗菌能力明显优于单独的Ca涂层或者Cu涂层。
(2)通过实施例1-3和实施例1-1、实施例1-2可知,当通孔直径为0.8mm的GBR膜阻隔软组织长入的效果降低,而通孔直径为0.1mm的GBR膜较实施例2会阻隔部分血供,从而可能会影响了成骨效果。但是实施例1-3的双涂层的GBR膜修复骨缺损效果和抗菌能力仍明显优于单独的Ca涂层或者Cu涂层。
而采用钛网虽然也可以实现修复骨缺损,但是其抗菌作用不如实施例2,且钛网无法降解,会长期存留在体内。
(3)通过实施例1、实施例4、实施例5、对比例1和对比例2可知,当GBR膜上,通孔的间距为1.2mm时,其降解周期为6个月,骨组织生长周期为6个月,此时既可以完成骨再生,GBR膜又可自行降解;而当通孔的间距为3mm(即大于1.6mm)时,其降解周期为9个月,由于降解周期明显变长,可能会对机体产生影响;而当通孔的间距为0.2mm(即小于0.8mm)时,其降解周期为3个月,降解周期明显变短,由于其不能为骨再生提供足够的修复时间和空间,软组织可能会对其产生干扰。
由此可知,通过调整双涂层的GBR膜上的通孔的孔径为0.1mm-0.8mm、同时调整相邻的两个通孔之间的间距为0.1-2mm,可以使所述引导骨再生膜的降解周期与骨再生周期相匹配。
(4)通过实施例2、实施例6和7可知,基体为纯锌、纯镁或纯铁时,引导骨再生膜的降解周期与骨再生周期能基本匹配,具有较好的生物相容性。
以上对本发明示例性的实施方式进行了说明。但是,本申请的保护范围不拘囿于上述实施方式。本领域技术人员在本发明的精神和原则之内,所做的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
- 一种生物活性可降解镁合金引导骨再生膜及其密集孔的加工方法
- 一种生物活性可降解镁合金引导骨再生膜及其密集孔的加工方法
