一种海带发酵物、含其皮肤外用剂及其制备方法和应用
文献发布时间:2023-06-19 18:34:06
技术领域
本公开属于发酵技术领域,尤其涉及一种海带发酵物,含其皮肤外用剂及其制备方法和应用。
背景技术
随着时代的发展,人们崇尚绿色、环保、安全的化妆品,同时也对化妆品的功效寄予厚望。目前在满足化妆品相关法律法规的情况下,化妆品行业更多使用化学合成原料,虽然其具有成分结构明确、功效明确、质量控制方法成熟等优点,但人们在使用这些化妆品时逐渐发现化学合成品对人体带来的不良作用,如致敏、致红、刺激等。因此,降低化学合成物带来的不良反应成为化妆品发展的方向之一。
海带(Laminaria japonica),大型食用褐藻,多分布于北半球,是一种重要的海生资源;目前我国的海带养殖主要分布在浙江、福建等沿海地区。海带种植区域广泛,成本低廉,是我国普遍食用的经济藻类;海带中含有岩藻多糖、甘露糖、碘、膳食纤维、维生素和矿物质等多种功效成分,食药两用,营养丰富,但其在化妆品领域的应用确鲜有报道。现有技术中有采用有机溶剂(乙醇、氯仿、正丁醇等)提取海带中的活性成分的相关报道,这不仅会造成环境污染,提高生产成本,而且实验操作步骤繁琐,除杂困难,提取效率低,会造成海带的浪费,不利于产业化。采用有机溶剂对海带中的活性成分进行提取,存在一定的安全性问题,不利于用作化妆品原料。
因此,本领域亟需研发一种具有理想抗氧化和抗炎功效,原料来源广泛,价格低廉,制备工艺简单,且制备过程中不使用有机溶剂,有效活性成分提取率高的海带提取物。
发明内容
本公开所要解决的技术问题是克服现有技术从海带中提取活性成分的方法主要为有机溶剂浸提法,提取生产成本高,有效活性成分提取率低,造成资源的浪费和环境污染,采用有机溶剂也会对操作人员的身体和产品使用者造成一定伤害等缺陷,而提供一种海带发酵物,含其皮肤外用剂及其制备方法和应用。本公开的海带发酵物在制备过程中减少了资源浪费,对植物全成分进行提取,减少海带中活性成分的流失,发酵条件温和,不采用任何化学试剂,降低生产成本,减少环境污染,肌肤零负担,具有理想的抗氧化、抗炎和修复受损皮肤的功效,还具有理想的使用安全性,在化妆品领域具有很好的应用前景,扩宽了海带的应用领域。
本公开采用以下技术方案解决上述技术问题:
本公开提供一种海带发酵物的制备方法,其包括如下步骤,将发酵菌接种到发酵底物中,经有氧发酵24~96h,灭菌,即可;其中,所述发酵底物包括海带粉末和水;所述发酵菌为酿酒酵母菌(Saccharomyces cerevisiae)。
一些实施例中,所述酿酒酵母菌包括购自北京市食品酿造研究所的产品编号为21392的黄酒酵母菌”和/或“保藏于中国微生物菌种保藏管理委员会普通微生物中心,保藏编号为CGMCC NO.17452的酿酒酵母菌。其中,保藏编号为CGMCC NO.17452的酿酒酵母菌是已知菌株,已在中国发明专利 ZL2020103727403中公开,公开日为2020年8月11日。
一较佳实施例中,当所述酿酒酵母菌包括所述黄酒酵母菌21392和所述酿酒酵母菌CGMCC NO.17452的混合菌种时,所述黄酒酵母菌21392和所述酿酒酵母菌CGMCCNO.17452的接种量的比可为1:(0.5~2),较佳地为1:1。
一些实施例中,所述酿酒酵母菌可按照本领域常规以酿酒酵母菌菌液的形式添加,所述酿酒酵母菌菌液中所述酿酒酵母菌的浓度可为10
其中,所述酿酒酵母菌菌液的制备方法可为本领域常规,一般包括如下步骤:将酿酒酵母菌接种到YPD固体培养基中进行划线活化,于28℃培养箱中培养48h,获得单菌落;采用接种环挑取获得的单菌落于YPD液体培养基中,在温度为28℃,转速为180r/min的震荡培养箱中发酵培养。所述发酵培养的时间可为36~72h,较佳地为48h。
一些实施例中,以所述发酵底物的体积为基准,所述发酵菌的接种量可为 10
一些实施例中,所述海带粉末的粒径可为50~150目。所述海带粉末的制备方法可为本领域常规,一般可为海带经烘干、粉碎和筛分制得。
一些实施例中,所述发酵底物中,所述海带粉末和所述水的质量比可为1: (20~200),较佳地为1:(50~150),例如1:66.7。
一些实施例中,所述发酵底物在使用前还可进一步包括灭菌的操作。
其中,所述灭菌的条件和方法可为本领域该类操作常规的条件和方法,一般可为高温灭菌法。
当采用所述高温灭菌法对所述发酵底物进行所述灭菌时,所述灭菌的温度可为本领域该类操作常规的温度,较佳地为110~125℃,更佳地为115~121℃。
当采用所述高温灭菌法对所述发酵底物进行所述灭菌时,所述灭菌的时间可为本领域该类操作常规的时间,较佳地为15~35min,更佳地为20~35min,例如30min。
当采用所述高温灭菌法对所述发酵底物进行所述灭菌时,所述灭菌的压力可为本领域该类操作常规的压力,较佳地为0.1~0.14Mpa,更佳地为 0.1~0.13MPa,例如,0.12MPa。
其中,按照本领域常规,对所述发酵底物进行所述灭菌的操作后还可进一步包括冷却的操作,一般可为冷却至室温。
一些实施例中,所述有氧发酵的条件和方法可为本领域常规,一般可在摇床上进行,所述摇床的转速可为150~250rpm,较佳地为180rpm。
一些实施例中,所述有氧发酵的时间较佳地为48~96h,例如72h。
一些实施例中,所述有氧发酵的温度可为25~35℃,例如25~30℃。
一些实施例中,所述灭菌的条件和方法可为本领域常规,一般可为高温灭菌法。
当采用所述高温灭菌法进行所述灭菌时,所述灭菌的温度可为本领域该类操作常规的温度,较佳地为110~125℃,更佳地为115~121℃。
当采用所述高温灭菌法进行所述灭菌时,所述灭菌的时间可为本领域该类操作常规的时间,较佳地为15~35min,更佳地为25~35min,例如30min。
当采用所述高温灭菌法进行所述灭菌时,所述灭菌的压力可为本领域该类操作常规的压力,较佳地为0.1~0.14MPa,更佳地为0.1~0.13MPa,例如0.12MPa。
一些实施例中,所述灭菌的操作后,还可进一步包括冷却和/或离心,收集上清液的操作。
其中,按照本领域常规,所述冷却可为冷却至室温。
其中,所述离心的转速可为本领域该类操作常规的转速,较佳地为 3000~9000rpm,更佳地为4000~6000rpm,例如4800rpm。
其中,所述离心的半径可为本领域该类操作常规的半径,较佳地为8~15cm。
其中,所述离心的时间可为本领域该类操作常规的时间,较佳地为 10~40min,更佳地为20~40min,例如,30min。
其中,所述离心的操作后还可进一步包括二次灭菌和/或与防腐剂混合的操作。
所述二次灭菌的方法可为本领域常规使用的高温灭菌法。
当所述二次灭菌采用所述高温灭菌法时,所述二次灭菌的温度可为本领域该类操作常规的温度,较佳地为110~125℃,更佳地为115~121℃。
当所述二次灭菌采用所述高温灭菌法时,所述二次灭菌的时间可为本领域该类操作常规的时间,较佳地为15~35min,更佳地为30min。
当所述二次灭菌采用所述高温灭菌法时,所述二次灭菌的压力可为本领域该类操作常规的压力,较佳地为0.1~0.14MPa,更佳地为0.1~0.13MPa。
与所述防腐剂混合的过程中,所述混合的温度可为本领域该类操作常规的温度,较佳地为60~80℃,更佳地为70~80℃,例如75℃。
与所述防腐剂混合的过程中,所述防腐剂可按照本领域常规包括对羟基苯乙酮和/或1,2-己二醇。
当所述防腐剂包括所述对羟基苯乙酮和所述1,2-己二醇时,所述对羟基苯乙酮占所述离心后制得物料的质量百分数可为0.3%~2%,所述1,2-己二醇占所述离心后制得物料的质量百分数可为0.3%~2%;较佳地,当所述防腐剂包括所述对羟基苯乙酮和所述1,2-己二醇时,所述对羟基苯乙酮占所述离心后制得物料的质量百分数为0.5%,所述1,2-己二醇占所述离心后制得物料的质量百分数为0.8%。
本公开还提供一种海带发酵物,其由如上所述的海带发酵物的制备方法制得。
本公开还提供一种如上所述的海带发酵物直接作为产品、作为添加剂或作为基底在制备皮肤外用剂中的应用。
一些实施例中,所述海带发酵物可作为所述皮肤外用剂中的抗炎舒缓活性成分、修复活性成分和抗氧化活性成分中至少一种。
其中,所述抗炎舒缓活性成分可为抑制炎性因子IL-8产生的抗炎舒缓活性成分。
其中,所述抗氧化活性成分可为具有羟自由基清除能力和/或总抗氧化能力的抗氧化活性成分。
本公开还提供一种皮肤外用剂,其包括如上所述的海带发酵物。
一些实施例中,所述皮肤外用剂中还可进一步包括本领域常规使用的活性成分,一般可包括保湿活性成分、美白活性成分、抗炎活性成分、抗敏活性成分和抗氧化活性成分中的至少一种。
一些实施例中,所述皮肤外用剂可按照本领域常规包括但不限于面膜、精华或爽肤水。
一些实施例中,所述海带发酵物占所述皮肤外用剂的质量百分比可为 5%~99%,较佳地为60%~99%。
在符合本领域常识的基础上,上述各优选条件,可任意组合,即得本公开各较佳实例。
本公开所用试剂和原料均市售可得。
本公开的积极进步效果在于:本公开海带发酵物在制备过程中减少资源浪费,对植物全成分进行提取,减少海带中活性成分的流失,发酵条件温和,不采用任何化学试剂,降低生产成本,减少环境污染,具有理想的抗炎舒缓功效、修复功效和抗氧化功效,拓展海带在皮肤外用剂领域的研究进展。
附图说明
本公开可以通过参考下文中结合附图所给出的描述而得到更好的理解。所述附图连同下面的详细说明一起包含在本说明书中并且形成本说明书的一部分,而且用来进一步举例说明本公开的优选实施例和解释本公开的原理和优点。其中:
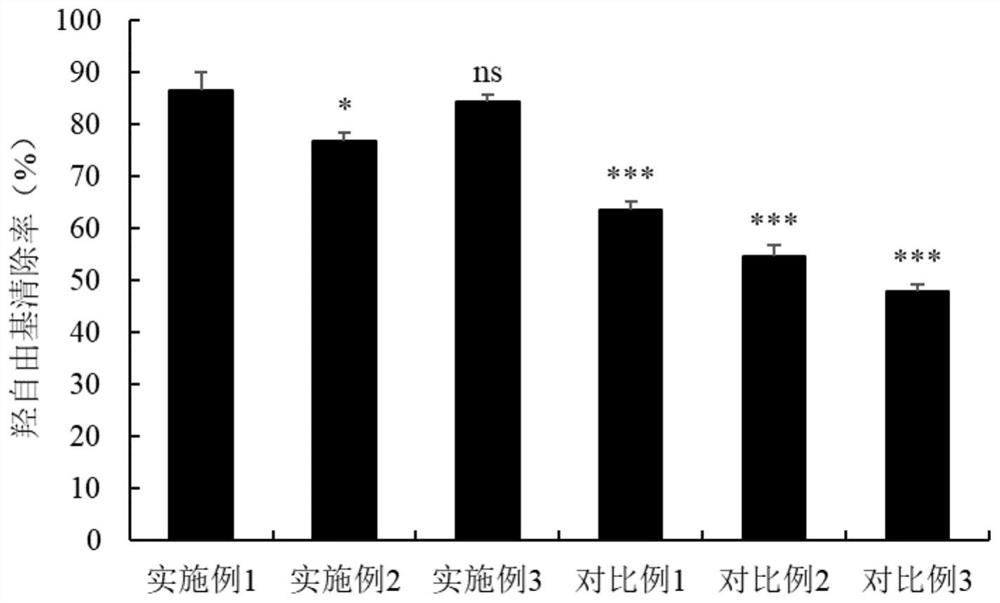
图1为实施例1~3和对比例1~3制得的海带发酵物对羟自由基清除能力对比图;
图2为实施例1~3和对比例1~3制得的海带发酵物总抗氧化能力对比图;
图3为实施例1~3和对比例1~3制得的海带发酵物对人体永生化表皮细胞毒性结果对比图;
图4为实施例1~3和对比例1~3制得的海带发酵物中总糖含量对比图;
图5为实施例1~3和对比例1~3制得的海带发酵物对HaCaT细胞保护功效对比图;
图6为实施例1~3和对比例1~3制得的海带发酵物对HaCaT细胞修护功效对比图。
具体实施方式
下面通过实施例的方式进一步说明本公开,但并不因此将本公开限制在所述的实施例范围之中。下列实施例中未注明具体条件的实验方法,按照常规方法和条件,或按照商品说明书选择。
下述实施例中所使用的实验方法如无特殊说明,均为常规方法。
下述实施例和对比例中,黄酒酵母菌购自北京市食品酿造研究所,产品编号为21392。
下述实施例和对比例中,酿酒酵母菌CGMCC No.17452保藏日期为2019年3 月27日,保藏编号为CGMCC No.17452,分类命名为:酿酒酵母(Saccharomyces cerevisiae)YWY-1,保藏单位名称为中国微生物菌种保藏管理委员会普通微生物中心(简称CGMCC),地址为:北京市朝阳区北辰西路1号院3号,邮编为100101;酿酒酵母菌CGMCC No.17452已在中国发明专利ZL2020103727403中公开,公开日为2020年8月11日。
下述对比例中,瑞士乳杆菌(Lactobacillus helveticus)为购自中国工业微生物菌种保藏管理中心,保藏编号为CICC 20243的瑞士乳杆菌。
实施例1
(1)将市售海带进行烘干,粉碎,过筛,制得目数为50~150目的海带粉末,称取海带粉末4.5g与300mL去离子水混合均匀,在温度为121℃,压力为 0.12MPa的高压灭菌锅中灭菌20min,灭菌后冷却至室温,得到发酵底物;
(2)将如上提及的黄酒酵母菌(北京市食品酿造研究生产,产品编号为 21392)接种到YPD固体培养基中进行划线活化,于28℃培养箱中培养48h,获得单菌落;采用接种环挑取获得的单菌落于YPD液体培养基中,在温度为 28℃,转速为180r/min的震荡培养箱中发酵培养48h,制得活菌数为10
在发酵底物中接种黄酒酵母菌菌液;其中,黄酒酵母菌的接种量为 10
实施例2
与实施例1相比,区别仅在于接种的菌种不同,将黄酒酵母菌21392替换为等量的酿酒酵母(CGMCC NO.17452),其他条件参数通实施例1。
实施例3
与实施例1相比,区别仅在于接种的菌种不同,将黄酒酵母菌21392替换为黄酒酵母菌21392和酿酒酵母(CGMCC NO.17452)的混合菌种,种菌的总添加量不变,两种菌的接种量的比为1:1。
对比例1
与实施例1相比,区别仅在于不进行发酵处理,为实施例1制得的发酵底物。
对比例2
与实施例1相比,区别仅在于发酵时间为4天,其他条件参数同实施例1。
对比例3
与实施例1相比,区别仅在于将发酵菌种替换为等量的黄酒酵母和瑞士乳杆菌(CICC 20243)的混合菌种,两种菌的接种量比例为1∶1;其中,将瑞士乳杆菌菌粉溶解在无菌水中制得瑞士乳杆菌菌液,瑞士乳杆菌菌液中瑞士乳杆菌的活菌数为10
效果实施例1
制备待测样品:本实验对实施例1~3和对比例1~3制得的产品进行冷冻干燥处理,制得冻干粉,将冻干粉与去离子水混合配置成8mg/mL的冻干粉溶液作为待测样品进行羟自由基清除率实验测试。
利用Fenton反应产生羟自由基(·OH),向反应体系中加入水杨酸,·OH 与水杨酸反应,生成的有色化合物2,3-二羟基苯甲酸在510nm处有特征吸收。采用固定反应时间法,在510nm处测定含被测物反应液的吸光度,并与空白液比较,测定被测样品对·OH的清除作用,按表1配方往试管中添加试剂,依次加入9mmol/L FeSO
羟自由基清除率计算公式为:
羟自由基清除率=(A
表1
表2
结果表明,本公开实施例1~3制得的海带发酵物的羟自由基清除能力显著或极显著高于对比例1~3制得的产品。
效果实施例2
将上述实施例1~3和对比例1~3制备的产品进行冷冻干燥处理得海带发酵物冻干粉;将上述冻干粉配置成浓度为20mg/mL溶液作为待测液。
采用碧云天生物技术有限公司生产的货号为S0119的总抗氧化能力检测试剂盒(ABTS法)测试上述实施例和对比例制得的待测液的总抗氧化能力,结果见表3和图2(图2中,***p<0.001,表示与实施例1相比有极其显著性统计学差异,极显著降低;**p<0.01,表示与实施例1相比有显著性差异,显著降低;*p<0.05,表示与实施例1相比有统计学差异,降低)。
表3
结果表明,本公开实施例1~3制得的海带发酵物的总抗氧化能力显著或极显著高于对比例1~3制得的产品。
效果实施例3:人体永生化表皮细胞毒性实验
本实验采用人体永生化表皮细胞,来自中国科学细胞库,检测上述实施例和对比例制得产品的细胞毒性。
试剂:0.25%(含EDTA)胰蛋白酶的生产厂家为美国GIBCO公司;DMEM 培养基的生产厂家为美国GIBCO公司;双抗的生产厂家为美国Corning公司; CCK-8的生产厂家为北京拜尔迪生物技术有限公司;胎牛血清的生产厂家为美国GIBCO公司;磷酸盐缓冲液的生产厂家为北京百瑞极生物科技有限公司。
设备:WJ-80A-Ⅱ型CO
1、实验步骤:
分别将上述实施例1~3和对比例1~3进行冷冻干燥处理,制得冻干粉,用无血清的DMEM培养基将冻干粉配置成浓度为4mg/mL的实验组待测液。人体永生化表皮细胞养于含10%胎牛血清以及1%双抗(1×10
细胞存活率(%)=(A实验组-A空白对照组)/(A对照组-A空白对照组) ×100%。
表4
结果表明,本公开实施例1~3制得的海带发酵物对人体永生化表皮细胞无毒性。
效果实施例4
将上述实施例1~3和对比例1~3制备的产品进行冷冻干燥处理得海带发酵物冻干粉。
采用索莱宝科技有限公司生产的货号为BC2715的总糖含量检测试剂盒测试实施例1~3和对比例1~3制得的产品制备成冻干粉中的总糖含量,结果见表 5和图4(图4中,***p<0.001,表示与实施例1相比有极其显著性统计学差异,极显著降低;ns,表示与实施例1相比无显著性差异)。
表5
结果表明,本公开实施例1~3制得的海带发酵物中总糖含量极显著高于对比例1~3制得的产品中总糖含量。
效果实施例5炎性因子IL-8的测定(保护细胞)
待测样品制备:将上述实施例1~3和对比例1~3制备的产品进行冷冻干燥处理得海带发酵物冻干粉;用无血清的DMEM培养基将冻干粉配置成浓度为 2mg/mL的实验组待测液。
取对数期HaCaT细胞,以25万个/mL的密度将细胞悬浮液接种于6孔细胞培养板上,每孔加入2mL细胞悬液,培养12h,吸弃上清。空白组加入DMEM 溶液2mL;实验组加入含有样品的待测液2mL处理细胞24h,模型组加入 DMEM溶液2mL处理细胞24h,处理结束后实验组和模型组均采用10mJ/cm
BCA试剂盒操作步骤:
1.样品前处理:根据使用量,按照RIPA∶PMSF为100∶1的比例配制裂解液,去培养液,用PBS清洗一边,按照6孔板每孔细胞量加入150~250μL 裂解液,用移液器吹打数下,使裂解液与细胞充分接触;
2.后处理:将裂解后的样品在10000rpm条件下离心10min,取上清,即可进行后续的蛋白浓度测定;
3.按照试剂(A)BCA溶液∶试剂(B)Cu
4.加入20μL待测蛋白样品于96孔板中;
5.各孔加入200μL配置好的BCA工作液,37℃放置20~30min。
6.于562nm下检测吸光度;
7.根据标准曲线与稀释倍数计算出样品的蛋白浓度。
ELISA试剂盒检测步骤:
1.试剂准备
1)试剂回温:首先在实验前30min将试剂盒回温,待测样本放置于室温下,浓缩洗涤液如出现结晶,放入37℃水浴直至结晶全部溶解。
2)配制洗涤液:预先计算好稀释后的洗涤液使用体积,然后用去离子水将 20倍浓缩洗涤液稀释成1倍应用液,未用完浓缩洗涤液放入4℃保存。
3)样品梯度稀释:加入标准品/样本稀释液(SR1)1mL至冻干标准品中,静置15分,待其完全溶解后轻轻混匀(浓度1000pg/mL)。然后在其余6管中各加入500μL标准品/样本稀释液(SR1),按照以下浓度进行2倍稀释:500、 250、125、62.5、31.25、15.62、0pg/mL进行稀释,1000pg/mL为标准曲线最高点浓度,标准品/样本稀释液(SR1)作为标准曲线零点。复溶过的标准品原液(浓度为1000pg/mL)未用完的需废弃或者根据需要按照一次用量分装,并将其储存在-80℃冰箱。
4)生物素化抗体工作液:预先计算好试验所需用量,用检测稀释液(SR2) 将100倍抗体浓缩液稀释成1倍应用工作液(稀释前充分混匀),在30分装内加入到反应孔中。
5)酶结合物工作液:按每次试验所需用量配制,用酶结合物稀释液(SR3) 将40倍浓缩酶结合物稀释成1倍应用工作液(稀释前离心),在30min内使用。
6)洗涤方法:甩尽酶标板孔中液体,在吸水纸上拍干,用洗瓶加入洗涤液 300μL/孔,静止30s后甩净酶标板孔中液体,在吸水纸上拍干。
2.检测步骤
1)实验前30min,拿出试剂盒,恢复至室温,加入标准品/样本前,洗板三次并甩干;
2)加入100μL标准品/样品至反应孔中,封板后于37℃孵育90min,拍板并洗板4次;
3)加入100μL生物素化抗体工作液至反应孔中,封板后于37℃孵育 60min,拍板并洗板4次;
4)加入100μL酶结合物工作液至反应孔中,封板后于37℃孵育30min,拍板并洗板5次;
5)加入50μL显色底物至反应孔中,封板后于37℃孵育箱避光显色15min;
6)加入50μL终止液,即刻用酶标仪450nm波长下测量OD值(5min内)。
表6
结果表明,本公开实施例1~3制得的海带发酵物处理HaCaT细胞后,再对处理后的细胞进行紫外线刺激,结果表明,可以阻碍细胞出现炎症反应,对细胞具有理想的保护作用;但对比例1~3制得的产品对HaCaT细胞没有保护作用,紫外线刺激后,细胞会出现明显的炎症反应。
效果实施例6炎性因子IL-8的测定(修复细胞)
待测样品制备:将上述实施例1~3和对比例1~3制备的产品进行冷冻干燥处理得海带发酵物冻干粉;用无血清的DMEM培养基将冻干粉配置成浓度为 0.5mg/mL的实验组待测液。
取对数期HaCaT细胞,以25万个/mL的密度将细胞悬浮液接种于6孔细胞培养板上,每孔加入2mL细胞悬液,培养12h,吸弃上清。空白组加入DMEM 溶液2mL;实验组和模型组采用10mJ/cm
表7
结果表明,本公开实施例1~3制得的海带发酵物对HaCaT细胞具有理想的修复作用,但对比例1~3制得的产品对HaCaT细胞的修复功效相对较差。
最后,还需要说明的是,在本公开中术语“包括”、“包含”或者其任何其他变体意在涵盖非排他性的包含,从而使得包括一系列要素的过程、方法、物品或者设备不仅包括那些要素,而且还包括没有明确列出的其他要素,或者是还包括为这种过程、方法、物品或者设备所固有的要素。
尽管上面已经通过本公开的具体实施例的描述对本公开进行了披露,但是,应该理解,本领域技术人员可在所附方案的精神和范围内设计对本公开的各种修改、改进或者等同物。这些修改、改进或者等同物也应当被认为包括在本公开所要求保护的范围内。
- 一种外用皮肤黏膜末梢神经麻醉剂及其制备方法
- 含氟氯吡啶肟酯结构的化合物及其制备方法和应用及一种除草剂
- 一种老面面包复合发酵剂及制备方法、应用和利用其制备的面包
- 一种含铜复合氧化物高低温脱硝催化剂及其制备方法
- 一种组合发酵物、含其皮肤外用剂及其制备方法和应用
- 一种组合发酵物、含其皮肤外用剂及其制备方法和应用
