一种高效液相色谱-质谱联用检测口服胰岛素药物中胰岛素包封率的方法
文献发布时间:2024-04-18 19:59:31
技术领域
本发明涉及一种高效液相色谱-质谱联用检测口服胰岛素药物中胰岛素包封率的方法,属于医药分析技术领域。
背景技术
糖尿病仍是全球医学上极其严重的问题之一,是由胰岛素分泌不足或功能障碍引起的。皮下注射和口服胰岛素是治疗糖尿病的两种主要方法,但是皮下给药会导致患者依从性差。目前口服胰岛素是一种有吸引力的非侵入性胰岛素输送途径,因为它可以防止患者依从性差。由于酶降解和肠道吸收不良严重降低了胰岛素的口服生物利用度。为了解决这一问题,已经开发了许多口服胰岛素聚合物递送系统,例如微球、聚合物胶束、水凝胶、脂质体和纳米颗粒。
脂质体适合口服胰岛素递送,脂质体不仅可以保护药物免受有害的胃环境的影响并促进肠道吸收,还可以提高药物稳定性。包封率是脂质体关键质量属性,可以反应出脂质体中药物的包封程度的高低,因此,研究脂质体的包封率对于口服胰岛素特定治疗蛋白的吸收和生物利用度具有重要意义。
目前,检测脂质体包封率的传统方法主要有分光光度法、液相色谱法等。虽然分光光度法操作简单、检测时间短,但是容易受环境影响,准确度和精准度较低,且对复杂实际样品检测能力差。液相色谱法具有分离效率高,应用范围广,不受试样的挥发性和热稳定性限制等优点,但是液相色谱法精确度较低,对样品检测的选择性要求高。因此,这些方法对于样品的定性和定量检测具有一定局限性。
质谱是一种测量气相离子质荷比的分析方法,主要由进样系统、离子源、质量分析器以及检测器组成。质谱具有样品用量少、通用性强、灵敏度及和准确度高等特点。近年来质谱技术被应用于各个领域,例如医学及临床实验、环境、能源以及生命科学等领域。液相色谱与质谱联用技术是一种强大的分析手段,它将液相色谱作为进样系统和分离系统,质谱作为检测系统。液相色谱-质谱联用可以用于定性和定量检测,具有液相色谱自动化程度高和分离能力强的优点,同时也具有质谱技术检测限低、灵敏度和准确度高的优点。
因此,采用液相色谱-质谱联用分析脂质体包封率十分具有意义,能够更加真实准确的检测口服胰岛素药物实际的包封情况,解决了传统方法准确度低,灵敏度差,预处理步骤复杂的问题,在医药分析领域也具有巨大的应用前景。
发明内容
发明目的:本发明的目的是提供一种高效液相色谱-质谱联用仪检测口服胰岛素包封率的方法。
技术方案:本发明所述一种高效液相色谱-质谱联用检测口服胰岛素药物中胰岛素包封率的方法,包括以下步骤:
(1)以德谷胰岛素为内标,配置内标储备液,并用胰岛素标准品配置胰岛素储备液;
(2)将内标储备液和胰岛素储备液混合,用甲酸水溶液稀释成标准工作溶液;
(3)将待检测口服胰岛素药物进行低温超滤离心,分离出上室脂质体溶液与下室游离胰岛素溶液,取上室脂质体溶液和下室游离胰岛素溶液,分别加入内标储备液,并分别用甲酸水溶液稀释成上室脂质体供试品溶液和下室游离胰岛素供试品溶液;
(4)将步骤(2)制备的标准工作溶液注入高效液相色谱-质谱联用仪进行检测,计算校正因子f;
(5)将步骤(3)得到上室脂质体供试品溶液和下室游离胰岛素试品溶液分别注入高效液相色谱-质谱联用仪进行检测,计算口服胰岛素药物样品中胰岛素含量和口服胰岛素包封率。
进一步地,步骤(1)中,所述内标储备液为使用50-60%甲醇溶液将德谷胰岛素配置成0.1-0.5mg/mL的溶液;所述胰岛素储备液为用0.1%甲酸水溶液将胰岛素标准品配置成1.0-5.0mg/mL的溶液。
进一步地,步骤(2)中,所述内标储备液和胰岛素储备液的体积比为1:-10:1,即标准工作溶液为1.0-25μL德谷胰岛素储备液与1.0-2.5μL胰岛素储备液混合,并用0.1%甲酸水溶液稀释至1000μL。
进一步地,步骤(3)中,所述低温超滤离心的温度为3-6℃,低温超滤离心的时间为10-15min,所述上室脂质体溶液与内标储备液的体积比为1-5:1,所述下室游离胰岛素溶液与内标储备液的体积比为1-5:1。
进一步地,步骤(4)和(5)中,所述高效液相色谱-质谱联用仪的色谱测定条件为:色谱柱为Phenomenex C18,规格为100mm×2.1 mm,色谱柱内径为1.6μm,流动相:以0.1%甲酸水溶液为流动相A,以0.1%甲酸乙腈溶液为流动相B。
更进一步地,高效液相色谱检测时采用梯度洗脱程序:0min→10min→13min→15min→20min,流动相相A的体积百分比:90%→10%→10%→90%→90%,流速0.3mL/min,柱温30℃,进样体积5μL。
进一步地,步骤(4)和(5)中,高效液相色谱-质谱联用仪的质谱测定条件为:采用电喷雾正离子模式,喷雾电压为3500V,鞘气为35Arb,辅助气为10Arb,反吹气为8Arb,离子传输毛细管温度300℃,气化温度350℃。
更进一步地,所述液相色谱-质谱联用仪的质谱检测中,胰岛素的主要离子为m/z968.79(z=+6),m/z 1162.34(z=+5),m/z 1452.67(z=+4),和m/z 1936.89(z=+3);德谷胰岛素的主要离子为m/z 1018.15(z=+6),m/z 1221.57(z=+5),和m/z 1526.72(z=+4)。
进一步地,步骤(4)中,进行检测的具体操作过程如下:将5μL标准工作溶液注入液相色谱-质谱联用仪中进行测定,根据液相色谱图中提取离子色谱峰峰面积数据计算标准品胰岛素与内标物德谷胰岛素的校正因子f。
进一步地,步骤(5)中,进行检测的具体操作过程如下:将5μL的上室脂质体供试品溶液或下室游离胰岛素试品溶液注入液相色谱-质谱联用仪中进行测定,根据上室脂质体供试品或下室游离胰岛素试品的色谱图的情况,以内标法计算上下室中胰岛素的含量。
进一步地,步骤(4)中,所述校正因子f按式(1)计算:
f=(As/Cs)/(Ar/Cr)(1),
其中,As、Ar分别为标准工作溶液中内标物德谷胰岛素、标准品胰岛素的液相色谱提取峰面积,Cs、Cr分别为标准工作溶液中内标物德谷胰岛素、标准品胰岛素的浓度。
进一步地,步骤(5)中,所述计算口服胰岛素药物样品中胰岛素含量(即上下室中胰岛素)按照式(2)计算:
Ci=f ×Ai ×(As/Cs)(2),
其中,Ai为上室脂质体供试品溶液或下室游离胰岛素试品溶液中待测物胰岛素的液相色谱提取峰面积,As为标准工作溶液中内标物德谷胰岛素的液相色谱提取峰面积,Ci为上室脂质体供试品溶液或下室游离胰岛素试品溶液中待测物胰岛素的浓度,Cs标准工作溶液中内标物德谷胰岛素的浓度。
进一步地,步骤(5)中,所述包封率按照式(3)计算:
包封率=上室脂质体供试品溶液中胰岛素浓度/胰岛素总浓度(3),
其中,胰岛素总浓度为上室中脂质体供试品溶液胰岛素浓度与下室游离胰岛素供试品溶液中胰岛素浓度的总和。
本发明采用低温超滤离心法对口服胰岛素药物预处理,预先分离脂质体和游离胰岛素,脂质体分布在上室,游离胰岛素分布在下室;采用德谷胰岛素作为胰岛素定量检测的内标物质,德谷胰岛素属于胰岛素类似物,与胰岛素性质相似,德谷胰岛素色谱峰的位置与胰岛素的色谱峰的位置相近,且又不共溢出;建立了高效液相色谱方法,对样品中脂质体组成成分和胰岛素进行了高效分离,以质谱作为检测器,实时检测液相色谱分离的各种物质和成分。
有益效果:与现有技术相比,本发明具有如下显著优点:
(1)本发明采用低温超滤离心预处理方法成本低,操作简单、快速,预处理过程仅需10-15min。
(2)本发明高效液相色谱分离效率高,对复杂样品中的各种成分有良好的分离效果,梯度洗脱可以使内标和胰岛素很好的分离,本发明液相色谱方法快速、高效。
(3)本发明以质谱作为检测器,准确检测复杂样品中的成分,样品不需要进行衍生化,且检测准确度高、灵敏度高。
(4)本发明液相色谱于与质谱联用技术自动化程度高,分离能力强,分析范围广,解决了分析热不稳定化合物的难题。
(5)本发明以德谷胰岛素作为内标法测定结果准确,实时校正仪器条件的波动;进样量、色谱条件以及环境因素的微小变化对内标法定量结果的影响不大。
(6)本发明采用液相色谱图中提取离子色谱峰的峰面积进行计算,通过峰面积积分可以切除干扰峰的影响,计算结果重复性好,灵敏度高。
附图说明
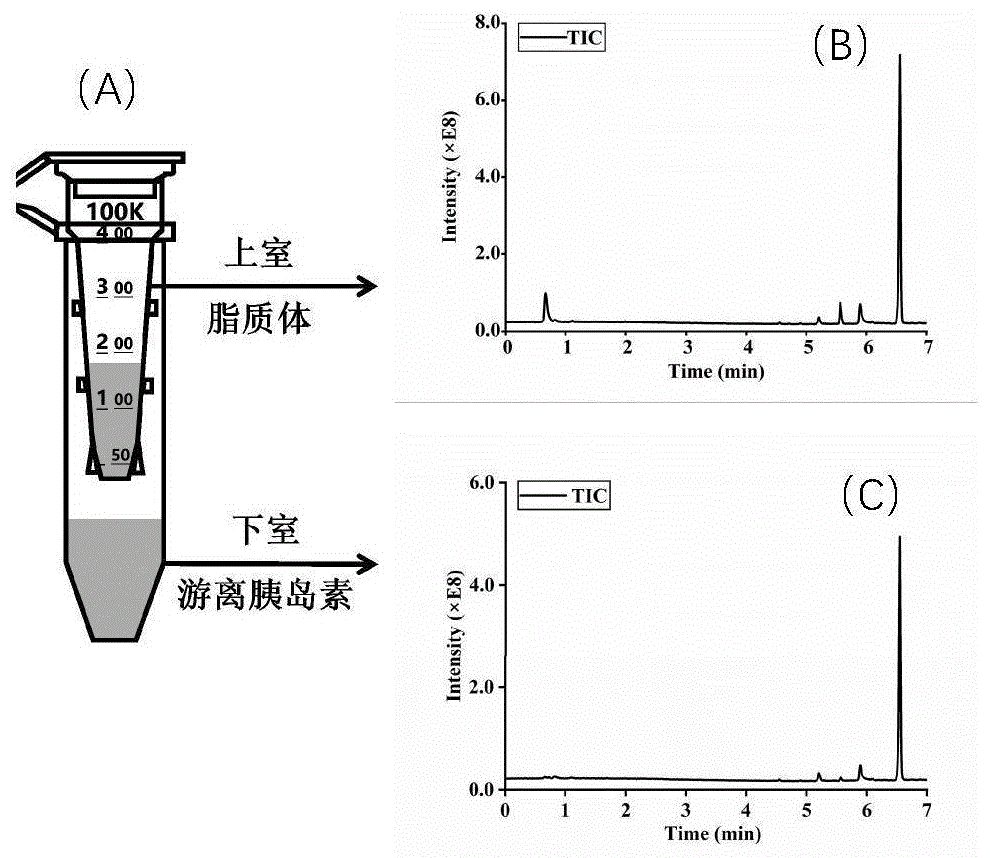
图1为口服胰岛素药物低温超滤离心示意图以及上室和下室的液相色谱总离子流图;
图2为标准品胰岛素与内标德谷胰岛素混合成的标准工作溶液的液相色谱总离子流图;
图3为标准品胰岛素和德谷胰岛素的质谱信号检测图;
图4为口服胰岛素药物低温超滤离心后,上室和下室的液相色谱总离子流图。
具体实施方式
下面结合附图对本发明的技术方案作进一步说明。
实施例1
(1)以德谷胰岛素为内标,使用50%甲醇溶液配置成0.2mg/mL的溶液,作为内标储备液;取胰岛素标准品用0.1%甲酸水溶液配置成2mg/mL的胰岛素储备液。
(2)标准工作溶液的配置:使用移液枪将25μL内标储备液与2.5μL胰岛素储备液混合在1.5mL离心管中,并用0.1%甲酸水溶液稀释至1000μL,作为标准工作溶液,德谷胰岛素和胰岛素浓度均为5μg/mL。
(3)本实施例中的供试样品为7个不同的口服胰岛素药物,它们是在不同加热温度、时间以及保温条件下制备的口服胰岛素药物样品。样品1为未进行36℃保温的口服胰岛素样品,样品2为进行36℃保温60min的口服胰岛素样品,样品3为36℃保温60min后并90℃加热4min的的口服胰岛素样品,样品4-7分别为90℃加热0min、4min、9min、10min的的口服胰岛素样品。用移液枪分别量取500μL的7个不同的口服胰岛素药物样品于0.5/1.5mL100KD的超滤离心管中,以4℃,5000g,10min的条件进行低温超滤离心,分离出7组上室脂质体溶液与下室游离胰岛素溶液,示意图见图1所示。
图1为口服胰岛素药物低温超滤离心示意图以及上室和下室的液相色谱总离子流图,其中,(A)为口服胰岛素药物低温超滤离心示意图,(B)为上室的液相色谱总离子流图,(C)为下室的液相色谱总离子流图。由图1可以看出,通过100KDa超滤膜,可以分离脂质体溶液(上室)和游离胰岛素溶液(下室),分别对上室脂质体溶液和下室游离胰岛素溶液进高效液相色谱-质谱联用定量检测,可有效分离溶液中的各种物质。(4)供试品溶液的配置:上室脂质体供试品溶液的配置:使用移液枪分别量取10μL步骤(3)中的7组上室脂质体溶液于1.5mL的离心管中,加入10μL的0.2mg/mL步骤(1)配置的内标德谷胰岛素储备液,并分别使用980μL 0.1%甲酸水溶液进行稀释,上室溶液被稀释100倍,内标德谷胰岛素稀释后浓度为2μg/mL。下室游离胰岛素供试品溶液的配置:使用移液枪分别量取10μL步骤(3)中的7组下室游离胰岛素溶液于1.5mL的离心管中,分别加入10μL的0.2mg/mL步骤(1)配置的内标德谷胰岛素储备液,并分别使用980μL 0.1%甲酸水溶液进行稀释,下室溶液被稀释100倍,内标德谷胰岛素稀释后浓度为2μg/mL。分别得到对应的7组上室脂质体供试品溶液和7组下室游离胰岛素供试品溶液。
(5)液相色谱条件:高效液相色谱仪型号为Dionex Ultimate 3000(ThermoFisher Scientific,USA),色谱柱的型号为Phenomenex C18(100× 2.1 mm,1.6μm),流动相:以0.1%甲酸水溶液为流动相A,以0.1%甲酸乙腈溶液为流动相B,流速0.3mL/min,梯度洗脱,进样体积为5μL,柱温为30℃。梯度洗脱程序为:0min,流动相A 90%;0-10min,流动相A从90%变为10%;10-13min,流动相A 10%;13-15min,流动相A从10%变为90%;15-20min,流动相A90%,具体简表1:
表1
质谱检测条件:采用轨道阱质谱分析器,电喷雾离子化,正离子模式,喷雾电压为3500V,鞘气为35Arb,辅助气为10Arb,反吹气为8Arb,气体均为高纯氮气(纯度为99.999%),离子传输毛细管温度300℃,气化温度350℃。
(6)内标法校正因子检测:取步骤(2)中标准工作溶液采用步骤(5)的高效液相色谱-质谱方法检测,进样体积5μL,连续进样3次,色谱和质谱检测结果分别如图2和3所示。
图2为标准品胰岛素与内标德谷胰岛素混合成的标准工作溶液的液相色谱总离子流图,根据图2标准工作溶液的液相色谱图,标准品胰岛素的保留时间为4.70min,德谷胰岛素的保留时间为5.58min。
图3为标准品胰岛素和德谷胰岛素的质谱信号检测图,其中,(A)为标准品胰岛素的质谱信号检测图,(B)为德谷胰岛素的质谱信号检测图。根据图3胰岛素和德谷胰岛素质谱图,观察到质谱检测到的标准品胰岛素离子信号为m/z968.79(z=+6),1162.34(z=+5),1452.67(z=+4),1936.89(z=+3);德谷胰岛素的离子信号是m/z 1018.15(z=+6),1221.57(z=+5),1526.72(z=+4)。根据液相色谱图2中标准品胰岛素和德谷胰岛素的提取离子色谱峰的峰面积,通过式(1)计算出标准品胰岛素与内标物之间的校正因子f:
f=(A
其中,As、Ar分别为标准工作溶液中内标物德谷胰岛素、标准品胰岛素的液相色谱提取峰面积,Cs、Cr分别为标准工作溶液中内标物德谷胰岛素、标准品胰岛素的浓度;标准工作溶液3次平行实验计算结果见表2。
表2标准品胰岛素与内标德谷胰岛素之间的校正因子计算结果:
由表2可知,根据计算结果显示平均校正因子为0.64,相对标准偏差RSD为4.07%。
(7)口服胰岛素药物样品检测:
分别取步骤(4)配制的上室脂质体供试品溶液和下室游离胰岛素供试品溶液采用步骤(5)的高效液相色谱-质谱方法检测,进样体积5μL,,每个样品连续进样3次,液相色谱-质谱联用仪检测结果见图4。
图4为口服胰岛素药物样品1低温超滤离心后,上室和下室溶液的液相色谱总离子流图,其中,(A)为上室脂质体供试品溶液的液相色谱总离子流图,(B)为下室游离胰岛素供试品溶液的液相色谱总离子流图。口服胰岛素药物样品1-7液相色谱总离子流图相似,物质的保留时间相同,仅信号强度不同,故仅展示样品1的上下室溶液的液相色谱总离子流图。根据图4供试品溶液的液相色谱图,上室脂质体供试品溶液样品检测到胆红素、胰岛素、德谷胰岛素、牛磺胆酸、甘氨胆酸,保留时间分别为0.67min、4.70min、5.58min、5.89min、6.55min,下室游离胰岛素供试品溶液样品检测到胰岛素、德谷胰岛素、牛磺胆酸、甘氨胆酸,保留时间分别为4.70min、5.58min、5.89min、6.55min。其中,胆红素、牛磺胆酸、甘氨胆酸为脂质体的组成成分或者脂质体药物包裹的其他药效成分。
根据液相色谱图中胰岛素和德谷胰岛素的提取离子色谱峰的峰面积,通过式(2)计算出上室脂质体供试品溶液中胰岛素的含量和下室游离胰岛素供试品溶液中胰岛素的含量:
C
其中,Ai为上室脂质体供试品溶液或下室游离胰岛素供试品溶液中待测物胰岛素的液相色谱提取峰面积,As为标准工作溶液中内标物德谷胰岛素的液相色谱提取峰面积,Ci为上室脂质体供试品溶液或下室游离胰岛素试品溶液中待测物胰岛素的浓度,Cs标准工作溶液中内标物德谷胰岛素的浓度。结果如表2所示。
根据式(3)计算口服胰岛素药物中胰岛素的包封率:
包封率=上室脂质体供试品溶液中胰岛素浓度/胰岛素总浓度(3)
其中,胰岛素总浓度为上室脂质体供试品溶液中胰岛素浓度与下室游离胰岛素供试品溶液中胰岛素浓度的和。
本实施案例中7个不同的口服胰岛素药物样品,每个样品进行平行实验3次,胰岛素的浓度和包封率结果见表3。
表3口服胰岛素样品液相色谱质谱定量分析与包封率结果:
由表3实验结果说明,本发明液相色谱-质谱联用方法分析口服胰岛素药物中胰岛素包封率方法简单、重复性好、准确度高,能够完全有效测定口服胰岛素药物中胰岛素的含量,测量结果的相对标准偏差RSD<10%,更加真实准确的检测不同口服胰岛素药物实际的包封情况。
最后应说明的是:以上实施例仅用于说明本发明的技术方案,而非对实施方式的限定,对于本领域的普通技术人员,其可以对上述记载的技术方案进行不同形式的变化或变动;而这些变化或变动,并不使相应技术方案的本质脱离本发明的范畴。
- 一种基于智慧工地的建筑工程管理方法及系统
- 一种基于无人机的智慧工地管理系统及方法
- 一种基于无人机的智慧工地管理系统及方法
